Растворы электролитов.ppt
- Количество слайдов: 16
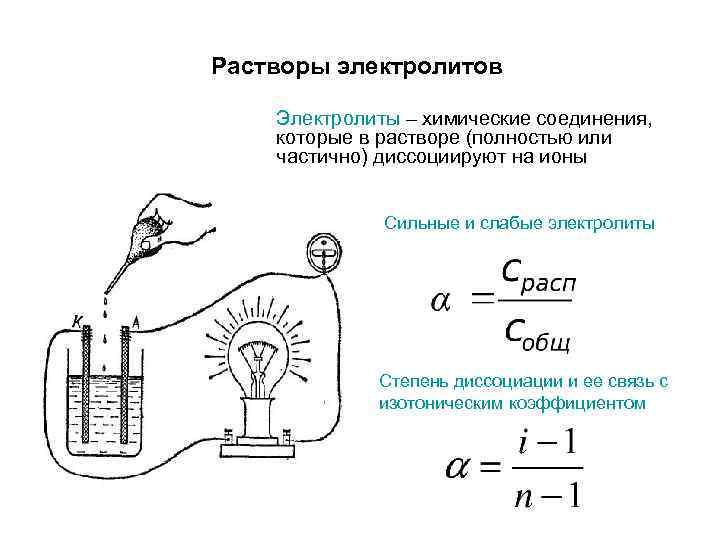 Растворы электролитов Электролиты – химические соединения, которые в растворе (полностью или частично) диссоциируют на ионы Сильные и слабые электролиты Степень диссоциации и ее связь с изотоническим коэффициентом
Растворы электролитов Электролиты – химические соединения, которые в растворе (полностью или частично) диссоциируют на ионы Сильные и слабые электролиты Степень диссоциации и ее связь с изотоническим коэффициентом
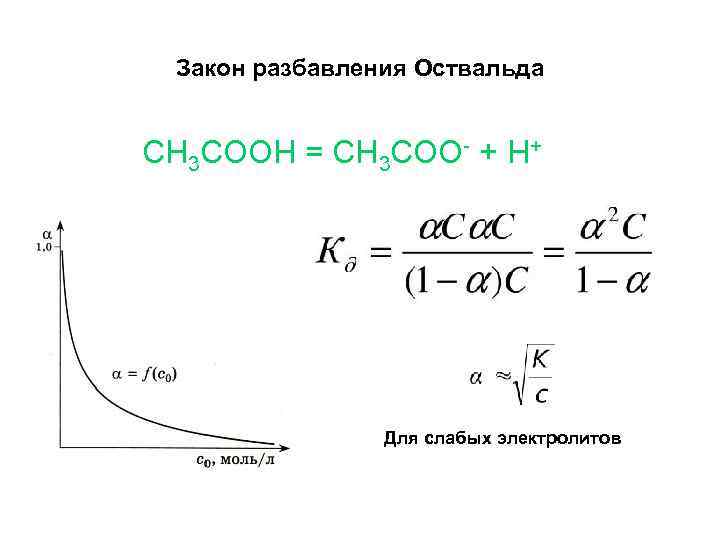 Закон разбавления Оствальда СH 3 COOH = CH 3 COO- + H+ Для слабых электролитов
Закон разбавления Оствальда СH 3 COOH = CH 3 COO- + H+ Для слабых электролитов
 Концентрационные и термодинамические константы диссоциации Активность компонентов раствора — эффективная (кажущаяся) концентрация компонентов с учетом различных взаимодействий между ними в растворе, то есть с учетом отклонения поведения системы от модели идеального раствора. Коэффициент активности Средний ионный коэффициент активности
Концентрационные и термодинамические константы диссоциации Активность компонентов раствора — эффективная (кажущаяся) концентрация компонентов с учетом различных взаимодействий между ними в растворе, то есть с учетом отклонения поведения системы от модели идеального раствора. Коэффициент активности Средний ионный коэффициент активности
 Теория сильных электролитов Дебая-Хюккеля (1923 г) • статистическая теория разбавленных растворов сильных электролитов, согласно которой каждый ион действием своего электрического заряда поляризует окружение и образует вокруг себя некоторое преобладание ионов противоположного знака — так называемую ионную атмосферу. • Предельный закон Дебая-Хюккеля Ионная сила растворов Допущения: Представление о ионах раствора как о материальных точках Пренебрежение ассоциацией ионов Представление о растворителе, как о непрерывной среде, характеризуемой только значением диэлектрической проницаемости и неучет молекулярной структуры растворителя и его взаимодействия с ионами.
Теория сильных электролитов Дебая-Хюккеля (1923 г) • статистическая теория разбавленных растворов сильных электролитов, согласно которой каждый ион действием своего электрического заряда поляризует окружение и образует вокруг себя некоторое преобладание ионов противоположного знака — так называемую ионную атмосферу. • Предельный закон Дебая-Хюккеля Ионная сила растворов Допущения: Представление о ионах раствора как о материальных точках Пренебрежение ассоциацией ионов Представление о растворителе, как о непрерывной среде, характеризуемой только значением диэлектрической проницаемости и неучет молекулярной структуры растворителя и его взаимодействия с ионами.
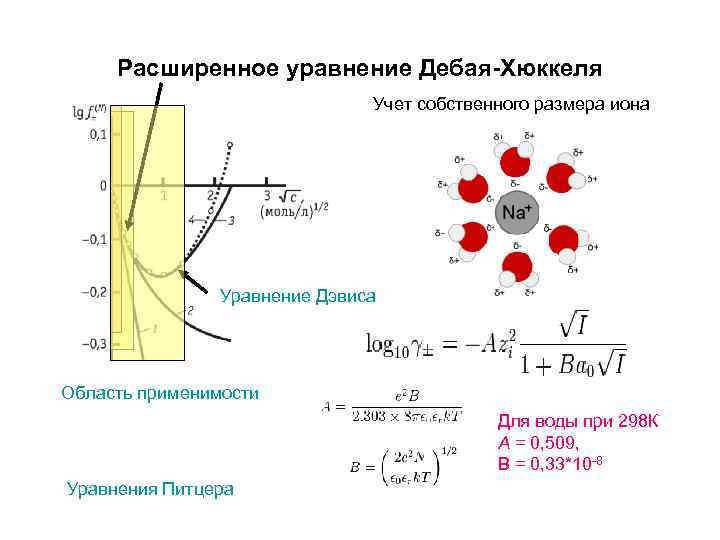 Расширенное уравнение Дебая-Хюккеля Учет собственного размера иона Уравнение Дэвиса Область применимости Для воды при 298 К А = 0, 509, В = 0, 33*10 -8 Уравнения Питцера
Расширенное уравнение Дебая-Хюккеля Учет собственного размера иона Уравнение Дэвиса Область применимости Для воды при 298 К А = 0, 509, В = 0, 33*10 -8 Уравнения Питцера
 Электрическая проводимость • • способность тела проводить электрический ток, а также физическая величина, характеризующая эту способность и обратная электрическому сопротивлению. В СИ единицей измерения электрической проводимости является сименс Электропроводность растворов зависит от природы электролита и растворителя, концентрации, температуры и др. Удельная электрическая проводимость раствора • Электропроводность объема раствора , заключенного между двумя параллельными электродами, имеющими площадь по одному квадратному метру и расположенными на расстоянии одного метра друг от друга
Электрическая проводимость • • способность тела проводить электрический ток, а также физическая величина, характеризующая эту способность и обратная электрическому сопротивлению. В СИ единицей измерения электрической проводимости является сименс Электропроводность растворов зависит от природы электролита и растворителя, концентрации, температуры и др. Удельная электрическая проводимость раствора • Электропроводность объема раствора , заключенного между двумя параллельными электродами, имеющими площадь по одному квадратному метру и расположенными на расстоянии одного метра друг от друга
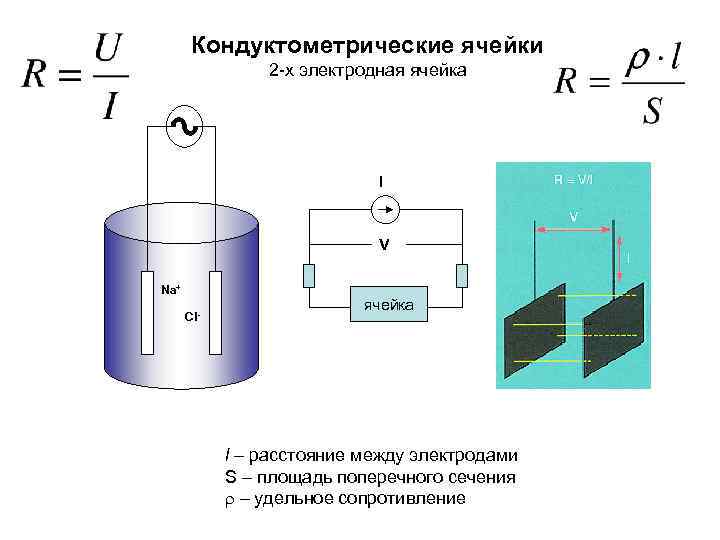 Кондуктометрические ячейки 2 -х электродная ячейка I V Na+ Cl- ячейка l – расстояние между электродами S – площадь поперечного сечения r - удельное сопротивление
Кондуктометрические ячейки 2 -х электродная ячейка I V Na+ Cl- ячейка l – расстояние между электродами S – площадь поперечного сечения r - удельное сопротивление
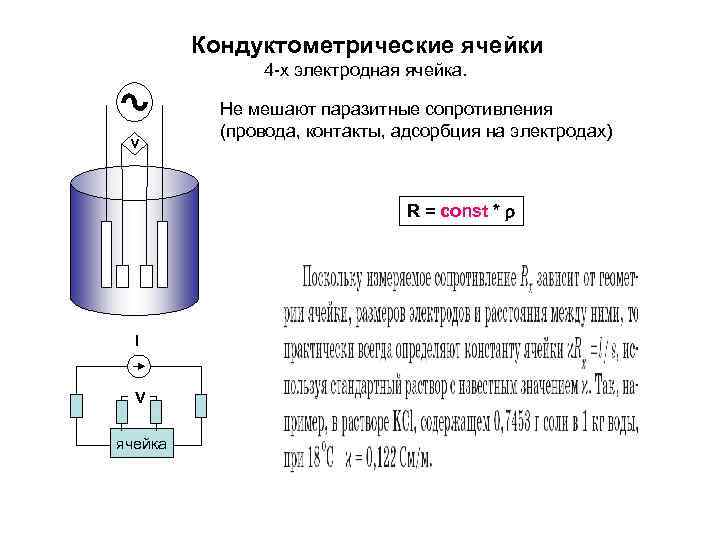 Кондуктометрические ячейки 4 -х электродная ячейка. V Не мешают паразитные сопротивления (провода, контакты, адсорбция на электродах) R = const * r I V ячейка
Кондуктометрические ячейки 4 -х электродная ячейка. V Не мешают паразитные сопротивления (провода, контакты, адсорбция на электродах) R = const * r I V ячейка
 Эквивалентная электрическая проводимость раствора Электропроводность объема электролита (Λ), содержащего 1 г-экв растворенного вещества и находящегося между двумя параллельными электродами площадью 1 м 2, которые расположены на расстоянии 1 м друг от друга. Закон Кольрауша в растворе электролита катионы и анионы переносят электрический ток независимо друг от друга Молярная электропроводность Подвижности ионов Выполняется только в предельно разбавленных растворах электролитов Как найти вклады ионов в молярную электропроводность ?
Эквивалентная электрическая проводимость раствора Электропроводность объема электролита (Λ), содержащего 1 г-экв растворенного вещества и находящегося между двумя параллельными электродами площадью 1 м 2, которые расположены на расстоянии 1 м друг от друга. Закон Кольрауша в растворе электролита катионы и анионы переносят электрический ток независимо друг от друга Молярная электропроводность Подвижности ионов Выполняется только в предельно разбавленных растворах электролитов Как найти вклады ионов в молярную электропроводность ?
 Числа переноса отношение количества электричества, перенесённого ионами данного рода через какое-либо поперечное сечение раствора электролита, к общему количеству электричества, прошедшего через такое же сечение этого раствора. Число переноса равно отношению скорости движения (или подвижности) данного иона к сумме скоростей движения (подвижностей) катиона и аниона и является характеристикой, зависящей от подвижностей всех ионов в растворе электролита, от их концентрации и температуры раствора. Обычно Числа переноса определяют по изменению концентраций ионов у электродов (метод Гитторфа). Если электропроводность одного и того же иона рассчитывать из данных, относящихся к различным солям, то получаются результаты, совпадающие в пределах точности эксперимента Экспериментальное подтверждение закона Кольрауша
Числа переноса отношение количества электричества, перенесённого ионами данного рода через какое-либо поперечное сечение раствора электролита, к общему количеству электричества, прошедшего через такое же сечение этого раствора. Число переноса равно отношению скорости движения (или подвижности) данного иона к сумме скоростей движения (подвижностей) катиона и аниона и является характеристикой, зависящей от подвижностей всех ионов в растворе электролита, от их концентрации и температуры раствора. Обычно Числа переноса определяют по изменению концентраций ионов у электродов (метод Гитторфа). Если электропроводность одного и того же иона рассчитывать из данных, относящихся к различным солям, то получаются результаты, совпадающие в пределах точности эксперимента Экспериментальное подтверждение закона Кольрауша
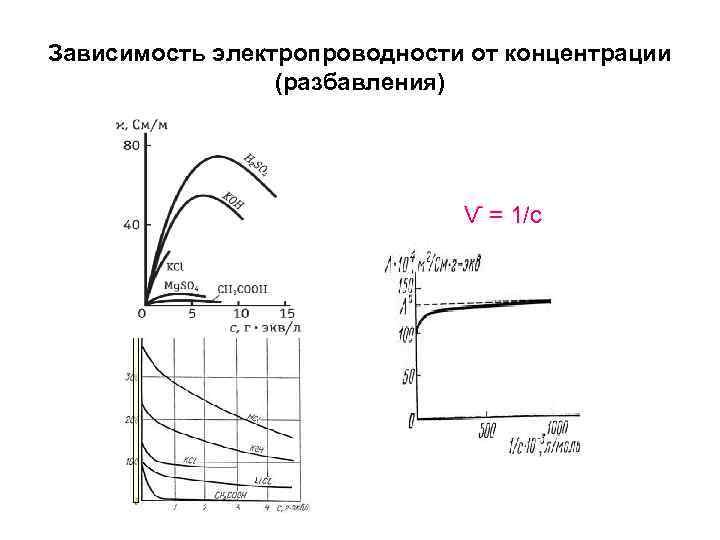 Зависимость электропроводности от концентрации (разбавления) Ѵ = 1/с
Зависимость электропроводности от концентрации (разбавления) Ѵ = 1/с
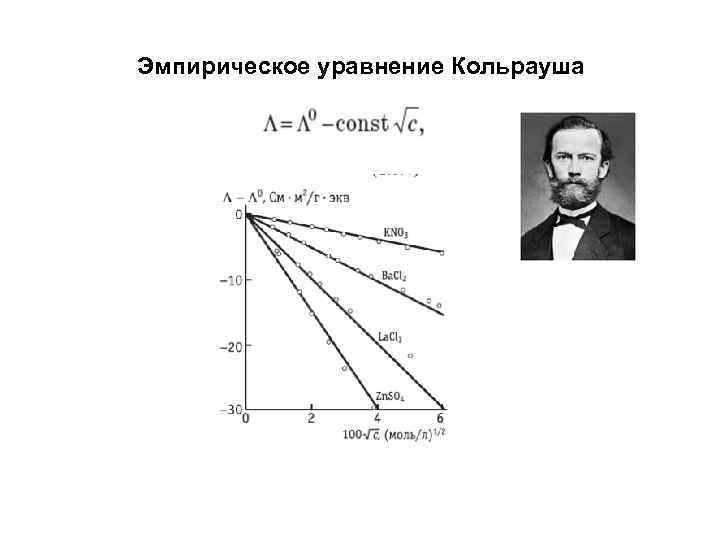 Эмпирическое уравнение Кольрауша
Эмпирическое уравнение Кольрауша
 Ионная атмосфера и эффекты торможения ионов в поле. Уравнение Дебая-Хюккеля-Онзагера. • • Электрофоретический эффект связан с тем, что из-за ионной атмосферы ионам приходится двигаться навстречу потоку других ионов, которые гидратированы в водных растворах. Релаксационный эффект - это нарушение симметрии ионной атмосферы при движении иона, ее рассеивание после иона и создание впереди. Симметрия нарушается из-за того, что на образование ионной атмосферы требуется определенное время • • 2/3 В воде для хлоридов щелочных металлов понижение электропроводности 1/3
Ионная атмосфера и эффекты торможения ионов в поле. Уравнение Дебая-Хюккеля-Онзагера. • • Электрофоретический эффект связан с тем, что из-за ионной атмосферы ионам приходится двигаться навстречу потоку других ионов, которые гидратированы в водных растворах. Релаксационный эффект - это нарушение симметрии ионной атмосферы при движении иона, ее рассеивание после иона и создание впереди. Симметрия нарушается из-за того, что на образование ионной атмосферы требуется определенное время • • 2/3 В воде для хлоридов щелочных металлов понижение электропроводности 1/3
 Уравнение Робинсона-Стокса Правило Вальдена-Писаржевского lo Уравнение Стокса-Эйнтштейна Стоксовский радиус Эстафетный механизм переноса протона
Уравнение Робинсона-Стокса Правило Вальдена-Писаржевского lo Уравнение Стокса-Эйнтштейна Стоксовский радиус Эстафетный механизм переноса протона
 Определение степени и константы диссоциации слабого электролита кондуктометрическим методом • Закон разбавления Оствальда — соотношение, выражающее зависимость эквивалентной электропроводности разбавленного раствора бинарного слабого электролита от концентрации раствора: • • К — константа диссоциации электролита, с — концентрация, λ и λ∞ — значения эквивалентной электропроводности соответственно при концентрации с и при бесконечном разбавлении.
Определение степени и константы диссоциации слабого электролита кондуктометрическим методом • Закон разбавления Оствальда — соотношение, выражающее зависимость эквивалентной электропроводности разбавленного раствора бинарного слабого электролита от концентрации раствора: • • К — константа диссоциации электролита, с — концентрация, λ и λ∞ — значения эквивалентной электропроводности соответственно при концентрации с и при бесконечном разбавлении.
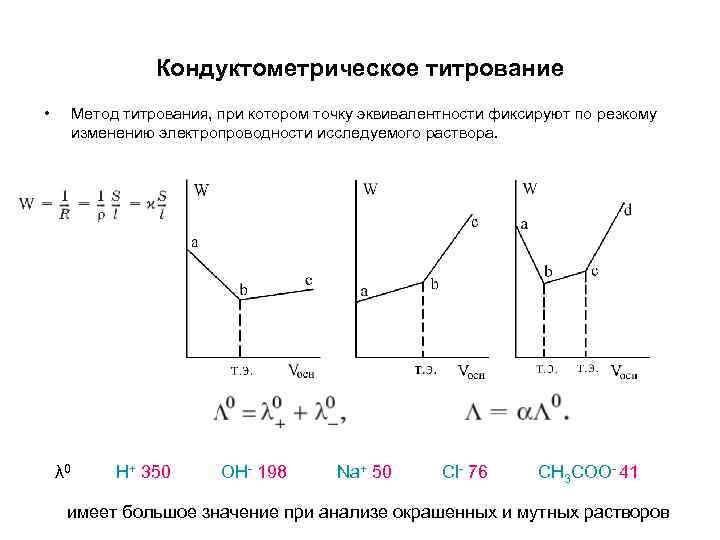 Кондуктометрическое титрование • Метод титрования, при котором точку эквивалентности фиксируют по резкому изменению электропроводности исследуемого раствора. λ 0 H+ 350 OH- 198 Na+ 50 Сl- 76 CH 3 COO- 41 имеет большое значение при анализе окрашенных и мутных растворов
Кондуктометрическое титрование • Метод титрования, при котором точку эквивалентности фиксируют по резкому изменению электропроводности исследуемого раствора. λ 0 H+ 350 OH- 198 Na+ 50 Сl- 76 CH 3 COO- 41 имеет большое значение при анализе окрашенных и мутных растворов


