растворы и диссоцияция.ppt
- Количество слайдов: 22
 Растворы. Электролитическая диссоциация.
Растворы. Электролитическая диссоциация.
 Растворы – это однородные системы, состоящие из двух и более самостоятельных веществ и продуктов их взаимодействия. Компоненты раствора: Растворитель (среда) Растворенное вещество (вещество равномерно распределяемое в растворителе в виде молекул и ионов) Пример: Вода (растворитель) +сахар ( растворенное вещество) = раствор сахара
Растворы – это однородные системы, состоящие из двух и более самостоятельных веществ и продуктов их взаимодействия. Компоненты раствора: Растворитель (среда) Растворенное вещество (вещество равномерно распределяемое в растворителе в виде молекул и ионов) Пример: Вода (растворитель) +сахар ( растворенное вещество) = раствор сахара
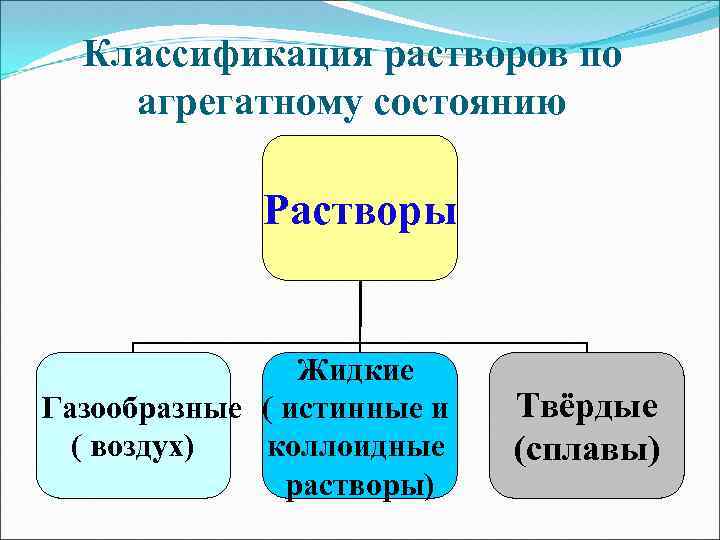 Классификация растворов по агрегатному состоянию Растворы Жидкие Газообразные ( истинные и коллоидные ( воздух) растворы) Твёрдые (сплавы)
Классификация растворов по агрегатному состоянию Растворы Жидкие Газообразные ( истинные и коллоидные ( воздух) растворы) Твёрдые (сплавы)
 Растворимостью называют способность одного вещества растворяться в другом. Количественно растворимость твердых веществ и жидкостей определяется коэффициентом растворимости. По растворимости в воде вещества: Растворимые (более 1, 0 г на 100 г воды) Малорастворимые(0, 1 г - 1, 0 г на 100 г воды); Нерастворимые (менее 0, 1 г на 100 г воды).
Растворимостью называют способность одного вещества растворяться в другом. Количественно растворимость твердых веществ и жидкостей определяется коэффициентом растворимости. По растворимости в воде вещества: Растворимые (более 1, 0 г на 100 г воды) Малорастворимые(0, 1 г - 1, 0 г на 100 г воды); Нерастворимые (менее 0, 1 г на 100 г воды).
 Растворы: Насыщенные Раствор, в котором при данной температуре вещество больше не растворяется. Перенасыщенные Раствор, в котором при данной температуре находится в растворенном состоянии больше вещества, чем в его насыщенном растворе при тех же условиях. Ненасыщенные Раствор, в котором при данной температуре находится меньше растворяемого вещества, чем в его насыщенном растворе.
Растворы: Насыщенные Раствор, в котором при данной температуре вещество больше не растворяется. Перенасыщенные Раствор, в котором при данной температуре находится в растворенном состоянии больше вещества, чем в его насыщенном растворе при тех же условиях. Ненасыщенные Раствор, в котором при данной температуре находится меньше растворяемого вещества, чем в его насыщенном растворе.
 Растворимость: Растворимость твердых веществ, как правило, с возрастанием температуры увеличивается. Исключение Сa(OH)2 Растворимость жидких веществ: Некоторые жидкости смешиваются в любых соотношениях. С повышением температуры взаимная растворимость в жидкостях возрастает.
Растворимость: Растворимость твердых веществ, как правило, с возрастанием температуры увеличивается. Исключение Сa(OH)2 Растворимость жидких веществ: Некоторые жидкости смешиваются в любых соотношениях. С повышением температуры взаимная растворимость в жидкостях возрастает.
 Растворимость газов в жидкостях: На растворимость газов оказывают влияние температура и давление. Растворимость газов описывается законом Генри: С= K * p где С – концентрация газов в насыщенном растворе; К – константа Генри Р – давление газа над раствором
Растворимость газов в жидкостях: На растворимость газов оказывают влияние температура и давление. Растворимость газов описывается законом Генри: С= K * p где С – концентрация газов в насыщенном растворе; К – константа Генри Р – давление газа над раствором
 Процесс растворения Физический : Диффузия, перемешивание Химический: Выделение или поглощение тепла, изменение цвета
Процесс растворения Физический : Диффузия, перемешивание Химический: Выделение или поглощение тепла, изменение цвета
 Современное представление о процессе растворения: Растворение - это физико-химический процесс. При физическом явлении разрушается кристаллическая решетка и происходит диффузия молекул растворенного вещества. При химическом явлении в процессе растворения молекулы растворенного вещества реагируют с молекулами растворителя.
Современное представление о процессе растворения: Растворение - это физико-химический процесс. При физическом явлении разрушается кристаллическая решетка и происходит диффузия молекул растворенного вещества. При химическом явлении в процессе растворения молекулы растворенного вещества реагируют с молекулами растворителя.
 Теория электролитической диссоциации (ТЭД). В 1887 г. Шведский учёный С. Аррениус для объяснения особенностей водных растворов веществ предложил теорию электролитической диссоциации. В дальнейшем эта теория была развита многими учёными, в том числе И. А. Каблуковым и В. А. Кистяковским. Сванте Аррениус
Теория электролитической диссоциации (ТЭД). В 1887 г. Шведский учёный С. Аррениус для объяснения особенностей водных растворов веществ предложил теорию электролитической диссоциации. В дальнейшем эта теория была развита многими учёными, в том числе И. А. Каблуковым и В. А. Кистяковским. Сванте Аррениус
 I-е положение ТЭД. Все вещества по их способности проводить электрический ток в растворах делятся на электролиты и неэлектролиты.
I-е положение ТЭД. Все вещества по их способности проводить электрический ток в растворах делятся на электролиты и неэлектролиты.
 Вещества в растворах Электролиты (водные растворы проводят эл. ток) Вещества с ионной и ковалентной полярной связью. Все растворимые кислоты, основания (щёлочи) и соли. Пример: HCl, Na. OH, KCl, и тд. Неэлектролиты (водные растворы не проводят эл. ток) Вещества с ковалентной неполярной и слабополярной связью Все простые вещества, все оксиды и н/р кислоты, основания и соли. Большинство органических веществ. Пример: Ca. O, и тд.
Вещества в растворах Электролиты (водные растворы проводят эл. ток) Вещества с ионной и ковалентной полярной связью. Все растворимые кислоты, основания (щёлочи) и соли. Пример: HCl, Na. OH, KCl, и тд. Неэлектролиты (водные растворы не проводят эл. ток) Вещества с ковалентной неполярной и слабополярной связью Все простые вещества, все оксиды и н/р кислоты, основания и соли. Большинство органических веществ. Пример: Ca. O, и тд.
 Задания к I-му положению ТЭД 1. 2. 3. 4. Какие вещества называются электролитами и неэлектролитами? Назовите по два вещества, которые являются электролитами и неэлектролитами. Укажите вид связи и принадлежность данных веществ к электролитам и неэлектролитам: KCl, O 2 , HNO 3 , Cu. O. Назовите из перечня веществ электролиты (не забудьте воспользоваться таблицей растворимости !): Ba. Cl 2 , Ca. O, H 2 SO 4 , Na. OH, Cl 2 , Zn(OH)2
Задания к I-му положению ТЭД 1. 2. 3. 4. Какие вещества называются электролитами и неэлектролитами? Назовите по два вещества, которые являются электролитами и неэлектролитами. Укажите вид связи и принадлежность данных веществ к электролитам и неэлектролитам: KCl, O 2 , HNO 3 , Cu. O. Назовите из перечня веществ электролиты (не забудьте воспользоваться таблицей растворимости !): Ba. Cl 2 , Ca. O, H 2 SO 4 , Na. OH, Cl 2 , Zn(OH)2
 II-е положение ТЭД В растворах электролиты диссоциируют(распадаются) на положительные ионы (катионы) и на отрицательные (анионы). Процесс распада электролита на ионы называется электролитической диссоциацией (ЭД). Причиной диссоциации электролита является его взаимодействие с молекулами воды (гидратация).
II-е положение ТЭД В растворах электролиты диссоциируют(распадаются) на положительные ионы (катионы) и на отрицательные (анионы). Процесс распада электролита на ионы называется электролитической диссоциацией (ЭД). Причиной диссоциации электролита является его взаимодействие с молекулами воды (гидратация).
 Типы ионов 1) По заряду: катионы (положительные) и анионы (отрицательные); 2) По отношению к воде: Гидратированные и негидратированные ( в безводных средах) 3) По составу: простые и сложные.
Типы ионов 1) По заряду: катионы (положительные) и анионы (отрицательные); 2) По отношению к воде: Гидратированные и негидратированные ( в безводных средах) 3) По составу: простые и сложные.
 Диссоциация кислот Кислоты - это сложные вещества, при диссоциации которых в водных растворах в качестве катионов отщепляются только ионы водорода. HCl == H+ + Cl. CH 3 COOH == CH 3 COO- + H+ Двухосновные кислоты распадаются на ионы в две ступени. Как правило, первая ступень осуществляется в большей степени, чем первая: H 2 SO 4 == H+ + HSO 4 - == H+ + SO 42 -
Диссоциация кислот Кислоты - это сложные вещества, при диссоциации которых в водных растворах в качестве катионов отщепляются только ионы водорода. HCl == H+ + Cl. CH 3 COOH == CH 3 COO- + H+ Двухосновные кислоты распадаются на ионы в две ступени. Как правило, первая ступень осуществляется в большей степени, чем первая: H 2 SO 4 == H+ + HSO 4 - == H+ + SO 42 -
 Диссоциация оснований Основания - это сложные вещества, при диссоциации которых в водных растворах в качестве анионов отщепляются только гидроксид-ионы. Na. OH == Na+ + OHBa(OH )2 == Ba 2+ + 2 OH Однако имеются электролиты, при диссоциации которых одновременно образуются и ионы водорода и гидроксид – ионы. Эти электролиты называются а м ф о т е р н ы м и или а м ф о -л и т а м и. К ним относятся вода, гидроксиды алюминия, хрома (!!!) и других веществ. Вода , например, в незначительных количествах диссоциирует на ионы Н+ и ОН-: Н 2 О ==Н+ + ОН-
Диссоциация оснований Основания - это сложные вещества, при диссоциации которых в водных растворах в качестве анионов отщепляются только гидроксид-ионы. Na. OH == Na+ + OHBa(OH )2 == Ba 2+ + 2 OH Однако имеются электролиты, при диссоциации которых одновременно образуются и ионы водорода и гидроксид – ионы. Эти электролиты называются а м ф о т е р н ы м и или а м ф о -л и т а м и. К ним относятся вода, гидроксиды алюминия, хрома (!!!) и других веществ. Вода , например, в незначительных количествах диссоциирует на ионы Н+ и ОН-: Н 2 О ==Н+ + ОН-
 Диссоциация солей Соли - это сложные вещества, которые в водных растворах диссоциируют на катионы металла и анионы кислотного остатка. K 2 CO 3 – средняя соль; KHCO 3 – кислая соль Al(OH)Cl 2 - основная соль; (NH 4)2 Fe ( SO 4)2*6 H 2 O – двойная соль – сульфат железааммония; [Cu(NH 3)4]SO 4 - комплексная соль сульфаттетраамминмеди(11).
Диссоциация солей Соли - это сложные вещества, которые в водных растворах диссоциируют на катионы металла и анионы кислотного остатка. K 2 CO 3 – средняя соль; KHCO 3 – кислая соль Al(OH)Cl 2 - основная соль; (NH 4)2 Fe ( SO 4)2*6 H 2 O – двойная соль – сульфат железааммония; [Cu(NH 3)4]SO 4 - комплексная соль сульфаттетраамминмеди(11).
 Средние соли – электролиты, при диссоциации которых образуются катионы металла(или аммония NН 4+) и анионы кислотного остатка: KCl == K+ + Cl. NH 4 NO 3 == NH 4+ + NO 3 Na 2 SO 4 == 2 Na+ + SO 2 Основные соли – электролиты, при диссоциации которых образуются два типа анионов: анион кислотного остатка и гидроксид-ион. Диссоциация основных солей протекает ступенчато, например: Ba. OHCl == Ba. OH+ + Cl- ( I ступень) Ba. OH+ == Ba 2+ + OH- (IIступень)
Средние соли – электролиты, при диссоциации которых образуются катионы металла(или аммония NН 4+) и анионы кислотного остатка: KCl == K+ + Cl. NH 4 NO 3 == NH 4+ + NO 3 Na 2 SO 4 == 2 Na+ + SO 2 Основные соли – электролиты, при диссоциации которых образуются два типа анионов: анион кислотного остатка и гидроксид-ион. Диссоциация основных солей протекает ступенчато, например: Ba. OHCl == Ba. OH+ + Cl- ( I ступень) Ba. OH+ == Ba 2+ + OH- (IIступень)
 Кислые соли - это электролиты, при диссоциации которых , . образуются два вида катионов : катионы металла и катионы водорода: KHSO 4 == K+ + HSO 4 - (1 cтупень) HSO 4 - == H+ + SO 42 - ( II ступень) Двойные соли - электролиты, при диссоциации которых образуются два типа катионов металлов ( или металла и NН 4+) : KAl(SO 4)2 == K+ + Al 3+ + 2 SO 42 - (алюмокалиевые квасцы) Na. KC 4 H 4 O 6 == Na+ + K+ + C 4 H 4 O 62 - (тартрат калия-натрия) Na 2 NH 4 PO 4 == 2 Na+ + NH 4+ + PO 43 - ( фосфат аммония-натрия) Комплексные соли - электролиты, при диссоциации образуются два типа ионов: простой и комплексный (сложны), причем комплексный ион может быть как катионом, так и анионом: K 4[Fe (CN)6] == 4 K+ + [Fe (CN)6]4[Ag (NH 3)2]Cl == [Ag (NH 3)2]+ + Cl-
Кислые соли - это электролиты, при диссоциации которых , . образуются два вида катионов : катионы металла и катионы водорода: KHSO 4 == K+ + HSO 4 - (1 cтупень) HSO 4 - == H+ + SO 42 - ( II ступень) Двойные соли - электролиты, при диссоциации которых образуются два типа катионов металлов ( или металла и NН 4+) : KAl(SO 4)2 == K+ + Al 3+ + 2 SO 42 - (алюмокалиевые квасцы) Na. KC 4 H 4 O 6 == Na+ + K+ + C 4 H 4 O 62 - (тартрат калия-натрия) Na 2 NH 4 PO 4 == 2 Na+ + NH 4+ + PO 43 - ( фосфат аммония-натрия) Комплексные соли - электролиты, при диссоциации образуются два типа ионов: простой и комплексный (сложны), причем комплексный ион может быть как катионом, так и анионом: K 4[Fe (CN)6] == 4 K+ + [Fe (CN)6]4[Ag (NH 3)2]Cl == [Ag (NH 3)2]+ + Cl-
 Задания ко II-му положению ТЭД 1. 2. 3. 4. 5. 6. Сформулируйте второе положение ТЭД. Что такое электролитическая диссоциация? Что является причиной ЭД? Каков механизм ЭД: а)веществ с ионной связью, б) веществ с ковалентной связью? Назовите частицы: а) H, H 2 , H+ ; б) Cl 2 , Cl. Назовите катионы и анионы в соединениях, формулы которых: Cu. Cl 2 , Ag. NO 3 , Ca(OH)2 , H 3 PO 4.
Задания ко II-му положению ТЭД 1. 2. 3. 4. 5. 6. Сформулируйте второе положение ТЭД. Что такое электролитическая диссоциация? Что является причиной ЭД? Каков механизм ЭД: а)веществ с ионной связью, б) веществ с ковалентной связью? Назовите частицы: а) H, H 2 , H+ ; б) Cl 2 , Cl. Назовите катионы и анионы в соединениях, формулы которых: Cu. Cl 2 , Ag. NO 3 , Ca(OH)2 , H 3 PO 4.
 Домашнее задание: 1)Написать уравнения ЭД и напишите какой тип связи в соединениях : H 2 SO 4, Ca(OH)2, Al. Cl 3. 2)Написать уравнения ступенчатой диссоциации и напишите какой тип связи в соединениях: H 2 CO 3, H 3 PO 4, H 3 As. O 3. 3) Cоставьте формулы солей, образованных следующими катионами и анионами: а) K+ и (NO 3)- , Na+ и (HSO 3)б) Ca 2+ и HS-, Zn 2+ и (SO 4)2 - . 4)Напишите уравнения ЭД и напишите к какому типу солей относятся данные вещества: KAl(SO 4)2 , Fe. OH(NO 3)2 , KCl*Mg. Cl 2 , Mg. Cl. NO 3.
Домашнее задание: 1)Написать уравнения ЭД и напишите какой тип связи в соединениях : H 2 SO 4, Ca(OH)2, Al. Cl 3. 2)Написать уравнения ступенчатой диссоциации и напишите какой тип связи в соединениях: H 2 CO 3, H 3 PO 4, H 3 As. O 3. 3) Cоставьте формулы солей, образованных следующими катионами и анионами: а) K+ и (NO 3)- , Na+ и (HSO 3)б) Ca 2+ и HS-, Zn 2+ и (SO 4)2 - . 4)Напишите уравнения ЭД и напишите к какому типу солей относятся данные вещества: KAl(SO 4)2 , Fe. OH(NO 3)2 , KCl*Mg. Cl 2 , Mg. Cl. NO 3.


