4. Растворимость солей.ppt
- Количество слайдов: 44
 Растворимость малорастворимого сильного электролита. Влияние ионной силы раствора на растворимость осадка. Солевой эффект.
Растворимость малорастворимого сильного электролита. Влияние ионной силы раствора на растворимость осадка. Солевой эффект.
 Растворимость – общая концентрация вещества в его насыщенном растворе. Молярная растворимость S – число молей растворенного вещества, содержащихся в 1 л насыщенного раствора (моль/л) Массовая растворимость Cm – масса растворенного вещества, содержащаяся в 1 л насыщенного раствора (г/л)
Растворимость – общая концентрация вещества в его насыщенном растворе. Молярная растворимость S – число молей растворенного вещества, содержащихся в 1 л насыщенного раствора (моль/л) Массовая растворимость Cm – масса растворенного вещества, содержащаяся в 1 л насыщенного раствора (г/л)
 S < 1· 10– 4 малорастворимые электролиты S < 1· 10– 2 среднерастворимые электролиты S > 1· 10– 2 хорошо растворимые электролиты
S < 1· 10– 4 малорастворимые электролиты S < 1· 10– 2 среднерастворимые электролиты S > 1· 10– 2 хорошо растворимые электролиты
![ПРK(Am. Bn) = [A]m·[B]n = (m. S)m·(n. S)n = mmnn. Sm+n ПРK(Am. Bn) = ПРK(Am. Bn) = [A]m·[B]n = (m. S)m·(n. S)n = mmnn. Sm+n ПРK(Am. Bn) =](https://present5.com/presentation/139200531_176428522/image-4.jpg) ПРK(Am. Bn) = [A]m·[B]n = (m. S)m·(n. S)n = mmnn. Sm+n ПРK(Am. Bn) = mmnn. Sm+n
ПРK(Am. Bn) = [A]m·[B]n = (m. S)m·(n. S)n = mmnn. Sm+n ПРK(Am. Bn) = mmnn. Sm+n
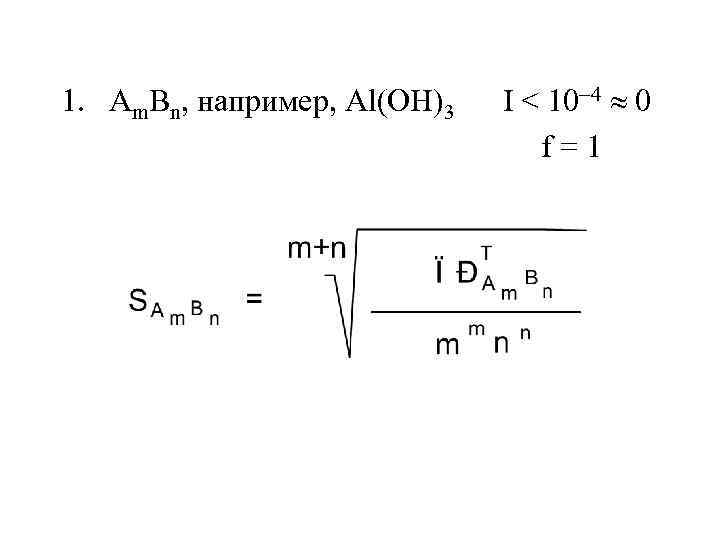 1. Am. Bn, например, Al(OH)3 I < 10 4 0 f=1
1. Am. Bn, например, Al(OH)3 I < 10 4 0 f=1
 Для бинарного электролита AB, например, Ca. SO 4, Ag. Cl m=n=1
Для бинарного электролита AB, например, Ca. SO 4, Ag. Cl m=n=1
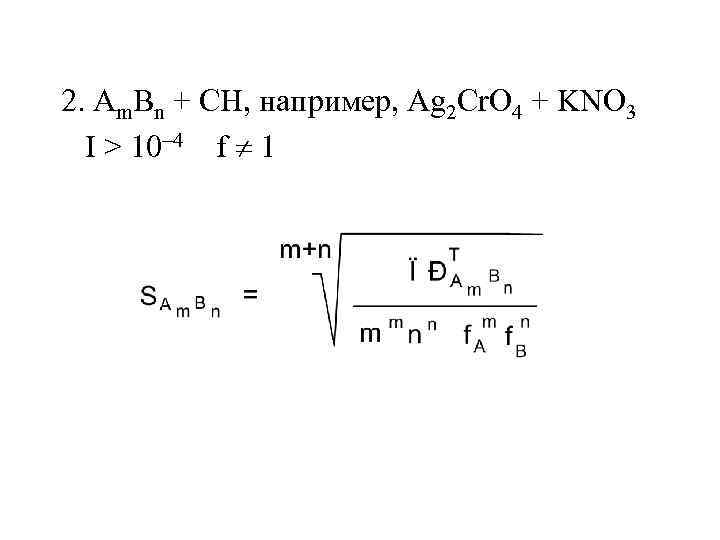 2. Am. Bn + CH, например, Ag 2 Cr. O 4 + KNO 3 I > 10 4 f 1
2. Am. Bn + CH, например, Ag 2 Cr. O 4 + KNO 3 I > 10 4 f 1
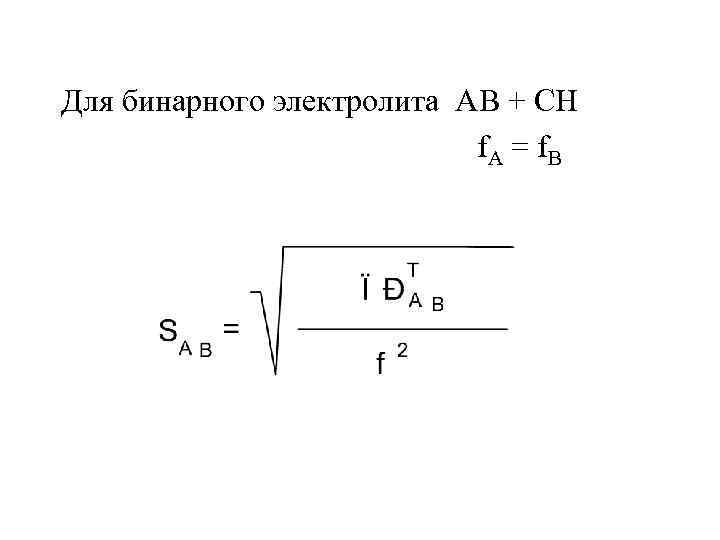 Для бинарного электролита AB + CH f. A = f. B
Для бинарного электролита AB + CH f. A = f. B
 Солевой эффект проявляется в увеличении растворимости малорастворимого сильного электролита с увеличением ионной силы раствора (разные сильные электролиты, прилитые в одинаковом количестве, дают разный солевой эффект)
Солевой эффект проявляется в увеличении растворимости малорастворимого сильного электролита с увеличением ионной силы раствора (разные сильные электролиты, прилитые в одинаковом количестве, дают разный солевой эффект)
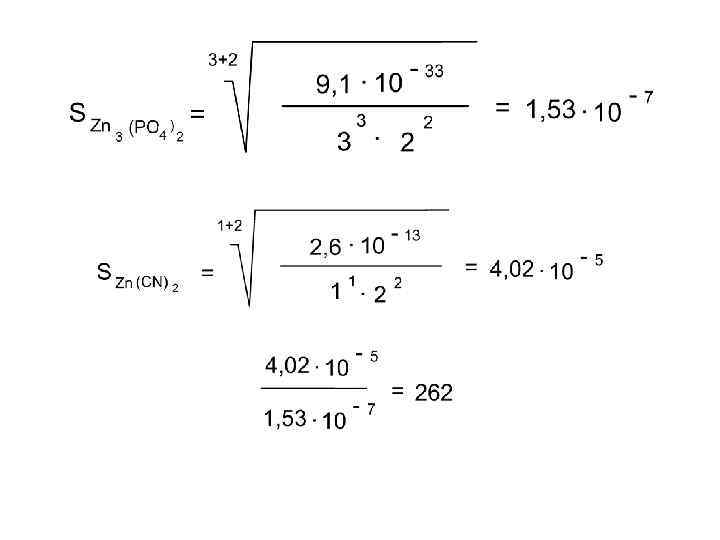
 Какая соль более растворима в воде: фосфат цинка или цианид цинка, и во сколько раз? Решение: Zn 3(PO 4)2 m=3 n=2 ПР = 9, 1· 10– 33 Zn(CN)2 m=1 n= 2 ПР = 2, 6· 10– 13
Какая соль более растворима в воде: фосфат цинка или цианид цинка, и во сколько раз? Решение: Zn 3(PO 4)2 m=3 n=2 ПР = 9, 1· 10– 33 Zn(CN)2 m=1 n= 2 ПР = 2, 6· 10– 13
 Вычислить растворимость Ag 2 Cr. O 4 в чистой воде, в 0, 01 М растворе Na. NO 3 и 0, 01 М растворе Na 3 PO 4. Решение: В чистой воде I 0, f = 1
Вычислить растворимость Ag 2 Cr. O 4 в чистой воде, в 0, 01 М растворе Na. NO 3 и 0, 01 М растворе Na 3 PO 4. Решение: В чистой воде I 0, f = 1
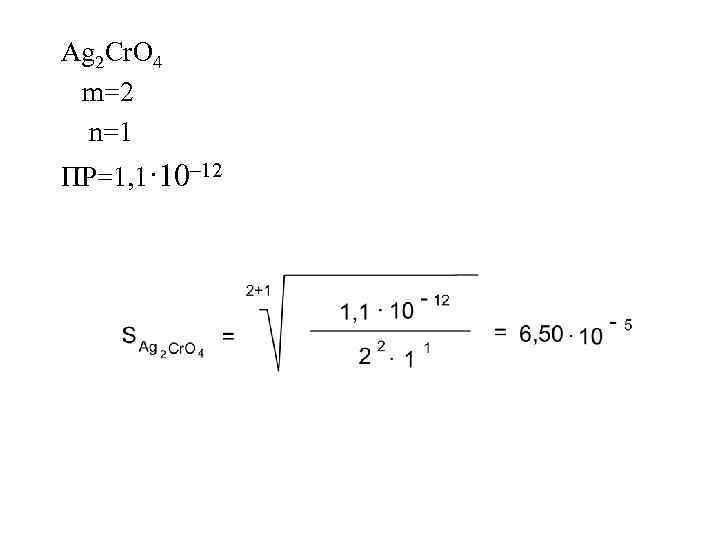 Ag 2 Cr. O 4 m=2 n=1 ПР=1, 1· 10– 12
Ag 2 Cr. O 4 m=2 n=1 ПР=1, 1· 10– 12
 в растворе 0, 01 М Na. NO 3 I = 0, 01 моль/л f(Ag) = 0, 898 f(Cr. O 4) = 0, 660
в растворе 0, 01 М Na. NO 3 I = 0, 01 моль/л f(Ag) = 0, 898 f(Cr. O 4) = 0, 660
 в растворе 0, 01 М Na 3 PO 4 3 Na+ 0, 01 + PO 3– 0, 03 0, 01 I = ½(0, 03 · 12 + 0, 01 · 32) = 0, 045 0, 05 (M) f(Ag) = 0, 80 f(Cr. O 4) = 0, 445
в растворе 0, 01 М Na 3 PO 4 3 Na+ 0, 01 + PO 3– 0, 03 0, 01 I = ½(0, 03 · 12 + 0, 01 · 32) = 0, 045 0, 05 (M) f(Ag) = 0, 80 f(Cr. O 4) = 0, 445
 Растворимость Ag 2 Cr. O 4 в чистой воде 6, 50 · 10– 5 в 0, 01 М Na. NO 3 8, 02 · 10– 5 (1, 23 ) в 0, 01 М Na 3 PO 4 9, 85 · 10– 5 (1, 52 )
Растворимость Ag 2 Cr. O 4 в чистой воде 6, 50 · 10– 5 в 0, 01 М Na. NO 3 8, 02 · 10– 5 (1, 23 ) в 0, 01 М Na 3 PO 4 9, 85 · 10– 5 (1, 52 )
 Сколько г роданида серебра растворяется в 250 мл воды? ПР(Ag. SCN) = 1, 1 · 10– 12 Решение. 1. Найдем растворимость Ag. SCN в чистой воде 2. Найдем массу растворившегося Ag. SCN в 250 мл раствора
Сколько г роданида серебра растворяется в 250 мл воды? ПР(Ag. SCN) = 1, 1 · 10– 12 Решение. 1. Найдем растворимость Ag. SCN в чистой воде 2. Найдем массу растворившегося Ag. SCN в 250 мл раствора
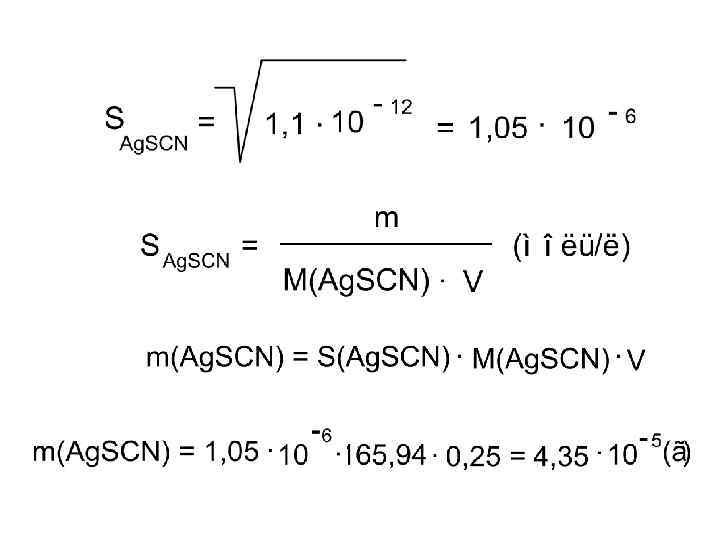
 Растворимость малорастворимого электролита в присутствии одноименных ионов
Растворимость малорастворимого электролита в присутствии одноименных ионов
 Am. Bn + AC Am. Bn + DB (Ag. Cl + Ag. NO 3) (Ag. Cl + KCl)
Am. Bn + AC Am. Bn + DB (Ag. Cl + Ag. NO 3) (Ag. Cl + KCl)
![ПРK(Am. Bn) = [A]m·[B]n = [A]m·(n. S)n = nn · Sn · [A]m ПРK(Am. ПРK(Am. Bn) = [A]m·[B]n = [A]m·(n. S)n = nn · Sn · [A]m ПРK(Am.](https://present5.com/presentation/139200531_176428522/image-21.jpg) ПРK(Am. Bn) = [A]m·[B]n = [A]m·(n. S)n = nn · Sn · [A]m ПРK(Am. Bn) = nn · Sn · [A]m
ПРK(Am. Bn) = [A]m·[B]n = [A]m·(n. S)n = nn · Sn · [A]m ПРK(Am. Bn) = nn · Sn · [A]m
![ПРK(Am. Bn) = [A]m·[B]n = [B]n · (m. S)m = m m · Sm ПРK(Am. Bn) = [A]m·[B]n = [B]n · (m. S)m = m m · Sm](https://present5.com/presentation/139200531_176428522/image-22.jpg) ПРK(Am. Bn) = [A]m·[B]n = [B]n · (m. S)m = m m · Sm · [B]n ПРK(Am. Bn) = mm · Sm · [B]n
ПРK(Am. Bn) = [A]m·[B]n = [B]n · (m. S)m = m m · Sm · [B]n ПРK(Am. Bn) = mm · Sm · [B]n

 Задача. Вычислить растворимость гидроксида железа(III) в чистой воде и 0, 025 М растворе гидроксида натрия. Решение. В чистой воде: Fe(OH)3 ПР = 6, 3 · 10– 38 m=1 n=3
Задача. Вычислить растворимость гидроксида железа(III) в чистой воде и 0, 025 М растворе гидроксида натрия. Решение. В чистой воде: Fe(OH)3 ПР = 6, 3 · 10– 38 m=1 n=3
 В 0, 025 М растворе Na. OH I = 0, 025 M f. Fe= 0, 325 Ответ: 2, 9 · 10– 10 1, 9 · 10– 32 f. OH = 0, 855
В 0, 025 М растворе Na. OH I = 0, 025 M f. Fe= 0, 325 Ответ: 2, 9 · 10– 10 1, 9 · 10– 32 f. OH = 0, 855
 Условие образования осадков малорастворимых электролитов
Условие образования осадков малорастворимых электролитов
 ИП > ПР ИП < ПР ИП = ПР осадок выпадет осадок не выпадет система в состоянии равновесия Am B n ПР = [A]m · [B]n для насыщенного раствора ИП = [A]m · [B]n для данного раствора ИП = ПК ИП – ионное произведение ПК – произведение концентраций
ИП > ПР ИП < ПР ИП = ПР осадок выпадет осадок не выпадет система в состоянии равновесия Am B n ПР = [A]m · [B]n для насыщенного раствора ИП = [A]m · [B]n для данного раствора ИП = ПК ИП – ионное произведение ПК – произведение концентраций
 Задача. Выпадет ли осадок при смешивании 10 мл 0, 01 М раствора Ca. Cl 2 и 5 мл 0, 05 М раствора K 2 Cr. O 4. Решение. Ca. Cl 2 + K 2 Cr. O 4 Ca. Cr. O 4 + 2 KCl ИП(Ca. Cr. O 4) ? ПР(Ca. Cr. O 4) ИП(Ca. Cr. O 4) = [Ca] · [Cr. O 4] C(Ca) = ? С(Cr. O 4) = ?
Задача. Выпадет ли осадок при смешивании 10 мл 0, 01 М раствора Ca. Cl 2 и 5 мл 0, 05 М раствора K 2 Cr. O 4. Решение. Ca. Cl 2 + K 2 Cr. O 4 Ca. Cr. O 4 + 2 KCl ИП(Ca. Cr. O 4) ? ПР(Ca. Cr. O 4) ИП(Ca. Cr. O 4) = [Ca] · [Cr. O 4] C(Ca) = ? С(Cr. O 4) = ?
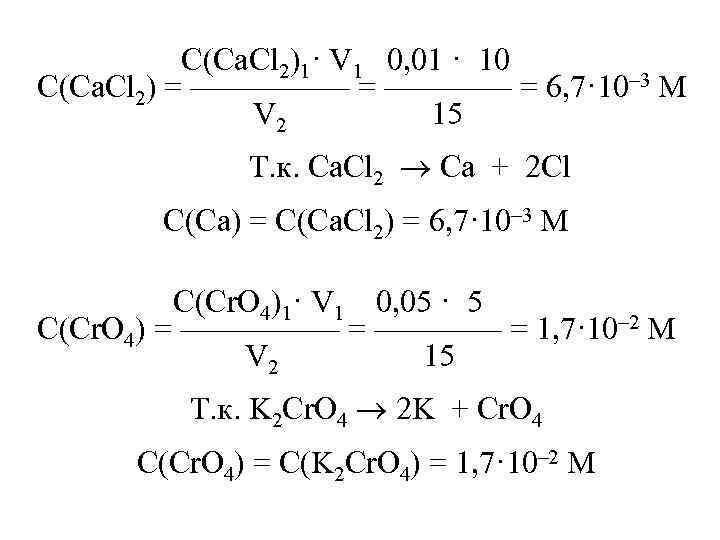 C(Ca. Cl 2)1· V 1 0, 01 · 10 С(Ca. Cl 2) = ————— = 6, 7· 10– 3 M V 2 15 Т. к. Ca. Cl 2 Ca + 2 Cl C(Ca) = С(Ca. Cl 2) = 6, 7· 10– 3 M C(Cr. O 4)1· V 1 0, 05 · 5 С(Cr. O 4) = ————— = 1, 7· 10– 2 M V 2 15 Т. к. K 2 Cr. O 4 2 K + Cr. O 4 C(Cr. O 4) = С(K 2 Cr. O 4) = 1, 7· 10– 2 M
C(Ca. Cl 2)1· V 1 0, 01 · 10 С(Ca. Cl 2) = ————— = 6, 7· 10– 3 M V 2 15 Т. к. Ca. Cl 2 Ca + 2 Cl C(Ca) = С(Ca. Cl 2) = 6, 7· 10– 3 M C(Cr. O 4)1· V 1 0, 05 · 5 С(Cr. O 4) = ————— = 1, 7· 10– 2 M V 2 15 Т. к. K 2 Cr. O 4 2 K + Cr. O 4 C(Cr. O 4) = С(K 2 Cr. O 4) = 1, 7· 10– 2 M
![ИП(Ca. Cr. O 4) = [Ca] · [Cr. O 4] ИП(Ca. Cr. O 4) ИП(Ca. Cr. O 4) = [Ca] · [Cr. O 4] ИП(Ca. Cr. O 4)](https://present5.com/presentation/139200531_176428522/image-30.jpg) ИП(Ca. Cr. O 4) = [Ca] · [Cr. O 4] ИП(Ca. Cr. O 4) = 6, 7· 10– 3 · 1, 7· 10– 2 = 1, 1· 10– 4 ПР(Ca. Cr. O 4) = 7, 1· 10– 4 ИП(Ca. Cr. O 4) ? ПР(Ca. Cr. O 4) 1, 1· 10– 4 < 7, 1· 10– 4 Ответ: Осадок не выпадет.
ИП(Ca. Cr. O 4) = [Ca] · [Cr. O 4] ИП(Ca. Cr. O 4) = 6, 7· 10– 3 · 1, 7· 10– 2 = 1, 1· 10– 4 ПР(Ca. Cr. O 4) = 7, 1· 10– 4 ИП(Ca. Cr. O 4) ? ПР(Ca. Cr. O 4) 1, 1· 10– 4 < 7, 1· 10– 4 Ответ: Осадок не выпадет.
 Задача. Образуется ли осадок гидроксида кальция, если смешать равные объемы 0, 03 М раствора Ca. Cl 2 и 0, 05 М раствора Na. OH. Решение. Ca. Cl 2 + 2 Na. OH Ca(OH)2 + 2 Na. Cl ИП(Ca(OH)2) = [Ca] · [OH]2 C(Ca. Cl 2)1· V 1 0, 03 · x С(Ca. Cl 2) = ————— = 0, 015 M V 2 2 x C(Ca) = 0, 015 M
Задача. Образуется ли осадок гидроксида кальция, если смешать равные объемы 0, 03 М раствора Ca. Cl 2 и 0, 05 М раствора Na. OH. Решение. Ca. Cl 2 + 2 Na. OH Ca(OH)2 + 2 Na. Cl ИП(Ca(OH)2) = [Ca] · [OH]2 C(Ca. Cl 2)1· V 1 0, 03 · x С(Ca. Cl 2) = ————— = 0, 015 M V 2 2 x C(Ca) = 0, 015 M
 C(Na. OH)1· V 1 0, 05 · x С(Na. OH) = ————— = 0, 025 M V 2 2 x Na. OH Na + OH С(Na. OH) = C(OH) = 0, 025 M ИП(Ca(OH)2) = [Ca] · [OH]2 ИП(Ca(OH)2) = 0, 015· 0, 0252 = 9, 38· 10– 6 M ПР(Ca(OH)2) = 6, 5· 10– 6 ИП > ПР - осадок выпадет
C(Na. OH)1· V 1 0, 05 · x С(Na. OH) = ————— = 0, 025 M V 2 2 x Na. OH Na + OH С(Na. OH) = C(OH) = 0, 025 M ИП(Ca(OH)2) = [Ca] · [OH]2 ИП(Ca(OH)2) = 0, 015· 0, 0252 = 9, 38· 10– 6 M ПР(Ca(OH)2) = 6, 5· 10– 6 ИП > ПР - осадок выпадет
 Задача. Образуется ли осадок гидроксида кальция, если смешать равные объемы 0, 03 М раствора Ca. Cl 2 и 0, 05 М раствора аммиака. Решение. Ca. Cl 2 + 2 Na. OH Ca(OH)2 + 2 Na. Cl ИП(Ca(OH)2) = [Ca] · [OH]2 C(Ca. Cl 2)1· V 1 0, 03 · x С(Ca. Cl 2) = ————— = 0, 015 M V 2 2 x C(Ca) = 0, 015 M
Задача. Образуется ли осадок гидроксида кальция, если смешать равные объемы 0, 03 М раствора Ca. Cl 2 и 0, 05 М раствора аммиака. Решение. Ca. Cl 2 + 2 Na. OH Ca(OH)2 + 2 Na. Cl ИП(Ca(OH)2) = [Ca] · [OH]2 C(Ca. Cl 2)1· V 1 0, 03 · x С(Ca. Cl 2) = ————— = 0, 015 M V 2 2 x C(Ca) = 0, 015 M
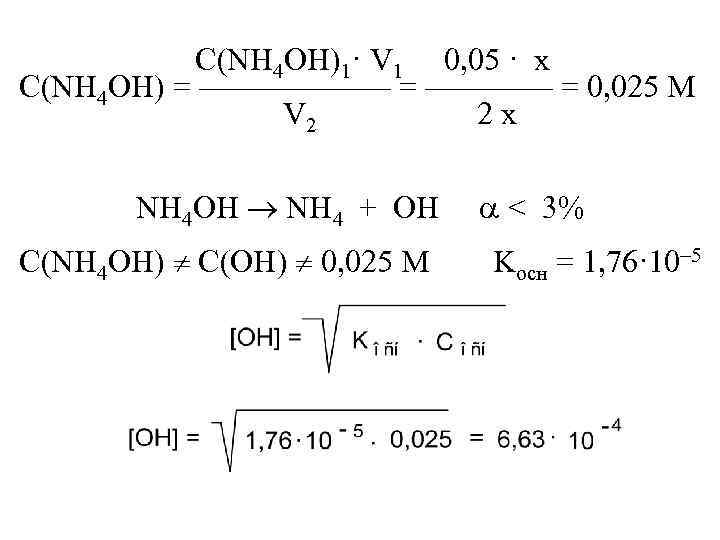 C(NH 4 OH)1· V 1 0, 05 · x С(NH 4 OH) = —————— = 0, 025 M V 2 2 x NH 4 OH NH 4 + OH С(NH 4 OH) C(OH) 0, 025 M < 3% Kосн = 1, 76· 10– 5
C(NH 4 OH)1· V 1 0, 05 · x С(NH 4 OH) = —————— = 0, 025 M V 2 2 x NH 4 OH NH 4 + OH С(NH 4 OH) C(OH) 0, 025 M < 3% Kосн = 1, 76· 10– 5
![ИП(Ca(OH)2) = [Ca] · [OH]2 ИП(Ca(OH)2) = 0, 015·(6, 63· 10– 4 )2 = ИП(Ca(OH)2) = [Ca] · [OH]2 ИП(Ca(OH)2) = 0, 015·(6, 63· 10– 4 )2 =](https://present5.com/presentation/139200531_176428522/image-35.jpg) ИП(Ca(OH)2) = [Ca] · [OH]2 ИП(Ca(OH)2) = 0, 015·(6, 63· 10– 4 )2 = = 6, 59· 10– 9 M ПР(Ca(OH)2) = 6, 5· 10– 6 ИП < ПР - осадок не выпадет
ИП(Ca(OH)2) = [Ca] · [OH]2 ИП(Ca(OH)2) = 0, 015·(6, 63· 10– 4 )2 = = 6, 59· 10– 9 M ПР(Ca(OH)2) = 6, 5· 10– 6 ИП < ПР - осадок не выпадет
 Задача. При какой концентрации ионов кальция будет образовываться осадок гидроксида кальция из раствора с р. Н = 9. Решение. ПР(Ca(OH)2) = [Ca] · [OH]2 = 6, 5· 10– 6 ПР(Ca(OH)2) [Ca] = —————— [OH]2 [OH] = 10–p. OH т. к. p. H + p. OH = 14 – 9 = 5
Задача. При какой концентрации ионов кальция будет образовываться осадок гидроксида кальция из раствора с р. Н = 9. Решение. ПР(Ca(OH)2) = [Ca] · [OH]2 = 6, 5· 10– 6 ПР(Ca(OH)2) [Ca] = —————— [OH]2 [OH] = 10–p. OH т. к. p. H + p. OH = 14 – 9 = 5
![ПР(Ca(OH)2) 6, 5· 10– 6 [Ca] = —————— = 6, 5· 103 [OH]2 (10 ПР(Ca(OH)2) 6, 5· 10– 6 [Ca] = —————— = 6, 5· 103 [OH]2 (10](https://present5.com/presentation/139200531_176428522/image-37.jpg) ПР(Ca(OH)2) 6, 5· 10– 6 [Ca] = —————— = 6, 5· 103 [OH]2 (10 – 5)2 Ответ: При р. Н=9 осадок Ca(OH)2 выпадет, если концентрация Ca 2+ будет 6, 5· 103 М и выше.
ПР(Ca(OH)2) 6, 5· 10– 6 [Ca] = —————— = 6, 5· 103 [OH]2 (10 – 5)2 Ответ: При р. Н=9 осадок Ca(OH)2 выпадет, если концентрация Ca 2+ будет 6, 5· 103 М и выше.
 Задача. При каком значении р. Н начнется образование осадка Zn(OH)2 из 0, 01 М раствора хлорида цинка. Решение. ПР(Zn(OH)2) = [Zn] · [OH]2 = 1, 4· 10– 17
Задача. При каком значении р. Н начнется образование осадка Zn(OH)2 из 0, 01 М раствора хлорида цинка. Решение. ПР(Zn(OH)2) = [Zn] · [OH]2 = 1, 4· 10– 17
![p. OH = – lg[OH] = – lg 3, 74· 10– 8 = 7, p. OH = – lg[OH] = – lg 3, 74· 10– 8 = 7,](https://present5.com/presentation/139200531_176428522/image-39.jpg) p. OH = – lg[OH] = – lg 3, 74· 10– 8 = 7, 43 т. к. p. H + p. OH = 14 p. H = 14 – 7, 43 = 6, 57 Ответ: При р. Н = 6, 57 выпадет Zn(OH)2 из 0, 01 М раствора хлорида цинка.
p. OH = – lg[OH] = – lg 3, 74· 10– 8 = 7, 43 т. к. p. H + p. OH = 14 p. H = 14 – 7, 43 = 6, 57 Ответ: При р. Н = 6, 57 выпадет Zn(OH)2 из 0, 01 М раствора хлорида цинка.
 Перевод малорастворимого осадка в раствор Mg(OH)2 Mg 2+ + 2 OH– + 2 HCl 2 Cl– + 2 H+ 2 H 2 O Mg(OH)2 Mg 2+ + 2 OH– + 2 NH 4 Cl 2 Cl– + 2 NH 4+ 2 H 2 O
Перевод малорастворимого осадка в раствор Mg(OH)2 Mg 2+ + 2 OH– + 2 HCl 2 Cl– + 2 H+ 2 H 2 O Mg(OH)2 Mg 2+ + 2 OH– + 2 NH 4 Cl 2 Cl– + 2 NH 4+ 2 H 2 O
 Перевод одного малорастворимого электролита в другой Ag 2 Cr. O 4 2 Ag+ + Cr. O 42– + 2 KCl 2 Cl– + 2 K+ 2 Ag. Cl ПР(Ag. Cl) = 1, 78· 10– 10 S(Ag. Cl) = 1, 33· 10– 5 ПР(Ag 2 Cr. O 4) = 3, 5· 10– 11 S(Ag 2 Cr. O 4) = 2, 06· 10– 4
Перевод одного малорастворимого электролита в другой Ag 2 Cr. O 4 2 Ag+ + Cr. O 42– + 2 KCl 2 Cl– + 2 K+ 2 Ag. Cl ПР(Ag. Cl) = 1, 78· 10– 10 S(Ag. Cl) = 1, 33· 10– 5 ПР(Ag 2 Cr. O 4) = 3, 5· 10– 11 S(Ag 2 Cr. O 4) = 2, 06· 10– 4
 Перевод сульфатов бария, стронция и кальция в карбонаты Ca. SO 4 + Na 2 CO 3 Ca. CO 3 + Na 2 SO 4 ПР(Ca. SO 4) = 2, 5· 10– 5 ПР(Ca. CO 3) = 3, 8· 10– 9 S(Ca. SO 4) = 5, 0· 10– 3 S(Ca. CO 3) = 6, 16· 10– 5 Sr. SO 4 + Na 2 CO 3 Sr. CO 3 + Na 2 SO 4 ПР(Sr. SO 4) = 3, 2· 10– 7 ПР(Sr. CO 3) = 1, 1· 10– 10 S(Sr. SO 4) = 5, 66· 10– 4 S(Sr. CO 3) = 1, 05· 10– 5
Перевод сульфатов бария, стронция и кальция в карбонаты Ca. SO 4 + Na 2 CO 3 Ca. CO 3 + Na 2 SO 4 ПР(Ca. SO 4) = 2, 5· 10– 5 ПР(Ca. CO 3) = 3, 8· 10– 9 S(Ca. SO 4) = 5, 0· 10– 3 S(Ca. CO 3) = 6, 16· 10– 5 Sr. SO 4 + Na 2 CO 3 Sr. CO 3 + Na 2 SO 4 ПР(Sr. SO 4) = 3, 2· 10– 7 ПР(Sr. CO 3) = 1, 1· 10– 10 S(Sr. SO 4) = 5, 66· 10– 4 S(Sr. CO 3) = 1, 05· 10– 5
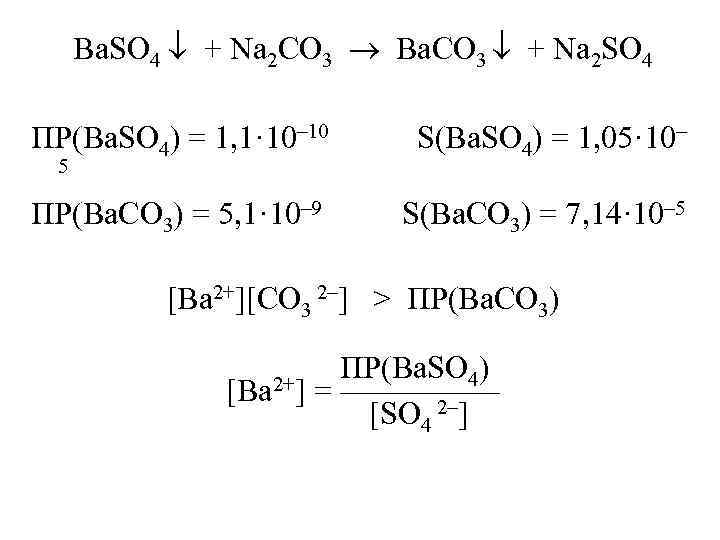 Ba. SO 4 + Na 2 CO 3 Ba. CO 3 + Na 2 SO 4 ПР(Ba. SO 4) = 1, 1· 10– 10 S(Ba. SO 4) = 1, 05· 10– ПР(Ba. CO 3) = 5, 1· 10– 9 S(Ba. CO 3) = 7, 14· 10– 5 5 [Ba 2+][CO 3 2–] > ПР(Ba. CO 3) [Ba 2+] ПР(Ba. SO 4) = ————— [SO 4 2–]
Ba. SO 4 + Na 2 CO 3 Ba. CO 3 + Na 2 SO 4 ПР(Ba. SO 4) = 1, 1· 10– 10 S(Ba. SO 4) = 1, 05· 10– ПР(Ba. CO 3) = 5, 1· 10– 9 S(Ba. CO 3) = 7, 14· 10– 5 5 [Ba 2+][CO 3 2–] > ПР(Ba. CO 3) [Ba 2+] ПР(Ba. SO 4) = ————— [SO 4 2–]
![ПР(Ba. SO 4) ————— > [SO 4 2–] ПР(Ba. CO 3) ————— [CO 3 ПР(Ba. SO 4) ————— > [SO 4 2–] ПР(Ba. CO 3) ————— [CO 3](https://present5.com/presentation/139200531_176428522/image-44.jpg) ПР(Ba. SO 4) ————— > [SO 4 2–] ПР(Ba. CO 3) ————— [CO 3 2–] ————— > [SO 4 2–] ПР(Ba. CO 3) ————— ПР(Ba. SO 4) [CO 3 2–] ————— > [SO 4 2–] 5, 1· 10– 9 ————— = 46, 4 1, 1· 10– 10
ПР(Ba. SO 4) ————— > [SO 4 2–] ПР(Ba. CO 3) ————— [CO 3 2–] ————— > [SO 4 2–] ПР(Ba. CO 3) ————— ПР(Ba. SO 4) [CO 3 2–] ————— > [SO 4 2–] 5, 1· 10– 9 ————— = 46, 4 1, 1· 10– 10


