Теория растворов.ppt
- Количество слайдов: 22
 Растворение. Растворимость веществ.
Растворение. Растворимость веществ.
 Цель урока: • Познакомиться с растворением как физико-химическим процессом и растворами как физико-химическими системами. • Выявить зависимость растворимости твердых веществ от температуры. • Рассмотреть классификацию растворов по признаку растворимости.
Цель урока: • Познакомиться с растворением как физико-химическим процессом и растворами как физико-химическими системами. • Выявить зависимость растворимости твердых веществ от температуры. • Рассмотреть классификацию растворов по признаку растворимости.
 Растворами называют гомогенную систему, состоящую из двух или большего числа составных частей (компонентов), относительное содержание которых может непрерывно изменяться в тех или иных пределах. Главный признак растворов- непрерывное изменение состава при сохранении однородности Важная особенность – простыми физическими приемами можно выделить чистые исходные компоненты. К растворам относят: • гомогенные смеси • соединения переменного состава Компоненты раствора Растворитель растворенное вещество
Растворами называют гомогенную систему, состоящую из двух или большего числа составных частей (компонентов), относительное содержание которых может непрерывно изменяться в тех или иных пределах. Главный признак растворов- непрерывное изменение состава при сохранении однородности Важная особенность – простыми физическими приемами можно выделить чистые исходные компоненты. К растворам относят: • гомогенные смеси • соединения переменного состава Компоненты раствора Растворитель растворенное вещество
 Теории растворов.
Теории растворов.
 Физическая теория. • Основоположники теории: Вант Гофф, Оствальд, Аррениус. • Растворение– процесс диффузии. • Растворы– однородные смеси. Сванте Аррениус
Физическая теория. • Основоположники теории: Вант Гофф, Оствальд, Аррениус. • Растворение– процесс диффузии. • Растворы– однородные смеси. Сванте Аррениус
 Химическая теория. • Основоположники: Менделеев, Каблуков, Иван Алексеевич Каблуков Кистяковский. • Растворение – это процесс химического взаимодействия растворяемого вещества с водой – процесс гидратации. • Растворы – это соединениягидраты.
Химическая теория. • Основоположники: Менделеев, Каблуков, Иван Алексеевич Каблуков Кистяковский. • Растворение – это процесс химического взаимодействия растворяемого вещества с водой – процесс гидратации. • Растворы – это соединениягидраты.
 Современная теория. • Растворение – это физико-химический процесс. • Растворы – это однородные (гомогенные) системы, состоящие из частиц растворенного вещества, растворителя и продуктов их взаимодействия – гидратов.
Современная теория. • Растворение – это физико-химический процесс. • Растворы – это однородные (гомогенные) системы, состоящие из частиц растворенного вещества, растворителя и продуктов их взаимодействия – гидратов.
 Растворение Физический процесс – результат диффузии веществ Химический процесс – взаимодействие вещества с водой и образование гидратов Состав раствора Растворенное вещество Растворитель Гидраты растворенных веществ
Растворение Физический процесс – результат диффузии веществ Химический процесс – взаимодействие вещества с водой и образование гидратов Состав раствора Растворенное вещество Растворитель Гидраты растворенных веществ
 Гидраты Постоянный состав (в растворах) Не постоянный состав (в кристаллогидратах) Медный купорос – Cu. SO 4 · 5 H 2 O Глауберова соль – Na 2 SO 4 · 10 H 2 O
Гидраты Постоянный состав (в растворах) Не постоянный состав (в кристаллогидратах) Медный купорос – Cu. SO 4 · 5 H 2 O Глауберова соль – Na 2 SO 4 · 10 H 2 O
 Признаки химического взаимодействия при растворении.
Признаки химического взаимодействия при растворении.
 1. Тепловые явления экзотермические эндотермические 2. Изменение цвета Белые кристаллы Cu. SO 4 (безводного) выпаривание Приливание воды Синие кристаллы Cu. SO 4 · 5 H 2 O, раствор голубого цвета
1. Тепловые явления экзотермические эндотермические 2. Изменение цвета Белые кристаллы Cu. SO 4 (безводного) выпаривание Приливание воды Синие кристаллы Cu. SO 4 · 5 H 2 O, раствор голубого цвета
 Растворимость - ? От чего зависит растворимость веществ?
Растворимость - ? От чего зависит растворимость веществ?
 Факторы влияющие на растворимость веществ • 1. Природа растворенного вещества • 2. Природа растворителя • 3. Температура • 4. Масса растворенного вещества
Факторы влияющие на растворимость веществ • 1. Природа растворенного вещества • 2. Природа растворителя • 3. Температура • 4. Масса растворенного вещества
 Природа растворенного вещества Хлорид кальция Ca. Cl 2 Гидроксид кальция Ca(OH)2 Карбонат кальция Ca. CO 3 хорошо растворимые (в 100 г H 2 O больше 1 г вещества) малорастворимые (в 100 г H 2 O меньше 1 г вещества) нерастворимые (в 100 г H 2 O меньше 0, 01 г вещества) Вещества РАСТВОРИМОСТЬ НЕКОТОРЫХ СОЛЕЙ В 100 г ВОДЫ ПРИ 20 °С Хорошо растворимые Сульфат меди Нитрат калия Иодид натрия Малорастворимые Cu. S 04 KN 03 Nal 22, 2 31, 6 179, 10 Сульфат серебра Сульфат кальция Иодид свинца Практически нерастворимые Ag 2 S 04 Ca. S 04 Pbl 2 0, 79 0, 20 0, 07 Бромид серебра Хлорид серебра Иодид серебра Ag. Br Ag. Cl Agl 0, 0037 0, 00009 0, 000003
Природа растворенного вещества Хлорид кальция Ca. Cl 2 Гидроксид кальция Ca(OH)2 Карбонат кальция Ca. CO 3 хорошо растворимые (в 100 г H 2 O больше 1 г вещества) малорастворимые (в 100 г H 2 O меньше 1 г вещества) нерастворимые (в 100 г H 2 O меньше 0, 01 г вещества) Вещества РАСТВОРИМОСТЬ НЕКОТОРЫХ СОЛЕЙ В 100 г ВОДЫ ПРИ 20 °С Хорошо растворимые Сульфат меди Нитрат калия Иодид натрия Малорастворимые Cu. S 04 KN 03 Nal 22, 2 31, 6 179, 10 Сульфат серебра Сульфат кальция Иодид свинца Практически нерастворимые Ag 2 S 04 Ca. S 04 Pbl 2 0, 79 0, 20 0, 07 Бромид серебра Хлорид серебра Иодид серебра Ag. Br Ag. Cl Agl 0, 0037 0, 00009 0, 000003
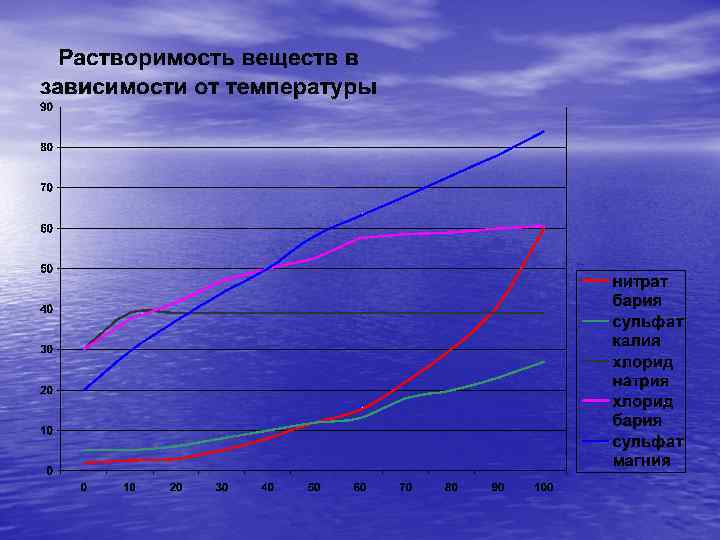
 Зависимость растворимости веществ от природы растворителя Растворение медного купороса в спирте Спиртовой раствор йода Растворение медного купороса в воде
Зависимость растворимости веществ от природы растворителя Растворение медного купороса в спирте Спиртовой раствор йода Растворение медного купороса в воде
 Классификация растворов по признаку растворимости Ненасыщенный раствор: при данной температуре находится меньше растворяемого вещества, чем в его насыщенном растворе Насыщенный раствор: при данной температуре вещество больше не растворяется Пересыщенный раствор: в растворенном состоянии больше вещества, чем его в насыщенном растворе
Классификация растворов по признаку растворимости Ненасыщенный раствор: при данной температуре находится меньше растворяемого вещества, чем в его насыщенном растворе Насыщенный раствор: при данной температуре вещество больше не растворяется Пересыщенный раствор: в растворенном состоянии больше вещества, чем его в насыщенном растворе
 Типы растворов по содержанию растворенного вещества Ненасыщенные – если содержание в растворенного вещества ниже отвечающего равновесию (ниже растворимости). Содержание вещества в растворе больше 0, но меньше растворимости. Насыщенный – такой раствор, в котором содержание растворенного вещества отвечает установлению при данной температуре равновесия между этим веществом и раствором. Перенасыщенный – такой раствор , где содержание вещества больше, чем насыщенном растворе.
Типы растворов по содержанию растворенного вещества Ненасыщенные – если содержание в растворенного вещества ниже отвечающего равновесию (ниже растворимости). Содержание вещества в растворе больше 0, но меньше растворимости. Насыщенный – такой раствор, в котором содержание растворенного вещества отвечает установлению при данной температуре равновесия между этим веществом и раствором. Перенасыщенный – такой раствор , где содержание вещества больше, чем насыщенном растворе.
 Ответьте на вопросы : 1. От чего не зависит растворимость твердых веществ? А) от природы растворителя Б) от природы растворенного вещества В) от давления Г) от температуры 2. Как меняется растворимость гидроксида кальция в воде при понижении температуры? А) понижается В) увеличивается Б) остается постоянной Г) не знаю 3. Какое из веществ является практически нерастворимым? А) нитрат серебра В) гидроксид кальция Б) сульфат бария Г) не знаю 4. К 100 мл H 2 O добавили 10 г карбоната кальция. Какова массовая доля вещества в полученном растворе? А) 10% Б) 9, 1% В) 5% Г) 0%
Ответьте на вопросы : 1. От чего не зависит растворимость твердых веществ? А) от природы растворителя Б) от природы растворенного вещества В) от давления Г) от температуры 2. Как меняется растворимость гидроксида кальция в воде при понижении температуры? А) понижается В) увеличивается Б) остается постоянной Г) не знаю 3. Какое из веществ является практически нерастворимым? А) нитрат серебра В) гидроксид кальция Б) сульфат бария Г) не знаю 4. К 100 мл H 2 O добавили 10 г карбоната кальция. Какова массовая доля вещества в полученном растворе? А) 10% Б) 9, 1% В) 5% Г) 0%
 Применение растворов в промышленности
Применение растворов в промышленности
 Применение растворов в сельском хозяйстве
Применение растворов в сельском хозяйстве
 Применение растворов в быту и медицине
Применение растворов в быту и медицине


