Презентация2.pptx
- Количество слайдов: 53

 Раствор - гомогенная (однородная) смесь, состоящая из частиц растворённого вещества, растворителя и продуктов их взаимодействия.
Раствор - гомогенная (однородная) смесь, состоящая из частиц растворённого вещества, растворителя и продуктов их взаимодействия.

 Растворитель — компонент, агрегатное состояние которого не изменяется при образовании раствора. В случае же растворов, образующихся при смешении газа с газом, жидкости с жидкостью, твёрдого вещества с твёрдым, растворителем считается компонент, количество которого в растворе преобладает.
Растворитель — компонент, агрегатное состояние которого не изменяется при образовании раствора. В случае же растворов, образующихся при смешении газа с газом, жидкости с жидкостью, твёрдого вещества с твёрдым, растворителем считается компонент, количество которого в растворе преобладает.
 Как происходит растворение? Существовали две теории растворов Физическая теория: Химическая теория: Аррениус Менделеев Оствальд Каблуков Вант-Гофф
Как происходит растворение? Существовали две теории растворов Физическая теория: Химическая теория: Аррениус Менделеев Оствальд Каблуков Вант-Гофф
 Физическая теория • Растворение – это проникновение частиц одного вещества между частицами другого (растворителя); • Это основано на явлении диффузии; • Нового вещества в растворе не образуется; • Растворение – физическое явление. Раствор – это система из 2 -х компонентов: растворителя и растворенного вещества.
Физическая теория • Растворение – это проникновение частиц одного вещества между частицами другого (растворителя); • Это основано на явлении диффузии; • Нового вещества в растворе не образуется; • Растворение – физическое явление. Раствор – это система из 2 -х компонентов: растворителя и растворенного вещества.
 Химическая теория • При растворении в воде серной кислоты выделяется тепло; • Растворение – это химическое явление; • Растворенное вещество вступает в реакцию с водой и образуются гидраты; • Гидраты – это продукты взаимодействия воды и растворенного вещества; Растворы – это системы из 3 -х компонентов: растворителя, растворенного вещества и продуктов их взаимодействия
Химическая теория • При растворении в воде серной кислоты выделяется тепло; • Растворение – это химическое явление; • Растворенное вещество вступает в реакцию с водой и образуются гидраты; • Гидраты – это продукты взаимодействия воды и растворенного вещества; Растворы – это системы из 3 -х компонентов: растворителя, растворенного вещества и продуктов их взаимодействия
 Растворимость - это масса вещества, способная раствориться в 100 г растворителя (воды) при стандартных условиях.
Растворимость - это масса вещества, способная раствориться в 100 г растворителя (воды) при стандартных условиях.
 Растворимость зависит от: Природы вещества, т. е. особенностей его строения От температуры
Растворимость зависит от: Природы вещества, т. е. особенностей его строения От температуры
 Зависимость растворимости от температуры • У твердых веществ при повышении температуры растворимость увеличивается (быстрее движутся молекулы, ускоряется диффузия) • У газов при повышении температуры растворимость уменьшается (молекулы улетучиваются)
Зависимость растворимости от температуры • У твердых веществ при повышении температуры растворимость увеличивается (быстрее движутся молекулы, ускоряется диффузия) • У газов при повышении температуры растворимость уменьшается (молекулы улетучиваются)
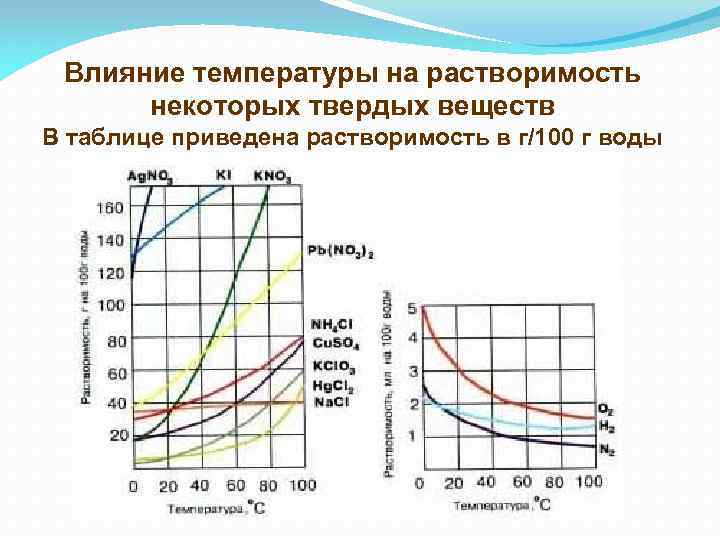 Влияние температуры на растворимость некоторых твердых веществ В таблице приведена растворимость в г/100 г воды
Влияние температуры на растворимость некоторых твердых веществ В таблице приведена растворимость в г/100 г воды
 По растворимости выделяют • Хорошо растворимые вещества (в 100 г воды растворяется > 1 г вещества) • Малорастворимые (в 100 г воды растворяется < 1 г вещества) • Нерастворимые (в 100 г воды растворяется < 0, 01 г вещества)
По растворимости выделяют • Хорошо растворимые вещества (в 100 г воды растворяется > 1 г вещества) • Малорастворимые (в 100 г воды растворяется < 1 г вещества) • Нерастворимые (в 100 г воды растворяется < 0, 01 г вещества)
 По способности проводить или не проводить электрический ток в растворе: Вещества Электролиты Неэлектролиты
По способности проводить или не проводить электрический ток в растворе: Вещества Электролиты Неэлектролиты
 Электролиты Вещества, расплавы или растворы которые проводят электрический ток вследствие диссоциации на ионы, однако сами вещества не проводят электрический ток. Примерами электролитов могут служить растворы кислот, солей и оснований.
Электролиты Вещества, расплавы или растворы которые проводят электрический ток вследствие диссоциации на ионы, однако сами вещества не проводят электрический ток. Примерами электролитов могут служить растворы кислот, солей и оснований.
 Неэлектролиты Вещества, водные растворы и распла-вы которых не проводят электрический ток. Они содержат ковалентные не-полярные или малополярные связи, которые не распадаются на ионы. К ним относятся газы, твердые вещества (неметаллы), органические соединения (сахароза, бензин, спирт).
Неэлектролиты Вещества, водные растворы и распла-вы которых не проводят электрический ток. Они содержат ковалентные не-полярные или малополярные связи, которые не распадаются на ионы. К ним относятся газы, твердые вещества (неметаллы), органические соединения (сахароза, бензин, спирт).
 Электролитическая диссоциация — процесс распада электролита на ионы при растворении его в полярном растворителе или при плавлении. Диссоциация в растворах: взаимодействие растворённого вещества с растворителем.
Электролитическая диссоциация — процесс распада электролита на ионы при растворении его в полярном растворителе или при плавлении. Диссоциация в растворах: взаимодействие растворённого вещества с растворителем.
 Особенности растворения различных веществ в воде • Металлы • Щелочные металлы • Оксиды
Особенности растворения различных веществ в воде • Металлы • Щелочные металлы • Оксиды
 Металлы Растворение кальция (Са) в воде: Са + H 2 O Ca(OH)2 +H 2 Раствор мутный, появляются белые взвешенные частицы – известь, или гидроксид кальция, выделяется водород.
Металлы Растворение кальция (Са) в воде: Са + H 2 O Ca(OH)2 +H 2 Раствор мутный, появляются белые взвешенные частицы – известь, или гидроксид кальция, выделяется водород.
 Металлы Растворение натрия (Na) в воде: 2 Na +2 H 2 O 2 Na. OH + H 2 В растворе содержится гидроксид натрия (Na. OH), натрий всплывает на поверхность, плавится, превращаясь в блестящую каплю, выделяется водород.
Металлы Растворение натрия (Na) в воде: 2 Na +2 H 2 O 2 Na. OH + H 2 В растворе содержится гидроксид натрия (Na. OH), натрий всплывает на поверхность, плавится, превращаясь в блестящую каплю, выделяется водород.
 Щелочные металлы Важное свойство щелочных металлов - их высокая активность по отношению к воде. Наиболее спокойно (без взрыва) реагирует с водой литий: Li + 2 H 2 O 2 Li. OH + H 2
Щелочные металлы Важное свойство щелочных металлов - их высокая активность по отношению к воде. Наиболее спокойно (без взрыва) реагирует с водой литий: Li + 2 H 2 O 2 Li. OH + H 2
 Щелочные металлы При проведении аналогичной реакции натрий горит жёлтым пламенем и происходит небольшой взрыв. 2 Na +2 H 2 O 2 Na. OH + H 2 Калий ещё более активен: в этом случае взрыв гораздо сильнее, а пламя окрашено в фиолетовый цвет.
Щелочные металлы При проведении аналогичной реакции натрий горит жёлтым пламенем и происходит небольшой взрыв. 2 Na +2 H 2 O 2 Na. OH + H 2 Калий ещё более активен: в этом случае взрыв гораздо сильнее, а пламя окрашено в фиолетовый цвет.
 Оксиды Растворимость в воде: • все кислотные оксиды, кроме Si. O 2, растворимы в воде; • основные только оксиды щелочных металлов( Li 2 O, Na 2 O, K 2 O, Rb 2 O, Cs 2 O) • щелочноземельные( Ca. O, Sr. O, Ba. O); • амфотерные оксиды не растворяются в воде
Оксиды Растворимость в воде: • все кислотные оксиды, кроме Si. O 2, растворимы в воде; • основные только оксиды щелочных металлов( Li 2 O, Na 2 O, K 2 O, Rb 2 O, Cs 2 O) • щелочноземельные( Ca. O, Sr. O, Ba. O); • амфотерные оксиды не растворяются в воде
 Оксиды Примеры растворения некоторых оксидов в воде: Основные оксиды: • K 2 O + H 2 O = 2 KOH Кислотные оксиды: • SO 3 + H 2 O = H 2 SO 4
Оксиды Примеры растворения некоторых оксидов в воде: Основные оксиды: • K 2 O + H 2 O = 2 KOH Кислотные оксиды: • SO 3 + H 2 O = H 2 SO 4
 Оксиды • При растворении основных оксидов в воде образуются кислоты (кислотные гидроксиды); • При растворении основных оксидов в воде образуются основания(основные гидроксиды); • Не все кислотные и основные оксиды растворяются в воде.
Оксиды • При растворении основных оксидов в воде образуются кислоты (кислотные гидроксиды); • При растворении основных оксидов в воде образуются основания(основные гидроксиды); • Не все кислотные и основные оксиды растворяются в воде.

 Виды растворов: Выделяют: • Водные - растворы, в которых растворителем служит вода. • Неводные - растворы, в которых растворителем служат органические вещества - спирты, эфиры, бензол и др.
Виды растворов: Выделяют: • Водные - растворы, в которых растворителем служит вода. • Неводные - растворы, в которых растворителем служат органические вещества - спирты, эфиры, бензол и др.
 Водные растворы • Если вещество образует водный раствор, который хорошо проводит электрический ток, то он называется сильным электролитом; в противном случае — слабым электролитом. Сильные электролиты в растворе почти полностью распадаются на ионы, а слабые практически не распадаются. • Вещества, растворяющиеся в воде, но не распадающиеся на ионы, называются неэлектролитами (пример — сахар).
Водные растворы • Если вещество образует водный раствор, который хорошо проводит электрический ток, то он называется сильным электролитом; в противном случае — слабым электролитом. Сильные электролиты в растворе почти полностью распадаются на ионы, а слабые практически не распадаются. • Вещества, растворяющиеся в воде, но не распадающиеся на ионы, называются неэлектролитами (пример — сахар).
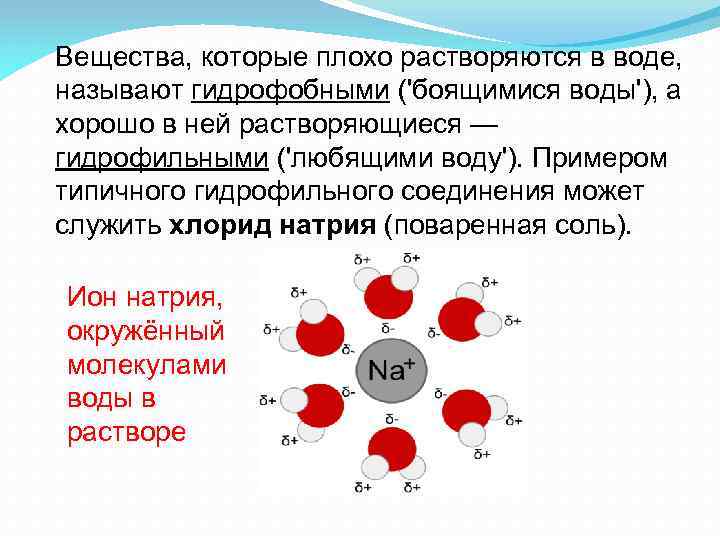 Вещества, которые плохо растворяются в воде, называют гидрофобными ('боящимися воды'), а хорошо в ней растворяющиеся — гидрофильными ('любящими воду'). Примером типичного гидрофильного соединения может служить хлорид натрия (поваренная соль). Ион натрия, окружённый молекулами воды в растворе
Вещества, которые плохо растворяются в воде, называют гидрофобными ('боящимися воды'), а хорошо в ней растворяющиеся — гидрофильными ('любящими воду'). Примером типичного гидрофильного соединения может служить хлорид натрия (поваренная соль). Ион натрия, окружённый молекулами воды в растворе
 Виды растворов по агрегатному состоянию Жидкие (растворы солей) Твердые (сплав Ni и Cu - монеты ) Газообразные (воздух)
Виды растворов по агрегатному состоянию Жидкие (растворы солей) Твердые (сплав Ni и Cu - монеты ) Газообразные (воздух)
 Виды растворов по количеству растворенного вещества Концентрированные Разбавлен -ные
Виды растворов по количеству растворенного вещества Концентрированные Разбавлен -ные
 • Концентрированные растворы - растворы с большим содержанием растворенного вещества. • Разбавленные растворы - растворы с небольшим содержанием растворенного вещества.
• Концентрированные растворы - растворы с большим содержанием растворенного вещества. • Разбавленные растворы - растворы с небольшим содержанием растворенного вещества.
 Виды растворов в зависимости от количества частиц, переходящих в раствор Ненасыщенные Насыщенные Пере-насыщенные
Виды растворов в зависимости от количества частиц, переходящих в раствор Ненасыщенные Насыщенные Пере-насыщенные
 • Ненасыщенный раствор - это раствор, в котором при данной температуре вещество ещё может растворяться. • Насыщенный раствор – это раствор, в котором данное вещество при данной температуре больше не растворяется. • Перенасыщенный раствор – раствор, в котором при заданной температуре и давлении концентрация растворенного вещества больше, чем в насыщенном растворе.
• Ненасыщенный раствор - это раствор, в котором при данной температуре вещество ещё может растворяться. • Насыщенный раствор – это раствор, в котором данное вещество при данной температуре больше не растворяется. • Перенасыщенный раствор – раствор, в котором при заданной температуре и давлении концентрация растворенного вещества больше, чем в насыщенном растворе.
 Структура и уникальные свойства воды Вода – самое распространенное неорганическое соединение на нашей планете. Свойства воды: H 2 O M=18 г/моль tзам = 00 С tкип = 1000 С
Структура и уникальные свойства воды Вода – самое распространенное неорганическое соединение на нашей планете. Свойства воды: H 2 O M=18 г/моль tзам = 00 С tкип = 1000 С
 Агрегатные состояния: Твердое Жидкое Газообразное
Агрегатные состояния: Твердое Жидкое Газообразное
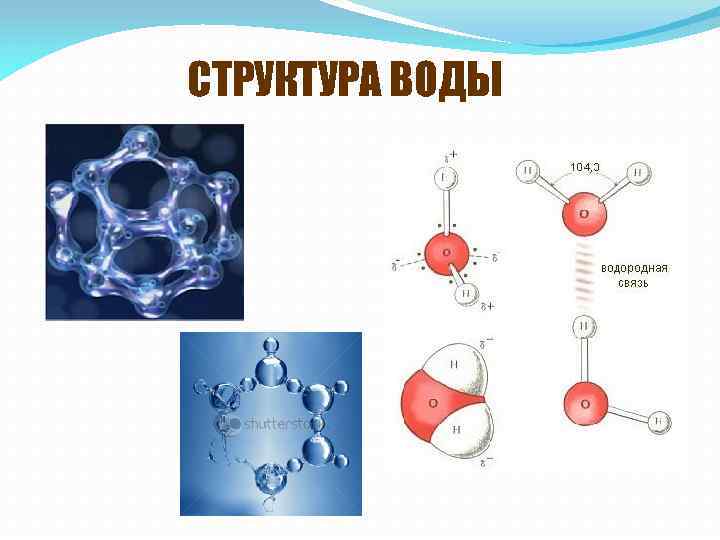 СТРУКТУРА ВОДЫ
СТРУКТУРА ВОДЫ
 Молекула воды представляет собой маленький диполь, содержащий положительный и отрицательный заряды на полюсах. Так как масса и заряд ядра кислорода больше чем у ядер водорода, то электронное облако стягивается в сторону кислородного ядра. При этом ядра водорода "оголяются". Таким образом, электронное облако имеет неоднородную плотность. Около ядер водорода имеется недостаток электронной плотности, а на противоположной стороне молекулы, около ядра кислорода, наблюдается избыток электронной плотности. Именно такая структура и определяет полярность молекулы воды. Если соединить прямыми линиями эпицентры положительных и отрицательных зарядов получится объемная геометрическая фигура - правильный тетраэдр.
Молекула воды представляет собой маленький диполь, содержащий положительный и отрицательный заряды на полюсах. Так как масса и заряд ядра кислорода больше чем у ядер водорода, то электронное облако стягивается в сторону кислородного ядра. При этом ядра водорода "оголяются". Таким образом, электронное облако имеет неоднородную плотность. Около ядер водорода имеется недостаток электронной плотности, а на противоположной стороне молекулы, около ядра кислорода, наблюдается избыток электронной плотности. Именно такая структура и определяет полярность молекулы воды. Если соединить прямыми линиями эпицентры положительных и отрицательных зарядов получится объемная геометрическая фигура - правильный тетраэдр.
 Уникальные свойства воды • Вода - единственная жидкость на Земле, у которой зависимость удельной теплоемкости от температуры имеет минимум. Этот минимум наблюдается при температуре +35 0 С. При этом нормальная температура тела человека, состоящего на две трети (а в юном возрасте и того более) из воды, находится в диапазоне температур 36 -38 0 С.
Уникальные свойства воды • Вода - единственная жидкость на Земле, у которой зависимость удельной теплоемкости от температуры имеет минимум. Этот минимум наблюдается при температуре +35 0 С. При этом нормальная температура тела человека, состоящего на две трети (а в юном возрасте и того более) из воды, находится в диапазоне температур 36 -38 0 С.
 • Теплоемкость воды аномально высока. Чтобы нагреть определенное ее количество на один градус, необходимо затратить больше энергии, чем при нагреве других жидкостей. • Удельная теплоемкость воды составляет 4180 Дж/(кг· 0 С) при 0 0 С. Удельная теплота плавления при переходе льда в жидкое состояние составляет 330 к. Дж/кг, удельная теплота парообразования - 2250 к. Дж/кг при нормальном давлении и температуре 100 0 С.
• Теплоемкость воды аномально высока. Чтобы нагреть определенное ее количество на один градус, необходимо затратить больше энергии, чем при нагреве других жидкостей. • Удельная теплоемкость воды составляет 4180 Дж/(кг· 0 С) при 0 0 С. Удельная теплота плавления при переходе льда в жидкое состояние составляет 330 к. Дж/кг, удельная теплота парообразования - 2250 к. Дж/кг при нормальном давлении и температуре 100 0 С.
 Плотность - еще одна уникальность воды. Плотность воды при охлаждении от 100 до 3, 98 0 С возрастает, как и у подавляющего большинства жидкостей. Но, достигнув максимального значения при температуре 3, 98 0 С, плотность при дальнейшем охлаждении воды начинает уменьшаться. Другими словами, максимальная плотность воды наблюдается при температуре 3, 98 0 С , а не при температуре замерзания 0 0 С.
Плотность - еще одна уникальность воды. Плотность воды при охлаждении от 100 до 3, 98 0 С возрастает, как и у подавляющего большинства жидкостей. Но, достигнув максимального значения при температуре 3, 98 0 С, плотность при дальнейшем охлаждении воды начинает уменьшаться. Другими словами, максимальная плотность воды наблюдается при температуре 3, 98 0 С , а не при температуре замерзания 0 0 С.
 • Вода - самый сильный универсальный растворитель. Если ей дать достаточно времени, она может растворить практически любое твердое вещество. Именно из-за уникальной растворяющей способности воды никому до сих пор не удалось получить химически чистую воду - она всегда содержит растворенный материал сосуда.
• Вода - самый сильный универсальный растворитель. Если ей дать достаточно времени, она может растворить практически любое твердое вещество. Именно из-за уникальной растворяющей способности воды никому до сих пор не удалось получить химически чистую воду - она всегда содержит растворенный материал сосуда.
 Способы выражения состава раствора • Массовая доля – С% • Молярная концентрация – См • Нормальная (эквивалентная) концентрация – Сн
Способы выражения состава раствора • Массовая доля – С% • Молярная концентрация – См • Нормальная (эквивалентная) концентрация – Сн
 Массовая доля – отношение (обычно – процентное) массы растворённого вещества к массе раствора. Например, 15% (масс. ) водный раствор хлорида натрия – это такой раствор в 100 единицах массы которого содержится 15 единиц массы Na. Cl и 85 единиц массы воды.
Массовая доля – отношение (обычно – процентное) массы растворённого вещества к массе раствора. Например, 15% (масс. ) водный раствор хлорида натрия – это такой раствор в 100 единицах массы которого содержится 15 единиц массы Na. Cl и 85 единиц массы воды.
 Молярная концентрация, или молярность – отношение количества растворённого вещества к объёму раствора. Обычно молярность обозначается СМ или (после численного значения молярности) М. Так, 2 М H 2 SO 4 означает раствор, в каждом литре которого содержится 2 моля серной кислоты, т. е. СМ=2 моль/л.
Молярная концентрация, или молярность – отношение количества растворённого вещества к объёму раствора. Обычно молярность обозначается СМ или (после численного значения молярности) М. Так, 2 М H 2 SO 4 означает раствор, в каждом литре которого содержится 2 моля серной кислоты, т. е. СМ=2 моль/л.
 Эквивалентная, или нормальная концентрация – отношение числа эквивалентов растворённого вещест- ва к объёму раствора. Концентрация, выраженная этим способом, обозначается СН или (после численного значения нормальности) буквой н. Так 2 н H 2 SO 4 означает раствор, в каждом литре которого содержится 2 эквивалента серной кислоты, т. е. СН(1/2 H 2 SO 4)=2 моль/л.
Эквивалентная, или нормальная концентрация – отношение числа эквивалентов растворённого вещест- ва к объёму раствора. Концентрация, выраженная этим способом, обозначается СН или (после численного значения нормальности) буквой н. Так 2 н H 2 SO 4 означает раствор, в каждом литре которого содержится 2 эквивалента серной кислоты, т. е. СН(1/2 H 2 SO 4)=2 моль/л.
 Водородный показатель (PH) как мера кислотности (основности) среды Водородный показатель, p. H — мера активности (в очень разбавленных растворах она эквивалентна концентрации) ионов водорода в растворе, и количественно выражающая его кислотность, вычисляется как отрицательный десятичный логарифм активности водородных ионов, выраженной в молях на литр.
Водородный показатель (PH) как мера кислотности (основности) среды Водородный показатель, p. H — мера активности (в очень разбавленных растворах она эквивалентна концентрации) ионов водорода в растворе, и количественно выражающая его кислотность, вычисляется как отрицательный десятичный логарифм активности водородных ионов, выраженной в молях на литр.
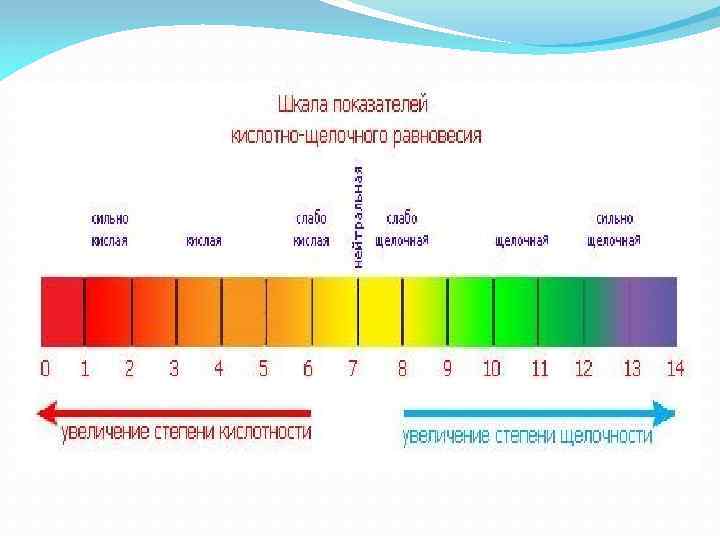
 Мера кислотности / щелочности водного раствора Чем меньше значение p. H, тем кислее раствор; чем оно больше, тем он щелочнее. Нейтральному состоянию соответствует значение p. H = 7.
Мера кислотности / щелочности водного раствора Чем меньше значение p. H, тем кислее раствор; чем оно больше, тем он щелочнее. Нейтральному состоянию соответствует значение p. H = 7.
 Нейтрализация - перевод раствора, демонстрирующего кислую или щелочную реакцию, в нейтральное состояние посредством добавки компонента с противоположной реак-цией. Таким образом, кислоты нейтрали-зуются щелочами, а щелочи – кислотами.
Нейтрализация - перевод раствора, демонстрирующего кислую или щелочную реакцию, в нейтральное состояние посредством добавки компонента с противоположной реак-цией. Таким образом, кислоты нейтрали-зуются щелочами, а щелочи – кислотами.
 Концентрация - в отношении концентрации действует следующее правило: как можно меньше – ровно столько, сколько нужно. Оптимальное значение может быть определено лишь с учетом местных условий.
Концентрация - в отношении концентрации действует следующее правило: как можно меньше – ровно столько, сколько нужно. Оптимальное значение может быть определено лишь с учетом местных условий.
![Водородный показатель (PH) +] р. Н=-lg[H р. Н влияет на: • возможность протекания той Водородный показатель (PH) +] р. Н=-lg[H р. Н влияет на: • возможность протекания той](https://present5.com/presentation/153280779_138290050/image-51.jpg) Водородный показатель (PH) +] р. Н=-lg[H р. Н влияет на: • возможность протекания той или иной реакции • результат той или иной реакции Также р. Н используется для характеристики кислотно-основных свойств различных биологических сред.
Водородный показатель (PH) +] р. Н=-lg[H р. Н влияет на: • возможность протекания той или иной реакции • результат той или иной реакции Также р. Н используется для характеристики кислотно-основных свойств различных биологических сред.
 Таким образом, растворы - однородная многокомпонентная система, состоящая из растворителя, растворённых веществ и продуктов их взаимодействия, относительные количества которых могут изменяться в широких пределах. Этот термин может относиться к любому агрегатному состоянию системы.
Таким образом, растворы - однородная многокомпонентная система, состоящая из растворителя, растворённых веществ и продуктов их взаимодействия, относительные количества которых могут изменяться в широких пределах. Этот термин может относиться к любому агрегатному состоянию системы.
 Растворы находят широкое применение в самых различных областях практики. Категории растворов относятся и природный раствор воды, и такие материалы, как сырая нефть и различные нефтепродукты - бензин, керосин, вазелин, парафин, смазочные масла, жидкие сплавы металлов, расплавленные смеси силикатов смеси органических растворителей, различные водно-спиртовые смеси и др.
Растворы находят широкое применение в самых различных областях практики. Категории растворов относятся и природный раствор воды, и такие материалы, как сырая нефть и различные нефтепродукты - бензин, керосин, вазелин, парафин, смазочные масла, жидкие сплавы металлов, расплавленные смеси силикатов смеси органических растворителей, различные водно-спиртовые смеси и др.


