yhlas.ppt
- Количество слайдов: 46

 Раство р — гомогенная (однородная) смесь, состоящая из частиц растворённого вещества, растворителя и продуктов их взаимодействия.
Раство р — гомогенная (однородная) смесь, состоящая из частиц растворённого вещества, растворителя и продуктов их взаимодействия.
 Растворение соли в воде
Растворение соли в воде
 l Растворитель — компонент, агрегатное состояние которого не изменяется при образовании раствора. В случае же растворов, образующихся при смешении газа с газом, жидкости с жидкостью, твёрдого вещества с твёрдым, растворителем считается компонент, количество которого в растворе преобладает.
l Растворитель — компонент, агрегатное состояние которого не изменяется при образовании раствора. В случае же растворов, образующихся при смешении газа с газом, жидкости с жидкостью, твёрдого вещества с твёрдым, растворителем считается компонент, количество которого в растворе преобладает.

 По характеру взятого растворителя: водные неводные
По характеру взятого растворителя: водные неводные
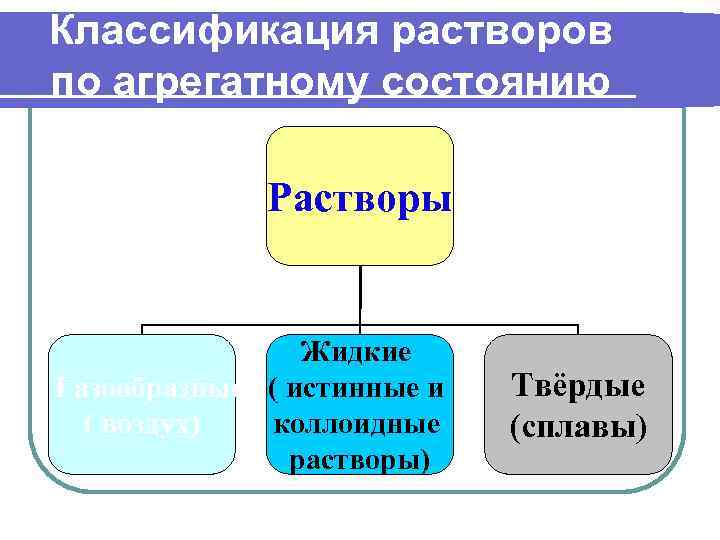 Классификация растворов по агрегатному состоянию Растворы Жидкие Газообразные ( истинные и ( воздух) коллоидные растворы) Твёрдые (сплавы)
Классификация растворов по агрегатному состоянию Растворы Жидкие Газообразные ( истинные и ( воздух) коллоидные растворы) Твёрдые (сплавы)

 По точности выражения концентрации приблизительные точные эмпирические
По точности выражения концентрации приблизительные точные эмпирические
 Следует также различать растворение: l твердых веществ, l растворение жидкостей l растворение газов.
Следует также различать растворение: l твердых веществ, l растворение жидкостей l растворение газов.
 1813 год, Лондон, Лаборатория Королевского института, Гемфри Дэви и Майкл Фарадей.
1813 год, Лондон, Лаборатория Королевского института, Гемфри Дэви и Майкл Фарадей.
 1889 г, Лейпциг l Сванте Аррениус n. Иван Алексеевич Каблуков
1889 г, Лейпциг l Сванте Аррениус n. Иван Алексеевич Каблуков
 l Концентрации растворов обычно выражают в массовых (весовых) и объемных (для жидкостей) процентах, в молях или грамм-эквивалентах, содержащихся в единице объема раствора, а также титром и моляльностью.
l Концентрации растворов обычно выражают в массовых (весовых) и объемных (для жидкостей) процентах, в молях или грамм-эквивалентах, содержащихся в единице объема раствора, а также титром и моляльностью.
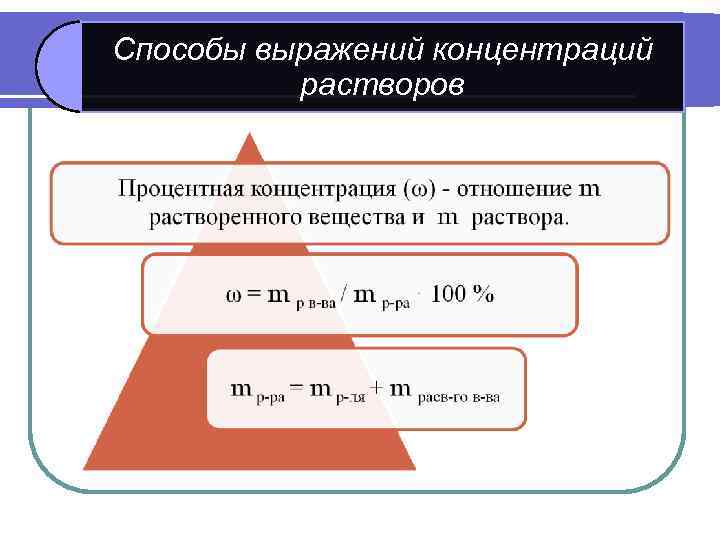 Способы выражений концентраций растворов
Способы выражений концентраций растворов
 Концентрации приблизительных растворов большей частью выражают в массовых процентах; точных — в молях, в грамм-эквивалентах, содержащихся в 1 л раствора, или титром. n
Концентрации приблизительных растворов большей частью выражают в массовых процентах; точных — в молях, в грамм-эквивалентах, содержащихся в 1 л раствора, или титром. n
 l Водные растворы широко использовать начали только несколько лет назад в строительстве. Сегодня без них туже не обойтись в процессе быстрого ремонта или монтаже. Главное преимущество водных растворов в том, что они быстро отвердевают из-за чего имеют очень большую адгезию и прочность. Именно этот фактор позволяет подвергать нагрузке как материал, так и компонент, к которому он крепится
l Водные растворы широко использовать начали только несколько лет назад в строительстве. Сегодня без них туже не обойтись в процессе быстрого ремонта или монтаже. Главное преимущество водных растворов в том, что они быстро отвердевают из-за чего имеют очень большую адгезию и прочность. Именно этот фактор позволяет подвергать нагрузке как материал, так и компонент, к которому он крепится

 l Существует несколько видов водных растворов. Самые растпротсраненные из них – быстросхватывающиеся цементы и быстросхватывающиеся смеси. На первый взгляд может показаться, что это одно и то же, однако существует большая разница в составе этих материалов. Быстросхватывающиеся цементы содержат специальные добавки, из-за чего они имеют усадку, которая значительно отличается от простого цемента. Быстросхватывающиеся смеси – содержат цемент, кварцевый песок и разные добавки. Новые, сверхустойчивые материалы делают входные растворы антикоррозийными, обладающими хорошей адгезией, стойкими к перепадам температуры и водонепроницаемыми.
l Существует несколько видов водных растворов. Самые растпротсраненные из них – быстросхватывающиеся цементы и быстросхватывающиеся смеси. На первый взгляд может показаться, что это одно и то же, однако существует большая разница в составе этих материалов. Быстросхватывающиеся цементы содержат специальные добавки, из-за чего они имеют усадку, которая значительно отличается от простого цемента. Быстросхватывающиеся смеси – содержат цемент, кварцевый песок и разные добавки. Новые, сверхустойчивые материалы делают входные растворы антикоррозийными, обладающими хорошей адгезией, стойкими к перепадам температуры и водонепроницаемыми.

 Где применяют водные растворы? Герметизация. Если в стене вашего дома, квартиры, офиса появились трещины – их легко устранить при помощи водного раствора. Водные растворы также используются для предотвращения протечек в конструкциях бетона, кирпича и натурального камня, мест пропуска труб и кабелей. В этом случае стоит использовать быстросхватывающиеся цементы, которые отличаются очень коротким временем отвердевания и практически сразу предотвращают протекание воды.
Где применяют водные растворы? Герметизация. Если в стене вашего дома, квартиры, офиса появились трещины – их легко устранить при помощи водного раствора. Водные растворы также используются для предотвращения протечек в конструкциях бетона, кирпича и натурального камня, мест пропуска труб и кабелей. В этом случае стоит использовать быстросхватывающиеся цементы, которые отличаются очень коротким временем отвердевания и практически сразу предотвращают протекание воды.
 Что же такое водный раствор?
Что же такое водный раствор?
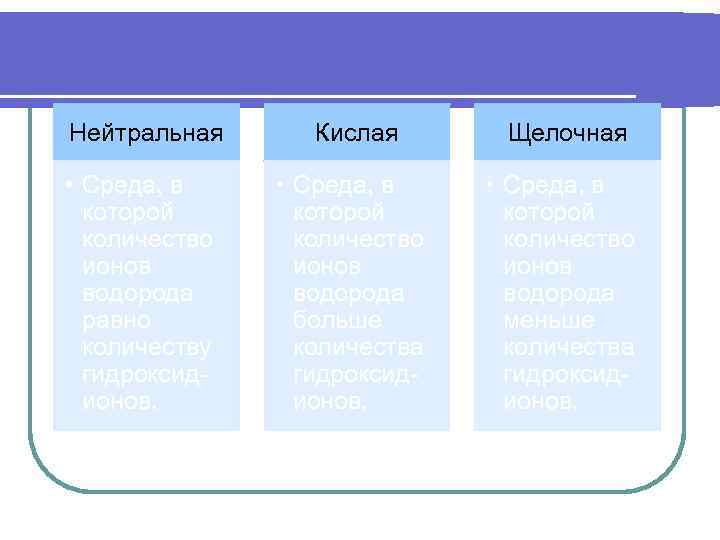 Нейтральная Кислая Щелочная • Среда, в которой количество ионов водорода равно количеству гидроксидионов. • Среда, в которой количество ионов водорода больше количества гидроксидионов. • Среда, в которой количество ионов водорода меньше количества гидроксидионов.
Нейтральная Кислая Щелочная • Среда, в которой количество ионов водорода равно количеству гидроксидионов. • Среда, в которой количество ионов водорода больше количества гидроксидионов. • Среда, в которой количество ионов водорода меньше количества гидроксидионов.
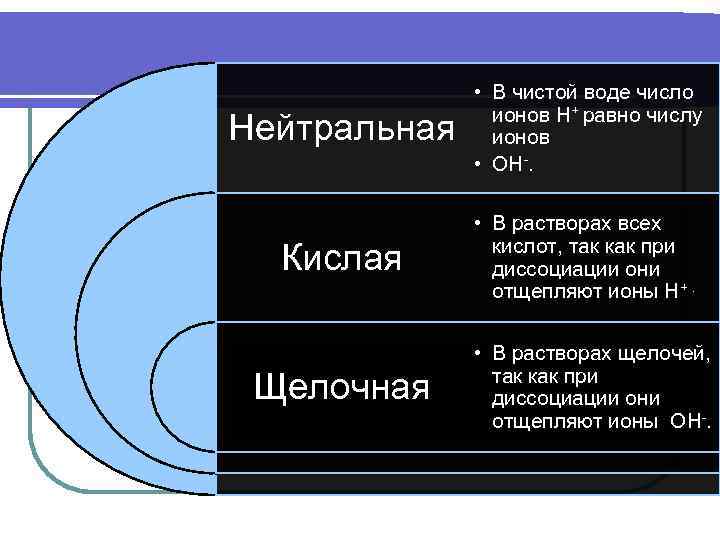 Нейтральная • В чистой воде число ионов H+ равно числу ионов • OH-. Кислая • В растворах всех кислот, так как при диссоциации они отщепляют ионы H+. Щелочная • В растворах щелочей, так как при диссоциации они отщепляют ионы OH-.
Нейтральная • В чистой воде число ионов H+ равно числу ионов • OH-. Кислая • В растворах всех кислот, так как при диссоциации они отщепляют ионы H+. Щелочная • В растворах щелочей, так как при диссоциации они отщепляют ионы OH-.


 Чистая Растворы кислот щелочей вода лакмус Фенол фталеин Метил оранж
Чистая Растворы кислот щелочей вода лакмус Фенол фталеин Метил оранж

 Водородный показатель р. Н – величина, характеризующая содержание ионов водорода в растворе. р. Н Среда раствора 123456 Кислая 7 нейтральная 8 9 10 11 12 13 14 щелочная
Водородный показатель р. Н – величина, характеризующая содержание ионов водорода в растворе. р. Н Среда раствора 123456 Кислая 7 нейтральная 8 9 10 11 12 13 14 щелочная

 l При приготовлении раствора необходимо учитывать особенности материала и самого раствора. Особенно быстро отвердевают быстросхватывающиеся монтажные цементы, поэтому их стоит использовать на протяжении как можно более короткого промежутка времени. Как правило это не более 4 -8 минут. Однако существуют составы, растворы которых можно использовать сразу – так как они моментально затвердевают.
l При приготовлении раствора необходимо учитывать особенности материала и самого раствора. Особенно быстро отвердевают быстросхватывающиеся монтажные цементы, поэтому их стоит использовать на протяжении как можно более короткого промежутка времени. Как правило это не более 4 -8 минут. Однако существуют составы, растворы которых можно использовать сразу – так как они моментально затвердевают.

 l Газы. В отсутствие химического взаимодействия газы смешиваются друг с другом в любых пропорциях, и в этом случае говорить о насыщении нет смысла. Однако при растворении газа в жидкости существует некая предельная концентрация, зависящая от давления и температуры. Растворимость газов в некоторых жидкостях коррелирует с их способностью к сжижению. Наиболее легко сжижаемые газы, например NH 3, HCl, SO 2, более растворимы, чем трудно сжижаемые газы, например O 2, H 2 и He. При наличии химического взаимодействия между растворителем и газом (например, между водой и NH 3 или HCl) растворимость увеличивается. Растворимость данного газа изменяется с природой растворителя, однако порядок, в котором располагаются газы в соответствии с увеличением их растворимости, остается примерно одинаковым для разных растворителей. Процесс растворения подчиняется принципу Ле Шателье (1884): если на систему, находящуюся в равновесии, оказывается какое-либо воздействие, то в результате протекающих в ней процессов равновесие сместится в таком направлении, что оказанное воздействие уменьшится. Растворение газов в жидкостях обычно сопровождается выделением тепла. При этом, в соответствии с принципом Ле Шателье, растворимость газов уменьшается. Это уменьшение тем заметнее, чем выше растворимость газов: такие газы имеют и большую теплоту растворения. "Мягкий" вкус кипяченой или дистиллированной воды объясняется отсутствием в ней воздуха, поскольку его растворимость при высокой температуре весьма мала. С ростом давления растворимость газов увеличивается. Согласно закону Генри (1803), масса газа, который может раствориться в данном объеме жидкости при постоянной температуре, пропорциональна его давлению. Это свойство используется для приготовления газированных напитков. Углекислый газ растворяют в жидкости при давлении 34 атм. ; в этих условиях в данном объеме может раствориться в 3 -4 раза больше газа (по массе), чем при 1 атм. Когда емкость с такой жидкостью открывают, давление в ней падает, и часть растворенного газа выделяется в виде пузырьков. Аналогичный эффект наблюдается при открывании бутылки шампанского или выходе на поверхность подземных вод, насыщенных на большой глубине углекислым газом. При растворении в одной жидкости смеси газов растворимость каждого из них остается такой же, как и в отсутствие
l Газы. В отсутствие химического взаимодействия газы смешиваются друг с другом в любых пропорциях, и в этом случае говорить о насыщении нет смысла. Однако при растворении газа в жидкости существует некая предельная концентрация, зависящая от давления и температуры. Растворимость газов в некоторых жидкостях коррелирует с их способностью к сжижению. Наиболее легко сжижаемые газы, например NH 3, HCl, SO 2, более растворимы, чем трудно сжижаемые газы, например O 2, H 2 и He. При наличии химического взаимодействия между растворителем и газом (например, между водой и NH 3 или HCl) растворимость увеличивается. Растворимость данного газа изменяется с природой растворителя, однако порядок, в котором располагаются газы в соответствии с увеличением их растворимости, остается примерно одинаковым для разных растворителей. Процесс растворения подчиняется принципу Ле Шателье (1884): если на систему, находящуюся в равновесии, оказывается какое-либо воздействие, то в результате протекающих в ней процессов равновесие сместится в таком направлении, что оказанное воздействие уменьшится. Растворение газов в жидкостях обычно сопровождается выделением тепла. При этом, в соответствии с принципом Ле Шателье, растворимость газов уменьшается. Это уменьшение тем заметнее, чем выше растворимость газов: такие газы имеют и большую теплоту растворения. "Мягкий" вкус кипяченой или дистиллированной воды объясняется отсутствием в ней воздуха, поскольку его растворимость при высокой температуре весьма мала. С ростом давления растворимость газов увеличивается. Согласно закону Генри (1803), масса газа, который может раствориться в данном объеме жидкости при постоянной температуре, пропорциональна его давлению. Это свойство используется для приготовления газированных напитков. Углекислый газ растворяют в жидкости при давлении 34 атм. ; в этих условиях в данном объеме может раствориться в 3 -4 раза больше газа (по массе), чем при 1 атм. Когда емкость с такой жидкостью открывают, давление в ней падает, и часть растворенного газа выделяется в виде пузырьков. Аналогичный эффект наблюдается при открывании бутылки шампанского или выходе на поверхность подземных вод, насыщенных на большой глубине углекислым газом. При растворении в одной жидкости смеси газов растворимость каждого из них остается такой же, как и в отсутствие
 l Жидкости. Взаимная растворимость двух жидкостей определяется тем, насколько сходно строение их молекул ("подобное растворяется в подобном"). Для неполярных жидкостей, например углеводородов, характерны слабые межмолекулярные взаимодействия, поэтому молекулы одной жидкости легко проникают между молекулами другой, т. е. жидкости хорошо смешиваются. Напротив, полярные и неполярные жидкости, например вода и углеводороды, смешиваются друг с другом плохо. Каждой молекуле воды нужно сначала вырваться из окружения других таких же молекул, сильно притягивающими ее к себе, и проникнуть между молекулами углеводорода, притягивающими ее слабо. И наоборот, молекулы углеводорода, чтобы раствориться в воде, должны протиснуться между молекулами воды, преодолевая их сильное взаимное притяжение, а для этого нужна энергия. При повышении температуры кинетическая энергия молекул возрастает, межмолекулярное взаимодействие ослабевает и растворимость воды и углеводородов увеличивается. При значительном повышении температуры можно добиться их полной взаимной растворимости. Такую температуру называют верхней критической температурой растворения (ВКТР). В некоторых случаях взаимная растворимость двух частично смешивающихся жидкостей увеличивается при понижении температуры. Этот эффект наблюдается в том случае, когда при смешивании выделяется тепло, обычно в результате химической реакции. При значительном понижении температуры, но не ниже точки замерзания, можно достичь нижней критической температуры растворения (НКТР). Можно предположить, что все системы, имеющие НКТР, имеют и ВКТР (обратное не обязательно). Однако в большинстве случаев одна из смешивающихся жидкостей кипит при температуре ниже ВКТР. У системы никотин-вода НКТР равна 61° С, а ВКТР составляет 208° C. В интервале 61 -208° C эти жидкости ограниченно растворимы, а вне этого интервала обладают полной взаимной растворимостью.
l Жидкости. Взаимная растворимость двух жидкостей определяется тем, насколько сходно строение их молекул ("подобное растворяется в подобном"). Для неполярных жидкостей, например углеводородов, характерны слабые межмолекулярные взаимодействия, поэтому молекулы одной жидкости легко проникают между молекулами другой, т. е. жидкости хорошо смешиваются. Напротив, полярные и неполярные жидкости, например вода и углеводороды, смешиваются друг с другом плохо. Каждой молекуле воды нужно сначала вырваться из окружения других таких же молекул, сильно притягивающими ее к себе, и проникнуть между молекулами углеводорода, притягивающими ее слабо. И наоборот, молекулы углеводорода, чтобы раствориться в воде, должны протиснуться между молекулами воды, преодолевая их сильное взаимное притяжение, а для этого нужна энергия. При повышении температуры кинетическая энергия молекул возрастает, межмолекулярное взаимодействие ослабевает и растворимость воды и углеводородов увеличивается. При значительном повышении температуры можно добиться их полной взаимной растворимости. Такую температуру называют верхней критической температурой растворения (ВКТР). В некоторых случаях взаимная растворимость двух частично смешивающихся жидкостей увеличивается при понижении температуры. Этот эффект наблюдается в том случае, когда при смешивании выделяется тепло, обычно в результате химической реакции. При значительном понижении температуры, но не ниже точки замерзания, можно достичь нижней критической температуры растворения (НКТР). Можно предположить, что все системы, имеющие НКТР, имеют и ВКТР (обратное не обязательно). Однако в большинстве случаев одна из смешивающихся жидкостей кипит при температуре ниже ВКТР. У системы никотин-вода НКТР равна 61° С, а ВКТР составляет 208° C. В интервале 61 -208° C эти жидкости ограниченно растворимы, а вне этого интервала обладают полной взаимной растворимостью.
 l Твердые вещества. Все твердые вещества проявляют ограниченную растворимость в жидкостях. Их насыщенные растворы имеют при данной температуре определенный состав, который зависит от природы растворенного вещества и растворителя. Так, растворимость хлорида натрия в воде в несколько миллионов раз выше растворимости нафталина в воде, а при растворении их в бензоле наблюдается обратная картина. Этот пример иллюстрирует общее правило, согласно которому твердое вещество легко растворяется в жидкости, имеющей с ним сходные химические и физические свойства, но не растворяется в жидкости с противоположными свойствами. Соли обычно легко растворяются в воде и хуже - в других полярных растворителях, например в спирте и жидком аммиаке. Однако растворимость солей тоже существенно различается: например, нитрат аммония обладает в миллионы раз большей растворимостью в воде, чем хлорид серебра. Растворение твердых веществ в жидкостях обычно сопровождается поглощением тепла, и в соответствии с принципом Ле Шателье их растворимость должна увеличиваться при нагревании. Этот эффект можно использовать для очистки веществ методом перекристаллизации. Для этого их растворяют при высокой температуре до получения насыщенного раствора, затем раствор охлаждают и после выпадения растворенного вещества в осадок профильтровывают. Есть вещества (например, гидроксид, сульфат и ацетат кальция), растворимость которых в воде с ростом температуры уменьшается. Твердые вещества, как и жидкости, тоже могут растворяться друг в друге полностью, образуя гомогенную смесь - истинный твердый раствор, аналогичный жидкому раствору. Частично растворимые друг в друге вещества образуют два равновесных сопряженных твердых раствора, составы которых изменяются с температурой.
l Твердые вещества. Все твердые вещества проявляют ограниченную растворимость в жидкостях. Их насыщенные растворы имеют при данной температуре определенный состав, который зависит от природы растворенного вещества и растворителя. Так, растворимость хлорида натрия в воде в несколько миллионов раз выше растворимости нафталина в воде, а при растворении их в бензоле наблюдается обратная картина. Этот пример иллюстрирует общее правило, согласно которому твердое вещество легко растворяется в жидкости, имеющей с ним сходные химические и физические свойства, но не растворяется в жидкости с противоположными свойствами. Соли обычно легко растворяются в воде и хуже - в других полярных растворителях, например в спирте и жидком аммиаке. Однако растворимость солей тоже существенно различается: например, нитрат аммония обладает в миллионы раз большей растворимостью в воде, чем хлорид серебра. Растворение твердых веществ в жидкостях обычно сопровождается поглощением тепла, и в соответствии с принципом Ле Шателье их растворимость должна увеличиваться при нагревании. Этот эффект можно использовать для очистки веществ методом перекристаллизации. Для этого их растворяют при высокой температуре до получения насыщенного раствора, затем раствор охлаждают и после выпадения растворенного вещества в осадок профильтровывают. Есть вещества (например, гидроксид, сульфат и ацетат кальция), растворимость которых в воде с ростом температуры уменьшается. Твердые вещества, как и жидкости, тоже могут растворяться друг в друге полностью, образуя гомогенную смесь - истинный твердый раствор, аналогичный жидкому раствору. Частично растворимые друг в друге вещества образуют два равновесных сопряженных твердых раствора, составы которых изменяются с температурой.
 l Коэффициент распределения. Если к равновесной системе двух несмешивающихся или частично смешивающихся жидкостей добавить раствор какого-либо вещества, то оно распределяется между жидкостями в определенной пропорции, не зависящей от общего количества вещества, в отсутствие химических взаимодействий в системе. Это правило получило название закона распределения, а отношение концентраций растворенного вещества в жидкостях - коэффициента распределения. Коэффициент распределения примерно равен отношению растворимостей данного вещества в двух жидкостях, т. е. вещество распределяется между жидкостями соответственно его растворимостям. Это свойство используется для экстракции данного вещества из его раствора в одном растворителе с помощью другого растворителя. Еще одним примером его применения является процесс экстракции серебра из руд, в состав которых оно часто входит вместе со свинцом. Для этого в расплавленную руду добавляют цинк, который не смешивается со свинцом. Серебро распределяется между расплавленным свинцом и цинком, преимущественно в верхнем слое последнего. Этот слой собирают и отделяют серебро дистилляцией цинка.
l Коэффициент распределения. Если к равновесной системе двух несмешивающихся или частично смешивающихся жидкостей добавить раствор какого-либо вещества, то оно распределяется между жидкостями в определенной пропорции, не зависящей от общего количества вещества, в отсутствие химических взаимодействий в системе. Это правило получило название закона распределения, а отношение концентраций растворенного вещества в жидкостях - коэффициента распределения. Коэффициент распределения примерно равен отношению растворимостей данного вещества в двух жидкостях, т. е. вещество распределяется между жидкостями соответственно его растворимостям. Это свойство используется для экстракции данного вещества из его раствора в одном растворителе с помощью другого растворителя. Еще одним примером его применения является процесс экстракции серебра из руд, в состав которых оно часто входит вместе со свинцом. Для этого в расплавленную руду добавляют цинк, который не смешивается со свинцом. Серебро распределяется между расплавленным свинцом и цинком, преимущественно в верхнем слое последнего. Этот слой собирают и отделяют серебро дистилляцией цинка.
 Произведение растворимости (ПР). Между избытком (осадком) твердого вещества Mx. By и его насыщенным раствором устанавливается динамическое равновесие, описываемое уравнением l <> Константа равновесия этой реакции равна l <> и называется произведением растворимости. Она постоянна при данных температуре и давлении и является величиной, на основании которой рассчитывают растворимость осадка и изменяют ее. Если в раствор добавить соединение, диссоциирующее на ионы, одноименные с ионами малорастворимой соли, то в соответствии с выражением для ПР растворимость соли уменьшается. При добавлении же соединения, реагирующего с одним из ионов, она, напротив, увеличится. О некоторых свойствах растворов ионных соединений l
Произведение растворимости (ПР). Между избытком (осадком) твердого вещества Mx. By и его насыщенным раствором устанавливается динамическое равновесие, описываемое уравнением l <> Константа равновесия этой реакции равна l <> и называется произведением растворимости. Она постоянна при данных температуре и давлении и является величиной, на основании которой рассчитывают растворимость осадка и изменяют ее. Если в раствор добавить соединение, диссоциирующее на ионы, одноименные с ионами малорастворимой соли, то в соответствии с выражением для ПР растворимость соли уменьшается. При добавлении же соединения, реагирующего с одним из ионов, она, напротив, увеличится. О некоторых свойствах растворов ионных соединений l
 l Где применяют водные растворы? Герметизация. Если в стене вашего дома, квартиры, офиса появились трещины – их легко устранить при помощи водного раствора. Водные растворы также используются для предотвращения протечек в конструкциях бетона, кирпича и натурального камня, мест пропуска труб и кабелей. В этом случае стоит использовать быстросхватывающиеся цементы, которые отличаются очень коротким временем отвердевания и практически сразу предотвращают протекание воды. Монтаж. Водные растворы применяются также при монтаже перил лестниц, стоек ворот, ограждения, электромонтажных коробок и разных видов креплений. Для этого лучше всего выбрать смеси на цементной основе. Быстросхватывающиеся смеси предоставляют возможность особенно прочно закрепить элементы и сделать этого очень быстро.
l Где применяют водные растворы? Герметизация. Если в стене вашего дома, квартиры, офиса появились трещины – их легко устранить при помощи водного раствора. Водные растворы также используются для предотвращения протечек в конструкциях бетона, кирпича и натурального камня, мест пропуска труб и кабелей. В этом случае стоит использовать быстросхватывающиеся цементы, которые отличаются очень коротким временем отвердевания и практически сразу предотвращают протекание воды. Монтаж. Водные растворы применяются также при монтаже перил лестниц, стоек ворот, ограждения, электромонтажных коробок и разных видов креплений. Для этого лучше всего выбрать смеси на цементной основе. Быстросхватывающиеся смеси предоставляют возможность особенно прочно закрепить элементы и сделать этого очень быстро.
 l Большинство растворов можно использовать только при температуре не ниже +5 градусов. Более докладную информацию можно прочитать на упаковке изготовителя. Однако стоит знать, что при теплой температуре водные растворы сохнут быстрее. Обратите внимание и на состав раствора. Возможно необходимо добавлять в него меньше воды, нежели указано на упаковке производителем. Это может повлиять на увеличение времени схватывания. Если вы сомневаетесь, какой раствор вам выбрать в зависимости от степени и быстроты высыхания – отдайте предпочтение тому, который быстро схватывается при высокой влажности воздуха и низкой температуре. Иногда, производители рекомендуют в жаркое время добавлять в раствор холодную воду, или наоборот. Интервал температур, в пределах которого можно применять раствор, должен быть указан на упаковке.
l Большинство растворов можно использовать только при температуре не ниже +5 градусов. Более докладную информацию можно прочитать на упаковке изготовителя. Однако стоит знать, что при теплой температуре водные растворы сохнут быстрее. Обратите внимание и на состав раствора. Возможно необходимо добавлять в него меньше воды, нежели указано на упаковке производителем. Это может повлиять на увеличение времени схватывания. Если вы сомневаетесь, какой раствор вам выбрать в зависимости от степени и быстроты высыхания – отдайте предпочтение тому, который быстро схватывается при высокой влажности воздуха и низкой температуре. Иногда, производители рекомендуют в жаркое время добавлять в раствор холодную воду, или наоборот. Интервал температур, в пределах которого можно применять раствор, должен быть указан на упаковке.

 l Раствовы, в зависимости от цели и назначения раствора, применяются или химически чистыми или в виде технических препаратов. Иногда химически чистые препараты могут быть получены из технических путем очистки.
l Раствовы, в зависимости от цели и назначения раствора, применяются или химически чистыми или в виде технических препаратов. Иногда химически чистые препараты могут быть получены из технических путем очистки.
 Растворы широко распространены в природе и играют важную роль во мн. отраслях пром-сти и техники. Химически чистые в-ва представляют собой лишь предельное состояние, к-рое в действительности не достигается; даже чистейшие металлы, получаемые методами вакуумной или зонной плавки, содержат ничтожные кол-ва примесей (10 -6 %) и по существу являются твердыми растворами. Образование растворов существенно изменяет условия протекания хим. р-ций между компонентами (см. Реакции в растворах); мн. процессы происходят исключительно в растворах. Изучение физ. -хим. св-в растворов тесно связано с проблемами разделения прир. и пром. смесей, получения чистых в-в методами ректификации, экстракции, кристаллизации, абсорбции и др. Водные растворы солей, к-т и оснований широко используют в гидрометаллургии при извлечении цветных металлов из руд. Исключительна роль водных растворов во всех биол. процессах. Использование неводных растворов связано с применением полимеров, красителей, лаков, приготовлением жидкостей с заданными физ. сввами (вязкостью, диэлектрич. проницаемостью и др. ).
Растворы широко распространены в природе и играют важную роль во мн. отраслях пром-сти и техники. Химически чистые в-ва представляют собой лишь предельное состояние, к-рое в действительности не достигается; даже чистейшие металлы, получаемые методами вакуумной или зонной плавки, содержат ничтожные кол-ва примесей (10 -6 %) и по существу являются твердыми растворами. Образование растворов существенно изменяет условия протекания хим. р-ций между компонентами (см. Реакции в растворах); мн. процессы происходят исключительно в растворах. Изучение физ. -хим. св-в растворов тесно связано с проблемами разделения прир. и пром. смесей, получения чистых в-в методами ректификации, экстракции, кристаллизации, абсорбции и др. Водные растворы солей, к-т и оснований широко используют в гидрометаллургии при извлечении цветных металлов из руд. Исключительна роль водных растворов во всех биол. процессах. Использование неводных растворов связано с применением полимеров, красителей, лаков, приготовлением жидкостей с заданными физ. сввами (вязкостью, диэлектрич. проницаемостью и др. ).




