Энцефаломиелит рассеянный (2011).ppt
- Количество слайдов: 69

Рассеянный склероз (sclerosis disseminate) Учебные вопросы: 1) Эпидемиология РС 2) Этиологические факторы и патогенез РС 3) Особенности клинического течения РС 4) Диагностика РС 5) Современное лечения РС

Рассеянный склероз • Рассеянный склероз - хроническое прогрессирующее заболевание ЦНС, развивающееся на фоне вторичного иммунодефицита, приводящего к развитию аутоиммунного процесса, повреждающего миелин в головном и спинном мозге. Заболевание поражает преимущественно лиц молодого возраста и приводит к быстрому развитию стойкой нетрудоспособности. • В происхождении болезни имеют значение: 1) фактор, повреждающий нервную и иммунную систему (чаще всего это неспецифический инфекционный агент); 2) генетический фактор; 3) географический фактор. • Рассеянный склероз - важнейшая проблема современной неврологии

Эпидемиология Распространенность PC: высокая (50 -120 чел на 10 000) в Северной Европе, Италии, США, Австралии, Новой Зеландии, России; средняя (5 -29 чел на 10 000) в Южной Европе, Средиземноморье; низкая (менее 5 чел на 10 000) в Африке, Мексике, странах Карибского бассейна. При этом в регионах с одинаковыми природными условиями отмечаются значительные различия, например на Сицилии PC встречается в 10 раз чаще, чем на Мальте. Некоторые популяции: цыгане, северо-американские индейцы, испанцы, якуты, австралийские аборигены, новозеландские майори -устойчивы к PC, несмотря на проживание в зонах высокого риска. В России распространенность этого заболевания колеблется от 10 до 60 случаев на 10 000 населения. • К эпидемиологическим особенностям PC относятся: • • • - наиболее частый возраст начала от 18 до 45 лет; - преимущественное заболевание европейской расы; - чаще болеют женщины; - увеличение частоты PC с юга на север и с востока на запад; - изменение риска возникновения PC при смене зон проживания (миграции); • - наличие зон резко повышенной частоты PC и резкое увеличение заболеваемости PC на ограниченной территории в определенный промежуток времени.

Своеобразие РС • • 1) Молодой возраст 2) Сырой и влажный климат (географический фактор) 3) Поражение многих функциональных систем. Причина PC остается неизвестной. Сегодня связывают возникновение РС с случайным индивидуальным сочетанием неблагоприятных эндогенных и экзогенных факторов риска. • К эндогенным факторам относят комплекс генов, возможно, обусловливающих генетическую несостоятельность иммунорегуляции. Из внешних факторов имеют значение: зона проживания, особенности питания, частота вирусных и бактериальных инфекций и др. Однако ни один взятый изолированно фактор не имеет значение в возникновении рассеянного склероза, Должно быть только определенное сочетание ряда факторов. В итоге в организме, имеющем генетически обусловленную несостоятельность регуляторных систем иммунитета, происходит активация иммунной системы одним из неспецифических провоцирующих факторов, например, вирусной инфекцией, травмой, стрессовой ситуацией.

ПРЕДСТАВЛЕНИЯ О ПАТОГЕНЕЗЕ ЗАБОЛЕВАНИЯ • Под влиянием вирусной инфекции или других факторов происходит активация Т-лимфоцитов крови, которые затем проникают через гематоэнцефалический барьер (ГЭБ) и взаимодействуют с клетками ЦНС, активизируя периваскулярные моноциты и микроглию, эндотелиальные клетки и астроциты. В результате этого взаимодействия выделяются провоспалительные цитокины, гаммаинтерферон, лимфотоксин и фактор некроза опухоли альфа. Возрастающая концентрация воспалительных медиаторов ведет к нарушению ГЭБ. Нарастает интенсивность клеточных аутоиммунных реакций на антигены миелина, воспаление и демиелинизация. • Одновременно в очагах PC происходят процессы ремиелинизации (восстановление миелина), однако в большинстве случаев малоэффективные. Причина прекращения воспалительной реакции в очагах PC неизвестна. Вероятно, в этот период увеличивается концентрация противовоспалительных цитокинов: астроциты продуцируют факторы, замедляющие пролиферацию Тклеток или происходит локальная элиминация аутореактивных Тклеток путем апоптоза (запрограммированной смерти).
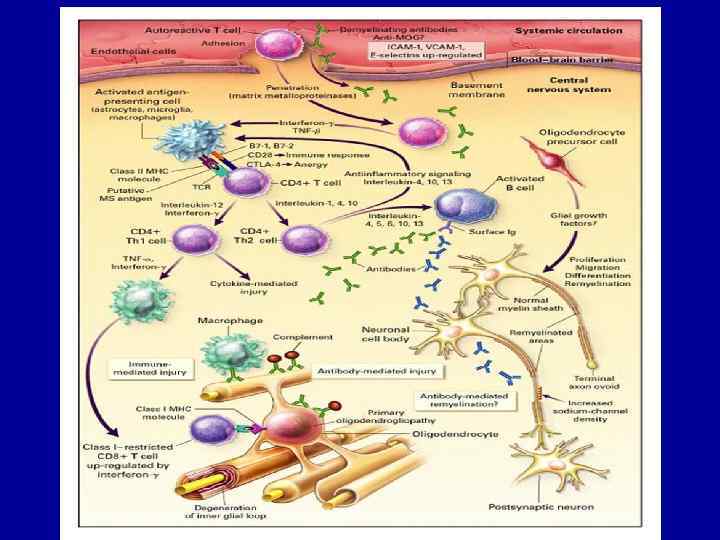

Figure 1. The paradigm for the role of B-cells in MS • Taken from Meinl E et al. B lineage cells in the inflammatory central nervous system environment: migration, maintenance, local antibody production, and therapeutic modulation. Ann Neurol 2006; 59: 880 -892. Reproduced with permission from John Wiley & Sons Ltd.

B-cells are directly linked to the pathogenesis of MS • B-cells are directly linked to the pathogenesis of • • MS Plasma cells and B-cells are commonly found in B-cell lesions 19 -21 and in all phenotypes of MS 22 More recently, B-cell follicles have been identified in the brain meninges of patients with secondary-progressive MS, linked to cortical lesion formation 23, 24 B-cells have also been identified in the CSF of patients with MS 25, 26 B-cells in CNS may be predictive of disease progression 26
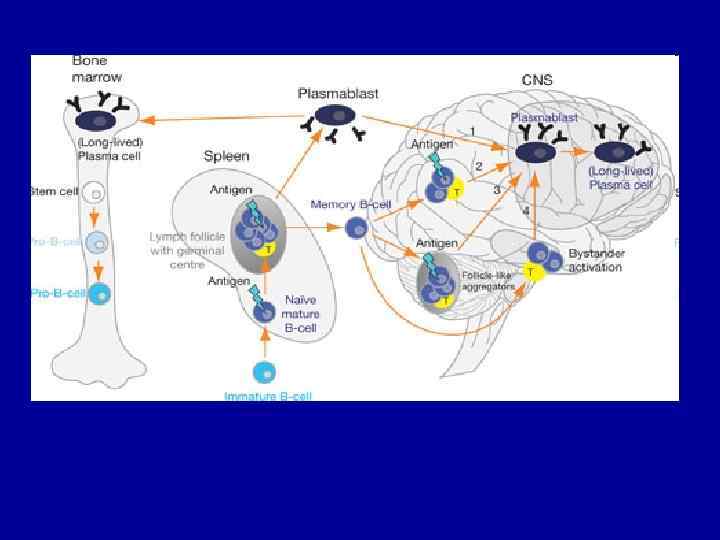

ПРЕДСТАВЛЕНИЯ О ПАТОГЕНЕЗЕ ЗАБОЛЕВАНИЯ • Результатом разрушения миелина является формирование в • разных отделах ЦНС (вокруг желудочков мозга, в стволе мозга, мозжечке, в шейном отделе спинного мозга) очагов демиелинизации ("бляшек"). Условно различают активную воспалительную стадию и хроническую дегенеративную стадию формирования очагов демиелинизации. • Для первой стадии характерны: наличие локального отека, повышение проницаемости гематоэнцефалического барьера, периваскулярная инфильтрация ткани мозга клетками крови, повышение продукции провоспалительных цитокинов, т. е. активные аутоиммунные и воспалительные процессы. • Для второй стадии характерны дегенеративные изменения: аксональная дегенерация, уменьшение количества олигодендроцитов и активная пролиферация астроцитов.

ПАТОМОРФОЛОГИЯ Основным патоморфологическим проявлением заболевания является разрушение миелиновой оболочки и формирование астроглиальных рубцовых уплотнений ("sclerosis"- "уплотнение"). (функции миелина - изоляция, ускорение проведения импульса, защита и питание нервного волокна. Белки и липиды, содержащиеся в нервном волокне, могут выступать в качестве аутоантигенов и вызывать аутоиммунные реакции). Таким образом, клиническая картина заболевания обусловлена блокированием проведения нервного импульса в результате демиелинизации, отека и дегенеративных изменений в аксонах.

Классификация форм РС Многообразие клинических синдромов рассеянного склероза находит свое отражение в соответствующих классификациях. А. Д. Марков и А. Л. Леонович (1976) выделяют: 1) типичную - цереброспинальную - форму, наблюдавшуюся примерно у половины всех больных; 2) атипичные формы - спинальную, мозжечковую, оптическую, псевдотабетическую, стволовую. 3) Перечень атипичных форм рассеянного склероза можно продолжить, добавив кортикальную, стриопаллидарную (гиперкинетическую), акустическую, псевдотуморозную, бульбарную, цервикальную, люмбосакральную, полиомиелитическую, амиотрофическую, псевдосирингомиелитическую, полиневритическую и другие.

ОСОБЕННОСТИ ТЕЧЕНИЯ ЗАБОЛЕВАНИЯ Выделяют варианты течения PC. • Ремитирующее течение (relapsing-remitting) - включает две основные стадии: - обострение (экзацербация) - ухудшение имеющихся симптомов или появление новых после того, как состояние больного было стабильным не менее месяца; - ремиссия - полное или неполное восстановление функций и отсутствие нарастания симптомов. В начале заболевания 80 -85% больных имеют этот вариант PC. • Первично-прогрессирующее течение (primary-progressive) отмечается у 15 -20% больных и с самого начала характеризуется прогрессированием с временной стабилизацией или временным незначительным улучшением. Среди этих больных преобладают мужчины и больные старшего возраста. • Вторично-прогрессирующее течение (secondary-progressive) - первоначально ремиттирующее течение сменяется прогрессированием без ремиссий с кратковременными периодами стабилизации. Этот вариант наблюдается у 60% больных и рассматривается как этап развития ремиттирующей формы.

ОСОБЕННОСТИ ТЕЧЕНИЯ ЗАБОЛЕВАНИЯ • Прогрессирующе-ремиттирующее течение (progressive- relapsing) - встречается примерно у 6% больных и характеризуется прогрессированием с самого начала болезни, на фоне которого в дальнейшем возникают обострения (между обострениями продолжается прогрессирование заболевания). Помимо этого выделяют также: • - доброкачественный вариант течения заболевания, при котором на протяжении более 10 лет больной имеет незначительные нарушения функций - не более 1 -2 баллов по шкале EDSS • - злокачественный вариант с быстрым прогрессированием, приводящим в течение 5 лет к значительной инвалидизации - более 6 баллов по шкале EDSS. • Определить вариант течения болезни в 20 -30% случаев достаточно сложно. Более благоприятен прогноз у лиц молодого возраста, женского пола, при начале заболевания с ретробульбарного неврита или нарушений чувствительности.
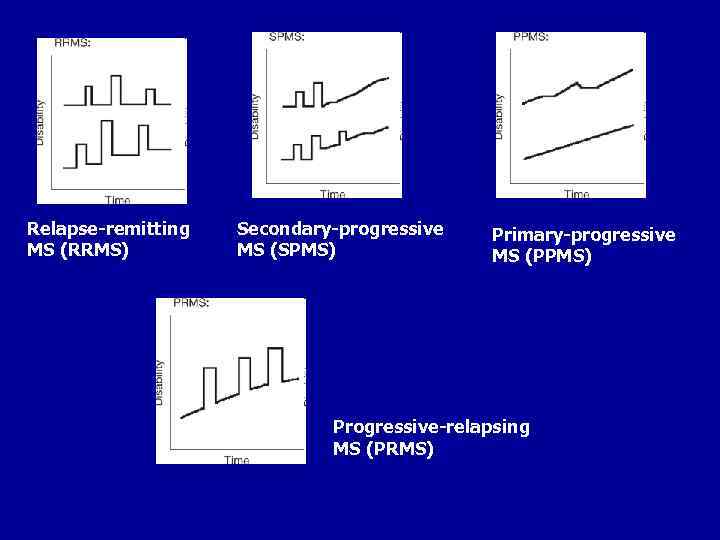
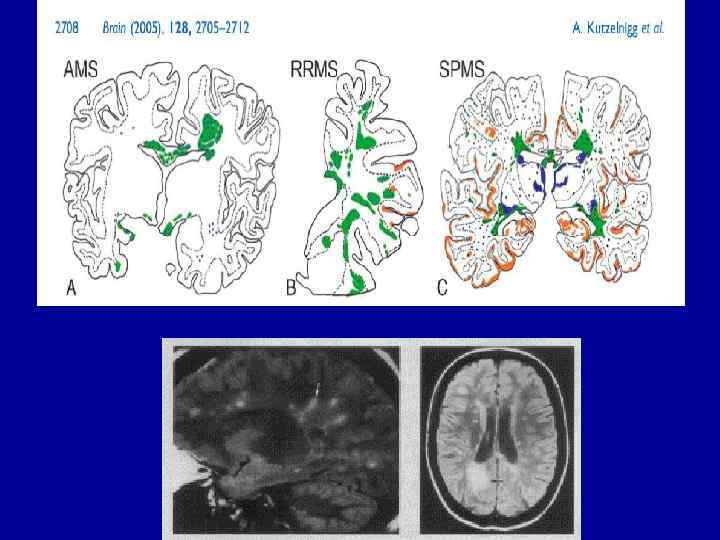
Relapse-remitting MS (RRMS) Secondary-progressive MS (SPMS) Primary-progressive MS (PPMS) Progressive-relapsing MS (PRMS)
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ ЗАБОЛЕВАНИЯ • Первым описанным симптомокомплексом • • • была триада, предложенная Шарко: нистагм, скандированная речь, интенционное дрожание; затем - пентада Марбурга: нижний спастический парапарез, битемпоральная деколорация дисков зрительных нервов, отсутствие брюшных рефлексов, нистагм, интенционное дрожание; Д. А. Марков объединил наиболее характерные симптомы в секстаду: зрительные нарушения, вестибулярные нарушения, непостоянные глазодвигательные расстройства, поражение пирамидной системы, снижение вибрационной чувствительности, белково-коллоидная диссоциация в ликворе. В настоящее время описанные классиками неврологии триады, пентады и др. несколько утратили свою актуальность для характеристики многообразных клинических проявлений этого заболевания.

Наиболее часто встречающиеся клинические симптомы при PC: • - нарушение активных движений при поражении пирамидного тракта: геми-, пара- и монопарезы, спастическое повышение тонуса, повышение сухожильных рефлексов, патологические пирамидные симптомы, клонусы и т. д. ; • - нарушение координации при поражении путей мозжечка: атаксия, гипотония, нистагм, скандированная речь, дисметрия, асинергия и т. д. ; • - нарушение чувствительности при поражении проводников глубокой и поверхностной чувствительности: гипестезия, нарушение вибрационной и температурной чувствительности, мышечно-суставного чувства и т. д. ; • - нарушение зрения из-за поражения зрительного нерва: снижение остроты, изменения полей зрения и т. д. (часто PC дебютирует развитием ретробульбарного неврита);

Наиболее часто встречающиеся клинические симптомы при PC: • - нарушение функции черепно-мозговых нервов при поражении белого вещества и ствола мозга: нарушение координации движений глазных яблок (межъядерная офтальмоплегия), парез лицевого нерва, псевдобульбарные синдромы и т. д. ; • - нарушение функций тазовых органов при поражении проводящих путей: императивные позывы на мочеиспускание, задержка и недержание мочи, импотенция, запоры и недержания кала; • - эмоционально-волевые, нейропсихические нарушения: депрессия, астенический синдром, эйфория - расторможенное поведение и склонность к неадекватным шуткам. • Реже наблюдаются болевые, пароксизмальные проявления, выраженные психические нарушения. Необходимо отметить, что в клинической картине PC у каждого больного особое, индивидуальное сочетание вышеуказанных симптомов.

Для характеристики состояния больного PC наиболее часто используются шкалы оценки тяжести по J. Kurtzke (1983) - Disability Status Scale (DSS) и Expanded Disability Status Scale (EDSS). Расширенная шкала инвалидизации по Курцтке (шкала EDSS) • • 0. 0 норма в неврологическом статусе. 1. 0 признаков инвалидизации нет. Минимальные признаки нарушений (1 степень) в одной функциональной системе (ФС), исключая церебральную. • 1. 5 признаков инвалидизации нет. Минимальные признаки нарушений (1 степень) в более чем одной ФС. • 2. 0 легкие признаки инвалидизации (2 степень) в одной ФС. • 2. 5 легкиe признаки инвалидизации ( 2 степень) в 2 -х ФС • 3. 0 умеренные признаки инвалидизации (3 степень) в одной ФС, либо легкие признаки инвалидизации (2 степень) в 3 или 4 ФС. Ходячий. • 3. 5 ходячий. Умеренные признаки инвалидизации ( 3 степень) в одной ФС и в 1 -2 ФС - 3 степени. Либо в 5 ФС-2 степени. • 4. 0 ходячий, посторонней помощи не требуется. Самообслуживание сохранено. Проводит в повседневной активности около 12 часов в день. Относительно выраженные признаки инвалидизации (4 степени) в одной ФС, либо сочетание меньших степеней инвалидизации, но превышающие значения предыдущих баллов. Может пройти без посторонней помощи или остановки 500 метров.

Расширенная шкала инвалидизации по Курцтке (шкала EDSS) • 4. 5 ходячий, посторонней помощи не требуется. Повседневная активность не нарушена. Может ходить в течении всего дня. Возможна необходимость в посторонней помощи. Относительно выраженные признаки инвалидизации (4 степени) в 1 ФС, либо сочетание меньших степеней инвалидизации, но превышающие значения предыдущих баллов. Может пройти без посторонней помощи или остановки 200 метров. • 5. 0 может пройти без посторонней помощи или остановки 200 метров. Повседневная активность нарушена. В 1 ФС -5 степень, либо сочетание меньших степеней инвалидизации, превышающие значения для 4 баллов. • 5. 5 может пройти без посторонней помощи или остановки около 100 метров. Повседневная активность ограничена. В 1 ФС- 5 степень, либо сочетание меньших степеней, но превышающие степени, оговоренные в п. 4 • 6. 0 ходьба с периодической /односторонней постоянной поддержкой около 100 м с или без отдыха. 3 степень в более, чем в 2 ФС. • 6. 5 ходьба с постоянной двусторонней поддержкой около 20 метров без отдыха. 3 степень более чем в 2 ФС.

Расширенная шкала инвалидизации по Курцтке (шкала EDSS) 7. 0 не может пройти и 5 метров без помощи. Прикован к инвалидной коляске, в которой передвигается самостоятельно. Посторонней помощи не требуется. Повседневная активность в инвалидной коляске 12 часов в сутки. 4 степень и более чем в 1 ФС. Очень редко 5 стeпень только в пирамидной системе. • 7. 5 может пройти всего несколько шагов. Передвигается только в инвалидной коляске. Требуется помощь в передвижении. Не может находиться в коляске в течении всего дня. 4 степень и более чем в 1 ФС. • 8. 0 прикован к кровати или передвигается в инвалидной коляске. Может находиться вне постели большую часть дня. Основные функции самообслуживания сохранены. Активно пользуется руками. 4 степень в нескольких ФС. • 8. 5 прикован к постели большую часть дня. В некоторой степени может пользоваться руками. Самообслуживание частичное. 4 степень в нескольких ФС. • 9. 0 беспомощный, прикованный к постели больной. Может вступать в контакт и есть. 4 степень в большинстве ФС. • 9. 5 полностью беспомощный, прикованный к постели больной. Не может полноценно вступать в контакт или есть/глотать. 4 степень практически во всех ФС. • 10. 0 смерть из-за рассеянного склероза.

Диагностика рассеянного склероза (РС) основывается на данных анамнеза, неврологического осмотра и результатах дополнительных методов обследования. Классическими клиническими критериями диагностики РС являются клинические диагностические критерии достоверного РС. К ним относятся: 1. Наличие объективных свидетельств поражения нервной системы. 2. На основании данных неврологического осмотра или анамнеза должны быть выявлены признаки по крайней мере 2 раздельно расположенных очагов. 3. Неврологические симптомы должны свидетельствовать о поражении белого вещества, головного и спинного мозга, т. е. проводников. 4. Клинические симптомы должны иметь преходящий характер, выполняя одно из следующих требований: а) должно быть два или более эпизодов ухудшения, разделенных периодом не менее 1 мес и продолжительностью не менее 24 ч. б) должно быть медленное, постепенное прогрессирование на протяжении по крайней мере 6 мес. 5. Заболевание начинается в возрасте от 10 до 50 лет включительно. 6. Имеющиеся неврологические нарушения не могут быть более адекватно объяснены другим патологическим процессом.

Диагностика PC • При проведении дифференциальной диагностики • • • целесообразно использовать следующие специфические проявления, характерные для PC: - тест "горячей ванны" - резкое ухудшение состояния больного при повышении температуры окружающей среды (в частично демиелинизированных волокнах повышение температуры вызывает преходящую блокаду проведения нервного импульса); - синдром клинической диссоциации - сочетание поражений разных проводящих систем и уровней, например, снижение мышечного тонуса в сочетании с гиперрефлексией и патологическими стопными знаками; - синдром непостоянства клинических симптомов - изменение неврологической симптоматики в течение нескольких минут, часов, обусловленное повышенной восприимчивостью демиелинизированного аксона на внешние воздействия.

Следует указать и на такие феномены, считающиеся характерными для РС, как: Симптом Крузона (сохранность ахиллова рефлекса при расстройствах мышечно-суставного чувства), Симптом Лермитта (появление болезненных неприятных ощущений по типу «прохождения тока» по спине от головы до ног при резком сгибании или разгибании шеи), Симптом "горячей ванны" (у 3/4 общего числа больных РС после десятиминутного пребывания в ванне с температурой воды 38°С временно углубляются имевшиеся расстройства, в первую очередь, слабость конечностей; иногда появляются новые симптомы). Состояние больных иногда ухудшается после питья горячей воды и при жаркой погоде.

Первые клинические симптомы могут включать: - развивающиеся подостро расстройства чувствительности (ее снижение или парестезии в конечностях); - мышечную слабость в одной или нескольких конечностях; -ухудшение зрения на один глаз (поражение зрительного нерва); - реже - системное головокружение с тошнотой, шаткость, - иногда - симптомы поражения других черепных нервов, - в единичных случаях - дисфункцию мочевого пузыря. Особенно характерно развитие этих симптомов в возрасте 20 -45 лет. Установление при неврологическом осмотре признаков многоочаговости процесса делает диагноз PC более вероятным. Вышеперечисленные симптомы, особенно их сочетания, по меньшей мере в половине случаев оказываются проявлениями PC. Однако только клинических данных недостаточно для точного диагноза. Еще сложнее диагностическая ситуация, когда имеют место редкие проявления болезни, а также ее начало после 50 лет или в детском возрасте.

Магнитно-резонансная томография Следующим шагом после клинического предположения о PC является МРТ - метод выбора инструментальной диагностики PC. МРТ позволяет визуализировать патологические очаги в ЦНС, демонстрируя необходимую для диагностики диссеминацию процесса в пространстве (многоочаговость) и во времени (очаги "разного возраста", а также исследование в динамике). Это наиболее информативный инструментальный метод диагностики PC. Его чувствительность при разных формах PC - 85 -95%. Разработаны дополнительные МРТ-характеристики, повышающие специфичность метода. Они включают определенные варианты локализации и ориентации очагов, особенности проявлений отека вещества мозга и накопления контраста, а также изменения, наблюдаемые в динамике.
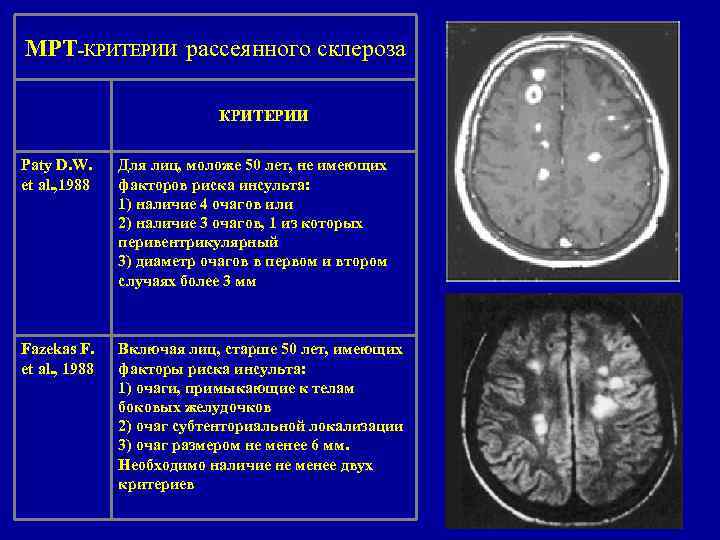
МРТ-КРИТЕРИИ рассеянного склероза КРИТЕРИИ Paty D. W. et al. , 1988 Для лиц, моложе 50 лет, не имеющих факторов риска инсульта: 1) наличие 4 очагов или 2) наличие 3 очагов, 1 из которых перивентрикулярный 3) диаметр очагов в первом и втором случаях более 3 мм Fazekas F. et al. , 1988 Включая лиц, старше 50 лет, имеющих факторы риска инсульта: 1) очаги, примыкающие к телам боковых желудочков 2) очаг субтенториальной локализации 3) очаг размером не менее 6 мм. Необходимо наличие не менее двух критериев

Магнитно-резонансная томография • На МРТ в Т 2 режиме видны очаги повышенной • интенсивности, характерных размеров, формы и локализации. На Т 1 -взвешенных томограммах видно только около 20% очагов - они соответствуют полному разрушению миелина. Размер очагов 1 -5 мм, но иногда за счет слияния и перифокального отека они достигают 10 мм. "Свежие" очаги имеют неровный, нечеткий контур. Типичные места локализации "бляшек" - это участки, прилегающие к верхнелатеральному углу боковых желудочков; нижняя часть мозолистого тела; полуовальные центры. Часто очаги локализуются в мозжечке, стволе и спинном мозге. Эти изменения наблюдаются почти у 90% больных. • Текущую активность можно оценивать по данным МРТ - исследования в Т 2 режиме с контрастированием: если введение препаратов гадолиния усиливает очаг, то это достоверно свидетельствует об активном воспалении; парамагнитное контрастное вещество накапливается в зонах повышения проницаемости ГЭБ.

Магнитно-резонансная томография Кроме характерной локализации и формы "бляшек" на МРТ для PC характерно изменение размеров очагов при повторном исследовании с интервалом не менее 1 мес. Количество и размеры очагов не всегда соответствуют клиническому состоянию: распространенность очагов не отражает степень инвалидизации, а частота появления новых очагов на МРТ не совпадает с частотой обострений. Вероятность развития PC в течение 5 лет у больных с впервые возникшими неврологическими нарушениями, типичными для демиелинизирующего поражения ЦНС, но с нормальной картиной МРТ, не превышает 5%. Если при таких же нарушениях выявляются множественные очаги в белом веществе на МРТ, то вероятность развития PC увеличивается до 60%.
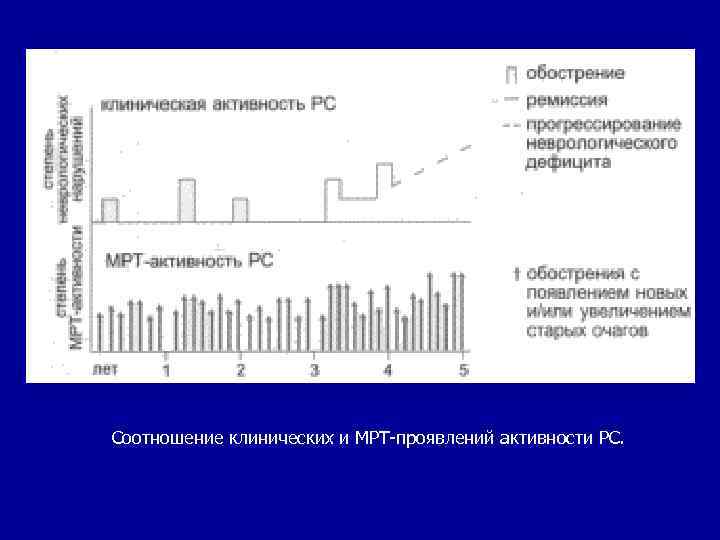
Соотношение клинических и МРТ-проявлений активности РС.

• Исследование изменений в спинномозговой жидкости (СМЖ) также помогает подтвердить диагноз PC. • В начальной стадии заболевания и ЛАБОРАТОРНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ в периоды обострения отмечается плеоцитоз (более 5 лимфоцитов в 1 мкл). У 75% больных повышен уровень гамма-глобулинов, несколько увеличено содержание общего белка. • При электрофорезе концентрированной цереброспинальной жидкости у 85 -95% больных PC выявляются олигоклональные Ig. G; этот тест можно использовать для подтверждения PC, так как он часто положителен на ранней стадии заболевания. • Аналогичной информативностью обладает выявление в СМЖ повышенного уровня свободных легких каппа-цепей иммуноглобулинов с помощью иммуноферментного анализа.
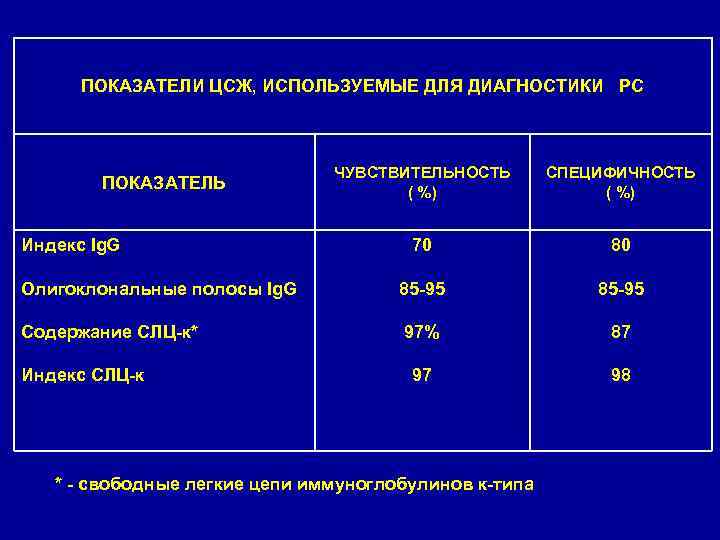
ПОКАЗАТЕЛИ ЦСЖ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ДИАГНОСТИКИ РС ПОКАЗАТЕЛЬ Индекс Ig. G ЧУВСТВИТЕЛЬНОСТЬ ( %) СПЕЦИФИЧНОСТЬ ( %) 70 Олигоклональные полосы Ig. G 85 -95 80 85 -95 Содержание СЛЦ-к* 97% 87 98 Индекс СЛЦ-к * - свободные легкие цепи иммуноглобулинов к-типа

ИНСТРУМЕНТАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ • Целесообразность исследования вызванных потенциалов у больных PC состоит в обнаружении очагов поражения ЦНС, которые не проявляют себя клинически. Изменения характеристик кривых вызванных потенциалов - неспецифичный для PC тест, характеризует замедление проведения импульса по определенным системам. Изменения зрительных вызванных потенциалов обнаруживают примерно у 80% больных; изменения слуховых вызванных потенциалов — у 50%; изменения соматосенсорных вызванных потенциалов - у 70%.
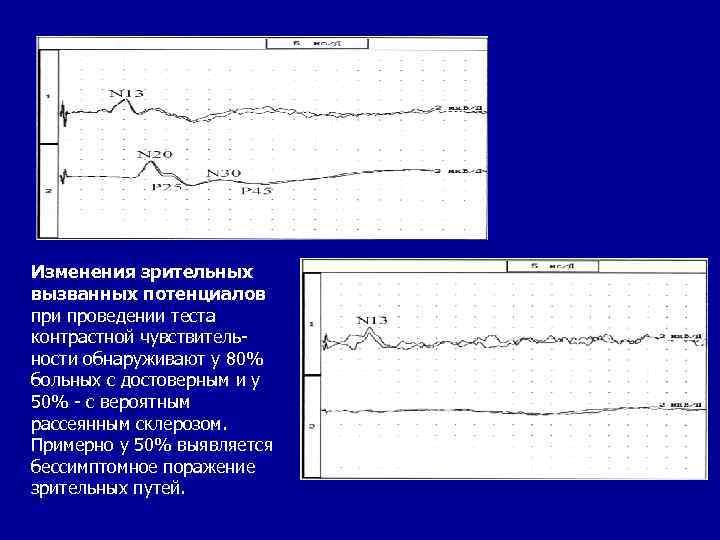
Изменения зрительных вызванных потенциалов при проведении теста контрастной чувствительности обнаруживают у 80% больных с достоверным и у 50% - с вероятным рассеянным склерозом. Примерно у 50% выявляется бессимптомное поражение зрительных путей.

Диагностические критерии фазы активности патологического процесса следующие: 1) Клинические - появление новых признаков поражения нервной системы или усугубление имеющихся, выявляемых при неврологическом осмотре с фиксацией в течение 7 -10 дней. К этой же группе относятся такие субъективные ощущения как онемение, парестезии, нарушения функции мочевого пузыря, возникающие при повторных экзацербациях РС; 2) Накопление парамагнитного контраста (гадолиний, магневист) в активных очагах демиелинизации проведении МРТ головного и спинного мозга (диагностика субклинической активности); накопление контрастного вещества (флуоресцеина) в ткани диска зрительного нерва с выходом в перипапиллярную область при флуоресцентной офтальмохромоскопии; 3) Появление "пика РС" снижения контрастной чувствительности в диапазоне 16 -20 цкл. /град на компьютерной визоконтрастограмме с положительной пробой на сердечные гликозиды (коргликон 0. 06%-1. 0 в/в) при повторных исследованиях; 4) Увеличение содержания основного белка миелина в спинномозговой жидкости в динамике (норма 2 -4 нг/мл) (диагностика субклинической активности);

КРИТЕРИИ ДИАГНОЗА РАССЕЯННОГО СКЛЕРОЗА (C. M. POSER , 1983) КАТЕГОРИЯ Клинически достоверный Достоверный, подтвержденный лабораторно КРИТЕРИИ 1) 2 обострения + 2 клинических очага 2) 2 обострения + 1 клинический очаг +1 параклинический очаг* 2 обострения + 1 клинический или параклинический очаг + олигоклональные полосы или повышенный синтез Ig. G в ЦСЖ 2) 1 обострение + 2 клинических очага + олигоклональные полосы или повышенный синтез Ig. G в ЦСЖ 3) 1 обострение + 1 клинический очаг + 1 паракпинический очаг + олигоклональные полосы или повышенный синтез Ig. G в ЦСЖ Клинически вероятный 1) 2 обострения + 1 клинический очаг 2) 1 обострение + 2 клинических очага 3) 1 обострение + 1 клинический очаг + 1 параклинический очаг Вероятный, подтвержденный лабораторно 2 обострения + олигоклональные полосы или повышенный синтез Iq. G в ЦСЖ * - очаг, зарегистрированный методами МРТ или вызванных потенциалов

При "вероятном" или "возможном" РС (W. Mac. Donald и A. Hallidey, 1977) , необходимо детальное обследование больного с привлечением дополнительных методов диагностики, с помощью которых возможно выявление субклинического поражения проводников нервной системы. На сегодняшний день наиболее информативными принято считать МРТ головного и спинного мозга и наличие олигоклональных иммуноглобулинов в ликворе больных.


ЛЕЧЕНИЕ Лечение PC остается одной из ведущих проблем неврологии. • Основными принципами лечения больных PC являются: — купирование обострения заболевания; — предотвращение или отдаление во времени развития новых обострений (либо уменьшение их выраженности и, как результат, последующих неврологических проявлений); — воздействие на симптомы, затрудняющие вести привычный образ жизни, - симптоматическое лечение; — социальная адаптация, позволяющая больному приспособиться к имеющимся проявлениям болезни, чтобы максимально облегчить его жизнь. Таким образом: В лечении рассеянного склероза существуют три основных стратегии: 1) краткосрочное лечение при обострении болезни, 2) долгосрочная профилактика, призванная предотвратить возникновение новых обострений, 3) лечение внешних проявлений болезни.
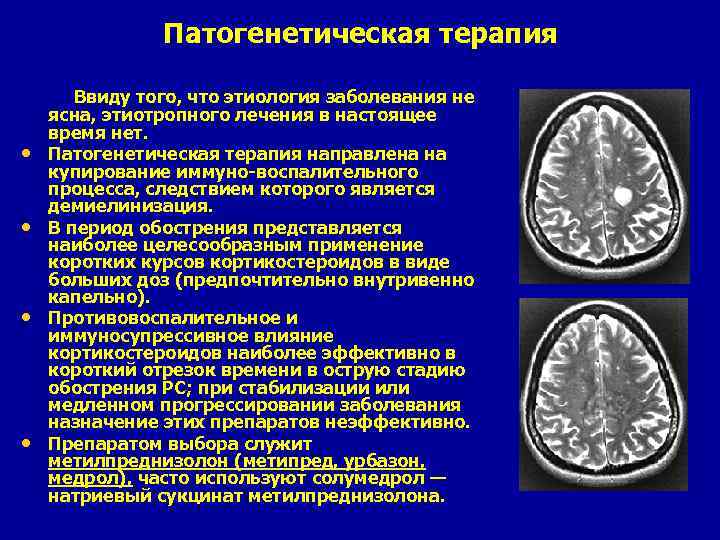
Патогенетическая терапия Ввиду того, что этиология заболевания не • • ясна, этиотропного лечения в настоящее время нет. Патогенетическая терапия направлена на купирование иммуно-воспалительного процесса, следствием которого является демиелинизация. В период обострения представляется наиболее целесообразным применение коротких курсов кортикостероидов в виде больших доз (предпочтительно внутривенно капельно). Противовоспалительное и иммуносупрессивное влияние кортикостероидов наиболее эффективно в короткий отрезок времени в острую стадию обострения PC; при стабилизации или медленном прогрессировании заболевания назначение этих препаратов неэффективно. Препаратом выбора служит метилпреднизолон (метипред, урбазон, медрол), часто используют солумедрол — натриевый сукцинат метилпреднизолона.

Патогенетическая терапия • Метилпреднизолон вводят по 1 г внутривенно 1 раз в сутки в • течение 5 -7 дней, затем переходят на преднизолон внутрь в дозе 60 -80 мг/сут в течение 7 дней, затем дозу преднизолона снижают на 10 мг каждые 4 суток и примерно через 1 мес отменяют. Метилпреднизолон уменьшает выраженность воспалительных реакций, отек и восстанавливает проведение импульсов по сохранным волокнам, что и вызывает быстрый положительный клинический эффект. Кортикостероиды уменьшают длительность и выраженность воспаления, однако не оказывают влияния на течение заболевания в последующем. Следует учитывать побочные действия гормональной терапии. Необходимо контролировать концентрацию электролитов в сыворотке и при необходимости возмещать потери калия. С целью профилактики возникновения стероидных язв и кровотечения из желудочнокишечного тракта (ЖКТ) используют антациды или циметидин. • Противопоказания для проведения гормональной терапии: непереносимость кортикостероидов; активная язва желудка, кишечника или пищевода; выраженные проявления иммунодефицита (туберкулез, герпес и другие инфекции в активных стадиях); тяжелый сахарный диабет; остеопороз; миелопролиферативные заболевания с анемией и тромбоцитопенией.

Патогенетическая терапия • При активном прогрессирующем течении PC и неэффективности кортикостероидной терапии применяются цитостатики. • Использование азатиоприна, циклофосфамида, циклоспорина А обусловлено прежде всего их системными • • иммуносупрессивными влияниями. Однако их применение ограничено из-за выраженного побочного действия. Более 7 лет при лечении PC применяется митоксантрона гидрохлорид. Это противоопухолевый синтетический препарат, применяемый для терапии миелолейкозов и лимфом. Митоксантрон эффективен при прогредиентноремиттирующем и вторично-прогрессирующем PC. Применение этого препарата уменьшает частоту и выраженность обострений, стабилизирует картину МРТ, снижает вероятность появления новых очагов демиелинизации. Его назначают внутривенно в дозе 5 -12 мг на 1 кв. м поверхности тела каждые 3 месяца в течение 2 лет. При злокачественных вариантах течения PC возможна его комбинация с кортикостероидами.

Патогенетическая терапия • В период ремиссии заболевания, а также для профилактики обострений используется группа препаратов рекомбинантного человеческого интерферона бета. • Результаты международных исследований показали, что длительный курс интерферона-beta в течение 2 лет позволяет снизить частоту обострений примерно на 30%.

Патогенетическая терапия • Бетаферон (интерферон бета-1 b) представляет собой очищенный лиофилизированный белковый продукт, получаемый методом рекомбинации ДНК. • Показания к применению этого препарата: ремиттирующее • течение PC; тяжесть заболевания не должна превышать 5, 5 балла по шкале EDSS; за предшествующие 2 года у больного должно быть менее двух достоверных обострений, после которых были периоды ремиссии или стабилизации длительностью не менее 30 дней. Бетаферон назначают в дозе 8 млн ME подкожно через день. Побочные действия: лихорадка, астения, депрессия, гриппоподобное состояние, мышечные и суставные боли, местные реакции в виде некротических изменений кожи. Противопоказания: первично-прогрессирующее течение, тяжелые сопутствующие заболевания или осложнения PC, беременность.

Патогенетическая терапия • Ребиф (интерферон бета-1 а) - высокоочищенный растворимый • белок, полученный в культуре клеток яичника китайского хомячка, идентичен интерферону бета-1 а, который образуется в человеческом организме и обладает иммуномодулирующим и антипролиферативными свойствами. Применение препарата также уменьшает выраженность и частоту обострений PC, по данным МРТ снижает вероятность появления новых очагов демиелинизации и стабилизирует состояние уже имеющихся старых. Показания к применению: ремиттирующая форма PC, характеризующаяся не менее чем двумя рецидивами за последние два года. Ребиф следует применять подкожно по 6 -12 млн ME (2244 мкг), в одно и то же время (желательно вечером) и в определенные дни недели с интервалом не менее 48 ч. Противопоказания: тяжелые нарушения функции сердца, почек, аутоиммунный гепатит, эпилепсия, беременность. К побочным действиям относятся анемия, лейкопения, тромбоцитопения, понижение АД, нарушение сна, миалгии, артралгии, повышение температуры, тошнота, рвота, депрессия, судорожные приступы.

Патогенетическая терапия • Авонекс (интерферон бета-1 а) - химическая структура, показания • • и противопоказания к применению аналогичны ребифу. Препарат вводят внутримышечно по 30 мг 1 раз в неделю. Авонекс также снижает частоту обострений PC, положительным качеством препарата является его редкое введение и отсутствие выраженных местных реакций. Выраженными иммуномодулирующими и противовирусными свойствами обладают также препараты интерферона альфа. В комплексной терапии PC эта группа препаратов изучена меньше, однако установлено снижение под действием интерферона альфа частоты обострений и числа активных очагов, выявляемых при МРТ. Выферон - (комплексный препарата содержит интерферон альфа 2 Ь, витамины Е и С); назначается в виде ректальных свечей в дозе 1 млн Ед 3 раза в неделю. Побочных эффектов от приема виферона не выявлено, противопоказание - повышенная чувствительность к маслу какао.

Патогенетическая терапия • К группе препаратов, осуществляющих антиген- специфическую иммунотерапию, относится копаксон (глатирамера ацетат). По своему строению он является смесью синтетических полипептидов, образованных природными аминокислотами (L-глютаминовой кислотой, L-аланином, L-тирозином, L-лизином), входящими в состав основного белка миелина. Копаксон обладает способностью конкурировать с этим белком и тем самым защищает его от разрушения. Основное действие копаксона - подавление миелинспецифических аутоиммунных реакций. У больных PC этот препарат уменьшает частоту обострения на треть. Наибольший эффект он оказывает у больных с минимальными функциональными нарушениями. • Копаксон вводят подкожно в дозе 20 мг ежедневно, предпочтительно в одно и то же время суток; лечение проводится длительно - в течение нескольких лет.

Патогенетическая терапия • При ремиттирующем течении PC с целью снижения частоты • обострений и прогрессирования заболевания может быть рекомендовано введение больших доз иммуноглобулинов (Santoglobulm) внутривенно 0, 15 -0, 2 г на 1 кг массы тела раз в месяц в течение 2 лет. Это лечение признано наиболее эффективным на начальной стадии заболевания (если пациент болен не более 5 лет), при частоте обострений не больше 2 раз в год. Побочные реакции крайне редки и развиваются преимущественно в начале введения препарата - тахикардия, тошнота, повышение температуры, артралгии.

Патогенетическая терапия • Важным дополнением в патогенетической терапии PC является комплексная • • • антиоксидантно-нейропротекторная терапия, проводимая в течение 1 месяца с применением: эспа-липона (тормозит экспрессию адгезивных молекул и синтез провоспалительных цитокинов, увеличивает внутриклеточное содержание глутатиона, удаляет ряд активных радикалов) - по 600 мг/сут внутривенно капельно № 10 и далее внутрь; никотинамида (защищает ДНК клеток от повреждающего действия свободных радикалов, интибирует экспрессию адгезивных молекул, уменьшает продукцию оксида азота) - по 250 -500 мг/сут внутривенно № 10 и далее внутрь; ацетилцистеина (поддерживает необходимый уровень синтеза восстановленного глутатиона) — по 600 мг/сут внутрь; токоферола (подавляет липидную пероксидацию) -- по 300 мг/сут внутрь; аскорбиновой кислоты (удаляет супероксидный радикал) - по 300 мг/сут внутрь; селена (усиливает антиоксидантные эффекты эспа-липона) - по 100 мг/сут внутрь; пентоксифиллина (снижает уровень фактора некроза опухолей альфа) - по 800 мг/сут внутрь; амантадина (блокирует глутаматные рецепторы) — по 300 мг/сут внутрь. Центральное место в такой терапии принадлежит эспа-липону (алъфа-липоевой кислоте) - универсальному антиоксиданту с наиболее широким спектром эффектов, который единственный проникает через гематоэнцефалический барьер. Указанная терапия не имеет побочных эффектов.

Патогенетическая терапия • Известные иммуномодуляторы (тималин, тимоген, Т- активин, тимозин, эхинацея) могут усиливать аутоиммунные процессы, поэтому целесообразность их применения при лечении PC сомнительна. Использование индукторов интерферона, являющихся одновременно и иммуномодуляторами (амиксина, ридостина, неовира, циклоферона), которые стимулируют выработку всех видов интерферонов, также требует осторожности. • Следует особо указать, что кортикостероиды, иммунодепрессанты, бета- и альфа-интерфероны, копаксон, антиоксиданты и иммуноглобулины не вылечивают полностью PC и не устраняют выраженные функциональные нарушения, однако позволяют оказывать положительное влияние на течение болезни.

Симптоматическая терапия • Снижение патологического мышечного гипертонуса • • наиболее важный аспект симптоматической терапии. Баклофен — активен при спинальной спастичности, оказывает сильное миорелаксирующее действие, его применяют, начиная с 5 мг 3 раза в день во время еды, затем при необходимости дозу увеличивают по 5 мг каждый 4 -й день до развития оптимального лечебного эффекта. Максимальная суточная доза ~ 60 -75 мг. Мидокалм - антиспастический препарат центрального действия; при его приеме снижение мышечного тонуса сопровождается сосудорасширяющим действием. Начальная доза устанавливается индивидуально, в зависимости от клинической картины и переносимости препарата - 50 -150 мг (1 -3 драже) 2 -3 раза в день.

Сирдалуд (тизанидина гидрохлорид) — миорелаксант центрального действия; эффективен как при остром болезненном мышечном спазме, так и при хронической спастичности спинального и церебрального происхождения; уменьшает спазмы и клонические судороги; снижает сопротивление пассивным движениям. Начальная суточная доза не должна превышать 6 мг, разделенных на 3 приема (по 2 мг 3 раза). Доза повышается постепенно с интервалами от 3 до 7 дней. Не следует превышать дозу 36 мг/сут. Побочные эффекты: головокружение, сухость во рту, сонливость, снижение АД, преходящее повышение печеночных трансаминаз (в случаях когда уровни АЛТ и ACT в сыворотке стойко превышают верхнюю границу нормы в 3 раза и более, лечение сирдалудом следует прекратить). Во время приема препарата следует избегать вождения транспортных средств или работы с механизмами и машинами.

Ботокс (гемаглютинин-комплекс ботулотоксина А) - его применение при спастичности показано, если нет контрактур, отмечаются мышечные спазмы, снижение объема движений и нарушение двигательной функции, связанные со спастичностью. Действие ботулинического токсина при внутримышечном введении связывается с блокированием нервномышечной передачи, что подавляет высвобождение ацетилхолина в синаптическую щель и приводит к парезу мышцы. При этом выделение трофических факторов в пресинаптическом окончании не нарушается и не наблюдается атрофия мышц. Клинический эффект достигается только через несколько дней и сохраняется после введения стандартных доз в течение нескольких месяцев. Восстановление способности мышцы к сокращению происходит вследствие восстановления белков, разрушенных ботулиническим токсином и разрастаний окончаний нерва (спрутинга), приводящих к образованию новых нервно-мышечных синапсов. Максимальная терапевтическая доза на 1 процедуру для взрослого человека - 400 Ед, в каждую точку разрешается вводить не более 50 Ед ботокса. Инъекции должен проводить квалифицированный врач, имеющий специальную подготовку и разрешение от фирмы-производителя.

Снижение мышечного тонуса можно добиться использованием лечебной физкультуры. Упражнения на растягивание напряженной мышцы не имеют побочных эффектов и позволяют иногда значительно снизить мышечный тонус. Важно не менее 30 мин в день делать упражнения, предназначенные для расслабления мышц, - маховые движения руками и ногами, наклоны туловища вперед и в стороны, потягиваться.

Одной из ведущих проблем больных PC является нарушение функции тазовых органов. Оно проявляется в виде частых императивных позывов, эпизодов недержания мочи или затруднения мочеиспускания. При недержании мочи, обусловленного нестабильностью функции мочевого пузыря нейрогенного характера, целесообразно использовать дриптан (оксибутинина гидрохлорид). Он оказывает расслабляющее действие на гладкую мускулатуру детрузора мочевого пузыря (как за счет прямого антиспастического эффекта, так и вследствие антихолинэргического эффекта, в результате взаимодействия ацетилхолина и мускариновых рецепторов). Препарат назначают по 5 мг 2 -3 раза в сутки. При наличии частых императивных позывов к мочеиспусканию и при недержании мочи также может быть рекомендован детрузитол (толтеродина L-тартрата). Толтеродин - антагонист холинергических мускариновых рецепторов, локализующихся в мочевом пузыре. Воздействие на эти рецепторы ведет к снижению сократительной функции мочевого пузыря. Начальная рекомендуемая доза 1 мг 2 раза в день, в дальнейшем доза может быть увеличена до 2 мг 2 раза в день. Через 6 мес следует оценить целесообразность дальнейшего лечения.

При учащенном мочеиспускании и никтурии применяют десмопрессин (адиуретин, дезурин, дефирин, минирин). Это синтетический аналог вазопрессина - увеличивая проницаемость почечных канальцев, он способствует реабсорбции воды и уменьшению диуреза. Препарат вводят интраназально по 1 - 4 капли 2 -3 раза в день. При отеке слизистой носа, вазомоторном рините возможно нарушение всасывания препарата; в таких случаях он применятся сублингвально. Противопоказания: анурия, задержка жидкости любой этиологии и состояния, при которых необходима терапия диуретиками. При задержке мочеиспускания наиболее эффективным методом являются повторные катетеризации, которые при необходимом соблюдении гигиенических норм могут проводится самим больным. Установка постоянного катетера или цистостомы проводится в экстренных случаях и сопровождается риском возникновения урологических инфекций.

Одной из ведущих проблем в симптоматической терапии PC является коррекция нарушений координации и тремора. Постуральный тремор возникает при очагах демиелинизации в области среднего мозга, красного ядра и путей, соединяющих зубчатое ядро и таламус. Рекомендуемые курсы трициклических антидепрессантов и неселективные бета-адреноблокаторы (пропранолол) приносят кратковременный эффект. Применение барбитуратов (примидон - в начальной дозе 20 -50 мг, с постепенным ее повышением) " дает нестойкое улучшение состояния. Для коррекции атаксических нарушений у больных с PC целесообразен прием бетагистина дигидрохлорида. Бетагистин (бетасерк) - синтетический аналог гистамина, он является агонистом рецепторов, участвующих в стимуляции нейронов вестибулярных ядер, что объясняет его благоприятное действие при головокружении; он стимулирует постсинаптические гистаминовые рецепторы, а также оказывает вазоактивное действие. Наиболее эффективно применение этого препарата при наличии очагов демиелинизации в области вестибулярных ядер. Бетагистин назначают в дозе 16 мг 3 раза в день во время еды.

Психопатологические симптомы - частые спутники PC. К ним относят депрессию, эйфорию, эмоциональную неустойчивость, нарушение памяти и интеллекта. При PC депрессия возникает как реакция больного на болезнь, или как следствие патологического процесса и применяемого лечения. Препаратами выбора являются блокаторы обратного захвата серотонина и трициклические антидепрессанты. К первой группе относятся прозак, золофт и др. Следует отметить, что эффект от применения этих препаратов возникает не ранее недели после начала лечения. На фоне лечения ими наблюдаются уменьшение состояния тревоги, нормализация сна. При применении трициклических антидепрессантов (амитриптилин) необходимо помнить, что эта группа препаратов значительно усиливает даже легкую задержку мочи. В некоторых случаях для коррекции психопатологических симптомов эффективна групповая и индивидуальная психотерапия.

Трансплантация клеток костного мозга Одним из возможных методов лечения PC является трансплантация клеток костного мозга (ТКМ). По данным предварительных исследований ТКМ вызывает длительный положительный эффект у животных с экспериментальным аллергическим энцефаломиелитом. Основываясь на этих результатах некоторые клинические центры начали рассматривать ТКМ как возможный способ лечения прогрессирующего рассеянного склероза. По данным Европейской группы по трансплантологии крови и костного мозга в Европе проведено несколько сот трансплантаций периферических стволовых клеток при вторично-прогрессирующем PC. У 78% пациентов в течение 3 лет состояние остается стабильным, без прогрессирования заболевания и обострений. Летальность среди них, связанная с процедурой трансплантации, составила 6% (Tyndall A. , 2001). Противопоказания: тяжелые соматические заболевания, выраженные нарушения функции печени, почек, инфекционные заболевания, степень тяжести PC более 7 баллов по EDSS.

Трансплантация стволовых клеток костного мозга проходит в несколько этапов: Первый этап - мобилизация. Производится стимуляция выхода в периферическую кровь гемопоэтических клеток и их сбор. Для этого используются препараты -циклофосфан и гранулоцитарный колониестимулирующий фактор (нейпоген). Через определенный промежуток времени осуществляется забор периферических стволовых клеток с помощью клеточного сепаратора. Эта процедура называется лейкоцитаферезом. Затем полученные клетки подвергаются криоконсервации. Второй этап - кондиционирование. Проводится высокодозная химиотерапия, которая уничтожает иммунную систему больного. Третий этап - трансплантация. Собранные гемопоэтические клетки вводятся внутривенно и формируют новую иммунную систему, в которой отсутствуют патологические клоны лимфоцитов, провоцирующие демиелинизацию. Следует учитывать, что этот метод лечения не имеет 100% положительного эффекта и обострение болезни может возникать повторно. Однако на настоящий момент ТКМ представляется одним из наиболее перспективных методов лечения PC.


ЭТИОЛОГИЧЕСКИЕ ФАКТОРЫ • Причина PC остается неизвестной. Наиболее вероятно, в основе этиологии лежит сочетание определенных внешних и генетических факторов, которое приводит к развитию патогенетических процессов с одинаковыми патоморфологическими и клиническими проявлениями. • Определенное значение в развитии заболевания имеет наличие генов • главного комплекса гистосовместимости (ВК 2 -галотип на хромосоме 6), генов цитокинов, иммуноглобулинов, белков миелина и ряда других генов. В 1995 -1997 гг. в Канаде, Великобритании, США и Финляндии проведены исследования по методу генетического скрининга, доказавшие, что РСмультигенное заболевание. Наиболее связанными с PC оказались определенные локусы на 3, 5, 6, 10, 17, 18, 19 хромосомах. • Факторы внешней среды, способствующие возникновению болезни не ясны. Высказывались предположения о роли вирусов бешенства, простого герпеса, кори, собачей чумки, Т-лимфоцитарного вируса человека (ТЛВЧ). Не исключается возможность развития при PC двойной или тройной вирусной инфекции - одновременное наличие экзогенного и эндогенного ретровирусов, один из которых запускает патогенное действие другого. Вирусные инфекции, воздействуя на иммунные реакции, способствуют развитию хронического воспалительного и аутоиммунного заболевания. Не исключается существование связи возникновения PC с хроническими интоксикациями - бензином, органическими растворителями, химикатами и с особенностями питания - преобладания в диете животных жиров и белков. Воздействие этих факторов, вероятно, также связано с иммунорегуляцией и изменением свойств миелина.

Диагностика PC • Диагностика PC основывается в первую очередь на клинических проявлениях. Одним из основных критериев является сочетание "рассеянной" симптоматики, обусловленной многоочаговым поражением белого вещества (т. е. выявление не менее двух отдельно расположенных очагов в белом веществе мозга, которые возникли не одновременно), и волнообразного течения заболевания (чередование обострений и ремиссий или колебания скорости прогрессирования). • При проведении дифференциальной диагностики целесообразно • • • использовать следующие специфические проявления, характерные для PC: - тест "горячей ванны" - резкое ухудшение состояния больного при повышении температуры окружающей среды (в частично демиелинизированных волокнах повышение температуры вызывает преходящую блокаду проведения нервного импульса); - синдром клинической диссоциации - сочетание поражений разных проводящих систем и уровней, например, снижение мышечного тонуса в сочетании с гиперрефлексией и патологическими стопными знаками; - синдром непостоянства клинических симптомов - изменение неврологической симптоматики в течение нескольких минут, часов, обусловленное повышенной восприимчивостью демиелинизированного аксона на внешние воздействия.

Своеобразие РС • • 1) Молодой возраст 2) Сырой и влажный климат (географический фактор) 3) Поражение многих функциональных систем. Возникновение РС связано со случайным индивидуальным сочетанием неблагоприятных эндогенных и экзогенных факторов риска. • К эндогенным факторам прежде всего следует отнести комплекс генов, возможно, обусловливающих генетическую несостоятельность иммунорегуляции. Из внешних факторов могут иметь значение: зона проживания, особенности питания, частота вирусных и бактериальных инфекций и др. Однако ни один взятый изолированно фактор не имеет значение в возникновении рассеянного склероза, Должно быть только определенное сочетание ряда факторов. В организме, имеющем генетически обусловленную несостоятельность регуляторных систем иммунитета, происходит активация иммунной системы одним из неспецифических провоцирующих факторов, например, вирусной инфекцией, травмой, стрессовой ситуацией. При этом антиген-стимулированные макрофаги и активированные Т-хелперы фиксируются на клетках эндотелия гематоэнцефалического барьера. Цитокины, выделяемые фиксированными клетками, экспрессируют на поверхности ГЭБ антигены основного комплекса гистосовместимости I и II класса, а также молекулы клеточной адгезии.

Диагностика рассеянного склероза (РС) основывается на данных анамнеза, неврологического осмотра и результатах дополнительных методов обследования. Главный критерий диагностики РС: "диссеминация симптомов в месте и времени". Этот термин подразумевает хроническое волнообразное течение заболевания с вовлечением в патологический процесс нескольких проводящих систем. Классическими клиническими критериями диагностики РС являются клинические диагностические критерии достоверного РС. К ним относятся: 1. Наличие объективных свидетельств поражения нервной системы. 2. На основании данных неврологического осмотра или анамнеза должны быть выявлены признаки по крайней мере 2 раздельно расположенных очагов. 3. Неврологические симптомы должны свидетельствовать о поражении белого вещества, головного и спинного мозга, т. е. проводников. 4. Клинические симптомы должны иметь преходящий характер, выполняя одно из следующих требований: а) должно быть два или более эпизодов ухудшения, разделенных периодом не менее 1 мес и продолжительностью не менее 24 ч. б) должно быть медленное, постепенное прогрессирование на протяжении по крайней мере 6 мес. 5. Заболевание начинается в возрасте от 10 до 50 лет включительно. 6. Имеющиеся неврологические нарушения не могут быть более адекватно объяснены другим патологическим процессом.

ЭТИОЛОГИЧЕСКИЕ ФАКТОРЫ • Причина PC остается неизвестной. Наиболее вероятно, в основе этиологии лежит сочетание определенных внешних и генетических факторов, которое приводит к развитию патогенетических процессов с одинаковыми патоморфологическими и клиническими проявлениями. • Определенное значение в развитии заболевания имеет наличие генов • главного комплекса гистосовместимости (ВК 2 -галотип на хромосоме 6), генов цитокинов, иммуноглобулинов, белков миелина и ряда других генов. В 1995 -1997 гг. в Канаде, Великобритании, США и Финляндии проведены исследования по методу генетического скрининга, доказавшие, что РСмультигенное заболевание. Наиболее связанными с PC оказались определенные локусы на 3, 5, 6, 10, 17, 18, 19 хромосомах. • Факторы внешней среды, способствующие возникновению болезни не ясны. • Высказывались предположения о роли вирусов бешенства, простого герпеса, кори, собачей чумки, Т-лимфоцитарного вируса человека (ТЛВЧ). Не исключается возможность развития при PC двойной или тройной вирусной инфекции - одновременное наличие экзогенного и эндогенного ретровирусов, один из которых запускает патогенное действие другого. Вирусные инфекции, воздействуя на иммунные реакции, способствуют развитию аутоиммунного воспалительного процесса. Не исключается существование связи возникновения PC с хроническими интоксикациями - бензином, органическими растворителями, химикатами и с особенностями питания - преобладания в диете животных жиров и белков. Воздействие этих факторов, вероятно, также связано с иммунорегуляцией и изменением свойств миелина.
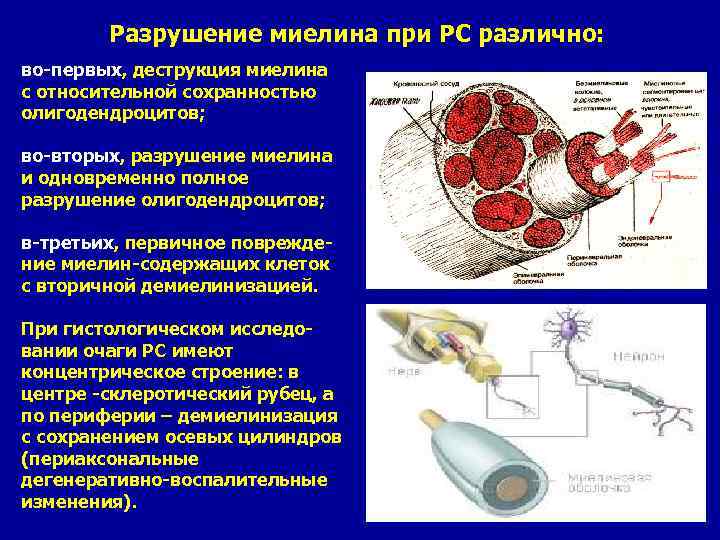
Разрушение миелина при PC различно: во-первых, деструкция миелина с относительной сохранностью олигодендроцитов; во-вторых, разрушение миелина и одновременно полное разрушение олигодендроцитов; в-третьих, первичное повреждение миелин-содержащих клеток с вторичной демиелинизацией. При гистологическом исследовании очаги PC имеют концентрическое строение: в центре -склеротический рубец, а по периферии – демиелинизация с сохранением осевых цилиндров (периаксональные дегенеративно-воспалительные изменения).
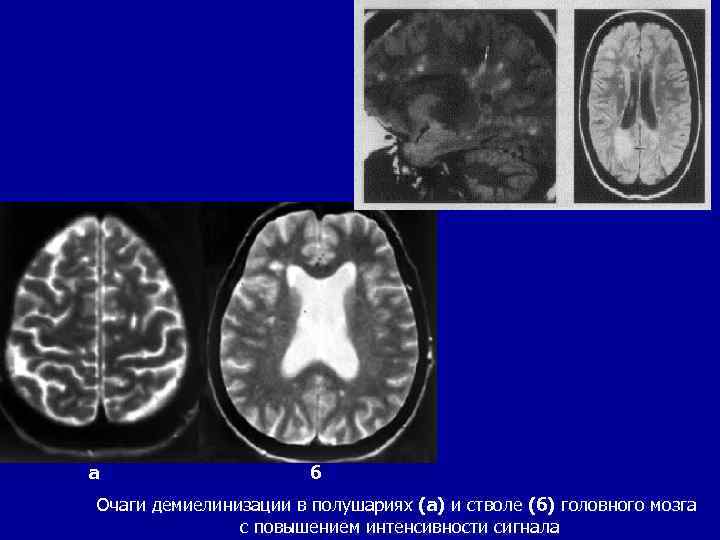
а б Очаги демиелинизации в полушариях (а) и стволе (б) головного мозга с повышением интенсивности сигнала
Энцефаломиелит рассеянный (2011).ppt