 Распределение электронов по уровням и подуровням
Распределение электронов по уровням и подуровням
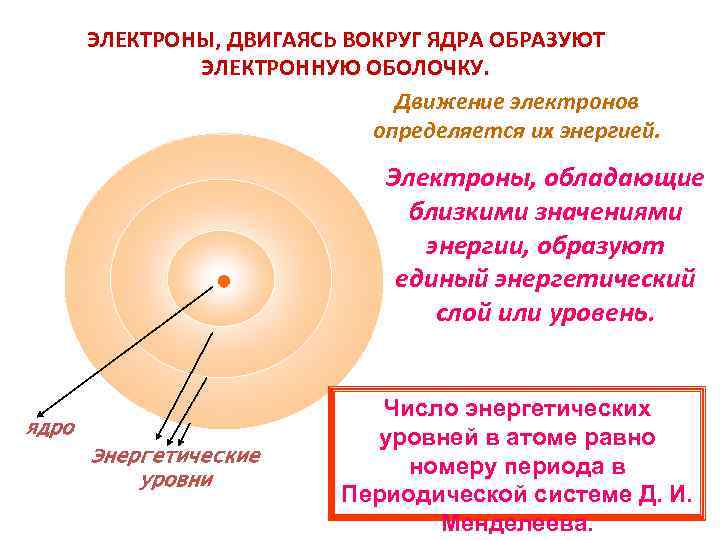 ЭЛЕКТРОНЫ, ДВИГАЯСЬ ВОКРУГ ЯДРА ОБРАЗУЮТ ЭЛЕКТРОННУЮ ОБОЛОЧКУ. Движение электронов определяется их энергией. Электроны, обладающие близкими значениями энергии, образуют единый энергетический слой или уровень. ядро Энергетические уровни Число энергетических уровней в атоме равно номеру периода в Периодической системе Д. И. Менделеева.
ЭЛЕКТРОНЫ, ДВИГАЯСЬ ВОКРУГ ЯДРА ОБРАЗУЮТ ЭЛЕКТРОННУЮ ОБОЛОЧКУ. Движение электронов определяется их энергией. Электроны, обладающие близкими значениями энергии, образуют единый энергетический слой или уровень. ядро Энергетические уровни Число энергетических уровней в атоме равно номеру периода в Периодической системе Д. И. Менделеева.
 Количество электронов на энергетическом уровне определяется по формуле 2 n 2, где n число обозначающее номер энергетического уровня и его называют главным квантовым числом. 2 х12 2 II уровень 2 х22 8 III уровень 2 х32 18 I уровень
Количество электронов на энергетическом уровне определяется по формуле 2 n 2, где n число обозначающее номер энергетического уровня и его называют главным квантовым числом. 2 х12 2 II уровень 2 х22 8 III уровень 2 х32 18 I уровень
 СХЕМЫ ЭЛЕКТРОННОГО СТРОЕНИЯ АТОМОВ Li Be B C N O F Ne 2 e, 1 e 2 e, 2 e 2 e 3 e 2 e, 4 e 2 e, 5 e 2 e, 6 e 2 e, 7 e 2 e, 8 e Схемы электронного строения атомов показывают как электроны размещаются на энергетических уровнях. Завершенный уровень
СХЕМЫ ЭЛЕКТРОННОГО СТРОЕНИЯ АТОМОВ Li Be B C N O F Ne 2 e, 1 e 2 e, 2 e 2 e 3 e 2 e, 4 e 2 e, 5 e 2 e, 6 e 2 e, 7 e 2 e, 8 e Схемы электронного строения атомов показывают как электроны размещаются на энергетических уровнях. Завершенный уровень
 Энергетические уровни (начиная со 2 -го) подразделяются на подуровни (n), несколько отличающиеся друг от друга энергией связи с ядром Число подуровней (n) равно значению главного квантового числа: 1 2 3 4 уровень -1 -2 -3 - 4 Каждому значению (n) соответствует число орбиталей, равное n 2.
Энергетические уровни (начиная со 2 -го) подразделяются на подуровни (n), несколько отличающиеся друг от друга энергией связи с ядром Число подуровней (n) равно значению главного квантового числа: 1 2 3 4 уровень -1 -2 -3 - 4 Каждому значению (n) соответствует число орбиталей, равное n 2.
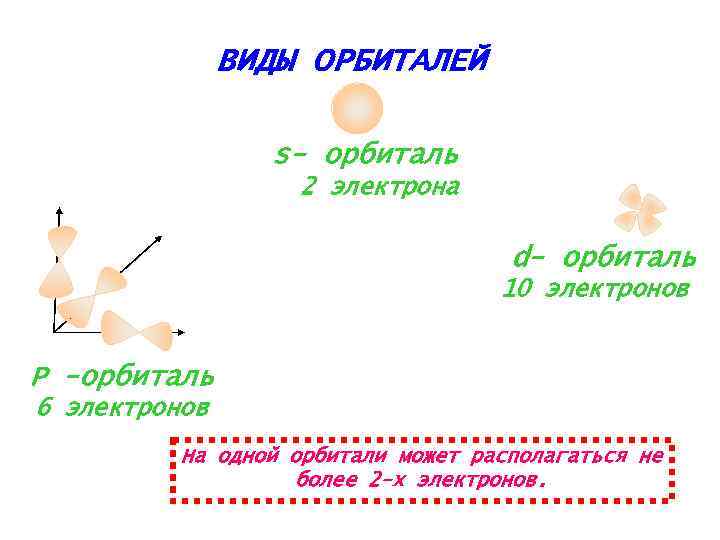 ВИДЫ ОРБИТАЛЕЙ s- орбиталь 2 электрона d- орбиталь 10 электронов Р -орбиталь 6 электронов На одной орбитали может располагаться не более 2 -х электронов.
ВИДЫ ОРБИТАЛЕЙ s- орбиталь 2 электрона d- орбиталь 10 электронов Р -орбиталь 6 электронов На одной орбитали может располагаться не более 2 -х электронов.
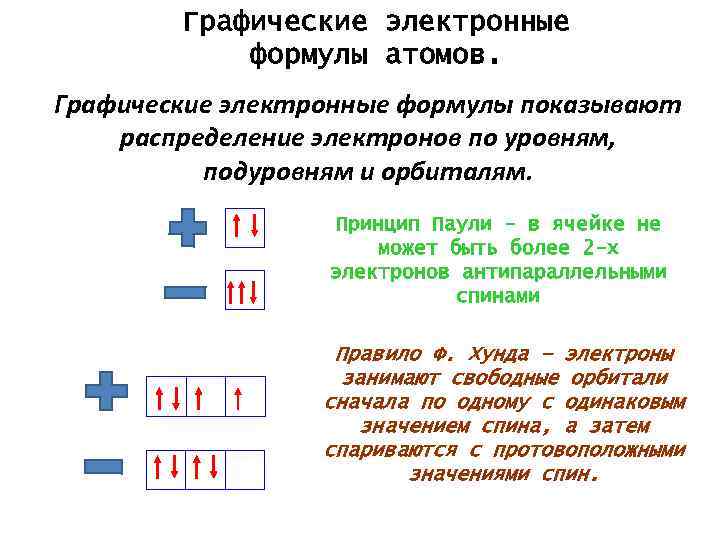 Графические электронные формулы атомов. Графические электронные формулы показывают распределение электронов по уровням, подуровням и орбиталям. Принцип Паули - в ячейке не может быть более 2 -х электронов антипараллельными спинами Правило Ф. Хунда – электроны занимают свободные орбитали сначала по одному с одинаковым значением спина, а затем спариваются с протовоположными значениями спин.
Графические электронные формулы атомов. Графические электронные формулы показывают распределение электронов по уровням, подуровням и орбиталям. Принцип Паули - в ячейке не может быть более 2 -х электронов антипараллельными спинами Правило Ф. Хунда – электроны занимают свободные орбитали сначала по одному с одинаковым значением спина, а затем спариваются с протовоположными значениями спин.
 Распределение электронов по уровням 1 уровень - 2 2 уровень - 8 3 уровень - 18 4 уровень - 32 8
Распределение электронов по уровням 1 уровень - 2 2 уровень - 8 3 уровень - 18 4 уровень - 32 8
 Подуровни принято обозначать теми же буквами, что и формы орбиталей: s, p, d, f. S - подуровень – первый, ближайший к ядру атома подуровень каждого энергетического уровня, состоит из одной s-орбитали. P - подуровень – второй подуровень каждого ( кроме 1 -го) энергетического уровня, состоит из 3 -х p-орбиталей d - подуровень – третий подуровень каждого, начиная с 3 -го , энергетического уровня, состоит из 5 d-орбиталей f- подуровень – четвертый подуровень каждого, начиная с 4 -го энергетического уровня, состоит из 7 -ми f-орбиталей.
Подуровни принято обозначать теми же буквами, что и формы орбиталей: s, p, d, f. S - подуровень – первый, ближайший к ядру атома подуровень каждого энергетического уровня, состоит из одной s-орбитали. P - подуровень – второй подуровень каждого ( кроме 1 -го) энергетического уровня, состоит из 3 -х p-орбиталей d - подуровень – третий подуровень каждого, начиная с 3 -го , энергетического уровня, состоит из 5 d-орбиталей f- подуровень – четвертый подуровень каждого, начиная с 4 -го энергетического уровня, состоит из 7 -ми f-орбиталей.
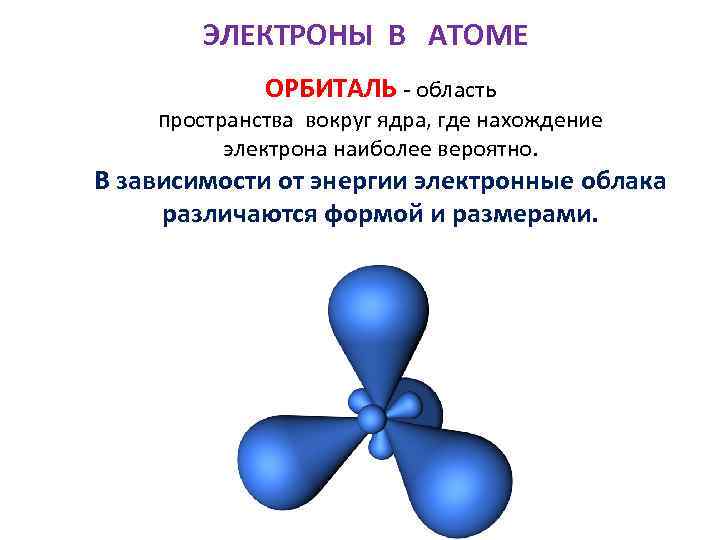 ЭЛЕКТРОНЫ В АТОМЕ ОРБИТАЛЬ - область пространства вокруг ядра, где нахождение электрона наиболее вероятно. В зависимости от энергии электронные облака различаются формой и размерами.
ЭЛЕКТРОНЫ В АТОМЕ ОРБИТАЛЬ - область пространства вокруг ядра, где нахождение электрона наиболее вероятно. В зависимости от энергии электронные облака различаются формой и размерами.
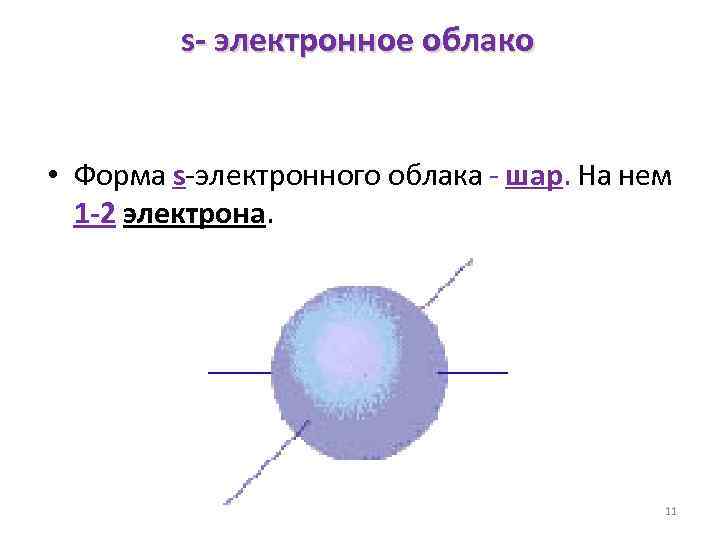 s- электронное облако • Форма s-электронного облака - шар. На нем 1 -2 электрона. 11
s- электронное облако • Форма s-электронного облака - шар. На нем 1 -2 электрона. 11
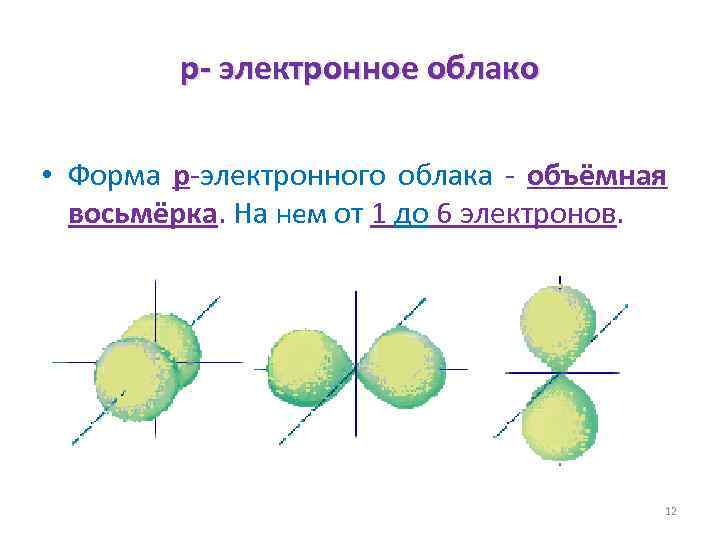 p- электронное облако • Форма p-электронного облака - объёмная восьмёрка. На нем от 1 до 6 электронов. 12
p- электронное облако • Форма p-электронного облака - объёмная восьмёрка. На нем от 1 до 6 электронов. 12
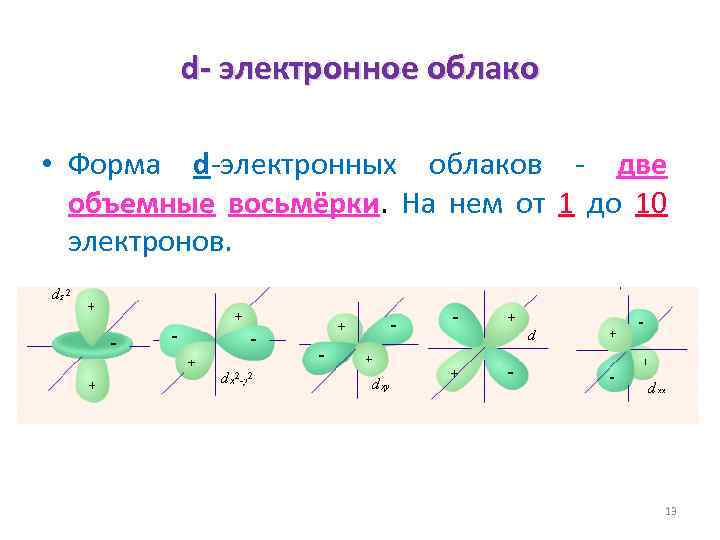 d- электронное облако • Форма d-электронных облаков - две объемные восьмёрки. На нем от 1 до 10 электронов. 13
d- электронное облако • Форма d-электронных облаков - две объемные восьмёрки. На нем от 1 до 10 электронов. 13
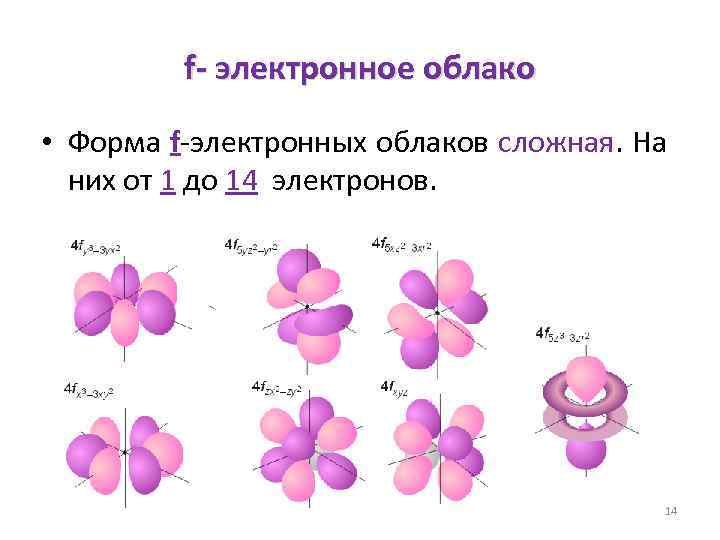 f- электронное облако • Форма f-электронных облаков сложная. На них от 1 до 14 электронов. 14
f- электронное облако • Форма f-электронных облаков сложная. На них от 1 до 14 электронов. 14