Презентация Материаловедения (2).ppt
- Количество слайдов: 134
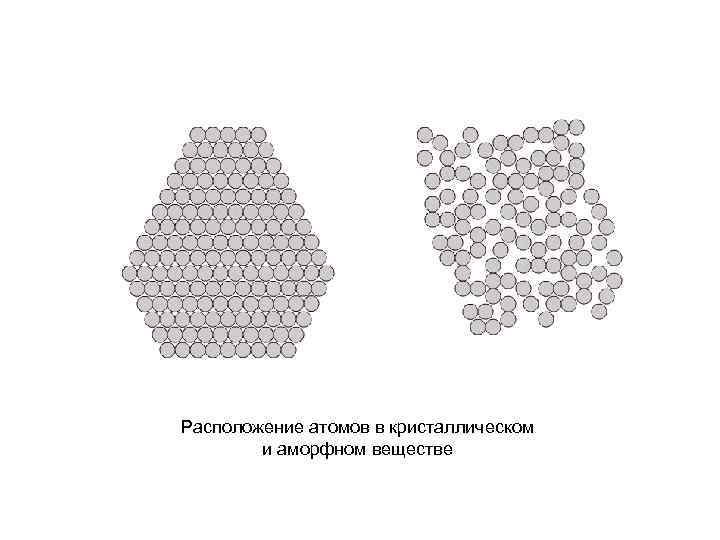 Расположение атомов в кристаллическом и аморфном веществе
Расположение атомов в кристаллическом и аморфном веществе
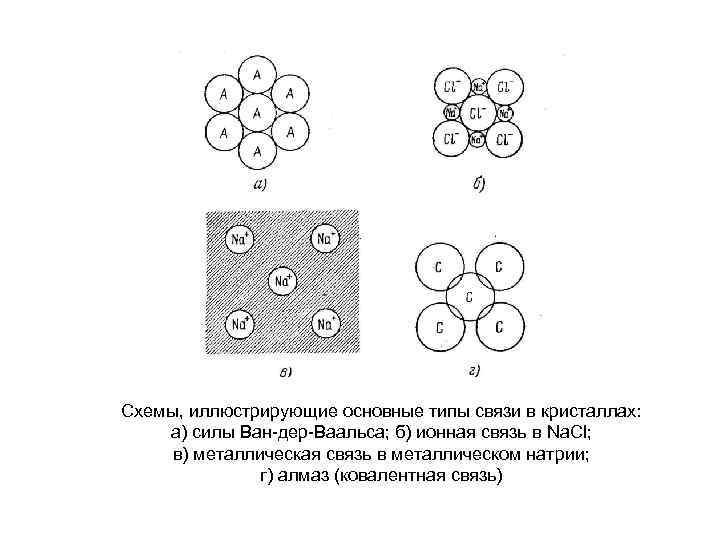 Схемы, иллюстрирующие основные типы связи в кристаллах: а) силы Ван дер Ваальса; б) ионная связь в Na. Cl; в) металлическая связь в металлическом натрии; г) алмаз (ковалентная связь)
Схемы, иллюстрирующие основные типы связи в кристаллах: а) силы Ван дер Ваальса; б) ионная связь в Na. Cl; в) металлическая связь в металлическом натрии; г) алмаз (ковалентная связь)
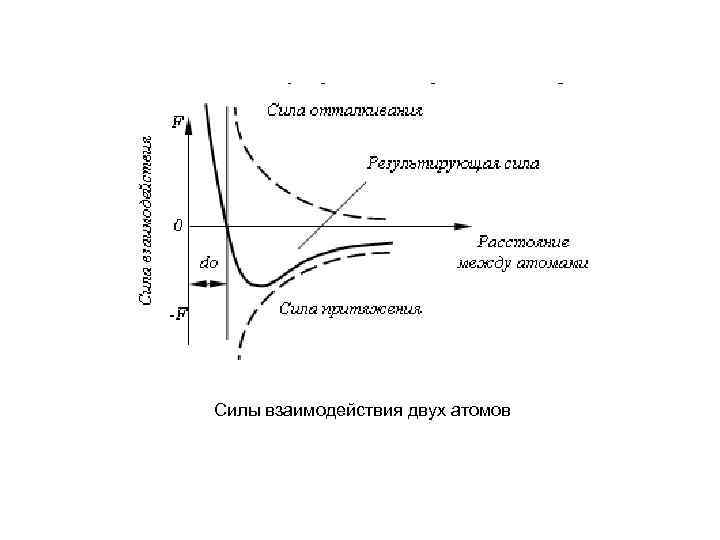 Силы взаимодействия двух атомов
Силы взаимодействия двух атомов
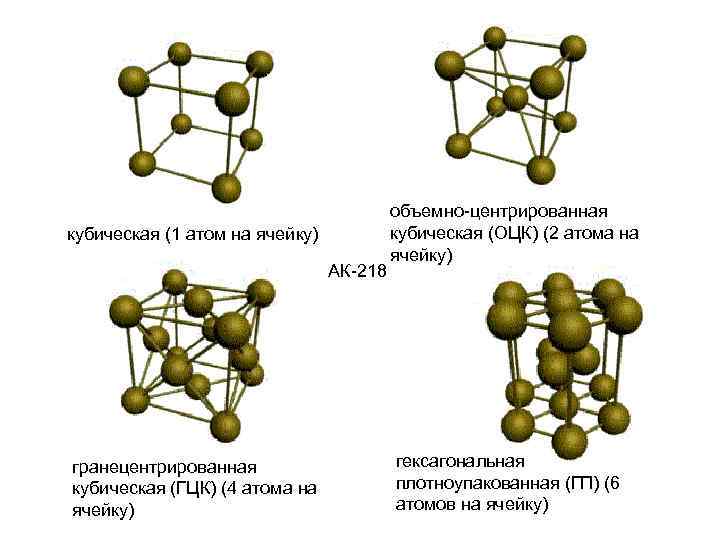 кубическая (1 атом на ячейку) АК 218 гранецентрированная кубическая (ГЦК) (4 атома на ячейку) объемно центрированная кубическая (ОЦК) (2 атома на ячейку) гексагональная плотноупакованная (ГП) (6 атомов на ячейку)
кубическая (1 атом на ячейку) АК 218 гранецентрированная кубическая (ГЦК) (4 атома на ячейку) объемно центрированная кубическая (ОЦК) (2 атома на ячейку) гексагональная плотноупакованная (ГП) (6 атомов на ячейку)
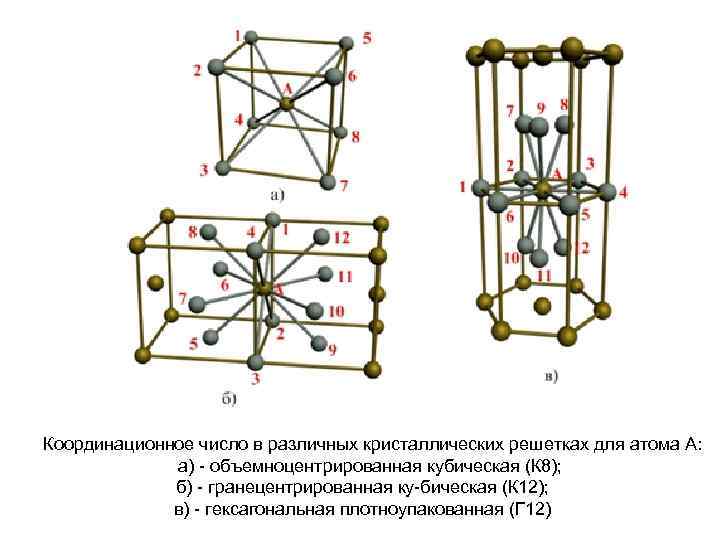 Координационное число в различных кристаллических решетках для атома А: а) объемноцентрированная кубическая (К 8); б) гранецентрированная ку бическая (К 12); в) гексагональная плотноупакованная (Г 12)
Координационное число в различных кристаллических решетках для атома А: а) объемноцентрированная кубическая (К 8); б) гранецентрированная ку бическая (К 12); в) гексагональная плотноупакованная (Г 12)
![[001] z z (111) (110) (010) [010] y y [100] x x (100) [110] [001] z z (111) (110) (010) [010] y y [100] x x (100) [110]](https://present5.com/presentation/3/-30190121_127121967.pdf-img/-30190121_127121967.pdf-6.jpg) [001] z z (111) (110) (010) [010] y y [100] x x (100) [110] Кристаллографические направления и плоскости в кристаллической решетке: основные направления [001]; основные плоскости (001)
[001] z z (111) (110) (010) [010] y y [100] x x (100) [110] Кристаллографические направления и плоскости в кристаллической решетке: основные направления [001]; основные плоскости (001)
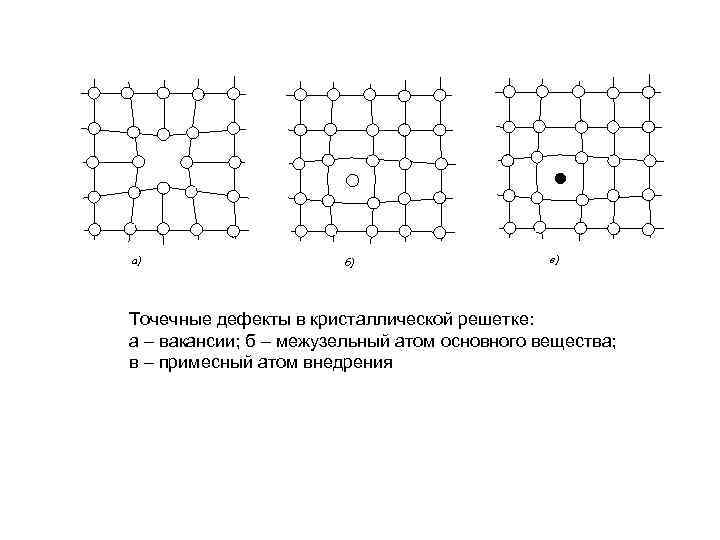 а) б) в) Точечные дефекты в кристаллической решетке: а – вакансии; б – межузельный атом основного вещества; в – примесный атом внедрения
а) б) в) Точечные дефекты в кристаллической решетке: а – вакансии; б – межузельный атом основного вещества; в – примесный атом внедрения
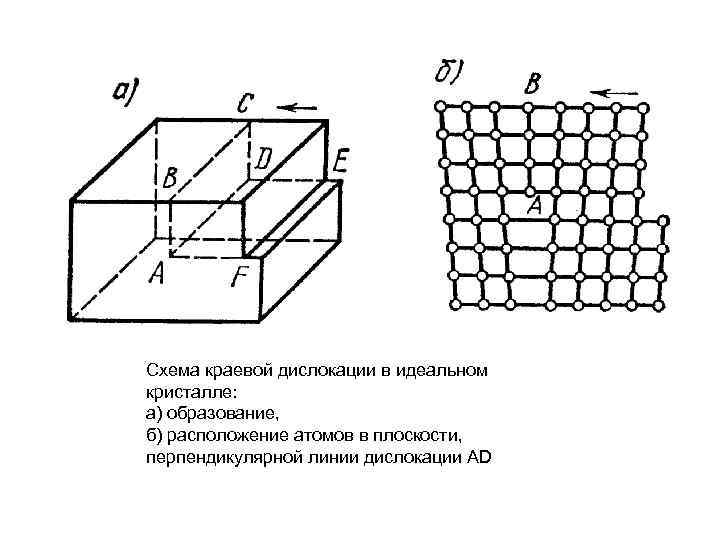 Схема краевой дислокации в идеальном кристалле: а) образование, б) расположение атомов в плоскости, перпендикулярной линии дислокации AD
Схема краевой дислокации в идеальном кристалле: а) образование, б) расположение атомов в плоскости, перпендикулярной линии дислокации AD
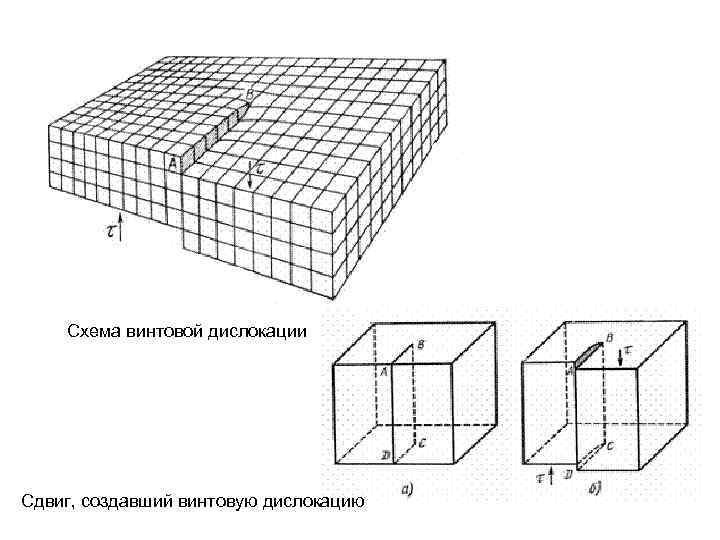 Схема винтовой дислокации Сдвиг, создавший винтовую дислокацию
Схема винтовой дислокации Сдвиг, создавший винтовую дислокацию
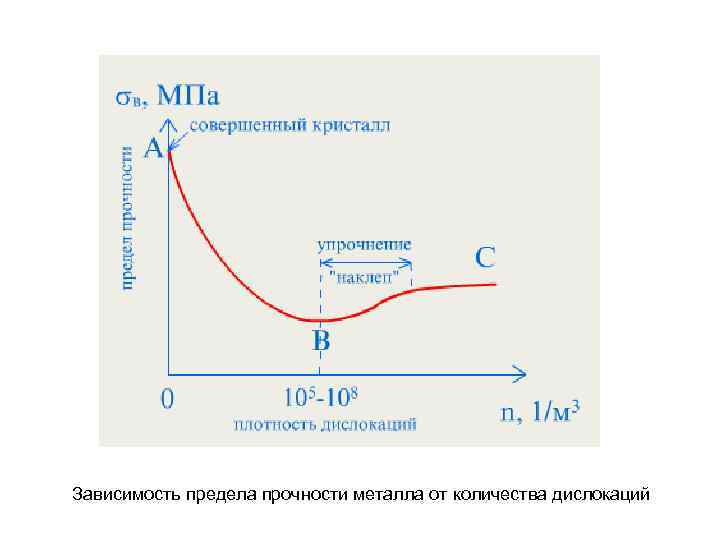 Зависимость предела прочности металла от количества дислокаций
Зависимость предела прочности металла от количества дислокаций
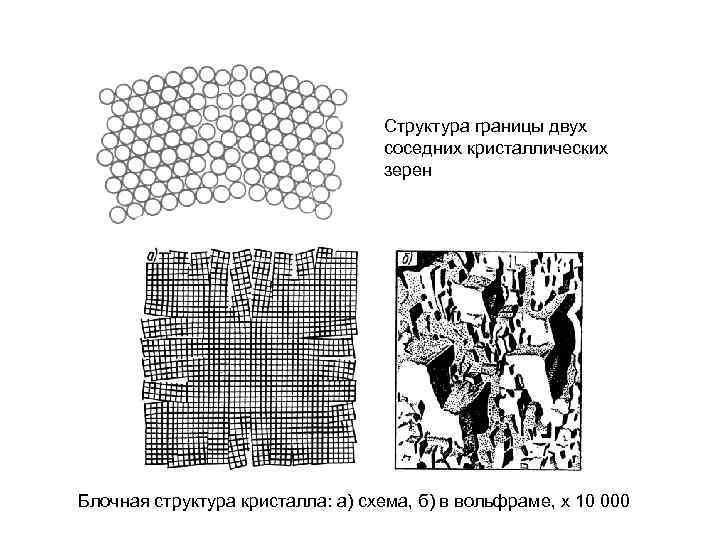 Структура границы двух соседних кристаллических зерен Блочная структура кристалла: а) схема, б) в вольфраме, х 10 000
Структура границы двух соседних кристаллических зерен Блочная структура кристалла: а) схема, б) в вольфраме, х 10 000
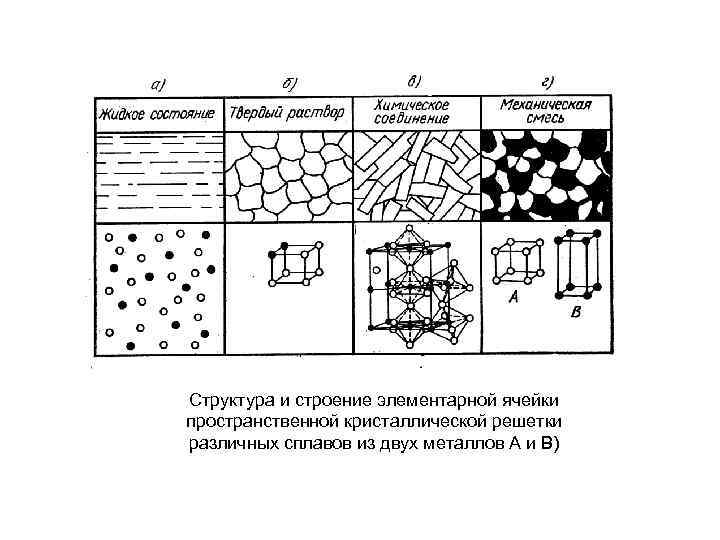 Структура и строение элементарной ячейки пространственной кристаллической решетки различных сплавов из двух металлов А и В)
Структура и строение элементарной ячейки пространственной кристаллической решетки различных сплавов из двух металлов А и В)
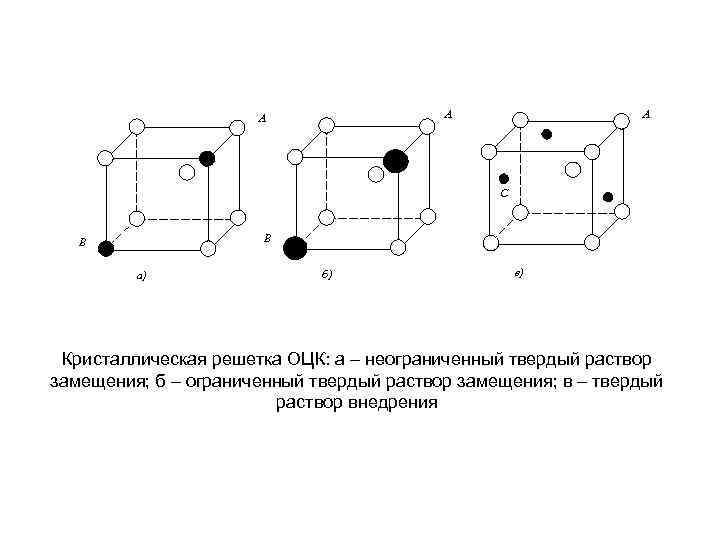 А А А С В В а) б) в) Кристаллическая решетка ОЦК: а – неограниченный твердый раствор замещения; б – ограниченный твердый раствор замещения; в – твердый раствор внедрения
А А А С В В а) б) в) Кристаллическая решетка ОЦК: а – неограниченный твердый раствор замещения; б – ограниченный твердый раствор замещения; в – твердый раствор внедрения
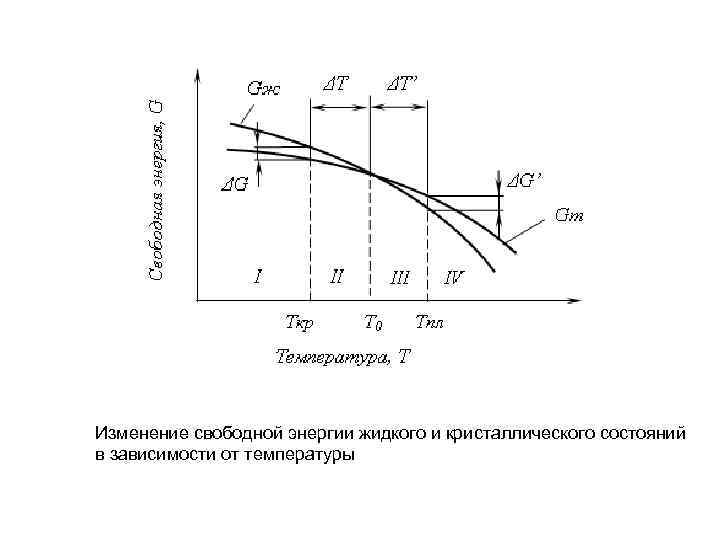 Изменение свободной энергии жидкого и кристаллического состояний в зависимости от температуры
Изменение свободной энергии жидкого и кристаллического состояний в зависимости от температуры
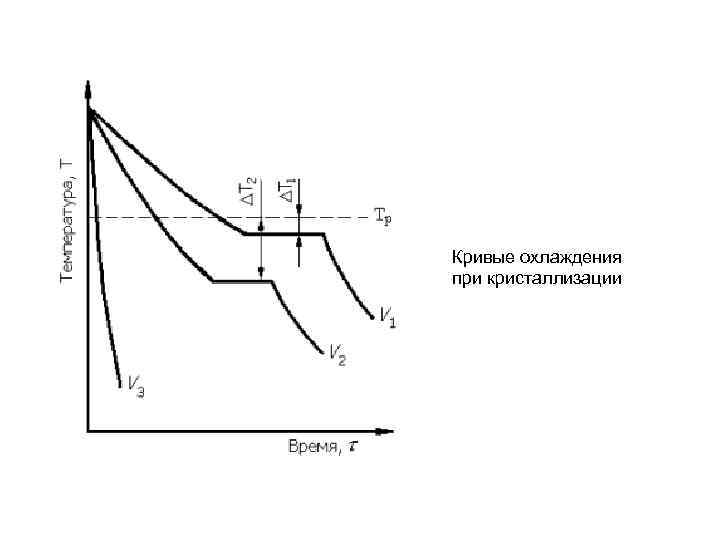 Кривые охлаждения при кристаллизации
Кривые охлаждения при кристаллизации
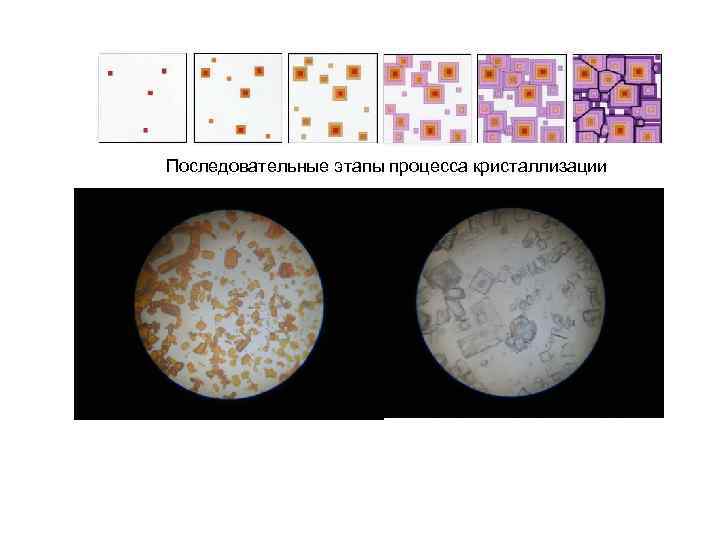 Последовательные этапы процесса кристаллизации
Последовательные этапы процесса кристаллизации
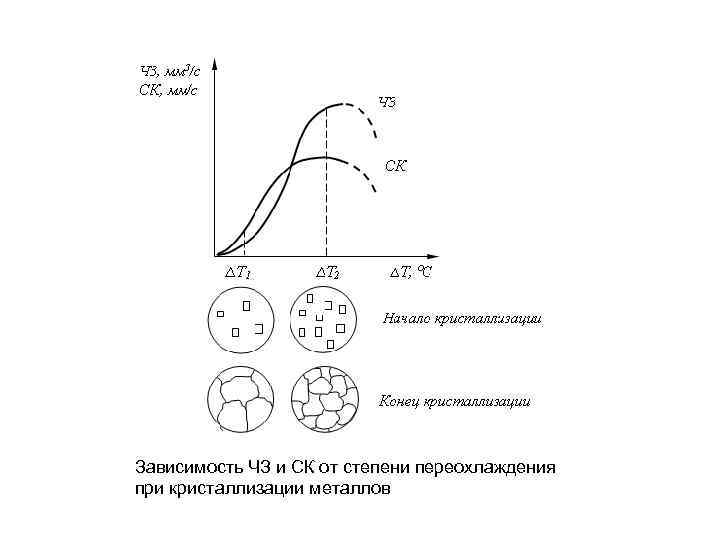 Зависимость ЧЗ и СК от степени переохлаждения при кристаллизации металлов
Зависимость ЧЗ и СК от степени переохлаждения при кристаллизации металлов
 Схема строения дендрита: 1– 3 – оси первого, второго и третьего порядка
Схема строения дендрита: 1– 3 – оси первого, второго и третьего порядка
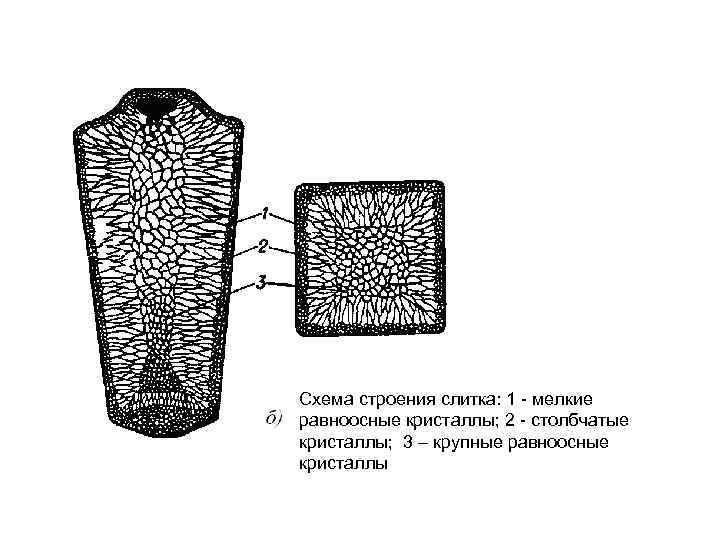 Схема строения слитка: 1 мелкие равноосные кристаллы; 2 столбчатые кристаллы; 3 – крупные равноосные кристаллы
Схема строения слитка: 1 мелкие равноосные кристаллы; 2 столбчатые кристаллы; 3 – крупные равноосные кристаллы
 Строение реального стального слитка
Строение реального стального слитка
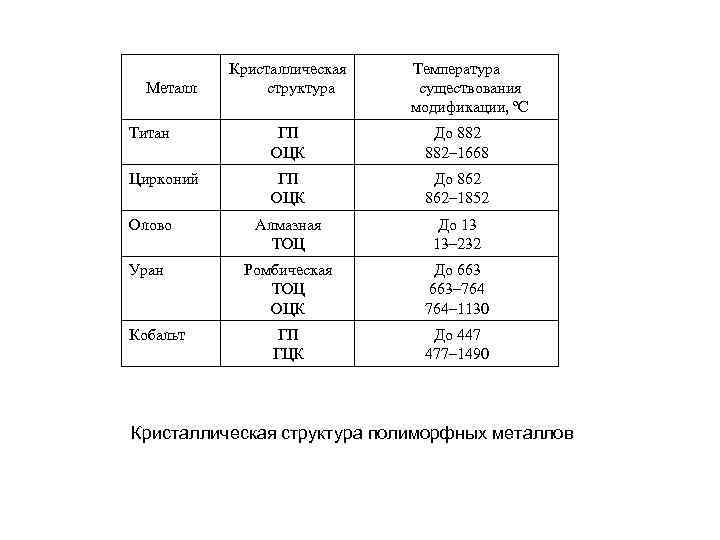 Металл Кристаллическая структура Температура существования модификации, ºС Титан ГП ОЦК До 882– 1668 Цирконий ГП ОЦК До 862– 1852 Олово Алмазная ТОЦ До 13 13– 232 Уран Ромбическая ТОЦ ОЦК До 663– 764– 1130 ГП ГЦК До 447 477– 1490 Кобальт Кристаллическая структура полиморфных металлов
Металл Кристаллическая структура Температура существования модификации, ºС Титан ГП ОЦК До 882– 1668 Цирконий ГП ОЦК До 862– 1852 Олово Алмазная ТОЦ До 13 13– 232 Уран Ромбическая ТОЦ ОЦК До 663– 764– 1130 ГП ГЦК До 447 477– 1490 Кобальт Кристаллическая структура полиморфных металлов
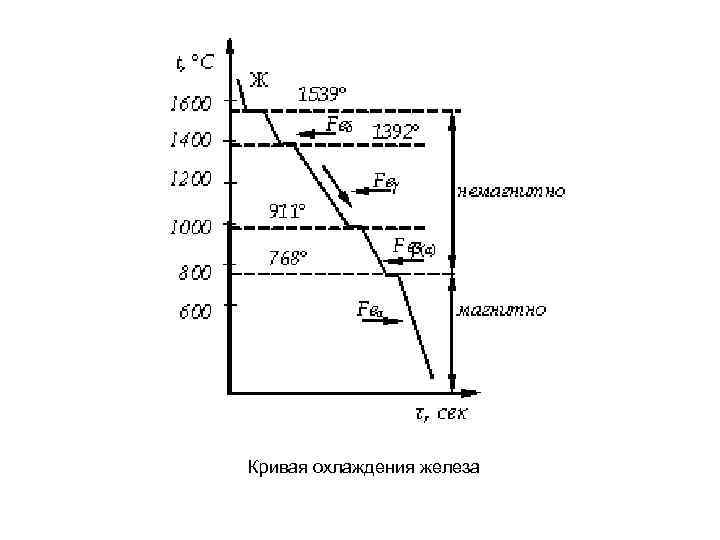 Кривая охлаждения железа
Кривая охлаждения железа
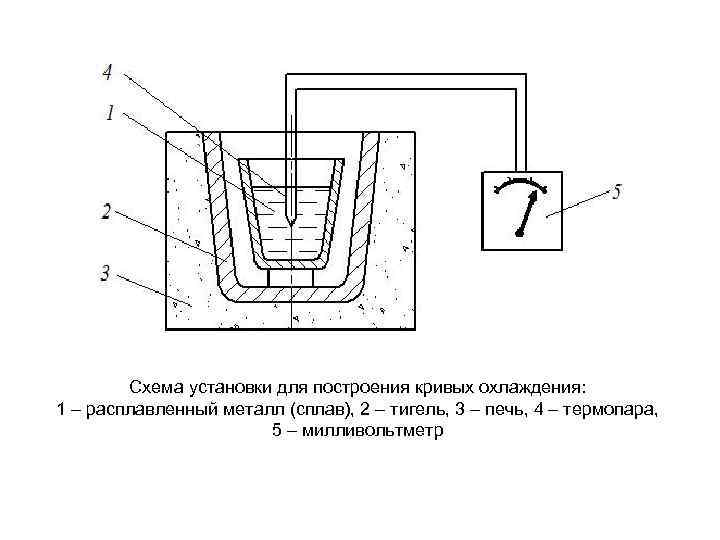 Схема установки для построения кривых охлаждения: 1 – расплавленный металл (сплав), 2 – тигель, 3 – печь, 4 – термопара, 5 – милливольтметр
Схема установки для построения кривых охлаждения: 1 – расплавленный металл (сплав), 2 – тигель, 3 – печь, 4 – термопара, 5 – милливольтметр
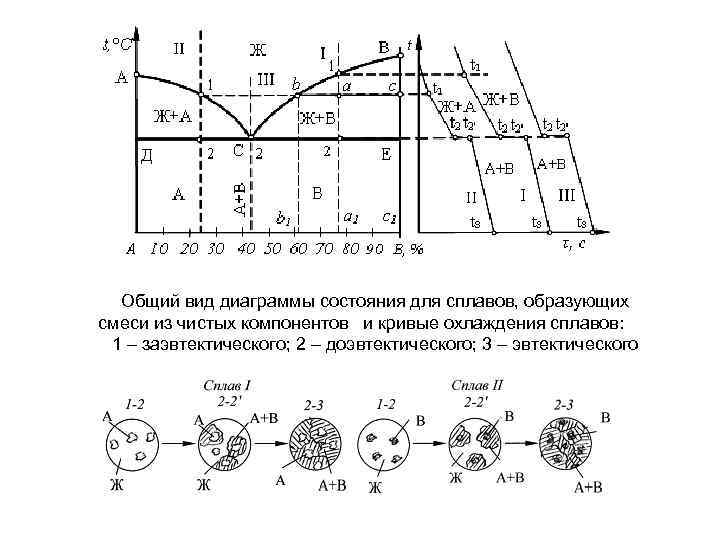 Общий вид диаграммы состояния для сплавов, образующих смеси из чистых компонентов и кривые охлаждения сплавов: 1 – заэвтектического; 2 – доэвтектического; 3 – эвтектического
Общий вид диаграммы состояния для сплавов, образующих смеси из чистых компонентов и кривые охлаждения сплавов: 1 – заэвтектического; 2 – доэвтектического; 3 – эвтектического
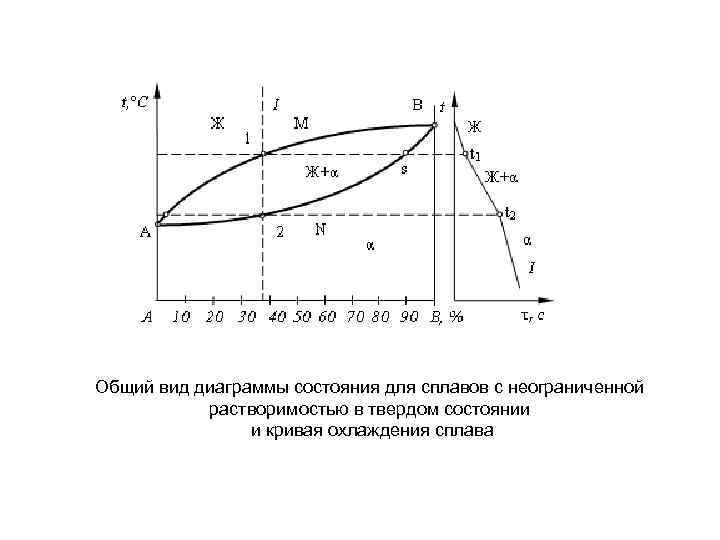 Общий вид диаграммы состояния для сплавов с неограниченной растворимостью в твердом состоянии и кривая охлаждения сплава
Общий вид диаграммы состояния для сплавов с неограниченной растворимостью в твердом состоянии и кривая охлаждения сплава
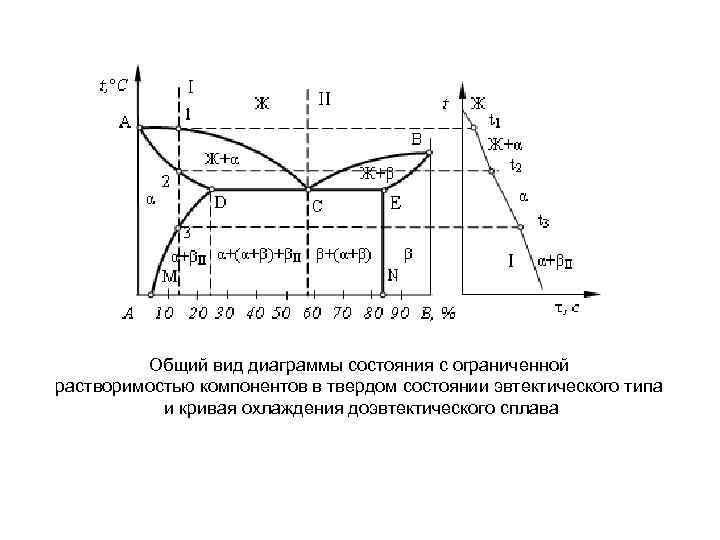 Общий вид диаграммы состояния с ограниченной растворимостью компонентов в твердом состоянии эвтектического типа и кривая охлаждения доэвтектического сплава
Общий вид диаграммы состояния с ограниченной растворимостью компонентов в твердом состоянии эвтектического типа и кривая охлаждения доэвтектического сплава
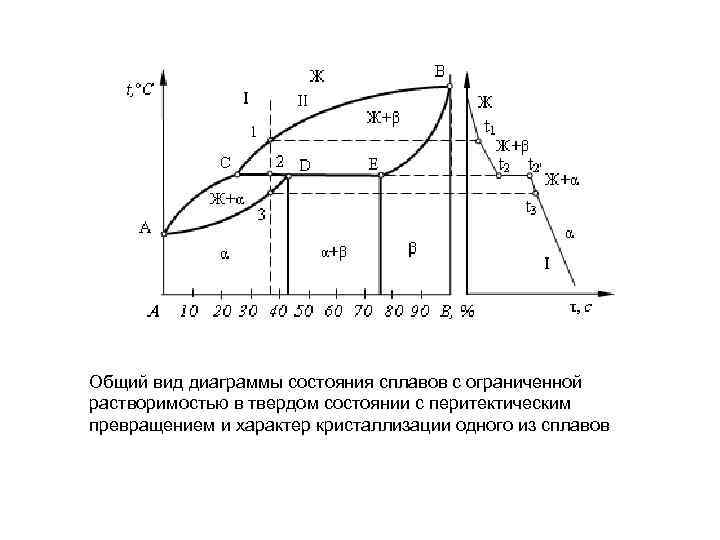 Общий вид диаграммы состояния сплавов с ограниченной растворимостью в твердом состоянии с перитектическим превращением и характер кристаллизации одного из сплавов
Общий вид диаграммы состояния сплавов с ограниченной растворимостью в твердом состоянии с перитектическим превращением и характер кристаллизации одного из сплавов
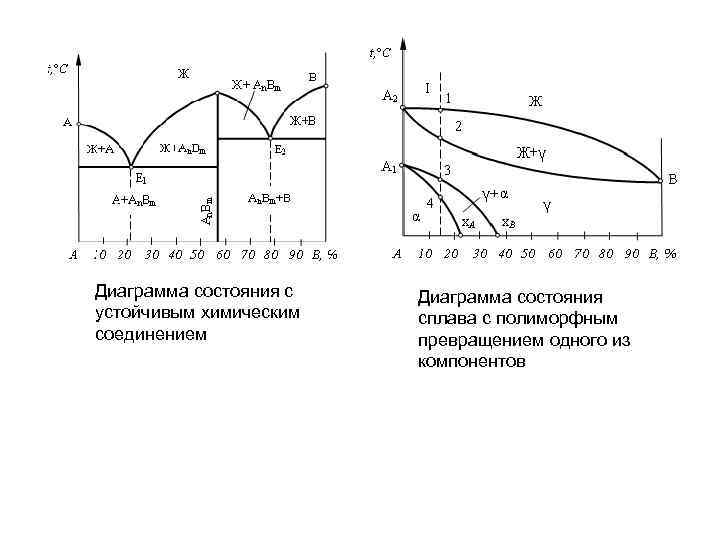 Диаграмма состояния с устойчивым химическим соединением Диаграмма состояния сплава с полиморфным превращением одного из компонентов
Диаграмма состояния с устойчивым химическим соединением Диаграмма состояния сплава с полиморфным превращением одного из компонентов
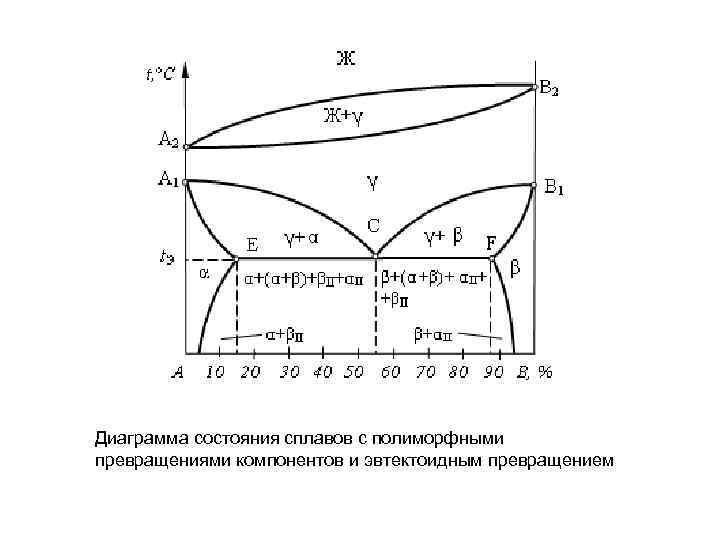 Диаграмма состояния сплавов с полиморфными превращениями компонентов и эвтектоидным превращением
Диаграмма состояния сплавов с полиморфными превращениями компонентов и эвтектоидным превращением
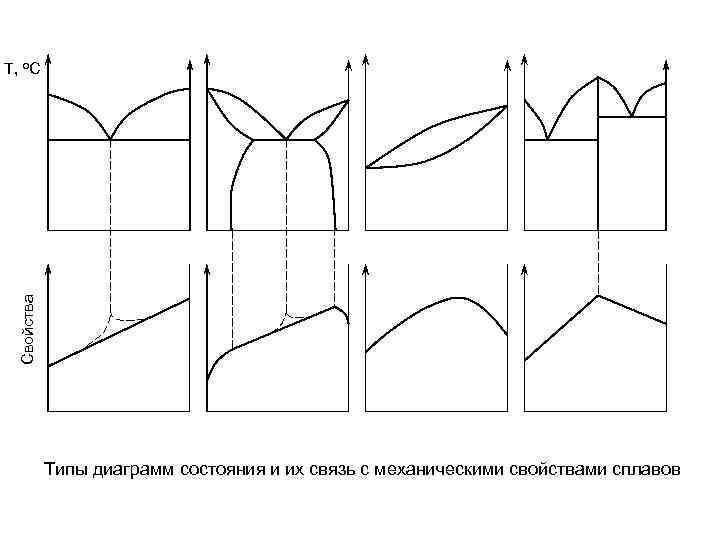 Свойства Т, о. С Типы диаграмм состояния и их связь с механическими свойствами сплавов
Свойства Т, о. С Типы диаграмм состояния и их связь с механическими свойствами сплавов
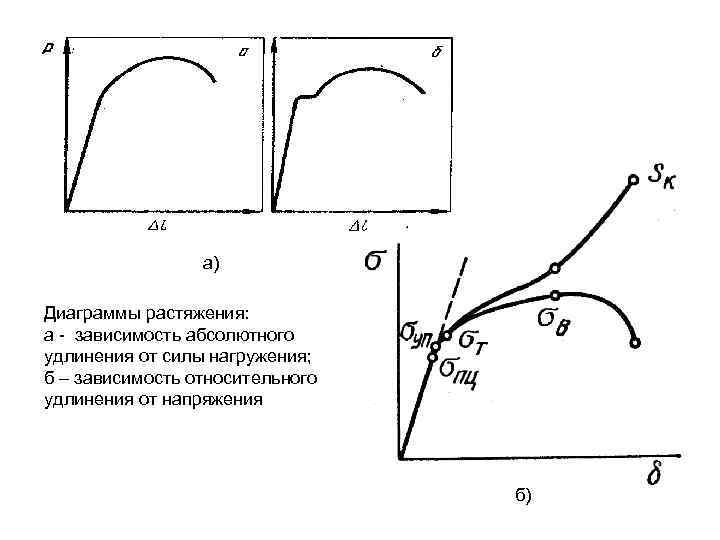 а) Диаграммы растяжения: а зависимость абсолютного удлинения от силы нагружения; б – зависимость относительного удлинения от напряжения б)
а) Диаграммы растяжения: а зависимость абсолютного удлинения от силы нагружения; б – зависимость относительного удлинения от напряжения б)
 Дислокационный механизм образования трещины
Дислокационный механизм образования трещины
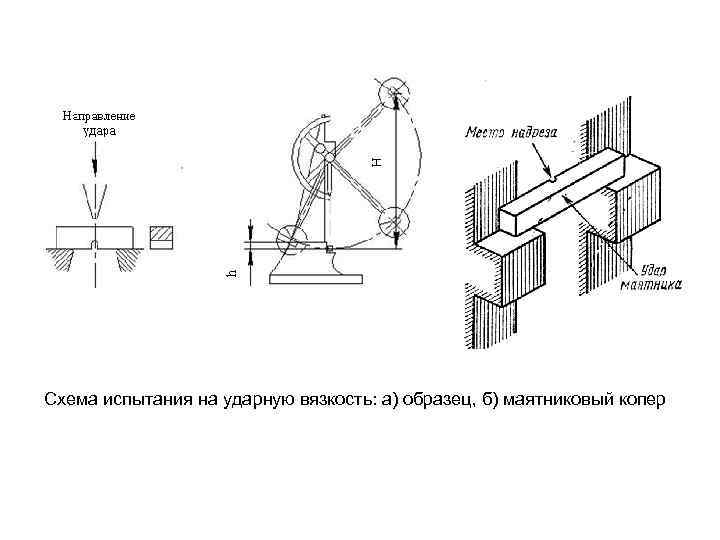 Схема испытания на ударную вязкость: а) образец, б) маятниковый копер
Схема испытания на ударную вязкость: а) образец, б) маятниковый копер
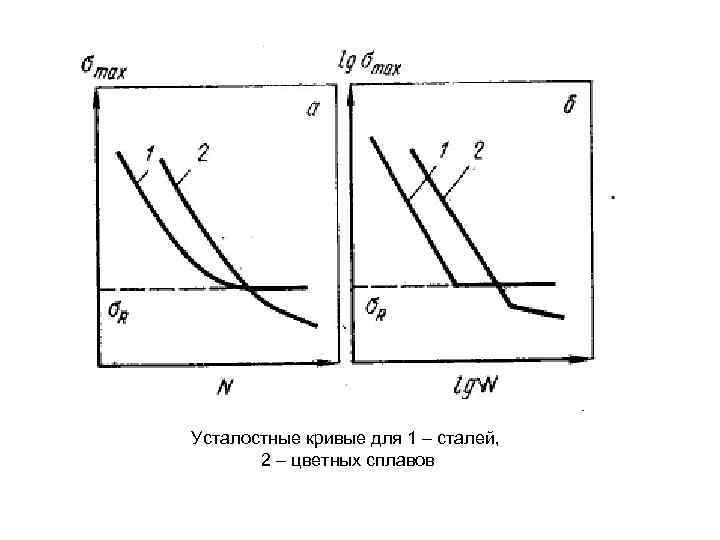 Усталостные кривые для 1 – сталей, 2 – цветных сплавов
Усталостные кривые для 1 – сталей, 2 – цветных сплавов
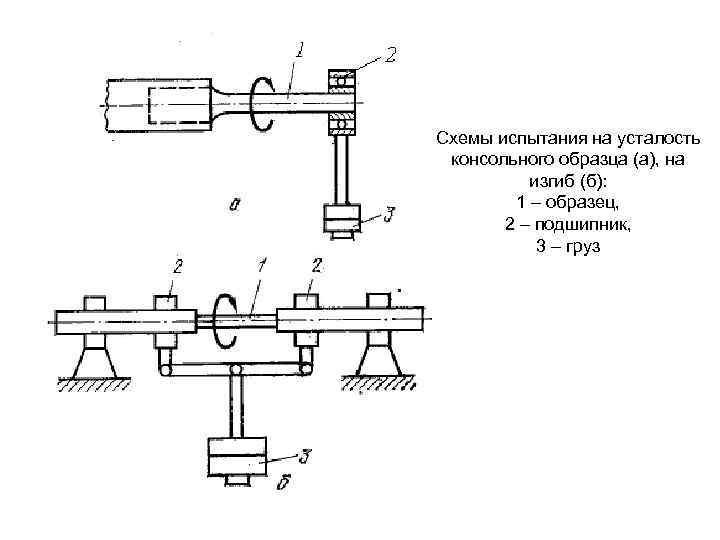 Схемы испытания на усталость консольного образца (а), на изгиб (б): 1 – образец, 2 – подшипник, 3 – груз
Схемы испытания на усталость консольного образца (а), на изгиб (б): 1 – образец, 2 – подшипник, 3 – груз
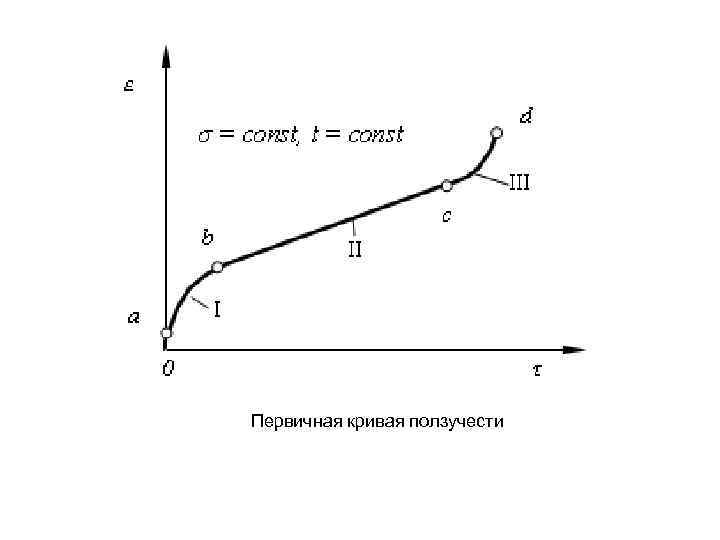 Первичная кривая ползучести
Первичная кривая ползучести
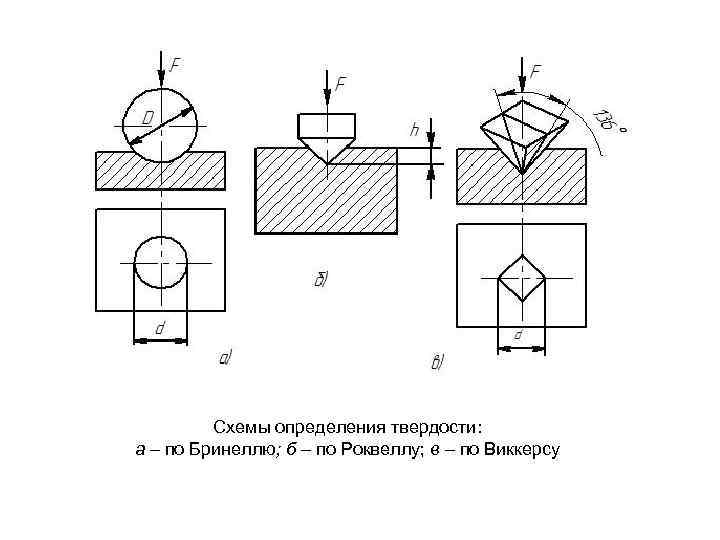 Схемы определения твердости: а – по Бринеллю; б – по Роквеллу; в – по Виккерсу
Схемы определения твердости: а – по Бринеллю; б – по Роквеллу; в – по Виккерсу
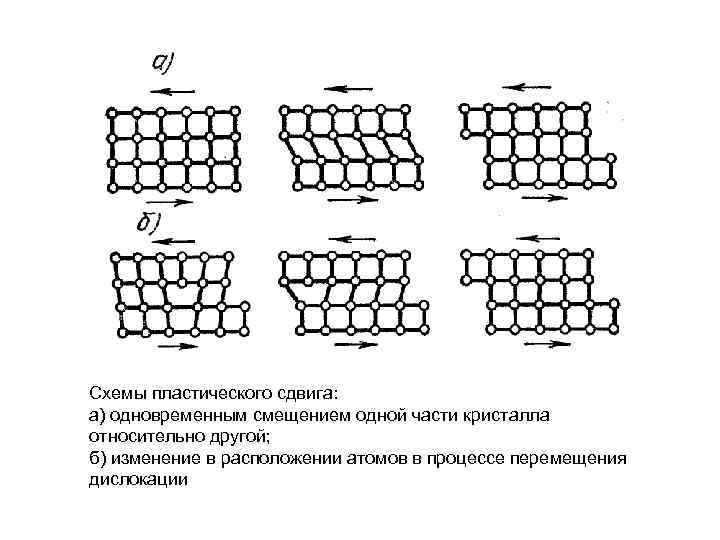 Схемы пластического сдвига: а) одновременным смещением одной части кристалла относительно другой; б) изменение в расположении атомов в процессе перемещения дислокации
Схемы пластического сдвига: а) одновременным смещением одной части кристалла относительно другой; б) изменение в расположении атомов в процессе перемещения дислокации
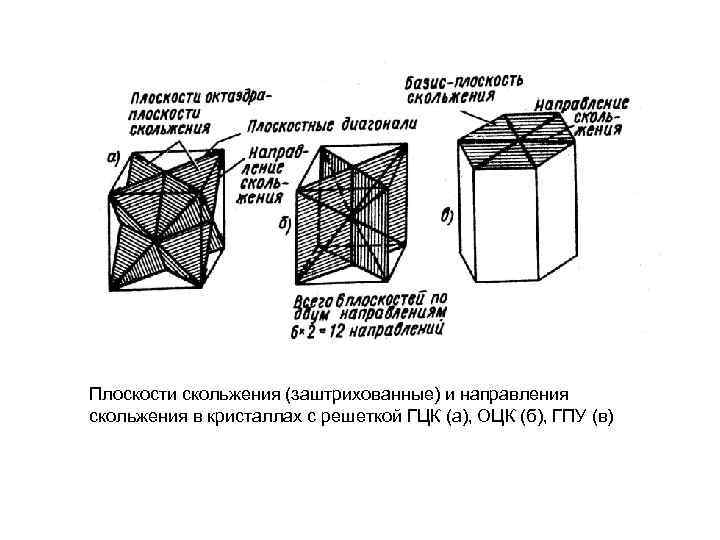 Плоскости скольжения (заштрихованные) и направления скольжения в кристаллах с решеткой ГЦК (а), ОЦК (б), ГПУ (в)
Плоскости скольжения (заштрихованные) и направления скольжения в кристаллах с решеткой ГЦК (а), ОЦК (б), ГПУ (в)
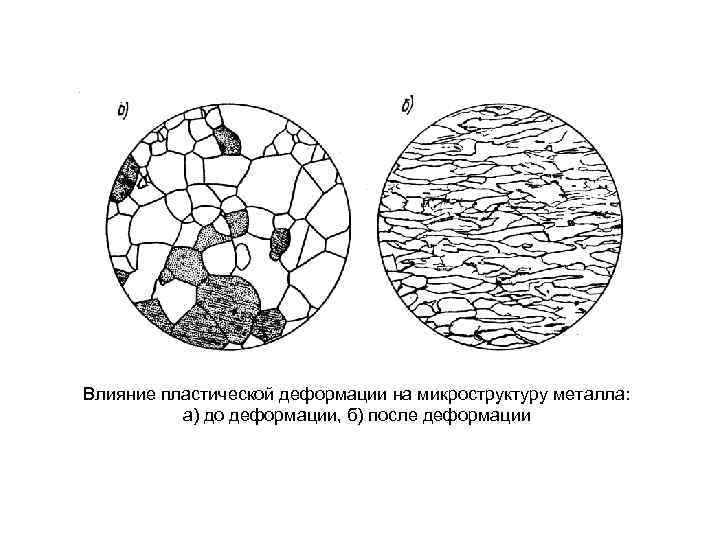 Влияние пластической деформации на микроструктуру металла: а) до деформации, б) после деформации
Влияние пластической деформации на микроструктуру металла: а) до деформации, б) после деформации
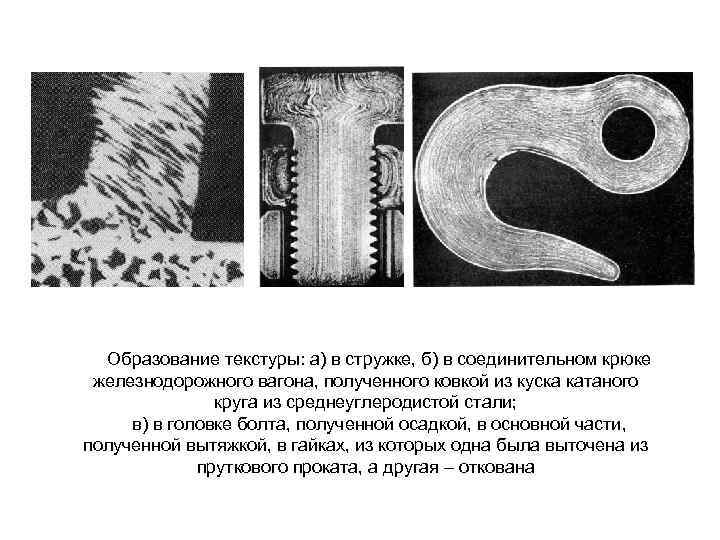 Образование текстуры: а) в стружке, б) в соединительном крюке железнодорожного вагона, полученного ковкой из куска катаного круга из среднеуглеродистой стали; в) в головке болта, полученной осадкой, в основной части, полученной вытяжкой, в гайках, из которых одна была выточена из пруткового проката, а другая – откована
Образование текстуры: а) в стружке, б) в соединительном крюке железнодорожного вагона, полученного ковкой из куска катаного круга из среднеуглеродистой стали; в) в головке болта, полученной осадкой, в основной части, полученной вытяжкой, в гайках, из которых одна была выточена из пруткового проката, а другая – откована
 а) зарождение новых мелких недеформированных зерен в) вторичная рекристаллизация Рекристаллизация холоднодеформированной стали б) конец первичной рекристаллизации
а) зарождение новых мелких недеформированных зерен в) вторичная рекристаллизация Рекристаллизация холоднодеформированной стали б) конец первичной рекристаллизации
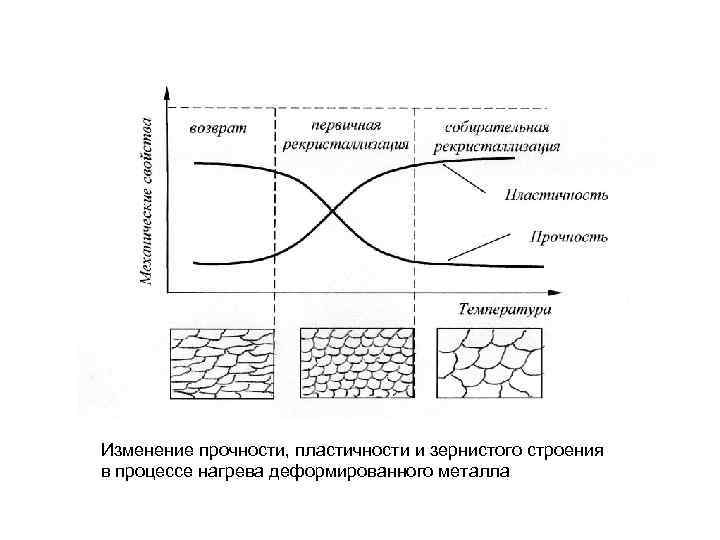 Изменение прочности, пластичности и зернистого строения в процессе нагрева деформированного металла
Изменение прочности, пластичности и зернистого строения в процессе нагрева деформированного металла
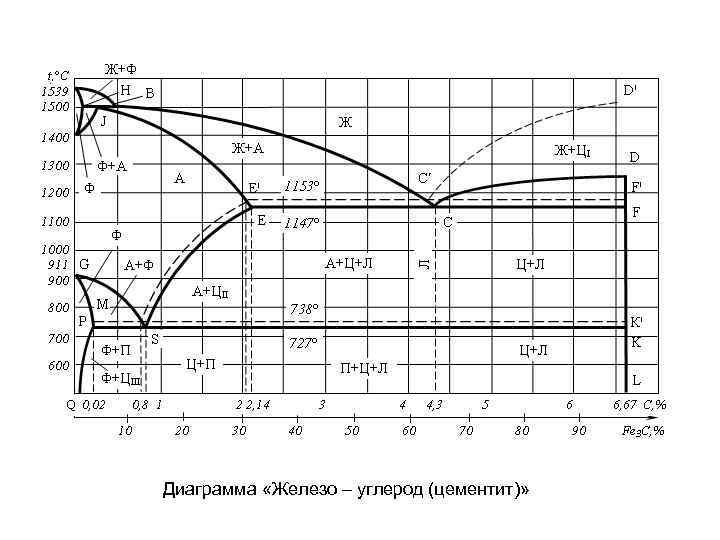 Диаграмма «Железо – углерод (цементит)»
Диаграмма «Железо – углерод (цементит)»
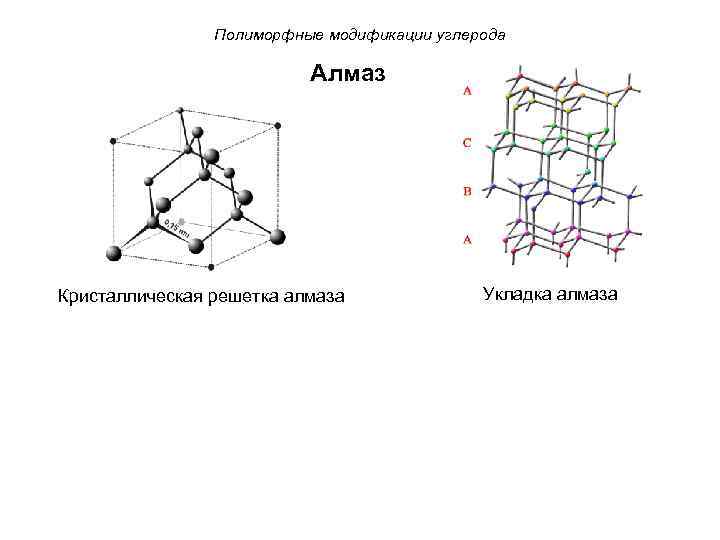 Полиморфные модификации углерода Алмаз Кристаллическая решетка алмаза Укладка алмаза
Полиморфные модификации углерода Алмаз Кристаллическая решетка алмаза Укладка алмаза
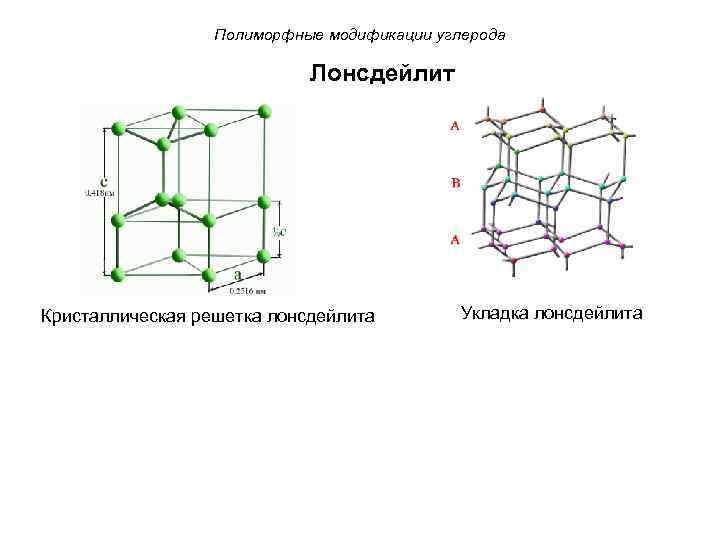 Полиморфные модификации углерода Лонсдейлит Кристаллическая решетка лонсдейлита Укладка лонсдейлита
Полиморфные модификации углерода Лонсдейлит Кристаллическая решетка лонсдейлита Укладка лонсдейлита
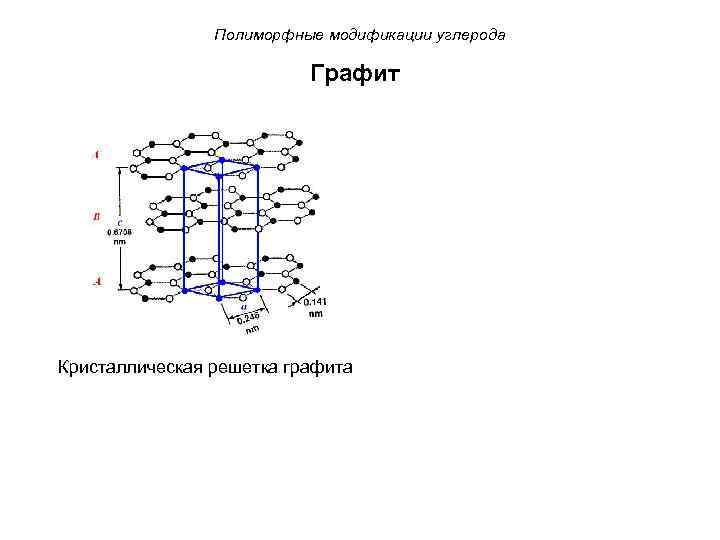 Полиморфные модификации углерода Графит Кристаллическая решетка графита
Полиморфные модификации углерода Графит Кристаллическая решетка графита
 Полиморфные модификации углерода Фуллерены Кристаллическая решетка фуллерена С 60
Полиморфные модификации углерода Фуллерены Кристаллическая решетка фуллерена С 60
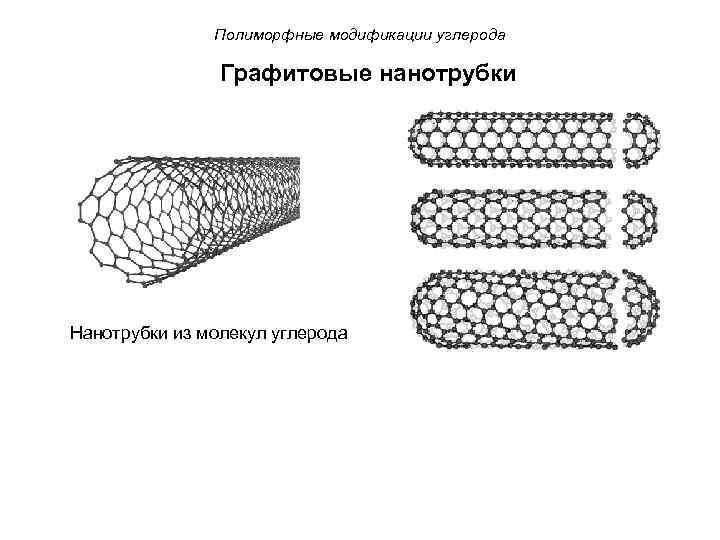 Полиморфные модификации углерода Графитовые нанотрубки Нанотрубки из молекул углерода
Полиморфные модификации углерода Графитовые нанотрубки Нанотрубки из молекул углерода
 Полиморфные модификации углерода Карбин – углеродный полимер с линейной структурой. В молекулу карбина входит до 2000 атомов. Длина полимерных Нитей колеблется от 50 до 250 нм. Плотность 1900… 3200 кг/м 3. Химически инертен, обладает полупроводниковыми свойствами. При облучении светом его проводимость резко возрастает.
Полиморфные модификации углерода Карбин – углеродный полимер с линейной структурой. В молекулу карбина входит до 2000 атомов. Длина полимерных Нитей колеблется от 50 до 250 нм. Плотность 1900… 3200 кг/м 3. Химически инертен, обладает полупроводниковыми свойствами. При облучении светом его проводимость резко возрастает.
 Полиморфные модификации углерода Стекловидный углерод
Полиморфные модификации углерода Стекловидный углерод
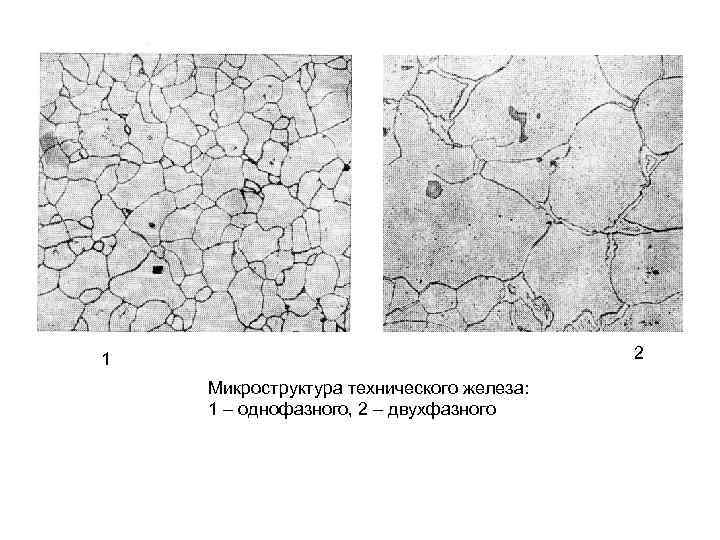 2 1 Микроструктура технического железа: 1 – однофазного, 2 – двухфазного
2 1 Микроструктура технического железа: 1 – однофазного, 2 – двухфазного
 а) б) Микроструктура доэвтектоидной стали: а) сталь 25; б) сталь 45
а) б) Микроструктура доэвтектоидной стали: а) сталь 25; б) сталь 45
 Микроструктура аустенита
Микроструктура аустенита
 а) Микроструктура эвтектоидной (а) и заэвтектоидной (б) стали б)
а) Микроструктура эвтектоидной (а) и заэвтектоидной (б) стали б)
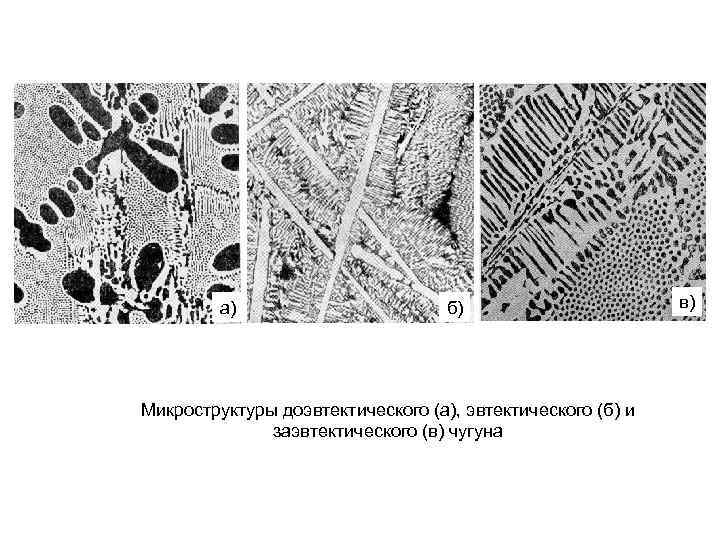 а) б) Микроструктуры доэвтектического (а), эвтектического (б) и заэвтектического (в) чугуна в)
а) б) Микроструктуры доэвтектического (а), эвтектического (б) и заэвтектического (в) чугуна в)
 Расшифруйте следующие марки стали: 12 Х 2 НВФА, 14 Г 2, 10 ХСНД, 18 Г 2 С, 15, 20 Х, 15 ХФ, 20 Х 2 Н 4 А, 20 ХГНР, сталь 2 кп, 40 ХН 2 МА, 35, 70 С 2 ХАБ, А 12, А 40 Г, сталь 4 сп, 20 Х 12 ВНМФ, 40 Х 15 Н 7 Г 7 Ф 2 МС, У 12, У 10 А, ХВСГ
Расшифруйте следующие марки стали: 12 Х 2 НВФА, 14 Г 2, 10 ХСНД, 18 Г 2 С, 15, 20 Х, 15 ХФ, 20 Х 2 Н 4 А, 20 ХГНР, сталь 2 кп, 40 ХН 2 МА, 35, 70 С 2 ХАБ, А 12, А 40 Г, сталь 4 сп, 20 Х 12 ВНМФ, 40 Х 15 Н 7 Г 7 Ф 2 МС, У 12, У 10 А, ХВСГ
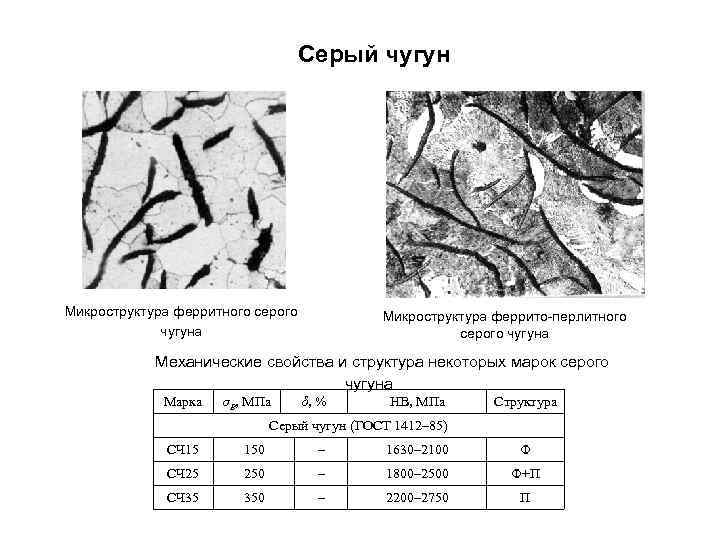 Серый чугун Микроструктура ферритного серого чугуна Микроструктура феррито перлитного серого чугуна Механические свойства и структура некоторых марок серого чугуна Марка σВ, МПа δ, % НВ, МПа Структура Серый чугун (ГОСТ 1412– 85) СЧ 15 150 – 1630– 2100 Ф СЧ 25 250 – 1800– 2500 Ф+П СЧ 35 350 – 2200– 2750 П
Серый чугун Микроструктура ферритного серого чугуна Микроструктура феррито перлитного серого чугуна Механические свойства и структура некоторых марок серого чугуна Марка σВ, МПа δ, % НВ, МПа Структура Серый чугун (ГОСТ 1412– 85) СЧ 15 150 – 1630– 2100 Ф СЧ 25 250 – 1800– 2500 Ф+П СЧ 35 350 – 2200– 2750 П
 Высокопрочный чугун Микроструктура феррито перлитного высокопрочного чугуна Микроструктура ферритного высокопрочного чугуна Механические свойства и структура некоторых марок высокопрочного чугуна Марка σв, МПа δ, % НВ, МПа Структура Высокопрочный чугун (ГОСТ 7293– 85) ВЧ 35 350 22 1400– 1700 Ф ВЧ 45 450 10 1400– 2250 Ф+П ВЧ 60 600 3 1920– 2270 Ф+П ВЧ 80 800 2 2480– 3510 П
Высокопрочный чугун Микроструктура феррито перлитного высокопрочного чугуна Микроструктура ферритного высокопрочного чугуна Механические свойства и структура некоторых марок высокопрочного чугуна Марка σв, МПа δ, % НВ, МПа Структура Высокопрочный чугун (ГОСТ 7293– 85) ВЧ 35 350 22 1400– 1700 Ф ВЧ 45 450 10 1400– 2250 Ф+П ВЧ 60 600 3 1920– 2270 Ф+П ВЧ 80 800 2 2480– 3510 П
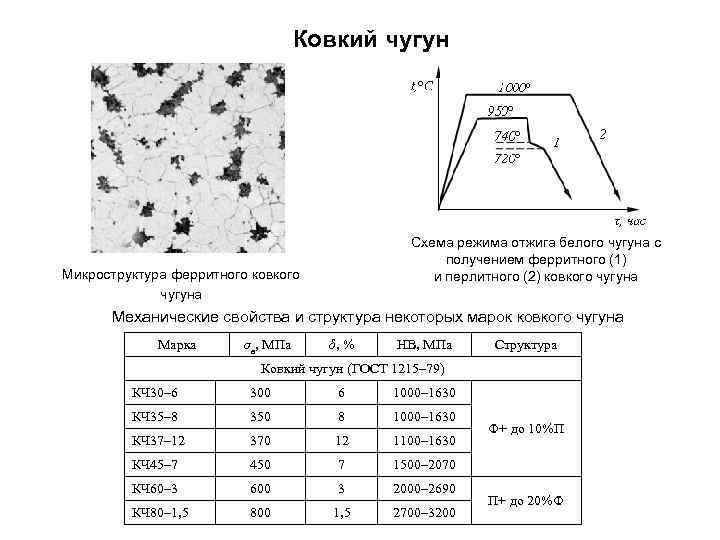 Ковкий чугун Схема режима отжига белого чугуна с получением ферритного (1) и перлитного (2) ковкого чугуна Микроструктура ферритного ковкого чугуна Механические свойства и структура некоторых марок ковкого чугуна Марка σв, МПа δ, % НВ, МПа Структура Ковкий чугун (ГОСТ 1215– 79) КЧ 30– 6 300 6 1000– 1630 КЧ 35– 8 350 8 1000– 1630 КЧ 37– 12 370 12 1100– 1630 КЧ 45– 7 450 7 1500– 2070 КЧ 60– 3 600 3 2000– 2690 КЧ 80– 1, 5 800 1, 5 2700– 3200 Ф+ до 10%П П+ до 20%Ф
Ковкий чугун Схема режима отжига белого чугуна с получением ферритного (1) и перлитного (2) ковкого чугуна Микроструктура ферритного ковкого чугуна Механические свойства и структура некоторых марок ковкого чугуна Марка σв, МПа δ, % НВ, МПа Структура Ковкий чугун (ГОСТ 1215– 79) КЧ 30– 6 300 6 1000– 1630 КЧ 35– 8 350 8 1000– 1630 КЧ 37– 12 370 12 1100– 1630 КЧ 45– 7 450 7 1500– 2070 КЧ 60– 3 600 3 2000– 2690 КЧ 80– 1, 5 800 1, 5 2700– 3200 Ф+ до 10%П П+ до 20%Ф
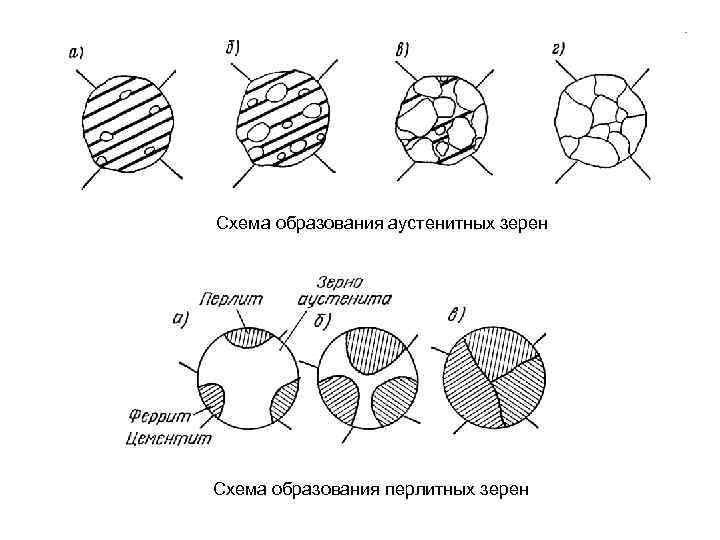 Схема образования аустенитных зерен Схема образования перлитных зерен
Схема образования аустенитных зерен Схема образования перлитных зерен
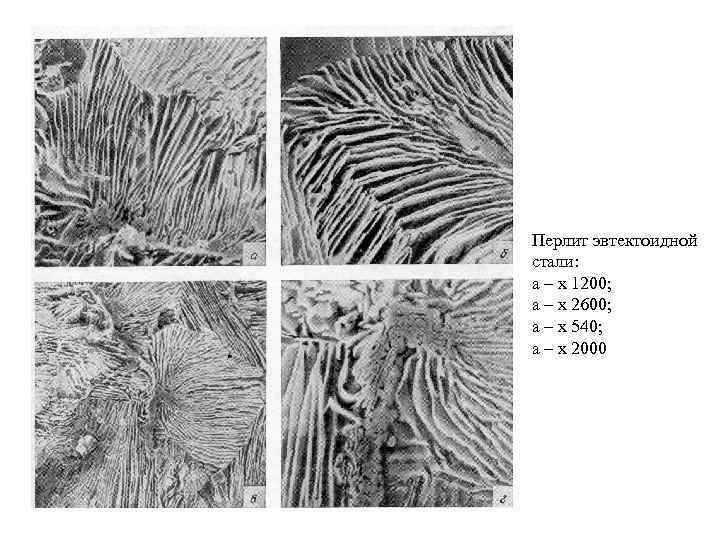 Перлит эвтектоидной стали: а – х 1200; а – х 2600; а – х 540; а – х 2000
Перлит эвтектоидной стали: а – х 1200; а – х 2600; а – х 540; а – х 2000
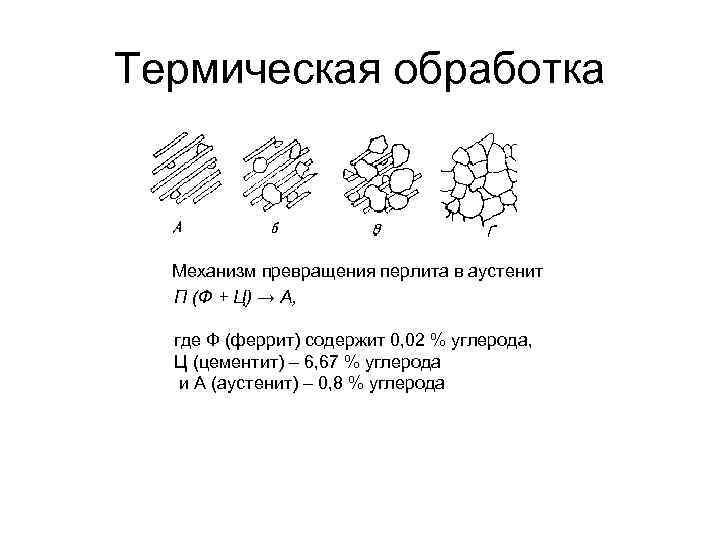 Термическая обработка Механизм превращения перлита в аустенит П (Ф + Ц) → А, где Ф (феррит) содержит 0, 02 % углерода, Ц (цементит) – 6, 67 % углерода и А (аустенит) – 0, 8 % углерода
Термическая обработка Механизм превращения перлита в аустенит П (Ф + Ц) → А, где Ф (феррит) содержит 0, 02 % углерода, Ц (цементит) – 6, 67 % углерода и А (аустенит) – 0, 8 % углерода
 а) б) Фотография (а) и схема (б) микроструктуры Видманштетта
а) б) Фотография (а) и схема (б) микроструктуры Видманштетта
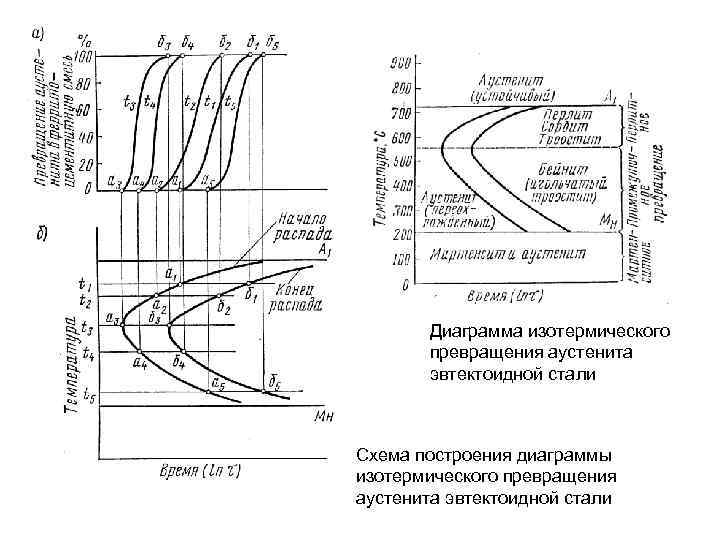 Диаграмма изотермического превращения аустенита эвтектоидной стали Схема построения диаграммы изотермического превращения аустенита эвтектоидной стали
Диаграмма изотермического превращения аустенита эвтектоидной стали Схема построения диаграммы изотермического превращения аустенита эвтектоидной стали
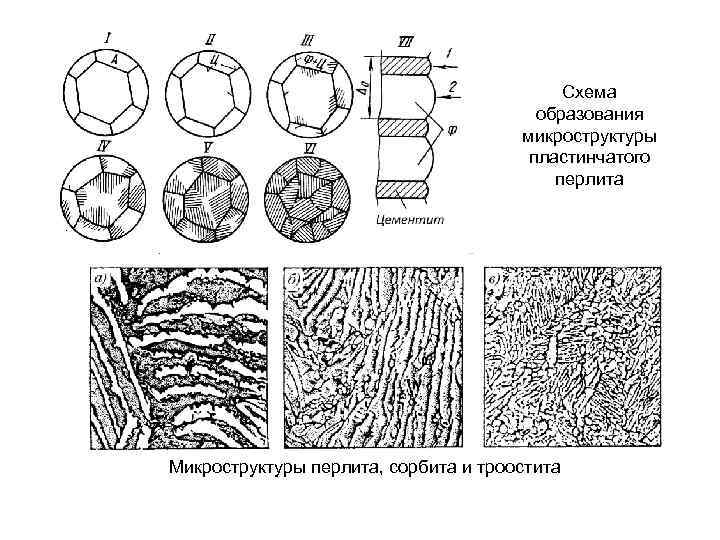 Схема образования микроструктуры пластинчатого перлита Микроструктуры перлита, сорбита и троостита
Схема образования микроструктуры пластинчатого перлита Микроструктуры перлита, сорбита и троостита
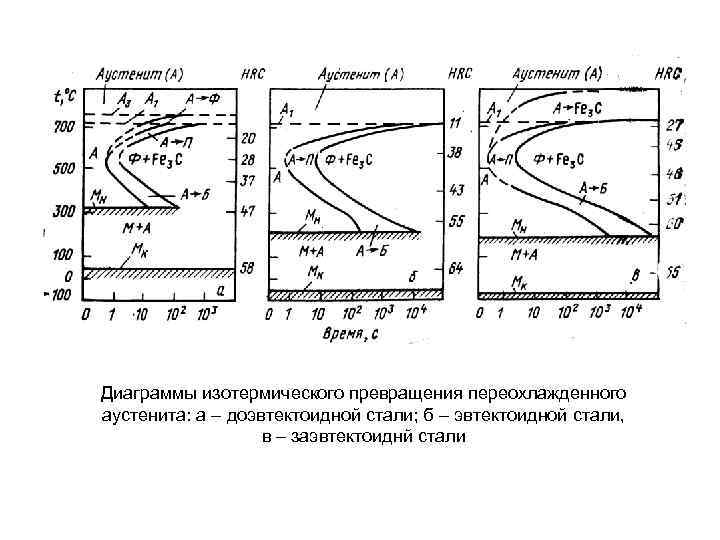 Диаграммы изотермического превращения переохлажденного аустенита: а – доэвтектоидной стали; б – эвтектоидной стали, в – заэвтектоиднй стали
Диаграммы изотермического превращения переохлажденного аустенита: а – доэвтектоидной стали; б – эвтектоидной стали, в – заэвтектоиднй стали
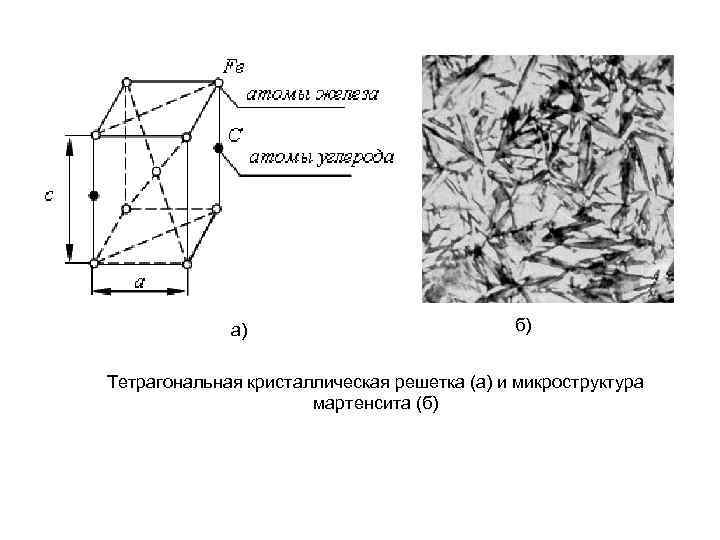 а) б) Тетрагональная кристаллическая решетка (а) и микроструктура мартенсита (б)
а) б) Тетрагональная кристаллическая решетка (а) и микроструктура мартенсита (б)
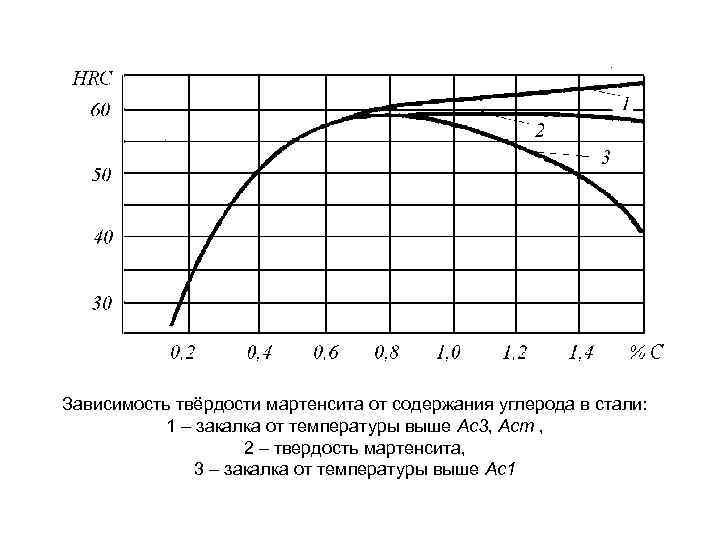 Зависимость твёрдости мартенсита от содержания углерода в стали: 1 – закалка от температуры выше Ас3, Аст , 2 – твердость мартенсита, 3 – закалка от температуры выше Ас1
Зависимость твёрдости мартенсита от содержания углерода в стали: 1 – закалка от температуры выше Ас3, Аст , 2 – твердость мартенсита, 3 – закалка от температуры выше Ас1
 Электронные микроструктуры бейнита (х15000): а) верхнего, б) нижнего
Электронные микроструктуры бейнита (х15000): а) верхнего, б) нижнего
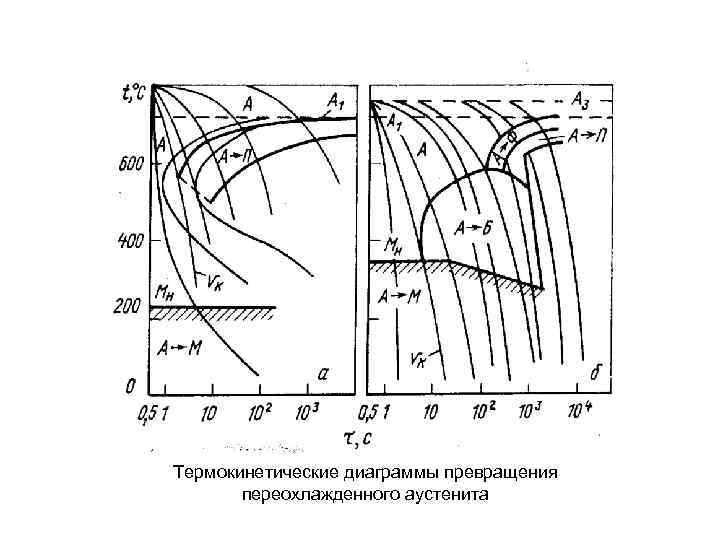 Термокинетические диаграммы превращения переохлажденного аустенита
Термокинетические диаграммы превращения переохлажденного аустенита
 Наложение кривых охлаждения на диаграмму изотермического распада аустенита
Наложение кривых охлаждения на диаграмму изотермического распада аустенита
 . Структура медно никелевого сплава а) литого, б) после диффузионного отжига
. Структура медно никелевого сплава а) литого, б) после диффузионного отжига
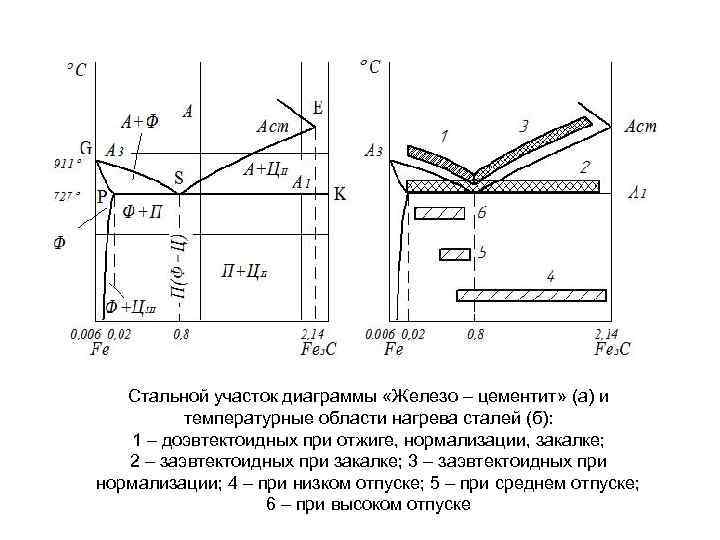 Стальной участок диаграммы «Железо – цементит» (а) и температурные области нагрева сталей (б): 1 – доэвтектоидных при отжиге, нормализации, закалке; 2 – заэвтектоидных при закалке; 3 – заэвтектоидных при нормализации; 4 – при низком отпуске; 5 – при среднем отпуске; 6 – при высоком отпуске
Стальной участок диаграммы «Железо – цементит» (а) и температурные области нагрева сталей (б): 1 – доэвтектоидных при отжиге, нормализации, закалке; 2 – заэвтектоидных при закалке; 3 – заэвтектоидных при нормализации; 4 – при низком отпуске; 5 – при среднем отпуске; 6 – при высоком отпуске
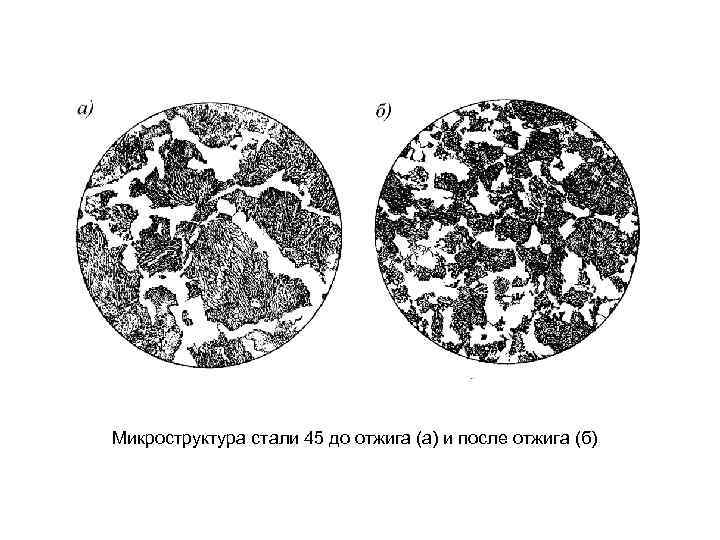 Микроструктура стали 45 до отжига (а) и после отжига (б)
Микроструктура стали 45 до отжига (а) и после отжига (б)
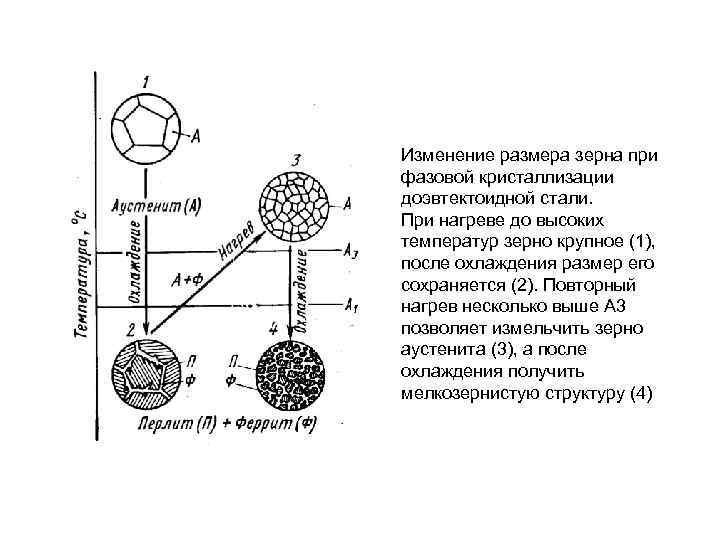 Изменение размера зерна при фазовой кристаллизации доэвтектоидной стали. При нагреве до высоких температур зерно крупное (1), после охлаждения размер его сохраняется (2). Повторный нагрев несколько выше А 3 позволяет измельчить зерно аустенита (3), а после охлаждения получить мелкозернистую структуру (4)
Изменение размера зерна при фазовой кристаллизации доэвтектоидной стали. При нагреве до высоких температур зерно крупное (1), после охлаждения размер его сохраняется (2). Повторный нагрев несколько выше А 3 позволяет измельчить зерно аустенита (3), а после охлаждения получить мелкозернистую структуру (4)
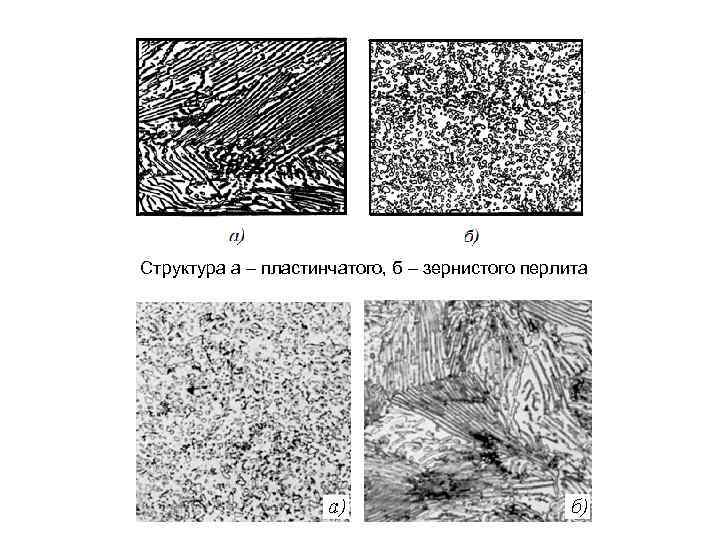 Структура а – пластинчатого, б – зернистого перлита
Структура а – пластинчатого, б – зернистого перлита
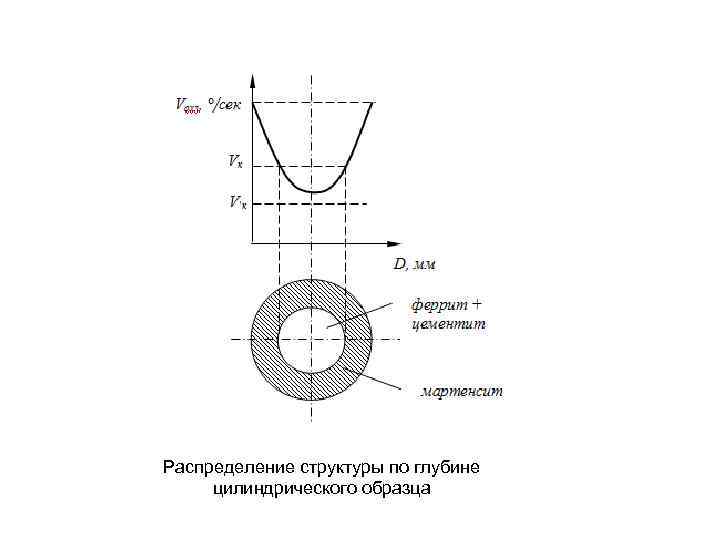 Распределение структуры по глубине цилиндрического образца
Распределение структуры по глубине цилиндрического образца
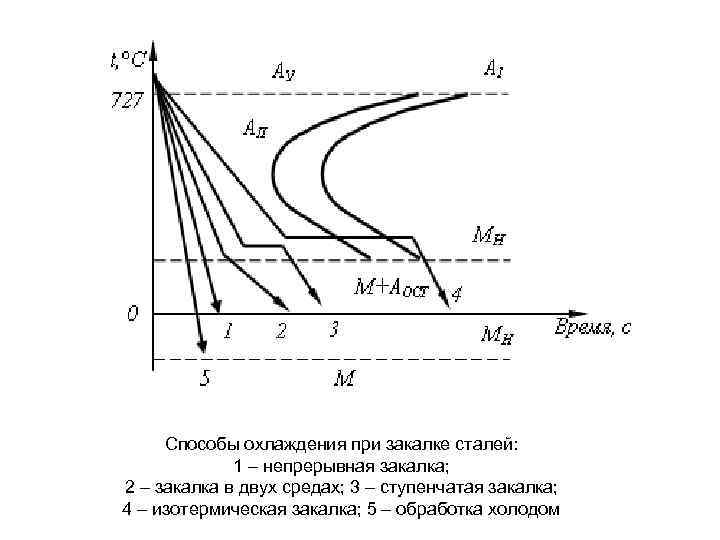 Способы охлаждения при закалке сталей: 1 – непрерывная закалка; 2 – закалка в двух средах; 3 – ступенчатая закалка; 4 – изотермическая закалка; 5 – обработка холодом
Способы охлаждения при закалке сталей: 1 – непрерывная закалка; 2 – закалка в двух средах; 3 – ступенчатая закалка; 4 – изотермическая закалка; 5 – обработка холодом
 Схемы структур стали У 8: а – мартенсит мелкоигольчатый; б – мартенсит крупноиголъчатый
Схемы структур стали У 8: а – мартенсит мелкоигольчатый; б – мартенсит крупноиголъчатый
 Диаграмма состояния сплава с переменной растворимостью компонента В в А
Диаграмма состояния сплава с переменной растворимостью компонента В в А
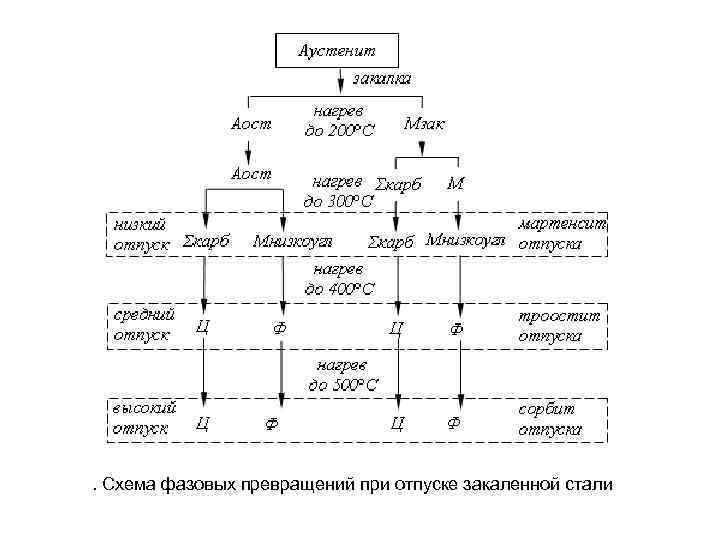 . Схема фазовых превращений при отпуске закаленной стали
. Схема фазовых превращений при отпуске закаленной стали
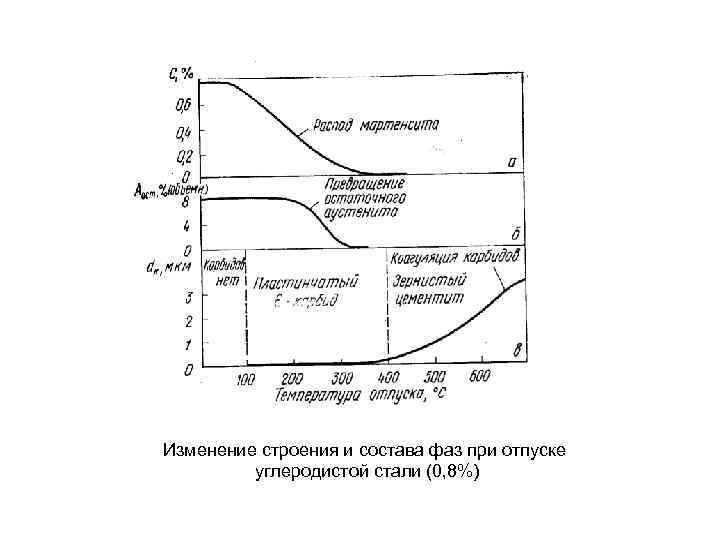 Изменение строения и состава фаз при отпуске углеродистой стали (0, 8%)
Изменение строения и состава фаз при отпуске углеродистой стали (0, 8%)
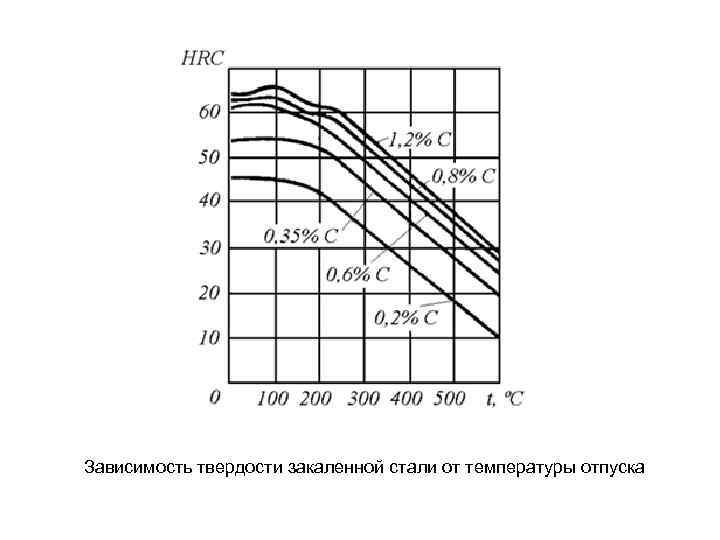 Зависимость твердости закаленной стали от температуры отпуска
Зависимость твердости закаленной стали от температуры отпуска
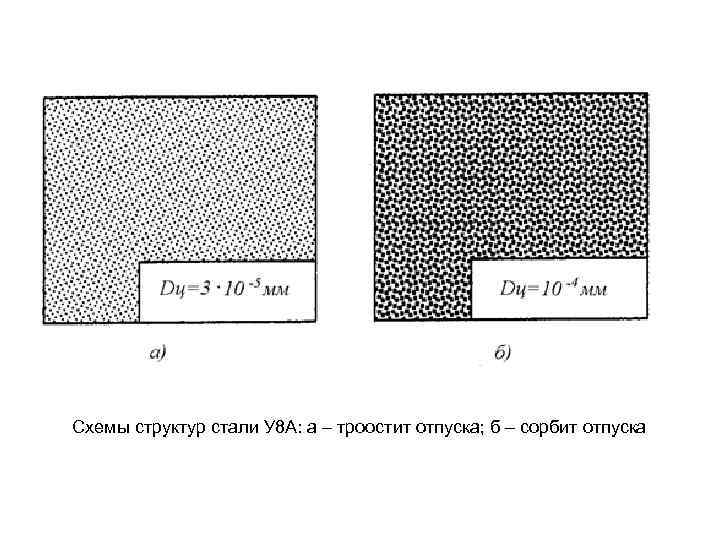 Схемы структур стали У 8 А: а – троостит отпуска; б – сорбит отпуска
Схемы структур стали У 8 А: а – троостит отпуска; б – сорбит отпуска
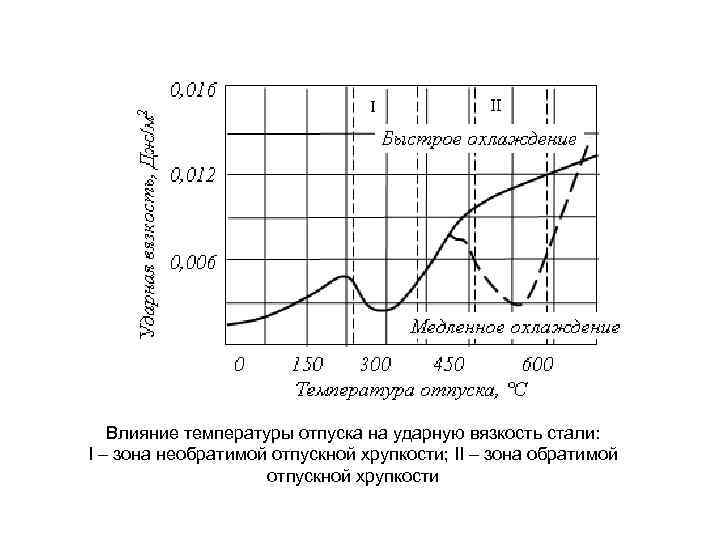 Влияние температуры отпуска на ударную вязкость стали: Ι – зона необратимой отпускной хрупкости; ΙΙ – зона обратимой отпускной хрупкости
Влияние температуры отпуска на ударную вязкость стали: Ι – зона необратимой отпускной хрупкости; ΙΙ – зона обратимой отпускной хрупкости
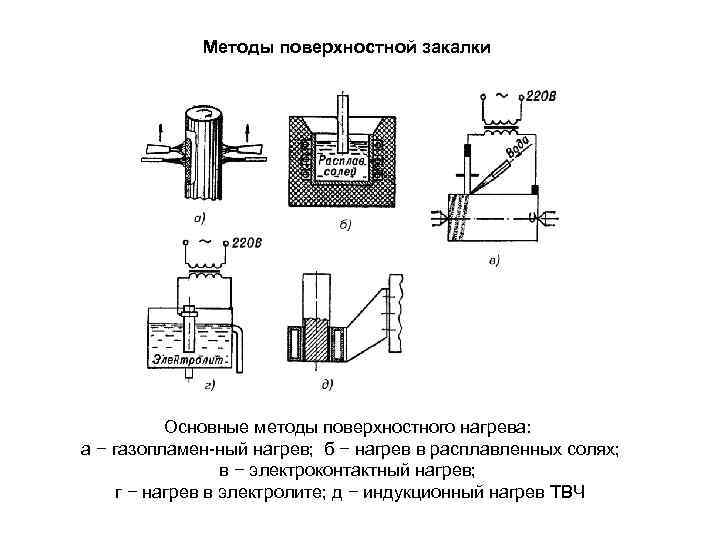 Методы поверхностной закалки Основные методы поверхностного нагрева: а − газопламен ный нагрев; б − нагрев в расплавленных солях; в − электроконтактный нагрев; г − нагрев в электролите; д − индукционный нагрев ТВЧ
Методы поверхностной закалки Основные методы поверхностного нагрева: а − газопламен ный нагрев; б − нагрев в расплавленных солях; в − электроконтактный нагрев; г − нагрев в электролите; д − индукционный нагрев ТВЧ
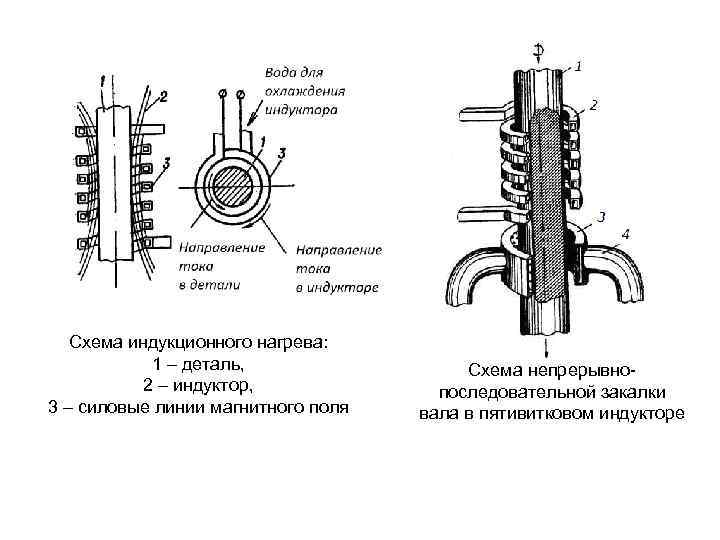 Схема индукционного нагрева: 1 – деталь, 2 – индуктор, 3 – силовые линии магнитного поля Схема непрерывно последовательной закалки вала в пятивитковом индукторе
Схема индукционного нагрева: 1 – деталь, 2 – индуктор, 3 – силовые линии магнитного поля Схема непрерывно последовательной закалки вала в пятивитковом индукторе
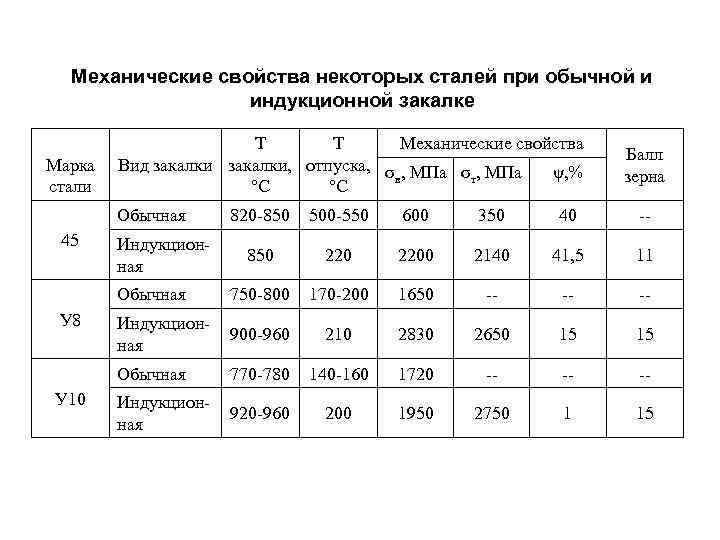 Механические свойства некоторых сталей при обычной и индукционной закалке Марка стали Т Т Механические свойства Вид закалки, отпуска, σ , МПа ψ, % в т °С °С Обычная Балл зерна У 10 600 350 40 -- 850 2200 2140 41, 5 11 750 -800 170 -200 1650 -- -- -- Индукционная 900 -960 210 2830 2650 15 15 Обычная У 8 500 -550 Обычная 45 820 -850 770 -780 140 -160 1720 -- -- -- Индукционная 920 -960 200 1950 2750 1 15 Индукционная
Механические свойства некоторых сталей при обычной и индукционной закалке Марка стали Т Т Механические свойства Вид закалки, отпуска, σ , МПа ψ, % в т °С °С Обычная Балл зерна У 10 600 350 40 -- 850 2200 2140 41, 5 11 750 -800 170 -200 1650 -- -- -- Индукционная 900 -960 210 2830 2650 15 15 Обычная У 8 500 -550 Обычная 45 820 -850 770 -780 140 -160 1720 -- -- -- Индукционная 920 -960 200 1950 2750 1 15 Индукционная
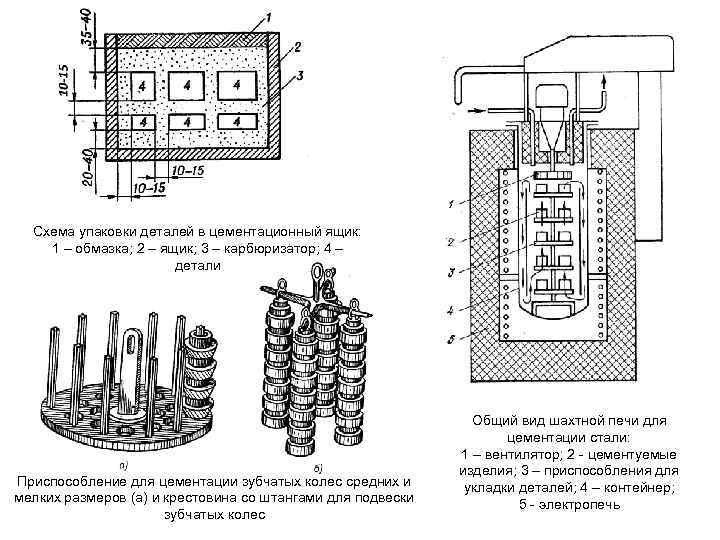 Схема упаковки деталей в цементационный ящик: 1 – обмазка; 2 – ящик; 3 – карбюризатор; 4 – детали Приспособление для цементации зубчатых колес средних и мелких размеров (а) и крестовина со штангами для подвески зубчатых колес Общий вид шахтной печи для цементации стали: 1 – вентилятор; 2 цементуемые изделия; 3 – приспособления для укладки деталей; 4 – контейнер; 5 электропечь
Схема упаковки деталей в цементационный ящик: 1 – обмазка; 2 – ящик; 3 – карбюризатор; 4 – детали Приспособление для цементации зубчатых колес средних и мелких размеров (а) и крестовина со штангами для подвески зубчатых колес Общий вид шахтной печи для цементации стали: 1 – вентилятор; 2 цементуемые изделия; 3 – приспособления для укладки деталей; 4 – контейнер; 5 электропечь
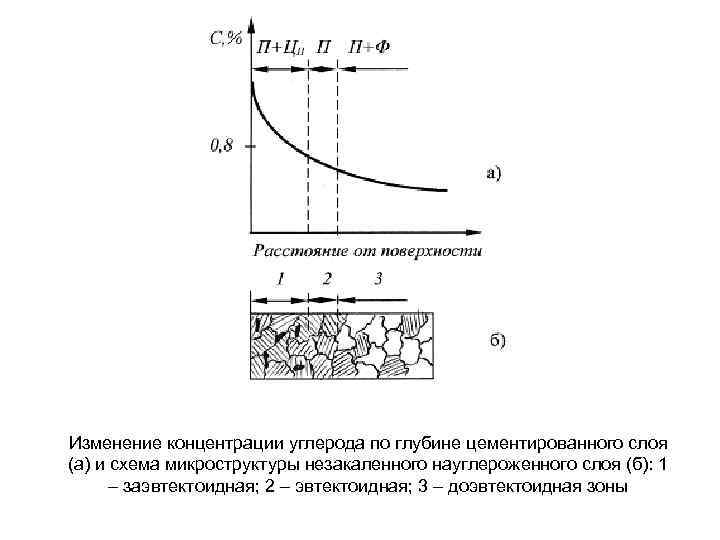 Изменение концентрации углерода по глубине цементированного слоя (а) и схема микроструктуры незакаленного науглероженного слоя (б): 1 – заэвтектоидная; 2 – эвтектоидная; 3 – доэвтектоидная зоны
Изменение концентрации углерода по глубине цементированного слоя (а) и схема микроструктуры незакаленного науглероженного слоя (б): 1 – заэвтектоидная; 2 – эвтектоидная; 3 – доэвтектоидная зоны
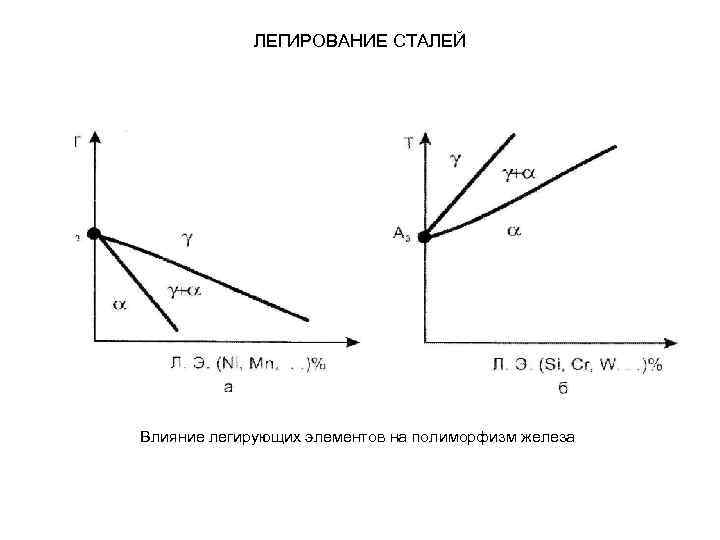 ЛЕГИРОВАНИЕ СТАЛЕЙ Влияние легирующих элементов на полиморфизм железа
ЛЕГИРОВАНИЕ СТАЛЕЙ Влияние легирующих элементов на полиморфизм железа
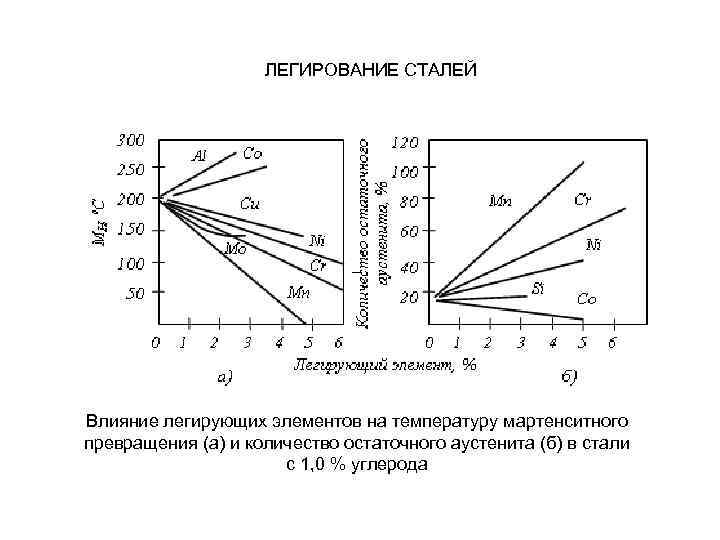 ЛЕГИРОВАНИЕ СТАЛЕЙ – Влияние легирующих элементов на температуру мартенситного превращения (а) и количество остаточного аустенита (б) в стали с 1, 0 % углерода
ЛЕГИРОВАНИЕ СТАЛЕЙ – Влияние легирующих элементов на температуру мартенситного превращения (а) и количество остаточного аустенита (б) в стали с 1, 0 % углерода
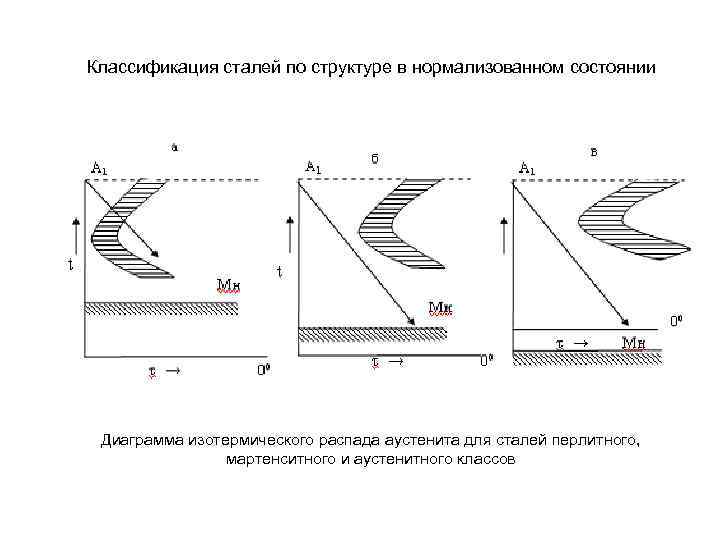 Классификация сталей по структуре в нормализованном состоянии Диаграмма изотермического распада аустенита для сталей перлитного, мартенситного и аустенитного классов
Классификация сталей по структуре в нормализованном состоянии Диаграмма изотермического распада аустенита для сталей перлитного, мартенситного и аустенитного классов
 Каждый легирующий элемент обозначается буквой: А – азот, Б – ниобий, В – вольфрам, Г – марганец, Д – медь, Е – селен, К –кобальт, Н – никель, М – молибден, П – фосфор, Р – бор, С – кремний, Т – титан, Ф – ванадий, Х – хром, Ц – цирконий, Ч – редкоземельные элементы, Ю – алюминий. 12 Х 2 НВФА, 14 Г 2, 10 ХСНД, 18 Г 2 С, 15, 20 Х, 15 ХФ, 20 Х 2 Н 4 А, 20 ХГНР, 40 ХН 2 МА, 35, 70 С 2 ХАБ ШХ 15, А 12, А 40 Г, 20 Х 12 ВНМФ, 40 Х 15 Н 7 Г 7 Ф 2 МС, У 12, У 10 А, ХВСГ
Каждый легирующий элемент обозначается буквой: А – азот, Б – ниобий, В – вольфрам, Г – марганец, Д – медь, Е – селен, К –кобальт, Н – никель, М – молибден, П – фосфор, Р – бор, С – кремний, Т – титан, Ф – ванадий, Х – хром, Ц – цирконий, Ч – редкоземельные элементы, Ю – алюминий. 12 Х 2 НВФА, 14 Г 2, 10 ХСНД, 18 Г 2 С, 15, 20 Х, 15 ХФ, 20 Х 2 Н 4 А, 20 ХГНР, 40 ХН 2 МА, 35, 70 С 2 ХАБ ШХ 15, А 12, А 40 Г, 20 Х 12 ВНМФ, 40 Х 15 Н 7 Г 7 Ф 2 МС, У 12, У 10 А, ХВСГ
 Инструментальные стали б) а) Сталь Х для режущего инструмента (х1000): а) зернистый перлит после отжига, б) отпущенный мартенсит после закалки и отпуска
Инструментальные стали б) а) Сталь Х для режущего инструмента (х1000): а) зернистый перлит после отжига, б) отпущенный мартенсит после закалки и отпуска
 а) б) Быстрорежущая сталь Р 18 (х1000): а) литая, б) прокатанная и отожженная
а) б) Быстрорежущая сталь Р 18 (х1000): а) литая, б) прокатанная и отожженная
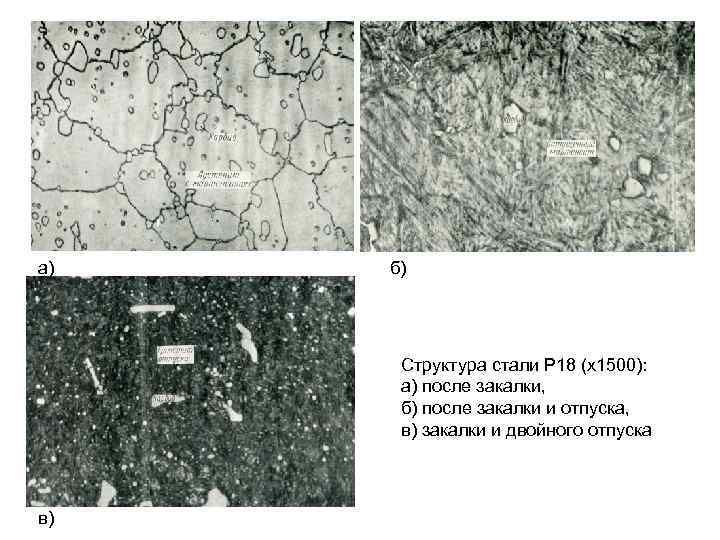 а) б) Структура стали Р 18 (х1500): а) после закалки, б) после закалки и отпуска, в) закалки и двойного отпуска в)
а) б) Структура стали Р 18 (х1500): а) после закалки, б) после закалки и отпуска, в) закалки и двойного отпуска в)
 а) б) Структура твердых сплавов а) мелкозернистого ВК 15, б) крупнозернистого ВК 15, в) Т 15 К 6)
а) б) Структура твердых сплавов а) мелкозернистого ВК 15, б) крупнозернистого ВК 15, в) Т 15 К 6)
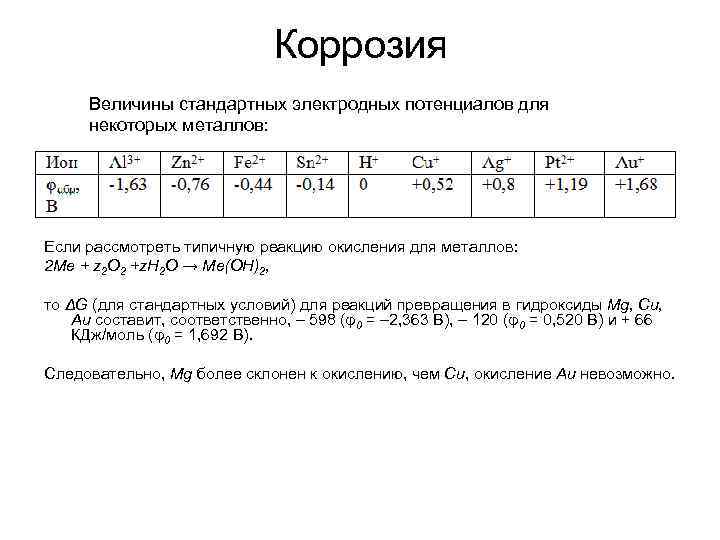 Коррозия Величины стандартных электродных потенциалов для некоторых металлов: Если рассмотреть типичную реакцию окисления для металлов: 2 Ме + z 2 O 2 +z. Н 2 O → Ме(OН)2, то ΔG (для стандартных условий) для реакций превращения в гидроксиды Мg, Cu, Аu составит, соответственно, – 598 (φ0 = – 2, 363 В), – 120 (φ0 = 0, 520 В) и + 66 КДж/моль (φ0 = 1, 692 В). Следовательно, Мg более склонен к окислению, чем Сu, окисление Аu невозможно.
Коррозия Величины стандартных электродных потенциалов для некоторых металлов: Если рассмотреть типичную реакцию окисления для металлов: 2 Ме + z 2 O 2 +z. Н 2 O → Ме(OН)2, то ΔG (для стандартных условий) для реакций превращения в гидроксиды Мg, Cu, Аu составит, соответственно, – 598 (φ0 = – 2, 363 В), – 120 (φ0 = 0, 520 В) и + 66 КДж/моль (φ0 = 1, 692 В). Следовательно, Мg более склонен к окислению, чем Сu, окисление Аu невозможно.
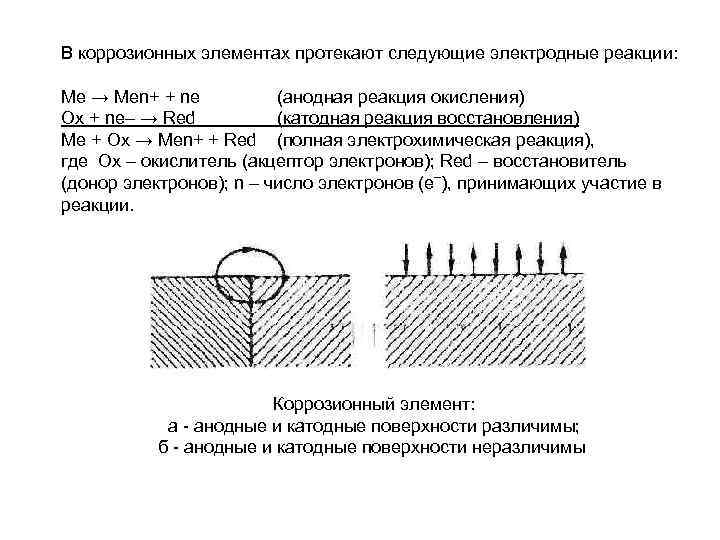 В коррозионных элементах протекают следующие электродные реакции: Ме → Меn+ + nе (анодная реакция окисления) Ох + ne– → Red (катодная реакция восстановления) Ме + Ох → Меn+ + Red (полная электрохимическая реакция), где Ох – окислитель (акцептор электронов); Red – восстановитель (донор электронов); n – число электронов (е–), принимающих участие в реакции. Коррозионный элемент: а анодные и катодные поверхности различимы; б анодные и катодные поверхности неразличимы
В коррозионных элементах протекают следующие электродные реакции: Ме → Меn+ + nе (анодная реакция окисления) Ох + ne– → Red (катодная реакция восстановления) Ме + Ох → Меn+ + Red (полная электрохимическая реакция), где Ох – окислитель (акцептор электронов); Red – восстановитель (донор электронов); n – число электронов (е–), принимающих участие в реакции. Коррозионный элемент: а анодные и катодные поверхности различимы; б анодные и катодные поверхности неразличимы
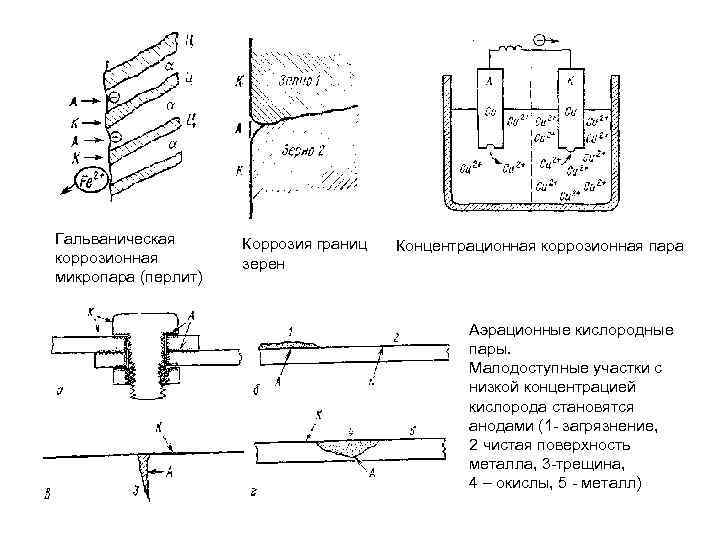 Гальваническая коррозионная микропара (перлит) Коррозия границ зерен Концентрационная коррозионная пара Аэрационные кислородные пары. Малодоступные участки с низкой концентрацией кислорода становятся анодами (1 загрязнение, 2 чистая поверхность металла, 3 трещина, 4 – окислы, 5 металл)
Гальваническая коррозионная микропара (перлит) Коррозия границ зерен Концентрационная коррозионная пара Аэрационные кислородные пары. Малодоступные участки с низкой концентрацией кислорода становятся анодами (1 загрязнение, 2 чистая поверхность металла, 3 трещина, 4 – окислы, 5 металл)
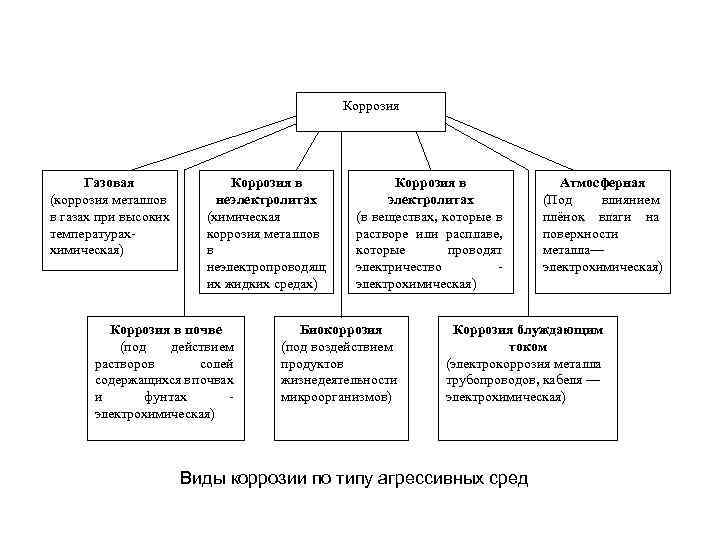 Коррозия Газовая (коррозия металлов в газах при высоких температураххимическая) Коррозия в неэлектролитах (химическая коррозия металлов в неэлектропроводящ их жидких средах) Коррозия в почве (под действием растворов солей содержащихся в почвах и фунтах электрохимическая) Коррозия в электролитах (в веществах, которые в растворе или расплаве, которые проводят электричество электрохимическая) Биокоррозия (под воздействием продуктов жизнедеятельности микроорганизмов) Атмосферная (Под влиянием плёнок влаги на поверхности металла— электрохимическая) Коррозия блуждающим током (электрокоррозия металла трубопроводов, кабеля — электрохимическая) Виды коррозии по типу агрессивных сред
Коррозия Газовая (коррозия металлов в газах при высоких температураххимическая) Коррозия в неэлектролитах (химическая коррозия металлов в неэлектропроводящ их жидких средах) Коррозия в почве (под действием растворов солей содержащихся в почвах и фунтах электрохимическая) Коррозия в электролитах (в веществах, которые в растворе или расплаве, которые проводят электричество электрохимическая) Биокоррозия (под воздействием продуктов жизнедеятельности микроорганизмов) Атмосферная (Под влиянием плёнок влаги на поверхности металла— электрохимическая) Коррозия блуждающим током (электрокоррозия металла трубопроводов, кабеля — электрохимическая) Виды коррозии по типу агрессивных сред
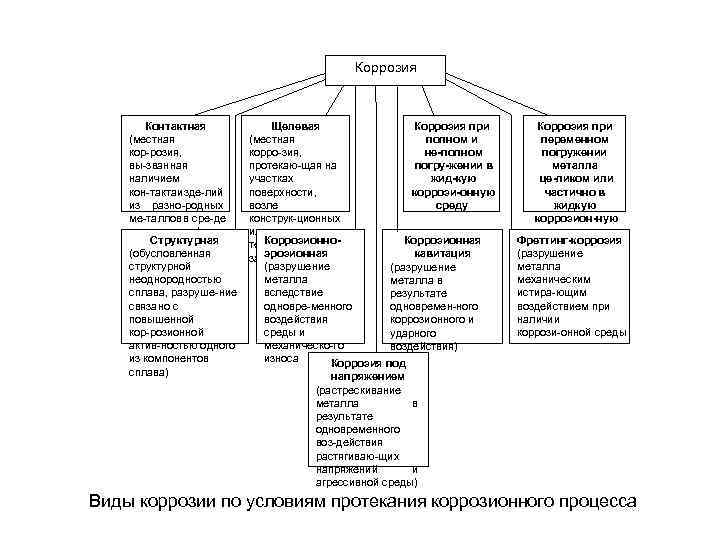 Коррозия Контактная (местная кор розия, вы званная наличием кон такта изде лий из разно родных ме талловв сре де электролите) Структурная (обусловленная структурной неоднородностью сплава, разруше ние связано с повышенной кор розионной актив ностью одного из компонентов сплава) Щелевая Коррозия при (местная полном и корро зия, не полном протекаю щая на погру жении в участках жид кую поверхности, коррози онную возле среду конструк ционных или Коррозионно Коррозионная технологических эрозионная кавитация зазоров) (разрушение металла в вследствие результате одновре менного одновремен ного воздействия коррозионного и среды и ударного механическо го воздействия) износа Коррозия под Коррозия при переменном погружении металла це ликом или частично в жидкую коррозион ную среду Фреттинг коррозия (разрушение металла механическим истира ющим воздействием при наличии коррози онной среды напряжением (растрескивание металла в результате одновременного воз действия растягиваю щих напряжений и агрессивной среды) Виды коррозии по условиям протекания коррозионного процесса
Коррозия Контактная (местная кор розия, вы званная наличием кон такта изде лий из разно родных ме талловв сре де электролите) Структурная (обусловленная структурной неоднородностью сплава, разруше ние связано с повышенной кор розионной актив ностью одного из компонентов сплава) Щелевая Коррозия при (местная полном и корро зия, не полном протекаю щая на погру жении в участках жид кую поверхности, коррози онную возле среду конструк ционных или Коррозионно Коррозионная технологических эрозионная кавитация зазоров) (разрушение металла в вследствие результате одновре менного одновремен ного воздействия коррозионного и среды и ударного механическо го воздействия) износа Коррозия под Коррозия при переменном погружении металла це ликом или частично в жидкую коррозион ную среду Фреттинг коррозия (разрушение металла механическим истира ющим воздействием при наличии коррози онной среды напряжением (растрескивание металла в результате одновременного воз действия растягиваю щих напряжений и агрессивной среды) Виды коррозии по условиям протекания коррозионного процесса
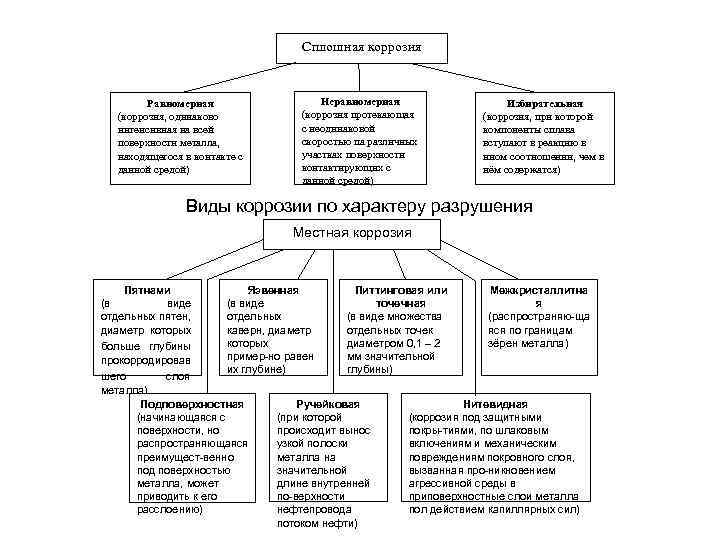 Сплошная коррозия Равномерная (коррозия, одинаково интенсивная на всей поверхности металла, находящегося в контакте с данной средой) Неравномерная (коррозия протекающая с неодинаковой скоростью па различных участках поверхности контактирующих с данной средой) Избирательная (коррозия, при которой компоненты сплава вступают в реакцию в ином соотношении, чем в нём содержатся) Виды коррозии по характеру разрушения Местная коррозия Пятнами Язвенная Питтинговая или Межкристаллитна (в виде точечная я отдельных пятен, отдельных (в виде множества (распространяю ща диаметр которых каверн, диаметр отдельных точек яся по границам которых диаметром 0, 1 – 2 зёрен металла) больше глубины пример но равен мм значительной прокорродировав их глубине) глубины) шего слоя металла) Подповерхностная Ручейковая Нитевидная (начинающаяся с (при которой (коррозия под защитными поверхности, но происходит вынос покры тиями, по шлаковым распространяющаяся узкой полоски включениям и механическим преимущест венно металла на повреждениям покровного слоя, под поверхностью значительной вызванная про никновением металла, может длине внутренней агрессивной среды в приводить к его по верхности приповерхностные слои металла расслоению) нефтепровода пол действием капиллярных сил) потоком нефти)
Сплошная коррозия Равномерная (коррозия, одинаково интенсивная на всей поверхности металла, находящегося в контакте с данной средой) Неравномерная (коррозия протекающая с неодинаковой скоростью па различных участках поверхности контактирующих с данной средой) Избирательная (коррозия, при которой компоненты сплава вступают в реакцию в ином соотношении, чем в нём содержатся) Виды коррозии по характеру разрушения Местная коррозия Пятнами Язвенная Питтинговая или Межкристаллитна (в виде точечная я отдельных пятен, отдельных (в виде множества (распространяю ща диаметр которых каверн, диаметр отдельных точек яся по границам которых диаметром 0, 1 – 2 зёрен металла) больше глубины пример но равен мм значительной прокорродировав их глубине) глубины) шего слоя металла) Подповерхностная Ручейковая Нитевидная (начинающаяся с (при которой (коррозия под защитными поверхности, но происходит вынос покры тиями, по шлаковым распространяющаяся узкой полоски включениям и механическим преимущест венно металла на повреждениям покровного слоя, под поверхностью значительной вызванная про никновением металла, может длине внутренней агрессивной среды в приводить к его по верхности приповерхностные слои металла расслоению) нефтепровода пол действием капиллярных сил) потоком нефти)
 Цветные металлы Магний и сплавы на его основе Физические и механические свойства магния: Температура плавления, °С 651 Плотность, кг/м 3 1740 t, ºC σB, МПа ψ, % +17 -196 -253 180 200 210 10 7 8
Цветные металлы Магний и сплавы на его основе Физические и механические свойства магния: Температура плавления, °С 651 Плотность, кг/м 3 1740 t, ºC σB, МПа ψ, % +17 -196 -253 180 200 210 10 7 8
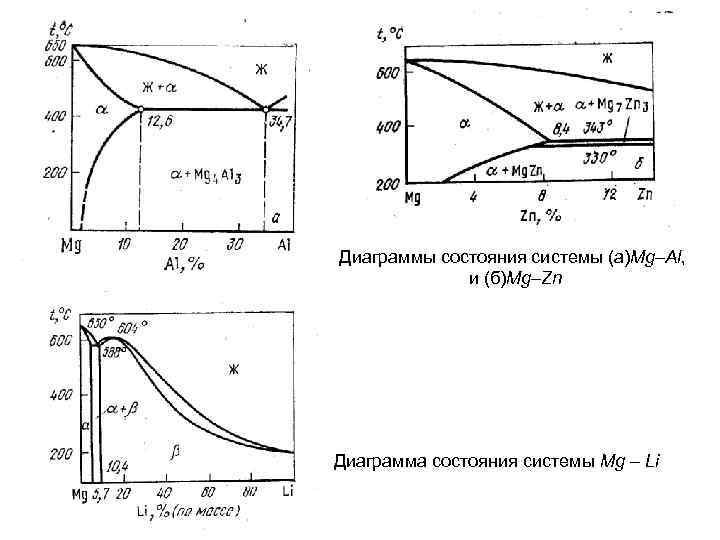 Диаграммы состояния системы (a)Mg–Al, и (б)Mg–Zn Диаграмма состояния системы Mg – Li
Диаграммы состояния системы (a)Mg–Al, и (б)Mg–Zn Диаграмма состояния системы Mg – Li
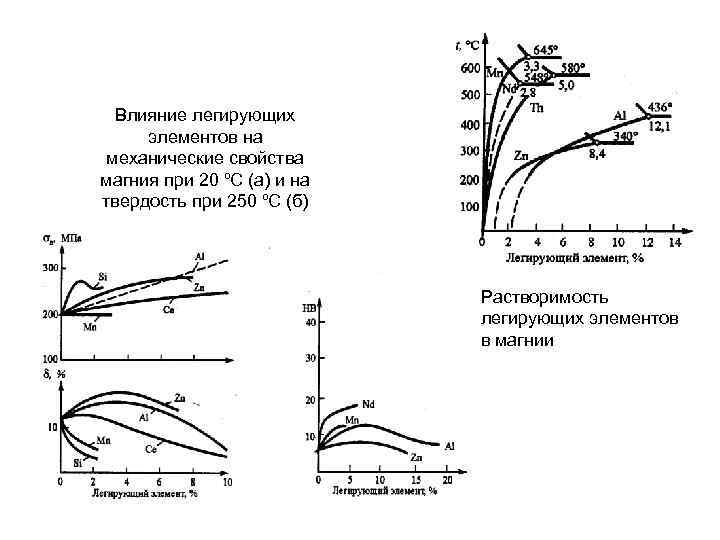 Влияние легирующих элементов на механические свойства магния при 20 ºС (а) и на твердость при 250 ºС (б) Растворимость легирующих элементов в магнии
Влияние легирующих элементов на механические свойства магния при 20 ºС (а) и на твердость при 250 ºС (б) Растворимость легирующих элементов в магнии
 Бериллий и сплавы на его основе Физические свойства бериллия: температура плавления, °С плотность, кг/м 3 теплопроводность, Вт/(м·К) теплоемкость удельная, Дж/(кг·К) температурный коэффициент линейного расширения, К− 1 1283 1844, 8 150 1674 13 модуль нормальной упругости, ГПа 310
Бериллий и сплавы на его основе Физические свойства бериллия: температура плавления, °С плотность, кг/м 3 теплопроводность, Вт/(м·К) теплоемкость удельная, Дж/(кг·К) температурный коэффициент линейного расширения, К− 1 1283 1844, 8 150 1674 13 модуль нормальной упругости, ГПа 310
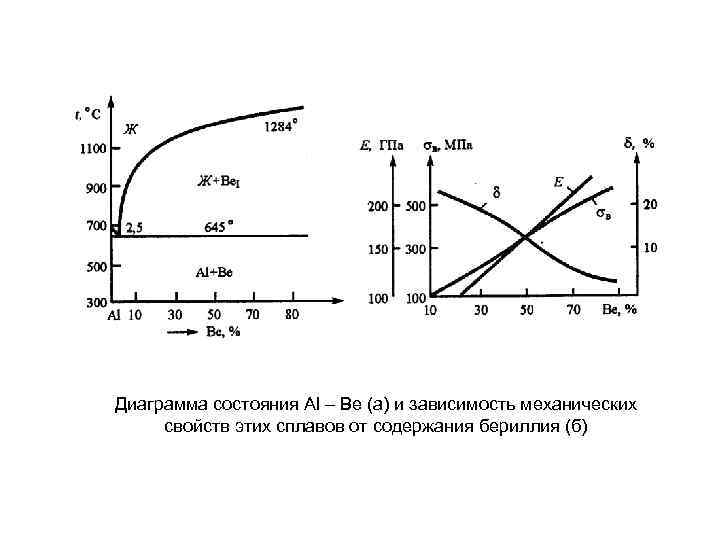 Диаграмма состояния Al – Be (а) и зависимость механических свойств этих сплавов от содержания бериллия (б)
Диаграмма состояния Al – Be (а) и зависимость механических свойств этих сплавов от содержания бериллия (б)
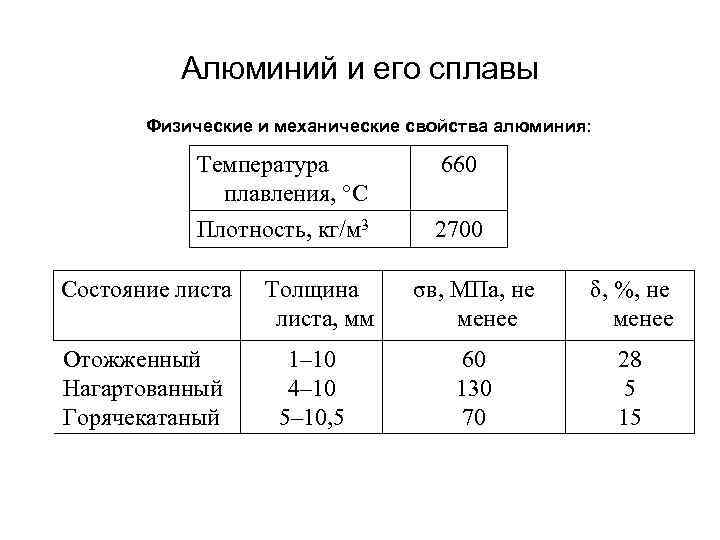 Алюминий и его сплавы Физические и механические свойства алюминия: Температура плавления, °С 660 Плотность, кг/м 3 2700 Состояние листа Отожженный Нагартованный Горячекатаный Толщина листа, мм 1– 10 4– 10 5– 10, 5 σв, МПа, не менее δ, %, не менее 60 130 70 28 5 15
Алюминий и его сплавы Физические и механические свойства алюминия: Температура плавления, °С 660 Плотность, кг/м 3 2700 Состояние листа Отожженный Нагартованный Горячекатаный Толщина листа, мм 1– 10 4– 10 5– 10, 5 σв, МПа, не менее δ, %, не менее 60 130 70 28 5 15
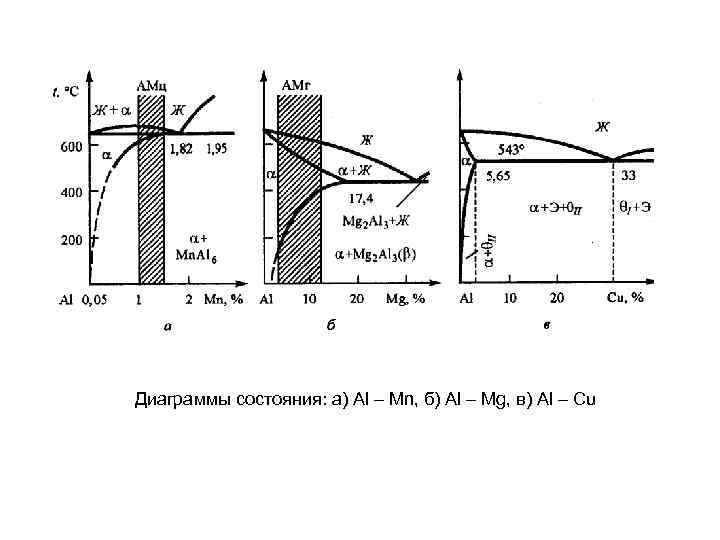 Диаграммы состояния: а) Al – Mn, б) Al – Mg, в) Al – Cu
Диаграммы состояния: а) Al – Mn, б) Al – Mg, в) Al – Cu
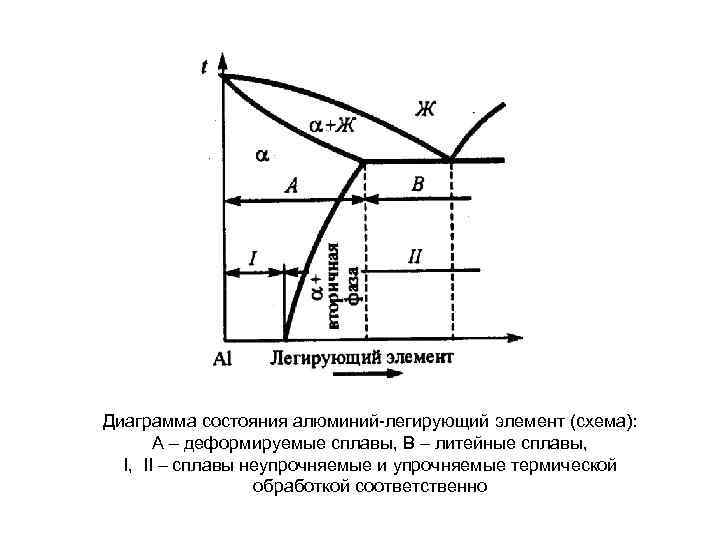 Диаграмма состояния алюминий легирующий элемент (схема): А – деформируемые сплавы, В – литейные сплавы, I, II – сплавы неупрочняемые и упрочняемые термической обработкой соответственно
Диаграмма состояния алюминий легирующий элемент (схема): А – деформируемые сплавы, В – литейные сплавы, I, II – сплавы неупрочняемые и упрочняемые термической обработкой соответственно
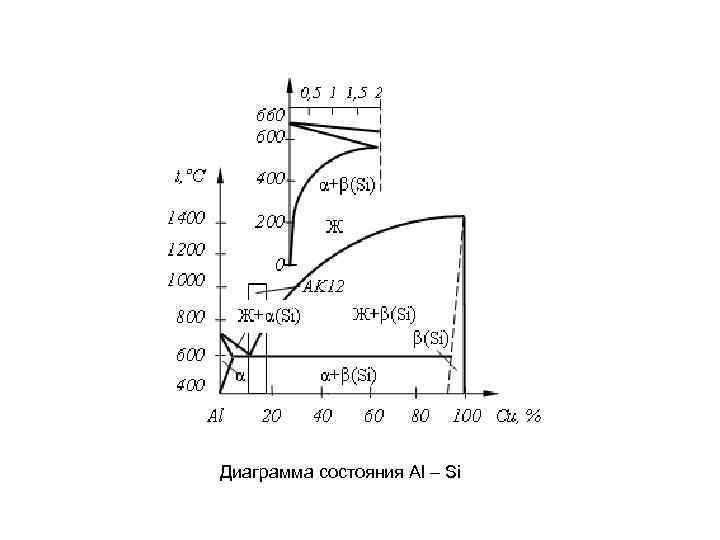 Диаграмма состояния Al – Si
Диаграмма состояния Al – Si
 Титан и сплавы на его основе Физические свойства титана: температура плавления, °С плотность, кг/м 3 теплопроводность, Вт/(м·К) температурный коэффициент линейного расширения, К− 1 1700 4500 18, 85 8, 15 модуль нормальной упругости, ГПа 112
Титан и сплавы на его основе Физические свойства титана: температура плавления, °С плотность, кг/м 3 теплопроводность, Вт/(м·К) температурный коэффициент линейного расширения, К− 1 1700 4500 18, 85 8, 15 модуль нормальной упругости, ГПа 112
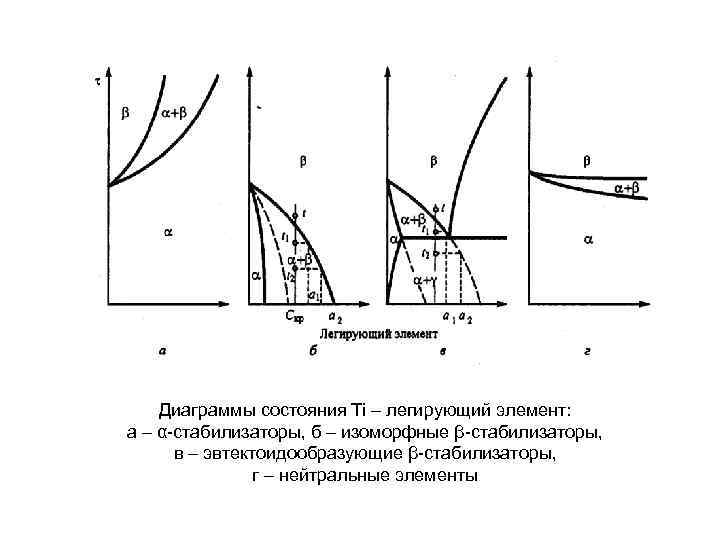 Диаграммы состояния Тi – легирующий элемент: а – α стабилизаторы, б – изоморфные β стабилизаторы, в – эвтектоидообразующие β стабилизаторы, г – нейтральные элементы
Диаграммы состояния Тi – легирующий элемент: а – α стабилизаторы, б – изоморфные β стабилизаторы, в – эвтектоидообразующие β стабилизаторы, г – нейтральные элементы
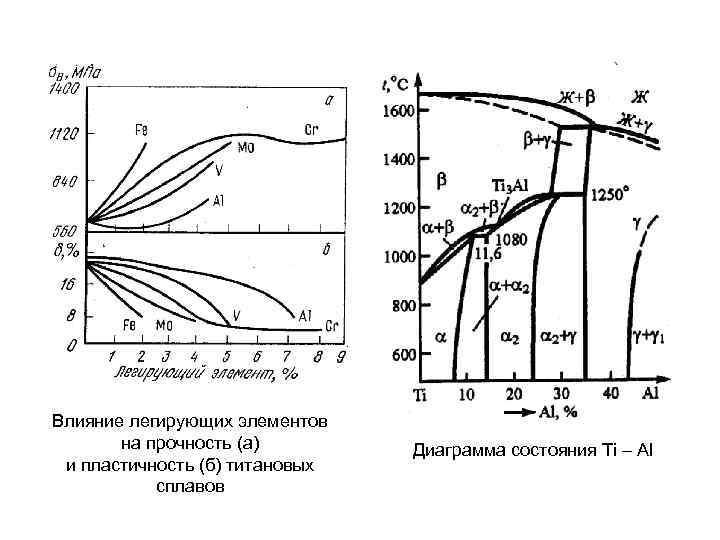 Влияние легирующих элементов на прочность (а) и пластичность (б) титановых сплавов Диаграмма состояния Ti – Al
Влияние легирующих элементов на прочность (а) и пластичность (б) титановых сплавов Диаграмма состояния Ti – Al
 Медь и ее сплавы Физические и механические свойства меди: Температура плавления, ºС 1083 Плотность, кг/м 3 8940 Предел прочности, МПа 200– 250 Относительное удлинение, % 40– 50
Медь и ее сплавы Физические и механические свойства меди: Температура плавления, ºС 1083 Плотность, кг/м 3 8940 Предел прочности, МПа 200– 250 Относительное удлинение, % 40– 50
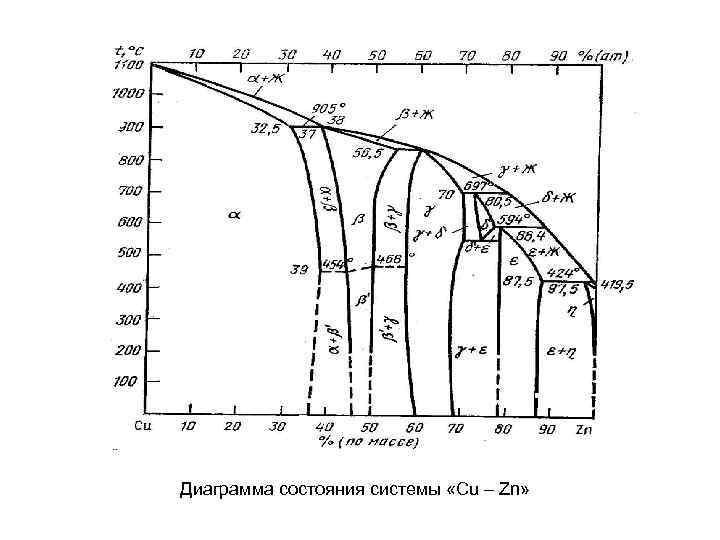 Диаграмма состояния системы «Cu – Zn»
Диаграмма состояния системы «Cu – Zn»
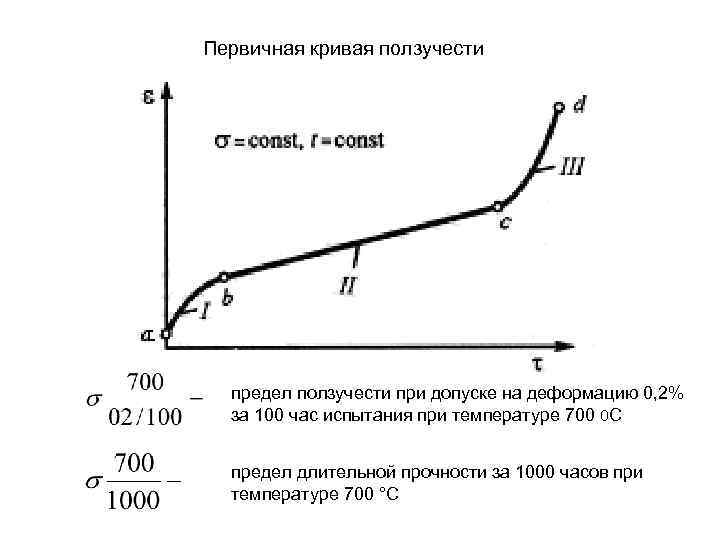 Первичная кривая ползучести предел ползучести при допуске на деформацию 0, 2% за 100 час испытания при температуре 700 0 С предел длительной прочности за 1000 часов при температуре 700 °С
Первичная кривая ползучести предел ползучести при допуске на деформацию 0, 2% за 100 час испытания при температуре 700 0 С предел длительной прочности за 1000 часов при температуре 700 °С
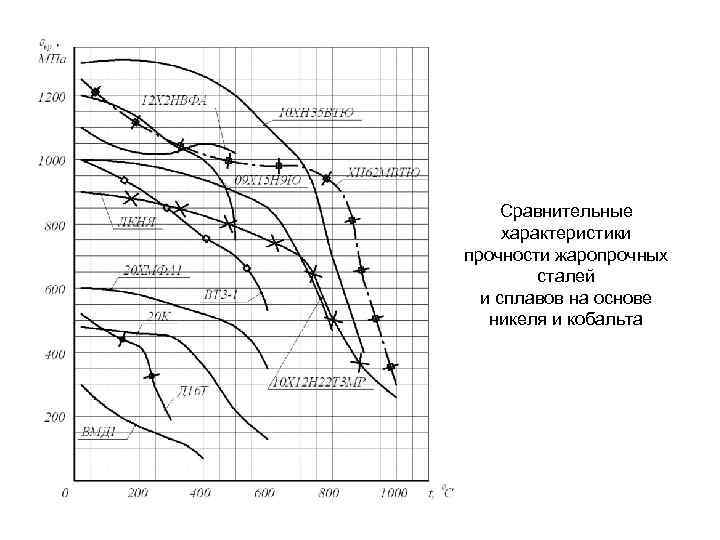 Сравнительные характеристики прочности жаропрочных сталей и сплавов на основе никеля и кобальта
Сравнительные характеристики прочности жаропрочных сталей и сплавов на основе никеля и кобальта
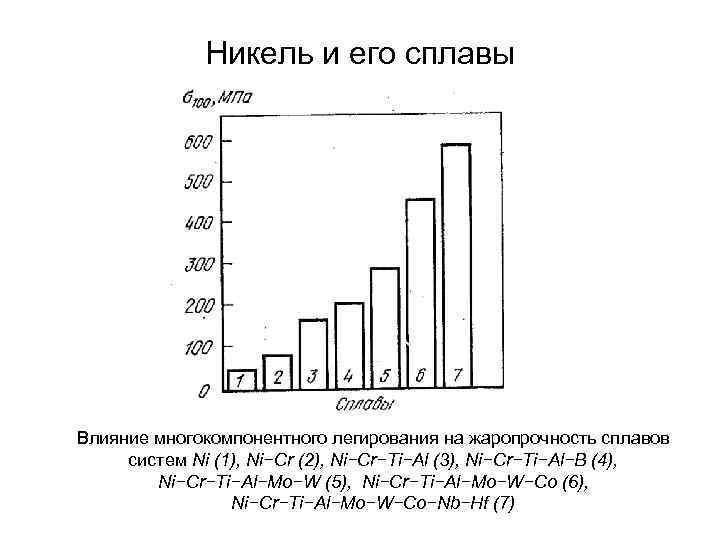 Никель и его сплавы Влияние многокомпонентного легирования на жаропрочность сплавов систем Ni (1), Ni−Cr (2), Ni−Cr−Ti−Al (3), Ni−Cr−Ti−Al−B (4), Ni−Cr−Ti−Al−Mo−W (5), Ni−Cr−Ti−Al−Mo−W−Co (6), Ni−Cr−Ti−Al−Mo−W−Co−Nb−Hf (7)
Никель и его сплавы Влияние многокомпонентного легирования на жаропрочность сплавов систем Ni (1), Ni−Cr (2), Ni−Cr−Ti−Al (3), Ni−Cr−Ti−Al−B (4), Ni−Cr−Ti−Al−Mo−W (5), Ni−Cr−Ti−Al−Mo−W−Co (6), Ni−Cr−Ti−Al−Mo−W−Co−Nb−Hf (7)
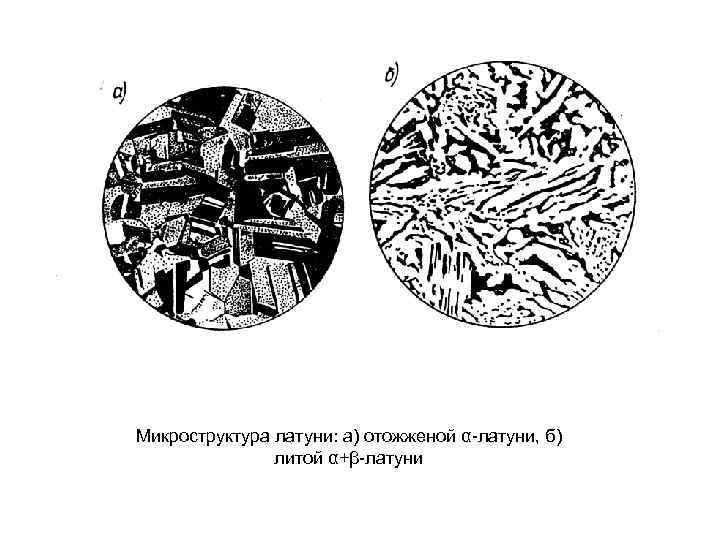 Микроструктура латуни: а) отожженой α латуни, б) литой α+β латуни
Микроструктура латуни: а) отожженой α латуни, б) литой α+β латуни
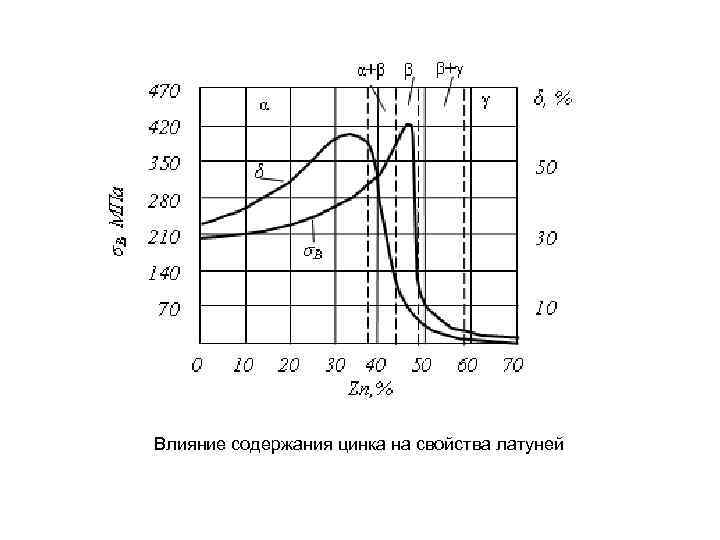 Влияние содержания цинка на свойства латуней
Влияние содержания цинка на свойства латуней
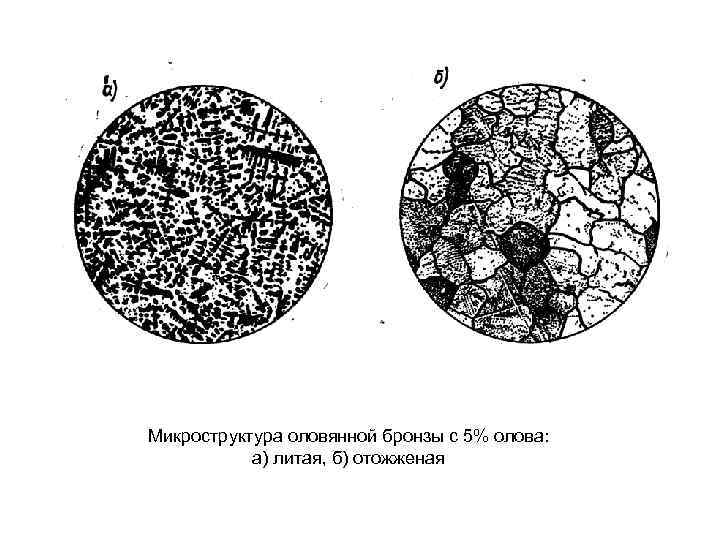 Микроструктура оловянной бронзы с 5% олова: а) литая, б) отожженая
Микроструктура оловянной бронзы с 5% олова: а) литая, б) отожженая
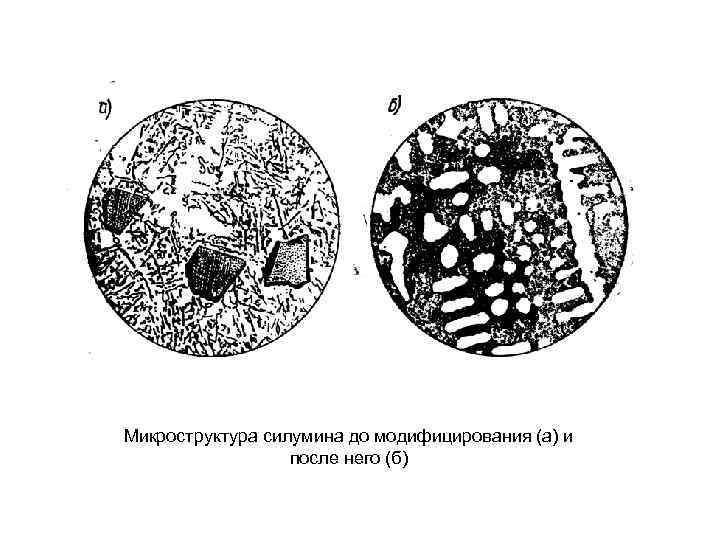 Микроструктура силумина до модифицирования (а) и после него (б)
Микроструктура силумина до модифицирования (а) и после него (б)
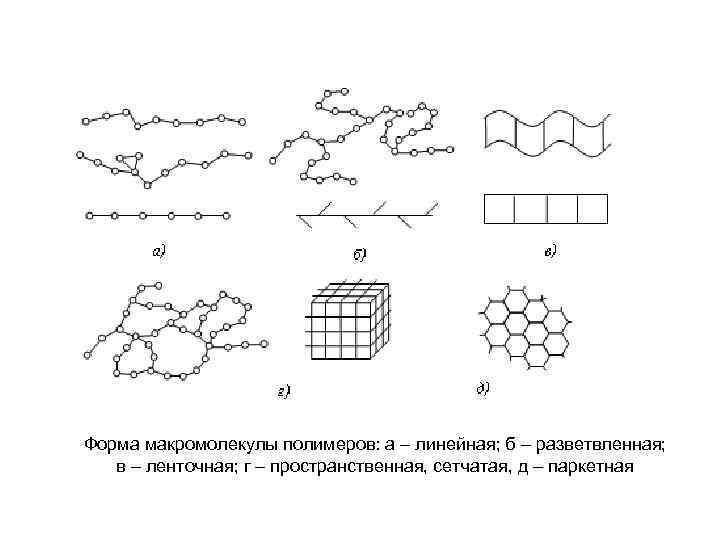 Форма макромолекулы полимеров: а – линейная; б – разветвленная; в – ленточная; г – пространственная, сетчатая, д – паркетная
Форма макромолекулы полимеров: а – линейная; б – разветвленная; в – ленточная; г – пространственная, сетчатая, д – паркетная
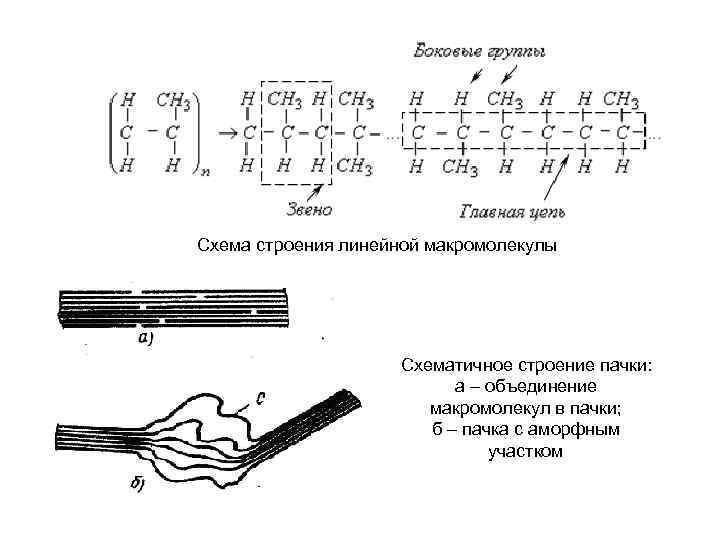 Схема строения линейной макромолекулы Схематичное строение пачки: а – объединение макромолекул в пачки; б – пачка с аморфным участком
Схема строения линейной макромолекулы Схематичное строение пачки: а – объединение макромолекул в пачки; б – пачка с аморфным участком
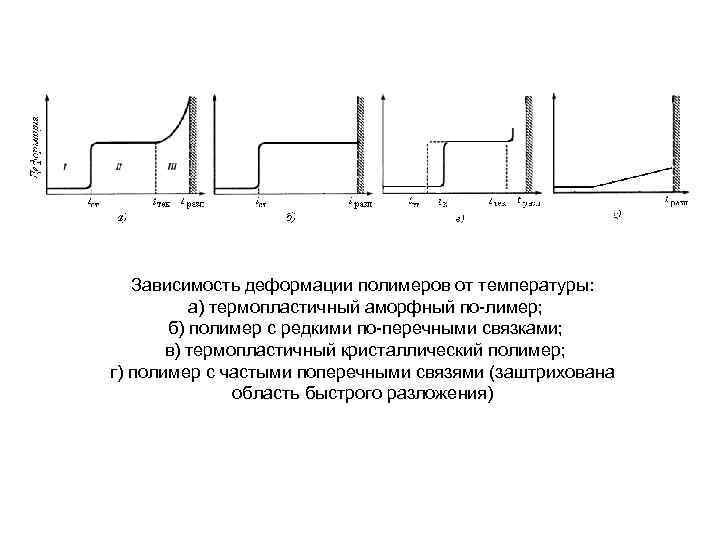 Зависимость деформации полимеров от температуры: а) термопластичный аморфный по лимер; б) полимер с редкими по перечными связками; в) термопластичный кристаллический полимер; г) полимер с частыми поперечными связями (заштрихована область быстрого разложения)
Зависимость деформации полимеров от температуры: а) термопластичный аморфный по лимер; б) полимер с редкими по перечными связками; в) термопластичный кристаллический полимер; г) полимер с частыми поперечными связями (заштрихована область быстрого разложения)
 Схематичное изображение молекулярных процессов при деформации: 1 – упругое, 2 – высокоэластичное, 3 – вязкое
Схематичное изображение молекулярных процессов при деформации: 1 – упругое, 2 – высокоэластичное, 3 – вязкое
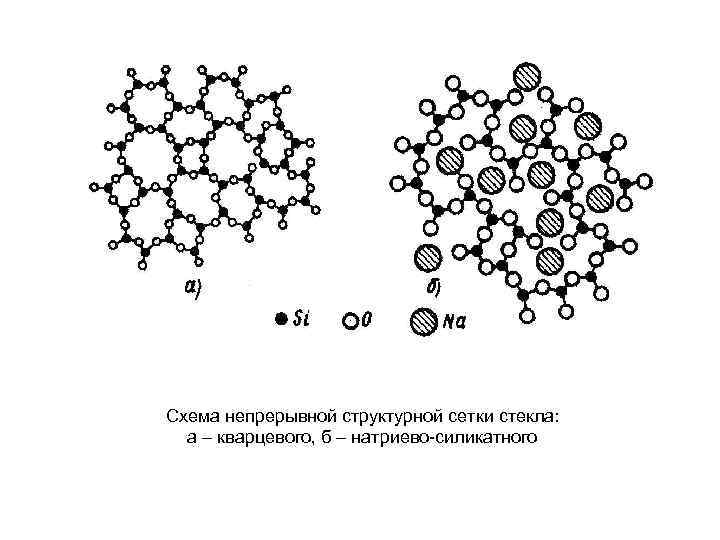 Схема непрерывной структурной сетки стекла: а – кварцевого, б – натриево силикатного
Схема непрерывной структурной сетки стекла: а – кварцевого, б – натриево силикатного
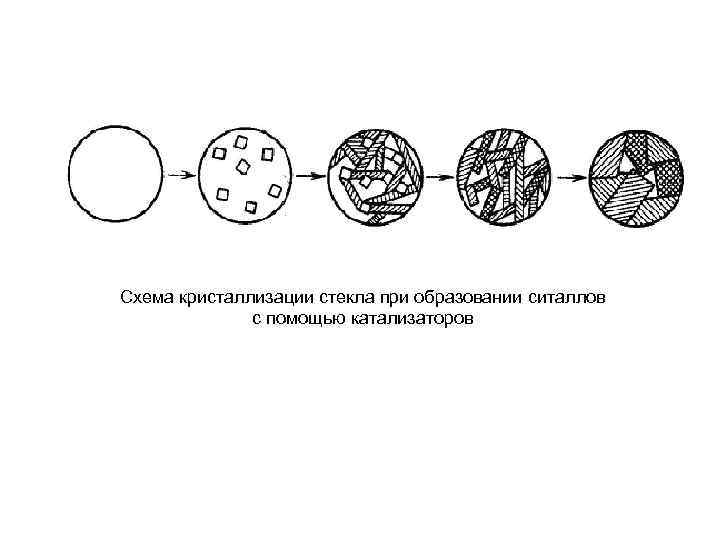 Схема кристаллизации стекла при образовании ситаллов с помощью катализаторов
Схема кристаллизации стекла при образовании ситаллов с помощью катализаторов
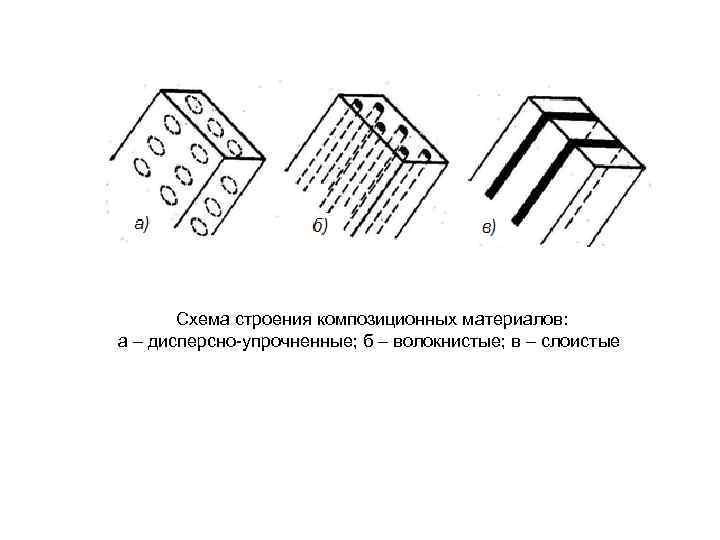 Схема строения композиционных материалов: а – дисперсно упрочненные; б – волокнистые; в – слоистые
Схема строения композиционных материалов: а – дисперсно упрочненные; б – волокнистые; в – слоистые
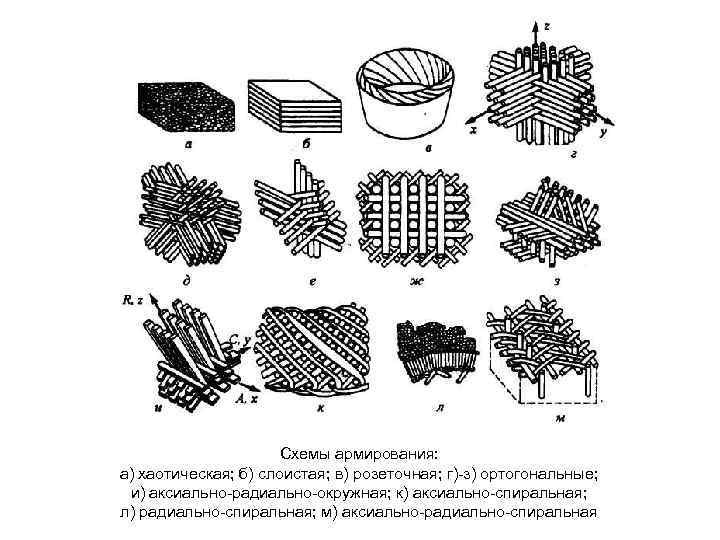 Схемы армирования: а) хаотическая; б) слоистая; в) розеточная; г) з) ортогональные; и) аксиально радиально окружная; к) аксиально спиральная; л) радиально спиральная; м) аксиально радиально спиральная
Схемы армирования: а) хаотическая; б) слоистая; в) розеточная; г) з) ортогональные; и) аксиально радиально окружная; к) аксиально спиральная; л) радиально спиральная; м) аксиально радиально спиральная


