РАСЧЕТЫ КОЭФФИЦИЕНТОВ РАЗДЕЛЕНИЯ.ppt
- Количество слайдов: 98

РАСЧЕТЫ КОЭФФИЦИЕНТОВ РАЗДЕЛЕНИЯ ПРИ ИЗОТОПНОМ ОБМЕНЕ. Учебное пособие

ВВЕДЕНИЕ w Важнейшими факторами, влияющими на эффективность процесса разделения изотопов, является величина коэффициента обогащения и значение термодинамического коэффициента полезного действия. w Минимальное число ступеней в каскаде обратнопропорционально величине .

w Такого же характера зависимость от коэффициента обогащения и величины потоков в каскаде. w где Sразр — изменение энтропии при разделении смеси w Е 0=-RT (ln C 0 -1) (2) w Здесь - величина отбора; w C 0 - начальная концентрация. w Термодинамический КПД ( ) сильно зависит от того, является ли метод разделения обратимым.

w К числу обратимых методов относятся дистилляция, изотопный обмен. Для указанных методов имеет порядок 104. w. К необратимым методам разделения относятся такие как газовая диффузия, электролиз, центрифугированиемасс, диффузия. В указанных методах величина составляет 10 -6 – 10 -8.

w В случае обратимых методов энергия в системе подводится только для обеспечения продольного потока вещества. w В необратимых методах затраты энергии связаны непосредственно с процессом разделения в каждой ступени.

w Важной характеристикой процесса разделения является так же скорость его протекания. w Рассмотрим более подробно указанные факторы процесса разделения изотопов. Главное внимание будет уделено обратимым методам разделения, использование которых имеет большие перспективы.

w Величина коэффициента разделения и обогащения имеющего место в обменных процессах между двумя произвольными соединениями данного элемента, определяется как отношение -факторов этих соединений. w w (3)

w -факторы однозначно связаны с отношением сумм по состояниям изотопных форм соединений и, следовательно, они исчерпывающим образом характеризуют термодинамические возможности соединений в отношении разделения изотопов.

w Решение указанных термодинамических вопросов возможно путем изучения закономерностей, связывающих факторы с другими характеристиками химических соединений, а также с характеристиками составляющих эти соединения элементов.

w Материалы для обнаружения таких закономерностей мог бы дать массовый расчет -факторов. w Для такого расчета необходимо знание точных значений колебательных частот изотопных форм соединений. Однако частоты колебаний изотопных форм экспериментально определены лишь для небольшого числа соединений.

w Есть и другой путь, заключающийся в том, что за основу берутся измеренные собственные частоты колебаний соединений с естественным изотопным составом. Методы теории колебаний молекул позволяют рассчитывать по этим частотам данные для любых изотопных форм соединений. Причем точность таких расчетов особенно велика для двухатомных молекул.

w Точность расчета для многоатомных молекул зависит от характера применяемой кинематической модели молекулы. w В этом случае погрешности при подсчете -факторов возникают по следующим причинам: w 1)неверное отношение частот; w 2)неточный расчет изотопических соединений колебательных частот;

w 3)неточное измерение самих частот; w 4)неучёт ангармонических колебаний; w 5)неучет поправок на взаимодействие колебательных и вращательных движений; w 6)применение приближенных соотношений для расчета факторов. w Основной вклад в погрешность расчета вносит неточность расчёта изотопических смещений.

w Ошибка расчёта смещений складывается из ошибки расчета силовых постоянных и ошибки смещений по данным значениям силовых постоянных. w Вычисление термодинамических функций, необходимых для расчёта равновесных характеристик процесса разделения значительно упрощается при вычислении констант равновесия обменных процессов,

w поскольку при этом учитывается лишь изменение масс и таких непосредственно связанных с массой величин, как момент инерции, частоты колебаний атомных ядер и нулевые колебательные энергии. w Ряд параметров и функций (размеры изотопических разновидностей молекул, потенциальные функции их и др. ) выпадают из расчёта,

w т. к. они практически не изменяются при замене одного изотопа другим. В основе вычисления констант равновесия лежит определение сумм по состояниям молекул, отношений статистических сумм со состояниям. w Рассмотрим указанные величины более подробно.

§ I. ЭНЕРГЕТИЧЕСКИЕ УРОВНИ МОЛЕКУЛ.

w Суммарную анергию молекулы газообразного вещества можно разделить на поступательную и внутримолекулярную. Если за нуль энергии принять значение, отстоящее от минимума потенциальной энергии вниз на расстояние 0 ‘ то величину 0 ‘ можно рассматривать как энергию химической связи (рис. 1).
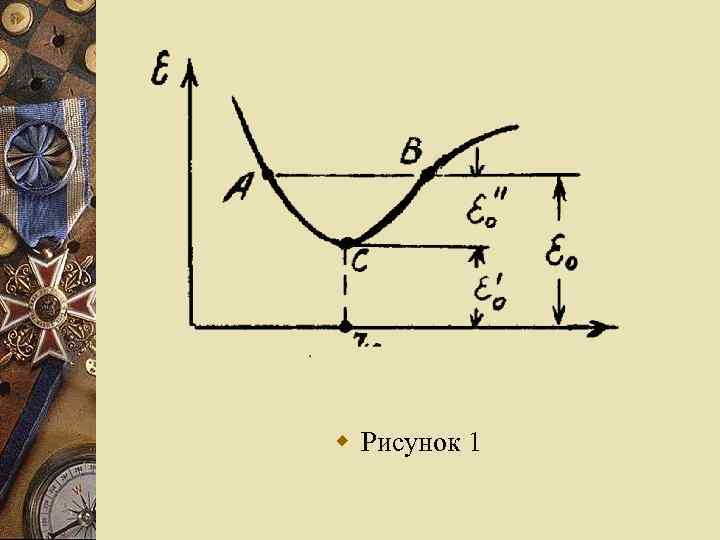
w Рисунок 1

w Величина 0 ‘’ представляет нулевую колебательную энергию, равную h /2. Нулевая энергия молекулы: w 0 = 0 ‘ + 0" (4) w а общая энергия молекулы: w = 0 + пост + внутрь, (5) w где внутрь - равно энергии внутренних движений молекулы, отсчитанной от уровня АВ при нулевых значениях квантовых чисел этих движений.

w Если одному и тому же уровню энергии отвечает несколько состояний, говорят, что уровень энергии вырожден. Степень вырождения или статистический вес qi есть число состояний с одинаковой или почти одинаковой энергией. w Для определения термодинамических свойств веществ помимо энергетических уровней молекулы, известных из спектроскопии, необходимо знать распределение молекул по этим уровням.

w Если число молекул, обладающих минимальной энергией, т. е. находящиеся в низшем (невозбужденном) энергетическом уровне равно n 0 , то по закону распределения Максвелла-Больцмана число молекул на i-ом уровне будет: w (6) w где i- избыток энергии по сравнению с нулевой.

w Учитывая вырождение уровней, получим для одного моля: w N= qini=q 0 n 0+q 1 n 1 e- 1/k. T+q 2 n 2 e- 2/k. T (7) w где N - число Авогадро. w Величина w Q = qie- i/k. T (8) w характеризующая распределение молекул по энергетическим уровням, называется суммой по состояниям (или функцией распределения) молекул.

w Выражение (8) можно переписать в виде w w Beличинa е- 0/k. T может быть вынесена за знак суммы. Выполняя суммирование по квантовым числам поступательного движения (вес пост = I) и вынося результат за знак второй суммы, будем иметь: w (9)

w или (10) w Вычисление термодинамических свойств сводится к нахождению Q и её производных по температуре. Для подсчета величины Q нужно знать уровни энергии и статистические веса, которые определяются обычно из результатов спектральных исследований.

w Для одноатомных и большинства двухатомных молекул точный расчет не вызывает затруднений. w Для многоатомных молекул почта всегда можно произвести лишь приближенный расчет, который во многих случаях дает результаты, близкие к точным. Только для водорода и дейтерия при температурах ниже 250 и 150 К соответственно, приближенные методы приводят к значительным ошибкам.

w Поэтому мы ограничимся изложением приближенного метода, считая, что нам известны данные о строении молекул. w Для большинства молекул, начиная от Т 50 К и до Т 5000 К можно принять w Q=e- 0/k. T Qпост Qвнутр=e- 0/k. T Qпост Qэл Qвр. кол Qсп w т. е. взаимное влияние вращательноколебательных, электронных и w ядерных сумм состояния невелико.

w Ввиду сложности учета взаимного влияния вращений и колебаний будем считать его незначительным, что, впрочем, приводит к небольшой погрешности. w Тогда: w Q=e- 0/k. T Qпост Qвр Qэл Q кол Qспин (11) w т. е. мы принимаем также адекватность энергии: w 0+ пост+ эл+ кол+ вр+ спин

w В силу принятой взаимозависимости Q , вычисления для каждого вида движения молекул производится раздельно. w Для одноатомного газа: w w (13) w Для расчета Q многоатомных газов надо принять уравнение w (), содержащее все сомножители.

w Однако при вычислении констант равновесия в большинстве случаев можно пренебречь электронной составляющей в спине ядра, w т. е. учитывать только Q пост, Qкол и Q вр. Тогда для двухатомной молекулы, например, Q будет равна: w w w (14)

w В формулы для расчета констант равновесия войдет, как мы увидим позже, разность нулевых компонентов реакции. Эта разность для двух атомных изотопических молекул, имеющих одинаковую энергию диссоциации, сводится к разности нулевых энергии колебаний h /2, поэтому уравнение (14) можно переписать в виде: w (15)

w Для многоатомной молекулы в общем случае (IA IB IC) для не очень малых значений Т и I получим w w w (16)

§ 2. КОНСТАНТА РАВНОВЕСИЯ РЕАКЦИИ ИЗОТОПНОГО ОБМЕНА.

w Пусть дана реакция типа: w А 2 + В 2 2 АВ w где А и В символы двух изотопов одного и того жe элемента. Примерами таких реакций являются: w Н 2 + D 2 2 HD, w 35 Cl + 37 Cl 235 Cl 37 Cl (18) 2 2

w Для константы равновесия реакции типа (18) имеем: w (19) w где = 2 АВ - А 2 - В 2 w При низких температурах, когда hv k. T , выражение в фигурных скобках близко к единице.

w Тогда w (20) w Наоборот, при достаточно высоких температурах, когда выражение w Qкол = (1 -e-h i k. T)-1 примет классическое значение к. Т/h i. Тогда при достаточно высоких температурах имеем w (21)

Отношение сумм по состояниям молекул. w Если уровни колебательной энергии в достаточной степени приближаются к гармоническим, то для средних и высоких температур, когда КТ велико по сравнению с расстояниями между уровнями вращательной энергии (как это действительно имеет место в большинстве случаев), отношение сумм

w по состояниям в случае 2 -х атомных молекул будет равно: w w (22). w Для многоатомных молекул, имеющих 3 n-x нормальных колебаний, получим: w (23)

w В этих уравнениях М 1 и М 2 представляют молекулярные веса изотопических разновидностей молекул, пропорциональные их массам, а величины Ui , называемые приведенными частотами, связаны с основными частотами колебаний соотношениями вида: w (24)

w Расчет отношений сумм по состояниям по уравнению (23) не всегда может быть выполнен для сложных многоатомных молекул. Затруднения, связанные с отсутствием экспериментальных данных о моментах инерции второй изотопической разновидности молекул, могут быть преодолены, а выражения (22) и (23) значительно упрощены при использовании правила произведения частот, предложенного Теллером и Редлихом.

w Это правило (или, как его иногда называют, теорема) применимо для всех видов симметрии и для всех колебаний по теореме Теллера и Редлиха: w w (25) w где m 1 и m 2 атомные веса, а ‘n’ — число обменивающихся изотопных атомов.
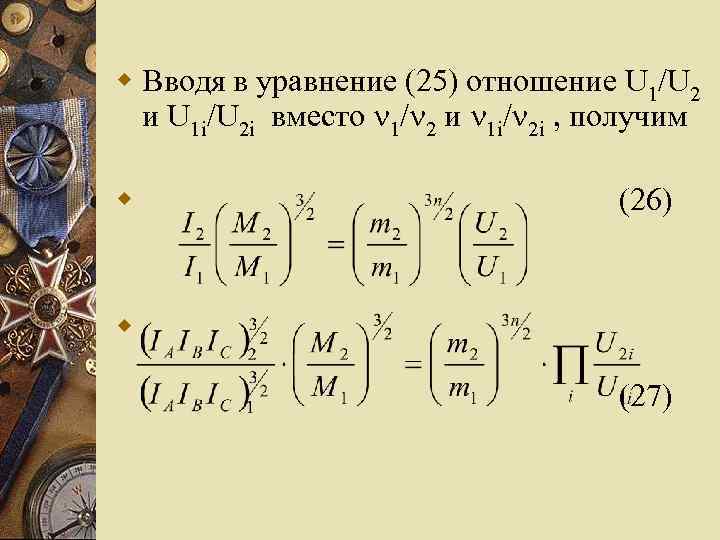
w Вводя в уравнение (25) отношение U 1/U 2 и U 1 i/U 2 i вместо 1 2 и 1 i 2 i , получим w (26) w (27)

w Подставляя эти выражения в уравнение (16) и (17) найдем отношение сумм по состояниям двухатомных и изотопических разновидностей молекул: w (28)
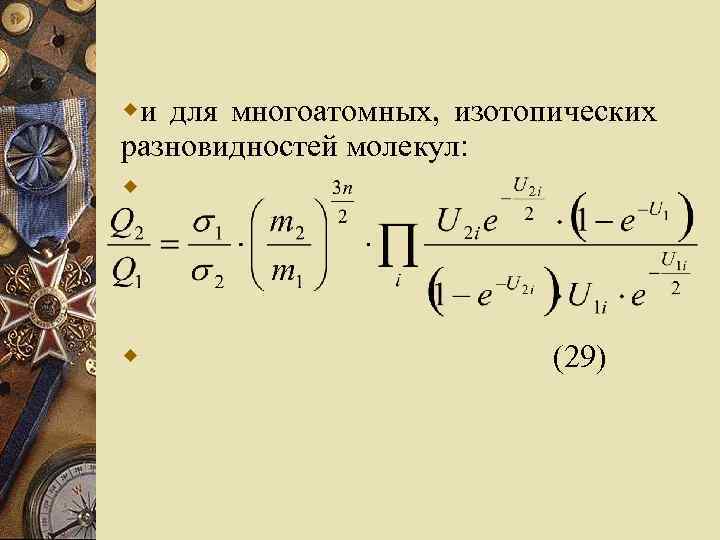
wи для многоатомных, изотопических разновидностей молекул: w w (29)

w Определив отношение Q 2/Q 1 с помощью этих формул, можно далее на основании соотношения (19) вычислить значения К. С небольшим ущербом для точности можно упростить вычисления, если воспользоваться приближенными методами расчета констант равновесия реакции изотопного обмена, разработанными независимо друг от друга М. В. Татевским и Бигеляйзином и Майер.

§ 3. МЕТОДЫ РАСЧЕТА КОНСТАНТ РАВНОВЕСИЯ

а) Метод Бигеляйзена и Майер. w Вычисление константы равновесия реакции изотопного обмена можно упростить, если вместо Q 2/Q 1 ввести производные: w (30)

Пусть в реакции a. A 1 + b. B 2 = a. A 2 + b. B 1 (31) w в молекулах A 1 и A 2 обменивается n 1 атомов, в молекулах B 1 и В 2 – n 2 атомов данного изотопа. w Общее число обменивающихся атомов в реакции (31) будет w n 1 a + n 2 b w Так, для реакции обмена 180 и 160 между 160 и Н 180 2 w n 2= 2, а =1, n 2=1, b=2.

w На основании формулы (30) имеем: w (32) w (33)
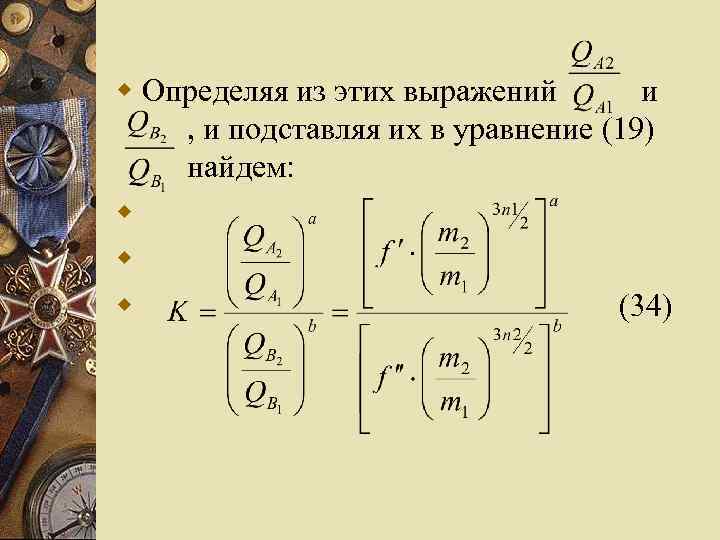
w Определяя из этих выражений и , и подставляя их в уравнение (19) найдем: w w w (34)

w откуда в силу равенства (33) w (35) w Нетрудно убедиться, что величина, определяемая формулой (30), представляет отношение констант равновесия образования изотопических молекул из атомов в газообразной фазе.

w Бигеляйзен и Майер показали, что w w (36) w где w (37)

w При изменении Ui от 0 до величина изменяется от 0 до 0, 5. Значения функции Y вычислены Бигеляйзеным и Майер для разных возможных значений ui и приводятся в соответствующих таблицах. w Пример I. w Вычисление с помощью таблиц Бигеляйзена и Майер константы реакции: w С 16 О 2 + 2 Н 218 О С 18 О 2 + 2 Н 216 О при 600 К.

w Из таблиц и формулы (25) значения f равны: w w Подставив эти значения в формулу для расчета К, получим w

w При повышении температуры величины ui и Yi приближаются к нулю, поэтому при достаточно высокой температуре w , wа константа равновесия имеет предельное значение К 0, определяемое числами симметрии и отвечающее равновероятностному распределению изотопов между молекулами системы:

w (38) w Далее будет показано, что при К = K 0 коэффициент разделения = I обменная реакция не приводит к разделению изотопов. w Мерой эффективности разделения путем обменных реакций будет служить отношение.

б) Метод Татевского В. М. w При высоких температурах отношение колебательных сумм по состояниям изотопических молекул можно аппроксимировать при помощи первых членов разложения в ряд Макларена: w (39)

w Однако величина поправочного члена в скобках велика даже при сравнительно высоких температурах, если разность частот W 1 i и W 2 i велика (Ui=hc. Wi/k. T; т. к. Wi= i/c) w Пренебрежение поправочным членом в скобках дает значительную ошибку, которая при составляет w 4, 5% для и 19% при .

w При одновременном разложении в ряд членов с нулевой колебательной энергией получаем приближенное соотношение вида: (40) w Последнее выражение дает заниженные значения для fi. Хорошее приближение дается более простым выражением: w
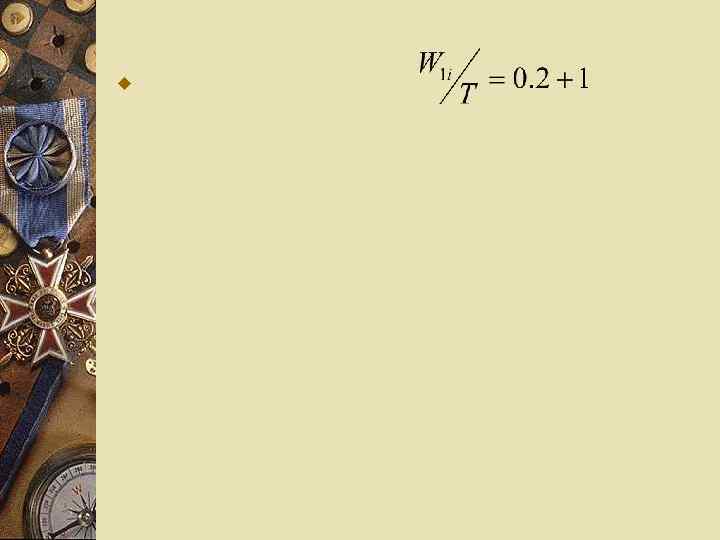
w

w Выразим fi в виде (см. 29): w (42) w Или w w где (43)

w В выражении (42) i, как показывает расчет, может представлена как: w (44) w причем x и в первом приближении не зависят от ri и W 1 i.

в) Уточнение расчета констант равновесия. w Обычный метод статистического расчета констант равновесия основан на знании всех частот и моментов инерции обменивающихся молекул. w Для типичной реакции обмена изотопов w a. A 1+b. В 2= а. А 2+в. В 1 (45)

w между многоатомными молекулами расчет по схеме гармонический осциллятор - жесткий ротатор приводит к следующему значению K: w (46) w частоты изотопических разновидностей молекул определяется либо экспериментально, либо путем вычисления.

w Для точных расчетов надо учитывать и ангармонические члены в колебательной энергии. Ошибки при расчете К могут быть вследствие неучета ангармонических членов, а также вследствие неточностей при вычислении основных частот редких изотопных разновидностей молекул.

г) Константа равновесия и коэффициент разделения. w Для реакции w АХ + ВХ* АХ* + ВХ (47) w в каждой из молекул которой имеется лишь по одному обменивающемуся атому Х, константа равновесия совпадает с коэффициентом разделения: w w (48)

w Соотношения более сложны, если в реакции участвуют молекулы, имеющие по нескольку обменивающихся атомов. Рассмотрим обменную реакцию типа АХn + b. BXm* АXn-1 Xi* +Bbxm-j. Xj (49) w По определению, коэффициент разделения в этом случае будет равен, как и в реакции (47)
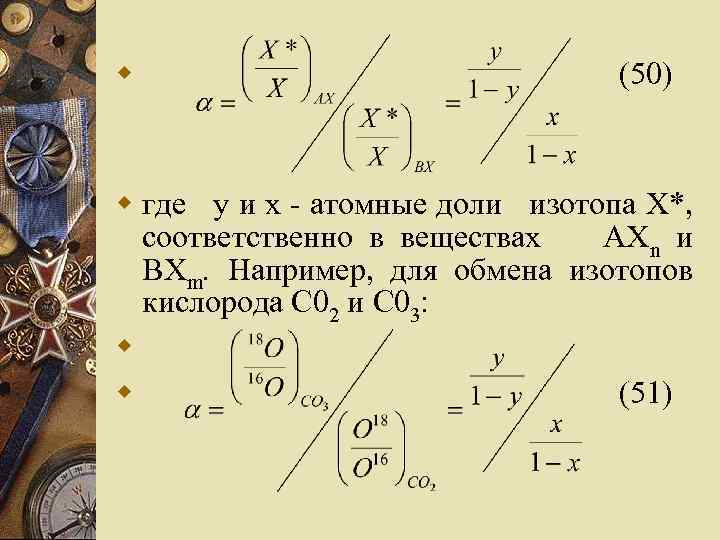
w (50) w где у и х - атомные доли изотопа Х*, соответственно в веществах АХn и BXm. Например, для обмена изотопов кислорода С 02 и С 03: w w (51)

w где y и X - атомные доли 180, С 03 и С 02 как показал А. И. Бродский, w равновесные концентрации каждого сорта молекул AXn-1 Xi* и ВХm-j. Xj пропорциональные вероятностным величинам: w w (52)

w Выражение (51) можно тождественно получить из (42), если под x и у подразумевать значения, которые они принимали бы при чисто вероятностном распределении, отвечающем классической константе К 0 w (53)

Рассмотрим теперь связь между константой равновесия и коэффициентом разделения. Реакцию обмена 180 между CO 2 и СО 3 можно представить любым уравнением обмена, связывающим две изотопные молекулы С 02 с двумя изотопными ионами С 03. От выбора этого уравнения не зависит результат вычислений, так как в состоянии изотопного равновесия все семь разновидностей С 03 и С 02 также находятся в равновесии между собой.

w Выберем, например, уравнение w С 1603 = ЗС 16 О 18 0 С 1803 = +3 С 16 02 с константой равновесия w w Вводя в это уравнение отношение концентраций, отвечающее чисто вероятностному разделению, при котором К=K 0 , получим (54).

w (54) w здесь 0 - тоже раздельное значение коэффициента разделения , отвечающее чисто вероятностному распределению.

w С другой стороны, подставляя в уравнение (53) числа симметрии w С 1803 = , С 1603=, С 16 О 18 0 и С 1602, w равные соответственно 2, 3, I и 2, получим К 0 = 1/23, откуда =1. В этом случае обмен не ведет к разделению изотопов.

w Для истинного разделения коэффициента хорошим приближением будет выражение, аналогичное (54) с истинной константой равновесия К вместо: (55) w Если принять во внимание, что I/23 = К 0, то выражение (44) можно переписать в виде: (56)

w Полученный результат нетрудно обобщить. Для обменной реакции типа: w а. AXn+b. BXm*=a. AX m* + b. BXm w В рассматриваемом приближении: w (57)

w Для изотопных реакций водорода надо принимать во внимание отсутствие чисто вероятностного распределения молекул, заключающегося в том, что, например, при 25°С константа равновесия реакции H 2 O + Д 2 О = 2 НДО равна 4, а не 3, 26. w Для таких реакций следует вместо уравнения (57) использовать уравнение (56).

w -Пример расчета коэффициента разделения реакции изотопного обмена по методу Бигеляйзена. w I) Функция Бигеляйзена принимает значения 1+25. w f = 1 + yi Ui
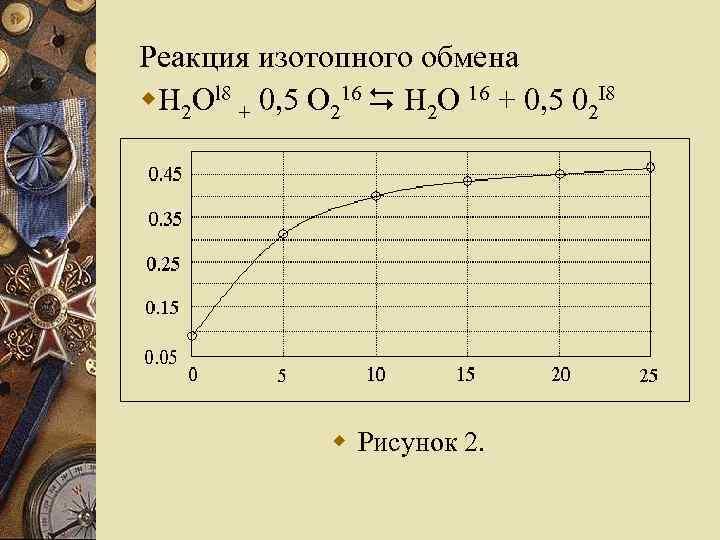
Реакция изотопного обмена w. H 2 Оl 8 + 0, 5 О 216 H 2 О 16 + 0, 5 02 I 8 w Рисунок 2.
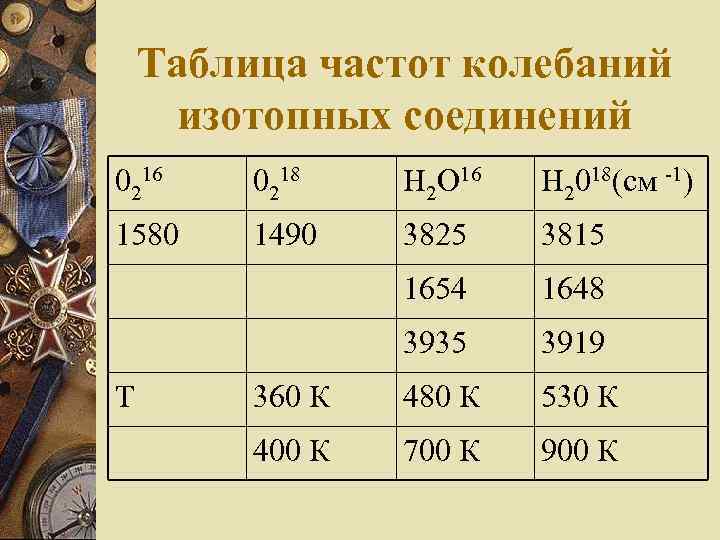
Таблица частот колебаний изотопных соединений 0216 0218 Н 2 О 16 Н 2018(см -1) 1580 1490 3825 3815 1654 1648 3935 3919 360 К 480 К 530 К 400 К 700 К 900 К Т
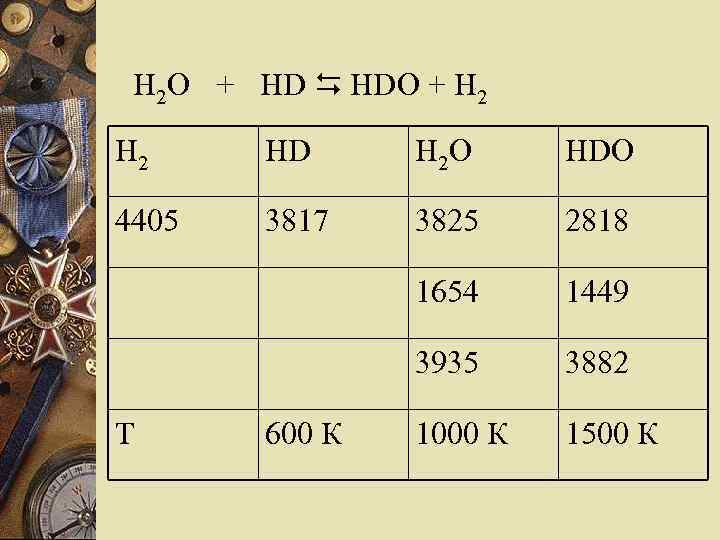
H 2 O + HD НDО + H 2 HD H 2 O НDО 4405 3817 3825 2818 1654 1449 3935 3882 1000 К 1500 К Т 600 К

§ 4. РАСЧЕТ КОЭФИЦИЕНТОВ РАЗДЕЛЕНИЯ В ИОНООБМЕННЫХ ПРОЦЕССАХ.

w Органические ионообменные смолы представляют собой полиэлектролиты. Трехмерная структурная сетка матрицы ионита поддерживает высокую концентрацию ионов внутри ионита (до 6 н) и создает давление внутри зерна ионообменника. В бинарной смеси ионов А и В коэффициент селективности ионита может быть записан в следующем виде: w (58)

w где — осмотическое давление в смоле; w -(VA-VB) — разность молярных объемов набухания смолы в форме иона А и В; w -( В/ А)R В/ А)S ( — отношение коэффициента активности ионов в ионите и растворе. w При изучении водных растворов электролитов обнаружена монотонная зависимость коэффициента активности кристаллохимических радиусов ионов, принадлежащих одной подгруппе таблицы Менделеева.

w Иониты являются смешанными растворами солей, участвующими в ионном обмене. Поэтому, если в пределах одной подгруппы периодической системы выберем ион сравнения, с которым производим обмен других ионов подгруппы, то получим монотонную зависимость коэффициента селективности от кристаллохимического радиуса ионов. w Такая зависимость для ионитов различной степени сшитости приведена на рисунке 3.
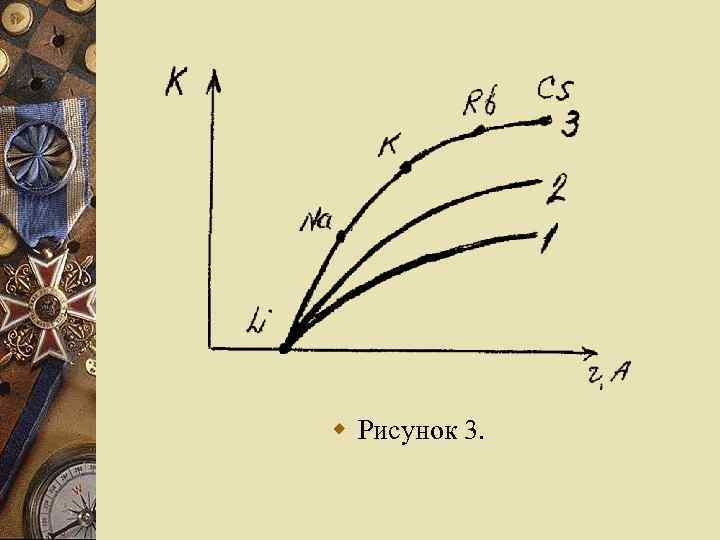
w Рисунок 3.

w Зависимость коэффициентов селективности ионов щелочных элементов от их кристаллических радиусов при обмене на ионите Дауэк 50 различной степени сшитости ( I- 4%, 2 - 8%, 3 - 16% дивинил—бензола). w На основании приведенных зависимостей можно перейти к расчету коэффициентов разделения изотопов в системе ионит-раствор.

w Обозначим коэффициенты селективности легкого и тяжелого w ионита по отношение к иону сравнены следующим образом: w ; (59) w где х. Л, х. Т, - мольные доли легкого, тяжелого изотопов и иона сравнения в фазе ионита, а х. Л*, х. Т*, *соответствующие величины для внешнего раствора.

w Тогда величина разделения запишется: w коэффициента (60) w Так коэффициент селективности является монотонной функцией кристаллохимических радиусов ионита, т. е. К=К(r) , то изменение радиуса на величину r приводит к изменению величины К на К: w К = К| (r) r (61)

w Отношение коэффициента селективности ионов, обладающего большим радиусом к коэффициенту иона, имеющего малый радиус, w запишется: w Выведем величину обогащения w (62) коэффициента

w Таким образом, для расчета коэффициента обогащения изотопов при наличии зависимости коэффициента селективности от их кристаллохимического радиуса необходимо графически определить величину производной, соответствующей рассматриваемому элементу и знать разность кристаллохимических радиусов разделяемых изотопов.

Литература. w I. А. И. Бродский. Химия изотопов. М. , Изд-во АН СССР, 1957. w 2. Н. И. Годнев. Вычисление термодинамических функций по молекулярным данным. М. , ГИТТЛ, 1956. w 3. Г. Юри. Термодинамика реакции изотопного обмена. w 4. В. М. Таевский. Ж. Ф. Х. , 25, 261, 1951.

w 5. Е. Н. Ерёмин. Основы химической термодинамики, М. , 1974. w 6. A. M. Розен. Теория разделения изотопов в колоннах. М. , Aтoмиздат, I 960. w 7. Гвардцителли И. Г. , Николаев Ю. В. , Озиашвили Е. Д. и др. Атомная энергия. 1961, Т. 10, с. 487. w 8. Кузнецова Е. М. , Панченков Г. М. , Филиппова Р. С. Жур. физ. химии, I 960, Т. 34. с. 2370.

w 9. Стельцов Л. B. , Жаворонков Н. М. , Гумениюк Т. Д. и др. Химическая промышленность, 1974, № 3, с. 221. w 10. Горшков В. И. , Епифанова С. С. , Сафонов М. С. Журнал физической химии, 1971. Т. 45, с. 732. w 11. Жаворонков Н. М. , Князев Д. А. , Ивлев А. А. и др. Успехи химии, | 1980, Т. 49, № 3, с. 385. w 12» Тихомиров И. А. , Ворошилов С. П. , Вергун А. П. Журнал физической химии, 44, 1021, 1980.

w 13. Тихомиров И. А. , Ворошилов С. П. , Вергун А. П. Журнал физической химии, 44, 1870, 1980. w 14. Тихомиров И. А. , Ворошилов С. П. , Вергун А. П. , Сафонова Г. Д. Журнал физической химии, 46, 1283, 1982. w 15. Б. М. Андреев, Я. Д. Зельвенский, С. Г. Катальникова. Разделение стабильных изотопов физико-химическими методами, М. , Энергоатомиздат, 1982.

w 16. Тихомиров И. А. , Вергун А. П. , Тихонов Г. С. Доклад на Международной научно-практической конференции "Технический университет: реформы в обществе и открытое образовательное пространство". Тезисы доклада. г. Томск, ТПУ, 1996. с. 115.

w 17. Тихомиров И. А. , Вергун А. П. , Тихонов Г. С. Учебно—методическое пособие "Формирование учебнонаучного и тренировочного центра по процессам разделения изотопов и тонкой очистке веществ”. Томск, ТПУ, 1998. Регистрационный № 98.

w 18. Вергун А. П. "Построение математических моделей процессов разделения изотопов и тонкой очистки веществ методами планирования экстремальных экспериментов”, г. Томcк, ТПУ, Регистрационный № 5 от 19. 01. 2000 г.
РАСЧЕТЫ КОЭФФИЦИЕНТОВ РАЗДЕЛЕНИЯ.ppt