Рак тела матки практич занятие .ppt
- Количество слайдов: 170
 РАК ТЕЛА МАТКИ ЛИТВИНОВА Т. М. Доктор медицинских наук, доцент
РАК ТЕЛА МАТКИ ЛИТВИНОВА Т. М. Доктор медицинских наук, доцент
 Рак тела матки • 2 -я по частоте опухоль женских половых органов в мире после рака шейки матки • Самая частая опухоль женских половых органов в развитых странах • Заболеваемость в развитых странах почти в 10 раз выше, чем в развивающихся
Рак тела матки • 2 -я по частоте опухоль женских половых органов в мире после рака шейки матки • Самая частая опухоль женских половых органов в развитых странах • Заболеваемость в развитых странах почти в 10 раз выше, чем в развивающихся
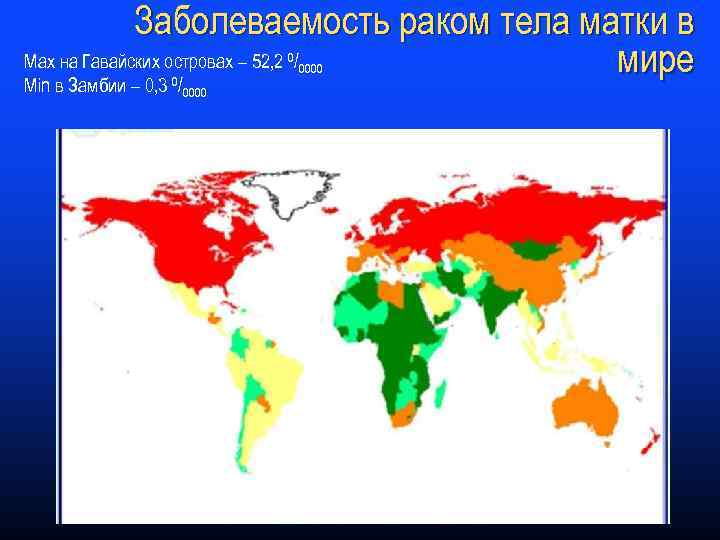 Заболеваемость раком тела матки в Max на Гавайских островах – 52, 2 / мире Min в Замбии – 0, 3 / 0 0 0000
Заболеваемость раком тела матки в Max на Гавайских островах – 52, 2 / мире Min в Замбии – 0, 3 / 0 0 0000
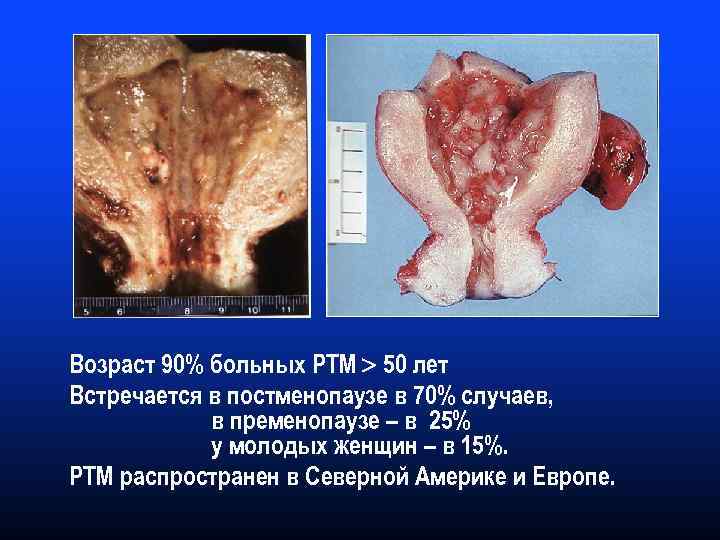 Возраст 90% больных РТМ 50 лет Встречается в постменопаузе в 70% случаев, в пременопаузе – в 25% у молодых женщин – в 15%. РТМ распространен в Северной Америке и Европе.
Возраст 90% больных РТМ 50 лет Встречается в постменопаузе в 70% случаев, в пременопаузе – в 25% у молодых женщин – в 15%. РТМ распространен в Северной Америке и Европе.
 Рак тела матки q Заболеваемость в развитых странах – выросла на 15, 1% (за последние 5 лет) • 1 -е место среди опухолей органов репродуктивной сферы • 10 -е место среди злокачественных опухолей у женщин • средний возраст больных 60 -62 года q Причины роста РШМ: – увеличение • средней продолжительности жизни женщин • числа пациенток, страдающих ожирением, сахарным диабетом и заболеваниями сердечно-сосудистой системы
Рак тела матки q Заболеваемость в развитых странах – выросла на 15, 1% (за последние 5 лет) • 1 -е место среди опухолей органов репродуктивной сферы • 10 -е место среди злокачественных опухолей у женщин • средний возраст больных 60 -62 года q Причины роста РШМ: – увеличение • средней продолжительности жизни женщин • числа пациенток, страдающих ожирением, сахарным диабетом и заболеваниями сердечно-сосудистой системы
 Смертность от рака тела матки По смертности – 7 место; 1 -2% от всех раковых заболеваний
Смертность от рака тела матки По смертности – 7 место; 1 -2% от всех раковых заболеваний
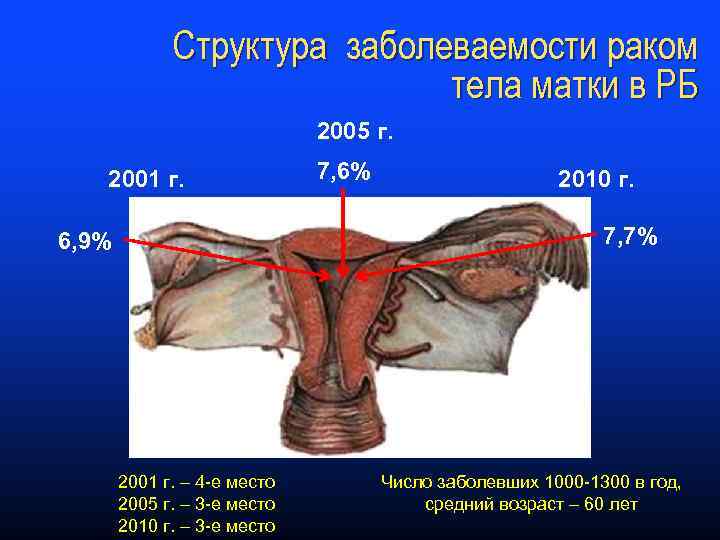 Структура заболеваемости раком тела матки в РБ 2005 г. 2001 г. 7, 6% 2010 г. 7, 7% 6, 9% 2001 г. – 4 -е место 2005 г. – 3 -е место 2010 г. – 3 -е место Число заболевших 1000 -1300 в год, средний возраст – 60 лет
Структура заболеваемости раком тела матки в РБ 2005 г. 2001 г. 7, 6% 2010 г. 7, 7% 6, 9% 2001 г. – 4 -е место 2005 г. – 3 -е место 2010 г. – 3 -е место Число заболевших 1000 -1300 в год, средний возраст – 60 лет
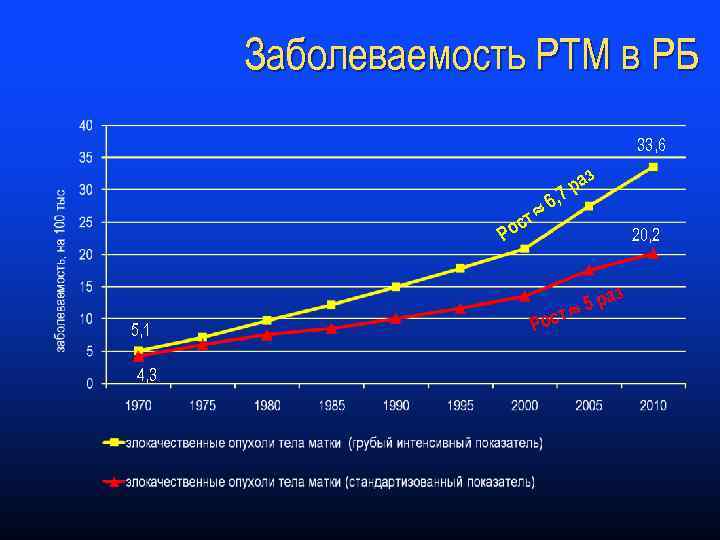 Заболеваемость РТМ в РБ 33, 6 т с Ро 6, з ра 7 20, 2 з 5, 1 4, 3 5 ра ост Р
Заболеваемость РТМ в РБ 33, 6 т с Ро 6, з ра 7 20, 2 з 5, 1 4, 3 5 ра ост Р
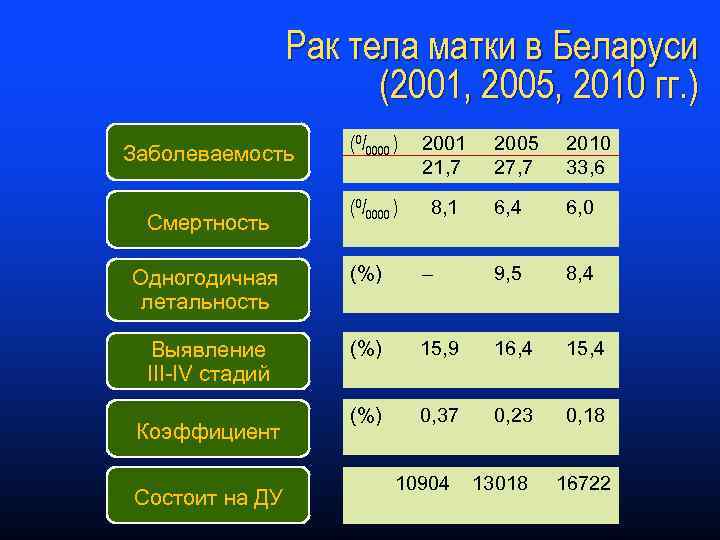 Рак тела матки в Беларуси (2001, 2005, 2010 гг. ) (0/0000 ) 2001 21, 7 2005 27, 7 2010 33, 6 (0/0000 ) 8, 1 6, 4 6, 0 Одногодичная летальность (%) – 9, 5 8, 4 Выявление III-IV стадий (%) 15, 9 16, 4 15, 4 (%) 0, 37 0, 23 0, 18 Заболеваемость Смертность Коэффициент Состоит на ДУ 10904 13018 16722
Рак тела матки в Беларуси (2001, 2005, 2010 гг. ) (0/0000 ) 2001 21, 7 2005 27, 7 2010 33, 6 (0/0000 ) 8, 1 6, 4 6, 0 Одногодичная летальность (%) – 9, 5 8, 4 Выявление III-IV стадий (%) 15, 9 16, 4 15, 4 (%) 0, 37 0, 23 0, 18 Заболеваемость Смертность Коэффициент Состоит на ДУ 10904 13018 16722
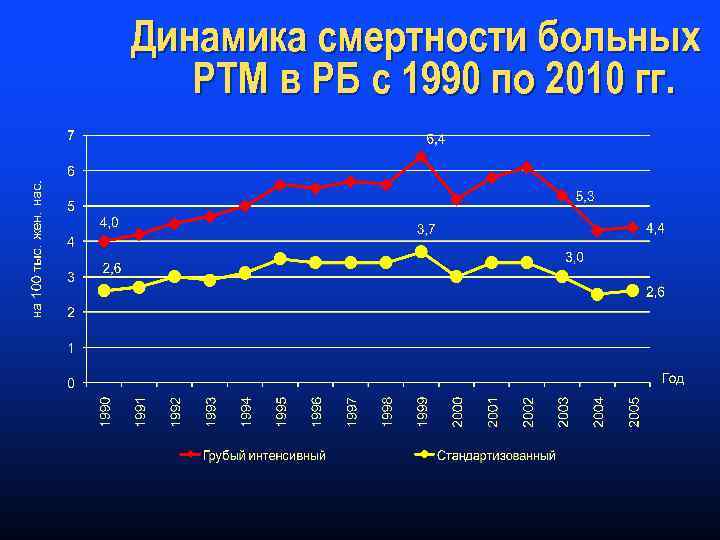 Динамика смертности больных РТМ в РБ с 1990 по 2010 гг.
Динамика смертности больных РТМ в РБ с 1990 по 2010 гг.
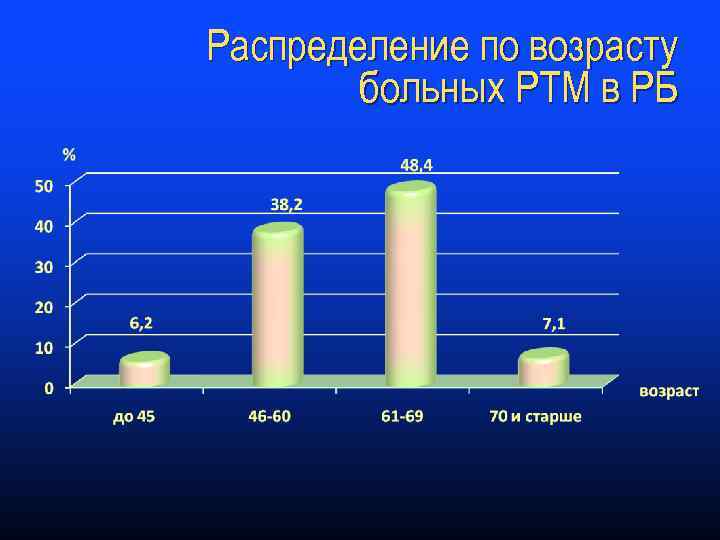 Распределение по возрасту больных РТМ в РБ
Распределение по возрасту больных РТМ в РБ
 Повозрастные показатели заболеваемости раком тела матки женщин РБ в 2010 г. 0/ 0000
Повозрастные показатели заболеваемости раком тела матки женщин РБ в 2010 г. 0/ 0000
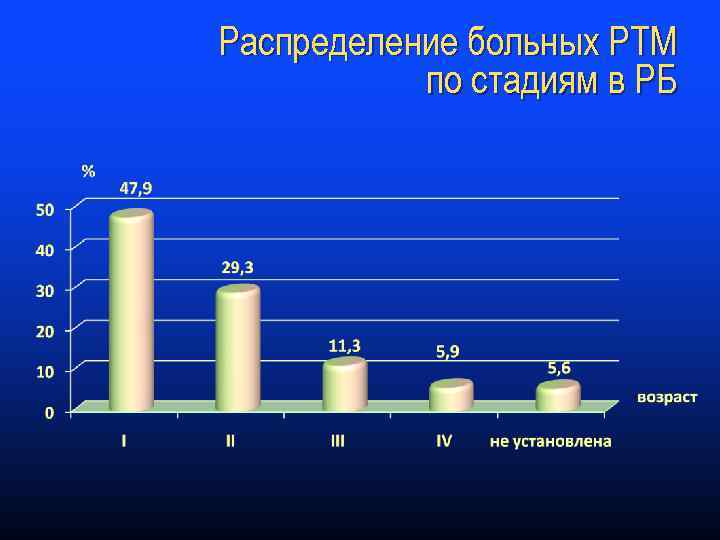 Распределение больных РТМ по стадиям в РБ
Распределение больных РТМ по стадиям в РБ
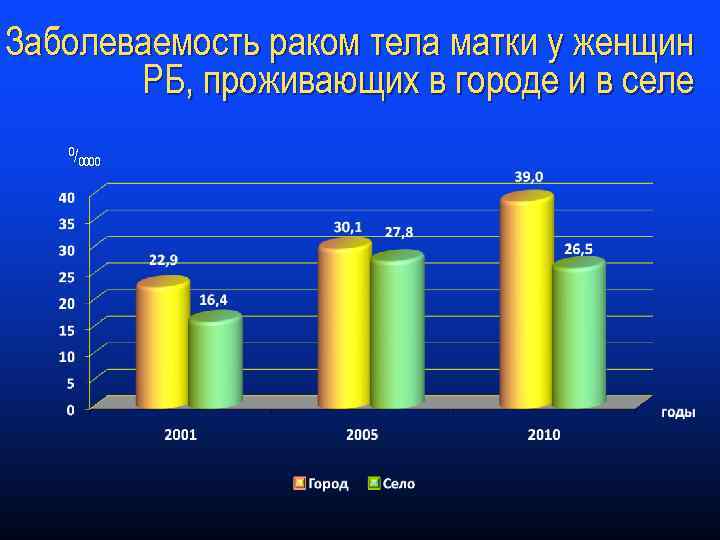 Заболеваемость раком тела матки у женщин РБ, проживающих в городе и в селе 0/ 0000
Заболеваемость раком тела матки у женщин РБ, проживающих в городе и в селе 0/ 0000
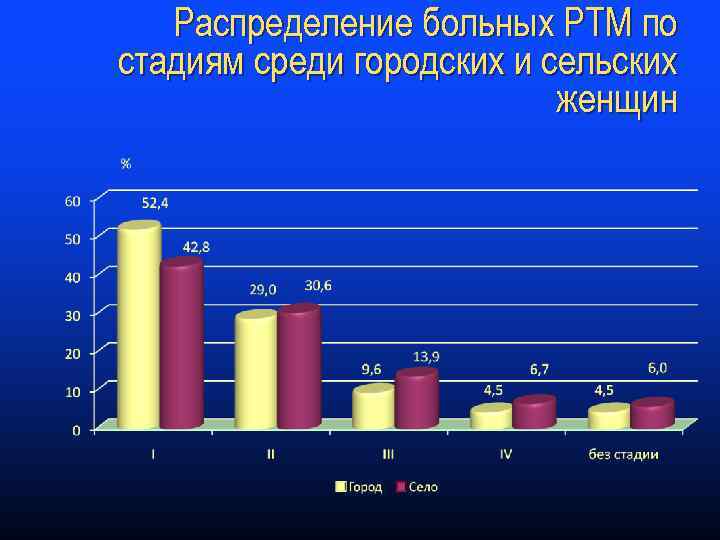 Распределение больных РТМ по стадиям среди городских и сельских женщин
Распределение больных РТМ по стадиям среди городских и сельских женщин
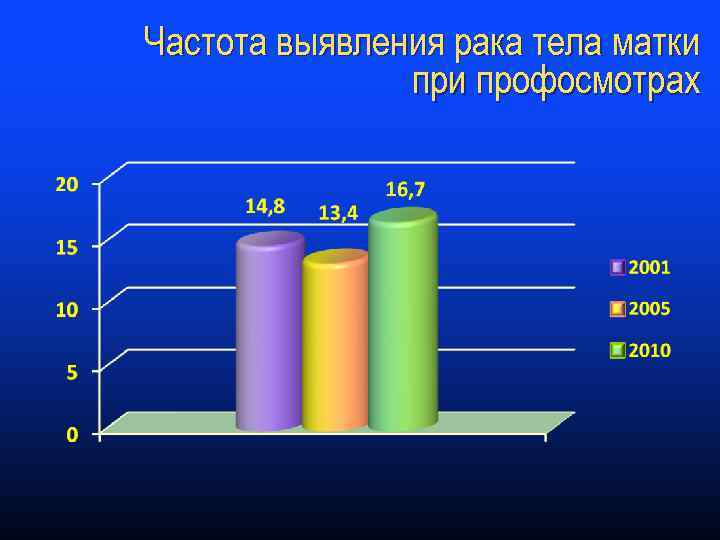 Частота выявления рака тела матки профосмотрах
Частота выявления рака тела матки профосмотрах
 Скрининг ü Нет методов, пригодных для популяционного скрининга ü Для оппортунистического и селективного скрининга можно использовать цитологию и УЗИ ü У 70 -80% больных распространенность опухоли соответствует I-II стадиям Опухоль растет достаточно медленно, поэтому отсутствие скрининга мало влияет на выживаемость больных
Скрининг ü Нет методов, пригодных для популяционного скрининга ü Для оппортунистического и селективного скрининга можно использовать цитологию и УЗИ ü У 70 -80% больных распространенность опухоли соответствует I-II стадиям Опухоль растет достаточно медленно, поэтому отсутствие скрининга мало влияет на выживаемость больных
 Факторы риска
Факторы риска
 Клинико-генетические признаки РТМ ü Отягощенный семейный анамнез (3 случая РТМ и более у родственников I степени) ü Вертикальная передача заболевания ü Наличие в семье первично-множественных опухолей ü Более молодой возраст у родственников, имеющих РТМ ü Благоприятное течение опухолевого процесса ü Наличие наследственного синдрома
Клинико-генетические признаки РТМ ü Отягощенный семейный анамнез (3 случая РТМ и более у родственников I степени) ü Вертикальная передача заболевания ü Наличие в семье первично-множественных опухолей ü Более молодой возраст у родственников, имеющих РТМ ü Благоприятное течение опухолевого процесса ü Наличие наследственного синдрома
 Рак тела матки имеет мультифакториальную природу, т. е. в его возникновении играют роль как эндогенные (гормональные и генетические), так и экзогенные (внешнесредовые) факторы
Рак тела матки имеет мультифакториальную природу, т. е. в его возникновении играют роль как эндогенные (гормональные и генетические), так и экзогенные (внешнесредовые) факторы
 Синдром Линча тип II (аутосомо-доминантный синдром) Наследственный рак толстой кишки без полипоза + рак яичников + тела матки + рак молочной железы. Синдром вызывают генеративные мутации одного из 5 генов MLH 1, MSH 2, MSH 3, PMS 1 и PMS 2, которые участвуют в репарации неправильно спаренных нуклеотидов ДНК. Риск развития рака толстой кишки – 39 -54% РТМ – 30 -61%, который возникает у женщин в 40 -45 лет (до рака толстой кишки). В 10 -20% случаев РТМ имеют место мутации онкогена K-RAS 2 и суперэкспрессия онкогена – BRСА 1 (при наличии метастазов).
Синдром Линча тип II (аутосомо-доминантный синдром) Наследственный рак толстой кишки без полипоза + рак яичников + тела матки + рак молочной железы. Синдром вызывают генеративные мутации одного из 5 генов MLH 1, MSH 2, MSH 3, PMS 1 и PMS 2, которые участвуют в репарации неправильно спаренных нуклеотидов ДНК. Риск развития рака толстой кишки – 39 -54% РТМ – 30 -61%, который возникает у женщин в 40 -45 лет (до рака толстой кишки). В 10 -20% случаев РТМ имеют место мутации онкогена K-RAS 2 и суперэкспрессия онкогена – BRСА 1 (при наличии метастазов).
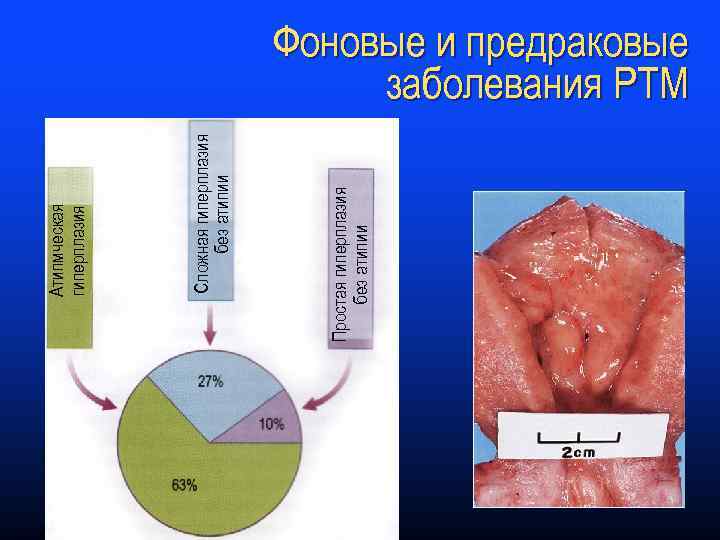 Простая гиперплазия без атипии Сложная гиперплазия без атипии Атипмческая гиперплазия Фоновые и предраковые заболевания РТМ
Простая гиперплазия без атипии Сложная гиперплазия без атипии Атипмческая гиперплазия Фоновые и предраковые заболевания РТМ
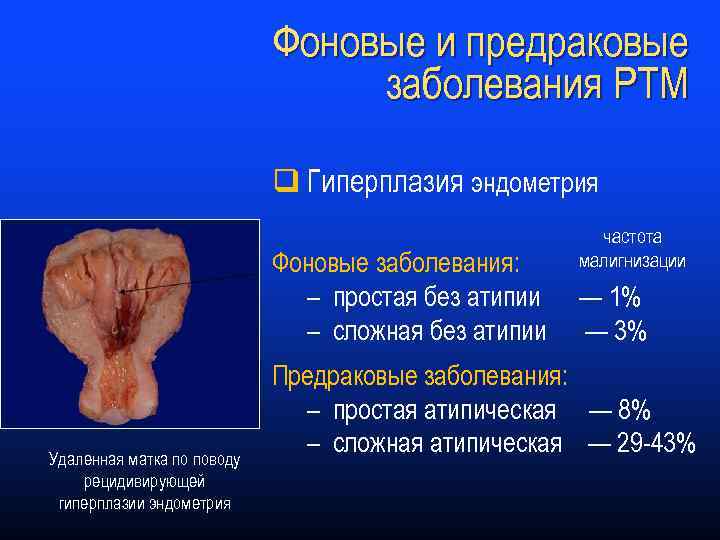 Фоновые и предраковые заболевания РТМ q Гиперплазия эндометрия частота малигнизации Фоновые заболевания: – простая без атипии — 1% – сложная без атипии — 3% Удаленная матка по поводу рецидивирующей гиперплазии эндометрия Предраковые заболевания: – простая атипическая — 8% – сложная атипическая — 29 -43%
Фоновые и предраковые заболевания РТМ q Гиперплазия эндометрия частота малигнизации Фоновые заболевания: – простая без атипии — 1% – сложная без атипии — 3% Удаленная матка по поводу рецидивирующей гиперплазии эндометрия Предраковые заболевания: – простая атипическая — 8% – сложная атипическая — 29 -43%
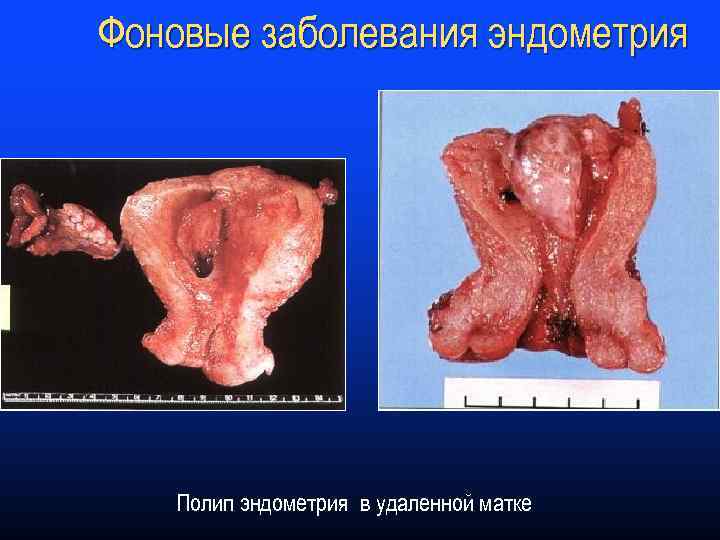 Фоновые заболевания эндометрия Полип эндометрия в удаленной матке
Фоновые заболевания эндометрия Полип эндометрия в удаленной матке
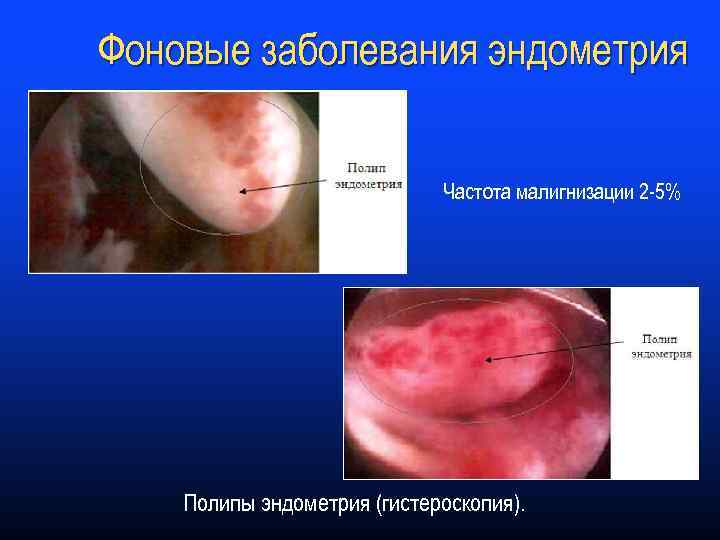 Фоновые заболевания эндометрия Частота малигнизации 2 -5% Полипы эндометрия (гистероскопия).
Фоновые заболевания эндометрия Частота малигнизации 2 -5% Полипы эндометрия (гистероскопия).
 Этиология и патогенез q Рак тела матки — гормонально-зависимая опухоль (наличие длительной гиперэстрогении) q Патогенетические варианты (Я. В. Бохман, 1972) – I патогенетический вариант (60 -70%) – II патогенетический вариант (30 -40%)
Этиология и патогенез q Рак тела матки — гормонально-зависимая опухоль (наличие длительной гиперэстрогении) q Патогенетические варианты (Я. В. Бохман, 1972) – I патогенетический вариант (60 -70%) – II патогенетический вариант (30 -40%)
 Клиника РТМ в зависимости от патогенеза Показатели Клиника Продолжительность симптомов Степень дифференцировки РТМ Инвазия в миометрий Чувствительность к прогестагенам Первично-множественная опухоль Прогноз I патогенетический вариант II патогенетический вариант Кровянистые выделения Нет Длительная Короткая Высокая (I и II) Снижена (III и IV) Небольшая Высокая Низкая Яичники, молочная железа, толстая кишка Нет Благоприятный Сомнительный
Клиника РТМ в зависимости от патогенеза Показатели Клиника Продолжительность симптомов Степень дифференцировки РТМ Инвазия в миометрий Чувствительность к прогестагенам Первично-множественная опухоль Прогноз I патогенетический вариант II патогенетический вариант Кровянистые выделения Нет Длительная Короткая Высокая (I и II) Снижена (III и IV) Небольшая Высокая Низкая Яичники, молочная железа, толстая кишка Нет Благоприятный Сомнительный
 I патогенетический вариант (гормональный) q Характеризуется: – хронической гиперэстрогенией; – нарушением жирового обмена; – нарушением углеводного обмена.
I патогенетический вариант (гормональный) q Характеризуется: – хронической гиперэстрогенией; – нарушением жирового обмена; – нарушением углеводного обмена.
 – ановуляторное маточное кровотечение – бесплодие – поздняя менопауза (после 50 лет) – гиперплазия тека-ткани яичников – поликистоз яичников – феминизирующие опухоли яичников – миома – эндометриоз – гиперплазия эндометрия – полип эндометрия – ожирение – сахарный диабет – гипертоническая болезнь – ишемическая болезнь сердца Клиника
– ановуляторное маточное кровотечение – бесплодие – поздняя менопауза (после 50 лет) – гиперплазия тека-ткани яичников – поликистоз яичников – феминизирующие опухоли яичников – миома – эндометриоз – гиперплазия эндометрия – полип эндометрия – ожирение – сахарный диабет – гипертоническая болезнь – ишемическая болезнь сердца Клиника
 II патогенетический вариант (автономный) q Характеризуется отсутствием: – хронической гиперэстрогении; – нарушения жирового обмена; – нарушения углеводного обмена.
II патогенетический вариант (автономный) q Характеризуется отсутствием: – хронической гиперэстрогении; – нарушения жирового обмена; – нарушения углеводного обмена.
 Клиника (1) – менструальная функция не нарушена – менопауза до 50 лет – атрофия эндометрия – фиброз стромы яичников – иммунодепрессия – мутации в гене р53 – потеря зиготности в нескольких хромосомных локусах – быстрое разростание – плохой прогноз – молекулярная перестройка в отдельных генах
Клиника (1) – менструальная функция не нарушена – менопауза до 50 лет – атрофия эндометрия – фиброз стромы яичников – иммунодепрессия – мутации в гене р53 – потеря зиготности в нескольких хромосомных локусах – быстрое разростание – плохой прогноз – молекулярная перестройка в отдельных генах
 Клиника (2) Отсутствуют: – феминизирующие опухоли яичников – миома – эндометриоз – гиперплазия эндометрия – полип эндометрия – ожирение – сахарный диабет – гипертоническая болезнь – ишемическая болезнь сердца
Клиника (2) Отсутствуют: – феминизирующие опухоли яичников – миома – эндометриоз – гиперплазия эндометрия – полип эндометрия – ожирение – сахарный диабет – гипертоническая болезнь – ишемическая болезнь сердца
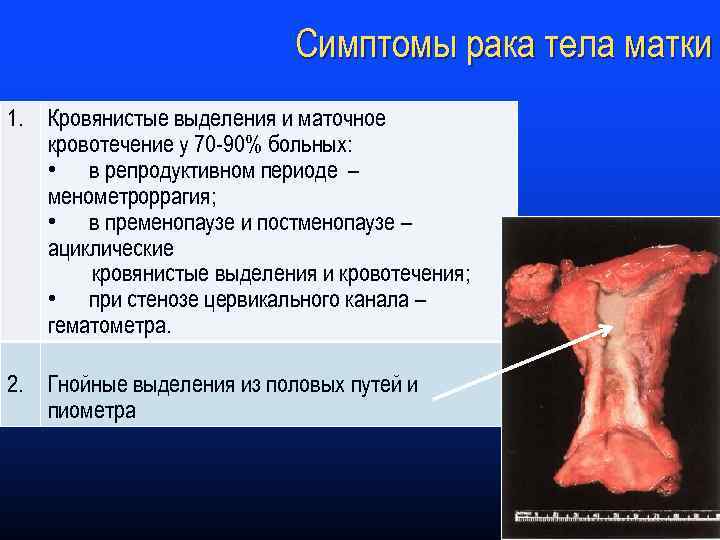 Симптомы рака тела матки 1. Кровянистые выделения и маточное кровотечение у 70 -90% больных: • в репродуктивном периоде – менометроррагия; • в пременопаузе и постменопаузе – ациклические кровянистые выделения и кровотечения; • при стенозе цервикального канала – гематометра. 2. Гнойные выделения из половых путей и пиометра
Симптомы рака тела матки 1. Кровянистые выделения и маточное кровотечение у 70 -90% больных: • в репродуктивном периоде – менометроррагия; • в пременопаузе и постменопаузе – ациклические кровянистые выделения и кровотечения; • при стенозе цервикального канала – гематометра. 2. Гнойные выделения из половых путей и пиометра
 Симптомы рака тела матки 3. Боли: • схваткообразные – при скоплении крови, серозной жидкости и гноя в полости матки; • тупые – при поражении нервных стволов, метастазах в лимфатических узлах. 4. Жалоб нет у 5% больных I-II стадии рака диагностируются в Беларуси у 80, 3% (I – 66, 5%, II- 13, 8%; III-IV – 19, 7%)
Симптомы рака тела матки 3. Боли: • схваткообразные – при скоплении крови, серозной жидкости и гноя в полости матки; • тупые – при поражении нервных стволов, метастазах в лимфатических узлах. 4. Жалоб нет у 5% больных I-II стадии рака диагностируются в Беларуси у 80, 3% (I – 66, 5%, II- 13, 8%; III-IV – 19, 7%)
 Кровянистые выделения из половых путей Причина Атрофия эндометрия Заместительная гормональная терапия Полип эндометрия Гиперплазия эндометрия Рак тела матки q Вероятность того, что кровотечение в постменопаузе обусловлено раком тела матки ü 50 лет — 9% ü 60 лет — 16% ü 70 лет — 28% ü 80 лет и старше — 60%
Кровянистые выделения из половых путей Причина Атрофия эндометрия Заместительная гормональная терапия Полип эндометрия Гиперплазия эндометрия Рак тела матки q Вероятность того, что кровотечение в постменопаузе обусловлено раком тела матки ü 50 лет — 9% ü 60 лет — 16% ü 70 лет — 28% ü 80 лет и старше — 60%
 Эндометриальный рак: 1) эндометриоидный рак Патоморфология • Аденокарцинома G 1, G 2, G 3 (80% больных) – аденокарцинома с плоскоклеточной метаплазией (20% случаев)
Эндометриальный рак: 1) эндометриоидный рак Патоморфология • Аденокарцинома G 1, G 2, G 3 (80% больных) – аденокарцинома с плоскоклеточной метаплазией (20% случаев)
 2) неэндометриоидный рак Патоморфология • Прогностически неблагоприятные гистологические типы (15% больных) – плоскоклеточный рак – светлоклеточный рак – папиллярный серозный рак – недифференцированный рак – карциносаркома – муцинозный рак – мелкоклеточный рак – смешанноклеточный рак
2) неэндометриоидный рак Патоморфология • Прогностически неблагоприятные гистологические типы (15% больных) – плоскоклеточный рак – светлоклеточный рак – папиллярный серозный рак – недифференцированный рак – карциносаркома – муцинозный рак – мелкоклеточный рак – смешанноклеточный рак
 Обследование больных раком тела матки в ЖК 1. Анамнез. 2. Общий осмотр + молочные железы. 3. Осмотр женских половых органов (в зеркалах, вагинальный и ректовагинальный) 4. Эхоскопия органов малого таза и брюшной полости и забрюшинного пространства. 5. Аспират из полости матки для цитологического исследования. 6. Гистероскопия (при наличии гистероскопа) с прицельной биопсией. 7. Раздельное диагностическое выскабливание слизистых цервикального канала и полости матки. 8. Рентгенография легких.
Обследование больных раком тела матки в ЖК 1. Анамнез. 2. Общий осмотр + молочные железы. 3. Осмотр женских половых органов (в зеркалах, вагинальный и ректовагинальный) 4. Эхоскопия органов малого таза и брюшной полости и забрюшинного пространства. 5. Аспират из полости матки для цитологического исследования. 6. Гистероскопия (при наличии гистероскопа) с прицельной биопсией. 7. Раздельное диагностическое выскабливание слизистых цервикального канала и полости матки. 8. Рентгенография легких.
 Эхоскопия рака тела матки Метод позволяет: l оценить размеры первичной опухоли, ее форму, структуру, локализацию и глубину инвазии в миометрий, наличие сосудов в опухоли; l определить местную распространенность процесса на шейку и яичники; l выявить регионарные и отдаленные метастазы. Информативность трансвагинального УЗИ выше трансабдоминального при осмотре матки с придатками. Для оценки лимфоузлов и большого сальника показано абдоминальное УЗИ. Если невозможно выполнить трансвагинальное УЗИ, то выполняется трансректальное.
Эхоскопия рака тела матки Метод позволяет: l оценить размеры первичной опухоли, ее форму, структуру, локализацию и глубину инвазии в миометрий, наличие сосудов в опухоли; l определить местную распространенность процесса на шейку и яичники; l выявить регионарные и отдаленные метастазы. Информативность трансвагинального УЗИ выше трансабдоминального при осмотре матки с придатками. Для оценки лимфоузлов и большого сальника показано абдоминальное УЗИ. Если невозможно выполнить трансвагинальное УЗИ, то выполняется трансректальное.
 Показания к трансректальному УЗИ 1) маточное кровотечение; 2) кровотечение вследствие распадающейся опухоли экзо- и эндоцервикса; 3) сужение преддверия влагалища после предшествующих хирургических вмешательств; 4) аномалии развития половых органов (заращение влагалища, перегородки влагалища); 5) пациентки, не живущие половой жизнью; 6) ретропозиция матки в полости таза (retroversio, retroflexio); 7) ожирение III степени и выраженный рубцовоспаечный процесс в малом тазу.
Показания к трансректальному УЗИ 1) маточное кровотечение; 2) кровотечение вследствие распадающейся опухоли экзо- и эндоцервикса; 3) сужение преддверия влагалища после предшествующих хирургических вмешательств; 4) аномалии развития половых органов (заращение влагалища, перегородки влагалища); 5) пациентки, не живущие половой жизнью; 6) ретропозиция матки в полости таза (retroversio, retroflexio); 7) ожирение III степени и выраженный рубцовоспаечный процесс в малом тазу.
 Ведущие эхографические симптомы: 1. Толщина М-эхо ( 4 мм). 2. Эхоструктура эндометрия l неоднородность внутренней структуры опухоли; l неровность контуров; l более высокая эхогенность, чем миометрия; l большие размеры образования; l наличие жидкостных включений; l рост образования при динамическом наблюдении; l отсутствие четких контуров матки из-за прорастания опухолью смежных органов. 3. Инвазия опухоли в миометрий. 4. Наличие внутриопухолевого кровотока у 90% больных при допплерометрии.
Ведущие эхографические симптомы: 1. Толщина М-эхо ( 4 мм). 2. Эхоструктура эндометрия l неоднородность внутренней структуры опухоли; l неровность контуров; l более высокая эхогенность, чем миометрия; l большие размеры образования; l наличие жидкостных включений; l рост образования при динамическом наблюдении; l отсутствие четких контуров матки из-за прорастания опухолью смежных органов. 3. Инвазия опухоли в миометрий. 4. Наличие внутриопухолевого кровотока у 90% больных при допплерометрии.
 Этапы комплексного УЗИ рака тела матки I – трансабдоминальное сканирование органов малого таза в режиме серой шкалы и реального времени; II – трансвагинальное УЗИ в режиме реального времени; III – цветное допплеровское картирование; IV – допплерометрия.
Этапы комплексного УЗИ рака тела матки I – трансабдоминальное сканирование органов малого таза в режиме серой шкалы и реального времени; II – трансвагинальное УЗИ в режиме реального времени; III – цветное допплеровское картирование; IV – допплерометрия.
 III и IV этапы комплексного УЗИ Цель: определить наличие сосудов в опухоли и локализацию артерий с расчетом их гемодинамических показателей. У 90% больных РТМ встречаются 3 типа внутриопухолевого кровотока: Ø «бедный кровоток» – до 4 сосудистых локусов; Ø «средний кровоток» – 5 -8 локусов; Ø «выраженный кровоток» – 8 локусов.
III и IV этапы комплексного УЗИ Цель: определить наличие сосудов в опухоли и локализацию артерий с расчетом их гемодинамических показателей. У 90% больных РТМ встречаются 3 типа внутриопухолевого кровотока: Ø «бедный кровоток» – до 4 сосудистых локусов; Ø «средний кровоток» – 5 -8 локусов; Ø «выраженный кровоток» – 8 локусов.
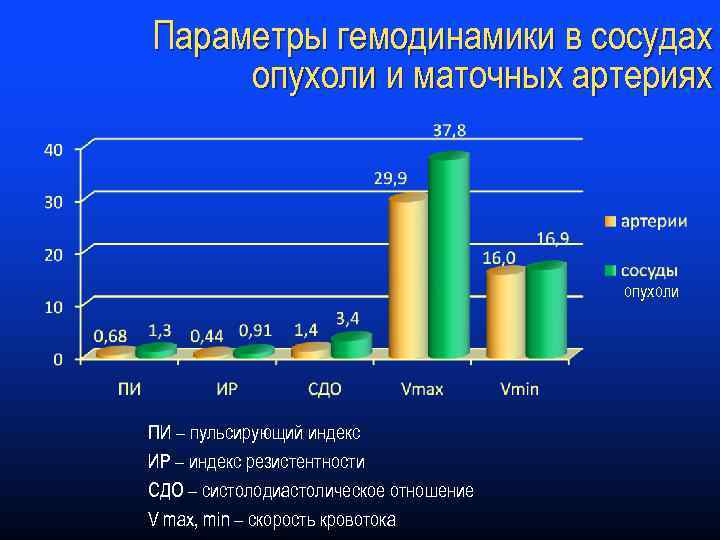 Параметры гемодинамики в сосудах опухоли и маточных артериях опухоли ПИ – пульсирующий индекс ИР – индекс резистентности СДО – систолодиастолическое отношение V max, min – скорость кровотока
Параметры гемодинамики в сосудах опухоли и маточных артериях опухоли ПИ – пульсирующий индекс ИР – индекс резистентности СДО – систолодиастолическое отношение V max, min – скорость кровотока
 Информативность сонографии при РТМ у женщин различных возрастных групп Репродуктивный период 48, 3% Перименопауза 56, 8% Постменопауза СОНОГРАФИЯ 97, 1% Точность – 96, 5% Чувствительность – 90, 9% Специфичность – 92, 3%
Информативность сонографии при РТМ у женщин различных возрастных групп Репродуктивный период 48, 3% Перименопауза 56, 8% Постменопауза СОНОГРАФИЯ 97, 1% Точность – 96, 5% Чувствительность – 90, 9% Специфичность – 92, 3%
 Диагностика • Морфологическое и цитологическое подтверждение диагноза – Аспирационная биопсия слизистой и цервикального канала – Гистероскопия с прицельной биопсией – Соскоб слизистой матки и цервикального канала
Диагностика • Морфологическое и цитологическое подтверждение диагноза – Аспирационная биопсия слизистой и цервикального канала – Гистероскопия с прицельной биопсией – Соскоб слизистой матки и цервикального канала
 Аспирационная биопсия Цель: получить содержимое из полости матки для цитологического исследования а б в г а – шприц Брауна; б – подключичный катетер с проводником; в – маточный шприц в собранном состоянии; г – маточный шприц с обрезанным наконечником Маточный шприц увеличивает выявление числа женщин с патологией эндометрия с 72, 1% до 95, 7%
Аспирационная биопсия Цель: получить содержимое из полости матки для цитологического исследования а б в г а – шприц Брауна; б – подключичный катетер с проводником; в – маточный шприц в собранном состоянии; г – маточный шприц с обрезанным наконечником Маточный шприц увеличивает выявление числа женщин с патологией эндометрия с 72, 1% до 95, 7%
 Аспирационная биопсия • в РБ в настоящее время для этой процедуры используется аспирационный зонд отечественного производства Зонд аспирационный
Аспирационная биопсия • в РБ в настоящее время для этой процедуры используется аспирационный зонд отечественного производства Зонд аспирационный
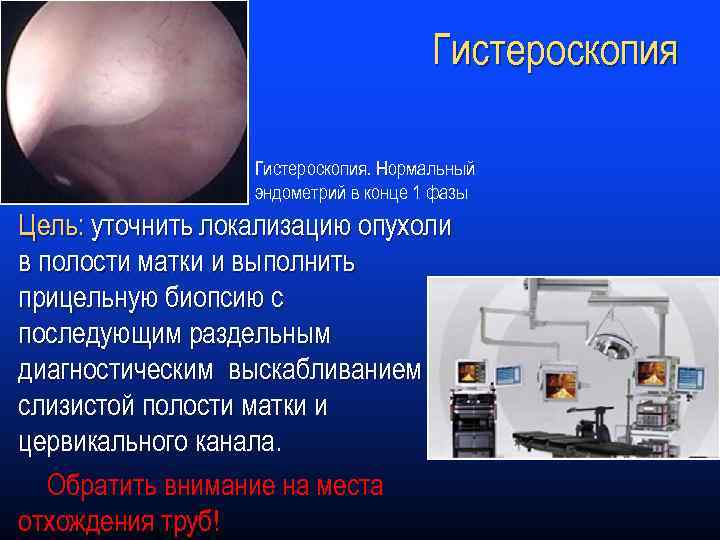 Гистероскопия. Нормальный эндометрий в конце 1 фазы Цель: уточнить локализацию опухоли в полости матки и выполнить прицельную биопсию с последующим раздельным диагностическим выскабливанием слизистой полости матки и цервикального канала. Обратить внимание на места отхождения труб!
Гистероскопия. Нормальный эндометрий в конце 1 фазы Цель: уточнить локализацию опухоли в полости матки и выполнить прицельную биопсию с последующим раздельным диагностическим выскабливанием слизистой полости матки и цервикального канала. Обратить внимание на места отхождения труб!
 Гистероскопия матки – уникальный метод, который позволяет: Взять биопсию для выявления РТМ • а также значительно расширить диагностические возможности при выявлении внутриматочных патологий; • разделить под контролем гистероскопа внутриматочные сращения, которые мешают наступлению беременности, и даже удалить миому матки, которая растет внутрь полости; • в ряде случаев избежать травмирующей процедуры выскабливания или взять биопсию только с подозрительного участка; • быстро выбрать способ лечения или скоррегировать тактику ведения больных, проводить контроль эффективности лечения и выполнять оперативные манипуляции.
Гистероскопия матки – уникальный метод, который позволяет: Взять биопсию для выявления РТМ • а также значительно расширить диагностические возможности при выявлении внутриматочных патологий; • разделить под контролем гистероскопа внутриматочные сращения, которые мешают наступлению беременности, и даже удалить миому матки, которая растет внутрь полости; • в ряде случаев избежать травмирующей процедуры выскабливания или взять биопсию только с подозрительного участка; • быстро выбрать способ лечения или скоррегировать тактику ведения больных, проводить контроль эффективности лечения и выполнять оперативные манипуляции.
 Гистероскопы
Гистероскопы
 Раздельное диагностическое выскабливание слизистых цервикального канала и полости матки Аппарат АПБ-02 для взятия вакуум-аспирата из полости матки У 84, 6% женщин удается выявить патологию эндометрия Длительность процедуры – 5, 2 1, 5 мин
Раздельное диагностическое выскабливание слизистых цервикального канала и полости матки Аппарат АПБ-02 для взятия вакуум-аспирата из полости матки У 84, 6% женщин удается выявить патологию эндометрия Длительность процедуры – 5, 2 1, 5 мин
 Обследование • Оценка общего состояния – общий анализ крови и мочи, биохимическое исследование крови, коагулограмма – допплеровское исследование вен нижних конечностей и подвздошных вен – ЭКГ – исследование функции внешнего дыхания
Обследование • Оценка общего состояния – общий анализ крови и мочи, биохимическое исследование крови, коагулограмма – допплеровское исследование вен нижних конечностей и подвздошных вен – ЭКГ – исследование функции внешнего дыхания
 Обследование • Первичная опухоль, местное распространение – физикальное исследование (гинекологическое исследование) – гистологический тип и степень дифференцировки (по представленным препаратам) – кольпоскопия (по показаниям) – УЗИ малого таза — глубина инвазии – МРТ малого таза – цистоскопия – ректороманоскопия – экскреторная урография • Регионарное распространение – УЗИ малого таза и забрюшинного пространства (метастазы в большом сальнике, лимфоузлах, печени) – экскреторная урография – КТ брюшной полости
Обследование • Первичная опухоль, местное распространение – физикальное исследование (гинекологическое исследование) – гистологический тип и степень дифференцировки (по представленным препаратам) – кольпоскопия (по показаниям) – УЗИ малого таза — глубина инвазии – МРТ малого таза – цистоскопия – ректороманоскопия – экскреторная урография • Регионарное распространение – УЗИ малого таза и забрюшинного пространства (метастазы в большом сальнике, лимфоузлах, печени) – экскреторная урография – КТ брюшной полости
 Обследование • Отдаленные метастазы – физикальное исследование (пальпация живота, паховых и шейных лимфатических узлов) – УЗИ органов брюшной полости – рентгенография грудной клетки – КТ грудной клетки и брюшной полости – определение уровня CA-125 в сыворотке – позитронно-эмиссионная томография (ПЭТ)
Обследование • Отдаленные метастазы – физикальное исследование (пальпация живота, паховых и шейных лимфатических узлов) – УЗИ органов брюшной полости – рентгенография грудной клетки – КТ грудной клетки и брюшной полости – определение уровня CA-125 в сыворотке – позитронно-эмиссионная томография (ПЭТ)
 Онкомаркеры рака тела матки HCE ферритин При РТМ в 1, 8 раза N При РТМ в 1, 6 раза N N – 7, 1 0, 7 нг/мл N – 60, 8 4, 8 нг/мл РТМ – 13, 1 1, 4 нг/мл РТМ – 100, 8 18, 2 нг/мл СА-125 У 22% больных I-II ст У 80% больных III-IV ст Mts в л/узлах N в л/узлах Mts в яичниках N в яичниках
Онкомаркеры рака тела матки HCE ферритин При РТМ в 1, 8 раза N При РТМ в 1, 6 раза N N – 7, 1 0, 7 нг/мл N – 60, 8 4, 8 нг/мл РТМ – 13, 1 1, 4 нг/мл РТМ – 100, 8 18, 2 нг/мл СА-125 У 22% больных I-II ст У 80% больных III-IV ст Mts в л/узлах N в л/узлах Mts в яичниках N в яичниках
 Онкомаркеры 1. Са-125 – опухолевый маркер, синтезируется в эндометрии, эндоцервиксе и эпителии маточных труб 2. HCE – изофермент, синтезируется нейронами и нейроэндокринными клетками ЦНС 3. Ферритин – белок с. Fe+ – подавляет активность иммунологической системы и усиливает опухолевый рост
Онкомаркеры 1. Са-125 – опухолевый маркер, синтезируется в эндометрии, эндоцервиксе и эпителии маточных труб 2. HCE – изофермент, синтезируется нейронами и нейроэндокринными клетками ЦНС 3. Ферритин – белок с. Fe+ – подавляет активность иммунологической системы и усиливает опухолевый рост
 МАТКА: ЭНДОМЕТРИЙ (ICD-0 С 54. 1; С 55) Определения категорий Т, N и М соответствуют стадиям FIGO. Для сравнения включены обе системы. Правила классификации Классификацию применяют к эндометриальным карциномам и карциносаркомам (злокачественные смешанные мезодермальные опухоли). Требуется гистологическое подтверждение новообразования и разделение по гистологическому типу с указанием гистологической степени злокачественности (Grade, G). Для определения категорий Т, N и М показано проведение следующих исследований: Категория Т физикальное обследование и лучевые методы исследования, включая урографию и цистоскопию Категория N физикальное обследование и лучевые методы исследования, включая урографию Категория М физикальное обследование и лучевые методы исследования
МАТКА: ЭНДОМЕТРИЙ (ICD-0 С 54. 1; С 55) Определения категорий Т, N и М соответствуют стадиям FIGO. Для сравнения включены обе системы. Правила классификации Классификацию применяют к эндометриальным карциномам и карциносаркомам (злокачественные смешанные мезодермальные опухоли). Требуется гистологическое подтверждение новообразования и разделение по гистологическому типу с указанием гистологической степени злокачественности (Grade, G). Для определения категорий Т, N и М показано проведение следующих исследований: Категория Т физикальное обследование и лучевые методы исследования, включая урографию и цистоскопию Категория N физикальное обследование и лучевые методы исследования, включая урографию Категория М физикальное обследование и лучевые методы исследования
 АНАТОМИЧЕСКИЕ ОТДЕЛЫ • • • Перешеек матки (С 54. 0) Дно матки (С 54. 3) Эндометрий (С 54. 1) РЕГИОНАЛЬНЫЕ ЛИМФАТИЧЕСКИЕ УЗЛЫ Региональными лимфатическими узлами являются тазовые [подчревные (внутренние подвздошные, запирательные), общие и наружные подвздошные, околоматочные и крестцовые] и околоаортальные узлы.
АНАТОМИЧЕСКИЕ ОТДЕЛЫ • • • Перешеек матки (С 54. 0) Дно матки (С 54. 3) Эндометрий (С 54. 1) РЕГИОНАЛЬНЫЕ ЛИМФАТИЧЕСКИЕ УЗЛЫ Региональными лимфатическими узлами являются тазовые [подчревные (внутренние подвздошные, запирательные), общие и наружные подвздошные, околоматочные и крестцовые] и околоаортальные узлы.
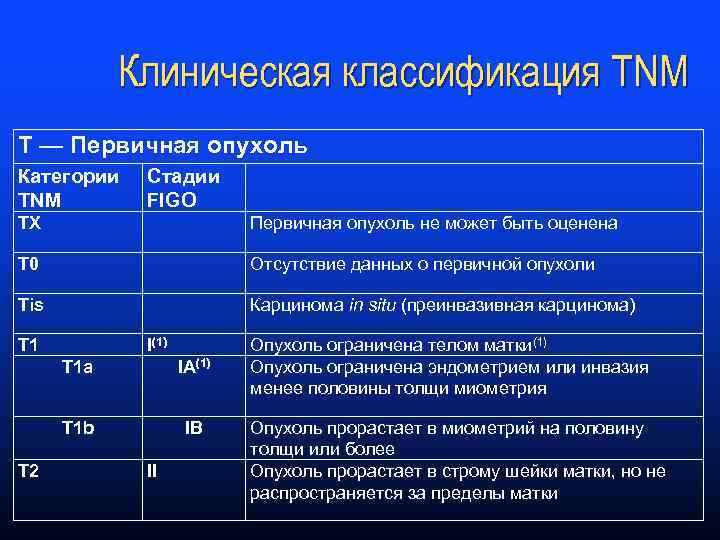 Клиническая классификация TNM Т — Первичная опухоль Категории TNM Стадии FIGO ТХ Первичная опухоль не может быть оценена Т 0 Отсутствие данных о первичной опухоли Tis Карцинома in situ (преинвазивная карцинома) T 1 I(1) T 1 a T 1 b T 2 IA(1) IB II Опухоль ограничена телом матки(1) Опухоль ограничена эндометрием или инвазия менее половины толщи миометрия Опухоль прорастает в миометрий на половину толщи или более Опухоль прорастает в строму шейки матки, но не распространяется за пределы матки
Клиническая классификация TNM Т — Первичная опухоль Категории TNM Стадии FIGO ТХ Первичная опухоль не может быть оценена Т 0 Отсутствие данных о первичной опухоли Tis Карцинома in situ (преинвазивная карцинома) T 1 I(1) T 1 a T 1 b T 2 IA(1) IB II Опухоль ограничена телом матки(1) Опухоль ограничена эндометрием или инвазия менее половины толщи миометрия Опухоль прорастает в миометрий на половину толщи или более Опухоль прорастает в строму шейки матки, но не распространяется за пределы матки
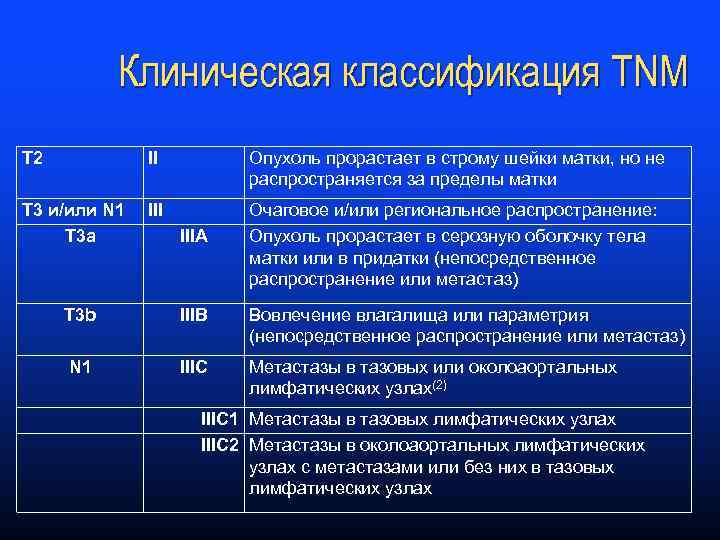 Клиническая классификация TNM T 2 II Опухоль прорастает в строму шейки матки, но не распространяется за пределы матки T 3 и/или N 1 T 3 a III Очаговое и/или региональное распространение: Опухоль прорастает в серозную оболочку тела матки или в придатки (непосредственное распространение или метастаз) IIIA T 3 b IIIB Вовлечение влагалища или параметрия (непосредственное распространение или метастаз) N 1 IIIC Метастазы в тазовых или околоаортальных лимфатических узлах(2) IIIC 1 Метастазы в тазовых лимфатических узлах IIIC 2 Метастазы в околоаортальных лимфатических узлах с метастазами или без них в тазовых лимфатических узлах
Клиническая классификация TNM T 2 II Опухоль прорастает в строму шейки матки, но не распространяется за пределы матки T 3 и/или N 1 T 3 a III Очаговое и/или региональное распространение: Опухоль прорастает в серозную оболочку тела матки или в придатки (непосредственное распространение или метастаз) IIIA T 3 b IIIB Вовлечение влагалища или параметрия (непосредственное распространение или метастаз) N 1 IIIC Метастазы в тазовых или околоаортальных лимфатических узлах(2) IIIC 1 Метастазы в тазовых лимфатических узлах IIIC 2 Метастазы в околоаортальных лимфатических узлах с метастазами или без них в тазовых лимфатических узлах
 Клиническая классификация TNM T 4 IVA M 1(4) Опухоль прорастает в слизистую оболочку мочевого пузыря/прямой кишки(3) IVB(4) Примечания: (1) В настоящее время поражение только железистого эпителия эндоцервикса расценивают как стадию I. (2) Наличие буллёзного отёка не является достаточным доказательством стадии Т 4. Такое образование должно быть подтверждено биопсией. (3) Наличие буллёзного отёка не является достаточным доказательством стадии Т 4.
Клиническая классификация TNM T 4 IVA M 1(4) Опухоль прорастает в слизистую оболочку мочевого пузыря/прямой кишки(3) IVB(4) Примечания: (1) В настоящее время поражение только железистого эпителия эндоцервикса расценивают как стадию I. (2) Наличие буллёзного отёка не является достаточным доказательством стадии Т 4. Такое образование должно быть подтверждено биопсией. (3) Наличие буллёзного отёка не является достаточным доказательством стадии Т 4.
 N — Регионарные лимфатические узлы NX Регионарные лимфатические узлы не могут быть оценены N 0 Нет метастазов в регионарных лимфатических узлах N 1 Есть метастазы в регионарных лимфатических узлах М — Отдаленные метастазы МО Нет отдаленных метастазов М 1 Есть отдаленные метастазы, в т. ч. метастазы в паховых лимфатических узлах и внутрибрюшных лимфатических узлах, кроме околоаортальных или тазовых узлов (исключены метастазы во влагалище, серозные оболочки органов малого таза или придатки)
N — Регионарные лимфатические узлы NX Регионарные лимфатические узлы не могут быть оценены N 0 Нет метастазов в регионарных лимфатических узлах N 1 Есть метастазы в регионарных лимфатических узлах М — Отдаленные метастазы МО Нет отдаленных метастазов М 1 Есть отдаленные метастазы, в т. ч. метастазы в паховых лимфатических узлах и внутрибрюшных лимфатических узлах, кроме околоаортальных или тазовых узлов (исключены метастазы во влагалище, серозные оболочки органов малого таза или придатки)
 Патологоанатомическая классификация p. TNM Категории р. Т и p. N соответствуют категориям Т и N. p. NO. При тазовой лимфаденэктомии гистологическое исследование должно включать не менее 6 лимфатических узлов. Если в лимфатических узлах метастазы не выявлены, но исследовано меньшее количество узлов, то классифицируют как p. NO (в классификации FIGO такие случаи обозначают как p. NX). Гистологическая классификация Для данной классификации используют G 1, G 2 или G 3.
Патологоанатомическая классификация p. TNM Категории р. Т и p. N соответствуют категориям Т и N. p. NO. При тазовой лимфаденэктомии гистологическое исследование должно включать не менее 6 лимфатических узлов. Если в лимфатических узлах метастазы не выявлены, но исследовано меньшее количество узлов, то классифицируют как p. NO (в классификации FIGO такие случаи обозначают как p. NX). Гистологическая классификация Для данной классификации используют G 1, G 2 или G 3.
 СТАДИИ Стадия IA Т 1 а N 0 М 0 Стадия IB T 1 b N 0 М 0 Стадия II Т 2 N 0 М 0 Стадия IIIA ТЗа N 0 М 0 Стадия IIIB ТЗb N 0 М 0 Стадия IIIС Т 1, Т 2, ТЗ N 1 М 0 Стадия IVA Т 4 Любая N М 0 Стадия IVB Любая Т Любая N М 1
СТАДИИ Стадия IA Т 1 а N 0 М 0 Стадия IB T 1 b N 0 М 0 Стадия II Т 2 N 0 М 0 Стадия IIIA ТЗа N 0 М 0 Стадия IIIB ТЗb N 0 М 0 Стадия IIIС Т 1, Т 2, ТЗ N 1 М 0 Стадия IVA Т 4 Любая N М 0 Стадия IVB Любая Т Любая N М 1
 ГИСТОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ (ВОЗ, 2003 Г. ). Эндометриальная карцинома. q Эндометриоидная аденокарцинома: § аденокарцинома с плоскоклеточной дифференцировкой; § виллогландулярная аденокарцинома; § секреторная аденокарцинома; § цилиарно-клеточная аденокарцинома.
ГИСТОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ (ВОЗ, 2003 Г. ). Эндометриальная карцинома. q Эндометриоидная аденокарцинома: § аденокарцинома с плоскоклеточной дифференцировкой; § виллогландулярная аденокарцинома; § секреторная аденокарцинома; § цилиарно-клеточная аденокарцинома.
 ГИСТОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ (ВОЗ, 2003 Г. ). q Неэндометриоидная аденокарцинома (редкие формы): § муцинозная карцинома; § серозная карцинома; § светлоклеточная карцинома; § смешанно-клеточная карцинома; § плоскоклеточная карцинома; § переходно-клеточная карцинома; § мелкоклеточная карцинома; § недифференцированная карцинома; § другие (аденоидно-кистозная карцинома, стекловидно-клеточная карцинома, мезонефральная, онкоцитарная/оксифильная карцинома). Эндометриоидная аденокарцинома эндометрия встречается часто и составляет 75 -80% от общего числа злокачественных опухолей тела матки.
ГИСТОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ (ВОЗ, 2003 Г. ). q Неэндометриоидная аденокарцинома (редкие формы): § муцинозная карцинома; § серозная карцинома; § светлоклеточная карцинома; § смешанно-клеточная карцинома; § плоскоклеточная карцинома; § переходно-клеточная карцинома; § мелкоклеточная карцинома; § недифференцированная карцинома; § другие (аденоидно-кистозная карцинома, стекловидно-клеточная карцинома, мезонефральная, онкоцитарная/оксифильная карцинома). Эндометриоидная аденокарцинома эндометрия встречается часто и составляет 75 -80% от общего числа злокачественных опухолей тела матки.
 Пути метастазирования • Лимфогенный — дно матки — поясничные лимфатические узлы – средняя и нижняя трети тела матки — тазовые лимфатические узлы • Имплантационный • Распространение на соседние органы • Гематогенный – легкие, печень, кости, головной мозг
Пути метастазирования • Лимфогенный — дно матки — поясничные лимфатические узлы – средняя и нижняя трети тела матки — тазовые лимфатические узлы • Имплантационный • Распространение на соседние органы • Гематогенный – легкие, печень, кости, головной мозг
 Метастазирование РТМ Метастазы поясничные тазовые л/у Низкодифференцированная опухоль (предоперационное исследование) 18% 11% Инвазия миометрия > ½ 25% 17% Распространение на шейку матки Поражение придатков матки или брюшины Опухолевые клетки в смывах Опухоль > 2 см 15— 30% 32% 20% 25% 19% 15— 35%
Метастазирование РТМ Метастазы поясничные тазовые л/у Низкодифференцированная опухоль (предоперационное исследование) 18% 11% Инвазия миометрия > ½ 25% 17% Распространение на шейку матки Поражение придатков матки или брюшины Опухолевые клетки в смывах Опухоль > 2 см 15— 30% 32% 20% 25% 19% 15— 35%
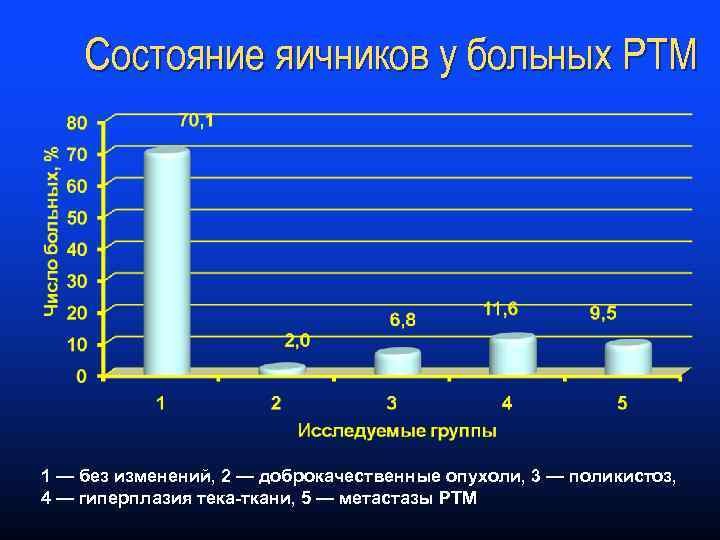 Состояние яичников у больных РТМ 1 — без изменений, 2 — доброкачественные опухоли, 3 — поликистоз, 4 — гиперплазия тека-ткани, 5 — метастазы РТМ
Состояние яичников у больных РТМ 1 — без изменений, 2 — доброкачественные опухоли, 3 — поликистоз, 4 — гиперплазия тека-ткани, 5 — метастазы РТМ
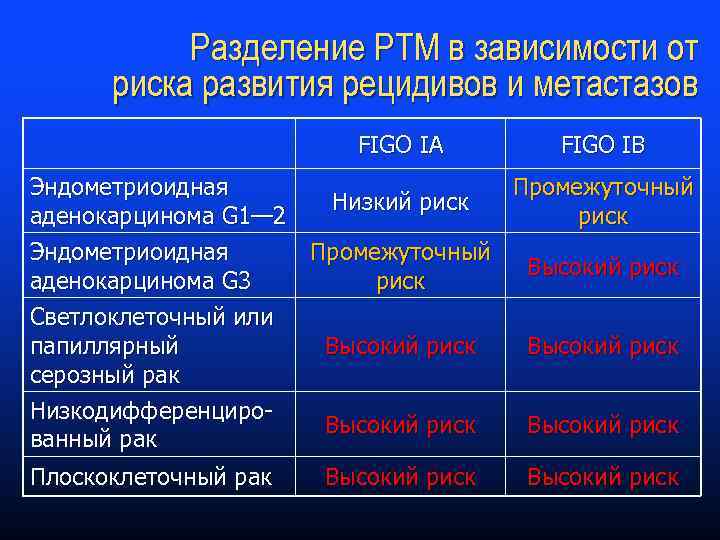 Разделение РТМ в зависимости от риска развития рецидивов и метастазов FIGO IА FIGO IВ Эндометриоидная Промежуточный Низкий риск аденокарцинома G 1— 2 риск Эндометриоидная Промежуточный Высокий риск аденокарцинома G 3 риск Светлоклеточный или папиллярный Высокий риск серозный рак Низкодифференциро. Высокий риск ванный рак Плоскоклеточный рак Высокий риск
Разделение РТМ в зависимости от риска развития рецидивов и метастазов FIGO IА FIGO IВ Эндометриоидная Промежуточный Низкий риск аденокарцинома G 1— 2 риск Эндометриоидная Промежуточный Высокий риск аденокарцинома G 3 риск Светлоклеточный или папиллярный Высокий риск серозный рак Низкодифференциро. Высокий риск ванный рак Плоскоклеточный рак Высокий риск
 Объем операции в зависимости от степени риска Низкий риск Экстирпация матки с придатками, смывы из брюшной полости Промежуточный риск + тазовая лимфаденэктомия Высокий риск + поясничная лимфаденэктомия
Объем операции в зависимости от степени риска Низкий риск Экстирпация матки с придатками, смывы из брюшной полости Промежуточный риск + тазовая лимфаденэктомия Высокий риск + поясничная лимфаденэктомия
 Лимфадиссекция l Цели лимфаденэктомии n уточнение стадии n определение тактики дальнейшего лечения (возможность отказа от послеоперационной лучевой терапии) n улучшение выживаемости
Лимфадиссекция l Цели лимфаденэктомии n уточнение стадии n определение тактики дальнейшего лечения (возможность отказа от послеоперационной лучевой терапии) n улучшение выживаемости
 Лапароскопия l 1992 г. — первое сообщение о выполнении лапароскопической операции при раке тела матки l Количество удаленных лимфатических узлов при лапароскопических операциях и операциях абдоминальным доступом не различается. При лапароскопически-ассистированных операциях ниже частота осложнений и меньше длительность пребывания в стационаре. Однако осложнения после лапароскопическиассистированных операций обычно тяжелее, чем после абдоминальной экстирпации матки.
Лапароскопия l 1992 г. — первое сообщение о выполнении лапароскопической операции при раке тела матки l Количество удаленных лимфатических узлов при лапароскопических операциях и операциях абдоминальным доступом не различается. При лапароскопически-ассистированных операциях ниже частота осложнений и меньше длительность пребывания в стационаре. Однако осложнения после лапароскопическиассистированных операций обычно тяжелее, чем после абдоминальной экстирпации матки.
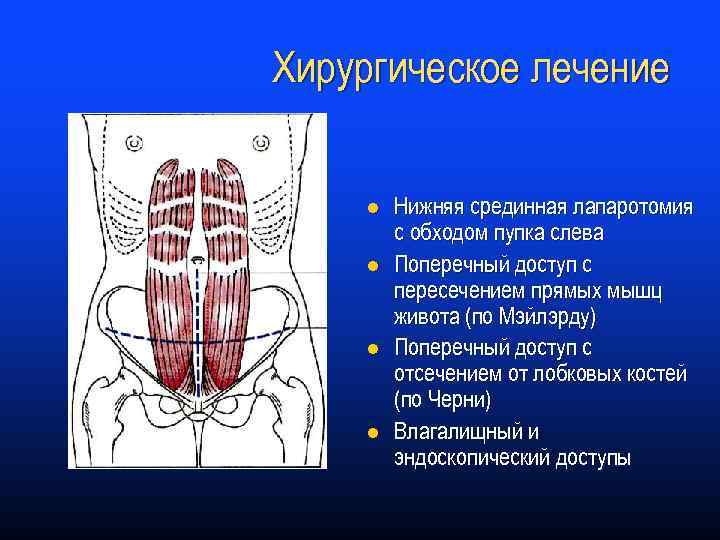 Хирургическое лечение l l Нижняя срединная лапаротомия с обходом пупка слева Поперечный доступ с пересечением прямых мышц живота (по Мэйлэрду) Поперечный доступ с отсечением от лобковых костей (по Черни) Влагалищный и эндоскопический доступы
Хирургическое лечение l l Нижняя срединная лапаротомия с обходом пупка слева Поперечный доступ с пересечением прямых мышц живота (по Мэйлэрду) Поперечный доступ с отсечением от лобковых костей (по Черни) Влагалищный и эндоскопический доступы
 Хирургическое лечение (влагалищный доступ) l Существенными недостатками влагалищного доступа являются сложность удаления придатков матки, невозможность ревизии брюшной полости и биопсии лимфатических узлов l Влагалищный доступ при раке тела матки возможен только при низком риске диссеминации, то есть при высокодифференцированных опухолях I стадии l Влагалищная экстирпация матки с придатками, предпочтительнее сочетанной лучевой терапии, однако должна выполняться только определенной группе больных строго по показаниям
Хирургическое лечение (влагалищный доступ) l Существенными недостатками влагалищного доступа являются сложность удаления придатков матки, невозможность ревизии брюшной полости и биопсии лимфатических узлов l Влагалищный доступ при раке тела матки возможен только при низком риске диссеминации, то есть при высокодифференцированных опухолях I стадии l Влагалищная экстирпация матки с придатками, предпочтительнее сочетанной лучевой терапии, однако должна выполняться только определенной группе больных строго по показаниям
 Хирургическое лечение • ОСНОВНОЙ МЕТОД: Экстрафасциальная экстирпация матки с придатками (гистерэктомия I типа) и ревизией органов малого таза и брюшной полости, тазовых и поясничных лимфатических узлов, биопсией всех измененных лимфатических узлов и выявленных образований ОБЪЕМ ОПЕРАЦИИ РАСШИРЯЮТ ДО УДАЛЕНИЯ БОЛЬШОГО САЛЬНИКА ПРИ: ü метастазах в яичниках, üналичии раковых клеток в смывах из брюшной полости, üпапиллярном серозном раке тела матки, когда высок риск имплантационного метастазирования
Хирургическое лечение • ОСНОВНОЙ МЕТОД: Экстрафасциальная экстирпация матки с придатками (гистерэктомия I типа) и ревизией органов малого таза и брюшной полости, тазовых и поясничных лимфатических узлов, биопсией всех измененных лимфатических узлов и выявленных образований ОБЪЕМ ОПЕРАЦИИ РАСШИРЯЮТ ДО УДАЛЕНИЯ БОЛЬШОГО САЛЬНИКА ПРИ: ü метастазах в яичниках, üналичии раковых клеток в смывах из брюшной полости, üпапиллярном серозном раке тела матки, когда высок риск имплантационного метастазирования
 Хирургическое лечение l Показания к лимфаденэктомии n низкодифференцированная эндометриоидная аденокарцинома n инвазия миометрия более чем на половину его толщины n переход опухоли на перешеек или шейку матки n распространение опухоли за пределы матки n опухоль более 2 см n светлоклеточный, папиллярный серозный, плоскоклеточный и недифференцированный рак
Хирургическое лечение l Показания к лимфаденэктомии n низкодифференцированная эндометриоидная аденокарцинома n инвазия миометрия более чем на половину его толщины n переход опухоли на перешеек или шейку матки n распространение опухоли за пределы матки n опухоль более 2 см n светлоклеточный, папиллярный серозный, плоскоклеточный и недифференцированный рак
 Хирургическое лечение • У 38% больных раком тела матки I клинической стадии во время операции обнаруживаются метастазы в лимфатических узлах, яичниках, маточных трубах, распространение по париетальной и висцеральной брюшине или опухолевые клетки в смывах из брюшной полости • Пред- и послеоперационный гистологический диагнозы не совпадают у 27% больных, степень дифференцировки — у 34%, стадия — у 51%
Хирургическое лечение • У 38% больных раком тела матки I клинической стадии во время операции обнаруживаются метастазы в лимфатических узлах, яичниках, маточных трубах, распространение по париетальной и висцеральной брюшине или опухолевые клетки в смывах из брюшной полости • Пред- и послеоперационный гистологический диагнозы не совпадают у 27% больных, степень дифференцировки — у 34%, стадия — у 51%
 Хирургическое лечение • Метастатически измененные лимфатические узлы на момент операции оказываются увеличенными не менее чем у 10 -40% больных • Оценка состояния тазовых и поясничных лимфатических узлов – предоперационные КТ и МРТ – пальпация и биопсия увеличенных лимфатических узлов – биопсия одного лимфатического узла – селективная лимфаденэктомия – тотальная лимфаденэктомия
Хирургическое лечение • Метастатически измененные лимфатические узлы на момент операции оказываются увеличенными не менее чем у 10 -40% больных • Оценка состояния тазовых и поясничных лимфатических узлов – предоперационные КТ и МРТ – пальпация и биопсия увеличенных лимфатических узлов – биопсия одного лимфатического узла – селективная лимфаденэктомия – тотальная лимфаденэктомия
 Лучевая терапия • Лучевая терапия снижает частоту рецидивов и метастазов в тазовых лимфатических узлах (прогрессирование в зоне облучения), но не влияет на общую выживаемость • Предоперационную лучевую терапию не проводят во всех странах, кроме РБ • Показания – Европа — в зависимости от степени дифференцировки и глубины инвазии – США и Австралия — в зависимости от наличия опухоли за пределами матки и риска прогрессирования • Лучевая терапия не показана – высокодифференцированные опухоли I стадии – умереннодифференцированные опухоли IA и IB стадий
Лучевая терапия • Лучевая терапия снижает частоту рецидивов и метастазов в тазовых лимфатических узлах (прогрессирование в зоне облучения), но не влияет на общую выживаемость • Предоперационную лучевую терапию не проводят во всех странах, кроме РБ • Показания – Европа — в зависимости от степени дифференцировки и глубины инвазии – США и Австралия — в зависимости от наличия опухоли за пределами матки и риска прогрессирования • Лучевая терапия не показана – высокодифференцированные опухоли I стадии – умереннодифференцированные опухоли IA и IB стадий
 Лучевая терапия • Послеоперационная дистанционная лучевая терапия на область малого таза (СОД 45 -50 Гр) при определении морфологической стадии опухоли – многие авторы проводят лучевую терапию только при прогрессировании – низкодифференцированные опухоли IC стадии • Внутриполостная лучевая терапия (СОД 21 Гр) при определении морфологической стадии опухоли – умереннодифференцированные опухоли IC стадии – низкодифференцированные опухоли IA и IB стадий
Лучевая терапия • Послеоперационная дистанционная лучевая терапия на область малого таза (СОД 45 -50 Гр) при определении морфологической стадии опухоли – многие авторы проводят лучевую терапию только при прогрессировании – низкодифференцированные опухоли IC стадии • Внутриполостная лучевая терапия (СОД 21 Гр) при определении морфологической стадии опухоли – умереннодифференцированные опухоли IC стадии – низкодифференцированные опухоли IA и IB стадий
 Лучевая терапия • Лучевая терапия как самостоятельный метод лечения (сочетанная лучевая терапия или внутриполостная) при: – противопоказаниях к операции – отказе больной от операции Каждый случай отказа хирурга от операции при раке тела матки должен быть тщательно аргументирован
Лучевая терапия • Лучевая терапия как самостоятельный метод лечения (сочетанная лучевая терапия или внутриполостная) при: – противопоказаниях к операции – отказе больной от операции Каждый случай отказа хирурга от операции при раке тела матки должен быть тщательно аргументирован
 Гормонотерапия • Медроксипрогестерона ацетат, мегестрола ацетат и тамоксифен • Преимущества – системное действие – низкая частота осложнений – первый опыт применения прогестагенов при диссеминированном раке тела матки • Адъювантная гормонотерапия неэффективна? ? ?
Гормонотерапия • Медроксипрогестерона ацетат, мегестрола ацетат и тамоксифен • Преимущества – системное действие – низкая частота осложнений – первый опыт применения прогестагенов при диссеминированном раке тела матки • Адъювантная гормонотерапия неэффективна? ? ?
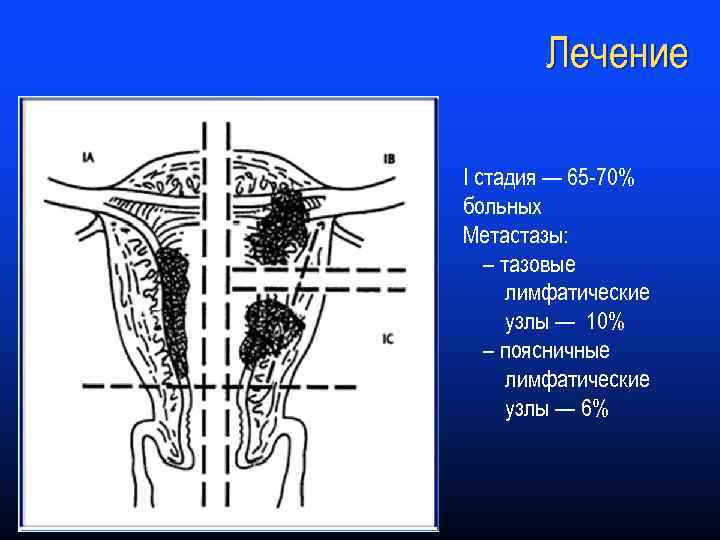 Лечение I стадия — 65 -70% больных Метастазы: – тазовые лимфатические узлы — 10% – поясничные лимфатические узлы — 6%
Лечение I стадия — 65 -70% больных Метастазы: – тазовые лимфатические узлы — 10% – поясничные лимфатические узлы — 6%
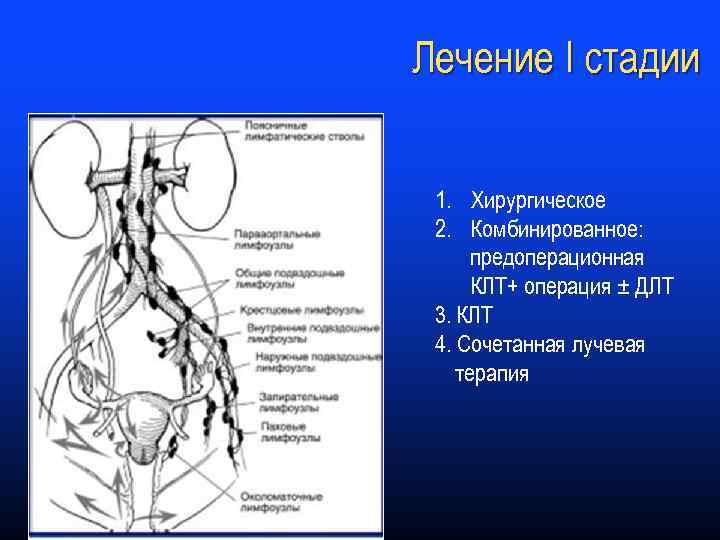 Лечение I стадии 1. Хирургическое 2. Комбинированное: предоперационная КЛТ+ операция ± ДЛТ 3. КЛТ 4. Сочетанная лучевая терапия
Лечение I стадии 1. Хирургическое 2. Комбинированное: предоперационная КЛТ+ операция ± ДЛТ 3. КЛТ 4. Сочетанная лучевая терапия
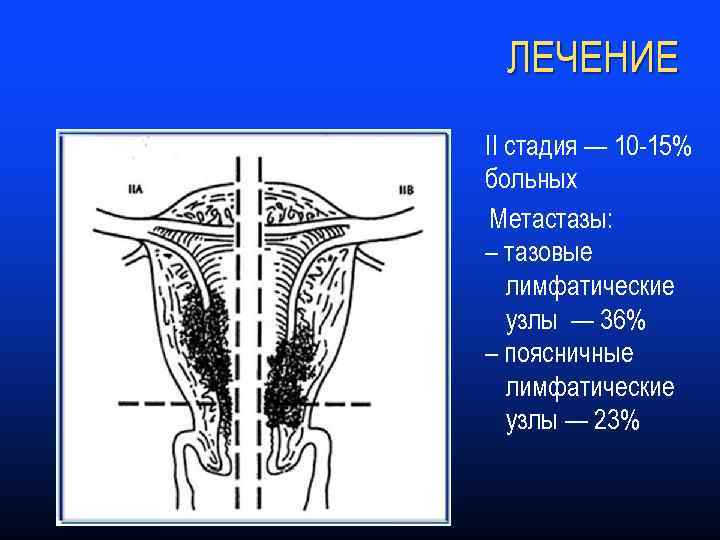 ЛЕЧЕНИЕ II стадия — 10 -15% больных Метастазы: – тазовые лимфатические узлы — 36% – поясничные лимфатические узлы — 23%
ЛЕЧЕНИЕ II стадия — 10 -15% больных Метастазы: – тазовые лимфатические узлы — 36% – поясничные лимфатические узлы — 23%
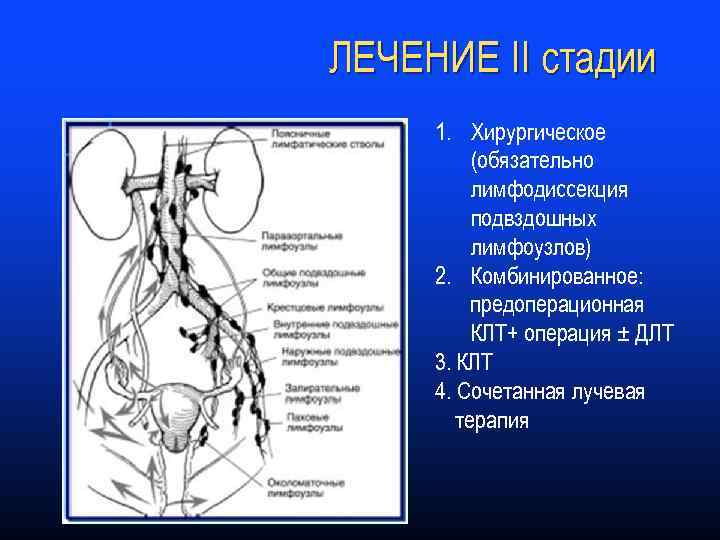 ЛЕЧЕНИЕ II стадии 1. Хирургическое (обязательно лимфодиссекция подвздошных лимфоузлов) 2. Комбинированное: предоперационная КЛТ+ операция ± ДЛТ 3. КЛТ 4. Сочетанная лучевая терапия
ЛЕЧЕНИЕ II стадии 1. Хирургическое (обязательно лимфодиссекция подвздошных лимфоузлов) 2. Комбинированное: предоперационная КЛТ+ операция ± ДЛТ 3. КЛТ 4. Сочетанная лучевая терапия
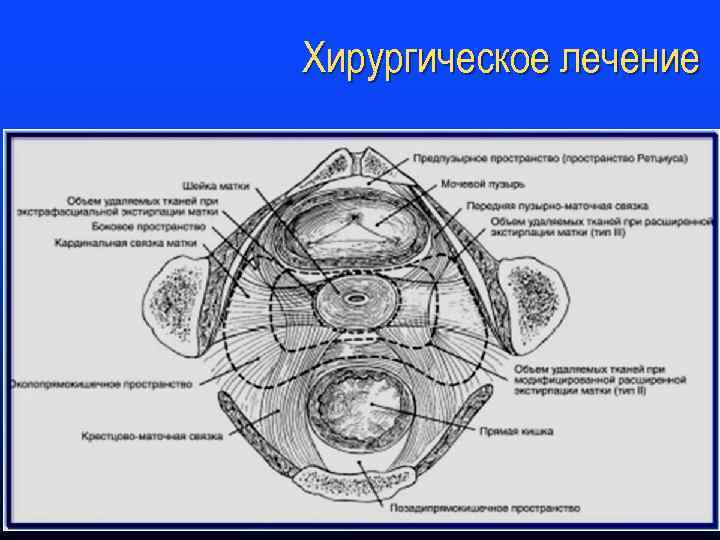 Хирургическое лечение
Хирургическое лечение
 ЛЕЧЕНИЕ РТМ III A-В стадий • ИНДИВИДУАЛЬНЫЙ ПЛАН III стадия • (10 -15%) Операция на первом этапе обязательна, если при обследовании выявляется объемное образование в области придатков матки • Следует стремиться к максимальному уменьшению массы опухоли, поскольку это улучшает прогноз. Результаты комбинированного лечения рака тела матки III стадии лучше, чем результаты сочетанной лучевой терапии • При метастазах в яичниках проводят химиотерапию после операции
ЛЕЧЕНИЕ РТМ III A-В стадий • ИНДИВИДУАЛЬНЫЙ ПЛАН III стадия • (10 -15%) Операция на первом этапе обязательна, если при обследовании выявляется объемное образование в области придатков матки • Следует стремиться к максимальному уменьшению массы опухоли, поскольку это улучшает прогноз. Результаты комбинированного лечения рака тела матки III стадии лучше, чем результаты сочетанной лучевой терапии • При метастазах в яичниках проводят химиотерапию после операции
 ЛЕЧЕНИЕ РТМ III C стадии • Хирургическое лечение, определение стадии, удаление метастазов • При морфологическом подтверждении поражения тазовых или поясничных лимфатических узлов — дистанционная лучевая терапия на область малого таза или поясничную область (СОД 45 -50 Гр) соответственно
ЛЕЧЕНИЕ РТМ III C стадии • Хирургическое лечение, определение стадии, удаление метастазов • При морфологическом подтверждении поражения тазовых или поясничных лимфатических узлов — дистанционная лучевая терапия на область малого таза или поясничную область (СОД 45 -50 Гр) соответственно
 IV стадия — 3% ЛЕЧЕНИЕ РТМ IV стадии Индивидуальные, паллиативные схемы, включающие хирургическое, лучевое, гормональное и химиотерапевтическое воздействия. При ограниченном распространении опухоли на мочевой пузырь и прямую кишку и удовлетворительном состоянии больной выполняют экзентерацию таза. В плане хирургического лечения выполняются различные по объему паллиативные операции с целью: удалить очаг инфекции и остановить или предотвратить возникающее кровотечение из полости матки. К ним относятся: надвлагалищная ампутация матки с придатками, перевязка внутренних подвздошных артерий или их эмболизация, селективная лимфаденэктомия опухолевоизмененных лимфатических узлов (паховых, парааортальных, подвздошных).
IV стадия — 3% ЛЕЧЕНИЕ РТМ IV стадии Индивидуальные, паллиативные схемы, включающие хирургическое, лучевое, гормональное и химиотерапевтическое воздействия. При ограниченном распространении опухоли на мочевой пузырь и прямую кишку и удовлетворительном состоянии больной выполняют экзентерацию таза. В плане хирургического лечения выполняются различные по объему паллиативные операции с целью: удалить очаг инфекции и остановить или предотвратить возникающее кровотечение из полости матки. К ним относятся: надвлагалищная ампутация матки с придатками, перевязка внутренних подвздошных артерий или их эмболизация, селективная лимфаденэктомия опухолевоизмененных лимфатических узлов (паховых, парааортальных, подвздошных).
 ЛЕЧЕНИЕ • Лечение рака тела матки III-IV стадий должно быть комплексным и включать операцию, лучевую, химиотерапию и гормоны. • Цель операции и лучевой терапии — снизить риск маточного кровотечения, нормализовать функцию мочевого пузыря и прямой кишки. • Показана химиотерапия доксорубицином и цисплатином, если остаточные опухоли не превышают 2 см.
ЛЕЧЕНИЕ • Лечение рака тела матки III-IV стадий должно быть комплексным и включать операцию, лучевую, химиотерапию и гормоны. • Цель операции и лучевой терапии — снизить риск маточного кровотечения, нормализовать функцию мочевого пузыря и прямой кишки. • Показана химиотерапия доксорубицином и цисплатином, если остаточные опухоли не превышают 2 см.
 Гормонотерапия • Эффективность при диссеминированном раке тела матки и прогрессировании определяется – степенью дифференцировки – уровнями рецепторов стероидных гормонов в опухоли • Частота частичных и полных ремиссий 11 -19%, стабилизации 15 -52% • Эффективность лечения не зависит ни от используемого препарата, ни от режима его назначения
Гормонотерапия • Эффективность при диссеминированном раке тела матки и прогрессировании определяется – степенью дифференцировки – уровнями рецепторов стероидных гормонов в опухоли • Частота частичных и полных ремиссий 11 -19%, стабилизации 15 -52% • Эффективность лечения не зависит ни от используемого препарата, ни от режима его назначения
 Химиотерапия • При прогрессировании РТМ применяют различные комбинации препаратов платины, антрациклинов, таксанов, 5 -фторурацила, циклофосфамида, ифосфамида, этопозида • Наиболее эффективны комбинации, включающие препараты платины, таксаны и антрациклины • Большинство ремиссий частичные и непродолжительные
Химиотерапия • При прогрессировании РТМ применяют различные комбинации препаратов платины, антрациклинов, таксанов, 5 -фторурацила, циклофосфамида, ифосфамида, этопозида • Наиболее эффективны комбинации, включающие препараты платины, таксаны и антрациклины • Большинство ремиссий частичные и непродолжительные
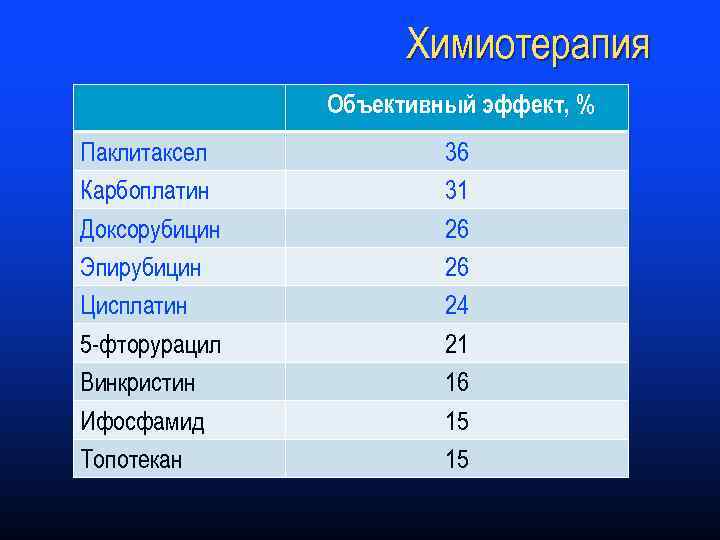 Химиотерапия Объективный эффект, % Паклитаксел Карбоплатин Доксорубицин Эпирубицин Цисплатин 5 -фторурацил Винкристин Ифосфамид Топотекан 36 31 26 26 24 21 16 15 15
Химиотерапия Объективный эффект, % Паклитаксел Карбоплатин Доксорубицин Эпирубицин Цисплатин 5 -фторурацил Винкристин Ифосфамид Топотекан 36 31 26 26 24 21 16 15 15
 СХЕМЫ ХИМИОТЕРАПИИ q Доксорубицин 50 мг/м 2 внутривенно в течение 20 -30 мин в 1 -й день, цисплатин 75 мг/м 2 внутривенная инфузия со скоростью не более 1 мг/мин с пред- и постгидратацией в 1 -й день. q Винорельбин 25 мг/м 2 внутривенно в течение 6 -10 мин в 1 -й и 8 -й дни, этопозид 50 мг/м 2/сут внутривенно в течение 1 ч в 1 -, 2 -, 3 -, 4 -, 5 -й дни, цисплатин 20 мг/м 2 внутривенная инфузия со скоростью не более 1 мг/мин с пред- и постгидратацией в 1 -, 2 -, 3 -й дни.
СХЕМЫ ХИМИОТЕРАПИИ q Доксорубицин 50 мг/м 2 внутривенно в течение 20 -30 мин в 1 -й день, цисплатин 75 мг/м 2 внутривенная инфузия со скоростью не более 1 мг/мин с пред- и постгидратацией в 1 -й день. q Винорельбин 25 мг/м 2 внутривенно в течение 6 -10 мин в 1 -й и 8 -й дни, этопозид 50 мг/м 2/сут внутривенно в течение 1 ч в 1 -, 2 -, 3 -, 4 -, 5 -й дни, цисплатин 20 мг/м 2 внутривенная инфузия со скоростью не более 1 мг/мин с пред- и постгидратацией в 1 -, 2 -, 3 -й дни.
 Национальные стандарты лечения СТАДИЯ IA (GI-II) БЕЗ ИНВАЗИИ СТАДИЯ 0, РАК IN SITU СТАНДАРТ Тотальная гистерэктомия с гистерэктомия (тип I) без придатков у билатеральной сальпинго-оофорэктомией менструирующих женщин, с (тип I)*. придатками у женщин в Индивидуализированно постменопаузе. контактная лучевая терапия (при соматической неоперабельности). СТАДИЯ IА (GI, II) ИНВАЗИЯ ДО 12 СТАНДАРТ предоперационная контактная лучевая терапия +тотальная гистерэктомия с билатеральной сальпинго-оофорэктомией (тип I)*, **** СТАДИЯ IA (GIII И ДР. НЕБЛАГОПРИЯТНЫЙ ГИСТОТИП, LVSI+) СТАНДАРТ предоперационная контактная лучевая терапия + тотальная гистерэктомия с билатеральной сальпинго-оофорэктомией (тип I)*, **** + дистанционная лучевая терапия **. (В случае невыполненной лимфодиссекции рекомендовано проведение лучевой терапии на область малого таза).
Национальные стандарты лечения СТАДИЯ IA (GI-II) БЕЗ ИНВАЗИИ СТАДИЯ 0, РАК IN SITU СТАНДАРТ Тотальная гистерэктомия с гистерэктомия (тип I) без придатков у билатеральной сальпинго-оофорэктомией менструирующих женщин, с (тип I)*. придатками у женщин в Индивидуализированно постменопаузе. контактная лучевая терапия (при соматической неоперабельности). СТАДИЯ IА (GI, II) ИНВАЗИЯ ДО 12 СТАНДАРТ предоперационная контактная лучевая терапия +тотальная гистерэктомия с билатеральной сальпинго-оофорэктомией (тип I)*, **** СТАДИЯ IA (GIII И ДР. НЕБЛАГОПРИЯТНЫЙ ГИСТОТИП, LVSI+) СТАНДАРТ предоперационная контактная лучевая терапия + тотальная гистерэктомия с билатеральной сальпинго-оофорэктомией (тип I)*, **** + дистанционная лучевая терапия **. (В случае невыполненной лимфодиссекции рекомендовано проведение лучевой терапии на область малого таза).
 СТАДИЯ IB (GI-II) СТАНДАРТ предоперационная контактная лучевая терапия + тотальная гистерэктомия с билатеральной сальпингооофорэктомией (тип I) с тазовой лимфаденэктомией + дистанционная лучевая терапия **. СТАДИЯ IВ (GIII) СТАНДАРТ предоперационная контактная лучевая терапия + тотальная гистерэктомия с билатеральной сальпингооофорэктомией (тип I) с тазовой лимфаденэктомией + оментэктомия + дистанционная лучевая терапия **.
СТАДИЯ IB (GI-II) СТАНДАРТ предоперационная контактная лучевая терапия + тотальная гистерэктомия с билатеральной сальпингооофорэктомией (тип I) с тазовой лимфаденэктомией + дистанционная лучевая терапия **. СТАДИЯ IВ (GIII) СТАНДАРТ предоперационная контактная лучевая терапия + тотальная гистерэктомия с билатеральной сальпингооофорэктомией (тип I) с тазовой лимфаденэктомией + оментэктомия + дистанционная лучевая терапия **.
 СТАДИЯ II СТАНДАРТ предоперационная контактная лучевая терапия + радикальная гистерэктомия с тазовой лимфаденэктомией (тип III)**** + дистанционная лучевая терапия. ИНДИВИДУАЛИЗИРОВАННО предоперационная контактная лучевая терапия + гистерэктомия с верхней третью влагалища (при невозможности осуществления радикальной операции) + дистанционная лучевая терапия; сочетанная лучевая терапия***.
СТАДИЯ II СТАНДАРТ предоперационная контактная лучевая терапия + радикальная гистерэктомия с тазовой лимфаденэктомией (тип III)**** + дистанционная лучевая терапия. ИНДИВИДУАЛИЗИРОВАННО предоперационная контактная лучевая терапия + гистерэктомия с верхней третью влагалища (при невозможности осуществления радикальной операции) + дистанционная лучевая терапия; сочетанная лучевая терапия***.
 СТАДИЯ IIIA СТАНДАРТ предоперационная контактная лучевая терапия + радикальная гистерэктомия с тазовой лимфаденэктомией (тип III) + оментэктомия + дистанционная лучевая терапия + полихимиотерапия. СТАДИЯ IIIB ИНДИВИДУАЛИЗИРОВАНО неоадъювантная дистанционная лучевая терапия + гистерэктомия с резекцией влагалища + эндовагинальное облучение + полихимиотерапия; химиолучевая терапия ***.
СТАДИЯ IIIA СТАНДАРТ предоперационная контактная лучевая терапия + радикальная гистерэктомия с тазовой лимфаденэктомией (тип III) + оментэктомия + дистанционная лучевая терапия + полихимиотерапия. СТАДИЯ IIIB ИНДИВИДУАЛИЗИРОВАНО неоадъювантная дистанционная лучевая терапия + гистерэктомия с резекцией влагалища + эндовагинальное облучение + полихимиотерапия; химиолучевая терапия ***.
 СТАДИЯ IIIC 1 СТАНДАРТ гистерэктомия с тазовой лимфодиссекцией ± забрюшинной лимфодиссецией + дистанционная лучевая терапия + полихимиотерапия; гистерэктомия (при нерезектабельности патологических очагов или ослабленном физическом статусе больной – IV класс летальных осложнений по ASA) + дистанционная лучевая терапия; сочетанная лучевая терапия***. при наличии метастазов в подвздошных лимфоузлах показано дополнительное облучение парааортальных лимфоузлов
СТАДИЯ IIIC 1 СТАНДАРТ гистерэктомия с тазовой лимфодиссекцией ± забрюшинной лимфодиссецией + дистанционная лучевая терапия + полихимиотерапия; гистерэктомия (при нерезектабельности патологических очагов или ослабленном физическом статусе больной – IV класс летальных осложнений по ASA) + дистанционная лучевая терапия; сочетанная лучевая терапия***. при наличии метастазов в подвздошных лимфоузлах показано дополнительное облучение парааортальных лимфоузлов
 СТАДИЯ IIIС 2 СТАНДАРТ гистерэктомия с тазовой лимфодиссекцией + забрюшинной лимфодиссецией + дистанционная лучевая терапия + полихимиотерапия; гистерэктомия (при нерезектабельности патологических очагов или ослабленном физическом статусе больной – IV класс летальных осложнений по ASA) + дистанционная лучевая терапия; сочетанная лучевая терапия***.
СТАДИЯ IIIС 2 СТАНДАРТ гистерэктомия с тазовой лимфодиссекцией + забрюшинной лимфодиссецией + дистанционная лучевая терапия + полихимиотерапия; гистерэктомия (при нерезектабельности патологических очагов или ослабленном физическом статусе больной – IV класс летальных осложнений по ASA) + дистанционная лучевая терапия; сочетанная лучевая терапия***.
 IV СТАДИЯ И РЕЦИДИВЫ ИНДИВИДУАЛИЗИРОВАНО различные по объему циторедуктивные или паллиативные оперативные вмешательства; химиогормонотерапия; лучевая терапия. при переходе опухоли на перешеек, серозной, светлоклеточной, низкодифференцированной, недифференцированной карциноме, карциносаркоме, наличии подозрения на опухолевое поражение лимфоузлов показана гистерэктомия (тип II) с тазовой лимфодиссекцией; ** инвазия в миометрий менее ½ - без лимфодиссекции и более ½, серозный, светлоклеточный, высокодифференцированный, умереннодифференцированный, низкодифференцированный и недифференцированный рак, переход опухоли на перешеек, поражение тазовых лимфоузлов; *** при нерезектабельности опухоли или неоперабельности больной; ****в случае серозной, светлоклеточной аденокарциномы, карциносаркомы показано удаление сальника. *
IV СТАДИЯ И РЕЦИДИВЫ ИНДИВИДУАЛИЗИРОВАНО различные по объему циторедуктивные или паллиативные оперативные вмешательства; химиогормонотерапия; лучевая терапия. при переходе опухоли на перешеек, серозной, светлоклеточной, низкодифференцированной, недифференцированной карциноме, карциносаркоме, наличии подозрения на опухолевое поражение лимфоузлов показана гистерэктомия (тип II) с тазовой лимфодиссекцией; ** инвазия в миометрий менее ½ - без лимфодиссекции и более ½, серозный, светлоклеточный, высокодифференцированный, умереннодифференцированный, низкодифференцированный и недифференцированный рак, переход опухоли на перешеек, поражение тазовых лимфоузлов; *** при нерезектабельности опухоли или неоперабельности больной; ****в случае серозной, светлоклеточной аденокарциномы, карциносаркомы показано удаление сальника. *
 КЛТ у больных раком тела матки (отечественные стандарты)
КЛТ у больных раком тела матки (отечественные стандарты)
 Методы лечения больных РТМ, используемые в РБ l l l l l хирургический – операция и ДЛТ – КЛТ, операция – операция, ДЛТ, ПХТ, ГТ – операция, ГТ – ПХТ, ГТ – КЛТ – ДЛТ – КЛТ + ДЛТ – 13, 9% 41, 0% 14, 9% 2, 0% 14, 2% 3, 4% 1, 0% 0, 5% 4, 9% 4, 1% Симптоматическое лечение проводится в 6, 1% случае
Методы лечения больных РТМ, используемые в РБ l l l l l хирургический – операция и ДЛТ – КЛТ, операция – операция, ДЛТ, ПХТ, ГТ – операция, ГТ – ПХТ, ГТ – КЛТ – ДЛТ – КЛТ + ДЛТ – 13, 9% 41, 0% 14, 9% 2, 0% 14, 2% 3, 4% 1, 0% 0, 5% 4, 9% 4, 1% Симптоматическое лечение проводится в 6, 1% случае
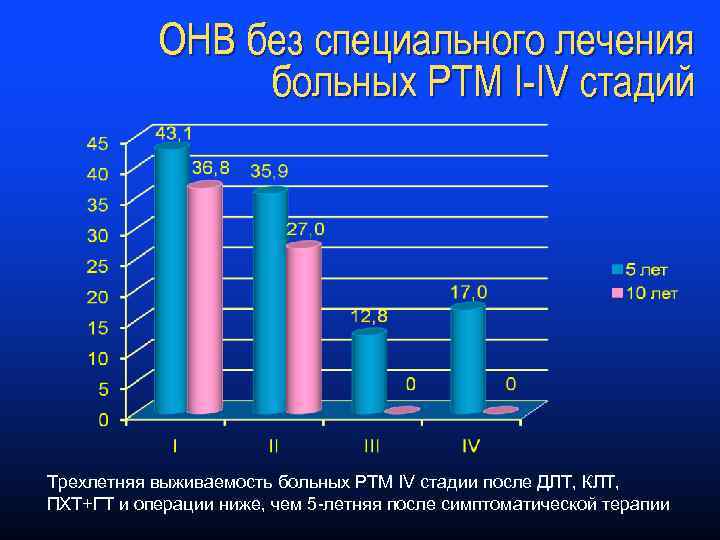 ОНВ без специального лечения больных РТМ I-IV стадий Трехлетняя выживаемость больных РТМ IV стадии после ДЛТ, КЛТ, ПХТ+ГТ и операции ниже, чем 5 -летняя после симптоматической терапии
ОНВ без специального лечения больных РТМ I-IV стадий Трехлетняя выживаемость больных РТМ IV стадии после ДЛТ, КЛТ, ПХТ+ГТ и операции ниже, чем 5 -летняя после симптоматической терапии
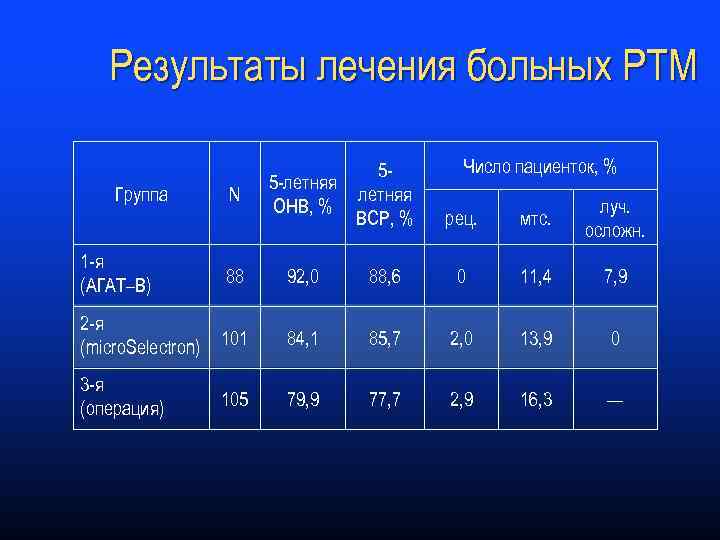 Результаты лечения больных РТМ Группа N 55 -летняя ОНВ, % ВСР, % Число пациенток, % рец. мтс. луч. осложн. 1 -я (АГАТ–В) 88 92, 0 88, 6 0 11, 4 7, 9 2 -я (micro. Selectron) 101 84, 1 85, 7 2, 0 13, 9 0 3 -я (операция) 105 79, 9 77, 7 2, 9 16, 3 —
Результаты лечения больных РТМ Группа N 55 -летняя ОНВ, % ВСР, % Число пациенток, % рец. мтс. луч. осложн. 1 -я (АГАТ–В) 88 92, 0 88, 6 0 11, 4 7, 9 2 -я (micro. Selectron) 101 84, 1 85, 7 2, 0 13, 9 0 3 -я (операция) 105 79, 9 77, 7 2, 9 16, 3 —
 Предоперационная КЛТ Аппарат «АГАТ–В» , 60 Со, доза в т. А — 13, 5 Гр Изодозное распределение: фронтальное (1), сагиттальное (2), поперечное (3)
Предоперационная КЛТ Аппарат «АГАТ–В» , 60 Со, доза в т. А — 13, 5 Гр Изодозное распределение: фронтальное (1), сагиттальное (2), поперечное (3)
 Предоперационная КЛТ эндостатом «Rotte Endometrial Applicator» Аппарат «micro. Selectron–HDR» , 192 Ir, доза на середину миометрия — 13, 5 Гр Изодозное распределение: фронтальное (1), сагиттальное (2), поперечное (3)
Предоперационная КЛТ эндостатом «Rotte Endometrial Applicator» Аппарат «micro. Selectron–HDR» , 192 Ir, доза на середину миометрия — 13, 5 Гр Изодозное распределение: фронтальное (1), сагиттальное (2), поперечное (3)
 Предоперационная КЛТ метракольпостатом «Ring Applicator» Аппарат «micro. Selectron–HDR» , 192 Ir, доза на середину миометрия — 13, 5 Гр Изодозное распределение: фронтальное (1), сагиттальное (2), поперечное (3)
Предоперационная КЛТ метракольпостатом «Ring Applicator» Аппарат «micro. Selectron–HDR» , 192 Ir, доза на середину миометрия — 13, 5 Гр Изодозное распределение: фронтальное (1), сагиттальное (2), поперечное (3)
 Предоперационная КЛТ 4 -канальным эндостатом Аппарат «micro. Selectron–HDR» , 192 Ir, доза на середину миометрия — 13, 5 Гр Изодозное распределение: фронтальное (1), сагиттальное (2), поперечное (3)
Предоперационная КЛТ 4 -канальным эндостатом Аппарат «micro. Selectron–HDR» , 192 Ir, доза на середину миометрия — 13, 5 Гр Изодозное распределение: фронтальное (1), сагиттальное (2), поперечное (3)
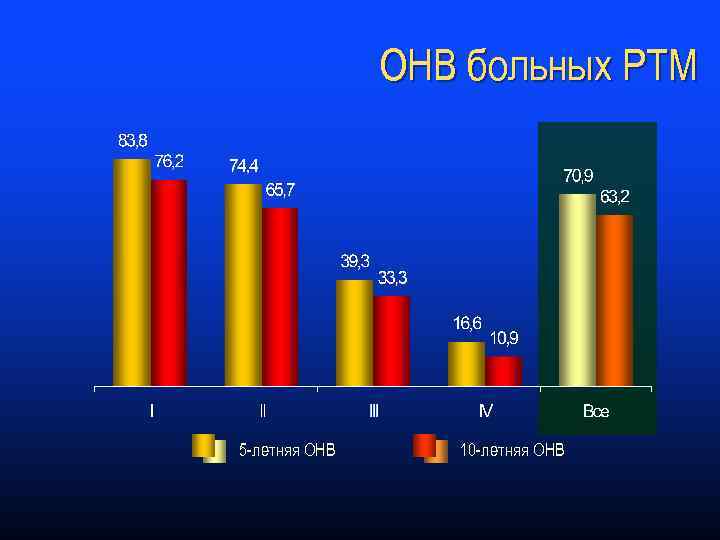 ОНВ больных РТМ 5 -летняя ОНВ 10 -летняя ОНВ
ОНВ больных РТМ 5 -летняя ОНВ 10 -летняя ОНВ
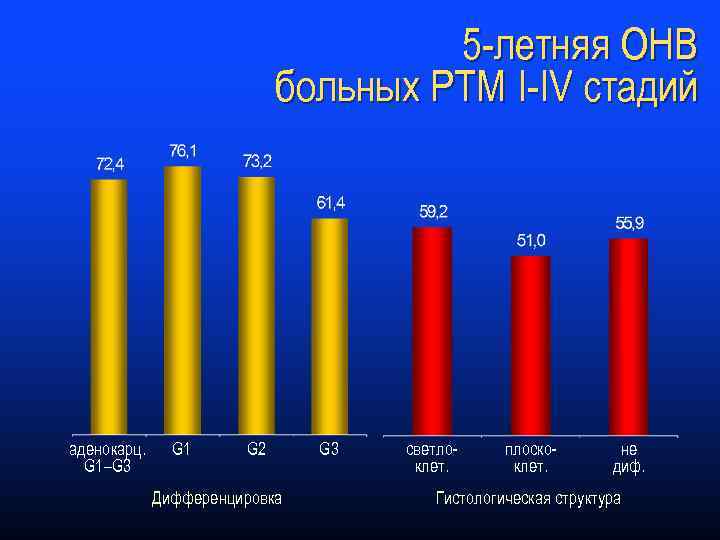 5 -летняя ОНВ больных РТМ I-IV стадий аденокарц. G 1–G 3 G 1 G 2 Дифференцировка G 3 светлоклет. плоскоклет. не диф. Гистологическая структура
5 -летняя ОНВ больных РТМ I-IV стадий аденокарц. G 1–G 3 G 1 G 2 Дифференцировка G 3 светлоклет. плоскоклет. не диф. Гистологическая структура
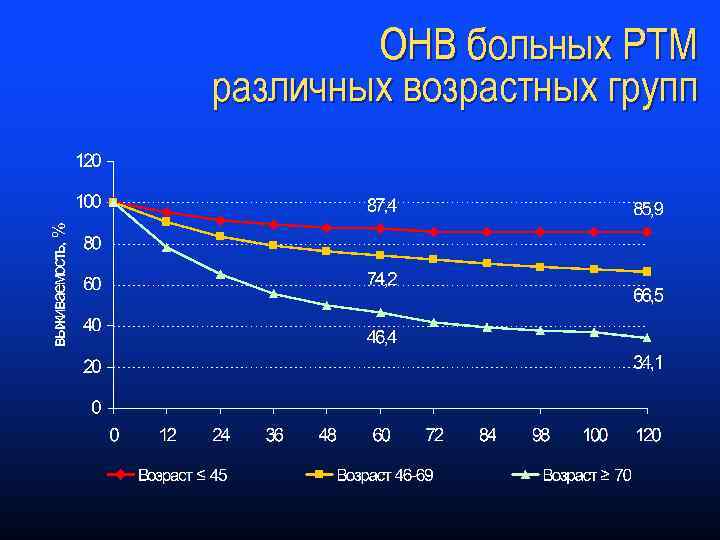 ОНВ больных РТМ различных возрастных групп
ОНВ больных РТМ различных возрастных групп
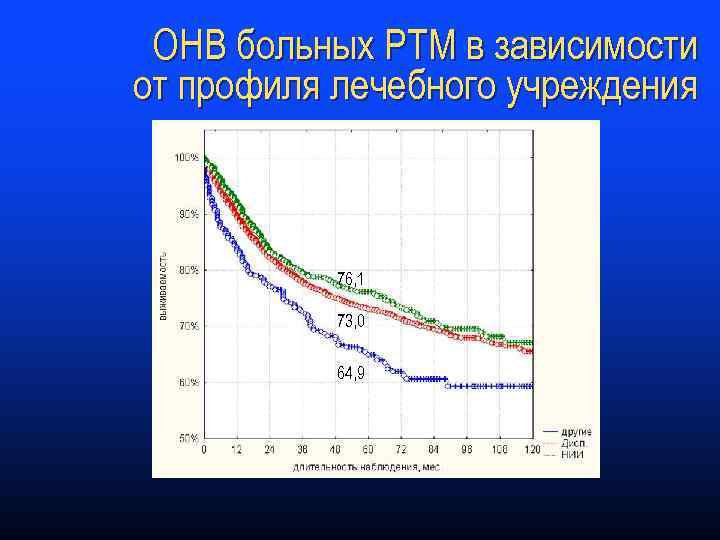 ОНВ больных РТМ в зависимости от профиля лечебного учреждения 76, 1 73, 0 64, 9
ОНВ больных РТМ в зависимости от профиля лечебного учреждения 76, 1 73, 0 64, 9
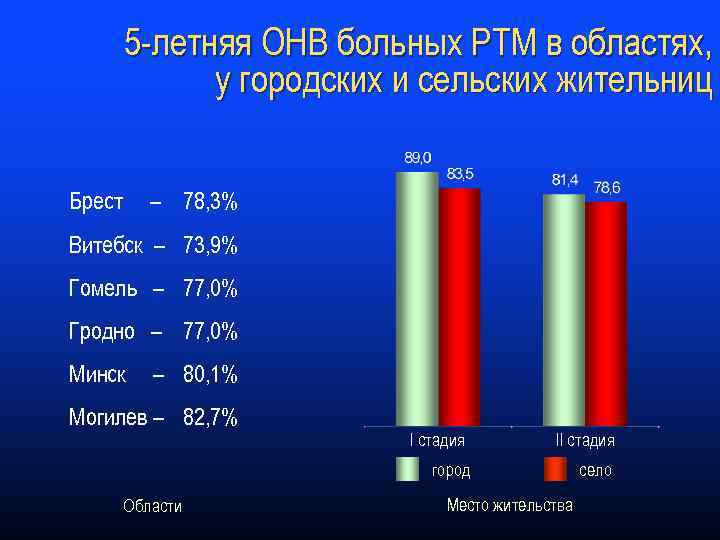 5 -летняя ОНВ больных РТМ в областях, у городских и сельских жительниц Брест – 78, 3% Витебск – 73, 9% Гомель – 77, 0% Гродно – 77, 0% Минск – 80, 1% Могилев – 82, 7% I стадия II стадия город Области Место жительства село
5 -летняя ОНВ больных РТМ в областях, у городских и сельских жительниц Брест – 78, 3% Витебск – 73, 9% Гомель – 77, 0% Гродно – 77, 0% Минск – 80, 1% Могилев – 82, 7% I стадия II стадия город Области Место жительства село
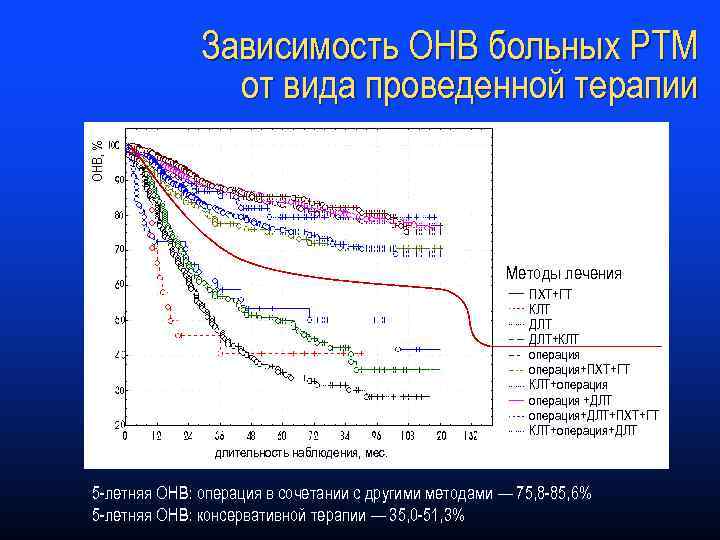 ОНВ, % Зависимость ОНВ больных РТМ от вида проведенной терапии Методы лечения ПХТ+ГТ КЛТ ДЛТ+КЛТ операция+ПХТ+ГТ КЛТ+операция +ДЛТ операция+ДЛТ+ПХТ+ГТ КЛТ+операция+ДЛТ длительность наблюдения, мес. 5 -летняя ОНВ: операция в сочетании с другими методами — 75, 8 -85, 6% 5 -летняя ОНВ: консервативной терапии — 35, 0 -51, 3%
ОНВ, % Зависимость ОНВ больных РТМ от вида проведенной терапии Методы лечения ПХТ+ГТ КЛТ ДЛТ+КЛТ операция+ПХТ+ГТ КЛТ+операция +ДЛТ операция+ДЛТ+ПХТ+ГТ КЛТ+операция+ДЛТ длительность наблюдения, мес. 5 -летняя ОНВ: операция в сочетании с другими методами — 75, 8 -85, 6% 5 -летняя ОНВ: консервативной терапии — 35, 0 -51, 3%
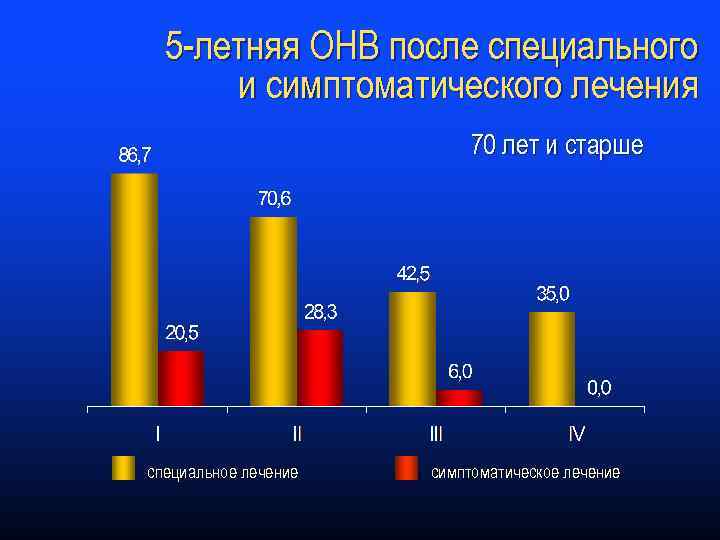 5 -летняя ОНВ после специального и симптоматического лечения 70 лет и старше специальное лечение симптоматическое лечение
5 -летняя ОНВ после специального и симптоматического лечения 70 лет и старше специальное лечение симптоматическое лечение
 Локализация рецидивов и метастазов Стадия I – метастазы в культе влагалища и парааортальных лимфоузлах II – метастазы в культе влагалища и подвздошных лимфоузлах III – метастазы в надключичных лимфоузлах Гистотип опухоли Степень дифференцировки опухоли эндометриоидный рак – рецидивы неэндометриоидный рак – метастазы в подвздошных лимфоузлах G 2 – метастазы в культе влагалища G 3 – метастазы в большом сальнике и по брюшине
Локализация рецидивов и метастазов Стадия I – метастазы в культе влагалища и парааортальных лимфоузлах II – метастазы в культе влагалища и подвздошных лимфоузлах III – метастазы в надключичных лимфоузлах Гистотип опухоли Степень дифференцировки опухоли эндометриоидный рак – рецидивы неэндометриоидный рак – метастазы в подвздошных лимфоузлах G 2 – метастазы в культе влагалища G 3 – метастазы в большом сальнике и по брюшине
 Результаты лечения с использованием новых методик предоперационной КЛТ Аппарат «micro. Selectron–HDR» , 192 Ir, доза — 13, 5 Гр Ring Applicator 4 -канальный Rotte Endometrial Applicator Рецидивы 0, 0% 2, 0% Метастазы 3, 9% 3, 3% 13, 9% Лучевые осложнения 5, 9% 3, 3% 0, 0% 5 -летняя ОНВ 100% 86, 1% 5 -летняя ВСР 96, 1% 96, 7% 87, 8% Параметр
Результаты лечения с использованием новых методик предоперационной КЛТ Аппарат «micro. Selectron–HDR» , 192 Ir, доза — 13, 5 Гр Ring Applicator 4 -канальный Rotte Endometrial Applicator Рецидивы 0, 0% 2, 0% Метастазы 3, 9% 3, 3% 13, 9% Лучевые осложнения 5, 9% 3, 3% 0, 0% 5 -летняя ОНВ 100% 86, 1% 5 -летняя ВСР 96, 1% 96, 7% 87, 8% Параметр
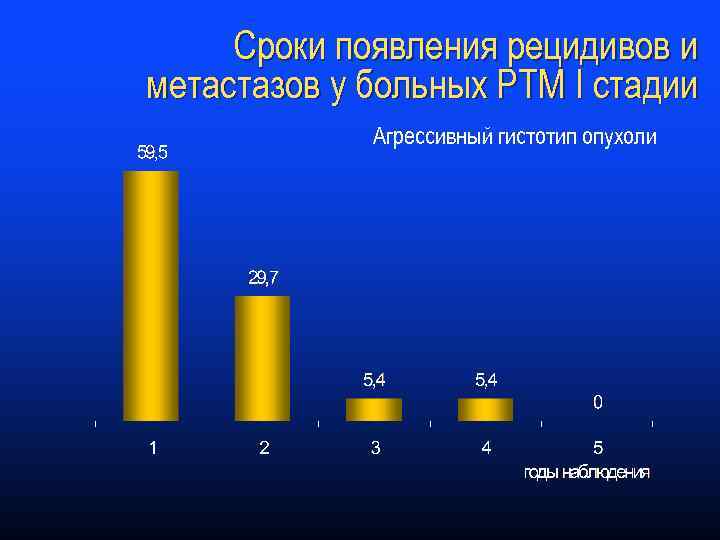 Сроки появления рецидивов и метастазов у больных РТМ I стадии Агрессивный гистотип опухоли
Сроки появления рецидивов и метастазов у больных РТМ I стадии Агрессивный гистотип опухоли
 Локализация рецидивов и метастазов у больных РТМ I стадии Агрессивный гистотип опухоли l l Рецидивы Метастазы n n n брюшина лимфатические узлы легкие культя влагалища кости множественные Метастазы возникают в 6 раз чаще, чем рецидивы 14, 3 85, 7 20, 0 11, 4 8, 6 2, 8 34, 3
Локализация рецидивов и метастазов у больных РТМ I стадии Агрессивный гистотип опухоли l l Рецидивы Метастазы n n n брюшина лимфатические узлы легкие культя влагалища кости множественные Метастазы возникают в 6 раз чаще, чем рецидивы 14, 3 85, 7 20, 0 11, 4 8, 6 2, 8 34, 3
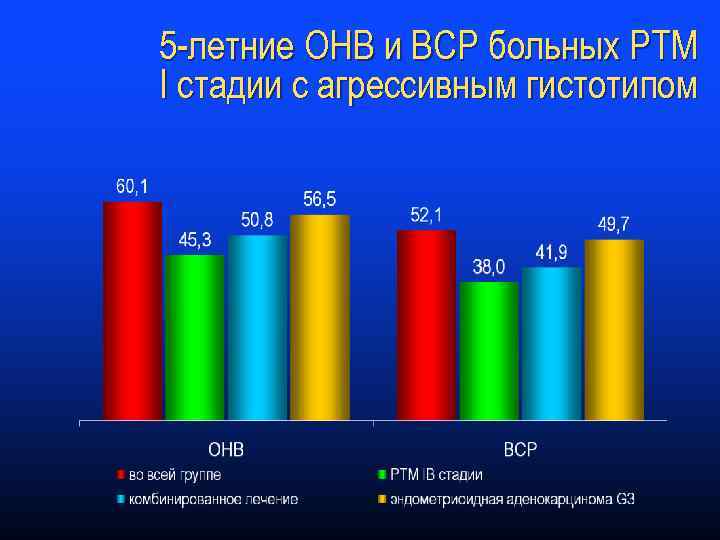 5 -летние ОНВ и ВСР больных РТМ I стадии с агрессивным гистотипом
5 -летние ОНВ и ВСР больных РТМ I стадии с агрессивным гистотипом
 Новая методика комплексного лечения резектабельного РТМ I–IV стадий Неблагоприятный прогноз ВЛОК КЛТ 5 процедур по 1 в день, 30 мин, аппарат «ЛЮЗАР-МП» 13, 5 Гр на середину миометрия, радионуклид 192 Ir операция пангистерэктомия, ЛАЭ, резекция большого сальника ВЛОК 5 процедур по 1 в день, 30 мин, аппарат «ЛЮЗАР-МП» 2 курса ПХТ+ВЛОК Винорельбин 25 мг/м 2, 1 -, 8 -й дни; цисплатин 20 мг/м 2, 1 -3 дни; этопозид 50 мг/м 2, 1 -5 дни ДЛТ+ВЛОК 40 Гр на область малого таза с 2 -х противолежащих полей размерами 16× 18, из которых 20 Гр с блоком 2– 4 курса ПХТ+ВЛОК Винорельбин 25 мг/м 2, 1 -, 8 -й дни; цисплатин 20 мг/м 2, 1 -3 дни; этопозид 50 мг/м 2, 1 -5 дни
Новая методика комплексного лечения резектабельного РТМ I–IV стадий Неблагоприятный прогноз ВЛОК КЛТ 5 процедур по 1 в день, 30 мин, аппарат «ЛЮЗАР-МП» 13, 5 Гр на середину миометрия, радионуклид 192 Ir операция пангистерэктомия, ЛАЭ, резекция большого сальника ВЛОК 5 процедур по 1 в день, 30 мин, аппарат «ЛЮЗАР-МП» 2 курса ПХТ+ВЛОК Винорельбин 25 мг/м 2, 1 -, 8 -й дни; цисплатин 20 мг/м 2, 1 -3 дни; этопозид 50 мг/м 2, 1 -5 дни ДЛТ+ВЛОК 40 Гр на область малого таза с 2 -х противолежащих полей размерами 16× 18, из которых 20 Гр с блоком 2– 4 курса ПХТ+ВЛОК Винорельбин 25 мг/м 2, 1 -, 8 -й дни; цисплатин 20 мг/м 2, 1 -3 дни; этопозид 50 мг/м 2, 1 -5 дни
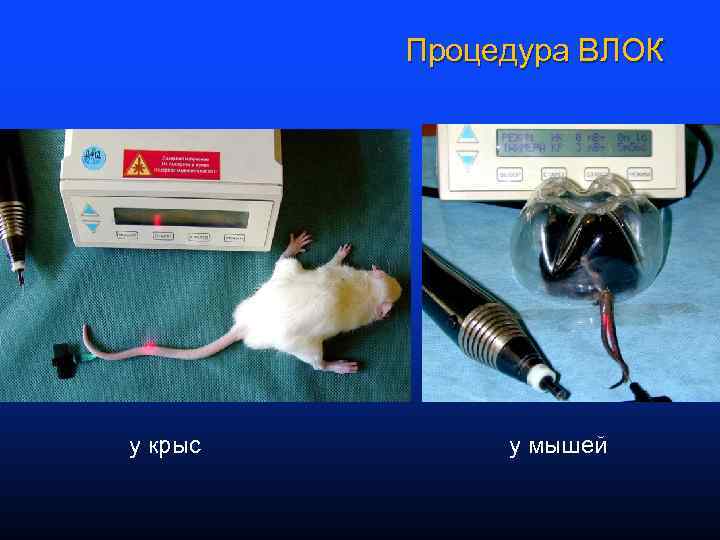 Процедура ВЛОК у крыс у мышей
Процедура ВЛОК у крыс у мышей
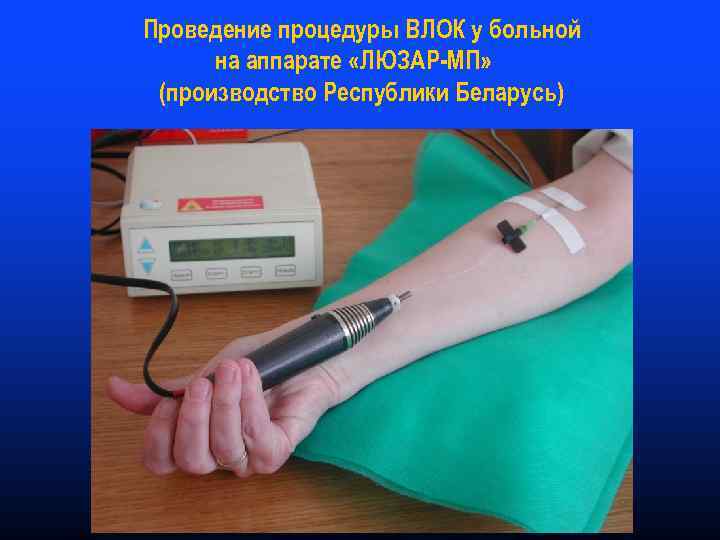 Проведение процедуры ВЛОК у больной на аппарате «ЛЮЗАР-МП» (производство Республики Беларусь)
Проведение процедуры ВЛОК у больной на аппарате «ЛЮЗАР-МП» (производство Республики Беларусь)
 Факторы прогноза 1. 2. 3. 4. 5. 6. 7. 8. 9. Стадия заболевания Гистотипы Степень дифференцировки опухоли Глубина инвазии в миометрий Распространение на другие структуры матки и на яичники Опухолевые эмболы в сосудах Размеры опухоли Раковые клетки в перитониальных смывах Содержание рецепторов прогестерона и эстрогенов в опухоли 10. Экспрессия отдельных онкогенов 11. Пожилой возраст 12. Метастазы в лимфоузлах 13. Диссеминация по брюшине
Факторы прогноза 1. 2. 3. 4. 5. 6. 7. 8. 9. Стадия заболевания Гистотипы Степень дифференцировки опухоли Глубина инвазии в миометрий Распространение на другие структуры матки и на яичники Опухолевые эмболы в сосудах Размеры опухоли Раковые клетки в перитониальных смывах Содержание рецепторов прогестерона и эстрогенов в опухоли 10. Экспрессия отдельных онкогенов 11. Пожилой возраст 12. Метастазы в лимфоузлах 13. Диссеминация по брюшине
 Общая наблюдаемая выживаемость больных раком тела матки % стадия
Общая наблюдаемая выживаемость больных раком тела матки % стадия
 ОБСЛЕДОВАНИЕ В ЖК ПЕРЕД НАПРАВЛЕНИЕМ В ОД: 1) общий анализ крови и мочи; 2) УЗИ органов малого таза и брюшной полости; 3) рентгенография легких (1 раз в год). РЕЖИМ НАБЛЮДЕНИЯ В ОД Ø первый и второй год – 1 раз в 3 мес. ; Ø третий год – 1 раз в 6 мес. ; Ø в последующем, пожизненно – 1 раз в год.
ОБСЛЕДОВАНИЕ В ЖК ПЕРЕД НАПРАВЛЕНИЕМ В ОД: 1) общий анализ крови и мочи; 2) УЗИ органов малого таза и брюшной полости; 3) рентгенография легких (1 раз в год). РЕЖИМ НАБЛЮДЕНИЯ В ОД Ø первый и второй год – 1 раз в 3 мес. ; Ø третий год – 1 раз в 6 мес. ; Ø в последующем, пожизненно – 1 раз в год.

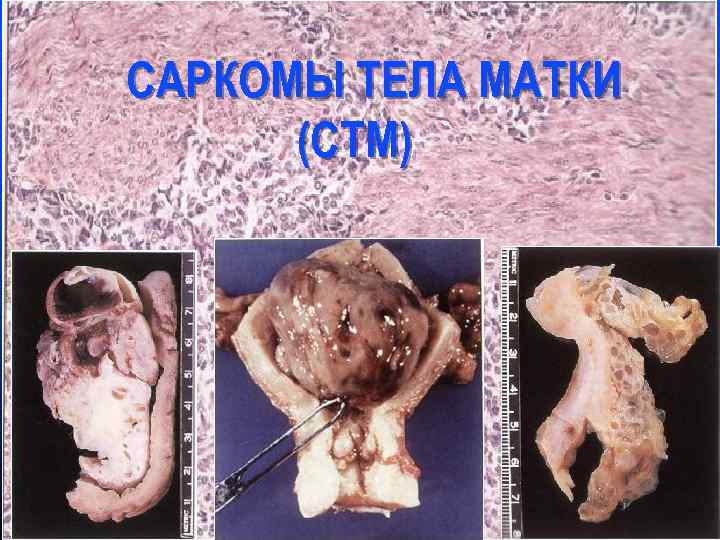 САРКОМЫ ТЕЛА МАТКИ (СТМ)
САРКОМЫ ТЕЛА МАТКИ (СТМ)
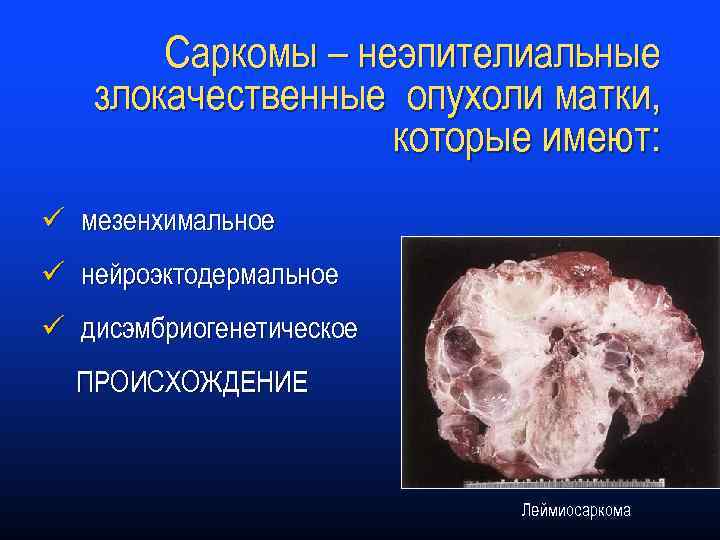 Саркомы – неэпителиальные злокачественные опухоли матки, которые имеют: ü мезенхимальное ü нейроэктодермальное ü дисэмбриогенетическое ПРОИСХОЖДЕНИЕ Леймиосаркома
Саркомы – неэпителиальные злокачественные опухоли матки, которые имеют: ü мезенхимальное ü нейроэктодермальное ü дисэмбриогенетическое ПРОИСХОЖДЕНИЕ Леймиосаркома
 Наиболее частые виды сарком тела матки В пубертатном возрасте – рабдомиосаркома В перименопаузальном – лейомиосаркома В постменопаузе – карциносаркома
Наиболее частые виды сарком тела матки В пубертатном возрасте – рабдомиосаркома В перименопаузальном – лейомиосаркома В постменопаузе – карциносаркома
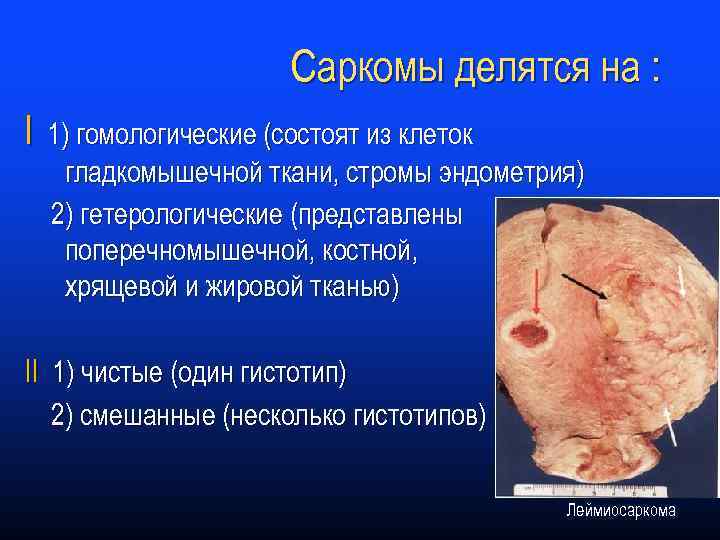 Саркомы делятся на : I 1) гомологические (состоят из клеток гладкомышечной ткани, стромы эндометрия) 2) гетерологические (представлены поперечномышечной, костной, хрящевой и жировой тканью) II 1) чистые (один гистотип) 2) смешанные (несколько гистотипов) Леймиосаркома
Саркомы делятся на : I 1) гомологические (состоят из клеток гладкомышечной ткани, стромы эндометрия) 2) гетерологические (представлены поперечномышечной, костной, хрящевой и жировой тканью) II 1) чистые (один гистотип) 2) смешанные (несколько гистотипов) Леймиосаркома
 ЗАБОЛЕВАЕМОСТЬ 0/ 0000 Грубый интенсивный показатель заболеваемости женщин Республики Беларусь в 2008 г. составил 2, 2% , 000 стандартизованный – 1, 5% 000.
ЗАБОЛЕВАЕМОСТЬ 0/ 0000 Грубый интенсивный показатель заболеваемости женщин Республики Беларусь в 2008 г. составил 2, 2% , 000 стандартизованный – 1, 5% 000.
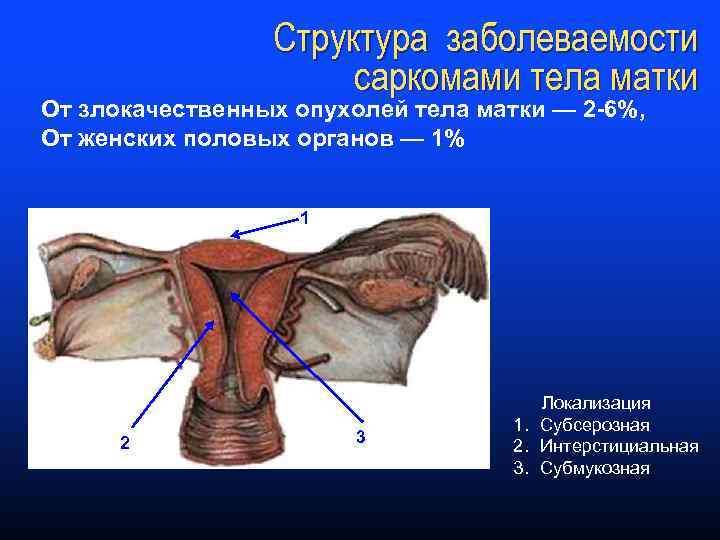 Структура заболеваемости саркомами тела матки От злокачественных опухолей тела матки — 2 -6%, От женских половых органов — 1% 1 2 3 Локализация 1. Субсерозная 2. Интерстициальная 3. Субмукозная
Структура заболеваемости саркомами тела матки От злокачественных опухолей тела матки — 2 -6%, От женских половых органов — 1% 1 2 3 Локализация 1. Субсерозная 2. Интерстициальная 3. Субмукозная
 Саркомы тела матки в РБ Составляют в структуре – 0, 6% У молодых женщин встречается в 6, 0% случаев Возраст больных – 40 -74 года (85%) Средний возраст больных – 56 лет За последние 5 лет число больных саркомами в стране увеличилось в 1, 5 раза
Саркомы тела матки в РБ Составляют в структуре – 0, 6% У молодых женщин встречается в 6, 0% случаев Возраст больных – 40 -74 года (85%) Средний возраст больных – 56 лет За последние 5 лет число больных саркомами в стране увеличилось в 1, 5 раза
 САРКОМЫ ТЕЛА МАТКИ Наиболее часто в Республике Беларусь диагностируются лейомиосаркома (41(35, 3%)), эндометриальная стромальная саркома (26(22, 4%)) и карциносаркома (21(18, 1%)). Встречаются также единичные случаи мелкоклеточной саркомы и аденосаркомы.
САРКОМЫ ТЕЛА МАТКИ Наиболее часто в Республике Беларусь диагностируются лейомиосаркома (41(35, 3%)), эндометриальная стромальная саркома (26(22, 4%)) и карциносаркома (21(18, 1%)). Встречаются также единичные случаи мелкоклеточной саркомы и аденосаркомы.
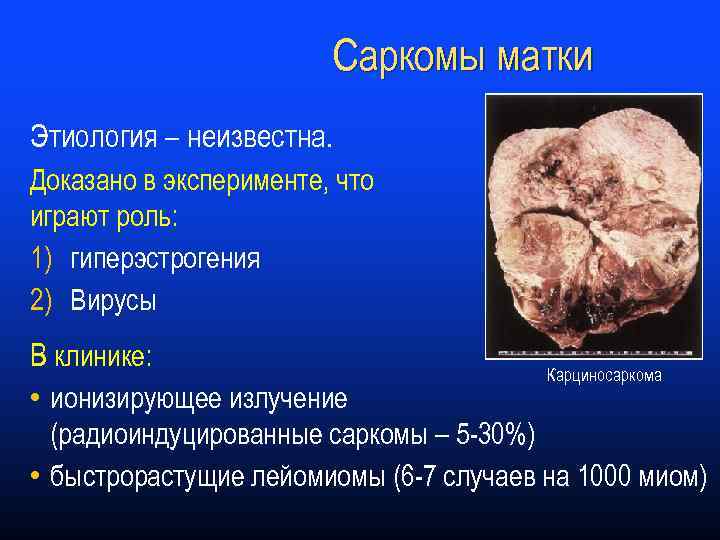 Саркомы матки Этиология – неизвестна. Доказано в эксперименте, что играют роль: 1) гиперэстрогения 2) Вирусы В клинике: • ионизирующее излучение Карциносаркома (радиоиндуцированные саркомы – 5 -30%) • быстрорастущие лейомиомы (6 -7 случаев на 1000 миом)
Саркомы матки Этиология – неизвестна. Доказано в эксперименте, что играют роль: 1) гиперэстрогения 2) Вирусы В клинике: • ионизирующее излучение Карциносаркома (радиоиндуцированные саркомы – 5 -30%) • быстрорастущие лейомиомы (6 -7 случаев на 1000 миом)
 Классификация сарком матки Гомологические Чистые Лейомиосаркома Стромальная саркома Эндолимфатический стромальный миоз Ангиосаркома Аденосаркома Смешанные Злокачественная мюллеровская смешанная опухоль с гомологическим компонентом Гетерологические Рабдомиосаркома Остеосаркома Липосаркома Хондросаркома Злокачественная мюллеровская смешанная опухоль с гетерологическим компонентом
Классификация сарком матки Гомологические Чистые Лейомиосаркома Стромальная саркома Эндолимфатический стромальный миоз Ангиосаркома Аденосаркома Смешанные Злокачественная мюллеровская смешанная опухоль с гомологическим компонентом Гетерологические Рабдомиосаркома Остеосаркома Липосаркома Хондросаркома Злокачественная мюллеровская смешанная опухоль с гетерологическим компонентом
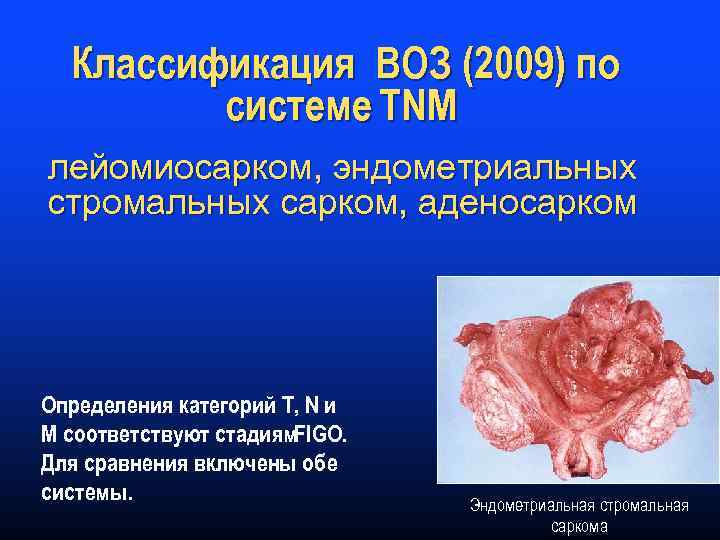 Классификация ВОЗ (2009) по системе TNM лейомиосарком, эндометриальных стромальных сарком, аденосарком Определения категорий Т, N и М соответствуют стадиям. FIGO. Для сравнения включены обе системы. Эндометриальная стромальная саркома
Классификация ВОЗ (2009) по системе TNM лейомиосарком, эндометриальных стромальных сарком, аденосарком Определения категорий Т, N и М соответствуют стадиям. FIGO. Для сравнения включены обе системы. Эндометриальная стромальная саркома
 Правила классификации Классификацию применяют ко всем саркомам, за исключением карциносаркомы, которую классифицирует вместе с карциномой эндометрия. Требуется гистологическое подтверждение новообразования и разделение по гистологическому типу. Для определения категорий Т, N и М показано проведение следующих исследовании: Категория Т фиэикальное обследование и лучевые методы исследования Категория N физикальное обследование и лучевые методы исследования Категория М физикальное обследование и лучевые методы исследования Стадии FIGO основаны на хирургических данных, а категории TNM основаны на клинической и/или патологоанатомической классификации.
Правила классификации Классификацию применяют ко всем саркомам, за исключением карциносаркомы, которую классифицирует вместе с карциномой эндометрия. Требуется гистологическое подтверждение новообразования и разделение по гистологическому типу. Для определения категорий Т, N и М показано проведение следующих исследовании: Категория Т фиэикальное обследование и лучевые методы исследования Категория N физикальное обследование и лучевые методы исследования Категория М физикальное обследование и лучевые методы исследования Стадии FIGO основаны на хирургических данных, а категории TNM основаны на клинической и/или патологоанатомической классификации.
 Правила классификации Анатомические отделы Шейка матки (С 53) Перешеек матки (С 54. 0) Дно матки (С 54. 3) Гистологические типы Лейомиосаркома Эндометриальная стромальная саркома Аденосаркома Региональные лимфатические узлы Региональными лимфатическими узлами являются тазовые [подчревные (внутренние подвздошные, запирательные), общие и наружные подвздошные, околоматочные и крестцовые] и околоаортальные узлы.
Правила классификации Анатомические отделы Шейка матки (С 53) Перешеек матки (С 54. 0) Дно матки (С 54. 3) Гистологические типы Лейомиосаркома Эндометриальная стромальная саркома Аденосаркома Региональные лимфатические узлы Региональными лимфатическими узлами являются тазовые [подчревные (внутренние подвздошные, запирательные), общие и наружные подвздошные, околоматочные и крестцовые] и околоаортальные узлы.
 Правила классификации Клиническая классификация TNM Лейомиосаркома, эндометриальная стромальная саркома Категории Стадии TNM FIGO T 1 I Опухоль ограничена маткой T 1 a IA Опухоль не более 5 см в наибольшем измерении T 1 b IB Опухоль более 5 см в наибольшем измерении Т 2 II Т 2 а Опухоль прорастает за пределы матки, но в пределах таза IIА Опухоль прорастает в придатки Т 2 b IIВ Опухоль прорастает в другие ткани таза
Правила классификации Клиническая классификация TNM Лейомиосаркома, эндометриальная стромальная саркома Категории Стадии TNM FIGO T 1 I Опухоль ограничена маткой T 1 a IA Опухоль не более 5 см в наибольшем измерении T 1 b IB Опухоль более 5 см в наибольшем измерении Т 2 II Т 2 а Опухоль прорастает за пределы матки, но в пределах таза IIА Опухоль прорастает в придатки Т 2 b IIВ Опухоль прорастает в другие ткани таза
 Правила классификации Клиническая классификация TNM Лейомиосаркома, эндометриальная стромальная саркома Т – первичная опухоль ТЗ и/или N 1 III Опухоль прорастает в тканибрюшной полости ТЗа IIIA Одна локализация ТЗb IIIB Более одной локализации N 1 IIIC Метастазы в региональных лимфатических узлах Т 4 IVA Опухоль прорастает в слизистую оболочку мочевого пузыря илипрямой кишки М 1 IVB Отдаленные метастазы Примечание: симультанные опухоли тела матки и яичников/ таза в сочетании с эндометриозом яичников/таза нужно классифицировать как самостоятельные первичные опухоли.
Правила классификации Клиническая классификация TNM Лейомиосаркома, эндометриальная стромальная саркома Т – первичная опухоль ТЗ и/или N 1 III Опухоль прорастает в тканибрюшной полости ТЗа IIIA Одна локализация ТЗb IIIB Более одной локализации N 1 IIIC Метастазы в региональных лимфатических узлах Т 4 IVA Опухоль прорастает в слизистую оболочку мочевого пузыря илипрямой кишки М 1 IVB Отдаленные метастазы Примечание: симультанные опухоли тела матки и яичников/ таза в сочетании с эндометриозом яичников/таза нужно классифицировать как самостоятельные первичные опухоли.
 Правила классификации Клиническая классификация TNM Аденосаркома Т – первичная опухоль Категории Стадии TNM Т 1 FIGO I Опухоль ограничена маткой Т 1 а IA Опухоль ограничена эндометрием /эндоцервиксом Т 1 b IB Опухоль прорастает в миометрий менее половины его толщи Т 1 с IС Опухоль прорастает в миометрий на половину или более Т 2 II Опухоль прорастает за пределы матки, но в пределах таза Т 2 а IIА Опухоль прорастает в придатки Т 2 b IIВ Опухоль прорастает в другие ткани таза
Правила классификации Клиническая классификация TNM Аденосаркома Т – первичная опухоль Категории Стадии TNM Т 1 FIGO I Опухоль ограничена маткой Т 1 а IA Опухоль ограничена эндометрием /эндоцервиксом Т 1 b IB Опухоль прорастает в миометрий менее половины его толщи Т 1 с IС Опухоль прорастает в миометрий на половину или более Т 2 II Опухоль прорастает за пределы матки, но в пределах таза Т 2 а IIА Опухоль прорастает в придатки Т 2 b IIВ Опухоль прорастает в другие ткани таза
 Правила классификации Клиническая классификация TNM Аденосаркома Т – первичная опухоль ТЗ и/или N 1 III Опухоль прорастает в тканибрюшной полости ТЗа IIIA Одна локализация ТЗb IIIB Более одной локализации N 1 IIIC Метастазы в региональных лимфатических узлах Т 4 IVA Опухоль прорастает в слизистую оболочку мочевого пузыря или прямой кишки М 1 IVB Отдаленные метастазы Примечание: симультанные опухоли тела матки и яичников/ таза в сочетании с эндометриозом яичников/таза нужно классифицировать как самостоятельные первичные опухоли.
Правила классификации Клиническая классификация TNM Аденосаркома Т – первичная опухоль ТЗ и/или N 1 III Опухоль прорастает в тканибрюшной полости ТЗа IIIA Одна локализация ТЗb IIIB Более одной локализации N 1 IIIC Метастазы в региональных лимфатических узлах Т 4 IVA Опухоль прорастает в слизистую оболочку мочевого пузыря или прямой кишки М 1 IVB Отдаленные метастазы Примечание: симультанные опухоли тела матки и яичников/ таза в сочетании с эндометриозом яичников/таза нужно классифицировать как самостоятельные первичные опухоли.
 Правила классификации N — Региональные лимфатические узлы NX Региональные лимфатические узлы не могут быть оценены N 0 Нет метастазов в региональных лимфатических узлах N 1 Есть метастазы в региональных лимфатических узлах М — Отдаленные метастазы М 0 Нет отдаленных метастазов М 1 Есть отдаленные метастазы за исключением метастазов в придатках, тканях малого таза и брюшной полости Патологоанатомическая классификацияp. TNM Категории р. Т и p. N соответствуют категориям Т и N.
Правила классификации N — Региональные лимфатические узлы NX Региональные лимфатические узлы не могут быть оценены N 0 Нет метастазов в региональных лимфатических узлах N 1 Есть метастазы в региональных лимфатических узлах М — Отдаленные метастазы М 0 Нет отдаленных метастазов М 1 Есть отдаленные метастазы за исключением метастазов в придатках, тканях малого таза и брюшной полости Патологоанатомическая классификацияp. TNM Категории р. Т и p. N соответствуют категориям Т и N.
 Правила классификации СТАДИИ T 1 N 0 Т 1 a N 0 T 1 b N 0 T 1 c N 0 T 2 N 0 Т 2 а N 0 Т 2 b N 0 ТЗа N 0 ТЗb N 0 T 1, T 2, T 3 N 1 Т 4 Любая N Любая Т Любая N Стадия I М 0 Стадия IA М 0 Стадия IB М 0 Стадия IC* М 0 Стадия IIА М 0 Стадия IIВ М 0 Стадия IIIА М 0 Стадия IIIВ М 0 Стадия IIIC М 0 Стадия IV А М 0 Стадия IVB М 1 * Стадию IС не применяют для лейомиосаркомы и эндометриальной стромальной саркомы.
Правила классификации СТАДИИ T 1 N 0 Т 1 a N 0 T 1 b N 0 T 1 c N 0 T 2 N 0 Т 2 а N 0 Т 2 b N 0 ТЗа N 0 ТЗb N 0 T 1, T 2, T 3 N 1 Т 4 Любая N Любая Т Любая N Стадия I М 0 Стадия IA М 0 Стадия IB М 0 Стадия IC* М 0 Стадия IIА М 0 Стадия IIВ М 0 Стадия IIIА М 0 Стадия IIIВ М 0 Стадия IIIC М 0 Стадия IV А М 0 Стадия IVB М 1 * Стадию IС не применяют для лейомиосаркомы и эндометриальной стромальной саркомы.
 МОРФОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ МЕЗЕНХИМАЛЬНЫХ И СМЕШАННЫХ ОПУХОЛЕЙ МАТКИ (ВОЗ, 2003 г. ). q Мезенхимальные опухоли q Эндометриальные стромальные опухоли: § эндометриальная стромальная саркома низкой степени злокачественности; § эндометриальный стромальный узелок; § недифференцированная эндометриальная саркома. q Гладкомышечные опухоли: § лейомиосаркома: - эпителиоидный вариант; - миксоидный вариант; § гладкомышечные опухоли с неясным злокачественным потенциалом;
МОРФОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ МЕЗЕНХИМАЛЬНЫХ И СМЕШАННЫХ ОПУХОЛЕЙ МАТКИ (ВОЗ, 2003 г. ). q Мезенхимальные опухоли q Эндометриальные стромальные опухоли: § эндометриальная стромальная саркома низкой степени злокачественности; § эндометриальный стромальный узелок; § недифференцированная эндометриальная саркома. q Гладкомышечные опухоли: § лейомиосаркома: - эпителиоидный вариант; - миксоидный вариант; § гладкомышечные опухоли с неясным злокачественным потенциалом;
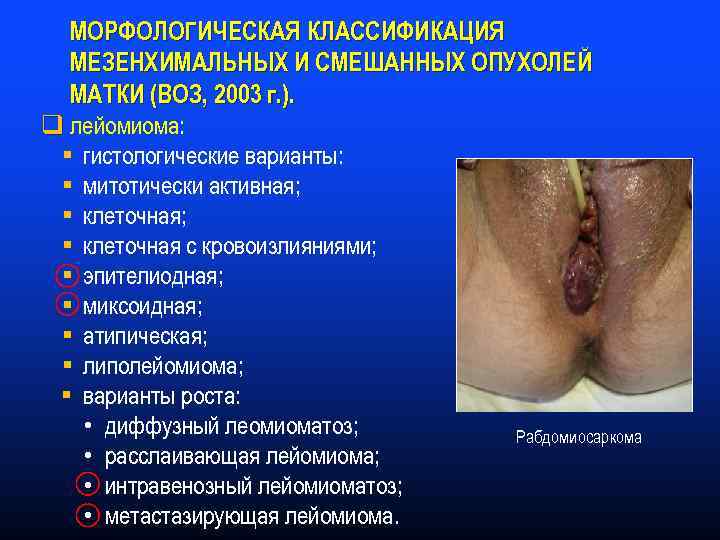 МОРФОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ МЕЗЕНХИМАЛЬНЫХ И СМЕШАННЫХ ОПУХОЛЕЙ МАТКИ (ВОЗ, 2003 г. ). q лейомиома: § гистологические варианты: § митотически активная; § клеточная с кровоизлияниями; § эпителиодная; § миксоидная; § атипическая; § липолейомиома; § варианты роста: • диффузный леомиоматоз; Рабдомиосаркома • расслаивающая лейомиома; • интравенозный лейомиоматоз; • метастазирующая лейомиома.
МОРФОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ МЕЗЕНХИМАЛЬНЫХ И СМЕШАННЫХ ОПУХОЛЕЙ МАТКИ (ВОЗ, 2003 г. ). q лейомиома: § гистологические варианты: § митотически активная; § клеточная с кровоизлияниями; § эпителиодная; § миксоидная; § атипическая; § липолейомиома; § варианты роста: • диффузный леомиоматоз; Рабдомиосаркома • расслаивающая лейомиома; • интравенозный лейомиоматоз; • метастазирующая лейомиома.
 МОРФОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ МЕЗЕНХИМАЛЬНЫХ И СМЕШАННЫХ ОПУХОЛЕЙ МАТКИ (ВОЗ, 2003 г. ). Другие мезенхимальные опухоли: • смешанные эндометриальные стромальные и гладкомышечные опухоли; • периваскулярная эпителиоидноклеточная опухоль; • аденоматоидная опухоль; • другие злокачественные мезенхимальные опухоли; • другие доброкачественные мезенхимальные опухоли. §Смешанные эпителиальные и мезенхимальные опухоли: • карциносаркома (злокачественная мюллеровская смешанная опухоль, метапластический рак); • аденосаркома; • карцинофиброма; • аденомиома: • атипичный полиповидный вариант
МОРФОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ МЕЗЕНХИМАЛЬНЫХ И СМЕШАННЫХ ОПУХОЛЕЙ МАТКИ (ВОЗ, 2003 г. ). Другие мезенхимальные опухоли: • смешанные эндометриальные стромальные и гладкомышечные опухоли; • периваскулярная эпителиоидноклеточная опухоль; • аденоматоидная опухоль; • другие злокачественные мезенхимальные опухоли; • другие доброкачественные мезенхимальные опухоли. §Смешанные эпителиальные и мезенхимальные опухоли: • карциносаркома (злокачественная мюллеровская смешанная опухоль, метапластический рак); • аденосаркома; • карцинофиброма; • аденомиома: • атипичный полиповидный вариант
 ДИАГНОСТИКА САРКОМ ТЕЛА МАТКИ 1. Гинекологический осмотр 2. Эхоскопия органов брюшной полости 3. Аспирация содержимого из полости матки для 4. 5. 6. 7. цитологического исследования Раздельное диагностическое выскабливание слизистой полости матки и цервикального канала, лучше в сочетании с гистероскопией. Информативность при КСМ – 80%, ЭСС – 58%, ЛМС – 10% ЭКГ Общий анализ крови, мочи, биохимический анализ сыворотки крови и другие Рентгенография легких
ДИАГНОСТИКА САРКОМ ТЕЛА МАТКИ 1. Гинекологический осмотр 2. Эхоскопия органов брюшной полости 3. Аспирация содержимого из полости матки для 4. 5. 6. 7. цитологического исследования Раздельное диагностическое выскабливание слизистой полости матки и цервикального канала, лучше в сочетании с гистероскопией. Информативность при КСМ – 80%, ЭСС – 58%, ЛМС – 10% ЭКГ Общий анализ крови, мочи, биохимический анализ сыворотки крови и другие Рентгенография легких
 ДИАГНОСТИКА САРКОМ ТЕЛА МАТКИ По показаниям 1. Экскреторная урография 2. Цистоскопия 3. Колоноскопия 4. Ирригоскопия 5. Сцинциграфия костей скелета 6. КТ органов брюшной полости 7. МРТ органов малого таза 8. Иммуногистохимическое исследование: р53, Bax, Her-2/neu, Bcl-2, Fas. L, v. FGF и др. , участвующие в апоптозе и ангиогенезе 9. Опухолевые маркеры: ЛМС – актин, ЭСС – виментин, КСМ – цитокератины и виментин, РМС – десмин
ДИАГНОСТИКА САРКОМ ТЕЛА МАТКИ По показаниям 1. Экскреторная урография 2. Цистоскопия 3. Колоноскопия 4. Ирригоскопия 5. Сцинциграфия костей скелета 6. КТ органов брюшной полости 7. МРТ органов малого таза 8. Иммуногистохимическое исследование: р53, Bax, Her-2/neu, Bcl-2, Fas. L, v. FGF и др. , участвующие в апоптозе и ангиогенезе 9. Опухолевые маркеры: ЛМС – актин, ЭСС – виментин, КСМ – цитокератины и виментин, РМС – десмин
 КЛИНИКА САРКОМ ТЕЛА МАТКИ Представлена 2 симптомами 1. Кровотечением из половых путей • при ЛМС – в 33% случаев; • ЭСС – в 55%; • КСМ – в 70% Источник кровотечения: у больных ЛМС и ЭСС – гиперплазированный или атрофичный эндометрий; при КСМ – распадающаяся опухоль 2. Быстрым ростом матки • при ЛМС – в 42% случаев; • при ЭСС – в 26%
КЛИНИКА САРКОМ ТЕЛА МАТКИ Представлена 2 симптомами 1. Кровотечением из половых путей • при ЛМС – в 33% случаев; • ЭСС – в 55%; • КСМ – в 70% Источник кровотечения: у больных ЛМС и ЭСС – гиперплазированный или атрофичный эндометрий; при КСМ – распадающаяся опухоль 2. Быстрым ростом матки • при ЛМС – в 42% случаев; • при ЭСС – в 26%
 Пути метастазирования 1. Гематогенный (основной) 2. Лимфогенный (редко) 3. Диссеминация по брюшине 4. Прорастание в близлежащие с маткой органы Аденосаркома
Пути метастазирования 1. Гематогенный (основной) 2. Лимфогенный (редко) 3. Диссеминация по брюшине 4. Прорастание в близлежащие с маткой органы Аденосаркома
 НЕБЛАГОПРИЯТНЫЕ ФАКТОРЫ ПРОГНОЗА САРКОМ ТЕЛА МАТКИ Эндометриальная стромальная саркома • Пери- и постменопауза • III-IV стадия • Возраст > 50 лет • Размер опухоли > 10 см • Нерадикальная • Высокая степень злокачественности • Число митозов > 10 в 10 операция (недифференцированная полях зрения под • Наличие эндометриальная микроскопом гетерологического саркома) саркоматозного • Наличие некрозов в компонента • Размер опухоли > 10 см опухоли • Инвазия в миометрий • Наличие некрозов в > ½ его толщины опухоли Лейомиосаркома Карциносаркома
НЕБЛАГОПРИЯТНЫЕ ФАКТОРЫ ПРОГНОЗА САРКОМ ТЕЛА МАТКИ Эндометриальная стромальная саркома • Пери- и постменопауза • III-IV стадия • Возраст > 50 лет • Размер опухоли > 10 см • Нерадикальная • Высокая степень злокачественности • Число митозов > 10 в 10 операция (недифференцированная полях зрения под • Наличие эндометриальная микроскопом гетерологического саркома) саркоматозного • Наличие некрозов в компонента • Размер опухоли > 10 см опухоли • Инвазия в миометрий • Наличие некрозов в > ½ его толщины опухоли Лейомиосаркома Карциносаркома
 ОБЩИЕ ПРИНЦИПЫ ЛЕЧЕНИЯ Основной метод терапии – хирургический . На I этапе выполняется операция – экстирпация матки с придатками. Объем расширяется: 1) при неблагоприятных факторах у больных с ЛМС до гистерэктомии II типа (ЭМП + лимфодиссекция), 2) при недифференцированной ЭСС и КСМ до гистерэктомии II типа и удаления большого сальника. У женщин репродуктивного возраста с ЛМС без неблагоприятных факторов возможно выполнить только консервативную миомэктомию и оставить яичники, т. к. при их удалении в 1, 5 раза чаще появляется диссеминация по брюшине и выживаемость уменьшается в 2 раза.
ОБЩИЕ ПРИНЦИПЫ ЛЕЧЕНИЯ Основной метод терапии – хирургический . На I этапе выполняется операция – экстирпация матки с придатками. Объем расширяется: 1) при неблагоприятных факторах у больных с ЛМС до гистерэктомии II типа (ЭМП + лимфодиссекция), 2) при недифференцированной ЭСС и КСМ до гистерэктомии II типа и удаления большого сальника. У женщин репродуктивного возраста с ЛМС без неблагоприятных факторов возможно выполнить только консервативную миомэктомию и оставить яичники, т. к. при их удалении в 1, 5 раза чаще появляется диссеминация по брюшине и выживаемость уменьшается в 2 раза.
 ОБЩИЕ ПРИНЦИПЫ ЛЕЧЕНИЯ При выполнении ампутации матки с придатками в гинекологических стационарах по поводу миомы в дальнейшем у больных с ЛМС шейка удаляется при наличии: 1) опухолевого узла в ней, 2) саркоматозных клеток в крае отсечения. Органосохраняющие операции при КСМ и ЭСС не допускаются.
ОБЩИЕ ПРИНЦИПЫ ЛЕЧЕНИЯ При выполнении ампутации матки с придатками в гинекологических стационарах по поводу миомы в дальнейшем у больных с ЛМС шейка удаляется при наличии: 1) опухолевого узла в ней, 2) саркоматозных клеток в крае отсечения. Органосохраняющие операции при КСМ и ЭСС не допускаются.
 ЛУЧЕВОЕ ЛЕЧЕНИЕ ДЛТ в дозе 40 -50 Гр на область малого таза при КСМ и ЭСС. КЛТ культи влагалища показана при наличии опухоли в крае отсечения. СЛТ показана при неоперабельности больной: ДЛТ – 40 -50 Гр, КЛТ – 60 -80 Гр. Лучевую терапию при ЛМС не проводят из-за низкой чувствительности опухоли к облучению
ЛУЧЕВОЕ ЛЕЧЕНИЕ ДЛТ в дозе 40 -50 Гр на область малого таза при КСМ и ЭСС. КЛТ культи влагалища показана при наличии опухоли в крае отсечения. СЛТ показана при неоперабельности больной: ДЛТ – 40 -50 Гр, КЛТ – 60 -80 Гр. Лучевую терапию при ЛМС не проводят из-за низкой чувствительности опухоли к облучению
 ХИМИОТЕРАПИЯ Самостоятельно не используется, т. к. эффективность составляет 15 -30%. В качестве комплексного лечения при: ЛМС с неблагоприятными факторами прогноза; ЭСС (недифференцированная) – I-II стадии КСМ (недифференцированная) – I-II стадии Число курсов – 6, интервал – 4 недели. Цитостатики: ифосфамид, доксорубицин, гемцитабин, цисплатин, паклитаксел, топотекан.
ХИМИОТЕРАПИЯ Самостоятельно не используется, т. к. эффективность составляет 15 -30%. В качестве комплексного лечения при: ЛМС с неблагоприятными факторами прогноза; ЭСС (недифференцированная) – I-II стадии КСМ (недифференцированная) – I-II стадии Число курсов – 6, интервал – 4 недели. Цитостатики: ифосфамид, доксорубицин, гемцитабин, цисплатин, паклитаксел, топотекан.
 ГОРМОНОТЕРАПИЯ Проводят только при прогрессировании любого вида сарком, как паллиативное лечение. Гормоны: § препараты прогестинового ряда, § ингибитор ароматазы, § аналоги гонадолиберина
ГОРМОНОТЕРАПИЯ Проводят только при прогрессировании любого вида сарком, как паллиативное лечение. Гормоны: § препараты прогестинового ряда, § ингибитор ароматазы, § аналоги гонадолиберина
 Наиболее распространенные схемы специального лечения сарком матки Адъювантная Гистотип лучевая Адъювантная терапия Лейомиосаркома Тотальная Нет При наличии двух и более гистерэктомия с неблагоприятных аднексэктомией. прогностических При наличии признаков неблагоприятных 3 цикла ифосфамидом признаков (1, 2 г/м 2 1 -3 дни) + прогноза + доксорубицином (20 мг/м 2 тазовая 1 -3 дни)/эпирубицином (25 лимфодиссекция мг/м 2 1 -3 дни) каждые 3 недели Хирургическое лечение
Наиболее распространенные схемы специального лечения сарком матки Адъювантная Гистотип лучевая Адъювантная терапия Лейомиосаркома Тотальная Нет При наличии двух и более гистерэктомия с неблагоприятных аднексэктомией. прогностических При наличии признаков неблагоприятных 3 цикла ифосфамидом признаков (1, 2 г/м 2 1 -3 дни) + прогноза + доксорубицином (20 мг/м 2 тазовая 1 -3 дни)/эпирубицином (25 лимфодиссекция мг/м 2 1 -3 дни) каждые 3 недели Хирургическое лечение
 Наиболее распространенные схемы специального лечения сарком матки Карциносаркома Тотальная Облучение гистерэктомия с малого таза аднексэктомией + тазовая и, или парааортальная лимфодиссекция + удаление большого сальника 3 цикла цисплатином (20 мг/м 2 1 -3 дни) + ифосфамидом (1, 2 г/м 2 1/3 дни) ± доксорубицином (20 мг/м 2 1 -3 дни) /эпирубицином (25 мг/м 2 1 -3 дни) каждые 3 недели
Наиболее распространенные схемы специального лечения сарком матки Карциносаркома Тотальная Облучение гистерэктомия с малого таза аднексэктомией + тазовая и, или парааортальная лимфодиссекция + удаление большого сальника 3 цикла цисплатином (20 мг/м 2 1 -3 дни) + ифосфамидом (1, 2 г/м 2 1/3 дни) ± доксорубицином (20 мг/м 2 1 -3 дни) /эпирубицином (25 мг/м 2 1 -3 дни) каждые 3 недели
 Наиболее распространенные схемы специального лечения сарком матки Эндометриальная стромальная саркома Низкой степени Тотальная Облучение дифференцировки гистерэктомия с малого таза при аднексэктомией остаточной опухоли в малом тазу Недифференциро- Тотальная Облучение ванная гистерэктомия с малого таза аднексэктомией + тазовая лимфодиссекция + удаление большого сальника Прогестинотерапия мегестрол ацетатом 160 мг ежедневно в течение 24 месяцев 3 цикла ифосфамидом (1, 2 г/м 2 1 -3 дни) + доксорубицином (20 мг/м 2 1 -3 дни) /эпирубицином (25 мг/м 2 1 -3 дни) каждые 3 недели
Наиболее распространенные схемы специального лечения сарком матки Эндометриальная стромальная саркома Низкой степени Тотальная Облучение дифференцировки гистерэктомия с малого таза при аднексэктомией остаточной опухоли в малом тазу Недифференциро- Тотальная Облучение ванная гистерэктомия с малого таза аднексэктомией + тазовая лимфодиссекция + удаление большого сальника Прогестинотерапия мегестрол ацетатом 160 мг ежедневно в течение 24 месяцев 3 цикла ифосфамидом (1, 2 г/м 2 1 -3 дни) + доксорубицином (20 мг/м 2 1 -3 дни) /эпирубицином (25 мг/м 2 1 -3 дни) каждые 3 недели
 Наблюдение, сроки и объем обследования Объем обследования: клиническое обследование; лабораторное исследование; гинекологическое исследование; взятие мазков из влагалища для цитологического исследования; эхоскопия органов брюшной полости и малого таза (при наличии жалоб); Ø осмотр молочных желез (1 раз в год); Ø рентгенография органов грудной клетки (1 раз в год). По показаниям: сцинтиграфия костей скелета, компьютерная томография, ирригоскопия, колоноскопия, внутривенная урография. Режим наблюдения: § первый и второй год – 1 раз в 3 мес. ; § третий год – 1 раз в 6 мес. ; § в последующем, пожизненно – 1 раз в год. Ø Ø Ø
Наблюдение, сроки и объем обследования Объем обследования: клиническое обследование; лабораторное исследование; гинекологическое исследование; взятие мазков из влагалища для цитологического исследования; эхоскопия органов брюшной полости и малого таза (при наличии жалоб); Ø осмотр молочных желез (1 раз в год); Ø рентгенография органов грудной клетки (1 раз в год). По показаниям: сцинтиграфия костей скелета, компьютерная томография, ирригоскопия, колоноскопия, внутривенная урография. Режим наблюдения: § первый и второй год – 1 раз в 3 мес. ; § третий год – 1 раз в 6 мес. ; § в последующем, пожизненно – 1 раз в год. Ø Ø Ø
 ПРИЧИНЫ НИЗКОЙ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ САРКОМ ТЕЛА МАТКИ Ø Поздняя диагностика Ø Большое число неблагоприятных факторов Ø Агрессивное течение Ø Отсутствие четких рекомендаций по лечению Ø Низкий уровень знаний медицинского персонала
ПРИЧИНЫ НИЗКОЙ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ САРКОМ ТЕЛА МАТКИ Ø Поздняя диагностика Ø Большое число неблагоприятных факторов Ø Агрессивное течение Ø Отсутствие четких рекомендаций по лечению Ø Низкий уровень знаний медицинского персонала
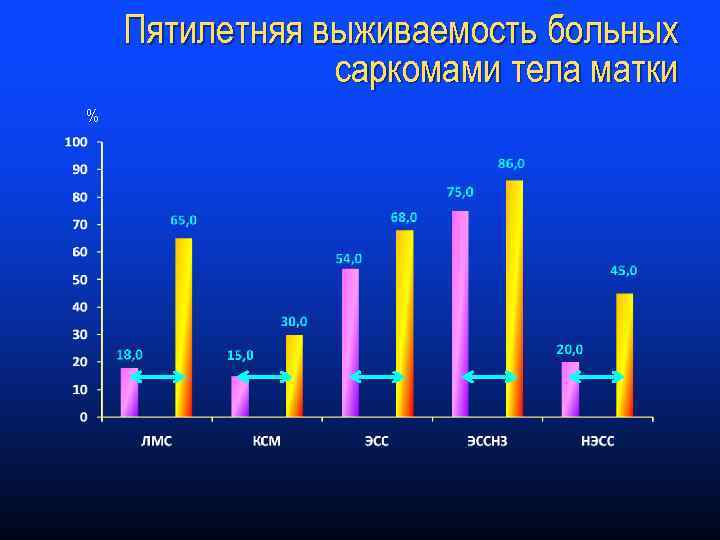 Пятилетняя выживаемость больных саркомами тела матки %
Пятилетняя выживаемость больных саркомами тела матки %



