Рак предстательной железы.pptx
- Количество слайдов: 31

Рак предстательной железы БГМУ Кафедра онкологии Е. Г. Мороз, к. м. н.

Заболеваемость • В США заболеваемость раком простаты росла в течение 20 лет и достигла пика 100 : 100 000 мужчин, затем вышла на плато. Рост заболеваемости объясняется в основном улучшением диагностики, прежде всего благодаря определению ПСА и ТРУЗИ. • С возрастом растет и заболеваемость. • В последние десять лет в Республике Беларусь наблюдается значительный рост числа ежегодно регистрируемых случаев рака предстательной железы: с 1202 в 2001 году до 2899 случаев в 2010 году (в 2, 4 раза). • В 2010 году у 103 больных (3, 6%) была установлена I стадия заболевания, у 1 008 (34, 8%) – II, у 1 219 (42, 0%) – III стадия, у 527 (18, 2%) – IV стадия заболевания.
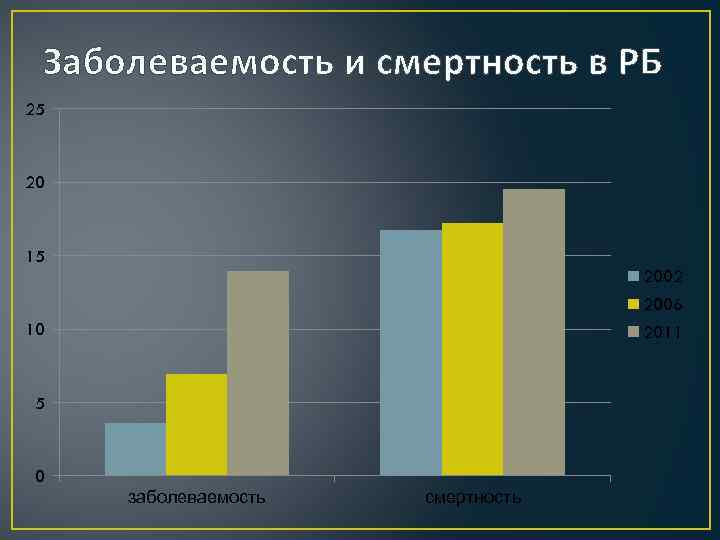
Заболеваемость и смертность в РБ 25 20 15 2002 2006 10 2011 5 0 заболеваемость смертность

Повозрастная заболеваемость в РБ заболеваемость 85+лет 80 -84 лет 75 -79 лет 70 -74 лет 65 -69 лет 60 -64 лет 55 -59 лет 50 -54 лет 45 -49 лет 40 -44 лет 35 -39 лет 30 -34 лет 25 -29 лет 20 -24 лет 15 -19 лет заболеваемость 0 100 200 300 400 500 600

Смертность в РБ • Одногодичная летальность была 10, 7%. • Соотношение смертности и заболеваемости раком предстательной железы было равно 0, 31.

Этиология • Демографические факторы. Заболеваемость максимальная в Швеции, промежуточная в Европе, в США и у японцев, эмигрировавших в США, и минимальная в Японии и на Тайване. У негров она на 30% выше, чем у белых. • Семейный анамнез. Рак простаты у отца или брата в возрасте до 50 лет повышает риск в 7 раз, а после 70 лет – в 4 раза. • Гормональные факторы. Развитие рака простаты связывают с изменением уровня эстрогенов и андрогенов. • Другие факторы. Работа с кадмием, в резиновой промышленности.

Морфология • В большинстве случаев – это аденокарцинома. Реже встречаются переходноклеточный, мелкоклеточный и плоскоклеточный рак. Еще реже встречаются саркомы. • Метастазы в простату бывают при раке мочевого пузыря, толстой кишки, легкого, меланоме, лимфомах.

Локализация и распространение • Опухоль в 70% случаев локализуется в периферических отделах железы. • Часто бывает мультицентрической. • Прогноз зависит от дифференцировки опухоли. Высокодифференцированные опухоли долгое время остаются локализованными. • Опухоль распространяется по периневральным пространствам, лимфатическим и кровеносным сосудам. • Отдаленные метастазы возможны без поражения лимфоузлов, но при наличии метастазов в лимфоузлах, они бывают почти всегда. • Метастазы бывают в костях и иногда в печени.

Клиника Наличие жалоб – признак запущенной опухоли. Затрудненное мочеиспускание. Императивные позывы. Вялая струя. Выделение мочи по каплям. Терминальная гематурия. Внезапное появление и быстрое нарастание жалоб у пожилого мужчины является признаком рака простаты. • Часто первое проявление – боли в костях. • Возможны неврологические нарушения. • •

Дифференциальный диагноз • • Острый простатит. Хронический простатит. Аденома предстательной железы. Другие причины (камни, амилоидоз и др. ).

Обследование • Пальцевое ректальное исследование. • Пальпация паховых лимфоузлов. • Пальпаторное исследование костей и прицельное неврологическое исследование. • Стандартное исследование анализов крови и мочи. • Рентгенография ОГК. • ПСА. • Биопсия простаты (пункционная или трансуретральная резекция простаты). • Сцинтиграфия костей. • КТ и МРТ.

Прогностические факторы • • Стадия заболевания. Степень дифференцировки опухоли. Инвазия семенных пузырьков. Номограммы.

Лечение • Лечение клинически локализованного РПЖ (с. T 1– 2 N 0 M 0). • Возможными вариантами лечения локализованного РПЖ являются: • радикальная простатэктомия ± адъювантная лучевая терапия; • брахитерапия; • комбинация лучевой и гормональной терапии; • активное наблюдение (отсроченное лечение); • гормонотерапия. • Радикальными методами лечения РПЖ являются радикальная простатэктомия и лучевая терапия по радикальной программе. •

Лечение • Активное наблюдение (отсроченное лечение) основано на нескольких положениях: • часто больные РПЖ — лица пожилого возраста, имеющие серьезные сопутствующие заболевания; • РПЖ зачастую прогрессирует медленно, и требуются годы, чтобы рак привел к значимым симптомам.

Лечение • Наблюдение может быть показано в следующих случаях: • T 1 a. N 0–XM 0 — опухоль диагностируется в результате гистологического исследования препарата после ТУРП или открытой аденомэктомии по поводу ДГПЖ, а объем опухоли не превышает 5% от объема удаленной ткани. Такая опухоль, если она высоко- или умереннодифференцированная, с высокой вероятностью является клинически «незначимой» . У молодых больных (ожидаемая продолжительность жизни более 10 лет) показано дообследование для исключения более распространенной опухоли: определение ПСА (не ранее, чем через 4 недели после ТУРП), Тр. УЗИ, систематическая биопсия остатков железы по показаниям.

Лечение • T 1 b– 2 N 0–XM 0 — при сумме Глисона от 2 до 4 у больных с ожидаемой продолжительностью жизни менее 10 лет при отсутствии или минимальной выраженности местных симптомов. • Радикальная простатэктомия. Является основным видом лечения больных опухолями T 1 b– 2 N 0 M 0, ожидаемой продолжительностью жизни > 10 лет и отсутствием медицинских противопоказаний к операции. Операция также показана у молодых больных РПЖ в стадии T 1 a. N 0 M 0 с предполагаемой продолжительностью жизни 15 лет и более, особенно при низкодифференцированных опухолях. Радикальная операция включает удаление всей предстательной железы, семенных пузырьков и простатического отдела уретры. В ходе операции выполняется тазовая лимфаденэктомия.

Лечение • Неоадъювантная гормональная терапия перед радикальной простатэктомией не показана, поскольку не улучшает отдаленные результаты операции. • Адъювантная лучевая терапия в суммарной дозе 60 Гр может быть показана при наличии опухоли по краю резекции, прорастанию опухоли за капсулу (p. T 3 a) или в семенные пузырьки (p. T 3 b) по данным гистологического исследования удаленного после радикальной простатэктомии препарата. Лучевая терапия проводится после нормализации мочеиспускания в условиях 3 D планирования. Альтернативным подходом может быть проведение дистанционной лучевой терапии после возникновения «биохимического рецидива» до достижения уровня ПСА 0, 5 -1, 0 нг/мл.

Лечение • Дистанционная лучевая терапия. Проводится пациентам с противопоказаниями к хирургическому лечению и тем, кто отказывается от операции. Тактика лечения различается в зависимости от принадлежности пациента к той или иной прогностической группе. • Локализованный РПЖ с благоприятным прогнозом (стадия T 1 T 2 a, N 0, M 0, сумма Глисона < 7 и ПСА < 10 нг/мл). При лечении больных с благоприятным прогнозом рекомендуется проведение дистанционной лучевой терапии с использованием конформной техники до СОД 70– 74 Гр. Облучение лимфоузлов таза или проведение неоадъювантной или адъювантной гормонотерапии не показано. •

Лечение • Локализованный РПЖ с промежуточным прогнозом (стадия T 2 b или сумма Глисона 7 или ПСА 10– 20 нг/мл). Увеличение дозы лучевой терапии до 76– 80 Гр (при использовании конформной техники облучения) улучшает отдаленные результаты лечения больных с промежуточным прогнозом. При подведении более низких доз этим больным показано проведение неоадъювантной, сопутствующей и кратковременной (4– 6 мес. ) адъювантной гормонотерапии. • Локализованный РПЖ с неблагоприятным прогнозом (стадия T 2 с или сумма Глисона > 7 или ПСА > 20 нг/мл). Увеличение дозы лучевой терапии до 76– 80 Гр (при использовании конформной техники облучения) улучшает отдаленные результаты лечения больных с неблагоприятным прогнозом. Этим больным показано проведение неоадъювантной, сопутствующей и длительной (24– 36 мес. ) адъювантной гормонотерапии.

Лечение • Противопоказаниями к лучевой терапии являются наличие цистостомы, обострение цистита или ректита, камни мочевого пузыря, выраженная инфравезикальная обструкция с наличием остаточной мочи. У больных, подвергшихся ТУРП, лучевая терапия не должна быть начинаться ранее, чем через 4 недели после операции.

Неоадъювантная и адъювантная гормонотерапия в сочетании с дистанционной лучевой терапией. • Гормональная терапия в течение 3 -х месяцев до лучевой терапии способствует уменьшению объема предстательной железы, купированию местных симптомов РПЖ и снижению частоты постлучевых осложнений. • Сочетание дистанционной лучевой терапии с кратковременной (4– 6 мес. ) адъювантной гормонотерапией показано больным клинически локализованным РПЖ с промежуточным прогнозом, если не используются высокие дозы лучевой терапии (76 -80 Гр); длительное (до 36 мес. ) адъювантное гормональное лечение показано при локализованном РПЖ с неблагоприятным прогнозом, поскольку такое лечение приводит к увеличению безрецидивной и общей выживаемости. • В этих случаях может использоваться фармакологическая кастрация, монотерапия антиандрогенами (бикалютамид 150 мг/сут, ципротерона ацетат 300 мг/нед внутримышечно или 200 мг/сут внутрь) или хирургическая кастрация.

Лечение • Показания к брахитерапии: • В самостоятельном виде: стадия Т 1 b-Т 2 а, сумма Глисона < 7 (при условии достаточного количества биопсий, позволяющих адекватно оценить дифференцировку опухоли), ПСА до применения любых методов лечения < 10 нг/мл; ≤ 50% биоптатов после систематической биопсии содержат рак. • В качестве буста перед дистанционной лучевой терапией: стадия Т 2 b-Т 2 с или меньшие стадии с суммой Глисона 8– 10 или ПСA >20 нг/мл. • При проведении брахитерапии клинический объем облучения включает предстательную железу с капсулой плюс 1– 2 мм здоровых тканей, а при неблагоприятных прогностических факторах — семенные пузырьки. Клинический объем облучения охватывается min 90%-й изодозой, доза за фракцию 8, 5 Гр, негомогенность дозы допускается ± 10%, а в локализованных «горячих» точках — до 30%.

Лечение • Противопоказания к брахитерапии: ожидаемая продолжительность жизни менее 5 лет, наличие большого или плохо заживающего дефекта (предпузыря) после ТУРП, нарушение коагуляции, большой объем предстательной железы (более 50 см 3). При выраженных нарушениях мочеиспускания (IPSS >20), снижении объемной скорости мочеиспускания (Qmax <10 мл/с) или количестве остаточной мочи >200 мл проведение брахитерапии сопряжено с высокой частотой осложнений.

Лечение • Гормонотерапия. • Может проводиться у больных локализованным РПЖ T 1– 2 с выраженными симптомами, которым противопоказаны другие виды лечения из-за тяжести состояния или сопутствующих заболеваний.

Лечение • Лечение местно-распространенного РПЖ и РПЖ с поражением регионарных лимфоузлов. К этим формам заболевания относятся опухоли, выходящие за пределы предстательной железы — T 3– 4 N 0 M 0 или T 1– 4 N 1 M 0. Вариантами лечения местнораспространенного РПЖ являются: • комбинация лучевой и гормональной терапии; • радикальная простатэктомия ± адъювантная лучевая терапия ± адъювантная гормональная терапия; • гормонотерапия.

Лечение • Гормонотерапия в самостоятельном виде. Проводится у больных с выраженными симптомами РПЖ, которым противопоказаны другие виды лечения из-за тяжести состояния или сопутствующих заболеваний, при местнораспространенном раке большого объема, а также массивном поражении тазовых лимфоузлов.

Лечение • Лечение РПЖ с отдаленными метастазами. Начало гормональной терапии сразу после выявления метастатического РПЖ по сравнению с началом лечения при возникновении симптомов прогрессирования приводит к отдалению прогрессирования рака и снижению частоты связанных с ним осложнений. Увеличение выживаемости не столь существенно (на 3– 4 месяца). Тем не менее, у большинства больных показано проведение гормонального лечения сразу после установления диагноза. Отсроченная гормонотерапия может применяться у отдельных больных без симптомов РПЖ при ответственном поведении больного и условии обеспечения тщательного наблюдения. • Стандартным методом лечения распространенного РПЖ является хирургическая или фармакологическая кастрация.

Лечение • Интермиттирующая гормональная терапия является альтернативой непрерывной терапии у информированных пациентов, готовых строго выполнять предписанное лечение. Интерамиттирующая гормонотерапия не менее эффективна, чем непрерывная, однако лучше переносится, менее нарушает качество жизни пациента и потенциально сопровождается меньшим количеством побочных эффектов.

Наблюдение за больными • После радикального лечения (радикальная простатэктомия, дистанционная лучевая терапия). У бессимптомных пациентов рекомендуется сбор специфического анамнеза, определение уровня ПСА и пальцевое ректальное исследование. Исследования выполняются через 3, 6 и 12 мес. после лечения, затем каждые 6 мес. до 3 лет, и далее 1 раз в год. • Повышение уровня ПСА более 0, 2 нг/мл после радикальной простатэктомии говорит о рецидиве заболевания или наличии субклинических метастазов или резидуальной опухоли. Для диагностики биохимического рецидива повышение ПСА более 0, 2 нг/мл должно быть зафиксировано в двух последовательных анализах, однако для решения вопроса о проведении терапии (лучевой, гормональной) необходимо зафиксировать рост ПСА после радикальной простатэктомии (более 0, 2 нг/мл) в трех последовательных анализах (интервал между анализами – 10 дней).

Наблюдение за больными • В соответствии с определением консенсуса RTOG-ASTRO в Фениксе (США) биохимический рецидив после лучевой терапии с или без гормонального лечения устанавливается в случае роста ПСА на 2 нг/мл над уровнем надира (плато ПСА после первоначального снижения на фоне терапии). • Верификация рецидива РПЖ после лучевой терапии с применением биопсии должна осуществляется только в тех случаях, когда планируется проведение радикального лечения второй линии (спасительная простатэктомия). • Метастазы могут быть выявлены при КТ/МРТ таза или остеосцинтиграфии. У больных без симптомов прогрессирования эти исследования могут не проводиться до достижения уровня ПСА 30 нг/мл. При наличии болей в костях показано выполнение остеосцинтиграфии либо рентгенологического исследования вне зависимости от уровня ПСА.

Наблюдение за больными • Наблюдение применении гормонального лечения. Эффект лечения должен быть оценен через 3 мес. после начала гормонотерапии. Обследование должно включать физикальное, пальцевое ректальное исследование и измерение уровня ПСА. Схема наблюдения должна быть индивидуализирована с учетом симптоматики заболевания, факторов прогноза и используемого лечения. • У пациентов без отдаленных метастазов и хорошим эффектом лечения наблюдение рекомендуется проводить каждые 6 мес. • У пациентов с отдаленными метастазами и хорошим эффектом лечения наблюдение рекомендуется проводить каждые 3 мес. • При стабилизации процесса использование методов визуализации (рентгенография, УЗИ, КТ, остеосцинтиграфия) не рекомендуется. При появлении признаков прогрессирования болезни или отсутствии эффекта от лечения наблюдение должно быть индивидуализировано.
Рак предстательной железы.pptx