ФХМИ часть 4.ppt
- Количество слайдов: 25
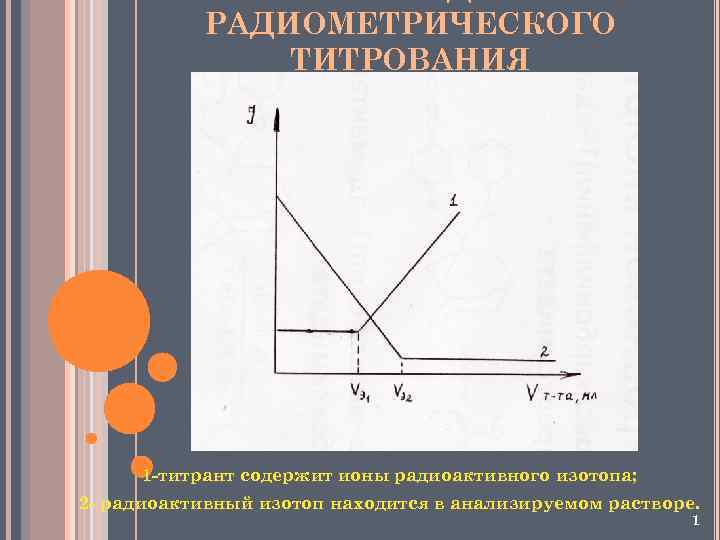 РАДИОМЕТРИЧЕСКОГО ТИТРОВАНИЯ 1 -титрант содержит ионы радиоактивного изотопа; 2 - радиоактивный изотоп находится в анализируемом растворе. 1
РАДИОМЕТРИЧЕСКОГО ТИТРОВАНИЯ 1 -титрант содержит ионы радиоактивного изотопа; 2 - радиоактивный изотоп находится в анализируемом растворе. 1
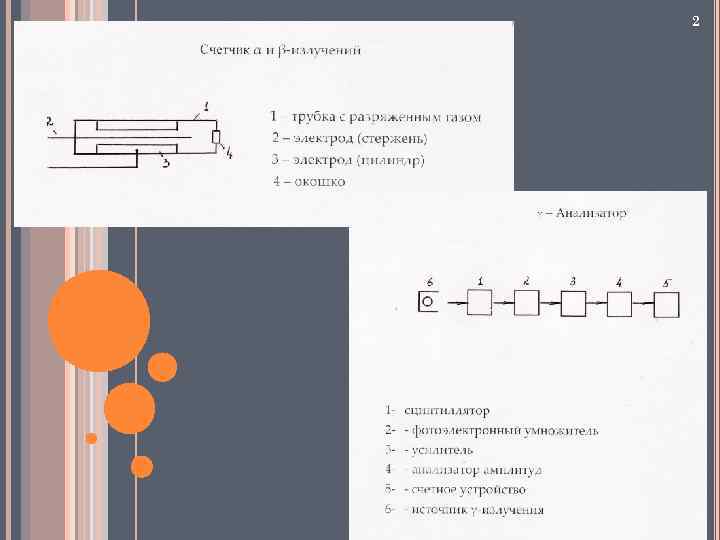 2
2
 Установка для радиометрического титрования 1 -емкость с анализируемым раствором; 2 -бюретка; 3 -перемешивающее устройство; 4 -насос; 5 -фильтрующуя перегородка; 6 -камера для радиометрического анализа; 7 -счетчик радиоактивности; 8 -свинцовый футляр. 3
Установка для радиометрического титрования 1 -емкость с анализируемым раствором; 2 -бюретка; 3 -перемешивающее устройство; 4 -насос; 5 -фильтрующуя перегородка; 6 -камера для радиометрического анализа; 7 -счетчик радиоактивности; 8 -свинцовый футляр. 3
 НЕКОТОРЫЕ ЭЛЕМЕНТЫ, ОПРЕДЕЛЯЕМЫЕ РАДИОАКТИВАЦИОННЫМ МЕТОДОМ Чувствительность, % Элементы 10 -5 – 10 -6 Ca, Si, S, Fe, Zr, Bi 10 -6 – 10 -7 Ni, Zn, Ge, Mo, Ag, Cd, Pt, Hg, Ce 10 -7 – 10 -8 P, Cr, Co, Cd, Sb, Os, Pd 10 -8 Mn, Cu, Zn, W, Au, Sm 4
НЕКОТОРЫЕ ЭЛЕМЕНТЫ, ОПРЕДЕЛЯЕМЫЕ РАДИОАКТИВАЦИОННЫМ МЕТОДОМ Чувствительность, % Элементы 10 -5 – 10 -6 Ca, Si, S, Fe, Zr, Bi 10 -6 – 10 -7 Ni, Zn, Ge, Mo, Ag, Cd, Pt, Hg, Ce 10 -7 – 10 -8 P, Cr, Co, Cd, Sb, Os, Pd 10 -8 Mn, Cu, Zn, W, Au, Sm 4
 МАСС-СПЕКТРОСКОПИЯ Общая схема образования фрагментов из 4 -х атомной молекулы в результате электронного удара Образование молекулярного иона (МИ) Фрагментация Перегруппировки 5 Ион – молекулярные столкновения 5
МАСС-СПЕКТРОСКОПИЯ Общая схема образования фрагментов из 4 -х атомной молекулы в результате электронного удара Образование молекулярного иона (МИ) Фрагментация Перегруппировки 5 Ион – молекулярные столкновения 5
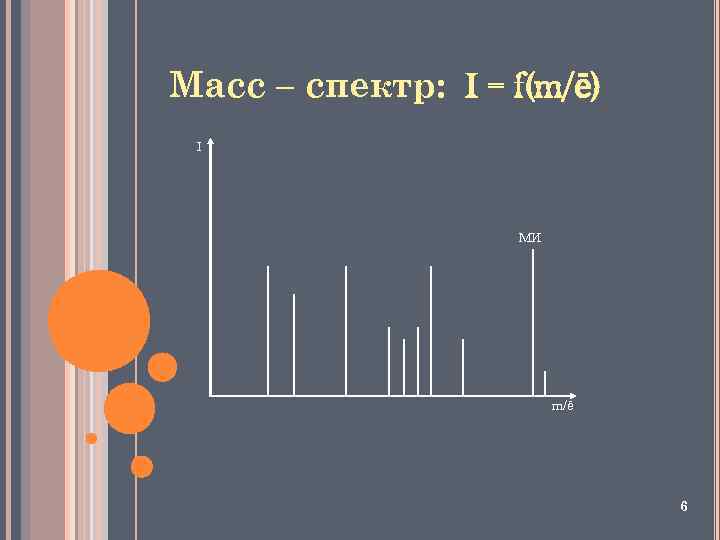 Масс – спектр: I = f(m/ē) I МИ m/ē 6
Масс – спектр: I = f(m/ē) I МИ m/ē 6
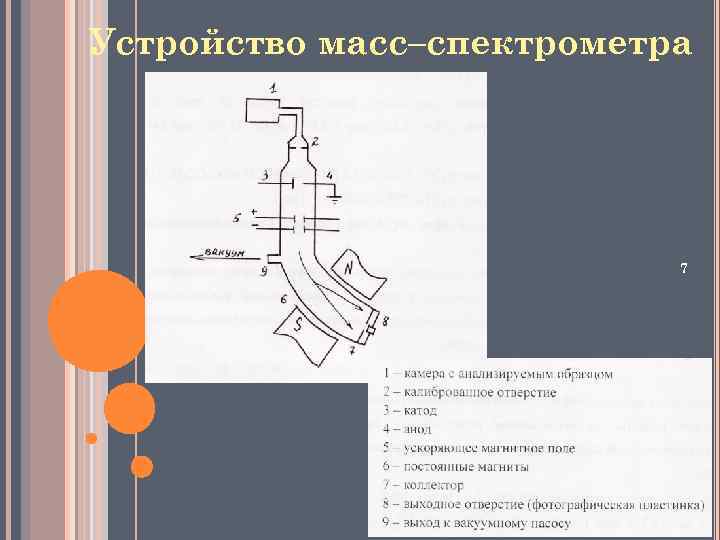 Устройство масс–спектрометра 7
Устройство масс–спектрометра 7
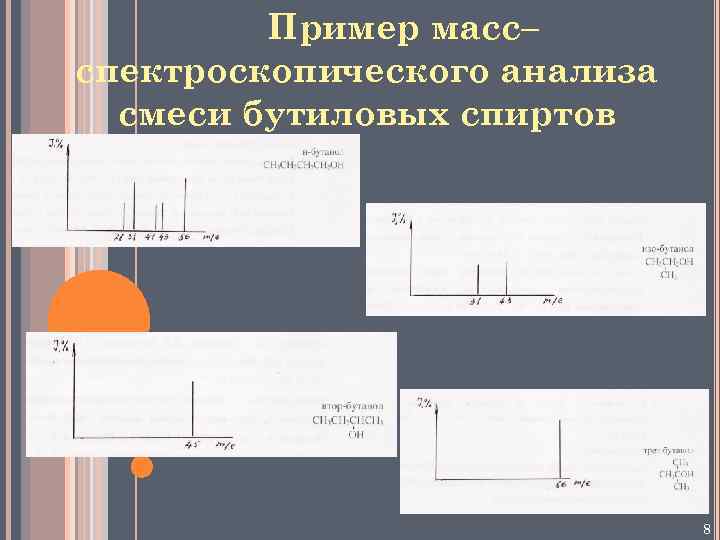 Пример масс– спектроскопического анализа смеси бутиловых спиртов 8
Пример масс– спектроскопического анализа смеси бутиловых спиртов 8
 Анализ обнаруженных осколков в масс–спектрах 9
Анализ обнаруженных осколков в масс–спектрах 9
 ПРАВИЛА ФРАГМЕНТАЦИИ 1. В углеводородной цепи разрыв химической происходит у наиболее разветвленного атома С. связи 2. В циклических углеводородах наиболее характерен разрыв химической связи у α-замещенного атома С. 3. В алкилзамещенных ароматических углеводородах прежде всего разрыв химической связи идет по β-замещенным атомам С. 4. Для непредельных алифатических соединений разрыв идет по βзамещенному атому относительно двойной связи. 5. В соединениях, содержащих гетероатом наиболее вероятен разрыв по βуглеродному атому относительно гетероатома. 6. Образование перегруппировочных ионов, выделением небольших устойчивых молекул: часто легче всего сопровождается и др. Часто перегруппировки сопровождаются миграцией атома водорода в молекуле. Например: 10
ПРАВИЛА ФРАГМЕНТАЦИИ 1. В углеводородной цепи разрыв химической происходит у наиболее разветвленного атома С. связи 2. В циклических углеводородах наиболее характерен разрыв химической связи у α-замещенного атома С. 3. В алкилзамещенных ароматических углеводородах прежде всего разрыв химической связи идет по β-замещенным атомам С. 4. Для непредельных алифатических соединений разрыв идет по βзамещенному атому относительно двойной связи. 5. В соединениях, содержащих гетероатом наиболее вероятен разрыв по βуглеродному атому относительно гетероатома. 6. Образование перегруппировочных ионов, выделением небольших устойчивых молекул: часто легче всего сопровождается и др. Часто перегруппировки сопровождаются миграцией атома водорода в молекуле. Например: 10
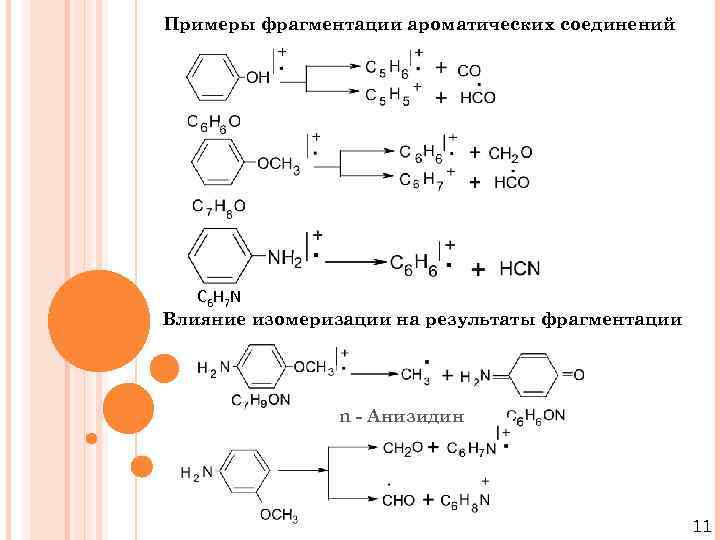 Примеры фрагментации ароматических соединений С 6 Н 7 N Влияние изомеризации на результаты фрагментации n - Анизидин 11
Примеры фрагментации ароматических соединений С 6 Н 7 N Влияние изомеризации на результаты фрагментации n - Анизидин 11
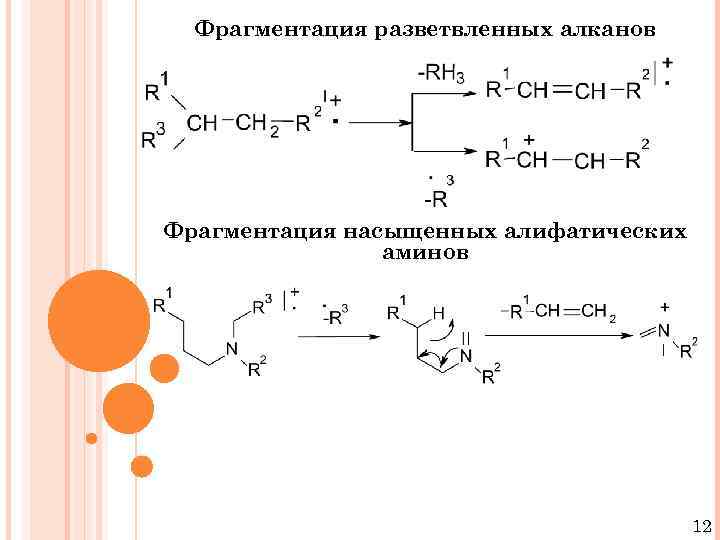 Фрагментация разветвленных алканов Фрагментация насыщенных алифатических аминов 12
Фрагментация разветвленных алканов Фрагментация насыщенных алифатических аминов 12
 ПРАКТИЧЕСКИЕ ЗАДАЧИ, РЕШАЕМЫЕ С ПОМОЩЬЮ СПЕКТРОМЕТРИЧЕСКИХ МЕТОДОВ АНАЛИЗА Провести отнесение сигналов в ПМР – спектре соединения: Транс Какие характеристические сигналы будут в ИК спектре этого соединения? Его ПМР спектр изображен на рисунке 13
ПРАКТИЧЕСКИЕ ЗАДАЧИ, РЕШАЕМЫЕ С ПОМОЩЬЮ СПЕКТРОМЕТРИЧЕСКИХ МЕТОДОВ АНАЛИЗА Провести отнесение сигналов в ПМР – спектре соединения: Транс Какие характеристические сигналы будут в ИК спектре этого соединения? Его ПМР спектр изображен на рисунке 13
 ИК спектр (см -1): СН 3 νas = 2975 -2950 (c) СН 2 νas = 2940 -2915 (c) νs = 2885 -2860 (c) νs = 2870 -2845 (c) δas = 1470 -1435 (cp) δs = 1480 -1440 (cр) δs = 1385 -1370 (c) 1370 -1365 (c) дублет СН=СН (сопряж. с С=О) ν = 1650 -1600(c) транс ν = 1675 -1665 (с) СН ν= 2900 -2880 (cл) δas = 1340 (cл) С-N перекрываются колебаниями СН=СН связи 14
ИК спектр (см -1): СН 3 νas = 2975 -2950 (c) СН 2 νas = 2940 -2915 (c) νs = 2885 -2860 (c) νs = 2870 -2845 (c) δas = 1470 -1435 (cp) δs = 1480 -1440 (cр) δs = 1385 -1370 (c) 1370 -1365 (c) дублет СН=СН (сопряж. с С=О) ν = 1650 -1600(c) транс ν = 1675 -1665 (с) СН ν= 2900 -2880 (cл) δas = 1340 (cл) С-N перекрываются колебаниями СН=СН связи 14
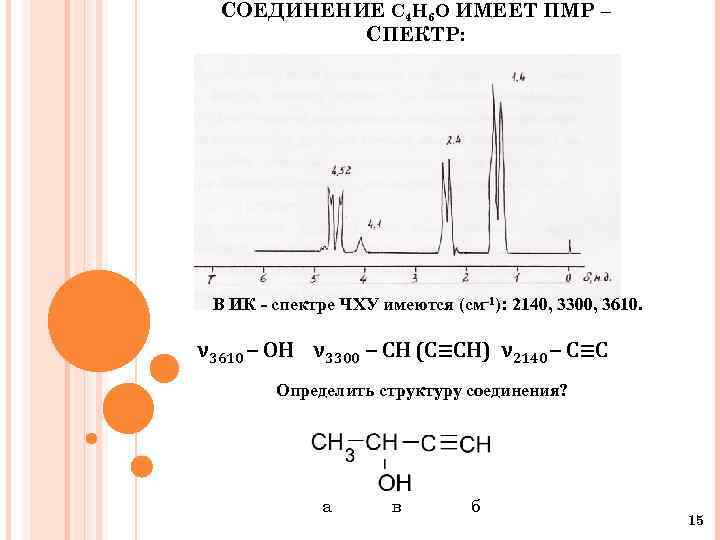 СОЕДИНЕНИЕ С 4 Н 6 О ИМЕЕТ ПМР – СПЕКТР: В ИК - спектре ЧХУ имеются (см-1): 2140, 3300, 3610. ν 3610 – OH ν 3300 – CH (C≡CH) ν 2140 – C≡C Определить структуру соединения? а в б 15
СОЕДИНЕНИЕ С 4 Н 6 О ИМЕЕТ ПМР – СПЕКТР: В ИК - спектре ЧХУ имеются (см-1): 2140, 3300, 3610. ν 3610 – OH ν 3300 – CH (C≡CH) ν 2140 – C≡C Определить структуру соединения? а в б 15
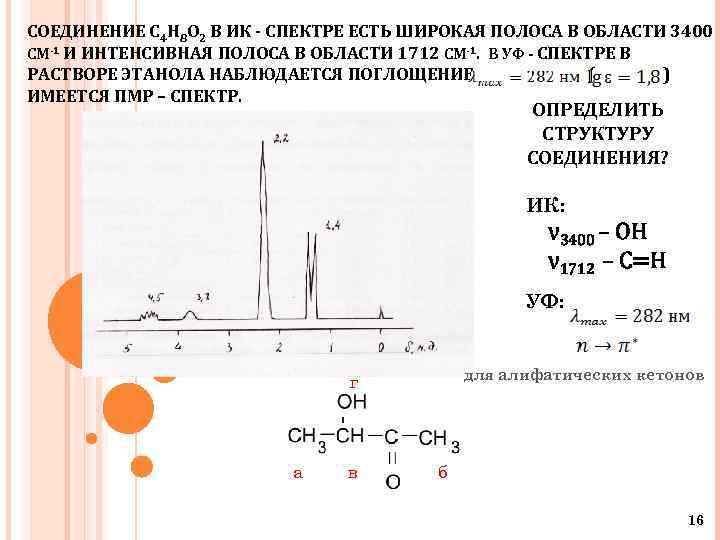 СОЕДИНЕНИЕ С 4 Н 8 О 2 В ИК - СПЕКТРЕ ЕСТЬ ШИРОКАЯ ПОЛОСА В ОБЛАСТИ 3400 СМ-1 И ИНТЕНСИВНАЯ ПОЛОСА В ОБЛАСТИ 1712 СМ-1. В УФ - СПЕКТРЕ В РАСТВОРЕ ЭТАНОЛА НАБЛЮДАЕТСЯ ПОГЛОЩЕНИЕ ( ) ИМЕЕТСЯ ПМР – СПЕКТР. ОПРЕДЕЛИТЬ СТРУКТУРУ СОЕДИНЕНИЯ? ИК: ν 3400 – OH ν 1712 – C=H УФ: для алифатических кетонов г а в б 16
СОЕДИНЕНИЕ С 4 Н 8 О 2 В ИК - СПЕКТРЕ ЕСТЬ ШИРОКАЯ ПОЛОСА В ОБЛАСТИ 3400 СМ-1 И ИНТЕНСИВНАЯ ПОЛОСА В ОБЛАСТИ 1712 СМ-1. В УФ - СПЕКТРЕ В РАСТВОРЕ ЭТАНОЛА НАБЛЮДАЕТСЯ ПОГЛОЩЕНИЕ ( ) ИМЕЕТСЯ ПМР – СПЕКТР. ОПРЕДЕЛИТЬ СТРУКТУРУ СОЕДИНЕНИЯ? ИК: ν 3400 – OH ν 1712 – C=H УФ: для алифатических кетонов г а в б 16
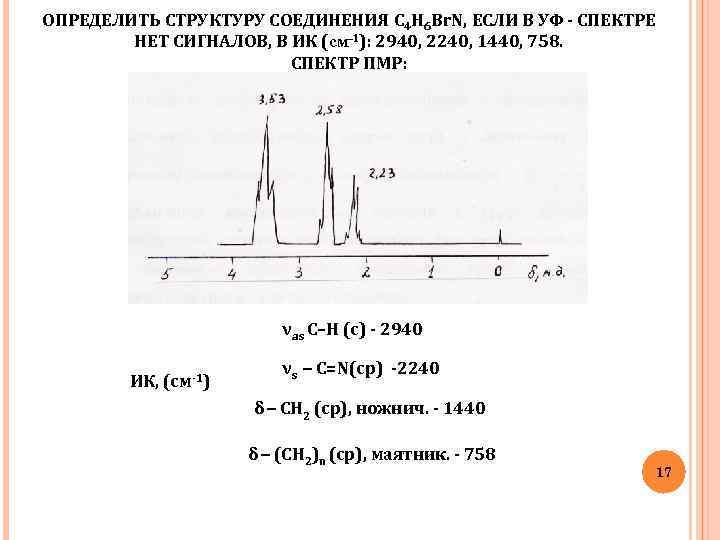 ОПРЕДЕЛИТЬ СТРУКТУРУ СОЕДИНЕНИЯ C 4 H 6 Br. N, ЕСЛИ В УФ - СПЕКТРЕ НЕТ СИГНАЛОВ, В ИК (см-1): 2940, 2240, 1440, 758. СПЕКТР ПМР: νas C–H (с) - 2940 ИК, (см-1) νs – C=N(ср) -2240 δ – CH 2 (ср), ножнич. - 1440 δ – (CH 2)n (ср), маятник. - 758 17
ОПРЕДЕЛИТЬ СТРУКТУРУ СОЕДИНЕНИЯ C 4 H 6 Br. N, ЕСЛИ В УФ - СПЕКТРЕ НЕТ СИГНАЛОВ, В ИК (см-1): 2940, 2240, 1440, 758. СПЕКТР ПМР: νas C–H (с) - 2940 ИК, (см-1) νs – C=N(ср) -2240 δ – CH 2 (ср), ножнич. - 1440 δ – (CH 2)n (ср), маятник. - 758 17
 СОЕДИНЕНИЕ C 3 H 8 O НЕ ИМЕЕТ ПОГЛОЩЕНИЯ В УФ - ОБЛАСТИ. В ИК - СПЕКТРЕ ИМЕЮТСЯ ПОЛОСЫ ПОГЛОЩЕНИЯ (см-1) 3280, 2940, 1460, 1375, 1355, 950, 815. В МАСС-СПЕКТРЕ: m/ē 27 28 29 31 39 41 43 45 59 60 Относительная интенсивность 10, 3 5, 2 5, 0 4, 5 5, 8 7, 2 19, 2 100 4, 3 0, 5 ОПРЕДЕЛИТЬ СТРУКТУРУ СОЕДИНЕНИЯ: ν О-H (c) – 3280 νas CH 3 (cp) – 2940 δ as CH 3 (cp). – 1460 δ s C (CH 3 ) 2(c). дублет – 1355, 1375 18
СОЕДИНЕНИЕ C 3 H 8 O НЕ ИМЕЕТ ПОГЛОЩЕНИЯ В УФ - ОБЛАСТИ. В ИК - СПЕКТРЕ ИМЕЮТСЯ ПОЛОСЫ ПОГЛОЩЕНИЯ (см-1) 3280, 2940, 1460, 1375, 1355, 950, 815. В МАСС-СПЕКТРЕ: m/ē 27 28 29 31 39 41 43 45 59 60 Относительная интенсивность 10, 3 5, 2 5, 0 4, 5 5, 8 7, 2 19, 2 100 4, 3 0, 5 ОПРЕДЕЛИТЬ СТРУКТУРУ СОЕДИНЕНИЯ: ν О-H (c) – 3280 νas CH 3 (cp) – 2940 δ as CH 3 (cp). – 1460 δ s C (CH 3 ) 2(c). дублет – 1355, 1375 18
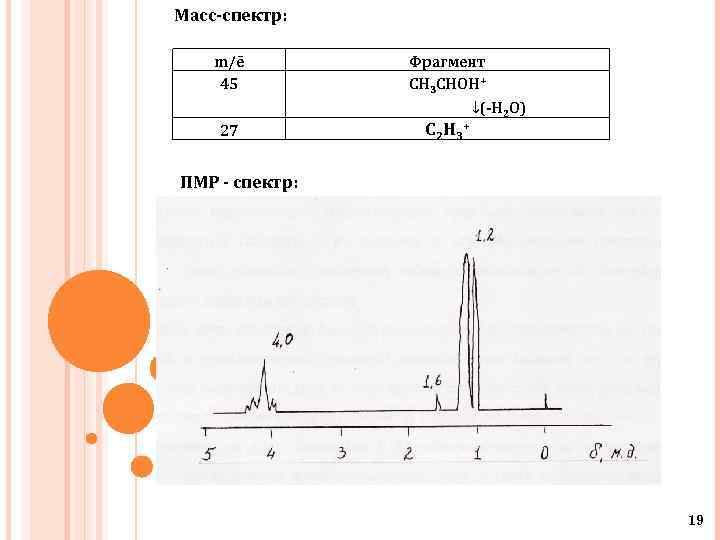 Масс-спектр: m/ē 45 27 Фрагмент СH 3 CHOH+ С 2 H 3+ ↓(-H 2 O) ПМР - спектр: 19
Масс-спектр: m/ē 45 27 Фрагмент СH 3 CHOH+ С 2 H 3+ ↓(-H 2 O) ПМР - спектр: 19
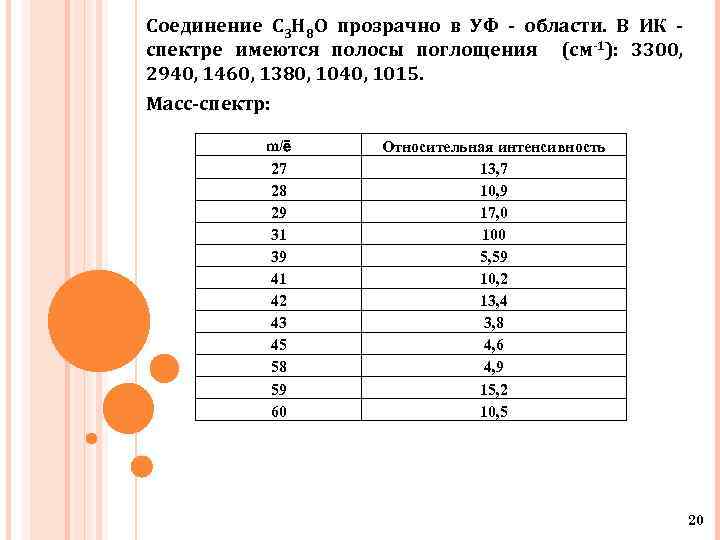 Соединение C 3 H 8 O прозрачно в УФ - области. В ИК спектре имеются полосы поглощения (cм-1): 3300, 2940, 1460, 1380, 1040, 1015. Масс-спектр: m/ē 27 28 29 31 39 41 42 43 45 58 59 60 Относительная интенсивность 13, 7 10, 9 17, 0 100 5, 59 10, 2 13, 4 3, 8 4, 6 4, 9 15, 2 10, 5 20
Соединение C 3 H 8 O прозрачно в УФ - области. В ИК спектре имеются полосы поглощения (cм-1): 3300, 2940, 1460, 1380, 1040, 1015. Масс-спектр: m/ē 27 28 29 31 39 41 42 43 45 58 59 60 Относительная интенсивность 13, 7 10, 9 17, 0 100 5, 59 10, 2 13, 4 3, 8 4, 6 4, 9 15, 2 10, 5 20
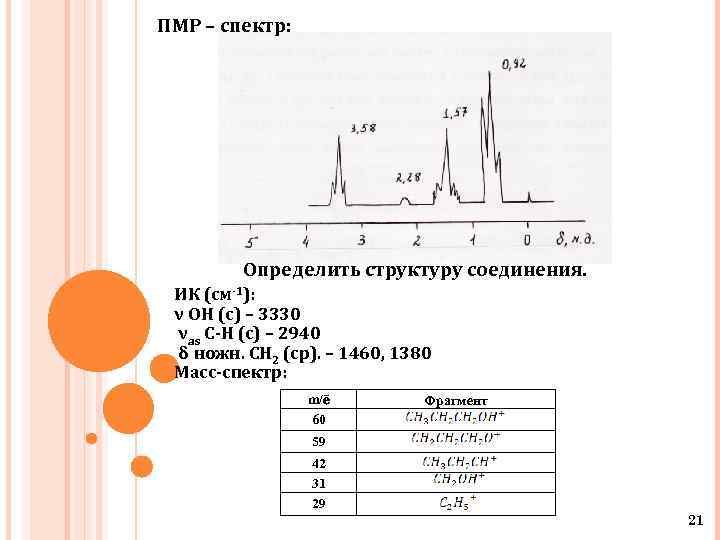 ПМР – спектр: Определить структуру соединения. ИК (см-1): ν OH (c) – 3330 νas C-H (c) – 2940 δ ножн. СН 2 (cp). – 1460, 1380 Масс-спектр: m/ē 60 Фрагмент 59 42 31 29 21
ПМР – спектр: Определить структуру соединения. ИК (см-1): ν OH (c) – 3330 νas C-H (c) – 2940 δ ножн. СН 2 (cp). – 1460, 1380 Масс-спектр: m/ē 60 Фрагмент 59 42 31 29 21
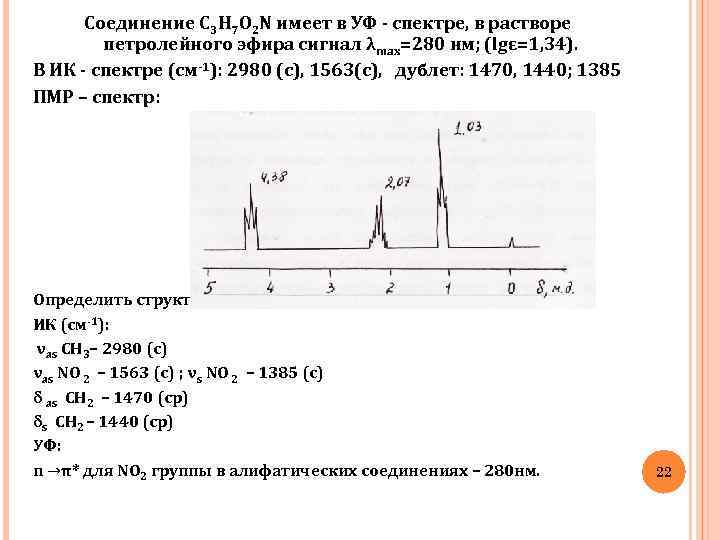 Соединение С 3 H 7 O 2 N имеет в УФ - спектре, в растворе петролейного эфира сигнал λmax=280 нм; (lgɛ=1, 34). В ИК - спектре (см-1): 2980 (с), 1563(с), дублет: 1470, 1440; 1385 ПМР – спектр: Определить структуру соединения. ИК (см-1): νas СН 3– 2980 (с) νas NO 2 – 1563 (с) ; νs NO 2 – 1385 (с) δ as СН 2 – 1470 (ср) δs СН 2 – 1440 (ср) УФ: n →π* для NO 2 группы в алифатических соединениях – 280 нм. 22
Соединение С 3 H 7 O 2 N имеет в УФ - спектре, в растворе петролейного эфира сигнал λmax=280 нм; (lgɛ=1, 34). В ИК - спектре (см-1): 2980 (с), 1563(с), дублет: 1470, 1440; 1385 ПМР – спектр: Определить структуру соединения. ИК (см-1): νas СН 3– 2980 (с) νas NO 2 – 1563 (с) ; νs NO 2 – 1385 (с) δ as СН 2 – 1470 (ср) δs СН 2 – 1440 (ср) УФ: n →π* для NO 2 группы в алифатических соединениях – 280 нм. 22
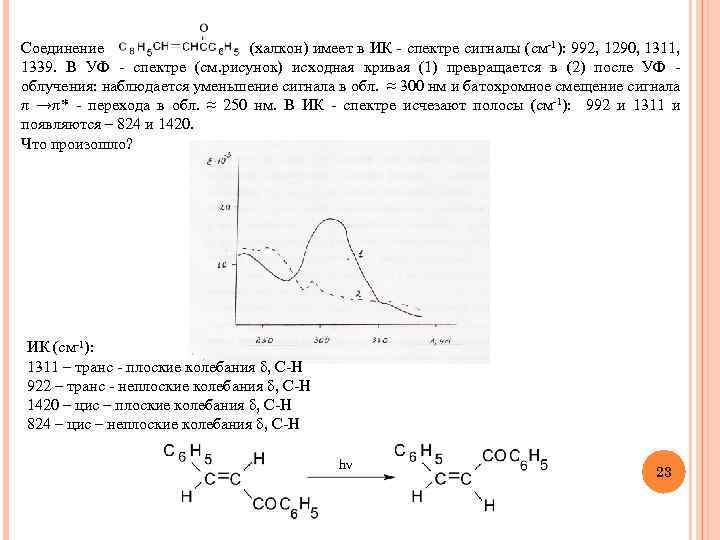 Соединение (халкон) имеет в ИК - спектре сигналы (см-1): 992, 1290, 1311, 1339. В УФ - спектре (см. рисунок) исходная кривая (1) превращается в (2) после УФ облучения: наблюдается уменьшение сигнала в обл. ≈ 300 нм и батохромное смещение сигнала π →π* - перехода в обл. ≈ 250 нм. В ИК - спектре исчезают полосы (см-1): 992 и 1311 и появляются – 824 и 1420. Что произошло? ИК (см-1): 1311 – транс - плоские колебания δ, C-H 922 – транс - неплоские колебания δ, C-H 1420 – цис – плоские колебания δ, C-H 824 – цис – неплоские колебания δ, C-H hν 23
Соединение (халкон) имеет в ИК - спектре сигналы (см-1): 992, 1290, 1311, 1339. В УФ - спектре (см. рисунок) исходная кривая (1) превращается в (2) после УФ облучения: наблюдается уменьшение сигнала в обл. ≈ 300 нм и батохромное смещение сигнала π →π* - перехода в обл. ≈ 250 нм. В ИК - спектре исчезают полосы (см-1): 992 и 1311 и появляются – 824 и 1420. Что произошло? ИК (см-1): 1311 – транс - плоские колебания δ, C-H 922 – транс - неплоские колебания δ, C-H 1420 – цис – плоские колебания δ, C-H 824 – цис – неплоские колебания δ, C-H hν 23
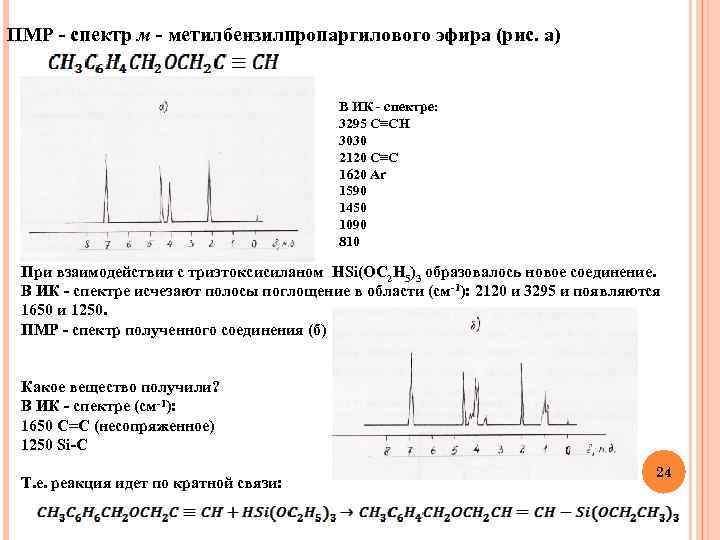 ПМР - спектр м - метилбензилпропаргилового эфира (рис. а) В ИК - спектре: 3295 C≡CH 3030 2120 C≡C 1620 Ar 1590 1450 1090 810 При взаимодействии с триэтоксисиланом HSi(OC 2 H 5)3 образовалось новое соединение. В ИК - спектре исчезают полосы поглощение в области (cм-1): 2120 и 3295 и появляются 1650 и 1250. ПМР - спектр полученного соединения (б) Какое вещество получили? В ИК - спектре (cм-1): 1650 C=C (несопряженное) 1250 Si-C Т. е. реакция идет по кратной связи: 24
ПМР - спектр м - метилбензилпропаргилового эфира (рис. а) В ИК - спектре: 3295 C≡CH 3030 2120 C≡C 1620 Ar 1590 1450 1090 810 При взаимодействии с триэтоксисиланом HSi(OC 2 H 5)3 образовалось новое соединение. В ИК - спектре исчезают полосы поглощение в области (cм-1): 2120 и 3295 и появляются 1650 и 1250. ПМР - спектр полученного соединения (б) Какое вещество получили? В ИК - спектре (cм-1): 1650 C=C (несопряженное) 1250 Si-C Т. е. реакция идет по кратной связи: 24
 В ИК - спектре о – нитротолуола имеются полосы поглощения (cм-1): 2960 νas CH 3 2870 νs CH 3 1520 νas NO 2 1465 Ar скелетные 1380 δ CH 3 плоские 1330 νs NO 2 850 δas NO 2 750 δs NO 2 После проведения реакции 1 исчезают полосы (cм-1): 1520, 1330, 850 и 750 и появляются: 3420, 3340, 1644, 680. Какая это реакция? После проведения реакции 2: исчезают полосы (cм-1): 2960, 2870, 1380 появляются: 3700 -3600 и 1680. 25
В ИК - спектре о – нитротолуола имеются полосы поглощения (cм-1): 2960 νas CH 3 2870 νs CH 3 1520 νas NO 2 1465 Ar скелетные 1380 δ CH 3 плоские 1330 νs NO 2 850 δas NO 2 750 δs NO 2 После проведения реакции 1 исчезают полосы (cм-1): 1520, 1330, 850 и 750 и появляются: 3420, 3340, 1644, 680. Какая это реакция? После проведения реакции 2: исчезают полосы (cм-1): 2960, 2870, 1380 появляются: 3700 -3600 и 1680. 25


