Лекция 4 СК 2013 Радиочувствительность.ppt
- Количество слайдов: 85
 Радиочувствительность тканей, органов и систем организма.
Радиочувствительность тканей, органов и систем организма.
 Вопросы: 1. Особенности лучевых реакций организма. 2. Реакции на облучение отдельных органов и тканей. 3. Лучевое поражение жизненно важных систем организма. Критические ткани и органы. 4. Способы модификации радиочувствительности.
Вопросы: 1. Особенности лучевых реакций организма. 2. Реакции на облучение отдельных органов и тканей. 3. Лучевое поражение жизненно важных систем организма. Критические ткани и органы. 4. Способы модификации радиочувствительности.
 1. Особенности лучевых реакций организма.
1. Особенности лучевых реакций организма.
 Особенности поражения организма определяются двумя факторами: 1) радиочувствительностью тканей, органов и систем, непосредственно подвергающихся облучению; 2) поглощенной дозой излучения и ее распределением во времени.
Особенности поражения организма определяются двумя факторами: 1) радиочувствительностью тканей, органов и систем, непосредственно подвергающихся облучению; 2) поглощенной дозой излучения и ее распределением во времени.
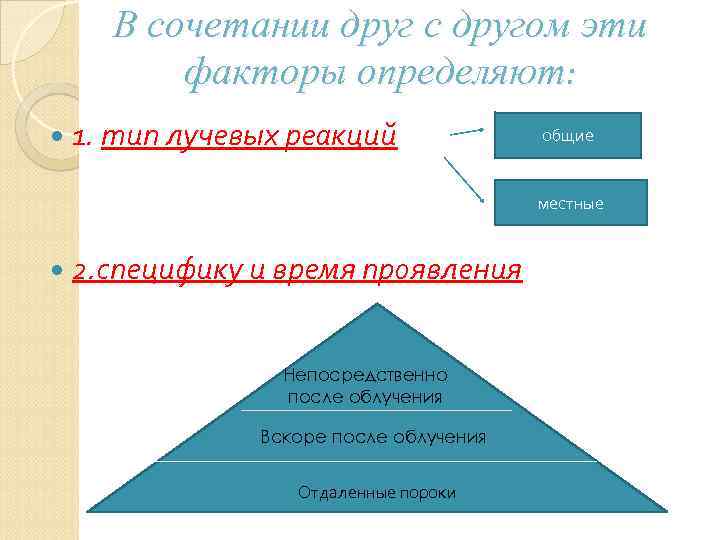 В сочетании друг с другом эти факторы определяют: 1. тип лучевых реакций общие местные 2. специфику и время проявления Непосредственно после облучения Вскоре после облучения Отдаленные пороки
В сочетании друг с другом эти факторы определяют: 1. тип лучевых реакций общие местные 2. специфику и время проявления Непосредственно после облучения Вскоре после облучения Отдаленные пороки
 Радиочувствительность на тканевом уровне На тканевом уровне выполняется правило Бергонье-Трибондо: радиочувствительность ткани прямо пропорциональна пролиферативной активности и обратно пропорциональна степени дифференцировки составляющих ее клеток.
Радиочувствительность на тканевом уровне На тканевом уровне выполняется правило Бергонье-Трибондо: радиочувствительность ткани прямо пропорциональна пролиферативной активности и обратно пропорциональна степени дифференцировки составляющих ее клеток.
 Высокоспециализированная клетка Малодифферецированная клетка
Высокоспециализированная клетка Малодифферецированная клетка
 Радиочувствительность на органном уровне зависит не только от радиочувствительности тканей, составляющих данный орган, но и от ее функций.
Радиочувствительность на органном уровне зависит не только от радиочувствительности тканей, составляющих данный орган, но и от ее функций.
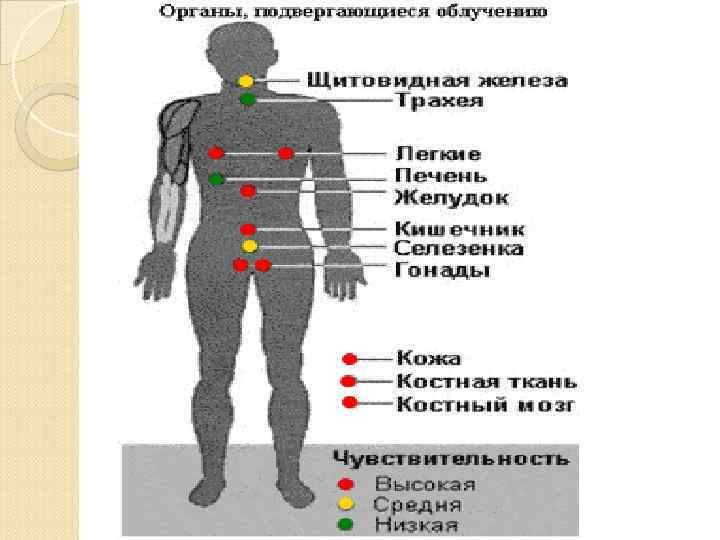
 На популяционном уровне радиочувствительность зависит от следующих факторов: Особенности генотипа (в человеческой популяции 10 12 людей отличаются повышенной радиочувствительностью). Связано это с наследственно сниженной способностью к ликвидации разрывов ДНК, а также со сниженной точностью процесса репарации. Повышенная радиочувствительность сопровождает также наследственные заболевания;
На популяционном уровне радиочувствительность зависит от следующих факторов: Особенности генотипа (в человеческой популяции 10 12 людей отличаются повышенной радиочувствительностью). Связано это с наследственно сниженной способностью к ликвидации разрывов ДНК, а также со сниженной точностью процесса репарации. Повышенная радиочувствительность сопровождает также наследственные заболевания;
 На популяционном уровне радиочувствительность зависит от следующих факторов: физиологическое (например, сон, бодрость, усталость, беременность) или патофизиологическое состояние организма (хронические заболевания, ожоги); пол (мужчины обладают большей радиочувствительностью); возраст (наименее чувствительны люди зрелого возраста).
На популяционном уровне радиочувствительность зависит от следующих факторов: физиологическое (например, сон, бодрость, усталость, беременность) или патофизиологическое состояние организма (хронические заболевания, ожоги); пол (мужчины обладают большей радиочувствительностью); возраст (наименее чувствительны люди зрелого возраста).
 2. Реакции на облучение отдельных органов и тканей.
2. Реакции на облучение отдельных органов и тканей.
 Семенники В них постоянно идет размножение сперматогониев, которые обладают высокой радиочувствительностью, а сперматозоиды (зрелые клетки) являются более радиорезистентными. Уже при дозах облучения свыше 0, 15 Гр (0, 4 Гр/год) происходит клеточное опустошение. При облучении в дозах 3, 5 – 6, 0 Гр (2 Гр/год) возникает постоянная стерильность.
Семенники В них постоянно идет размножение сперматогониев, которые обладают высокой радиочувствительностью, а сперматозоиды (зрелые клетки) являются более радиорезистентными. Уже при дозах облучения свыше 0, 15 Гр (0, 4 Гр/год) происходит клеточное опустошение. При облучении в дозах 3, 5 – 6, 0 Гр (2 Гр/год) возникает постоянная стерильность.
 Яичники В яичниках взрослой женщины содержится популяция незаменяемых ооцитов ( их образование заканчивается в ранние сроки после рождения). Воздействие однократного облучения в дозе 1 -2 Гр на оба яичника вызывает временное бесплодие и прекращении менструаций на 1 3 года.
Яичники В яичниках взрослой женщины содержится популяция незаменяемых ооцитов ( их образование заканчивается в ранние сроки после рождения). Воздействие однократного облучения в дозе 1 -2 Гр на оба яичника вызывает временное бесплодие и прекращении менструаций на 1 3 года.
 Яичники При остром облучении в диапазоне 2, 5 -6 Гр развивается стойкое бесплодие. Это связывают с тем, что образование женских половых клеток заканчивается в ранние сроки после рождения и во взрослом состоянии яичники не способны к активной регенерации. Поэтому если облучение вызывает гибель всех потенциальных яйцеклеток, то плодовитость утрачивается необратимо.
Яичники При остром облучении в диапазоне 2, 5 -6 Гр развивается стойкое бесплодие. Это связывают с тем, что образование женских половых клеток заканчивается в ранние сроки после рождения и во взрослом состоянии яичники не способны к активной регенерации. Поэтому если облучение вызывает гибель всех потенциальных яйцеклеток, то плодовитость утрачивается необратимо.
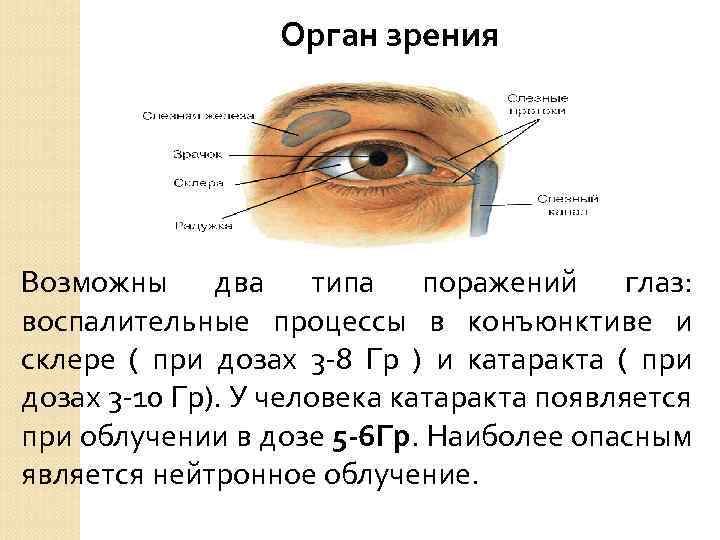 Орган зрения Возможны два типа поражений глаз: воспалительные процессы в конъюнктиве и склере ( при дозах 3 8 Гр ) и катаракта ( при дозах 3 10 Гр). У человека катаракта появляется при облучении в дозе 5 -6 Гр. Наиболее опасным является нейтронное облучение.
Орган зрения Возможны два типа поражений глаз: воспалительные процессы в конъюнктиве и склере ( при дозах 3 8 Гр ) и катаракта ( при дозах 3 10 Гр). У человека катаракта появляется при облучении в дозе 5 -6 Гр. Наиболее опасным является нейтронное облучение.
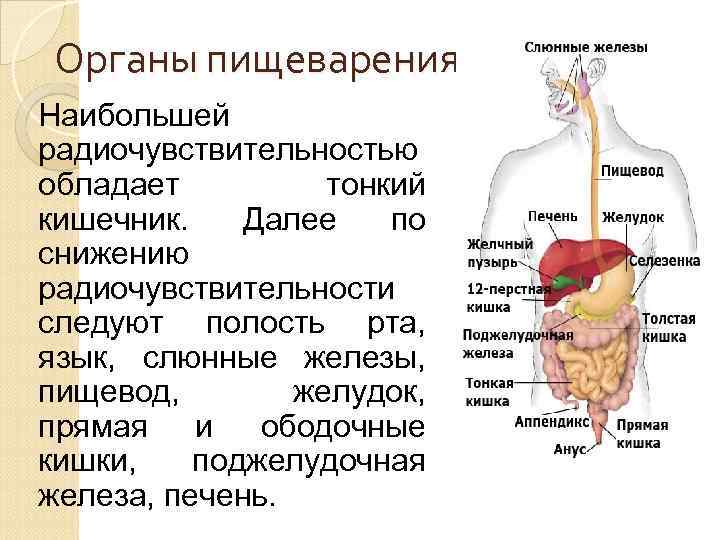 Органы пищеварения Наибольшей радиочувствительностью обладает тонкий кишечник. Далее по снижению радиочувствительности следуют полость рта, язык, слюнные железы, пищевод, желудок, прямая и ободочные кишки, поджелудочная железа, печень.
Органы пищеварения Наибольшей радиочувствительностью обладает тонкий кишечник. Далее по снижению радиочувствительности следуют полость рта, язык, слюнные железы, пищевод, желудок, прямая и ободочные кишки, поджелудочная железа, печень.
 Сердечно сосудистая система
Сердечно сосудистая система
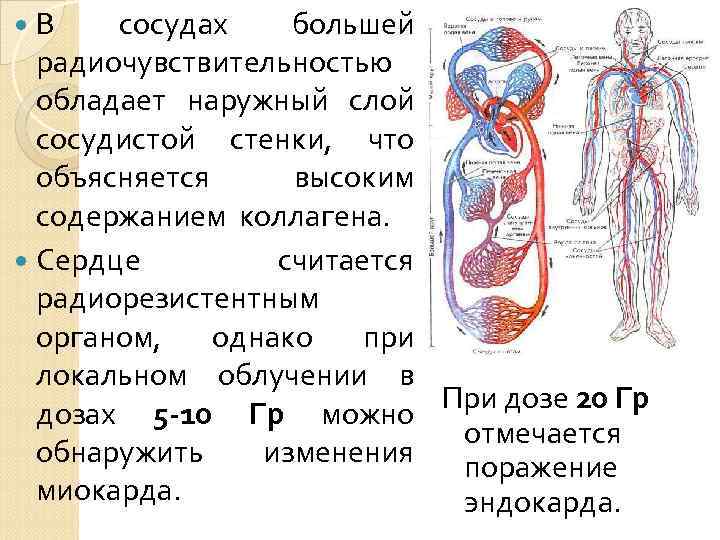 В сосудах большей радиочувствительностью обладает наружный слой сосудистой стенки, что объясняется высоким содержанием коллагена. Сердце считается радиорезистентным органом, однако при локальном облучении в дозах 5 -10 Гр можно При дозе 20 Гр отмечается обнаружить изменения поражение миокарда. эндокарда.
В сосудах большей радиочувствительностью обладает наружный слой сосудистой стенки, что объясняется высоким содержанием коллагена. Сердце считается радиорезистентным органом, однако при локальном облучении в дозах 5 -10 Гр можно При дозе 20 Гр отмечается обнаружить изменения поражение миокарда. эндокарда.
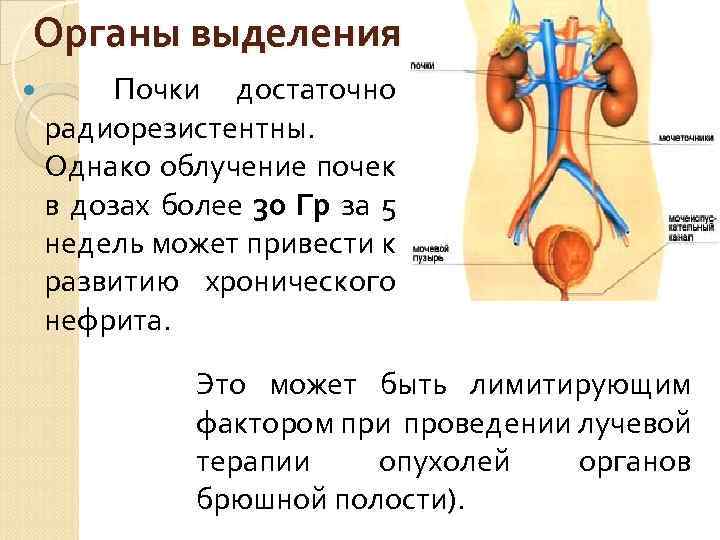 Органы выделения Почки достаточно радиорезистентны. Однако облучение почек в дозах более 30 Гр за 5 недель может привести к развитию хронического нефрита. Это может быть лимитирующим фактором при проведении лучевой терапии опухолей органов брюшной полости).
Органы выделения Почки достаточно радиорезистентны. Однако облучение почек в дозах более 30 Гр за 5 недель может привести к развитию хронического нефрита. Это может быть лимитирующим фактором при проведении лучевой терапии опухолей органов брюшной полости).
 Органы дыхания
Органы дыхания
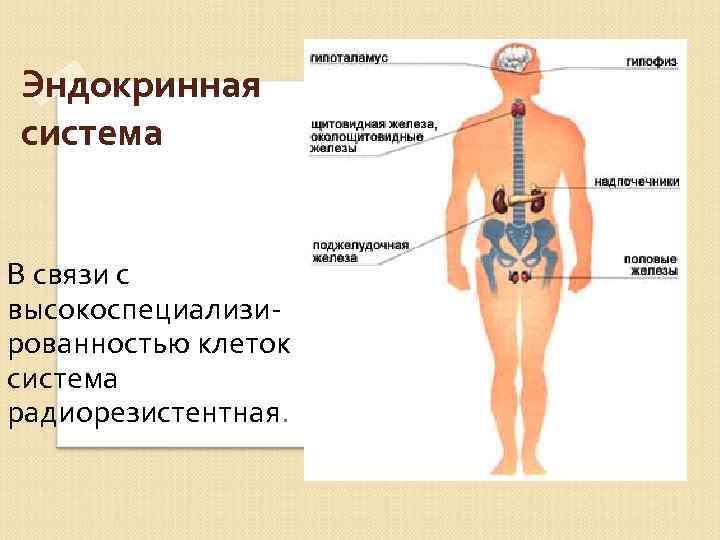 Эндокринная система В связи с высокоспециализи рованностью клеток система радиорезистентная.
Эндокринная система В связи с высокоспециализи рованностью клеток система радиорезистентная.
 Нервная система
Нервная система
 Костно-мышечная система
Костно-мышечная система
 Таким образом, при внешнем облучении по степени поражения органы можно расположить в следующей последовательности (от большей радиочувствительности к меньшей):
Таким образом, при внешнем облучении по степени поражения органы можно расположить в следующей последовательности (от большей радиочувствительности к меньшей):
 Рейтинг радиочувствительности органы кроветворения, костный мозг, половые железы, селезенка, лимфатические железы; желудочно кишечный тракт, органы дыхания; печень, железы внутренней секреции (надпочечники, гипофиз, щитовидная железа, оcтровки поджелудочной железы, паращитовидная железа); органы выделения, мышечная и соединительная ткань, хрящи, нервная ткань.
Рейтинг радиочувствительности органы кроветворения, костный мозг, половые железы, селезенка, лимфатические железы; желудочно кишечный тракт, органы дыхания; печень, железы внутренней секреции (надпочечники, гипофиз, щитовидная железа, оcтровки поджелудочной железы, паращитовидная железа); органы выделения, мышечная и соединительная ткань, хрящи, нервная ткань.
 3. Лучевое поражение жизненно важных систем организма. Критические ткани и органы.
3. Лучевое поражение жизненно важных систем организма. Критические ткани и органы.
 Критические органы – это жизненно важные органы и системы, которые повреждаются первыми в данном диапазоне доз, что обуславливает гибель организма в определенные сроки после облучения.
Критические органы – это жизненно важные органы и системы, которые повреждаются первыми в данном диапазоне доз, что обуславливает гибель организма в определенные сроки после облучения.
 В зависимости от вида излучений, дозы облучения и его условий возможны различные виды лучевого поражения. острая лучевая болезнь (ОЛБ) от внешнего облучения, ОЛБ от внутреннего облучения, хроническая лучевая болезнь, различные клинические формы с преимущественно локальным поражением отдельных органов (лучевые пневмониты, дерматиты, энтериты), которые могут характеризоваться острым, подострым или хроническим течением;
В зависимости от вида излучений, дозы облучения и его условий возможны различные виды лучевого поражения. острая лучевая болезнь (ОЛБ) от внешнего облучения, ОЛБ от внутреннего облучения, хроническая лучевая болезнь, различные клинические формы с преимущественно локальным поражением отдельных органов (лучевые пневмониты, дерматиты, энтериты), которые могут характеризоваться острым, подострым или хроническим течением;
 В зависимости от вида излучений, дозы облучения и его условий возможны различные виды лучевого поражения. отдаленные последствия, среди которых наиболее существенно возникновение злокачественных опухолей; дегенеративные и дистрофические процессы (катаракта, стерильность, cклеротические изменения). Сюда же следует отнести и генетические последствия, наблюдаемые у потомков облученных родителей.
В зависимости от вида излучений, дозы облучения и его условий возможны различные виды лучевого поражения. отдаленные последствия, среди которых наиболее существенно возникновение злокачественных опухолей; дегенеративные и дистрофические процессы (катаракта, стерильность, cклеротические изменения). Сюда же следует отнести и генетические последствия, наблюдаемые у потомков облученных родителей.
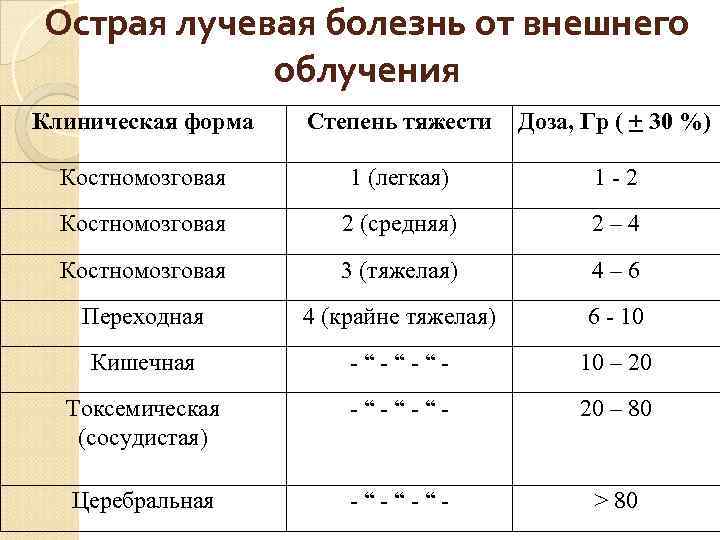 Острая лучевая болезнь от внешнего облучения Клиническая форма Степень тяжести Доза, Гр ( + 30 %) Костномозговая 1 (легкая) 1 -2 Костномозговая 2 (средняя) 2– 4 Костномозговая 3 (тяжелая) 4– 6 Переходная 4 (крайне тяжелая) 6 - 10 Кишечная -“-“-“- 10 – 20 Токсемическая (сосудистая) -“-“-“- 20 – 80 Церебральная -“-“-“- > 80
Острая лучевая болезнь от внешнего облучения Клиническая форма Степень тяжести Доза, Гр ( + 30 %) Костномозговая 1 (легкая) 1 -2 Костномозговая 2 (средняя) 2– 4 Костномозговая 3 (тяжелая) 4– 6 Переходная 4 (крайне тяжелая) 6 - 10 Кишечная -“-“-“- 10 – 20 Токсемическая (сосудистая) -“-“-“- 20 – 80 Церебральная -“-“-“- > 80
 В зависимости от критического органа выделяют три основных радиационных синдрома: Костно-мозговой Желудочно-кишечный Церебральный
В зависимости от критического органа выделяют три основных радиационных синдрома: Костно-мозговой Желудочно-кишечный Церебральный
 Костно-мозговой синдром – развивается при облучении в диапазоне доз 1 -10 Гр, средняя продолжительность жизни – не более 40 суток, на первый план выступают нарушения гемопоэза. основной причиной катастрофического опустошения костного мозга является снижение пролиферации и численности клеток.
Костно-мозговой синдром – развивается при облучении в диапазоне доз 1 -10 Гр, средняя продолжительность жизни – не более 40 суток, на первый план выступают нарушения гемопоэза. основной причиной катастрофического опустошения костного мозга является снижение пролиферации и численности клеток.
 Желудочно-кишечный синдром – развивается при облучении в диапазоне доз 10 -30 Гр, средняя продолжительность жизни около 8 суток, ведущим является поражение кишечника. Важные изменения заключаются в клеточном опустошении ворсинок, крипт, попадании инфекции.
Желудочно-кишечный синдром – развивается при облучении в диапазоне доз 10 -30 Гр, средняя продолжительность жизни около 8 суток, ведущим является поражение кишечника. Важные изменения заключаются в клеточном опустошении ворсинок, крипт, попадании инфекции.
 Церебральный синдром – развивается при облучении в дозах более 30 Гр, продолжительность жизни менее 2 суток, развиваются необратимые изменения в ЦНС. Отек мозга летальный исход при повреждении кровеносных сосудов.
Церебральный синдром – развивается при облучении в дозах более 30 Гр, продолжительность жизни менее 2 суток, развиваются необратимые изменения в ЦНС. Отек мозга летальный исход при повреждении кровеносных сосудов.
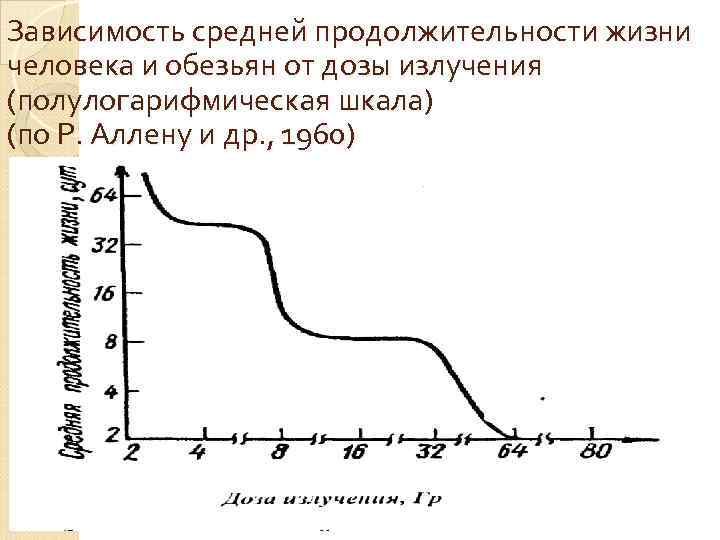 Зависимость средней продолжительности жизни человека и обезьян от дозы излучения (полулогарифмическая шкала) (по Р. Аллену и др. , 1960)
Зависимость средней продолжительности жизни человека и обезьян от дозы излучения (полулогарифмическая шкала) (по Р. Аллену и др. , 1960)
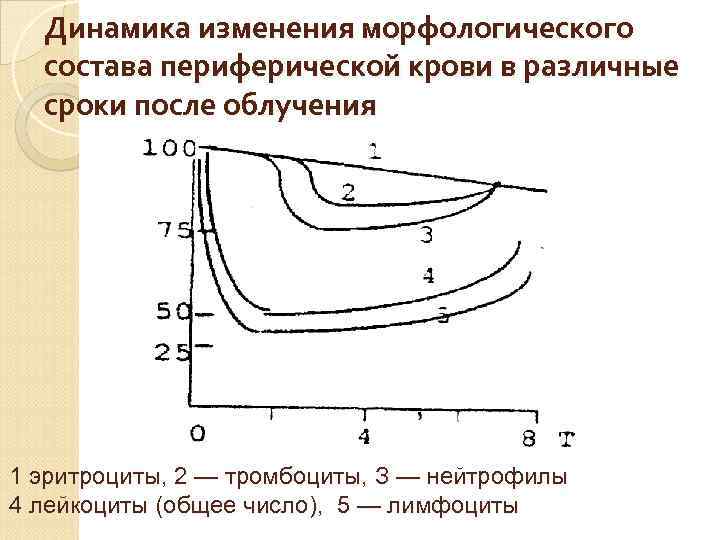 Динамика изменения морфологического состава периферической крови в различные сроки после облучения 1 эритроциты, 2 — тромбоциты, З — нейтрофилы 4 лейкоциты (общее число), 5 — лимфоциты
Динамика изменения морфологического состава периферической крови в различные сроки после облучения 1 эритроциты, 2 — тромбоциты, З — нейтрофилы 4 лейкоциты (общее число), 5 — лимфоциты
 Динамика изменения агранулоцитов (самая короткая продолжительность жизни) фаза дегенерации – характеризуется небольшим порогом и быстрым спадом. При этом в крови обнаруживаются только поврежденные клетки.
Динамика изменения агранулоцитов (самая короткая продолжительность жизни) фаза дегенерации – характеризуется небольшим порогом и быстрым спадом. При этом в крови обнаруживаются только поврежденные клетки.
 Динамика изменения агранулоцитов (самая короткая продолжительность жизни) фаза абортивного подъема – обусловлена размножением в костном мозге поврежденных облучением клеток со сниженной пролиферативной способностью, делящихся еще некоторое время.
Динамика изменения агранулоцитов (самая короткая продолжительность жизни) фаза абортивного подъема – обусловлена размножением в костном мозге поврежденных облучением клеток со сниженной пролиферативной способностью, делящихся еще некоторое время.
 Динамика изменения агранулоцитов (самая короткая продолжительность жизни) фаза восстановления – обеспечивается небольшим количеством стволовых клеток сохранившихся в костном мозге и полностью сохранивших пролиферативную способность.
Динамика изменения агранулоцитов (самая короткая продолжительность жизни) фаза восстановления – обеспечивается небольшим количеством стволовых клеток сохранившихся в костном мозге и полностью сохранивших пролиферативную способность.
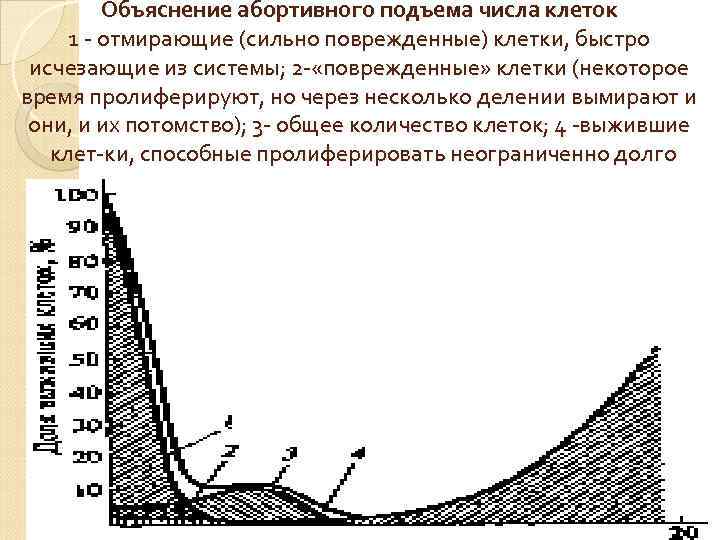 Объяснение абортивного подъема числа клеток 1 отмирающие (сильно поврежденные) клетки, быстро исчезающие из системы; 2 «поврежденные» клетки (некоторое время пролиферируют, но через несколько делении вымирают и они, и их потомство); 3 общее количество клеток; 4 выжившие клет ки, способные пролиферировать неограниченно долго
Объяснение абортивного подъема числа клеток 1 отмирающие (сильно поврежденные) клетки, быстро исчезающие из системы; 2 «поврежденные» клетки (некоторое время пролиферируют, но через несколько делении вымирают и они, и их потомство); 3 общее количество клеток; 4 выжившие клет ки, способные пролиферировать неограниченно долго
 Динамика гемопоэза после облучения в дозе 5 Гр. (1 стволовой пул, 2 пул делящихся и созревающих клеток, 3 пул созревающих клеток, 4 пул зрелых клеток крови)
Динамика гемопоэза после облучения в дозе 5 Гр. (1 стволовой пул, 2 пул делящихся и созревающих клеток, 3 пул созревающих клеток, 4 пул зрелых клеток крови)
 Желудочно кишечный синдром
Желудочно кишечный синдром
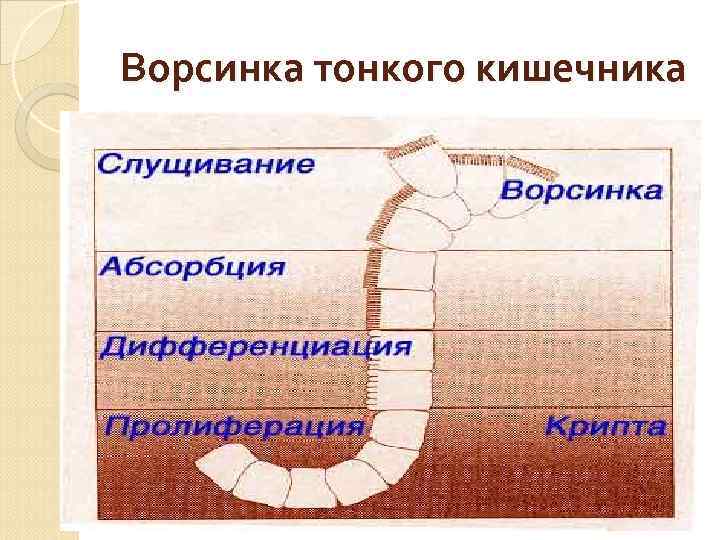 Ворсинка тонкого кишечника
Ворсинка тонкого кишечника
 Реакция эпителия тонкого кишечника на облучение гибнут, в первую очередь, стволовые и другие делящиеся клетки, тогда как неделящиеся (только созревающие и зрелые) продолжают свой путь к верхушкам ворсинок. При отсутствии пополнения новыми клетками из стволового отдела стенки крипт и ворсин обнажаются. Это явление получило название денудации (оголения) слизистой.
Реакция эпителия тонкого кишечника на облучение гибнут, в первую очередь, стволовые и другие делящиеся клетки, тогда как неделящиеся (только созревающие и зрелые) продолжают свой путь к верхушкам ворсинок. При отсутствии пополнения новыми клетками из стволового отдела стенки крипт и ворсин обнажаются. Это явление получило название денудации (оголения) слизистой.
 Реакция эпителия тонкого кишечника на облучение Денудация тонкой кишки сопровождается резким снижением всасывающей способности слизистой. В результате теряется значительное количество воды и электролитов. Во внутреннюю среду проникают эндотоксины и кишечная микрофлора. Клинические проявления кишечного синдрома и смертельные исходы при нем прямое следствие этих процессов.
Реакция эпителия тонкого кишечника на облучение Денудация тонкой кишки сопровождается резким снижением всасывающей способности слизистой. В результате теряется значительное количество воды и электролитов. Во внутреннюю среду проникают эндотоксины и кишечная микрофлора. Клинические проявления кишечного синдрома и смертельные исходы при нем прямое следствие этих процессов.
 Вероятность благоприятного исхода как при костномозговом, так и при кишечном синдромах, зависит, прежде всего, от состояния стволового отдела соответствующих критических систем, в значительной степени от количества сохранившихся после облучения стволовых клеток этих систем.
Вероятность благоприятного исхода как при костномозговом, так и при кишечном синдромах, зависит, прежде всего, от состояния стволового отдела соответствующих критических систем, в значительной степени от количества сохранившихся после облучения стволовых клеток этих систем.
 Церебральный лучевой синдром При действии на человека проникающей радиации ядерных взрывов, а также при аварийных воздействиях источников ионизирующих излучений большой мощности дозы облучения могут достигать значений, при которых ни костномозговой, ни кишечный синдромы не успевают развиться. Поражение приобретает характер неврологического расстройства – церебрального лучевого синдрома – и приводит к гибели в течение 2 3 сут.
Церебральный лучевой синдром При действии на человека проникающей радиации ядерных взрывов, а также при аварийных воздействиях источников ионизирующих излучений большой мощности дозы облучения могут достигать значений, при которых ни костномозговой, ни кишечный синдромы не успевают развиться. Поражение приобретает характер неврологического расстройства – церебрального лучевого синдрома – и приводит к гибели в течение 2 3 сут.
 Основные проявления и условия возникновения Церебральный лучевой синдром (ЦЛС) был описан в 50 е годы как эффект облучения млекопитающих в дозах десятки и сотни грей. Фаза возбуждения, атаксии, гиперкинезов сменялась через 5 30 мин угнетением и летаргией, перемежаемыми приступами судорог и, наконец, комой. Данный синдром наблюдался лишь при облучении головы, с чем и связано его название. Ранние проявления ЦЛС, отмечавшиеся в первые минуты после облучения, были обозначены как ранняя преходящая недееспособность (РПН).
Основные проявления и условия возникновения Церебральный лучевой синдром (ЦЛС) был описан в 50 е годы как эффект облучения млекопитающих в дозах десятки и сотни грей. Фаза возбуждения, атаксии, гиперкинезов сменялась через 5 30 мин угнетением и летаргией, перемежаемыми приступами судорог и, наконец, комой. Данный синдром наблюдался лишь при облучении головы, с чем и связано его название. Ранние проявления ЦЛС, отмечавшиеся в первые минуты после облучения, были обозначены как ранняя преходящая недееспособность (РПН).
 Механизмы развития церебрального лучевого синдрома Вероятно, пострадиационный дефицит АТФ в нейронах возникает в результате нарушения ресинтеза этого нуклеотида. В то время как потребление кислорода изолированными митохондриями не страдало при облучении в дозах до 104 Гр, дыхание гомогенатов и срезов мозга, т. е. объектов, содержащих ядерную ДНК, резко угнеталось при дозах порядка 102 Гр. На фоне угнетения клеточного дыхания отмечалось значительное уменьшение пула НАД.
Механизмы развития церебрального лучевого синдрома Вероятно, пострадиационный дефицит АТФ в нейронах возникает в результате нарушения ресинтеза этого нуклеотида. В то время как потребление кислорода изолированными митохондриями не страдало при облучении в дозах до 104 Гр, дыхание гомогенатов и срезов мозга, т. е. объектов, содержащих ядерную ДНК, резко угнеталось при дозах порядка 102 Гр. На фоне угнетения клеточного дыхания отмечалось значительное уменьшение пула НАД.
 Принципы коррекции ЦЛС применение ингибитора АДФРТ (аденозиндифосфорибозилтрансфераза) никотинамида результативность была прослежена на различных уровнях формирования этого синдрома. Необходимо, однако, подчеркнуть принципиальное отличие ингибитора АДФРТ от радиопротекторов: блокируя процессы репарации ДНК, он способен усиливать летальные эффекты облучения, радиосенсибилизируя клетки.
Принципы коррекции ЦЛС применение ингибитора АДФРТ (аденозиндифосфорибозилтрансфераза) никотинамида результативность была прослежена на различных уровнях формирования этого синдрома. Необходимо, однако, подчеркнуть принципиальное отличие ингибитора АДФРТ от радиопротекторов: блокируя процессы репарации ДНК, он способен усиливать летальные эффекты облучения, радиосенсибилизируя клетки.
 Принципы коррекции ЦЛС Радиосенсибилизирующего действия лишена вторая группа средств метаболической коррекции ЦЛС, представленная сукцинатом и другими субстратами НАД независимого фосфорилирующего окисления в нервной ткани. Экзогенный сукцинат способен проникать через гемато энцефалический барьер, поэтому при введении в достаточной дозе перед облучением он становится основным субстратом клеточного дыхания в мозгу.
Принципы коррекции ЦЛС Радиосенсибилизирующего действия лишена вторая группа средств метаболической коррекции ЦЛС, представленная сукцинатом и другими субстратами НАД независимого фосфорилирующего окисления в нервной ткани. Экзогенный сукцинат способен проникать через гемато энцефалический барьер, поэтому при введении в достаточной дозе перед облучением он становится основным субстратом клеточного дыхания в мозгу.
 Облучение в сравнительно невысоких дозах не летальные повреждения клеток, с возникновением передающихся по наследству повреждений генетического аппарата, следствием которых могут, в частности, оказаться возникновение злокачественных новообразований (при повреждении соматических клеток) или генетические аномалии у потомков облученных родителей (в результате повреждения зародышевых клеток).
Облучение в сравнительно невысоких дозах не летальные повреждения клеток, с возникновением передающихся по наследству повреждений генетического аппарата, следствием которых могут, в частности, оказаться возникновение злокачественных новообразований (при повреждении соматических клеток) или генетические аномалии у потомков облученных родителей (в результате повреждения зародышевых клеток).
 4. Способы модификации радиочувствительности.
4. Способы модификации радиочувствительности.
 1. Радиопротекторы В послевоенный период были апробированы тысячи препаратов с целью найти эффективные модификаторы лучевого поражения. Некоторые из них ослабляли поражение при однократном введении в организм до облучения, но были неэффективны в пострадиационный период. Такие препараты получили общее название радиопротекторов.
1. Радиопротекторы В послевоенный период были апробированы тысячи препаратов с целью найти эффективные модификаторы лучевого поражения. Некоторые из них ослабляли поражение при однократном введении в организм до облучения, но были неэффективны в пострадиационный период. Такие препараты получили общее название радиопротекторов.
 Характер влияния радиопротекторов на клеточный метаболизм введенные в радиозащитных дозах, эти препараты всегда отклоняют его параметры за пределы физиологической нормы. Такое явление, получившее название “биохимический шок”, обусловливает сравнительно высокую токсичность радиопротекторов при введении в оптимальных радиозащитных дозах, особенно при многократном введении.
Характер влияния радиопротекторов на клеточный метаболизм введенные в радиозащитных дозах, эти препараты всегда отклоняют его параметры за пределы физиологической нормы. Такое явление, получившее название “биохимический шок”, обусловливает сравнительно высокую токсичность радиопротекторов при введении в оптимальных радиозащитных дозах, особенно при многократном введении.
 В случаях внезапности или продолжительности возможного облучения, когда радиозащитные средства необходимо вводить многократно и длительно, радиопротекторы не применимы. Поиск менее токсичных препаратов, пригодных для систематического приема, стимулировала чернобыльская катастрофа.
В случаях внезапности или продолжительности возможного облучения, когда радиозащитные средства необходимо вводить многократно и длительно, радиопротекторы не применимы. Поиск менее токсичных препаратов, пригодных для систематического приема, стимулировала чернобыльская катастрофа.
 Радиопротекторы при облучении в малых дозах: препараты с адаптогенной активностью, одним из проявлений которой был небольшой, но зато не сопряженный с неблагоприятным побочным действием радиозащитный эффект. Такие противолучевые средства в последние годы выделены в самостоятельную группу средств повышения радиорезистентности организма.
Радиопротекторы при облучении в малых дозах: препараты с адаптогенной активностью, одним из проявлений которой был небольшой, но зато не сопряженный с неблагоприятным побочным действием радиозащитный эффект. Такие противолучевые средства в последние годы выделены в самостоятельную группу средств повышения радиорезистентности организма.
 Средства ранней патогенетической терапии лучевых поражений Препараты, влияющие на развитие начальных этапов лучевого поражения и тем самым ослабляющие его тяжесть при введении в ранние сроки после облучения.
Средства ранней патогенетической терапии лучевых поражений Препараты, влияющие на развитие начальных этапов лучевого поражения и тем самым ослабляющие его тяжесть при введении в ранние сроки после облучения.
 В отдельную группу выделяют средства борьбы с проявлениями первичной реакции на облучение.
В отдельную группу выделяют средства борьбы с проявлениями первичной реакции на облучение.
 Средства терапии в период разгара лучевых поражений. средства дезактивации, предназначенные для удаления радиоактивных веществ из объектов внешней среды и с поверхности тела, средства профилактики внутреннего облучения - препараты, препятствующие инкорпорации радионуклидов и способствующие выведению их из организма.
Средства терапии в период разгара лучевых поражений. средства дезактивации, предназначенные для удаления радиоактивных веществ из объектов внешней среды и с поверхности тела, средства профилактики внутреннего облучения - препараты, препятствующие инкорпорации радионуклидов и способствующие выведению их из организма.
 2. Лучевая терапия при злокачественных новообразованиях использования новых видов излучений, выбора рациональных режимов облучения, применения радиосенсибилизирующих средств, сочетания с другими способами воздействия на опухоль (химиотерапия, гипертермия). Кстати, и здесь снижение степени повреждения здоровых тканей оказывается существенным аспектом оптимизации лучевой терапии.
2. Лучевая терапия при злокачественных новообразованиях использования новых видов излучений, выбора рациональных режимов облучения, применения радиосенсибилизирующих средств, сочетания с другими способами воздействия на опухоль (химиотерапия, гипертермия). Кстати, и здесь снижение степени повреждения здоровых тканей оказывается существенным аспектом оптимизации лучевой терапии.
 3. Кислородный эффект Первым было обнаружено ослабление поражения биообъекта при снижении концентрации кислорода в окружающей среде во время облучения. В 1909 г. рентгенотерапевт Г. Шварц наблюдал отсутствие лучевого поражения в ишемизированных (за счет давления рентгеновского аппарата) участках кожи пациентов, подвергавшихся короткофокусной рентгенотерапии.
3. Кислородный эффект Первым было обнаружено ослабление поражения биообъекта при снижении концентрации кислорода в окружающей среде во время облучения. В 1909 г. рентгенотерапевт Г. Шварц наблюдал отсутствие лучевого поражения в ишемизированных (за счет давления рентгеновского аппарата) участках кожи пациентов, подвергавшихся короткофокусной рентгенотерапии.
 Кислородный эффект В строго контролируемых условиях радиозащитное действие гипоксии было впервые показано Д. Дауди в 1950 г. Дауди использовал предельно переносимое снижение концентрации кислорода во вдыхаемом воздухе (для мышей – до 7%, а для крыс – до 5%) и получил 100% выживаемость животных при абсолютно смертельных дозах облучения.
Кислородный эффект В строго контролируемых условиях радиозащитное действие гипоксии было впервые показано Д. Дауди в 1950 г. Дауди использовал предельно переносимое снижение концентрации кислорода во вдыхаемом воздухе (для мышей – до 7%, а для крыс – до 5%) и получил 100% выживаемость животных при абсолютно смертельных дозах облучения.
 Кислородный эффект В 1953 г. Л. Грей опубликовал результаты изучения зависимости радиочувствительности различных биообъектов от парциального давления или концентрации кислорода в среде. Оказалось, что эта зависимость не только по знаку, но и по величине близка у всех изученных организмов. Если их радиочувствительность в условиях экстремальной гипоксии принять за 1, то в тех же условных единицах радиочувствительность организмов при нормоксии и гипероксии составит 3.
Кислородный эффект В 1953 г. Л. Грей опубликовал результаты изучения зависимости радиочувствительности различных биообъектов от парциального давления или концентрации кислорода в среде. Оказалось, что эта зависимость не только по знаку, но и по величине близка у всех изученных организмов. Если их радиочувствительность в условиях экстремальной гипоксии принять за 1, то в тех же условных единицах радиочувствительность организмов при нормоксии и гипероксии составит 3.
 Кислородный эффект В большинстве работ, посвященных влиянию кислорода на радиочувствительность теплокровных животных, ее оценивали по дозе излучения, вызывающей гибель половины особей за 30 сут – то есть на модели гибели от костномозгового синдрома. Способность кислорода модифицировать проявления кишечного и церебрального синдромов оценивалась в меньшем числе исследований, но и в этих случаях, как правило, наблюдалось радиозащитное действие гипоксии, создаваемой во время облучения.
Кислородный эффект В большинстве работ, посвященных влиянию кислорода на радиочувствительность теплокровных животных, ее оценивали по дозе излучения, вызывающей гибель половины особей за 30 сут – то есть на модели гибели от костномозгового синдрома. Способность кислорода модифицировать проявления кишечного и церебрального синдромов оценивалась в меньшем числе исследований, но и в этих случаях, как правило, наблюдалось радиозащитное действие гипоксии, создаваемой во время облучения.
 ККУ Количественную характеристику изменению эффекта излучения в присутствии кислорода дает коэффициент кислородного усиления (ККУ); ККУ – это отношение равноэффективных доз излучения в отсутствие и в присутствии кислорода.
ККУ Количественную характеристику изменению эффекта излучения в присутствии кислорода дает коэффициент кислородного усиления (ККУ); ККУ – это отношение равноэффективных доз излучения в отсутствие и в присутствии кислорода.
 Всегда ли «работает» кислородный эффект? Учитывая положительную зависимость радиозащитного эффекта от глубины гипоксии, можно было бы предположить, что такая же зависимость существует и от длительности гипоксии, создаваемой перед облучением. Было, однако, показано, что по мере увеличения продолжительности предрадиационной гипоксии с 5 до 120 мин ее противолучевое действие на млекопитающих снижается на 30 40%.
Всегда ли «работает» кислородный эффект? Учитывая положительную зависимость радиозащитного эффекта от глубины гипоксии, можно было бы предположить, что такая же зависимость существует и от длительности гипоксии, создаваемой перед облучением. Было, однако, показано, что по мере увеличения продолжительности предрадиационной гипоксии с 5 до 120 мин ее противолучевое действие на млекопитающих снижается на 30 40%.
 Кислородный эффект кратковременен Объяснение этого феномена может заключаться в том, что для борьбы с гипоксией организм интенсифицирует внешнее дыхание и кровообращение, а также, возможно, повышает проницаемость биомембран для кислорода. В результате этого через несколько минут после начала гипоксического воздействия оксигенация клеток частично нормализуется, а радиозащитный эффект гипоксии ослабевает.
Кислородный эффект кратковременен Объяснение этого феномена может заключаться в том, что для борьбы с гипоксией организм интенсифицирует внешнее дыхание и кровообращение, а также, возможно, повышает проницаемость биомембран для кислорода. В результате этого через несколько минут после начала гипоксического воздействия оксигенация клеток частично нормализуется, а радиозащитный эффект гипоксии ослабевает.
 Проявляется ли радиомодифицирующее действие кислорода после облучения? В отсутствие мощных источников излучения этот вопрос был практически неразрешим. Однако в 50 е годы было показано что при облучении клеток в аноксических условиях оксигенированная среда, внесенная в суспензию клеток через 20 мс после облучения, уже не модифицирует лучевое поражение. В 70 е годы было установлено, что через 1, 5 мс после импульсного облучения клеток кислород не уменьшает их выживаемости.
Проявляется ли радиомодифицирующее действие кислорода после облучения? В отсутствие мощных источников излучения этот вопрос был практически неразрешим. Однако в 50 е годы было показано что при облучении клеток в аноксических условиях оксигенированная среда, внесенная в суспензию клеток через 20 мс после облучения, уже не модифицирует лучевое поражение. В 70 е годы было установлено, что через 1, 5 мс после импульсного облучения клеток кислород не уменьшает их выживаемости.
 Проявляется ли радиомодифицирующее действие кислорода после облучения? Таким образом, радиосенсибилизирующее действие кислорода на биообъекты – это эффект, наблюдаемый только при условии присутствия кислорода в среде во время облучения.
Проявляется ли радиомодифицирующее действие кислорода после облучения? Таким образом, радиосенсибилизирующее действие кислорода на биообъекты – это эффект, наблюдаемый только при условии присутствия кислорода в среде во время облучения.
 Обратный кислородный эффект Пострадиационная гипоксия не только не способствует, но, напротив, препятствует выживанию облученных клеток. Был показан не только на клетках, но и на многоклеточных организмах. В частности, гипоксия устраняет смягчающий радиационное поражение эффект фракционирования дозы.
Обратный кислородный эффект Пострадиационная гипоксия не только не способствует, но, напротив, препятствует выживанию облученных клеток. Был показан не только на клетках, но и на многоклеточных организмах. В частности, гипоксия устраняет смягчающий радиационное поражение эффект фракционирования дозы.
 Обратный кислородный эффект может найти применение в смежных с радиобиологией отраслях медицины, в частности, в онкологии. Показано, что при пострадиационном кратковременном наложении жгута на конечность перевитая в нее опухоль рецидивирует позже и в меньшем проценте случаев, чем при облучении в той же дозе без последующего создания циркуляторной гипоксии.
Обратный кислородный эффект может найти применение в смежных с радиобиологией отраслях медицины, в частности, в онкологии. Показано, что при пострадиационном кратковременном наложении жгута на конечность перевитая в нее опухоль рецидивирует позже и в меньшем проценте случаев, чем при облучении в той же дозе без последующего создания циркуляторной гипоксии.
 Таким образом: кислород, присутствующий в среде во время облучения, повышает чувствительность биообъектов к редкоионизирующим излучениям; зависимость радиочувствительности биообъектов от напряжения кислорода имеет параболический характер, причем при уровнях оксигенации, характерных для биотканей, эта зависимость весьма существенна;
Таким образом: кислород, присутствующий в среде во время облучения, повышает чувствительность биообъектов к редкоионизирующим излучениям; зависимость радиочувствительности биообъектов от напряжения кислорода имеет параболический характер, причем при уровнях оксигенации, характерных для биотканей, эта зависимость весьма существенна;
 Таким образом: радиозащитная эффективность гипоксии у млекопитающих снижается по мере увеличения продолжительности гипоксического воздействия сверх 5 минут; пострадиационная гипоксия обладает действием, усиливающим радиационное поражение биообъектов.
Таким образом: радиозащитная эффективность гипоксии у млекопитающих снижается по мере увеличения продолжительности гипоксического воздействия сверх 5 минут; пострадиационная гипоксия обладает действием, усиливающим радиационное поражение биообъектов.
 Роль кислорода в формировании природной и модифицированной радиочувствительности организма
Роль кислорода в формировании природной и модифицированной радиочувствительности организма
 Фактор 1. Судьба облученной клетки определяется радиационными повреждениями ядра, которое выступает в роли “критической” клеточной органеллы. Поэтому именно уровень оксигенации ядра в момент облучения служит фактором, от которого непосредственно зависит изменение радиочувствительности клетки при изменении содержания кислорода во внешней среде.
Фактор 1. Судьба облученной клетки определяется радиационными повреждениями ядра, которое выступает в роли “критической” клеточной органеллы. Поэтому именно уровень оксигенации ядра в момент облучения служит фактором, от которого непосредственно зависит изменение радиочувствительности клетки при изменении содержания кислорода во внешней среде.
 Фактор 2. Для обеспечения эффективной противолучевой защиты организма путем создания газовой гипоксии необходимо значительное снижение уровня кислорода во вдыхаемом воздухе, которое неблагоприятно отражается на функциональном состоянии организма.
Фактор 2. Для обеспечения эффективной противолучевой защиты организма путем создания газовой гипоксии необходимо значительное снижение уровня кислорода во вдыхаемом воздухе, которое неблагоприятно отражается на функциональном состоянии организма.
 Фактор 3 Более удобным для практического использования является метод снижения оксигенации тканей, основанный на нарушении их кровоснабжения. С этой целью применяют препараты, обладающие сосудосуживающим действием – индолилалкиламины и фенилалкиламины. Теоретически обосновано также применение индукторов гемической гипоксии – метгемоглобинообразователей и оксида углерода.
Фактор 3 Более удобным для практического использования является метод снижения оксигенации тканей, основанный на нарушении их кровоснабжения. С этой целью применяют препараты, обладающие сосудосуживающим действием – индолилалкиламины и фенилалкиламины. Теоретически обосновано также применение индукторов гемической гипоксии – метгемоглобинообразователей и оксида углерода.
 Фактор 4. Целенаправленное снижение напряжения кислорода во внутриклеточной среде может быть достигнуто путем интенсификации потребления диффундирующего в клетки кислорода в ходе процессов окислительного фосфорилирования. Преимуществом такого подхода является отсутствие побочных эффектов, обусловленных угнетением биоэнергетических процессов в тканях (как при газовой, гемической или циркуляторной гипоксии). Основной препарат сукцинат натрия.
Фактор 4. Целенаправленное снижение напряжения кислорода во внутриклеточной среде может быть достигнуто путем интенсификации потребления диффундирующего в клетки кислорода в ходе процессов окислительного фосфорилирования. Преимуществом такого подхода является отсутствие побочных эффектов, обусловленных угнетением биоэнергетических процессов в тканях (как при газовой, гемической или циркуляторной гипоксии). Основной препарат сукцинат натрия.
 Фактор 5. Перспективным является сочетанное применение различных агентов, нацеленных на снижение оксигенации внутриклеточной среды – газовой гипоксии, индолилалкиламинов и сукцината натрия, а также комбинирование этих средств с меркаптоалкиламинами.
Фактор 5. Перспективным является сочетанное применение различных агентов, нацеленных на снижение оксигенации внутриклеточной среды – газовой гипоксии, индолилалкиламинов и сукцината натрия, а также комбинирование этих средств с меркаптоалкиламинами.
 4. Негенетические (средовые) факторы, влияющие на радиочувствительность Диета Двигательная активность Нервно психическое состояние Гормональный баланс Приём лекарств и пищевых добавок Ненаследственные заболевания
4. Негенетические (средовые) факторы, влияющие на радиочувствительность Диета Двигательная активность Нервно психическое состояние Гормональный баланс Приём лекарств и пищевых добавок Ненаследственные заболевания
 5. Генетические факторы, влияющие на радиочувствительность Эффективность работы репарационных систем Наличие эндогенных радиопротекторов и антимутагенов Скорость синтеза АТФ и других необходимых белков и ферментов Амплификация генов, ответственных за радиорезистентность Включение мобильных элементов Наследственные заболевания И т. п.
5. Генетические факторы, влияющие на радиочувствительность Эффективность работы репарационных систем Наличие эндогенных радиопротекторов и антимутагенов Скорость синтеза АТФ и других необходимых белков и ферментов Амплификация генов, ответственных за радиорезистентность Включение мобильных элементов Наследственные заболевания И т. п.
 Выводы Радиочувствительность особей существенно различается, т. к. : ü 1. Радиочувствительность это генетический количественный признак, кодируемый полигенно. ü 2. На генетические различия накладывается влияние образа жизни. ü 3. Существенное влияние оказывают радиоадаптивный ответ, радиоиндуцированный байстэндер эффект и др. ü 4. Эти феномены также могут быть усилены или подавлены различными модификаторами.
Выводы Радиочувствительность особей существенно различается, т. к. : ü 1. Радиочувствительность это генетический количественный признак, кодируемый полигенно. ü 2. На генетические различия накладывается влияние образа жизни. ü 3. Существенное влияние оказывают радиоадаптивный ответ, радиоиндуцированный байстэндер эффект и др. ü 4. Эти феномены также могут быть усилены или подавлены различными модификаторами.
 ◦ СПАСИБО ЗА ВНИМАНИЕ
◦ СПАСИБО ЗА ВНИМАНИЕ


