Лекция опт.звено 2010.ppt
- Количество слайдов: 30
работы аптечног о склада, оптовой фирмы. Требова ния GDP, GSP, Лектор: доц. Хименко С. В. GPPP.

Литература Організація фармацевтичного забезпечення населення: навч. посіб. для студ. вищ. навч. закл. / А. С. Немченко, А. А. Котвіцька, Г. Л. Панфілова та ін. ; за ред. А. С. Немченко. -Х. : Авіста-ВЛТ, 2007. - С. 343 -397. Наказ № 44/27 від 3. 03. 2009 р. «Про затвердження ліцензійних умов провадження господарської діяльності з виробництва ЛЗ, оптової, роздрібної торгівлі ЛЗ» . Основы организации и экономики фармации в вопросах и ответах (учебное пособие) часть 1 / Под ред. проф. А. С. Немченко. -Х. : НФа. У. Закон Украины «О лекарственных средствах» № 507 -ХII от 4. 04. 1996 Приказ Госкомитета Украины по вопросам регуляторной политики и предпринимательства, Госинспекции по контролю качества ЛС № 44/27 “Лицензионные условия осуществления хозяйственной деятельности по производству ЛС, оптовой, розничной торговле ЛС” от 03. 2009 г.

План лекции 1. 2. 3. 4. 5. 6. Оптовая реализация ЛС и предъявляемые к ним требования Поставщики товаров аптечного ассортимента Организация работы аптечного склада, его требования. Организационная структура. Требования GDP Поставка товаров аптечного ассортимента Требования GSP, GPPP

Оптовая реализация ЛС - 1 деятельность по приобретению ЛС у производителя или других субъектов хозяйствования, которые имеют соответствующую лицензию, хранение и реализация ЛС с аптечных складов(баз) другим субъектам оптовой или розничной реализации ЛС, которые получили на это соответствующие лицензии, и непосредственно ЛПУ и производителям ЛС.

ЗАГАЛЬНІ ВИМОГИ ДО СУБ’ЄКТІВ ГОСПОДАРЮВАННЯ З ОПТОВОЇ ТОРГІВЛІ ЛЗ ТА ВМП 1 Ø мати приміщення, устаткування та обладнання для забезпечення належного зберігання ЛЗ, у т. ч. під час транспортування та торгівлі ними; Ø мати достатню кількість кваліфікованих працівників, але не менше двох спеціалістів з вищою фармацевтичною освітою; Ø забезпечувати дотримання визначених МОЗ України загальних та специфічних умов зберігання ЛЗ і ВМП відповідно до їх складу, фізико-хімічних властивостей, впливу навколишнього середовища та інших факторів; Ø забезпечити обов’язковий мінімальний асортимент ЛЗ і ВМП, що визначається МОЗ України; Ø забезпечити належне зберігання фармацевтичних товарів; Ø зберігати протягом не менше трьох років документи, що засвідчують факт купівлі або продажу із зазначенням дати, назви, кількості та серії отриманого та поставленого товару, інформації про покупця (постачальника) та реквізитів його ліцензії; Ø мати в штатному розкладі уповноважену особу; Ø забезпечити справність усіх засобів вимірювання шляхом проведення їх калібрування та регулярної метрологічної повірки; Ø мати паспорт аптечного складу (бази) згідно з додатком. Ø мати план термінових дій для відкликання у разі потреби ЛЗ і ВМП з продажу;

Вимоги до оптової торгівлі Вимоги до приміщень v Виробничі: загальна площа не менш ніж 250 кв. м. v Побутові і допоміжні приміщення: – – – кімната персоналу (0, 75 кв. м. , але не менш 8 кв. м. ); вбиральня (не менше 2 кв. м. ); приміщення для зберігання інвентарю (не менше 4 кв. м. ); v Приміщення повинні відповідати ДБН: – – – електрозабезпечення; опалення; освітлення; вентиляція; температура та вологість; – – – сильнодіючі, легкозаймисті наркотичні, психотропних імунобіологічні, термолабільні вогненебезпечні, отруйні вибухонебезпечні ЛЗ тощо. v Приміщення, які потребують особливих умов зберігання: Вимоги до технологічного процесу Ø Склад, розташування та площа виробничих приміщень повинна забезпечити послідовність процесів: § § § приймання контроль якості зберігання комплектація заказів відпуск ЛЗ транспортування товару Ø Стандартні робочі методики процесів: § § § отримання і перевірка поставок зберігання ЛЗ очищення і обслуговування приміщень реєстрація умов зберігання документації тощо. 1 Вимоги до оснащення » » стелажі піддони холодильники прибори для визначення температури та вологості » підтоварники

Вимоги до оптової торгівлі 1 Вимоги до персоналу Вимоги до умов зберігання Вимоги до транспортування Вимоги до матеріалу Ø Загальні вимоги: СПД повинен забезпечити загальні та специфічні умови зберігання на всіх етапах технологічного процесу – забезпечення умов зберігання ЛЗ під час транспортування – вимоги до прибирання в транспорті Для покриття стін (можливість вологого прибирання) Санітарно – епідеміологічні вимоги: v Треба мати достатню кількість кваліфікованих працівників, які відповідають кваліфікаційним вимогам; v Керівник персоналу повинен мати: – – – повноваження відповідну кваліфікацію досвід – вища фармацевтична освіта стаж роботи за спеціальністю не менше 2 -х років v Наявність уповноваженої особи: – Наказ Держком України з питань регуляторної політики та підприємництва № 44/27 від 3. 03. 2009 «Про затвердження ліцензійних умов провадження господарської діяльності з виробництва ЛЗ, оптової, роздрібної торгівля ЛЗ» –спеціальний одяг; –інструменти для прибирання; –наявність маркірованого інвентарю для прибирання.

1 Реалізація ЛЗ суб'єктам господарювання Відпуск (реалізація) ЛЗ може проводитись: ü суб'єктами господарювання, що мають ліцензії на оптову торгівлю ЛЗ; ü суб'єктами господарювання, що мають ліцензії на виробництво ЛЗ (для використання у виробництві) ü суб'єктами господарювання, що мають ліцензії на роздрібну торгівлю ЛЗ; ü безпосередньо закладами охорони здоров'я.

ПОСТАВЩИКИ Оптовое 2 звено (аптечные склады, оптовые компании, аптеки) Производители (заводы, фарм. фабрики) Отечественные Зарубежные
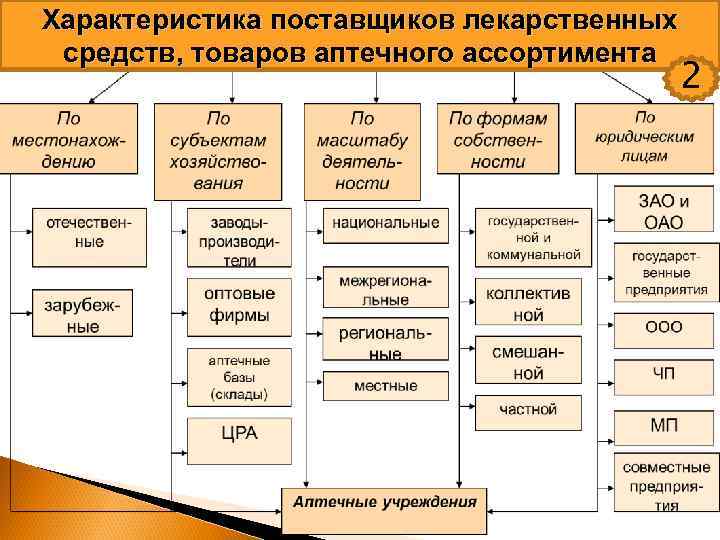
Характеристика поставщиков лекарственных средств, товаров аптечного ассортимента 2

Типичная структура оптовой фармацевтической фирмы 2 Отдел закупок: обеспечивает ассортимент оптовой фирмы (работа с поставщиками, заключение договоров, анализ и контроль поставок и др. ). Отдел торговли: занимается реализацией ЛС и ИМН покупателям (информирует о товарах, оформляет договора, контролирует товарную массу). Отдел хранения: приём ЛС и ИМН, контроль их качества, хранение согласно законодательных нормативов, отпуск товара покупателям). Отдел автоматизированного учета: осуществляет автоматизированный учет и анализ движения товара с помощью специальных компьютерных программ. Транспортный отдел: осуществляет доставку груза, полученного от поставщиков, и отправкой товара покупателям.

Процедура сертификации оптовых компаний 2 (Прик. МОЗ Украины от 23. 08. 2005 № 421) оценка комплектности поданных документов и определение сроков проведения инспекции, обобщение результатов инспекции в отчете принятие решения о выдаче (отказе) сертификата GDP. Срок действия сертификата не более 5 лет, и не более срока действия лицензии на оптовую реализацию ЛС.
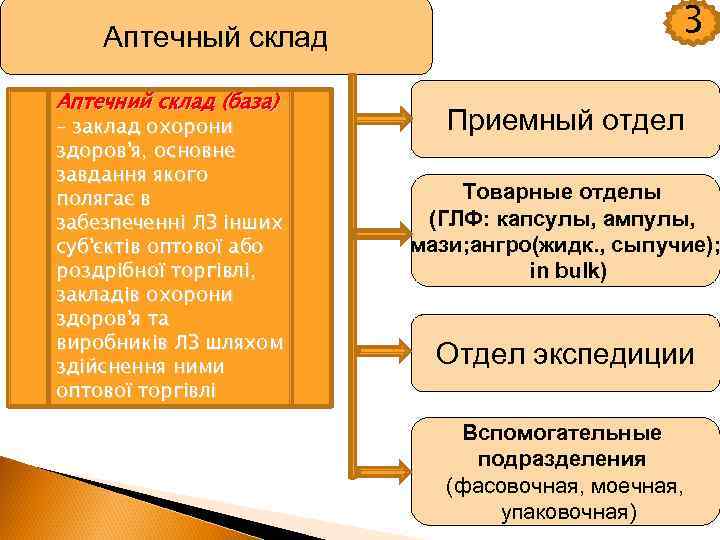
Аптечный склад Аптечний склад (база) – заклад охорони здоров'я, основне завдання якого полягає в забезпеченні ЛЗ інших суб'єктів оптової або роздрібної торгівлі, закладів охорони здоров'я та виробників ЛЗ шляхом здійснення ними оптової торгівлі 3 Приемный отдел Товарные отделы (ГЛФ: капсулы, ампулы, мази; ангро(жидк. , сыпучие); in bulk) Отдел экспедиции Вспомогательные подразделения (фасовочная, моечная, упаковочная)

Завдання аптечних складів: 3 визначати потребу в ЛЗ і ВМП (за номенклатурою та кількістю); укладати договори з постачальниками та покупцями; отримувати фармацевтичні товари від постачальників (виробники та оптові фірми різних форм власності, які мають відповідну ліцензію); здійснювати контроль якості товару; забезпечувати належні умови зберігання фармацевтичних товарів відповідно до фізикохімічних властивостей і затверджених правил, норм і вимог; організовувати раціональне постачання ЛЗ і ВМП аптечній мережі, ЛПЗ, іншим організаціям та підприємствам; створювати необхідний резерв товарів за встановленою номенклатурою і затвердженими нормами; забезпечувати транспортування відпущеного товару у відповідних умовах тощо.
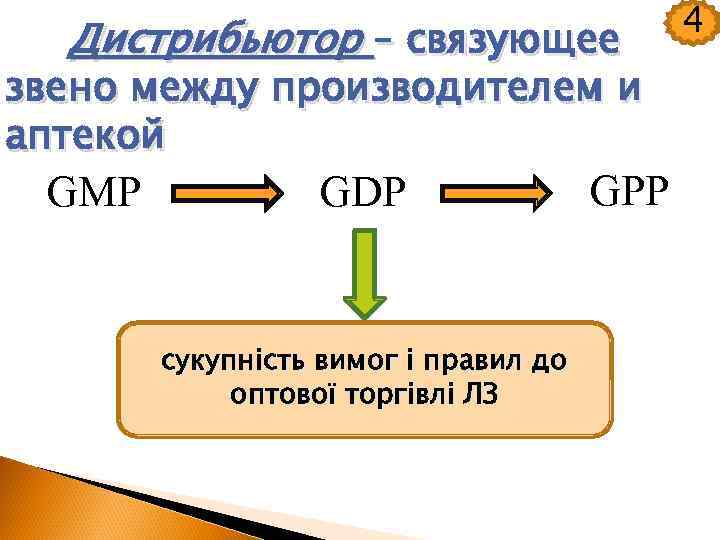
Дистрибьютор – связующее звено между производителем и аптекой GMP GDP сукупність вимог і правил до оптової торгівлі ЛЗ GPP 4

Система качества GDP должна гарантировать, что: 4 Все ЛС зарегистрированы в Украине, Будут соблюдены условия хранения ЛС, включая период транспортировки, Исключается контаминация ЛС другими ЛС и наоборот, В случае импорта ЛС будут соблюдены правила перемещения ЛС через границу Украины, Дистрибьютор примет все меры по недопущению поступления фальсифицированных ЛС в оборот и будет отслеживать движение ЛС каждой серии, поступившей в оборот.

Постанова 42 -01 -2002 (МОЗУ) «Лікарські засоби. Належна практика дистриб’юції” (GDP) (подготовлена в соответствии со ст. 10 Директивы Совета ЕС 92/25/ЕС от 31. 03. 1992. про правила оптовой реализации ЛС для человека) носит обязательный характер с 01. 2009 г. 4

4 КАБІНЕТ МІНІСТРІВ УКРАЇНИ П О С Т А Н О В А від 28 жовтня 2004 р. N 1419 Київ Деякі заходи щодо забезпечення якості лікарських засобів Відповідно до статті 9 Закону України "Про лікарські засоби" ( 123/96 -ВР ) Кабінет Міністрів України п о с т а н о в л я є: ( Із змінами, внесеними згідно з Постановою КМ N 376 від 26. 05. 2005 ) Кабінет Міністрів України п о с т а н о в л я є: 1. Міністерству охорони здоров'я забезпечити починаючи з 1 січня 2009 р. обіг лікарських засобів відповідно до вимог належної виробничої, належної виробничої дистрибуторської, лабораторної та клінічної практики, дистрибуторської, лабораторної та клінічної практики гармонізованої з відповідними директивами ЄС і ВООЗ. З цією метою: … Прем'єр-міністр України В. ЯНУКОВИЧ 18

Требование GDP: соблюдение принципа FI-FO «первым принят – первым отпущен» , заключается в том, что со склада первой должна отпускаться та продукция, которая имеет меньший срок годности. 4

Документы сопровождающие поставку 5 товара (основание для поставки – ДОГОВОР) Продавец→Покупателю 1. Накладная (ТТН) (2 экз. ) 2. Налоговая накладная 3. Сертификаты качества на каждую серию препаратов 4. Реестр ЛС (реестр сертификатов)

Поставка товара 5 Покупатель → Продавцу Подписанная накладная (1 экз) Доверенность - строгой отчетности (действит. 10 дней) - генеральная доверенность (действит. 1 год)

Документы при импорте товара: (основание для поставки – КОНТРАКТ) Инвойс (счет-фактура) Упаковочный лист Документы на перевозку ◦ автотранспорт: TIR или CMR ◦ по морю: коносамент ◦ по воздуху: авианакладная Сертификат происхождения Сертификаты качества Регистрационное свидетельство (копия) 5
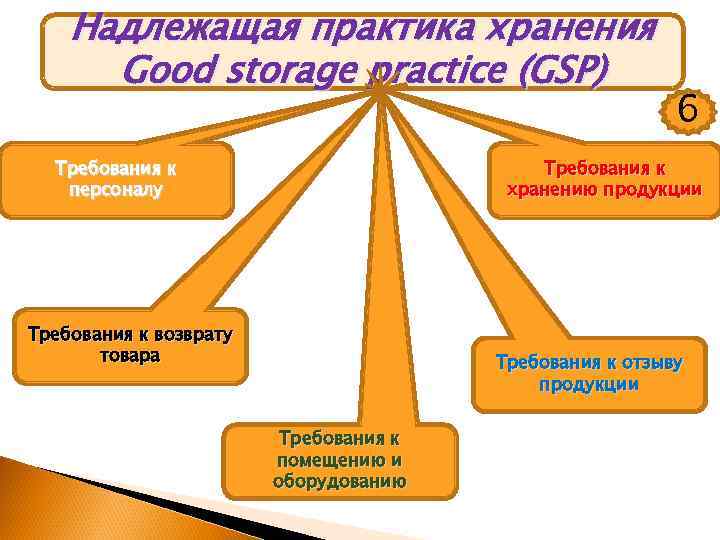
Надлежащая практика хранения Good storage practice (GSP) Требования к персоналу 6 Требования к хранению продукции Требования к возврату товара Требования к отзыву продукции Требования к помещению и оборудованию

Надлежащая практика хранения Good storage practice (GSP) Требования к возврату товара 6 Ø наличие процедуры возврата Ø процедура карантина возвращенной продукции Ø идентификация, документация, реализация, процедура уничтожения Требования к отзыву продукции детальная разработка процедуры отзыва фармацевтической продукции Требования к персоналу достаточный квалификационный уровень персонала на любом участке хранения продукции ü обучение персонала стандарту GSP ü соблюдение личной гигиены и санитарии ü наличие защитной или рабочей одежды ü

Надлежащая практика хранения Good storage practice (GSP) 6 Требования к помещению и оборудованию Наличие специально оборудованных помещений для: Ø Ø Ø исходных и упаковочных материалов промежуточных продуктов готовой продукции на карантине забракованной, возвращенной и отозванной продукции Помещения должны быть: ü ü ü чистыми, сухими с необходимой температурой защищены от погодных воздействий доступ только уполномоченного персонала санитарный контроль, уборка, дезинсекция и дератизация в случае необходимости средства безопасности и охраны (радиоактивные, взрывоопасные и др. материалы)

Надлежащая практика хранения Good storage practice (GSP) 6 Требования к хранению продукции Ø хранение письменных инструкций и отчетов по процедурам хранения продукции, движения товара Ø требования к контейнерам, их маркировке Ø требования к процедуре получения товара, его проверке (номер партии, количество, отбраковка и др. ) Ø требования к отбору проб, процедура карантина Ø требования к контролю хранимой продукции (повреждению, истечению срока годности и др. ) Ø требования к процедуре возврата продукции Ø требования к отправке, транспортировке продукции Ø приложения: требования к нормальным и специальным условиям хранения
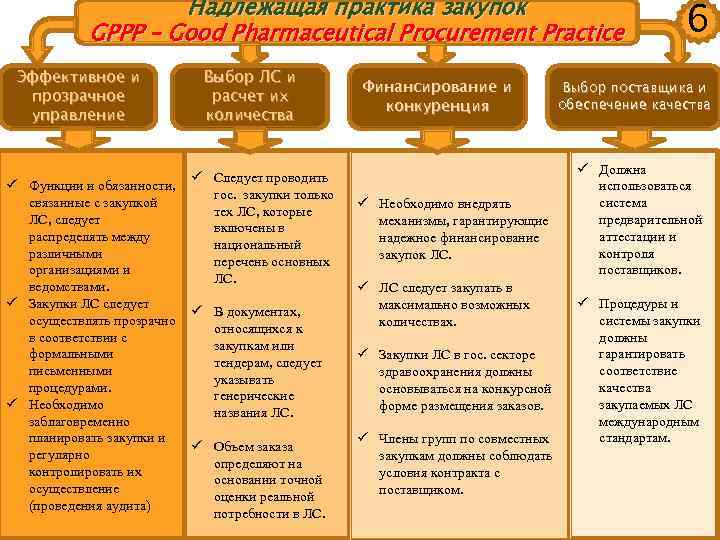
Надлежащая практика закупок GPPP – Good Pharmaceutical Procurement Practice Эффективное и прозрачное управление ü Функции и обязанности, связанные с закупкой ЛС, следует распределять между различными организациями и ведомствами. ü Закупки ЛС следует осуществлять прозрачно в соответствии с формальными письменными процедурами. ü Необходимо заблаговременно планировать закупки и регулярно контролировать их осуществление (проведения аудита) Выбор ЛС и расчет их количества ü Следует проводить гос. закупки только тех ЛС, которые включены в национальный перечень основных ЛС. ü В документах, относящихся к закупкам или тендерам, следует указывать генерические названия ЛС. ü Объем заказа определяют на основании точной оценки реальной потребности в ЛС. Финансирование и конкуренция ü Необходимо внедрять механизмы, гарантирующие надежное финансирование закупок ЛС. ü ЛС следует закупать в максимально возможных количествах. ü Закупки ЛС в гос. секторе здравоохранения должны основываться на конкурсной форме размещения заказов. ü Члены групп по совместных закупкам должны соблюдать условия контракта с поставщиком. 6 Выбор поставщика и обеспечение качества ü Должна использоваться система предварительной аттестации и контроля поставщиков. ü Процедуры и системы закупки должны гарантировать соответствие качества закупаемых ЛС международным стандартам.
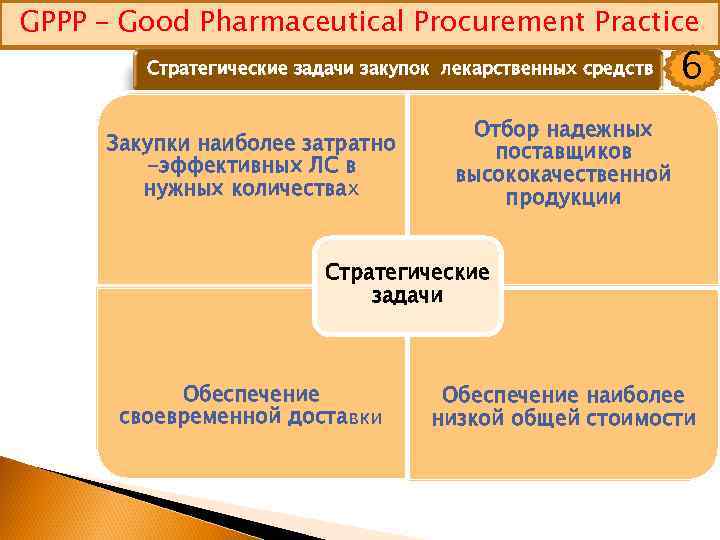
GPPP – Good Pharmaceutical Procurement Practice Стратегические задачи закупок лекарственных средств Закупки наиболее затратно -эффективных ЛС в нужных количествах 6 Отбор надежных поставщиков высококачественной продукции Стратегические задачи Обеспечение своевременной доставки Обеспечение наиболее низкой общей стоимости
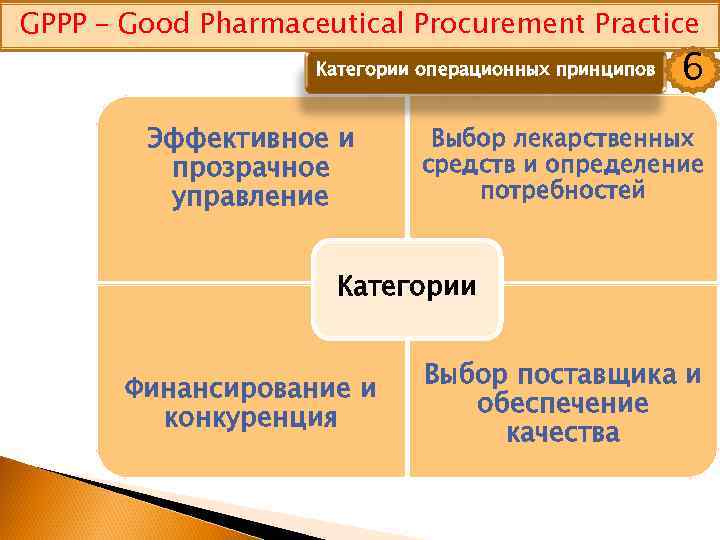
GPPP – Good Pharmaceutical Procurement Practice Категории операционных принципов Эффективное и прозрачное управление 6 Выбор лекарственных средств и определение потребностей Категории Финансирование и конкуренция Выбор поставщика и обеспечение качества

Дякую за увагу!
Лекция опт.звено 2010.ppt