р-елементи VІА групи. Оксиген та його сполуки. р-елементи



















































18926-16_p-elementi_via_grupi_oksigen_ta_sulyfur.ppt
- Количество слайдов: 69
 р-елементи VІА групи. Оксиген та його сполуки. р-елементи VІА групи. Сульфур, Селен, Телур. підготувала к.х.н., доц. Демид А.Є.
р-елементи VІА групи. Оксиген та його сполуки. р-елементи VІА групи. Сульфур, Селен, Телур. підготувала к.х.н., доц. Демид А.Є.
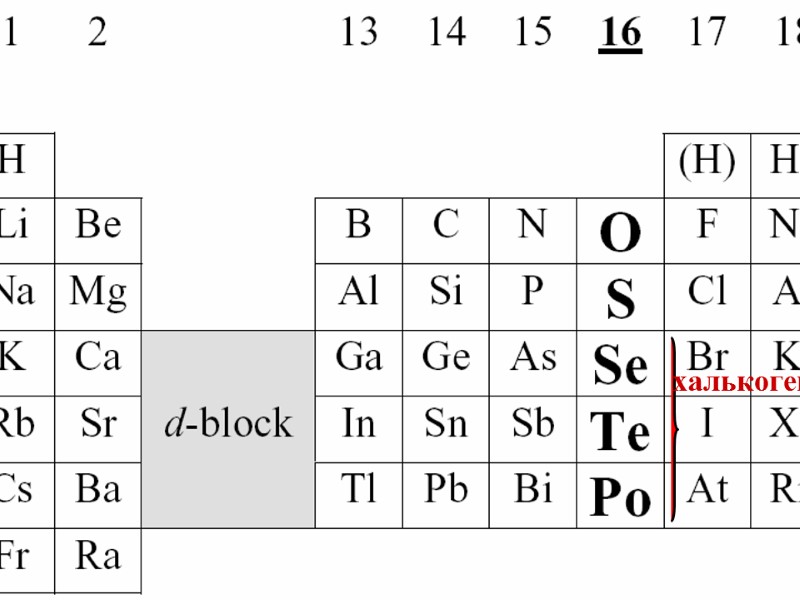
 халькогени
халькогени
 VI А група оксиген (8O), сульфур (16 S), та елементи підгрупи селену – селен (34Se), телур (52Te), полоній (84Po). O 1s22s22p4 S 2s22p63s23p4 Se 3s23p63d104s24p4 Te 4s24p64d105s25p4 Po 4s24p64d104f145s25p65d106s26p4 Полоній – радіоактивний елемент. С О, Н3О+
VI А група оксиген (8O), сульфур (16 S), та елементи підгрупи селену – селен (34Se), телур (52Te), полоній (84Po). O 1s22s22p4 S 2s22p63s23p4 Se 3s23p63d104s24p4 Te 4s24p64d105s25p4 Po 4s24p64d104f145s25p65d106s26p4 Полоній – радіоактивний елемент. С О, Н3О+

 Кисень (O2) Знаходження у природі W~23,1%; WV ~ 21%% у повітрі; Одержання Промисловий спосіб - фракціонування повітря або кріогенна ректифікація. Кисневі концентратори
Кисень (O2) Знаходження у природі W~23,1%; WV ~ 21%% у повітрі; Одержання Промисловий спосіб - фракціонування повітря або кріогенна ректифікація. Кисневі концентратори

 2. Лабораторний спосіб (розклад кисневмісних речовин): термічним розкладом оксидів неактивних металів (Ag2O, HgO): 2 HgO = 2 Hg + O2 ↑ 2) нагріванням оксидів Ме у вищих с.о. (PbO2, Pb3O4): PbO2 = Pb + O2 ↑ 3) нагріванням бертолетової солі при наявності каталізатора (MnO2): KClO3= 2KCl + 3O2 ↑ 4) розкладанням калій перманганату: 2KMnО4=K2MnО4+MnO2+О2↑
2. Лабораторний спосіб (розклад кисневмісних речовин): термічним розкладом оксидів неактивних металів (Ag2O, HgO): 2 HgO = 2 Hg + O2 ↑ 2) нагріванням оксидів Ме у вищих с.о. (PbO2, Pb3O4): PbO2 = Pb + O2 ↑ 3) нагріванням бертолетової солі при наявності каталізатора (MnO2): KClO3= 2KCl + 3O2 ↑ 4) розкладанням калій перманганату: 2KMnО4=K2MnО4+MnO2+О2↑

 5) розклад хроматів і дихроматів, у присутності H2SO4: 2K2Cr2O7+8H2SO4=2K2SO4+2Cr2(SO4)3+3O2↑+8H2O 7) розклад хлорного вапна при наявності Co2+, Cu2+: 2CaOCl2=2CaCl2+O2 ↑ 6) методом Бріна: 2BaO+O2↑=2BaO2(при 5000С) 2ВаО2= 2ВаО + О2 ↑ (при t) 8) розкладанням пероксиду гідрогену (водн.): 2Н2О2= 2Н2О + О2 ↑ 9) розкладанням нітрату: 2KNO3=2KNO2+O2 ↑ 10) із пероксидів або надпероксидів, дією на них води або СО2: 2Na2O2 + 2CO2= 2Na2CO3 + O2 ↑ 4KO2 + 2H2O= 4KOH + 3O2 ↑
5) розклад хроматів і дихроматів, у присутності H2SO4: 2K2Cr2O7+8H2SO4=2K2SO4+2Cr2(SO4)3+3O2↑+8H2O 7) розклад хлорного вапна при наявності Co2+, Cu2+: 2CaOCl2=2CaCl2+O2 ↑ 6) методом Бріна: 2BaO+O2↑=2BaO2(при 5000С) 2ВаО2= 2ВаО + О2 ↑ (при t) 8) розкладанням пероксиду гідрогену (водн.): 2Н2О2= 2Н2О + О2 ↑ 9) розкладанням нітрату: 2KNO3=2KNO2+O2 ↑ 10) із пероксидів або надпероксидів, дією на них води або СО2: 2Na2O2 + 2CO2= 2Na2CO3 + O2 ↑ 4KO2 + 2H2O= 4KOH + 3O2 ↑
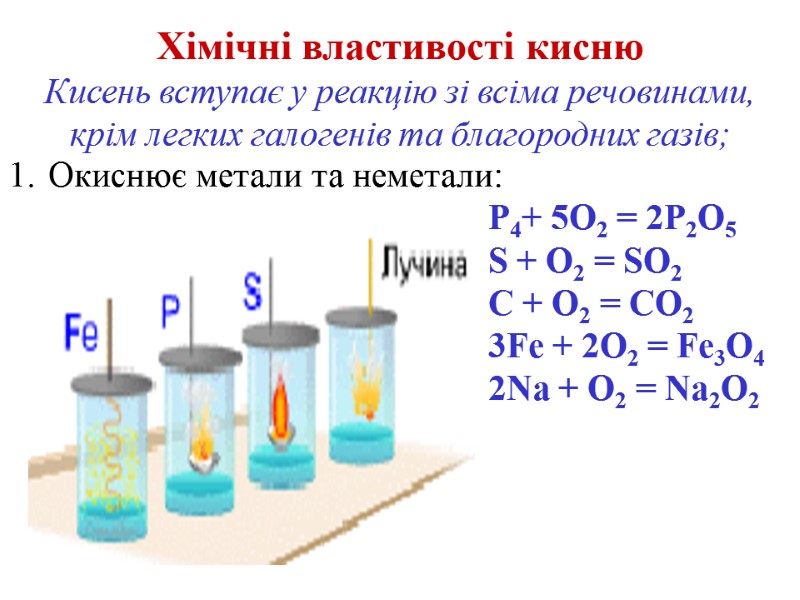
 Хімічні властивості кисню Кисень вступає у реакцію зі всіма речовинами, крім легких галогенів та благородних газів; Окиснює метали та неметали: P4+ 5O2 = 2P2O5 S + O2 = SO2 C + O2 = CO2 3Fe + 2O2 = Fe3O4 2Na + O2 = Na2O2
Хімічні властивості кисню Кисень вступає у реакцію зі всіма речовинами, крім легких галогенів та благородних газів; Окиснює метали та неметали: P4+ 5O2 = 2P2O5 S + O2 = SO2 C + O2 = CO2 3Fe + 2O2 = Fe3O4 2Na + O2 = Na2O2

 2. Окиснює неорганічні сполуки: 4NH3 + 3O2 = 2N2 + 6H2O СаН2+ О2= Са(ОН)2 4Fe(OH)2+O2+2H2O4Fe(OH)3 6FeO + O2 = 2Fe3O4 2Na2SO3 + O2 2Na2SO4 3PH3 + 4O2 = P2O5 + 3H2O 4. Окиснюється сильними окисниками: O2 + PtF6 = [O2+][PtF6-] 3. Окиснює органічні сполуки: СН4 + 2О2= СО2 + 2Н2О СН3СОН + 1/2О2= СН3СООН C6H6 + 9/2O2 = 6CO2 + 3H2O C2H5OH + 2O2 = 2CO2 + 3H2O
2. Окиснює неорганічні сполуки: 4NH3 + 3O2 = 2N2 + 6H2O СаН2+ О2= Са(ОН)2 4Fe(OH)2+O2+2H2O4Fe(OH)3 6FeO + O2 = 2Fe3O4 2Na2SO3 + O2 2Na2SO4 3PH3 + 4O2 = P2O5 + 3H2O 4. Окиснюється сильними окисниками: O2 + PtF6 = [O2+][PtF6-] 3. Окиснює органічні сполуки: СН4 + 2О2= СО2 + 2Н2О СН3СОН + 1/2О2= СН3СООН C6H6 + 9/2O2 = 6CO2 + 3H2O C2H5OH + 2O2 = 2CO2 + 3H2O
 Фізичні властивості кисню - О2 – безколірний газ, конденсується у рідину голубого кольору та тверду речовину синього кольору; - О2 тяжчий від повітря, ρ = 1,43 г/л; - парамагнітний в любому агрегатному стані; - погано розчинний у полярних розчинниках (3.15мл в 100 мл Н2О при 20оС). - добре розчинний у неполярних розчинниках;
Фізичні властивості кисню - О2 – безколірний газ, конденсується у рідину голубого кольору та тверду речовину синього кольору; - О2 тяжчий від повітря, ρ = 1,43 г/л; - парамагнітний в любому агрегатному стані; - погано розчинний у полярних розчинниках (3.15мл в 100 мл Н2О при 20оС). - добре розчинний у неполярних розчинниках;
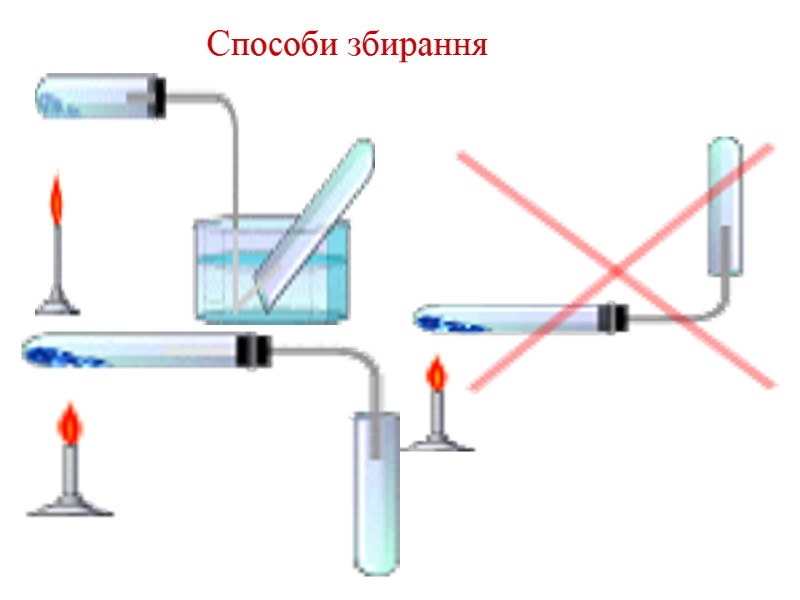
 Способи збирання
Способи збирання
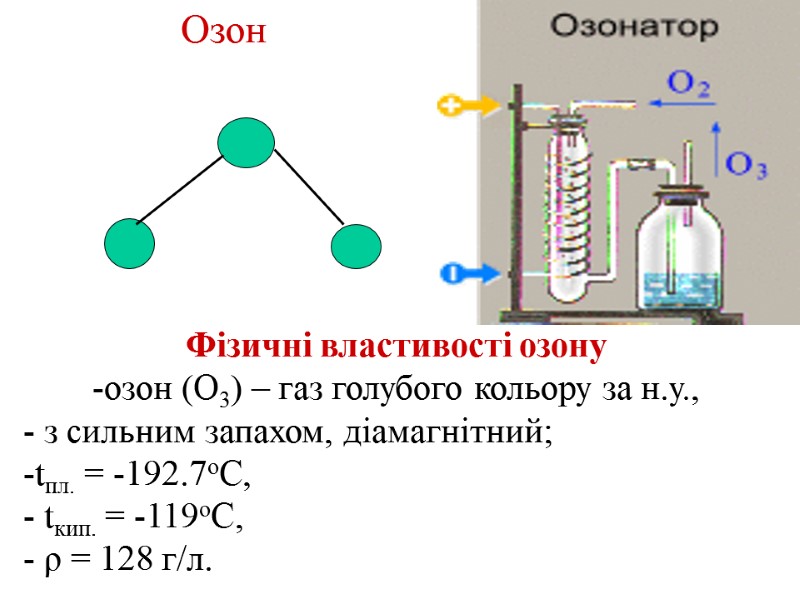
 Озон Фізичні властивості озону озон (О3) – газ голубого кольору за н.у., з сильним запахом, діамагнітний; tпл. = -192.7оС, tкип. = -119оС, - ρ = 128 г/л.
Озон Фізичні властивості озону озон (О3) – газ голубого кольору за н.у., з сильним запахом, діамагнітний; tпл. = -192.7оС, tкип. = -119оС, - ρ = 128 г/л.

 Хімічні властивості озону 1. Отримують при дії тихого електричного розряду на О2: 3O2 ⇔2O3 вихід ~10% 2. Дуже сильний окисник: O3 + 2H+ + 2e- = O2 + H20 O3 + H2O + 2e- = O2 + 2OH- O3 + S + H2O = H2SO4 в кислому середовищі O3 + 2KI + H2O = 2KOH + O2 + I2 в лужному середовищі 5O3 + 2KOH = 2KO3 (озонід)+ 5O2 + H2O
Хімічні властивості озону 1. Отримують при дії тихого електричного розряду на О2: 3O2 ⇔2O3 вихід ~10% 2. Дуже сильний окисник: O3 + 2H+ + 2e- = O2 + H20 O3 + H2O + 2e- = O2 + 2OH- O3 + S + H2O = H2SO4 в кислому середовищі O3 + 2KI + H2O = 2KOH + O2 + I2 в лужному середовищі 5O3 + 2KOH = 2KO3 (озонід)+ 5O2 + H2O
 Кисень – здатен підтримувати дихання Біологічна роль кисню та озону.
Кисень – здатен підтримувати дихання Біологічна роль кисню та озону.
 Хімічні основи використання кисню та озону в медицині та фармації
Хімічні основи використання кисню та озону в медицині та фармації


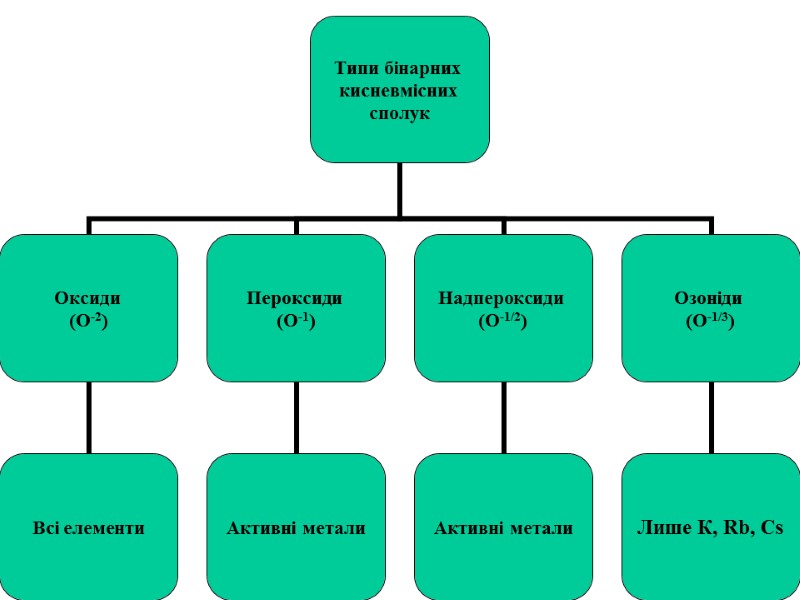
 1) Оксиди активних металів М2О, МО, М2О3, що реагують з водою; 2) Оксиди p- і d-елементів в низьких с.о. (від +1 до +3, іноді +4) ковалентні оксиди з полімерними структурами, не реагують з водою, не розчиняються у воді; 3) Оксиди p- і d-елементів в високих с.о., що є молекулярними структурами, розчинні в воді з утворенням кислот. Усі метали утворюють оксиди. Типи оксидів:
1) Оксиди активних металів М2О, МО, М2О3, що реагують з водою; 2) Оксиди p- і d-елементів в низьких с.о. (від +1 до +3, іноді +4) ковалентні оксиди з полімерними структурами, не реагують з водою, не розчиняються у воді; 3) Оксиди p- і d-елементів в високих с.о., що є молекулярними структурами, розчинні в воді з утворенням кислот. Усі метали утворюють оксиди. Типи оксидів:
 Способи отримання оксидів взаємодія простих речовин з киснем: 2Mg + O2 = 2MgO S + O2 = SO2 Cu + 1/2O2= CuO 3Fe + 2O2 = Fe3O4 N2 + O2= 2NO (30000С) - розклад кислот: 4HNO3=4NO2+2H2O+ O2 2H3BO3 = B2O3 + 3H2O -видалення води з кисневмісних кислот : 2HСlO4 + P2O5 = 2HPO4 + Cl2O7 2HNO3 + P2O5 = 2HPO3 + N2O5 - самочинна втрата води: H2CO3 = H2O + CO2
Способи отримання оксидів взаємодія простих речовин з киснем: 2Mg + O2 = 2MgO S + O2 = SO2 Cu + 1/2O2= CuO 3Fe + 2O2 = Fe3O4 N2 + O2= 2NO (30000С) - розклад кислот: 4HNO3=4NO2+2H2O+ O2 2H3BO3 = B2O3 + 3H2O -видалення води з кисневмісних кислот : 2HСlO4 + P2O5 = 2HPO4 + Cl2O7 2HNO3 + P2O5 = 2HPO3 + N2O5 - самочинна втрата води: H2CO3 = H2O + CO2
 Способи отримання оксидів Hg(OH)2 = HgO + H2O 2AgOH = Ag2O + H2O розклад основ: Mg(OH)2 = MgO + H2O Ba(OH)2 = BaO + H2O Якщо оксид металу термічно нестійкий, то утворюється вільний метал: 2Ag2CO3 4Ag + O2 +CO2 Hg(NO3)2 Hg + 2NO2 + O2 - розклад солей: CaCO3 CaO + CO2 Fe2(SO4)3 Fe2O3 + 3SO3 2Pb(NO3)2 2PbO + 4NO2 + O2
Способи отримання оксидів Hg(OH)2 = HgO + H2O 2AgOH = Ag2O + H2O розклад основ: Mg(OH)2 = MgO + H2O Ba(OH)2 = BaO + H2O Якщо оксид металу термічно нестійкий, то утворюється вільний метал: 2Ag2CO3 4Ag + O2 +CO2 Hg(NO3)2 Hg + 2NO2 + O2 - розклад солей: CaCO3 CaO + CO2 Fe2(SO4)3 Fe2O3 + 3SO3 2Pb(NO3)2 2PbO + 4NO2 + O2
 ряд P2O5 – SO3 – Cl2O7: 1/3P2O5(k)+H2O=2/3H3PO4(k),G=-52кДж/моль SO3(k) + H2O(p) = H2SO4(p), G= - 76 кДж/моль Сl2O7(г)+ H2O(p)= 2HClO4(p),G= - 331 кДж/моль Властивості оксидів ряд Na2O–MgO–Al2O3 Na2O(k) + H2O(p) = 2NaOH(k), G= - 147 кДж/моль MgO(k) + H2O(p) = Mg(OH)2(k), G= -27 кДж/моль 1/3Al2O3(k) + H2O(p) = 2/3Al(OH)3(k), G= 6 кДж/моль
ряд P2O5 – SO3 – Cl2O7: 1/3P2O5(k)+H2O=2/3H3PO4(k),G=-52кДж/моль SO3(k) + H2O(p) = H2SO4(p), G= - 76 кДж/моль Сl2O7(г)+ H2O(p)= 2HClO4(p),G= - 331 кДж/моль Властивості оксидів ряд Na2O–MgO–Al2O3 Na2O(k) + H2O(p) = 2NaOH(k), G= - 147 кДж/моль MgO(k) + H2O(p) = Mg(OH)2(k), G= -27 кДж/моль 1/3Al2O3(k) + H2O(p) = 2/3Al(OH)3(k), G= 6 кДж/моль

 ГІПС ХАЛЬКОПІРИТ САМОРОДНА СІРКА
ГІПС ХАЛЬКОПІРИТ САМОРОДНА СІРКА
 S1s22s22p63s23p33d1 с.о. +4 Будова атома, електронна формула та розміщення електронів по рівнях і підрівнях S1s22s22p63s23p43d0 с.о. -2, +2 S1s22s22p63s13p33d2 с.о. +6 найхарактерніші с.о. –2, +2, +4, +6.
S1s22s22p63s23p33d1 с.о. +4 Будова атома, електронна формула та розміщення електронів по рівнях і підрівнях S1s22s22p63s23p43d0 с.о. -2, +2 S1s22s22p63s13p33d2 с.о. +6 найхарактерніші с.о. –2, +2, +4, +6.
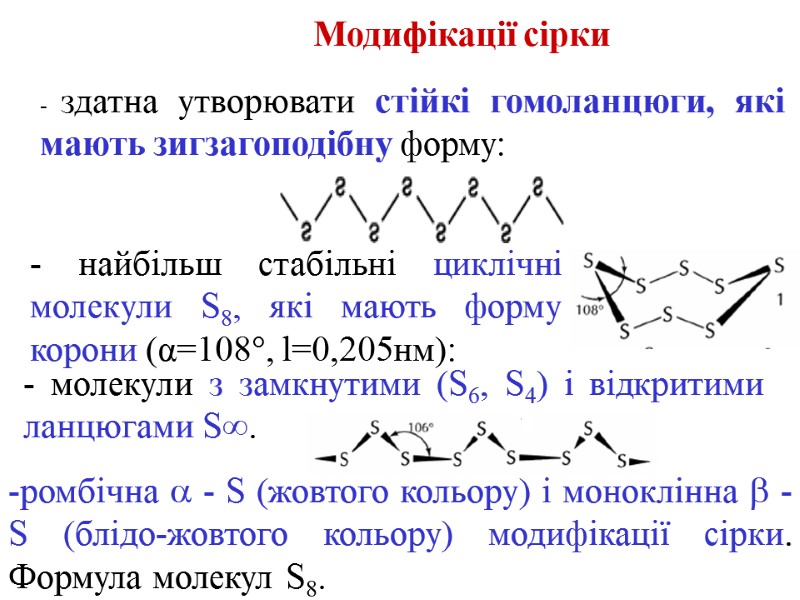
 - молекули з замкнутими (S6, S4) і відкритими ланцюгами S∞. Модифікації сірки - здатна утворювати стійкі гомоланцюги, які мають зигзагоподібну форму: - найбільш стабільні циклічні молекули S8, які мають форму корони (α=108, l=0,205нм): ромбічна - S (жовтого кольору) і моноклінна -S (блідо-жовтого кольору) модифікації сірки. Формула молекул S8.
- молекули з замкнутими (S6, S4) і відкритими ланцюгами S∞. Модифікації сірки - здатна утворювати стійкі гомоланцюги, які мають зигзагоподібну форму: - найбільш стабільні циклічні молекули S8, які мають форму корони (α=108, l=0,205нм): ромбічна - S (жовтого кольору) і моноклінна -S (блідо-жовтого кольору) модифікації сірки. Формула молекул S8.
 Модифікації сірки малостійка пластична сірка складається з нерегулярно розміщених зигзагоподібних ланцюгів Sn (де n досягає декількох тисяч). інші нестійкі модифікації S2 (пурпурна), S6(оранжево–жовта) та інші.
Модифікації сірки малостійка пластична сірка складається з нерегулярно розміщених зигзагоподібних ланцюгів Sn (де n досягає декількох тисяч). інші нестійкі модифікації S2 (пурпурна), S6(оранжево–жовта) та інші.
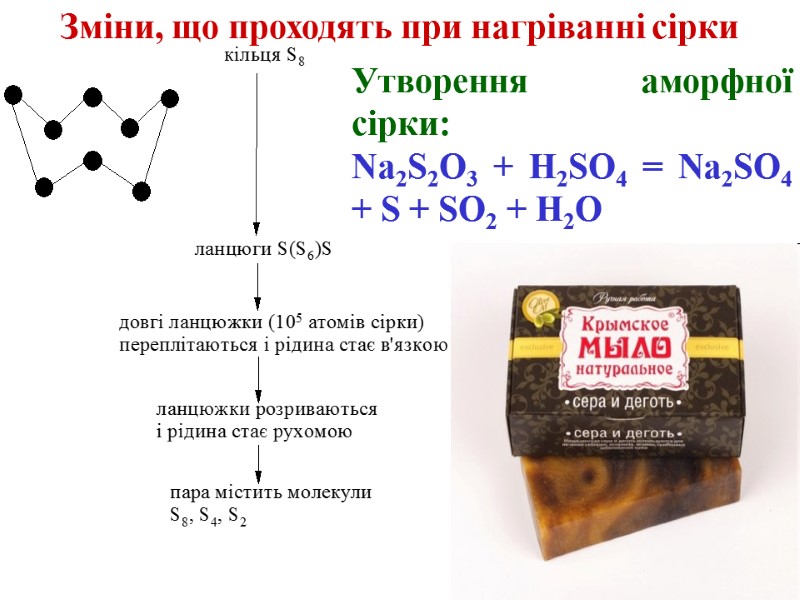
 Утворення аморфної сірки: Na2S2O3 + H2SO4 = Na2SO4 + S + SO2 + H2O Зміни, що проходять при нагріванні сірки
Утворення аморфної сірки: Na2S2O3 + H2SO4 = Na2SO4 + S + SO2 + H2O Зміни, що проходять при нагріванні сірки
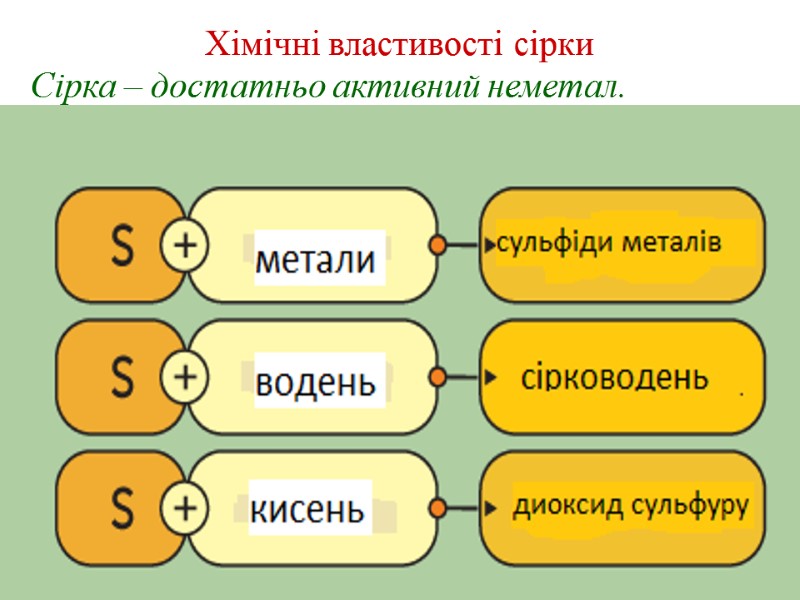
 Хімічні властивості сірки Сірка – достатньо активний неметал.
Хімічні властивості сірки Сірка – достатньо активний неметал.
 з лужними металами без нагрівання: 2Na + S Na2S з рештою металів (окрім Au, Pt) - при підвищеній t°: Zn + S ZnS S + Сu CuS + Q Fe + S FeS + Q
з лужними металами без нагрівання: 2Na + S Na2S з рештою металів (окрім Au, Pt) - при підвищеній t°: Zn + S ZnS S + Сu CuS + Q Fe + S FeS + Q

 з деякими неметалами сірка утворює бінарні сполуки: H2 + S H2S 2P + 3S P2S3 C + 2S CS2 легко окиснюється киснем, галогенами (крім йоду) та кислотами - окисниками: S + 6F SF6 S + O2 SO2 + Q S + 2H2SO4(конц) 3SO2 + 2H2O S + 6HNO3(конц) H2SO4 + 6NO2 + 2H2O при нагріванні у розчинах лугів сірка диспропорціонує: 3S + 6NaOH 2Na2S + Na2SO3 + 3H2O
з деякими неметалами сірка утворює бінарні сполуки: H2 + S H2S 2P + 3S P2S3 C + 2S CS2 легко окиснюється киснем, галогенами (крім йоду) та кислотами - окисниками: S + 6F SF6 S + O2 SO2 + Q S + 2H2SO4(конц) 3SO2 + 2H2O S + 6HNO3(конц) H2SO4 + 6NO2 + 2H2O при нагріванні у розчинах лугів сірка диспропорціонує: 3S + 6NaOH 2Na2S + Na2SO3 + 3H2O
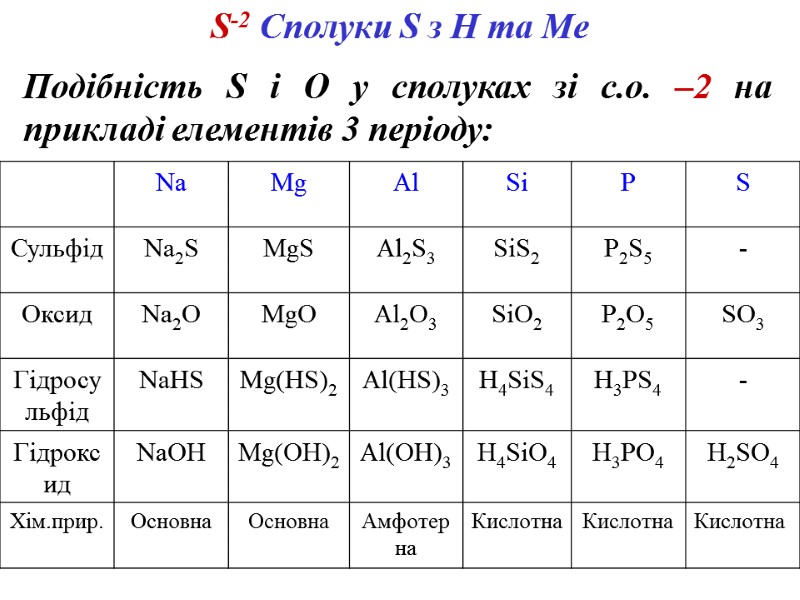
 Подібність S і О у сполуках зі с.о. –2 на прикладі елементів 3 періоду: S-2 Сполуки S з H та Me
Подібність S і О у сполуках зі с.о. –2 на прикладі елементів 3 періоду: S-2 Сполуки S з H та Me
 -сульфіди s – елементів І групи розчинні у воді: Na2S + HOH NaHS + NaOH S2– + H2O HS– + OH–, К/дис= 10–7 HS– + H2O H2S + OH–, К//дис= 1,3·10–13 - сульфіди неметалів гідролізують необоротно з утворенням відповідних кислот: SiS2 + 3H2O = H2SiO3 + 2H2S гідроліз амфотерних сульфідів, наприклад, Al2S3, Fe2S3, Cr2S3 повністю гідролізують: Al2S3 + 6H2O = 2Al(OH)3 + 3H2S
-сульфіди s – елементів І групи розчинні у воді: Na2S + HOH NaHS + NaOH S2– + H2O HS– + OH–, К/дис= 10–7 HS– + H2O H2S + OH–, К//дис= 1,3·10–13 - сульфіди неметалів гідролізують необоротно з утворенням відповідних кислот: SiS2 + 3H2O = H2SiO3 + 2H2S гідроліз амфотерних сульфідів, наприклад, Al2S3, Fe2S3, Cr2S3 повністю гідролізують: Al2S3 + 6H2O = 2Al(OH)3 + 3H2S
 молекула має кутову форму, тому вона полярна; сірководень в звичайних умовах – газ; -має неприємний запах і дуже отруйний; - трохи важчий за повітря; -розчинний у воді (0.1 М розчин - сірководнева вода або сульфідна кислота, (К1 = 6 10-8)). У воді H2S дисоціює: H2S + H2О H3O+ + HS–. Сірководень H2S
молекула має кутову форму, тому вона полярна; сірководень в звичайних умовах – газ; -має неприємний запах і дуже отруйний; - трохи важчий за повітря; -розчинний у воді (0.1 М розчин - сірководнева вода або сульфідна кислота, (К1 = 6 10-8)). У воді H2S дисоціює: H2S + H2О H3O+ + HS–. Сірководень H2S
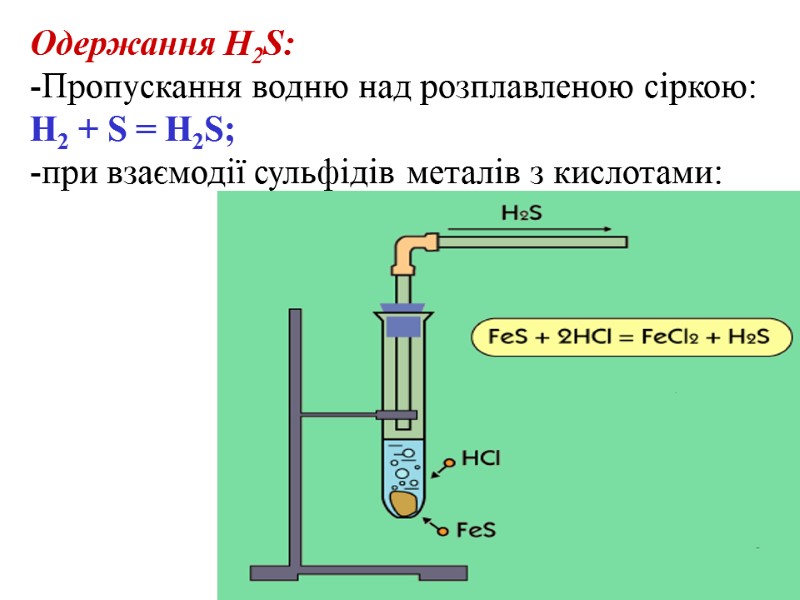
 Одержання H2S: Пропускання водню над розплавленою сіркою: Н2 + S = H2S; при взаємодії сульфідів металів з кислотами:
Одержання H2S: Пропускання водню над розплавленою сіркою: Н2 + S = H2S; при взаємодії сульфідів металів з кислотами:

 Хімічні властивості Н2S за окисно – відновними властивостями гідроген сульфід і солі сульфіди – відновники: S + 2e = S2-, E = - 0,48В
Хімічні властивості Н2S за окисно – відновними властивостями гідроген сульфід і солі сульфіди – відновники: S + 2e = S2-, E = - 0,48В
 H2S згоряє в повітрі (надлишок кисню): 2H2S + 3O2 = 2H2O + 2SO2 (недостача кисню): 2H2S + O2 = 2H2O + 2S при дії інших окисників: 2KMnO4+5H2S+3H2SO4=2MnSO4+5S+K2SO4+8H2O, H2S + Br2 = S + 2HBr H2S + 2FeCl3 = 2FeCl2 + S + 2HCl 4PbO2 + H2S = 4PbO + SO3 + H2O 3H2S + 8HNO3(розв) = 3H2SO4 + 8NO + 4H2O H2S + 4Br2 + 4H2O = H2SO4 + 8HBr
H2S згоряє в повітрі (надлишок кисню): 2H2S + 3O2 = 2H2O + 2SO2 (недостача кисню): 2H2S + O2 = 2H2O + 2S при дії інших окисників: 2KMnO4+5H2S+3H2SO4=2MnSO4+5S+K2SO4+8H2O, H2S + Br2 = S + 2HBr H2S + 2FeCl3 = 2FeCl2 + S + 2HCl 4PbO2 + H2S = 4PbO + SO3 + H2O 3H2S + 8HNO3(розв) = 3H2SO4 + 8NO + 4H2O H2S + 4Br2 + 4H2O = H2SO4 + 8HBr
 H2S взаємодіє з кислотами-окисниками та галогенами з утворенням аморфної сірки: H2SO4 + H2S = H2SO3 + H2O + S (при t): H2S + 3H2SO4 (конц) = 4S + 4O2 + 4H2O H2S + Hal2 = 2HHal + S H2S взаємодіє з солями з утворенням сульфідів: H2S + CuSO4 = CuS + H2SO4 - сульфіди отримують за обмінними реакціями (якісна реакція на S2-): MnSO4 + Na2S = Na2SO4 + MnS CuSO4 + Na2S = H2SO4 + CuS (чорні осади) срібло при контакті з гідроген сульфідом чорніє (якісна реакція на S2-): 4Ag+2H2S+O2= 2Ag2S + 2H2O
H2S взаємодіє з кислотами-окисниками та галогенами з утворенням аморфної сірки: H2SO4 + H2S = H2SO3 + H2O + S (при t): H2S + 3H2SO4 (конц) = 4S + 4O2 + 4H2O H2S + Hal2 = 2HHal + S H2S взаємодіє з солями з утворенням сульфідів: H2S + CuSO4 = CuS + H2SO4 - сульфіди отримують за обмінними реакціями (якісна реакція на S2-): MnSO4 + Na2S = Na2SO4 + MnS CuSO4 + Na2S = H2SO4 + CuS (чорні осади) срібло при контакті з гідроген сульфідом чорніє (якісна реакція на S2-): 4Ag+2H2S+O2= 2Ag2S + 2H2O
 Персульфіди M2Sn є аналогами H2O2. S22- - окисник: Na2S2 + SnS = SnS2 + Na2S S22- - відновник: 4FeS2 + 11O2 = 2Fe2O3 + 8SO2 S22- - окисник – відновник: Na2S2 = Na2S + S
Персульфіди M2Sn є аналогами H2O2. S22- - окисник: Na2S2 + SnS = SnS2 + Na2S S22- - відновник: 4FeS2 + 11O2 = 2Fe2O3 + 8SO2 S22- - окисник – відновник: Na2S2 = Na2S + S
 Оксигенвмісні сполуки Сульфуру зі с.о. +4 та +6 Деякі властивості оксидів елементів підгрупи сульфуру
Оксигенвмісні сполуки Сульфуру зі с.о. +4 та +6 Деякі властивості оксидів елементів підгрупи сульфуру
 Діоксид сульфуру – SO2 (оксид сульфуру (IV), сірчистий газ). молекула утворює рівнобедрений трикутник; газ з різким характерним запахом паленої сірки; - атом S знаходиться в sp2 – гібридизованому стані. У лабораторії:Na2SO3+H2SO4=Na2SO4+H2O+ SO2 добре розчинний у воді; водний розчин SO2 називають сульфітною кислотою (H2SO3) - SO2 – ангідрид сульфітної кислоти. В техніці : S + O2 = SO2 4FeS2 + 11O2 = 8SO2 + 2Fe2O3
Діоксид сульфуру – SO2 (оксид сульфуру (IV), сірчистий газ). молекула утворює рівнобедрений трикутник; газ з різким характерним запахом паленої сірки; - атом S знаходиться в sp2 – гібридизованому стані. У лабораторії:Na2SO3+H2SO4=Na2SO4+H2O+ SO2 добре розчинний у воді; водний розчин SO2 називають сульфітною кислотою (H2SO3) - SO2 – ангідрид сульфітної кислоти. В техніці : S + O2 = SO2 4FeS2 + 11O2 = 8SO2 + 2Fe2O3
 Сульфітна кислота - кислота середньої сили (Ка1=210–2, Ка2 = 610–8). ЇЇ солі – сульфіти та гідросульфіти: NaOH + SO2 = NaHSO3; 2NaOH + SO2 = Na2SO3 + H2O.
Сульфітна кислота - кислота середньої сили (Ка1=210–2, Ка2 = 610–8). ЇЇ солі – сульфіти та гідросульфіти: NaOH + SO2 = NaHSO3; 2NaOH + SO2 = Na2SO3 + H2O.

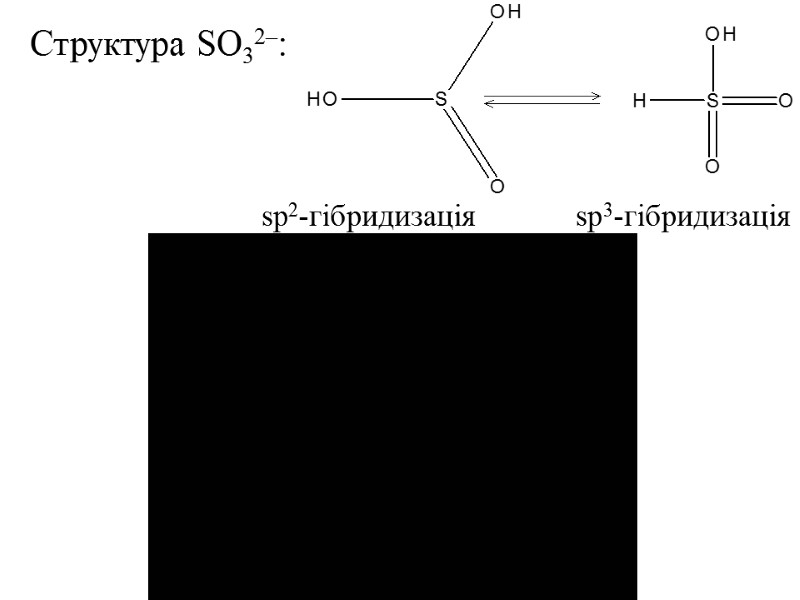
 Структура SO32–: sp2-гібридизація sp3-гібридизація
Структура SO32–: sp2-гібридизація sp3-гібридизація
 - піддаються гідролізу: SO32–+H2O=HSO3–+OH– HSO3– + H2O=H2SO3 + OH– - диспропорціонування: 2Na2SO3 (t)= 3Na2SO4 + Na2S. -окиснення: 2Na2SO3+O2=2Na2SO4 - відновні властивості SO2: SO2 + Cl2 (hν)= SO2Cl2 та при дії інших окисників: SO2 + Br2 + 2H2O = H2SO4 + 2HBr 5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4 -окисні властивості: SO2 + 2H2S = 3S + 2H2O.
- піддаються гідролізу: SO32–+H2O=HSO3–+OH– HSO3– + H2O=H2SO3 + OH– - диспропорціонування: 2Na2SO3 (t)= 3Na2SO4 + Na2S. -окиснення: 2Na2SO3+O2=2Na2SO4 - відновні властивості SO2: SO2 + Cl2 (hν)= SO2Cl2 та при дії інших окисників: SO2 + Br2 + 2H2O = H2SO4 + 2HBr 5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4 -окисні властивості: SO2 + 2H2S = 3S + 2H2O.
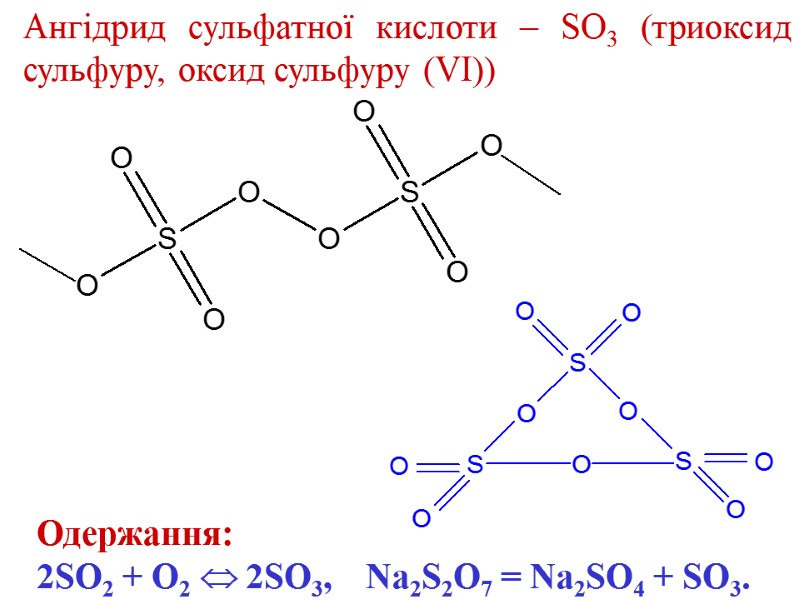
 Ангідрид сульфатної кислоти – SO3 (триоксид сульфуру, оксид сульфуру (VI)) модифікації SO3: α-SO3 – голчасті, азбестоподібні кристали; β-SO3 утворюється, коли на α-SO3 попадає волога; sp2-гібридизація -SO3 утворюється при охолодженні, прозора маса, подібна до льоду (льодоподібна модифікація).
Ангідрид сульфатної кислоти – SO3 (триоксид сульфуру, оксид сульфуру (VI)) модифікації SO3: α-SO3 – голчасті, азбестоподібні кристали; β-SO3 утворюється, коли на α-SO3 попадає волога; sp2-гібридизація -SO3 утворюється при охолодженні, прозора маса, подібна до льоду (льодоподібна модифікація).
 Ангідрид сульфатної кислоти – SO3 (триоксид сульфуру, оксид сульфуру (VI)) Одержання: 2SO2 + O2 2SO3, Na2S2O7 = Na2SO4 + SO3.
Ангідрид сульфатної кислоти – SO3 (триоксид сульфуру, оксид сульфуру (VI)) Одержання: 2SO2 + O2 2SO3, Na2S2O7 = Na2SO4 + SO3.
 - масляниста рідина; замерзає при 10,4С; в твердому і рідкому стані молекули H2SO4 зв’язані водневими зв’язками; сильна двоосновна кислота (K1 = 110-3, K2 = 1,2 10–2). тетраоксосульфат (IV) гідрогену
- масляниста рідина; замерзає при 10,4С; в твердому і рідкому стані молекули H2SO4 зв’язані водневими зв’язками; сильна двоосновна кислота (K1 = 110-3, K2 = 1,2 10–2). тетраоксосульфат (IV) гідрогену


 ZnO+H2SO4=ZnSO4+H2O Хімічні властивості сульфатної кислоти 2NaOH+H2SO4=Na2SO4+H2O Zn+H2SO4=ZnSO4+H2 2NaCl+H2SO4=2HCl+ Na2SO4
ZnO+H2SO4=ZnSO4+H2O Хімічні властивості сульфатної кислоти 2NaOH+H2SO4=Na2SO4+H2O Zn+H2SO4=ZnSO4+H2 2NaCl+H2SO4=2HCl+ Na2SO4
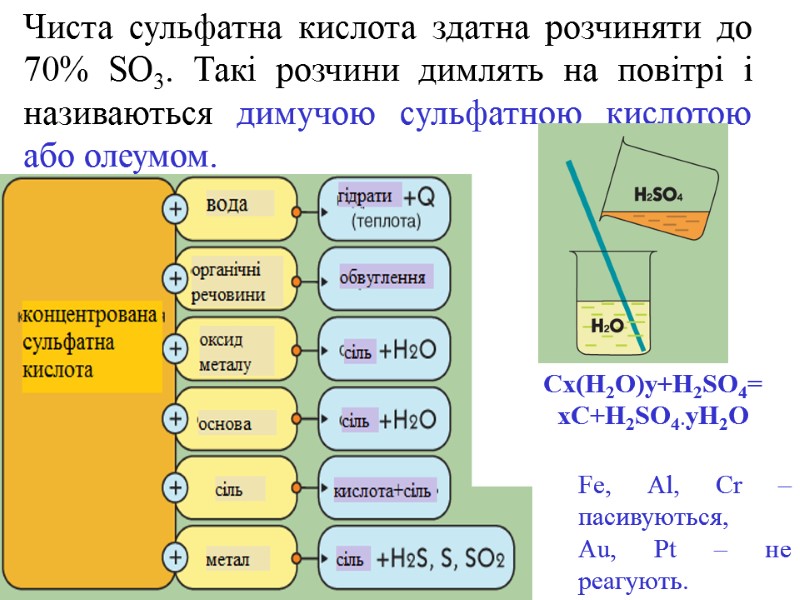
 Чиста сульфатна кислота здатна розчиняти до 70% SO3. Такі розчини димлять на повітрі і називаються димучою сульфатною кислотою або олеумом. Cx(H2O)y+H2SO4= xC+H2SO4·yH2O Fe, Al, Cr – пасивуються, Au, Pt – не реагують.
Чиста сульфатна кислота здатна розчиняти до 70% SO3. Такі розчини димлять на повітрі і називаються димучою сульфатною кислотою або олеумом. Cx(H2O)y+H2SO4= xC+H2SO4·yH2O Fe, Al, Cr – пасивуються, Au, Pt – не реагують.

 Схема взаємодії H2SO4 з металами
Схема взаємодії H2SO4 з металами
 Концентрована сульфатна кислота – сильнийний окисник. Окиснює НІ або HBr (але не HCl) до вільних галогенів, вугілля до СО2, сірку – до SO2: 8HI + H2SO4 = I2 + H2S + 4H2S 2HBr + H2SO4 = Br2 + SO2 + 2H2O реагує при нагріванні з деякими неметалами: С + 2H2SO4 (конц) = CO2 + 2SO2 + 2H2O S + 2H2SO4 (конц) = 3SO2 + 2H2O 2P + 5H2SO4 (конц) = 5SO2 + 2H3PO4 + 2H2O
Концентрована сульфатна кислота – сильнийний окисник. Окиснює НІ або HBr (але не HCl) до вільних галогенів, вугілля до СО2, сірку – до SO2: 8HI + H2SO4 = I2 + H2S + 4H2S 2HBr + H2SO4 = Br2 + SO2 + 2H2O реагує при нагріванні з деякими неметалами: С + 2H2SO4 (конц) = CO2 + 2SO2 + 2H2O S + 2H2SO4 (конц) = 3SO2 + 2H2O 2P + 5H2SO4 (конц) = 5SO2 + 2H3PO4 + 2H2O
 солі H2SO4 - сульфати. Погано розчинні сульфати Ba(II), Sr(II), Pb(II), Ca(II). кислі солі – гідросульфати NaHSO4. Вони водорозчинні.
солі H2SO4 - сульфати. Погано розчинні сульфати Ba(II), Sr(II), Pb(II), Ca(II). кислі солі – гідросульфати NaHSO4. Вони водорозчинні.
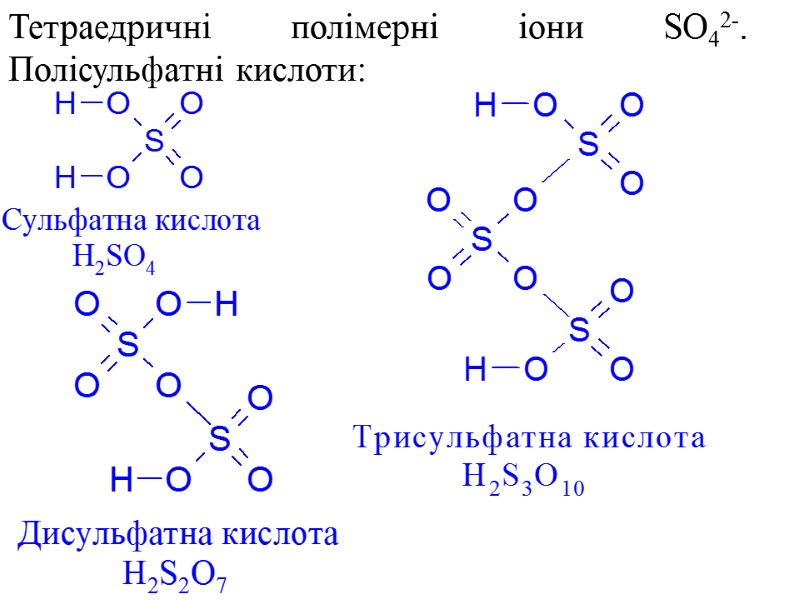
 Тетраедричні полімерні іони SO42-. Полісульфатні кислоти:
Тетраедричні полімерні іони SO42-. Полісульфатні кислоти:
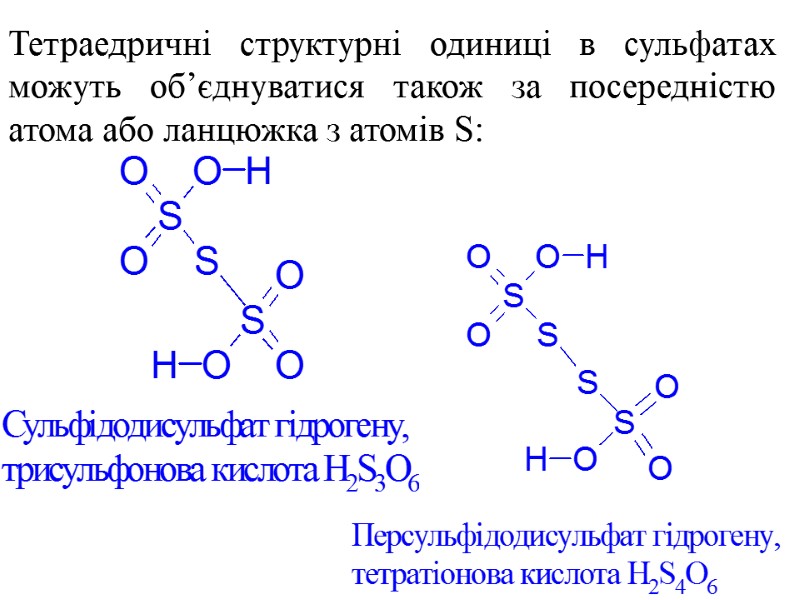
 Тетраедричні структурні одиниці в сульфатах можуть об’єднуватися також за посередністю атома або ланцюжка з атомів S:
Тетраедричні структурні одиниці в сульфатах можуть об’єднуватися також за посередністю атома або ланцюжка з атомів S:
 Хлорсульфонова кислота HSO3Cl – рідина, що димить на повітрі. Пероксомоносульфатна кислота (кислота Каро) H2SO5: H–O–SO2–Cl+H–O–O–HHO–SO2–O–OH+HCl Пероксодисульфатна кислота H2S2O8 електроліз H2SO4 або HSO4-: 2HSO4– - 2e = H2S2O8. Гідроліз H2S2O8 i H2SO5 : H2S2O8 + 2H2O = 2H2SO4 + H2O2, H2SO5 + H2O = H2O2 + H2SO4.
Хлорсульфонова кислота HSO3Cl – рідина, що димить на повітрі. Пероксомоносульфатна кислота (кислота Каро) H2SO5: H–O–SO2–Cl+H–O–O–HHO–SO2–O–OH+HCl Пероксодисульфатна кислота H2S2O8 електроліз H2SO4 або HSO4-: 2HSO4– - 2e = H2S2O8. Гідроліз H2S2O8 i H2SO5 : H2S2O8 + 2H2O = 2H2SO4 + H2O2, H2SO5 + H2O = H2O2 + H2SO4.
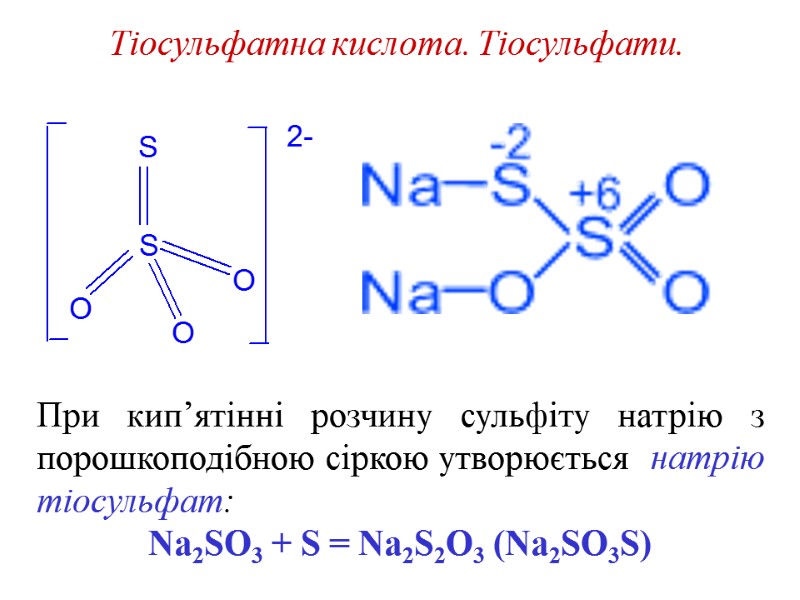
 Тіосульфатна кислота. Тіосульфати. При кип’ятінні розчину сульфіту натрію з порошкоподібною сіркою утворюється натрію тіосульфат: Na2SO3 + S = Na2S2O3 (Na2SO3S)
Тіосульфатна кислота. Тіосульфати. При кип’ятінні розчину сульфіту натрію з порошкоподібною сіркою утворюється натрію тіосульфат: Na2SO3 + S = Na2S2O3 (Na2SO3S)
 При дії сильних кислот (H2SO4) на тіосульфати утворюється тіосульфат гідрогену H2SO3S, який є нестійкий: Na2S2O3 + H2SO4 = Na2SO4 + H2S2O3 H2S2O3 = H2О + SO2 + S0 Властивості сульфідотриоксосульфатів (тіосульфатів) зумовлені присутністю атомів сульфуру в двох різних с.о.:
При дії сильних кислот (H2SO4) на тіосульфати утворюється тіосульфат гідрогену H2SO3S, який є нестійкий: Na2S2O3 + H2SO4 = Na2SO4 + H2S2O3 H2S2O3 = H2О + SO2 + S0 Властивості сульфідотриоксосульфатів (тіосульфатів) зумовлені присутністю атомів сульфуру в двох різних с.о.:
 Na2S2O3– сильний відновник. Сильні окисники (Cl2, Br2, KMnO4, K2Cr2O7) окиснюють його до SO42-: Na2SO3S + 4Cl2 + 5H2O 2Н2SO4 +2NaCl + 6HCl SO3S2– + 5H2O – 8e 2SO42– + 10H+ 1 Cl2 + 2e 2Cl– 4 SO3S2– + 5H2O + 4Cl2 2SO42– + 10H+ + 8Cl– При недостачі сильних окисників Na2SO3S окиснюється лише до S: Na2SO3S + Br2 + H2O Na2SO4 + S + 2HBr SO3S2– + H2O – 2e S + SO42– + 2H+ 1 Br2 + 2e 2Br– 1 SO3S2– + H2O + Br2 S + SO42– + 2H+ + 2Br–
Na2S2O3– сильний відновник. Сильні окисники (Cl2, Br2, KMnO4, K2Cr2O7) окиснюють його до SO42-: Na2SO3S + 4Cl2 + 5H2O 2Н2SO4 +2NaCl + 6HCl SO3S2– + 5H2O – 8e 2SO42– + 10H+ 1 Cl2 + 2e 2Cl– 4 SO3S2– + 5H2O + 4Cl2 2SO42– + 10H+ + 8Cl– При недостачі сильних окисників Na2SO3S окиснюється лише до S: Na2SO3S + Br2 + H2O Na2SO4 + S + 2HBr SO3S2– + H2O – 2e S + SO42– + 2H+ 1 Br2 + 2e 2Br– 1 SO3S2– + H2O + Br2 S + SO42– + 2H+ + 2Br–
 Слабкі окисники (I2, Fe3+, Cu2+) окиснюють S2O32- до тетратіонат-йону: 2Na2SO3S + I2 Na2S4O6 + 2NaI (йодометрія)
Слабкі окисники (I2, Fe3+, Cu2+) окиснюють S2O32- до тетратіонат-йону: 2Na2SO3S + I2 Na2S4O6 + 2NaI (йодометрія)
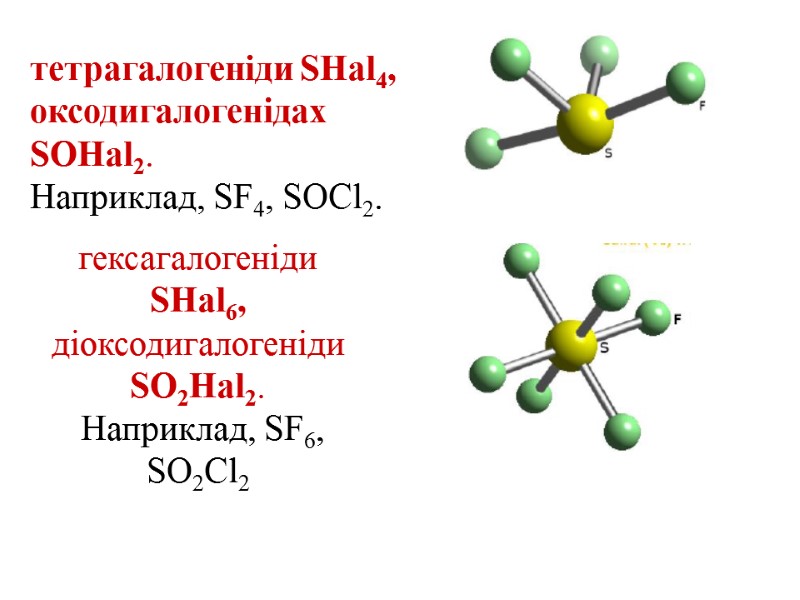
 тетрагалогеніди SHal4, оксодигалогенідах SOHal2. Наприклад, SF4, SOCl2. гексагалогеніди SHal6, діоксодигалогеніди SO2Hal2. Наприклад, SF6, SO2Сl2
тетрагалогеніди SHal4, оксодигалогенідах SOHal2. Наприклад, SF4, SOCl2. гексагалогеніди SHal6, діоксодигалогеніди SO2Hal2. Наприклад, SF6, SO2Сl2

