 Q цикл
Q цикл
 Q-цикл П. Митчелла l МИТЧЕЛЛ Питер (1920— 92), английский биохимик. Разработал хемиосмотическую теорию окислительного фосфорилирования, объясняющую механизм преобразования энергии в биологической мембране при синтезе аденозинтрифосфорной к-ты (АТФ) — основного аккумулятора и переносчика энергии в живых клетках. Нобелевская премия (1978).
Q-цикл П. Митчелла l МИТЧЕЛЛ Питер (1920— 92), английский биохимик. Разработал хемиосмотическую теорию окислительного фосфорилирования, объясняющую механизм преобразования энергии в биологической мембране при синтезе аденозинтрифосфорной к-ты (АТФ) — основного аккумулятора и переносчика энергии в живых клетках. Нобелевская премия (1978).
 l l Особенность Q-цикла состоит в том, что перенос Н+ через мембрану происходит в результате окисления и восстановления хинонов на самом комплексе. При этом хиноны соответственно отдают и забирают 2 Н+ из водной фазы избирательно с разных сторон мембраны. *Хиноны —полностью сопряжённые циклогексадиеноны и их аннелированные аналоги. Существуют два класса хинонов: пара-хиноны с пара — расположением карбонильных групп (1, 4 -хиноны) и орто-хиноны с орто -расположением карбонильных групп (1, 2 -хиноны). l п-бензохинон
l l Особенность Q-цикла состоит в том, что перенос Н+ через мембрану происходит в результате окисления и восстановления хинонов на самом комплексе. При этом хиноны соответственно отдают и забирают 2 Н+ из водной фазы избирательно с разных сторон мембраны. *Хиноны —полностью сопряжённые циклогексадиеноны и их аннелированные аналоги. Существуют два класса хинонов: пара-хиноны с пара — расположением карбонильных групп (1, 4 -хиноны) и орто-хиноны с орто -расположением карбонильных групп (1, 2 -хиноны). l п-бензохинон
 l Ферменты цепи переноса электронов фиксированы в митохондриальной мембране таким образом, что их действие векторно, т. е. характеризуется не только величиной скорости реакции, но и пространственной направленностью, подобно действию транспортных АТФаз.
l Ферменты цепи переноса электронов фиксированы в митохондриальной мембране таким образом, что их действие векторно, т. е. характеризуется не только величиной скорости реакции, но и пространственной направленностью, подобно действию транспортных АТФаз.
 l l Основным проявлением векторности в дыхательной цепи является перенос ионов водорода с внутренней стороны мембраны ( со стороны матрикса) на наружную (в межмембранное пространство). В дыхательной цепи есть три пункта, связанные с перекачкой протонов: комплексы I, III, IV.
l l Основным проявлением векторности в дыхательной цепи является перенос ионов водорода с внутренней стороны мембраны ( со стороны матрикса) на наружную (в межмембранное пространство). В дыхательной цепи есть три пункта, связанные с перекачкой протонов: комплексы I, III, IV.

 l Кофермент Q при участии НАДН-дегидрогеназы (комплекс I) присоединяет электроны(а также протоны) от компонентов дыхательной цепи с матриксной стороны мембраны, а освобождаются электроны и протоны на противоположной стороне мембраны, причем электроны акцептируются очередным компонентом дыхательной цепи, а протоны уходят в межмембранное пространство. Такой механизм называют Q-циклом. Сходным образом действует и цитохром-с-редуктаза( комплекс I I I). В области цитохромоксидазы (комплекс IV) в перекачке протонов возможно, участвуют ионы меди.
l Кофермент Q при участии НАДН-дегидрогеназы (комплекс I) присоединяет электроны(а также протоны) от компонентов дыхательной цепи с матриксной стороны мембраны, а освобождаются электроны и протоны на противоположной стороне мембраны, причем электроны акцептируются очередным компонентом дыхательной цепи, а протоны уходят в межмембранное пространство. Такой механизм называют Q-циклом. Сходным образом действует и цитохром-с-редуктаза( комплекс I I I). В области цитохромоксидазы (комплекс IV) в перекачке протонов возможно, участвуют ионы меди.
 l В структуре комплекса III есть два центра, или два «кармана» , в которых могут связываться хиноны. Один из них, Qout-центp, расположен между 2 Fe-28 -центром и гемом b. L вблизи внешней (out) стороны мембраны, обращенной в межмембранное пространство. В этом кармане связывается восстановленный QH 2. Другой, Qin-карман, предназначен для связывания окисленного убихинона (Q) и расположен вблизи внутренней (in) стороны мембраны, контактирующей с матриксом. Транспорт электрона в комплексе организован следующим образом. Сначала первый QH 2 связывается и окисляется в Qout-центре, освобождая при этом 2 Н+ в межмембранное пространство. При этом один е уходит на 2 Fe-2 S -центр белка и далее на цитохром с1 и цитохром с. В результате в Qout-центре остается анион-радикал — семихинон Q. В Qoutцентре Q крайне нестабилен и быстро отдает второй электрон на гем b. L и далее на гем b. H. Расположение этих гемов в комплексе перпендикулярно плоскости мембраны, в результате чего электрон пересекает мембрану в направлении к Qin-центру. В этом «кармане» уже связан окисленный Q, который принимает один е с гема b. H и восстанавливается до семихинона (Q), находящегося здесь в более стабильном состоянии. Затем все события повторяются при окислении второго QH 2.
l В структуре комплекса III есть два центра, или два «кармана» , в которых могут связываться хиноны. Один из них, Qout-центp, расположен между 2 Fe-28 -центром и гемом b. L вблизи внешней (out) стороны мембраны, обращенной в межмембранное пространство. В этом кармане связывается восстановленный QH 2. Другой, Qin-карман, предназначен для связывания окисленного убихинона (Q) и расположен вблизи внутренней (in) стороны мембраны, контактирующей с матриксом. Транспорт электрона в комплексе организован следующим образом. Сначала первый QH 2 связывается и окисляется в Qout-центре, освобождая при этом 2 Н+ в межмембранное пространство. При этом один е уходит на 2 Fe-2 S -центр белка и далее на цитохром с1 и цитохром с. В результате в Qout-центре остается анион-радикал — семихинон Q. В Qoutцентре Q крайне нестабилен и быстро отдает второй электрон на гем b. L и далее на гем b. H. Расположение этих гемов в комплексе перпендикулярно плоскости мембраны, в результате чего электрон пересекает мембрану в направлении к Qin-центру. В этом «кармане» уже связан окисленный Q, который принимает один е с гема b. H и восстанавливается до семихинона (Q), находящегося здесь в более стабильном состоянии. Затем все события повторяются при окислении второго QH 2.
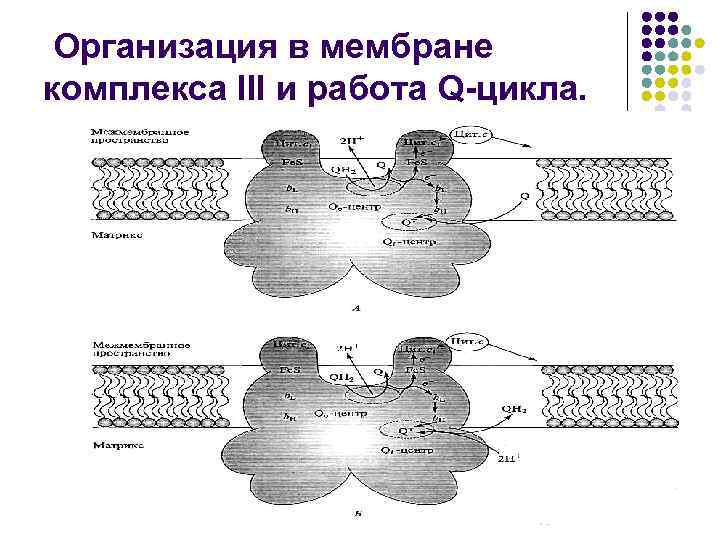 Организация в мембране комплекса III и работа Q-цикла.
Организация в мембране комплекса III и работа Q-цикла.
 l l Перенос двух электронов через каждый комплекс обеспечивает перекачку четырех протонов. Таким образом, цепь переноса электронов работает как протонный насос, перекачивая ионы водорода из матрикса на наружную сторону мембраны. В результате по сторонам мембраны возникает разность концентрации протонов и одновременно разность электрических потенциалов со знаком плюс на наружной поверхности. Иначе говоря, энергия разности окислительновосстановительных потенциалов веществ трансформируется в энергию протонного электрохимического потенциала.
l l Перенос двух электронов через каждый комплекс обеспечивает перекачку четырех протонов. Таким образом, цепь переноса электронов работает как протонный насос, перекачивая ионы водорода из матрикса на наружную сторону мембраны. В результате по сторонам мембраны возникает разность концентрации протонов и одновременно разность электрических потенциалов со знаком плюс на наружной поверхности. Иначе говоря, энергия разности окислительновосстановительных потенциалов веществ трансформируется в энергию протонного электрохимического потенциала.
 l l Электрохимический потенциал принуждает протоны двигаться в обратном направлении- с наружной поверхности внутрь. Однако мембрана непроницаема для них, за исключением участков, где располагается фермент Н+АТФ-синтетаза, катализирующий такую реакцию: АДФ+H 3 PO 4=ATФ+H 2 O
l l Электрохимический потенциал принуждает протоны двигаться в обратном направлении- с наружной поверхности внутрь. Однако мембрана непроницаема для них, за исключением участков, где располагается фермент Н+АТФ-синтетаза, катализирующий такую реакцию: АДФ+H 3 PO 4=ATФ+H 2 O
 l АТФ-синтетаза-очень крупный олигомерный белок, в котором выделяют три части: выступающую в матрикс митохондрии часть( F 1), построенную из трех пар димеров αβ; трансмембранную часть (F 0), образующую гидрофильный канал, и промежуточную область FA. субъединица F 1 содержит активные центры, синтезирующие АТФ. Протоны движутся через канал АТФ-синтетазы, и энергия этого движения используется для образования АТФ. Конкретные механизмы сопряжения(трансформации) электрохимического потенциала в энергию макроэргической связи АТФ, все еще не вполне ясны.
l АТФ-синтетаза-очень крупный олигомерный белок, в котором выделяют три части: выступающую в матрикс митохондрии часть( F 1), построенную из трех пар димеров αβ; трансмембранную часть (F 0), образующую гидрофильный канал, и промежуточную область FA. субъединица F 1 содержит активные центры, синтезирующие АТФ. Протоны движутся через канал АТФ-синтетазы, и энергия этого движения используется для образования АТФ. Конкретные механизмы сопряжения(трансформации) электрохимического потенциала в энергию макроэргической связи АТФ, все еще не вполне ясны.
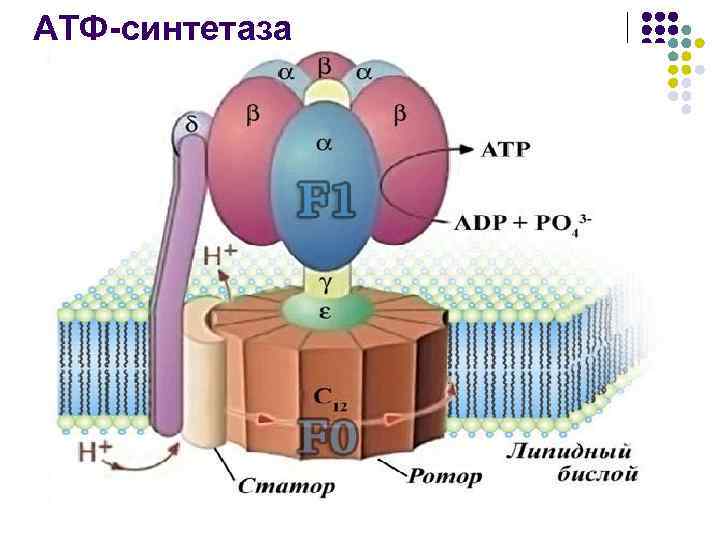 АТФ-синтетаза
АТФ-синтетаза
 l l Образующаяся АТФ при участии АДФ-АТФтранслоказы транспортируется из матрикса на наружную сторону мембраны и попадает в цитозоль. Одновременно та же транслоказа переносит АДФ в обратном направлении, из цитозоля в матрикс митохондрии. В искусственных условиях, в опытах in vitro(в пробирке) можно создать избыток АТФ со стороны внутренней поверхности внутренней мембраны. В этом случае реакция идет справа налево, т. е. фермент работает как транспортная АТФаза, переносящая протоны( H+АТФаза). Мембрана при этом энергизуется. Электрохимический потенциал возникает за счет энергии гидролиза АТФ.
l l Образующаяся АТФ при участии АДФ-АТФтранслоказы транспортируется из матрикса на наружную сторону мембраны и попадает в цитозоль. Одновременно та же транслоказа переносит АДФ в обратном направлении, из цитозоля в матрикс митохондрии. В искусственных условиях, в опытах in vitro(в пробирке) можно создать избыток АТФ со стороны внутренней поверхности внутренней мембраны. В этом случае реакция идет справа налево, т. е. фермент работает как транспортная АТФаза, переносящая протоны( H+АТФаза). Мембрана при этом энергизуется. Электрохимический потенциал возникает за счет энергии гидролиза АТФ.


