2011_inorg_medbiol_5.ppt
- Количество слайдов: 38
 Пятая лекция 1
Пятая лекция 1
 Хим. cвойства простых веществ Положение в ряду напряж. металлов …. Mg Mn Zn…H Cu Tc Re… Mn +2 HCl = Mn. Cl 2 + H 2 E 0 0 Mn + 4 HNO 3(конц)= Mn(NO 3)2 +2 NO 2 +2 H 2 O 4 Re + 4 KOH +7 O 2 = 4 KRe. O 4 +2 H 2 O (расплав) Re + 7 HNO 3(конц)= HRe. O 4 +7 NO 2 +3 H 2 O 2 Re + 7 H 2 O 2 = 2 HRe. O 4 +6 H 2 O 2
Хим. cвойства простых веществ Положение в ряду напряж. металлов …. Mg Mn Zn…H Cu Tc Re… Mn +2 HCl = Mn. Cl 2 + H 2 E 0 0 Mn + 4 HNO 3(конц)= Mn(NO 3)2 +2 NO 2 +2 H 2 O 4 Re + 4 KOH +7 O 2 = 4 KRe. O 4 +2 H 2 O (расплав) Re + 7 HNO 3(конц)= HRe. O 4 +7 NO 2 +3 H 2 O 2 Re + 7 H 2 O 2 = 2 HRe. O 4 +6 H 2 O 2
 Реакции при нагревании 3 Mn + 2 O 2 = Mn 3 O 4 (Mn. III 2 O 4) 3 Mn + N 2 = Mn 3 N 2 (1200 o. C) Mn + Cl 2 = Mn. Cl 2 Mn + F 2 = Mn. F 2 (и Mn. F 3) 4 Re + 7 O 2 = 2 Re 2 O 7 (летучий оксид) 2 Re + 5 Cl 2 = 2 Re. Cl 5 Re + 2 S = Re. S 2 3
Реакции при нагревании 3 Mn + 2 O 2 = Mn 3 O 4 (Mn. III 2 O 4) 3 Mn + N 2 = Mn 3 N 2 (1200 o. C) Mn + Cl 2 = Mn. Cl 2 Mn + F 2 = Mn. F 2 (и Mn. F 3) 4 Re + 7 O 2 = 2 Re 2 O 7 (летучий оксид) 2 Re + 5 Cl 2 = 2 Re. Cl 5 Re + 2 S = Re. S 2 3
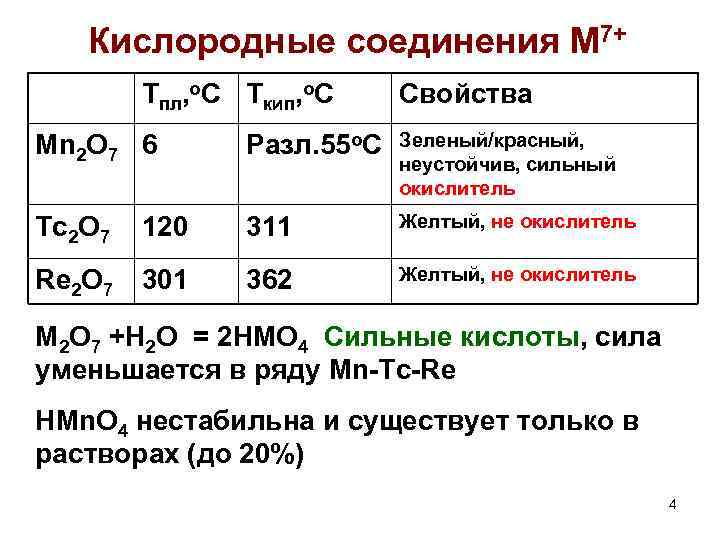 Кислородные соединения M 7+ Тпл, о. С Ткип, о. С Свойства Mn 2 O 7 6 Разл. 55 о. С Зеленый/красный, неустойчив, сильный окислитель Tc 2 O 7 120 311 Желтый, не окислитель Re 2 O 7 301 362 Желтый, не окислитель M 2 О 7 +Н 2 О = 2 НMО 4 Сильные кислоты, сила уменьшается в ряду Mn-Tc-Re HMn. O 4 нестабильна и существует только в растворах (до 20%) 4
Кислородные соединения M 7+ Тпл, о. С Ткип, о. С Свойства Mn 2 O 7 6 Разл. 55 о. С Зеленый/красный, неустойчив, сильный окислитель Tc 2 O 7 120 311 Желтый, не окислитель Re 2 O 7 301 362 Желтый, не окислитель M 2 О 7 +Н 2 О = 2 НMО 4 Сильные кислоты, сила уменьшается в ряду Mn-Tc-Re HMn. O 4 нестабильна и существует только в растворах (до 20%) 4
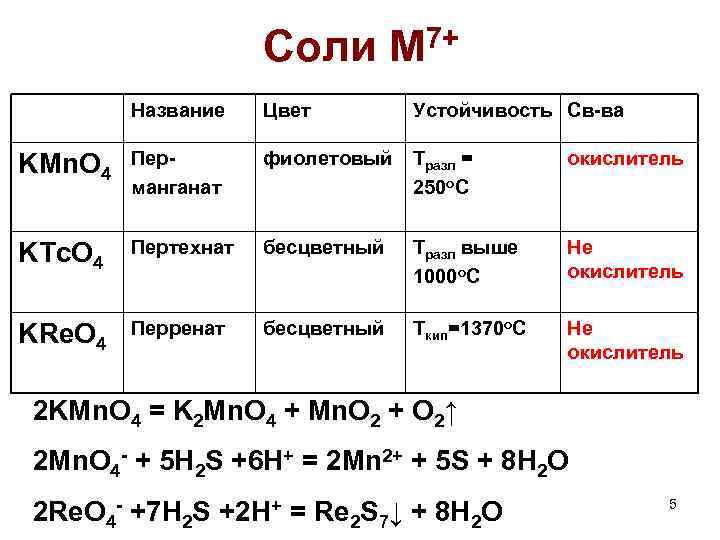 Соли M 7+ Название Цвет Устойчивость Св-ва KMn. O 4 Перманганат фиолетовый Тразл = 250 о. С окислитель KTc. O 4 Пертехнат бесцветный Тразл выше 1000 о. С Не окислитель KRe. O 4 Перренат бесцветный Ткип=1370 о. С Не окислитель 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2↑ 2 Mn. O 4 - + 5 H 2 S +6 H+ = 2 Mn 2+ + 5 S + 8 H 2 O 2 Re. O 4 - +7 H 2 S +2 H+ = Re 2 S 7↓ + 8 H 2 O 5
Соли M 7+ Название Цвет Устойчивость Св-ва KMn. O 4 Перманганат фиолетовый Тразл = 250 о. С окислитель KTc. O 4 Пертехнат бесцветный Тразл выше 1000 о. С Не окислитель KRe. O 4 Перренат бесцветный Ткип=1370 о. С Не окислитель 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2↑ 2 Mn. O 4 - + 5 H 2 S +6 H+ = 2 Mn 2+ + 5 S + 8 H 2 O 2 Re. O 4 - +7 H 2 S +2 H+ = Re 2 S 7↓ + 8 H 2 O 5
 KMn. O 4 как окислитель Среда p. H<7 p. H>>7 Продукт восстановления Mn 2+ Mn. O 2↓ Mn. O 42 - Цвет бесцветный бурый зеленый Конпропорционирование 3 Mn. SO 4 +2 KMn. O 4 + 2 H 2 O = 5 Mn. O 2 ↓ +K 2 SO 4 +2 H 2 SO 4 6
KMn. O 4 как окислитель Среда p. H<7 p. H>>7 Продукт восстановления Mn 2+ Mn. O 2↓ Mn. O 42 - Цвет бесцветный бурый зеленый Конпропорционирование 3 Mn. SO 4 +2 KMn. O 4 + 2 H 2 O = 5 Mn. O 2 ↓ +K 2 SO 4 +2 H 2 SO 4 6
 Получение KMn. O 4 Две стадии: 1) Щелочное плавление пиролюзита: 3 Mn. O 2 + KCl. O 3 + 6 KOH = 3 K 2 Mn. O 4 + KCl + 3 H 2 O 2) Окисление до перманганата : Cl 2, O 3, Pb. O 2, (NH 4)2 S 2 O 8, KBi. O 3, Xe. F 4 Экономично электрохимическое окисление: КАТОД: 2 H 2 O + 2 e = H 2 + 2 OHАНОД: Mn. O 4 2 - - e = Mn. O 4 2 K 2 Mn. O 4 + 2 H 2 O = 2 KMn. O 4 +2 KOH +H 2↑ 7 (формально)
Получение KMn. O 4 Две стадии: 1) Щелочное плавление пиролюзита: 3 Mn. O 2 + KCl. O 3 + 6 KOH = 3 K 2 Mn. O 4 + KCl + 3 H 2 O 2) Окисление до перманганата : Cl 2, O 3, Pb. O 2, (NH 4)2 S 2 O 8, KBi. O 3, Xe. F 4 Экономично электрохимическое окисление: КАТОД: 2 H 2 O + 2 e = H 2 + 2 OHАНОД: Mn. O 4 2 - - e = Mn. O 4 2 K 2 Mn. O 4 + 2 H 2 O = 2 KMn. O 4 +2 KOH +H 2↑ 7 (формально)
 Кислородные соединения Mn 6+ Mn. O 3 и H 2 Mn. O 4 – не известны Соли – манганаты (зеленый цвет) Манганаты склонны диспропорционировать, особенно в кислой среде 3 Mn. O 42 - + 4 H+ = 2 Mn. O 4 - + Mn. O 2↓ + 2 H 2 O (пропускание CO 2) 8
Кислородные соединения Mn 6+ Mn. O 3 и H 2 Mn. O 4 – не известны Соли – манганаты (зеленый цвет) Манганаты склонны диспропорционировать, особенно в кислой среде 3 Mn. O 42 - + 4 H+ = 2 Mn. O 4 - + Mn. O 2↓ + 2 H 2 O (пропускание CO 2) 8
 Кислородные соединения Mn 6+ Манганаты – сильные окислители, особенно в кислой среде, где восстанавливаются до Mn 2+; в щелочной среде восстанавливаются до Mn. O 2 Окисление органики 6 K 2 Mn. O 4 +C 2 H 5 OH +H 2 O = 6 Mn. O 2↓+ 2 K 2 CO 3 +8 KOH В зависимости от условий этанол можно окислить до альдегида или кислоты 9
Кислородные соединения Mn 6+ Манганаты – сильные окислители, особенно в кислой среде, где восстанавливаются до Mn 2+; в щелочной среде восстанавливаются до Mn. O 2 Окисление органики 6 K 2 Mn. O 4 +C 2 H 5 OH +H 2 O = 6 Mn. O 2↓+ 2 K 2 CO 3 +8 KOH В зависимости от условий этанол можно окислить до альдегида или кислоты 9
 Кислородные соединения Mn 4+ Mn. O 2 – важнейшее соединение Свойства окислителя (при нагревании): Mn. O 2 + 4 HClконц = Mn. Cl 2 + Cl 2↑ + 2 H 2 O 2 Mn. O 2 + 2 H 2 SO 4 = 2 Mn. SO 4 +O 2↑ +2 H 2 O Окисление до манганатов: (сплавление) 3 Mn. O 2 + KCl. O 3 + 3 K 2 CO 3 = 3 K 2 Mn. O 4 + KCl +3 CO 2 (KNO 3) 10
Кислородные соединения Mn 4+ Mn. O 2 – важнейшее соединение Свойства окислителя (при нагревании): Mn. O 2 + 4 HClконц = Mn. Cl 2 + Cl 2↑ + 2 H 2 O 2 Mn. O 2 + 2 H 2 SO 4 = 2 Mn. SO 4 +O 2↑ +2 H 2 O Окисление до манганатов: (сплавление) 3 Mn. O 2 + KCl. O 3 + 3 K 2 CO 3 = 3 K 2 Mn. O 4 + KCl +3 CO 2 (KNO 3) 10
 Кислородные соединения Mn 4+ Слабовыраженные амфотерные свойства Mn. O 2 + 4 HF = Mn. F 4 + 2 H 2 O Mn. O 2 + Ca. O = Ca. Mn. O 3 (метаманганат (IV)) Ca. Mn. O 3 + Ca. O = Ca 2 Mn. O 4 (ортоманганат (IV)) 11
Кислородные соединения Mn 4+ Слабовыраженные амфотерные свойства Mn. O 2 + 4 HF = Mn. F 4 + 2 H 2 O Mn. O 2 + Ca. O = Ca. Mn. O 3 (метаманганат (IV)) Ca. Mn. O 3 + Ca. O = Ca 2 Mn. O 4 (ортоманганат (IV)) 11
 Кислородные соединения Mn 2+ Mn. O – серо-зеленый, не растворим в воде Mn. CO 3 = Mn. O + CO 2 (при нагревании) Встречается в природе в виде минерала (розовые кристаллы) родохрозита (марганцевый шпат). Mn. Cl 2 + 2 Na. OH = Mn(OH)2↓ + 2 Na. Cl Mn(OH)2 – белый, окисляется на воздухе, легко растворим в кислотах, растворим в крепких щелочах Mn(OH)2 + H 2 SO 4 = Mn. SO 4 + 2 H 2 O Mn(OH)2 + KOH = K[Mn(OH)3] 12
Кислородные соединения Mn 2+ Mn. O – серо-зеленый, не растворим в воде Mn. CO 3 = Mn. O + CO 2 (при нагревании) Встречается в природе в виде минерала (розовые кристаллы) родохрозита (марганцевый шпат). Mn. Cl 2 + 2 Na. OH = Mn(OH)2↓ + 2 Na. Cl Mn(OH)2 – белый, окисляется на воздухе, легко растворим в кислотах, растворим в крепких щелочах Mn(OH)2 + H 2 SO 4 = Mn. SO 4 + 2 H 2 O Mn(OH)2 + KOH = K[Mn(OH)3] 12
 Соли Mn 2+ Водорастворимые соли: Mn. Cl 2. 4 H 2 O, Mn. SO 4. 5 H 2 O, Mn(NO 3)2. 6 H 2 O – в водных р-рах [Mn(H 2 O)6]2+ Не растворимые соли: Mn. CO 3, Mn. S, Mn. C 2 O 4 Mn. Cl 2 + (NH 4)2 S = Mn. S↓ + 2 NH 4 Cl Mn. S – темный, при стоянии зеленый ПРMn. S= 10 -10, поэтому не осаждается H 2 S, легко растворим в кислотах 13
Соли Mn 2+ Водорастворимые соли: Mn. Cl 2. 4 H 2 O, Mn. SO 4. 5 H 2 O, Mn(NO 3)2. 6 H 2 O – в водных р-рах [Mn(H 2 O)6]2+ Не растворимые соли: Mn. CO 3, Mn. S, Mn. C 2 O 4 Mn. Cl 2 + (NH 4)2 S = Mn. S↓ + 2 NH 4 Cl Mn. S – темный, при стоянии зеленый ПРMn. S= 10 -10, поэтому не осаждается H 2 S, легко растворим в кислотах 13
 VI группа периодической системы
VI группа периодической системы
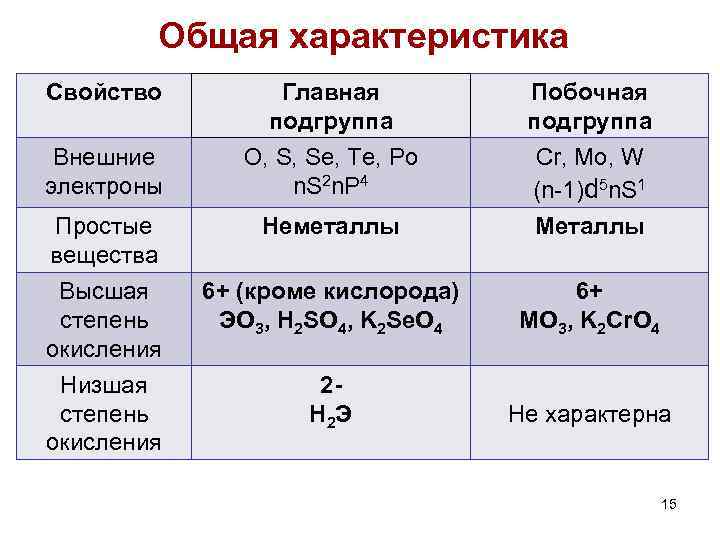 Общая характеристика Свойство Главная подгруппа O, S, Se, Te, Po n. S 2 n. P 4 Побочная подгруппа Cr, Mo, W (n-1)d 5 n. S 1 Простые вещества Неметаллы Металлы Высшая степень окисления Низшая степень окисления 6+ (кроме кислорода) ЭО 3, H 2 SO 4, K 2 Se. O 4 6+ MО 3, K 2 Cr. O 4 2 Н 2 Э Не характерна Внешние электроны 15
Общая характеристика Свойство Главная подгруппа O, S, Se, Te, Po n. S 2 n. P 4 Побочная подгруппа Cr, Mo, W (n-1)d 5 n. S 1 Простые вещества Неметаллы Металлы Высшая степень окисления Низшая степень окисления 6+ (кроме кислорода) ЭО 3, H 2 SO 4, K 2 Se. O 4 6+ MО 3, K 2 Cr. O 4 2 Н 2 Э Не характерна Внешние электроны 15
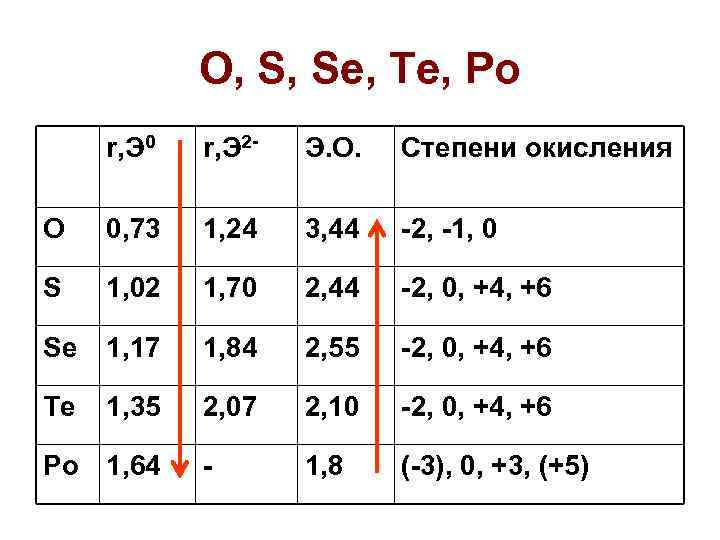 O, S, Se, Te, Po r, Э 0 r, Э 2 - Э. О. Степени окисления O 0, 73 1, 24 3, 44 -2, -1, 0 S 1, 02 1, 70 2, 44 -2, 0, +4, +6 Se 1, 17 1, 84 2, 55 -2, 0, +4, +6 Te 1, 35 2, 07 2, 10 -2, 0, +4, +6 - 1, 8 (-3), 0, +3, (+5) Po 1, 64
O, S, Se, Te, Po r, Э 0 r, Э 2 - Э. О. Степени окисления O 0, 73 1, 24 3, 44 -2, -1, 0 S 1, 02 1, 70 2, 44 -2, 0, +4, +6 Se 1, 17 1, 84 2, 55 -2, 0, +4, +6 Te 1, 35 2, 07 2, 10 -2, 0, +4, +6 - 1, 8 (-3), 0, +3, (+5) Po 1, 64
 Содержание в земной коре и минералы O – 1 место S – 14 место; самородная сера, Fe. S 2 (пирит) рисунок, Ca. SO 4. 2 H 2 O (гипс) и др. Se – 62 место, рассеянный; сопутствует сульфидам Te – 79 место, рассеянный; сопутствует сульфидам Po – радиоактивен, 210 Po (T 1/2 = 138 дней)
Содержание в земной коре и минералы O – 1 место S – 14 место; самородная сера, Fe. S 2 (пирит) рисунок, Ca. SO 4. 2 H 2 O (гипс) и др. Se – 62 место, рассеянный; сопутствует сульфидам Te – 79 место, рассеянный; сопутствует сульфидам Po – радиоактивен, 210 Po (T 1/2 = 138 дней)
 Открытие элементов O – 1774 г. , англ. Пристли, 1772 г. , швед Шееле, 1775 г. , француз Лавуазье; от греч. «рождающий кислоты» S – известна с очень давно Se – 1817 г. , швед Берцелиус, от греч. «Селена» - Луна Te – 1798 г. , немец Клапрот, от греч. «Теллус» - Земля Po – 1898 г. , Склодовская-Кюри и Кюри, «Полония» - Польша
Открытие элементов O – 1774 г. , англ. Пристли, 1772 г. , швед Шееле, 1775 г. , француз Лавуазье; от греч. «рождающий кислоты» S – известна с очень давно Se – 1817 г. , швед Берцелиус, от греч. «Селена» - Луна Te – 1798 г. , немец Клапрот, от греч. «Теллус» - Земля Po – 1898 г. , Склодовская-Кюри и Кюри, «Полония» - Польша
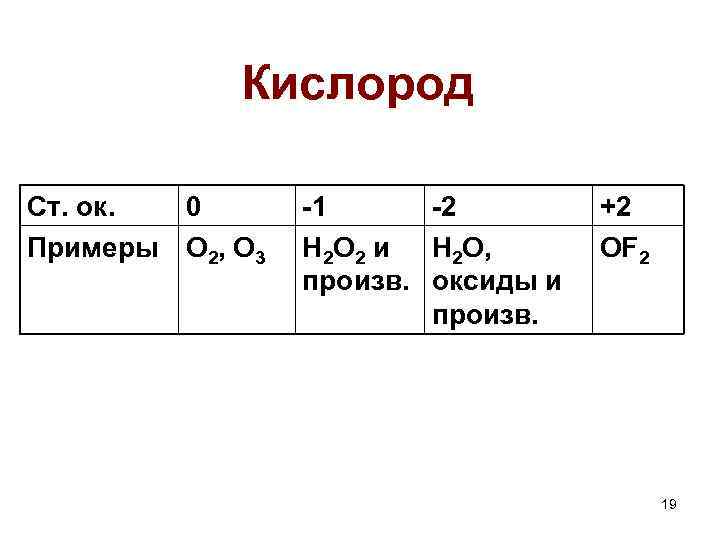 Кислород Ст. ок. 0 Примеры O 2, O 3 -1 -2 H 2 O 2 и H 2 O, произв. оксиды и произв. +2 OF 2 19
Кислород Ст. ок. 0 Примеры O 2, O 3 -1 -2 H 2 O 2 и H 2 O, произв. оксиды и произв. +2 OF 2 19
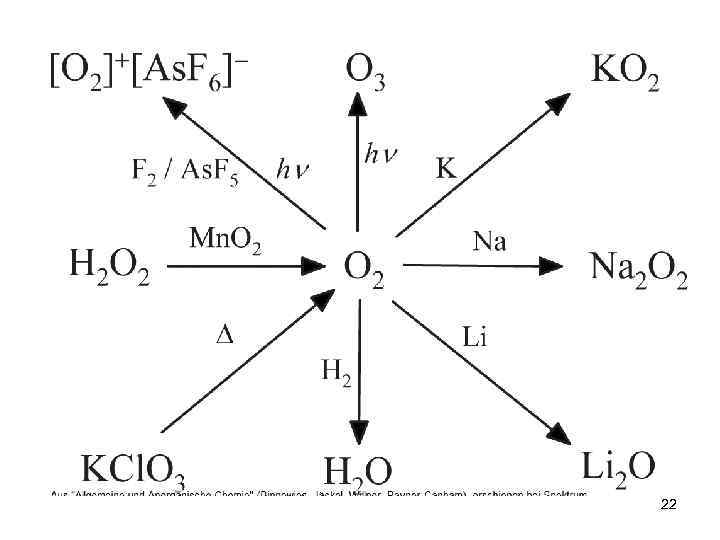
 Аллотропные модификации О O 2 – б/ц газ, Ткип = - 183 о. С, голубая жидкость О 3 – озон, синий газ, Ткип = - 112 о. С, f. G 0 = + 163 к. Дж/моль, взрывоопасен, очень реакционноспособный Ag + O 2 = нет реакции 2 Ag + O 3 = Ag 2 O + O 2 20
Аллотропные модификации О O 2 – б/ц газ, Ткип = - 183 о. С, голубая жидкость О 3 – озон, синий газ, Ткип = - 112 о. С, f. G 0 = + 163 к. Дж/моль, взрывоопасен, очень реакционноспособный Ag + O 2 = нет реакции 2 Ag + O 3 = Ag 2 O + O 2 20
 Получение О 2 В природе: воздух, вода, оксидные минералы. ПОЛУЧЕНИЕ: • В промышленности: 1) фракционная перегонка жидкого воздуха 2) электролиз воды • В лаборатории: 2 KMn. O 4 тв = K 2 Mn. O 4 + Mn. O 2 + O 2 KCl. O 3 тв = KCl + 3/2 O 2 KNO 3 тв = KNO 2 + 1/2 O 2 21
Получение О 2 В природе: воздух, вода, оксидные минералы. ПОЛУЧЕНИЕ: • В промышленности: 1) фракционная перегонка жидкого воздуха 2) электролиз воды • В лаборатории: 2 KMn. O 4 тв = K 2 Mn. O 4 + Mn. O 2 + O 2 KCl. O 3 тв = KCl + 3/2 O 2 KNO 3 тв = KNO 2 + 1/2 O 2 21
 22
22
 Пероксиды, надпероксиды, озониды 2 Na + O 2 = Na 2 O 2 (пероксид) Na + O 2 (300 атм) = Na. O 2 (надпероксид) M + O 3 = MO 3 (озонид) M = Na, K, Rb, Cs 2 MOH + 2 O 3 = 2 MO 3 + H 2 O + 1/2 O 2 Регенерация «воздуха» 4 KO 2 тв + 2 CO 2 газ = 2 K 2 CO 3 + 3 O 2 M 2 O 2 +2 H 2 O = 2 MOH + H 2 O 2 2 MO 2 + 2 H 2 O = 2 MOH + H 2 O 2 + O 2 2 MO 3 + 2 H 2 O = 2 MOH + H 2 O 2 + 2 O 2 23
Пероксиды, надпероксиды, озониды 2 Na + O 2 = Na 2 O 2 (пероксид) Na + O 2 (300 атм) = Na. O 2 (надпероксид) M + O 3 = MO 3 (озонид) M = Na, K, Rb, Cs 2 MOH + 2 O 3 = 2 MO 3 + H 2 O + 1/2 O 2 Регенерация «воздуха» 4 KO 2 тв + 2 CO 2 газ = 2 K 2 CO 3 + 3 O 2 M 2 O 2 +2 H 2 O = 2 MOH + H 2 O 2 2 MO 2 + 2 H 2 O = 2 MOH + H 2 O 2 + O 2 2 MO 3 + 2 H 2 O = 2 MOH + H 2 O 2 + 2 O 2 23
 Перекись водорода H 2 O 2 Б/ц вязкая жидкость, взрывает, продажный препарат 30% водный раствор Ba. O 2 + H 2 SO 4 разб!!! = Ba. SO 4↓ + H 2 O 2 Электролиз 50% H 2 SO 4: Анод : 2 HSO 4 - -2 e = H 2 S 2 O 8 + H 2 O = H 2 SO 4 + H 2 SO 5 (быстро) H 2 SO 5 + H 2 O = H 2 SO 4 + H 2 O 2 (медленно) Очень слабая кислота (но более сильная, чем вода): Ka 1 = 1, 5. 10 -12 Na 2 O 2 + 2 H 2 O = 2 Na. OH + H 2 O 2 24
Перекись водорода H 2 O 2 Б/ц вязкая жидкость, взрывает, продажный препарат 30% водный раствор Ba. O 2 + H 2 SO 4 разб!!! = Ba. SO 4↓ + H 2 O 2 Электролиз 50% H 2 SO 4: Анод : 2 HSO 4 - -2 e = H 2 S 2 O 8 + H 2 O = H 2 SO 4 + H 2 SO 5 (быстро) H 2 SO 5 + H 2 O = H 2 SO 4 + H 2 O 2 (медленно) Очень слабая кислота (но более сильная, чем вода): Ka 1 = 1, 5. 10 -12 Na 2 O 2 + 2 H 2 O = 2 Na. OH + H 2 O 2 24
 Перекись водорода H 2 O 2 • Окислительные свойства H 2 O 2 + 2 J- + 2 H+ = J 2 + 2 H 2 O 2 + Mn(OH)2 = Mn. O 2↓ + 2 H 2 O • Восстановительные свщйства 5 H 2 O 2 + 2 Mn. O 4 - + 6 H+ =2 Mn 2+ + 5 O 2 +8 H 2 O • Диспропорционирование 2 H 2 O 2 = 2 H 2 O + O 2 (Т, Mn. O 2, Fe 2+/Fe 3+, щелочи) 25
Перекись водорода H 2 O 2 • Окислительные свойства H 2 O 2 + 2 J- + 2 H+ = J 2 + 2 H 2 O 2 + Mn(OH)2 = Mn. O 2↓ + 2 H 2 O • Восстановительные свщйства 5 H 2 O 2 + 2 Mn. O 4 - + 6 H+ =2 Mn 2+ + 5 O 2 +8 H 2 O • Диспропорционирование 2 H 2 O 2 = 2 H 2 O + O 2 (Т, Mn. O 2, Fe 2+/Fe 3+, щелочи) 25
 ПОДГРУППА СЕРЫ 26
ПОДГРУППА СЕРЫ 26
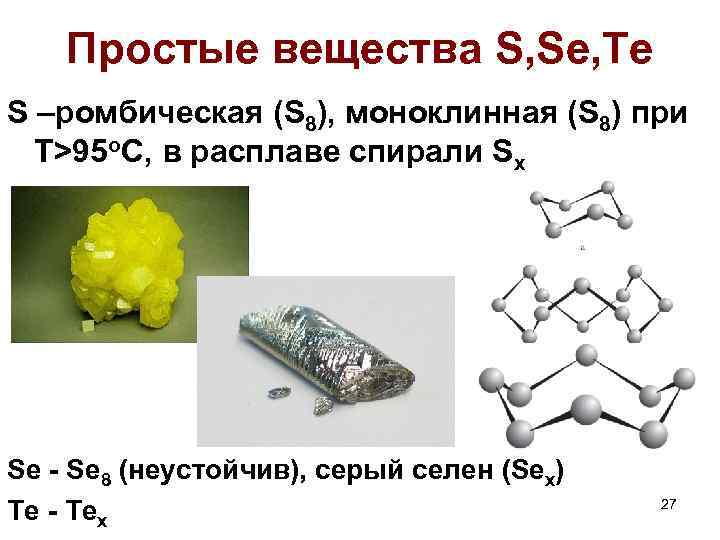 Простые вещества S, Se, Te S –ромбическая (S 8), моноклинная (S 8) при T>95 o. C, в расплаве спирали Sx Se - Se 8 (неустойчив), серый селен (Sex) Te - Tex 27
Простые вещества S, Se, Te S –ромбическая (S 8), моноклинная (S 8) при T>95 o. C, в расплаве спирали Sx Se - Se 8 (неустойчив), серый селен (Sex) Te - Tex 27
 Свойства S, Se, Te • Восстановительные Э +О 2 = ЭО 2 (Э = S, Se, Te) • Окислительные 3 Э + 2 Al = Al 2 Э 3 (Э = S, Se, Te) • Диспропорционирование 3 S + 6 Na. OH = 2 Na 2 S + Na 2 SO 3 + 3 H 2 O (кипячение), 3 S + 6 OH- = 2 S 2 - + SO 32 - +3 H 2 O E 0 = + 0, 13 B Se и Te не реагируют со щелочами ( E 0<0) 28
Свойства S, Se, Te • Восстановительные Э +О 2 = ЭО 2 (Э = S, Se, Te) • Окислительные 3 Э + 2 Al = Al 2 Э 3 (Э = S, Se, Te) • Диспропорционирование 3 S + 6 Na. OH = 2 Na 2 S + Na 2 SO 3 + 3 H 2 O (кипячение), 3 S + 6 OH- = 2 S 2 - + SO 32 - +3 H 2 O E 0 = + 0, 13 B Se и Te не реагируют со щелочами ( E 0<0) 28
 Реакции с кислотами • Кислоты не окислители Э + HCl = нет реакции (Э = S, Se, Te) • Кислоты окислители S + 6 HNO 3 конц = H 2 SO 4 + 6 NO 2 + 2 H 2 O Se – H 2 Se. O 3 Te – Te. O 2 29
Реакции с кислотами • Кислоты не окислители Э + HCl = нет реакции (Э = S, Se, Te) • Кислоты окислители S + 6 HNO 3 конц = H 2 SO 4 + 6 NO 2 + 2 H 2 O Se – H 2 Se. O 3 Te – Te. O 2 29
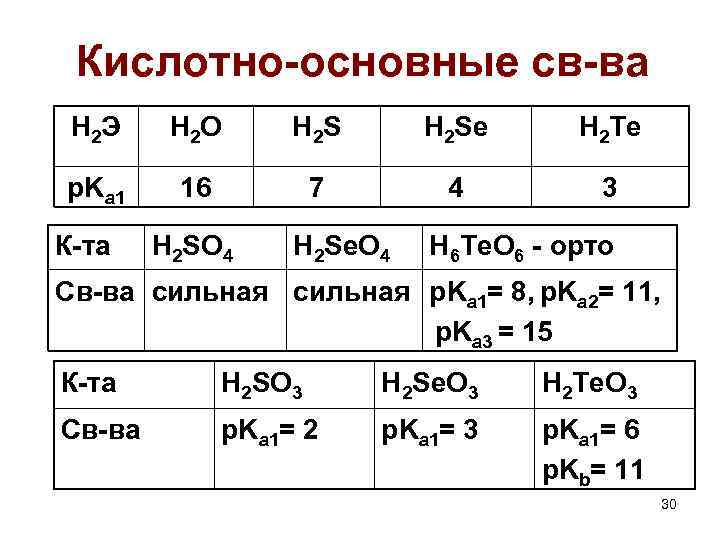 Кислотно-основные св-ва H 2 Э H 2 O H 2 Se H 2 Te p. Ka 1 16 7 4 3 К-та H 2 SO 4 H 2 Se. O 4 H 6 Te. O 6 - орто Св-ва сильная p. Ka 1= 8, p. Ka 2= 11, p. Ka 3 = 15 К-та H 2 SO 3 H 2 Se. O 3 H 2 Te. O 3 Св-ва p. Ka 1= 2 p. Ka 1= 3 p. Ka 1= 6 p. Kb= 11 30
Кислотно-основные св-ва H 2 Э H 2 O H 2 Se H 2 Te p. Ka 1 16 7 4 3 К-та H 2 SO 4 H 2 Se. O 4 H 6 Te. O 6 - орто Св-ва сильная p. Ka 1= 8, p. Ka 2= 11, p. Ka 3 = 15 К-та H 2 SO 3 H 2 Se. O 3 H 2 Te. O 3 Св-ва p. Ka 1= 2 p. Ka 1= 3 p. Ka 1= 6 p. Kb= 11 30
 H 2 S 31
H 2 S 31
 H 2 S Получение: H 2 + S = H 2 S (300 o. C) (промышленное) Al 2 S 3 тв +6 H 2 O = 2 Al(OH)3 + 3 H 2 S (лаб. ) Fe. Sтв + 2 H+ = Fe 2+ + H 2 S (лаб. ) Горение: 2 H 2 S + O 2 недостаток = 2 S + 2 H 2 O 2 H 2 S + 3 O 2 избыток = 2 SO 2 + 2 H 2 O 32
H 2 S Получение: H 2 + S = H 2 S (300 o. C) (промышленное) Al 2 S 3 тв +6 H 2 O = 2 Al(OH)3 + 3 H 2 S (лаб. ) Fe. Sтв + 2 H+ = Fe 2+ + H 2 S (лаб. ) Горение: 2 H 2 S + O 2 недостаток = 2 S + 2 H 2 O 2 H 2 S + 3 O 2 избыток = 2 SO 2 + 2 H 2 O 32
 H 2 S Окисление сероводорода в водных растворах: 1) до S: Mn. O 4 -, Cr 2 O 72 -, Fe 3+ 2) до SO 42 -: HNO 3 конц, Pb. O 2, Bi. O 33 -, Fe. O 42 Растворимые соли гидролизуются, в случае слабых оснований полностью Al 2 S 3, Cr 2 S 3 Нерастворимые сульфиды часто окрашены: Cd. S желтый, Sb 2 S 3 оранжевый, Pb. S черный, Zn. S белый, Cu. S черный. 33
H 2 S Окисление сероводорода в водных растворах: 1) до S: Mn. O 4 -, Cr 2 O 72 -, Fe 3+ 2) до SO 42 -: HNO 3 конц, Pb. O 2, Bi. O 33 -, Fe. O 42 Растворимые соли гидролизуются, в случае слабых оснований полностью Al 2 S 3, Cr 2 S 3 Нерастворимые сульфиды часто окрашены: Cd. S желтый, Sb 2 S 3 оранжевый, Pb. S черный, Zn. S белый, Cu. S черный. 33
 Полисульфиды Na 2 Sконц +(x-1)S = Na 2 Sx (получение) Na 2 Sx = 2 Na+ + Sx 2 - (диссоциация) Сульфаны Na 2 Sx + 2 HCl = H 2 Sx (получение) H 2 Sx - известны только для серы, Х=2 -6 выделены, Х=6 -9 в смесях. Более сильные кислоты, чем H 2 S 2: p. Ka 1 = 4; H 2 О 2: p. Ka 1 = 12 H 2 S: p. Ka 1 = 7; H 2 О: p. Ka 1 = 16 34
Полисульфиды Na 2 Sконц +(x-1)S = Na 2 Sx (получение) Na 2 Sx = 2 Na+ + Sx 2 - (диссоциация) Сульфаны Na 2 Sx + 2 HCl = H 2 Sx (получение) H 2 Sx - известны только для серы, Х=2 -6 выделены, Х=6 -9 в смесях. Более сильные кислоты, чем H 2 S 2: p. Ka 1 = 4; H 2 О 2: p. Ka 1 = 12 H 2 S: p. Ka 1 = 7; H 2 О: p. Ka 1 = 16 34
 SO 2 Tкип= -10 o. C, хорошо растворим в воде (10%) Получение. В промышленности – обжиг сульфидов: Zn. S + 3/2 O 2 = Zn. O + SO 2 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 (90% производства) В лаборатории: Na 2 SO 3 + 2 HCl = 2 Na. Cl + SO 2 + H 2 O Cu + 2 H 2 SO 4 конц = Cu. SO 4 + SO 2 + 2 H 2 O 35
SO 2 Tкип= -10 o. C, хорошо растворим в воде (10%) Получение. В промышленности – обжиг сульфидов: Zn. S + 3/2 O 2 = Zn. O + SO 2 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 (90% производства) В лаборатории: Na 2 SO 3 + 2 HCl = 2 Na. Cl + SO 2 + H 2 O Cu + 2 H 2 SO 4 конц = Cu. SO 4 + SO 2 + 2 H 2 O 35
 Кислородные соединения S 4+ Равновесия в воде: SO 2 газ + x. H 2 O = SO 2. x. H 2 O K 1 SO 2. x. H 2 O = H 2 SO 3 + (x-1)H 2 O K<<1 p. Ka 1 = 2; p. Ka 2 = 6 Взаимодействие со щелочью: 2 Na. OH + SO 2 = Na 2 SO 3 + H 2 O сульфит Na. OH + SO 2 = Na. HSO 3 гидросульфит, существует только в растворе 36
Кислородные соединения S 4+ Равновесия в воде: SO 2 газ + x. H 2 O = SO 2. x. H 2 O K 1 SO 2. x. H 2 O = H 2 SO 3 + (x-1)H 2 O K<<1 p. Ka 1 = 2; p. Ka 2 = 6 Взаимодействие со щелочью: 2 Na. OH + SO 2 = Na 2 SO 3 + H 2 O сульфит Na. OH + SO 2 = Na. HSO 3 гидросульфит, существует только в растворе 36
 Кислородные соединения S 4+ При упаривании раствора получают 2 Na. HSO 3 = Na 2 S 2 O 5 + H 2 O пиросульфит Кислота H 2 S 2 O 5 не известна Гидролиз сульфитов(p. H >7): SO 32 - + H 2 O = HSO 3 - + OH- Kh 10 -8 Гидролиз гидросульфитов(p. H <7): HSO 3 - + H 2 O = H 2 SO 3 + ОН- Kh 10 -12 HSO 3 - = SO 32 - + H+ Ka 2 10 -6 37
Кислородные соединения S 4+ При упаривании раствора получают 2 Na. HSO 3 = Na 2 S 2 O 5 + H 2 O пиросульфит Кислота H 2 S 2 O 5 не известна Гидролиз сульфитов(p. H >7): SO 32 - + H 2 O = HSO 3 - + OH- Kh 10 -8 Гидролиз гидросульфитов(p. H <7): HSO 3 - + H 2 O = H 2 SO 3 + ОН- Kh 10 -12 HSO 3 - = SO 32 - + H+ Ka 2 10 -6 37
 Кислородные соединения S 4+ • Диспропорционирование 4 SO 32 - = S 2 - + 3 SO 42 - (при нагревании) • Окисление (S 4+ S 6+) SO 2 + 1/2 O 2 = SO 3 (для синтеза H 2 SO 4) Na 2 SO 3 + 1/2 O 2 = Na 2 SO 4 (медленно) SO 2 + ОКИСЛИТЕЛЬ + H+ = SO 42(Mn. O 4 -, Cr 2 O 7 -, Cl. O 3 -, Cl 2, Br 2, I 2, H 2 O 2) • Восстановление SO 2 + 2 H 2 S = 3 S + 2 H 2 O 38
Кислородные соединения S 4+ • Диспропорционирование 4 SO 32 - = S 2 - + 3 SO 42 - (при нагревании) • Окисление (S 4+ S 6+) SO 2 + 1/2 O 2 = SO 3 (для синтеза H 2 SO 4) Na 2 SO 3 + 1/2 O 2 = Na 2 SO 4 (медленно) SO 2 + ОКИСЛИТЕЛЬ + H+ = SO 42(Mn. O 4 -, Cr 2 O 7 -, Cl. O 3 -, Cl 2, Br 2, I 2, H 2 O 2) • Восстановление SO 2 + 2 H 2 S = 3 S + 2 H 2 O 38


