Химия - Термодинамика и Кинетика.ppt
- Количество слайдов: 43

ПСПб. ГМУ им. акад. И. П. Павлова кафедра общей и биоорганической химии дисцисплина «ХИМИЯ» 12 лекций Равновесия в водных растворах

Рейтинговая система оценки усвоения курса «Химия» студентами 1 курса лечебного и педиатрического факультетов 2014 -2015 у. г. • Минимум за семестр - 36 баллов: • Контрольные тесты – 12 баллов • Лабораторные работы – 6 баллов • Практические занятия – 3 балла • Самостоятельная работа – 15 баллов • Экзамен – от 25 до 40 баллов • Итог – от 61 до 100 баллов

Лекция № 1 Основы химической термодинамики и кинетики химических реакций

Понятие о химической термодинамике • Термодинамика – наука, изучающая взаимные превращения различных видов энергии • Химическая термодинамика – это раздел физической химии, изучающий превращения различных видов энергии в химических процессах

Биоэнергетика изучает превращение энергии в биосистемах Энергия окисления пищевых продуктов, идет на поддержание температуры тела и совершение различных видов биологической работы Переход энергии в биосистеме в теплоту и работу осуществляется через образование промежуточных продуктов. Калорийность – энергия, выделяемая при полном окислении 1 г питательных веществ
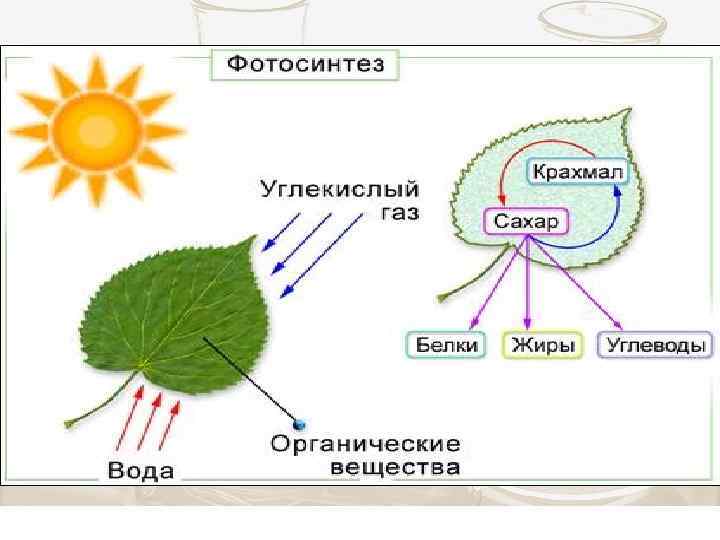
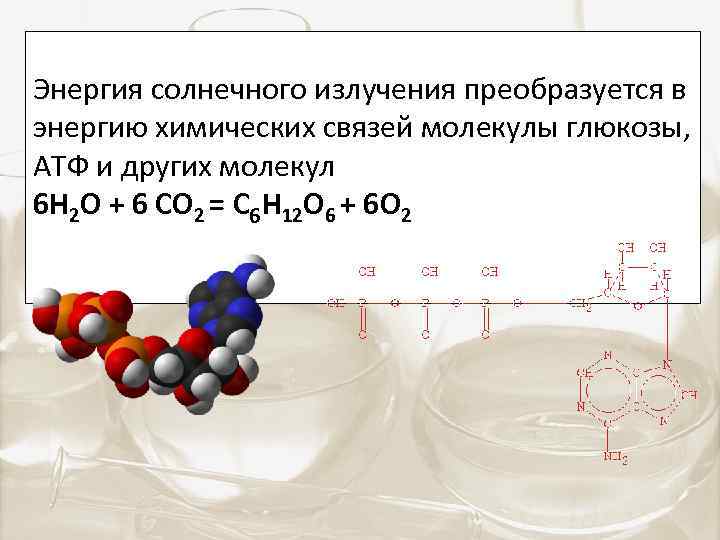
Энергия солнечного излучения преобразуется в энергию химических связей молекулы глюкозы, АТФ и других молекул 6 Н 2 О + 6 СО 2 = С 6 Н 12 О 6 + 6 О 2

110 ккал 30 ккал Работа, 1 час Ходьба, 10 мин 40 ккал Еда, 30 мин 70 ккал Спуск, 5 мин 580 ккал Сон, 8 ч 180 ккал 560 ккал Подъем, 10 мин Уборка, 2 ч 350 ккал За рулем 2 ч 270 ккал 250 ккал Глажение, 1 ч Мытье окон, 1 ч

Задача Потребность в энергии у студентов составляет 11732 к. Дж в сутки. Можно ли рекомендовать студенту следующий рацион питания: • белки – 97 г, • углеводы – 378 г, • жиры – 103 г. калорийность рациона: • Углеводов = 16, 7 к. Дж/г • Жиров = 37, 7 к. Дж/г • Белков = 16, 7 к. Дж/г

Термодинамическая система • это тело или группа тел, отделенные от окружающей среды реальной или воображаемой поверхностью раздела. • Однородная часть системы с одинаковыми химическими и термодинамическими свойствами, отделенная от других частей видимой поверхностью раздела, называется фазой. • Системы, состоящие только из одной фазы, называются гомогенными (однородными). • Системы, содержащие две или большее количество фаз, называются гетерогенными (неоднородными).

Термодинамические параметры основные общие Функции состояния • давление (Р) • внутренняя энергия(E) • температура (Т) • энтальпия (Н) • объем (V) • энтропия (S) • свободная энергия Гиббса измеряемые (G) Измеряются абсолютные значения неизмеряемые Измеряются ∆H, ∆E, ∆G, ∆S(s)

Первый закон термодинамики • Подведенное к системе тепло идет на увеличение внутренней энергии системы и на совершение внешней работы Q = ∆Е + А • В изолированной системе сумма всех видов энергии есть величина постоянная ∆Е = 0 (в изолированной системе)

Внутренняя энергия Е – сумма всех видов энергии частиц, составляющих систему. Энтальпия Н – теплосодержание системы. Q = ∆Е + А ∆Н = ∆E + P∆V Qр = ∆Н

Основной закон термохимии – закон Гесса. Тепловой эффект реакции не зависит от пути протекания реакции, а определяется только исходным и конечным состоянием системы ∆Н < 0 - экзотермическая реакция ∆Н> 0 - эндотермическая реакция

Энтропия S – мера хаотичности, беспорядка Второй закон термодинамики: В изолированных системах энтропия самопроизвольно протекающего процесса возрастает ∆S>0 Sт < Sж < Sгаз

Энергия Гиббса G Изобарно-изотермический потенциал – максимальная полезная работа, совершаемая системой при постоянных давлении и температуре. ∆G = ∆H - T ∆S

Критерии самопроизвольности процесса ∆Н< 0 - энтальпийный фактор ∆S> 0 – энтропийный фактор ∆G< 0 – универсальный критерий ∆G= 0 – термодинамическое равновесие

Термодинамическое равновесное состояние – постоянство свойств системы во времени, потоки вещества и энергии отсутствуют. Стационарное состояние - постоянство свойств системы во времени, которое поддерживается обменом веществом, энергией, информацией с окружающей средой (гомеостаз)

Факторы, определяющие ход процесса

Сопряженные реакции Глюкоза+Фруктоза=Сахароза+Н 2 О +20, 9 к. Дж/моль, Эндергонический процесс ∆G > 0 ведомая реакция АTФ + Н 2 О = AДФ + Н 3 РО 4 -30, 4 к. Дж/моль, Экзергонический процесс ∆G< 0 ведущая реакция Суммарное уравнение АТФ + Глюкоза + Фруктоза = Сахароза + AДФ+ Н 3 РО 4 -9, 5 к. Дж/моль ∆G< 0

Кинетика – учение о скоростях и механизмах химических реакций.

Скорость реакции число элементарных актов реакции, происходящих в единицу времени в единице объема (в случае гомогенной реакции) или на единице поверхности раздела фаз (в случае гетерогенной реакции).

Обратимые реакции протекают одновременно в прямую и обратную стороны Необратимые реакции - протекают в одну сторону до полного израсходования исходных продуктов
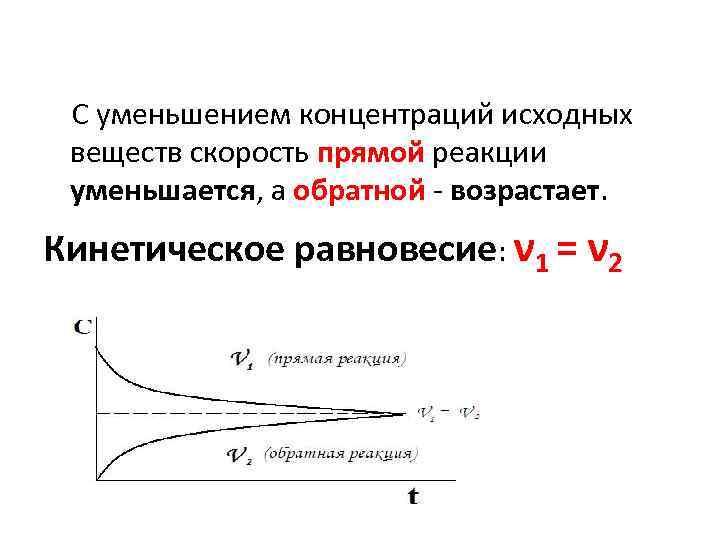
С уменьшением концентраций исходных веществ скорость прямой реакции уменьшается, а обратной - возрастает. Кинетическое равновесие: ν 1 = ν 2

Скорость химической реакции зависит от • - природы реагирующих веществ; • - концентрации; • - температуры; • - давления (для газов); • - катализатора; • - площади соприкосновения в гетерогенных реакциях.

Влияние концентрации Закон Гульдберга и Вааге (1867) m. A+n. B=d. D , где: k – константа скорости реакции; – скорость реакции , моль/л*с; С – молярные концентрации исходных веществ А и В (моль/л); m и n – стехиометрические коэффициенты

для гетерогенной реакции • Горение угля С + О 2 = СО 2 ν = k[O 2] • Константа скорости реакции (k) численно равна скорости реакции, когда концентрации реагирующих веществ равны единице (1 моль/л),

Влияние давления Р С Н СI 2, 2 ν 1

Влияние температуры. С увеличением Т скорость любой реакции возрастает Правило Вант – Гоффа При повышении температуры на каждые скорость реакции увеличивается в 2 – 4 раза где: и – конечная и начальная температуры; – температурный коэффициент реакции; и – скорости реакции при и

Влияние катализатора Катализаторы - вещества, влияющие на скорость протекания термодинамически возможных химических реакций, но остающиеся неизменными в результате этих реакций Вещества, увеличивающие скорость протекания процесса, называют положительными катализаторами, а уменьшающие – отрицательными катализаторами (ингибиторами)
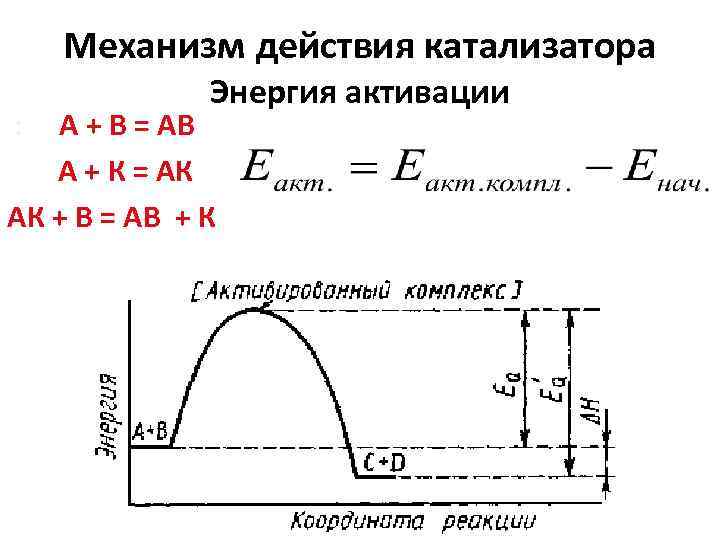
Механизм действия катализатора Энергия активации : А + В = АВ А + К = АК АК + В = АВ + К
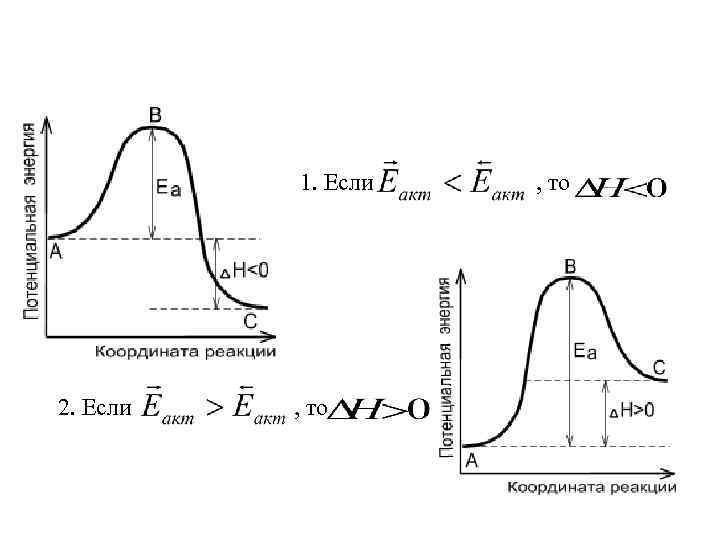
1. Если , то 2. Если , то
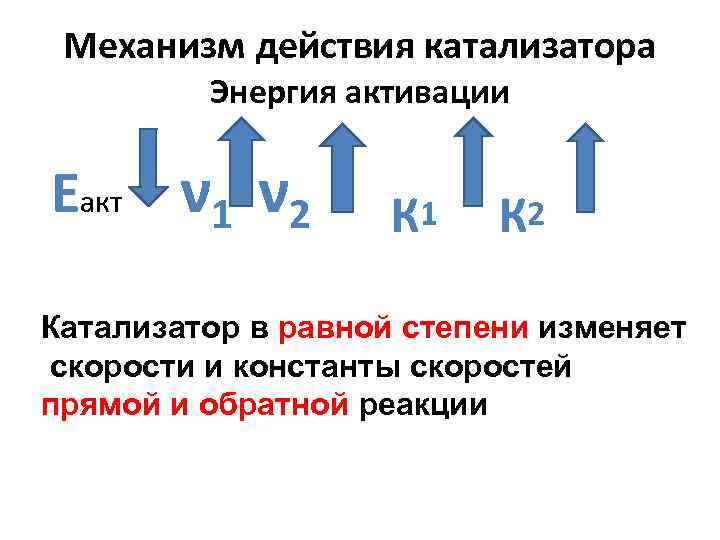
Механизм действия катализатора Энергия активации Еакт ν 1 ν 2 К 1 К 2 Катализатор в равной степени изменяет скорости и константы скоростей прямой и обратной реакции
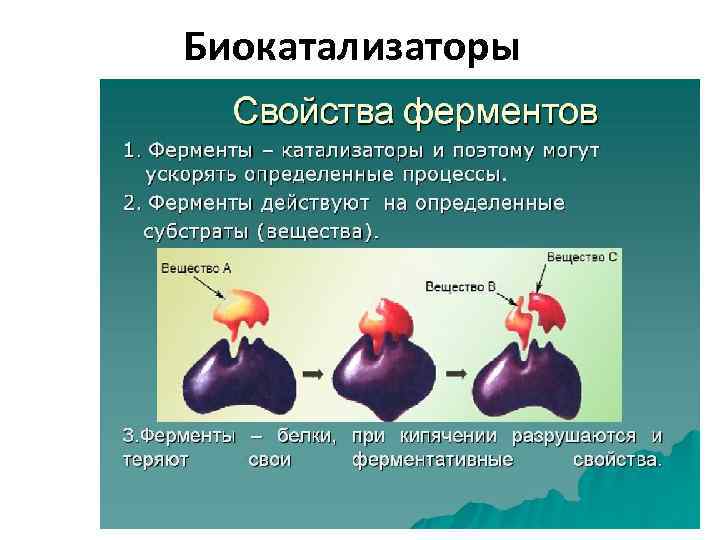
Биокатализаторы

Особенности ферментов как биокатализаторов 1. Высокая эффективность действия; 2. Избирательность (селективность); 3. Высокая чувствительность к условиям среды (t, p. H и др. ); 4. Сложное строение (белковые структуры).


Кинетические параметры: ν, k, Кравн. Константа скорости реакции (k) зависит от: 1. природы реагирующих веществ; 2. температуры; 3. катализатора (Еакт. )

Уравнение Аррениуса. где: k – константа скорости реакции; R – универсальная газовая постоянная (8, 31 Дж/моль. К); Т – абсолютная температура Кельвина(К); Еакт – энергия активации (Дж/моль) А – предэкспоненциальный коэффициент, учитывающий вероятность и число столкновений; е – основание натурального логарифма.

Константа равновесия В условиях равновесия для любого обратимого гомогенного процесса m. A + n. B p. C + q. D Константа равновесия зависит от: 1. природы реагирующих веществ; 2. температуры.

Кравн. k V -природы реагирующих веществ; -температуры; - катализатора; - концентрации; - давления (для газов);

Принцип Ле - Шателье Равновесие в системе всегда смещается в сторону того процесса, протекание которого уменьшает эффект внешнего воздействия на систему. На смещение влияют: 1. температура 2. концентрация 3. давление (для газов) ! Принцип Ле-Шателье не говорит об изменении скоростей, констант скоростей и константы

Термодинамика химического равновесия связь Кравн. со свободной энергией Гиббса: самопроизвольный процесс термодинамическое равновесие реакция не протекает

СПАСИБО ЗА ВНИМАНИЕ ПОЗДРАВЛЯЮ С ПОСТУПЛЕНИЕМ В ПСПБГМУ
Химия - Термодинамика и Кинетика.ppt