Инф и иммунитет 2013-2014.ppt
- Количество слайдов: 47
 Противовирусный иммунитет
Противовирусный иммунитет
 Селекция вирусов и хозяина • Селекция вирусов идет по их способности избегать иммунного ответа хозяина • Наиболее «успешные» вирусы снижают иммунитет хозяина и выживают. • Селекция хозяина – по устойчивости (адаптации) к возбудителям вирусных болезней • Самый «успешный» хозяин служит длительной мишенью для последующих генераций вирусов.
Селекция вирусов и хозяина • Селекция вирусов идет по их способности избегать иммунного ответа хозяина • Наиболее «успешные» вирусы снижают иммунитет хозяина и выживают. • Селекция хозяина – по устойчивости (адаптации) к возбудителям вирусных болезней • Самый «успешный» хозяин служит длительной мишенью для последующих генераций вирусов.
 Врожденный иммунитет. • • • 1. Интерфероны • 2. Комплемент (виролиз по альтернативному пути) 3. Лизоцим 4. Ферменты кишечника и желчи (разрушают некоторые вирусы) 5. Коллектины (взаимодействуют с гликопротеинами вируса и блокируют связь с клеткой): конглютинин, маннозасвязывающий лектин, сурфактанты(SP-A SP-B)- блок вирус гриппа. 6. Дефензины лейкоцитов и эпителиальных клеток- на вирусы (взаимодействие с вирусными гликопротеинами) и вирус инфицированные клетки (блок транскрипции вирусной РНК и внутриклеточных сигналных путей) Преждевременный апоптоз вирусинфицированных клеток( блок репликации вирусов) 7. НК 8. МФ
Врожденный иммунитет. • • • 1. Интерфероны • 2. Комплемент (виролиз по альтернативному пути) 3. Лизоцим 4. Ферменты кишечника и желчи (разрушают некоторые вирусы) 5. Коллектины (взаимодействуют с гликопротеинами вируса и блокируют связь с клеткой): конглютинин, маннозасвязывающий лектин, сурфактанты(SP-A SP-B)- блок вирус гриппа. 6. Дефензины лейкоцитов и эпителиальных клеток- на вирусы (взаимодействие с вирусными гликопротеинами) и вирус инфицированные клетки (блок транскрипции вирусной РНК и внутриклеточных сигналных путей) Преждевременный апоптоз вирусинфицированных клеток( блок репликации вирусов) 7. НК 8. МФ
 Интерфероны-особенно важны. Секретируются вирус-инфицированными клетками, защищают другие клетки от поражения. • • Тип 1 ИФ альфа (плазмацитоидные ДК – осн. продуцент; Л, Мо, МФ. )много изоформ. ИФ бетта (вирусинфицированные фибробласты) ИФ альфа 11 (Л, Мо, трофобласты) ИФ тетта (трофобласты жвачных) ИФ дельта ( трофобласты свиней) ИФ каппа (его формы ИЛ 28, ИЛ 29) • Тип 2 • ИФ –γ ( АГ стимулированные Тл, трофобласты, НК).
Интерфероны-особенно важны. Секретируются вирус-инфицированными клетками, защищают другие клетки от поражения. • • Тип 1 ИФ альфа (плазмацитоидные ДК – осн. продуцент; Л, Мо, МФ. )много изоформ. ИФ бетта (вирусинфицированные фибробласты) ИФ альфа 11 (Л, Мо, трофобласты) ИФ тетта (трофобласты жвачных) ИФ дельта ( трофобласты свиней) ИФ каппа (его формы ИЛ 28, ИЛ 29) • Тип 2 • ИФ –γ ( АГ стимулированные Тл, трофобласты, НК).
 • ИФ в большинстве случаев ингибируют репродукцию вирусов. • ИФ трофобластов регулируют иммунитет матери против плода.
• ИФ в большинстве случаев ингибируют репродукцию вирусов. • ИФ трофобластов регулируют иммунитет матери против плода.
 Индукция ИФ. Клетки животных могут распознавать вирусные нуклеиновые кислоты 2 рецепторными системами. 1 • Протеины-сенсоры нуклеиновых кислот в цитоплазме всех ядерных клеток- RIG-1 и MDA 5 • Эти молекулы распознают двуспиральную вирусную РНК или ДНК, посылает сигнал через несколько адапторных белков для активации ИФ бетта генов. 2 Система опосредована TLR 3, 7, 8, 9. Результат – синтез ИФ 1 типа.
Индукция ИФ. Клетки животных могут распознавать вирусные нуклеиновые кислоты 2 рецепторными системами. 1 • Протеины-сенсоры нуклеиновых кислот в цитоплазме всех ядерных клеток- RIG-1 и MDA 5 • Эти молекулы распознают двуспиральную вирусную РНК или ДНК, посылает сигнал через несколько адапторных белков для активации ИФ бетта генов. 2 Система опосредована TLR 3, 7, 8, 9. Результат – синтез ИФ 1 типа.
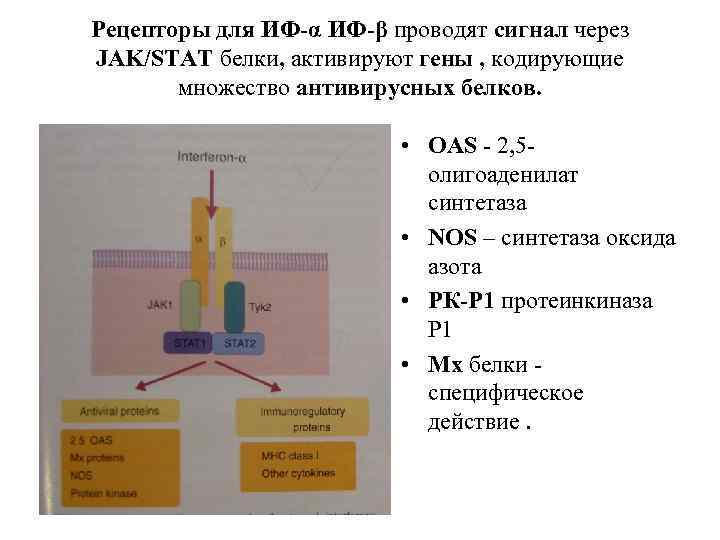 Рецепторы для ИФ-α ИФ-β проводят сигнал через JAK/STAT белки, активируют гены , кодирующие множество антивирусных белков. • ОАS - 2, 5 олигоаденилат синтетаза • NOS – синтетаза oксидa азота • РК-Р 1 протеинкиназа Р 1 • Мх белки специфическое действие.
Рецепторы для ИФ-α ИФ-β проводят сигнал через JAK/STAT белки, активируют гены , кодирующие множество антивирусных белков. • ОАS - 2, 5 олигоаденилат синтетаза • NOS – синтетаза oксидa азота • РК-Р 1 протеинкиназа Р 1 • Мх белки специфическое действие.
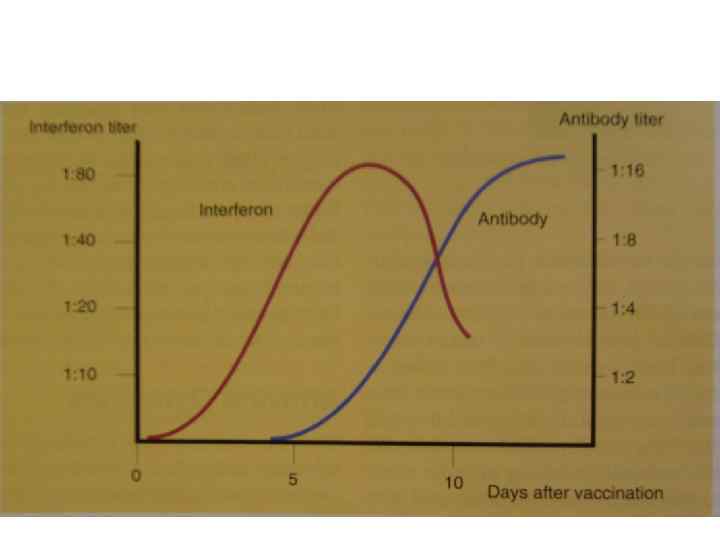
 . • ИФ-α и ИФ-β - синтез через несколько часов после поражения вирусом. Высокая концентрация сохраняется в течение длительного времени, до развития адаптивного иммунитета.
. • ИФ-α и ИФ-β - синтез через несколько часов после поражения вирусом. Высокая концентрация сохраняется в течение длительного времени, до развития адаптивного иммунитета.
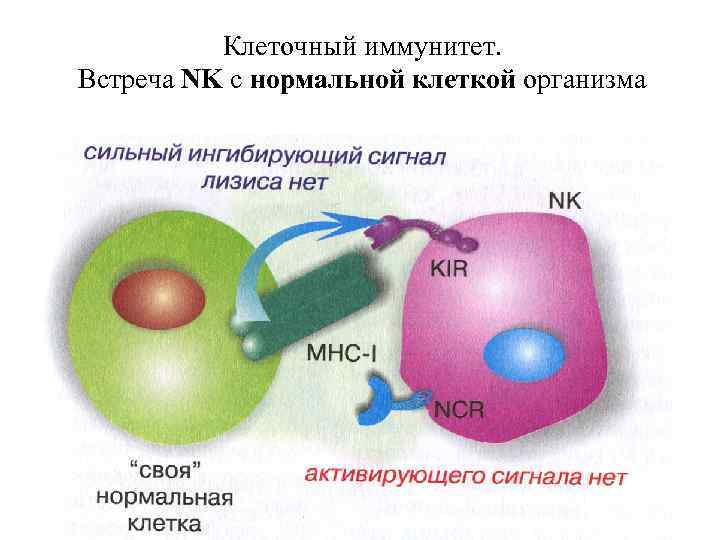 Клеточный иммунитет. Встреча NK с нормальной клеткой организма
Клеточный иммунитет. Встреча NK с нормальной клеткой организма
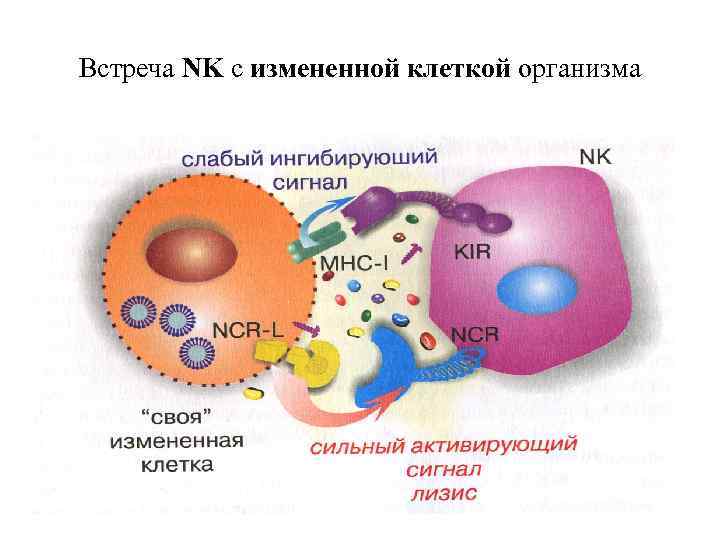 Встреча NK с измененной клеткой организма
Встреча NK с измененной клеткой организма
 Макрофаги
Макрофаги
 Адаптивный иммунитет. Гуморальный иммунитет ( АТ). • Нейтрализующие вирус АТ принадлежат к классам: Ig G, Ig. M, Ig. A. Ig. E играет протективную роль. • Люди с иммунодефицитом Ig. E класса страдают тяжелыми респираторными инфекциями. • АТ направлены против: • белков внеклеточных вирионов • против вирусных АГ, на инфицированной клетке.
Адаптивный иммунитет. Гуморальный иммунитет ( АТ). • Нейтрализующие вирус АТ принадлежат к классам: Ig G, Ig. M, Ig. A. Ig. E играет протективную роль. • Люди с иммунодефицитом Ig. E класса страдают тяжелыми респираторными инфекциями. • АТ направлены против: • белков внеклеточных вирионов • против вирусных АГ, на инфицированной клетке.
 Функции АТ. • 1. АТ к вирусу: блокируют адгезию на клеткимишени; • 2. АТ - опсонины-стимулируют фагоцитоз вирусов; • 3. АТ+Комплемент- виролиз; блок адгезии вирусов на клетке • 4. Аггрегация вирусов - снижение числа инфекционных единиц; • 5. АЗКЦ вирусинфицированных клеток;
Функции АТ. • 1. АТ к вирусу: блокируют адгезию на клеткимишени; • 2. АТ - опсонины-стимулируют фагоцитоз вирусов; • 3. АТ+Комплемент- виролиз; блок адгезии вирусов на клетке • 4. Аггрегация вирусов - снижение числа инфекционных единиц; • 5. АЗКЦ вирусинфицированных клеток;
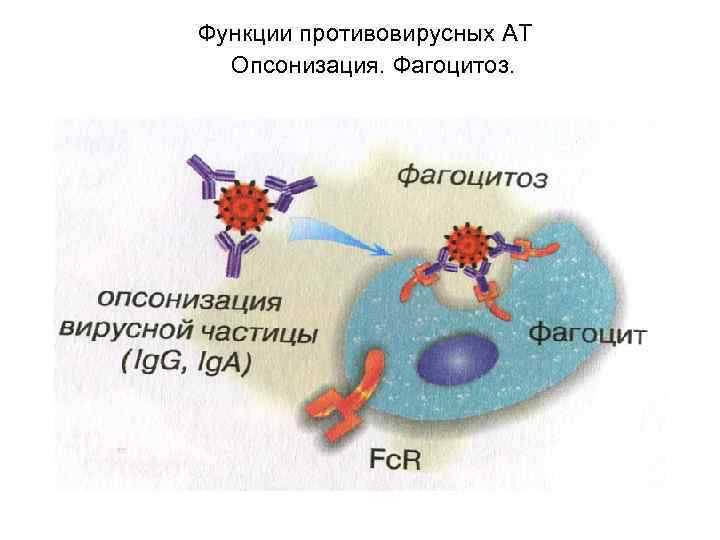 Функции противовирусных АТ Опсонизация. Фагоцитоз.
Функции противовирусных АТ Опсонизация. Фагоцитоз.
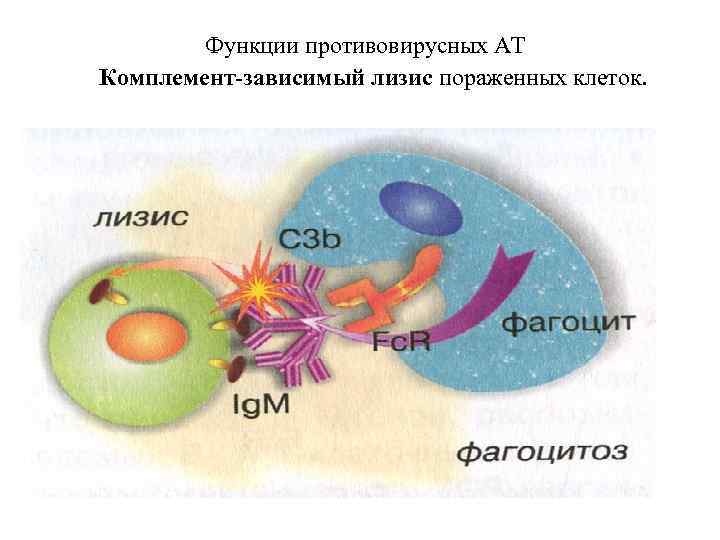 Функции противовирусных АТ Комплемент-зависимый лизис пораженных клеток.
Функции противовирусных АТ Комплемент-зависимый лизис пораженных клеток.
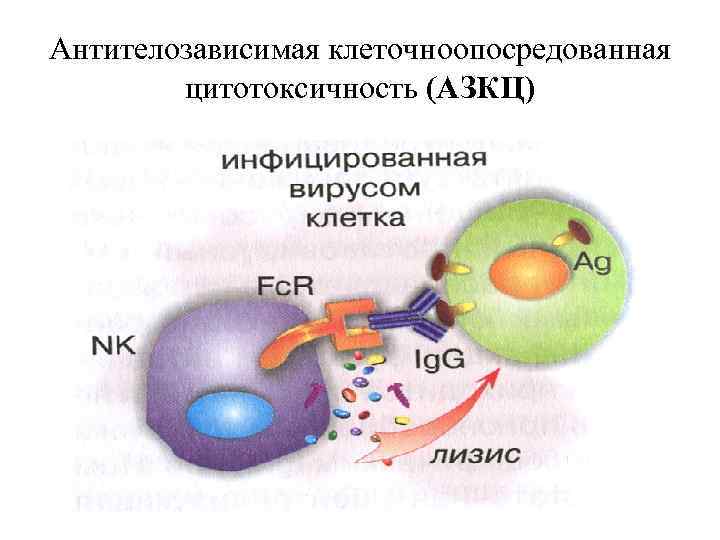 Антителозависимая клеточноопосредованная цитотоксичность (АЗКЦ)
Антителозависимая клеточноопосредованная цитотоксичность (АЗКЦ)
 Т-клеточный иммунитет. Наиболее важен для контроля вирусных инфекций. Обычно Т-л дефицитные особи устойчивы к большинству бактериальных инфекций, но высокочувствительны к вирусным болезням. • 1. СТL (перфоринзависимый механизм и Fas механизм) • 2. СТL –уничтожение вируса, без киллинга инфицированной клетки. • 2 пути уничтожения вируса: • А. Уничтожение вирусного нуклеокапсида. • В. Ингибирование вирусной РНК.
Т-клеточный иммунитет. Наиболее важен для контроля вирусных инфекций. Обычно Т-л дефицитные особи устойчивы к большинству бактериальных инфекций, но высокочувствительны к вирусным болезням. • 1. СТL (перфоринзависимый механизм и Fas механизм) • 2. СТL –уничтожение вируса, без киллинга инфицированной клетки. • 2 пути уничтожения вируса: • А. Уничтожение вирусного нуклеокапсида. • В. Ингибирование вирусной РНК.
 Некоторые вирусные белки являются суперантигенами.
Некоторые вирусные белки являются суперантигенами.
 Иммунологическая память при вирусных инфекциях как правило длительная. (Длительная персистенция вируса внутри клеткивозможная причина)- герпесвирусная инфекция • У вирусов белки и гликопротеины оболочки являются типичными тимусзависимыми антигенами. • Продолжительность иммунологической памяти к вирусным инфекциям значительно варьирует. • Тм и АТ могут персистировать много лет в отсутствии вирусов.
Иммунологическая память при вирусных инфекциях как правило длительная. (Длительная персистенция вируса внутри клеткивозможная причина)- герпесвирусная инфекция • У вирусов белки и гликопротеины оболочки являются типичными тимусзависимыми антигенами. • Продолжительность иммунологической памяти к вирусным инфекциям значительно варьирует. • Тм и АТ могут персистировать много лет в отсутствии вирусов.
 Вирусы обладают разными стратегиями выживания в организме хозяина. • У РНК –овых вирусов очень маленький геном, «экономят» на генах, ответственных за подавление иммунитета. • Протеины РНК-овых вирусов многофункциональны. • У ДНК-овых вирусов большие геномы, могут себе «позволить» иметь много различных генов для избегания иммунного ответа • У поксвирусов и герпесвирусов 50% генома посвящено иммунорегуляторным генам.
Вирусы обладают разными стратегиями выживания в организме хозяина. • У РНК –овых вирусов очень маленький геном, «экономят» на генах, ответственных за подавление иммунитета. • Протеины РНК-овых вирусов многофункциональны. • У ДНК-овых вирусов большие геномы, могут себе «позволить» иметь много различных генов для избегания иммунного ответа • У поксвирусов и герпесвирусов 50% генома посвящено иммунорегуляторным генам.
 Первый механизм избегания иммунного ответа. Изменчивость структуры АГ микроорганизмов.
Первый механизм избегания иммунного ответа. Изменчивость структуры АГ микроорганизмов.
 • Серологические варианты. Мутационный процесс внутри вида. К каждому варианту формируется специфический иммунный ответ. Смена синтеза вариант специфических антигенов. Поочередная экспрессия продуктов разных генов. Выход из-под контроля иммунных механизмов
• Серологические варианты. Мутационный процесс внутри вида. К каждому варианту формируется специфический иммунный ответ. Смена синтеза вариант специфических антигенов. Поочередная экспрессия продуктов разных генов. Выход из-под контроля иммунных механизмов
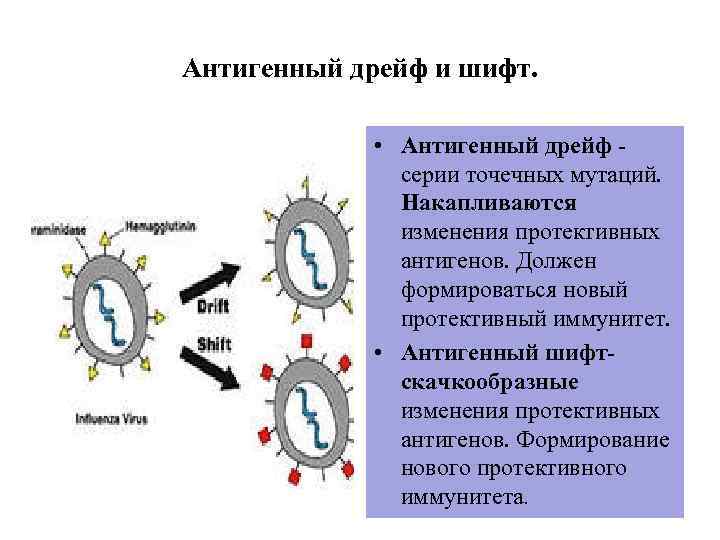 Антигенный дрейф и шифт. • Антигенный дрейф серии точечных мутаций. Накапливаются изменения протективных антигенов. Должен формироваться новый протективный иммунитет. • Антигенный шифтскачкообразные изменения протективных антигенов. Формирование нового протективного иммунитета.
Антигенный дрейф и шифт. • Антигенный дрейф серии точечных мутаций. Накапливаются изменения протективных антигенов. Должен формироваться новый протективный иммунитет. • Антигенный шифтскачкообразные изменения протективных антигенов. Формирование нового протективного иммунитета.
 Второй механизм избегания иммунного ответа. Отсутствие синтеза нейтрализующих АТ.
Второй механизм избегания иммунного ответа. Отсутствие синтеза нейтрализующих АТ.
 Вирусный энцефалит коз; Алеутская болезнь норок ; Африканская чума свиней • Животные не могут распознавать и отвечать на протективные эпитопы. • Синтез большого количества АТ против других гликопротеинов оболочки вирусов. • Иммунные комплексы инфекционны. • Большое количество других АТ связываются с вирусами, опсонизируют их, комплексы поглощаются МФ, инфекционный вирус реплицируется внутри МФ. ( Ускоренная АТ репликация вируса). Вакцинация утяжеляет болезнь.
Вирусный энцефалит коз; Алеутская болезнь норок ; Африканская чума свиней • Животные не могут распознавать и отвечать на протективные эпитопы. • Синтез большого количества АТ против других гликопротеинов оболочки вирусов. • Иммунные комплексы инфекционны. • Большое количество других АТ связываются с вирусами, опсонизируют их, комплексы поглощаются МФ, инфекционный вирус реплицируется внутри МФ. ( Ускоренная АТ репликация вируса). Вакцинация утяжеляет болезнь.
 Третий механизм избегания иммунного ответа Нейтрализующие АТ образуются очень медленно.
Третий механизм избегания иммунного ответа Нейтрализующие АТ образуются очень медленно.
 Меди-висна, комплекс болезней овец. (РНК-овый вирус) • АТ имеют низкое сродство к эпитопам вируса • ( 20 мин. для связывания и 30 мин для нейтрализации. Всего 2 мин для заражения клетки). Вирус быстро распространяется между клетками. • АТ не способны снизить вирусную нагрузку. Вирус поражает МО, МФ.
Меди-висна, комплекс болезней овец. (РНК-овый вирус) • АТ имеют низкое сродство к эпитопам вируса • ( 20 мин. для связывания и 30 мин для нейтрализации. Всего 2 мин для заражения клетки). Вирус быстро распространяется между клетками. • АТ не способны снизить вирусную нагрузку. Вирус поражает МО, МФ.
 Вирусы поражают клетки иммунной системы. • Иммуносупрессия • Вызывает персистентные инфекции, ведущие к хроническим заболеваниям и к формированию опухолей
Вирусы поражают клетки иммунной системы. • Иммуносупрессия • Вызывает персистентные инфекции, ведущие к хроническим заболеваниям и к формированию опухолей
 Противобактериальный иммунитет • Микроорганизмы, попавшие в организм млекопитающих, не стремятся нанести организму хозяина смертельный удар. • Болезнь или даже смерть животного может значительно снизит выживаемость бактерий как популяции.
Противобактериальный иммунитет • Микроорганизмы, попавшие в организм млекопитающих, не стремятся нанести организму хозяина смертельный удар. • Болезнь или даже смерть животного может значительно снизит выживаемость бактерий как популяции.
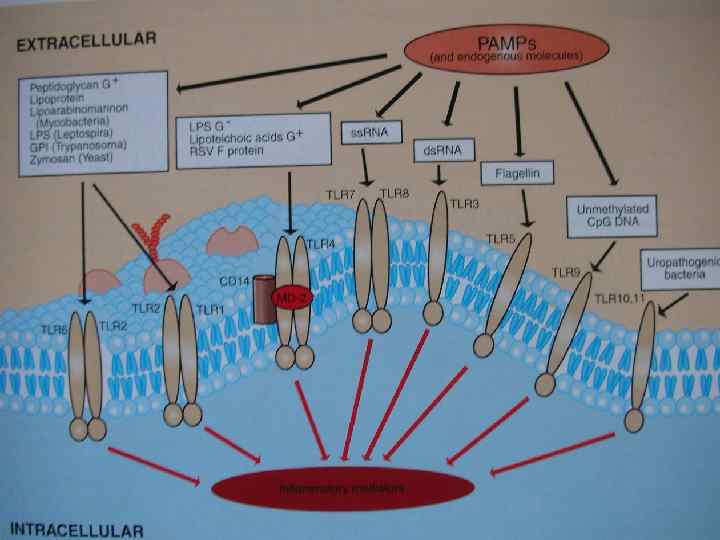
 Существует 5 механизмов защиты от бактерий. • 1. Нейтрализация токсинов или ферментов бактерий антителами. • 2. Киллинг бактерий антителами и комплементом. • АТ не только маркируют бактерии для разрушения, но и напрямую их убивают. • Так, АТ против E. coli бактериостатики нарушают синтез энтерохилина тем самым ингибируют использование железа бактериями. • АТ могут нарушать поверхностные белки бактерий и генерировать оксиданты.
Существует 5 механизмов защиты от бактерий. • 1. Нейтрализация токсинов или ферментов бактерий антителами. • 2. Киллинг бактерий антителами и комплементом. • АТ не только маркируют бактерии для разрушения, но и напрямую их убивают. • Так, АТ против E. coli бактериостатики нарушают синтез энтерохилина тем самым ингибируют использование железа бактериями. • АТ могут нарушать поверхностные белки бактерий и генерировать оксиданты.
 • 3. Опсонизация бактерий антителами и комплеменом, их фагоцитоз. • 4. Разрушение внутриклеточных бактерий активированными макрофагами. • 5. Киллинг бактерий CTL и NK. Вклад каждого механизма зависит от вида бактерий и от патогенеза болезни.
• 3. Опсонизация бактерий антителами и комплеменом, их фагоцитоз. • 4. Разрушение внутриклеточных бактерий активированными макрофагами. • 5. Киллинг бактерий CTL и NK. Вклад каждого механизма зависит от вида бактерий и от патогенеза болезни.
 Особенности иммунного ответа при: • 1. Токсикозах и токсикоинфекциях. • 2. Инфекциях, вызванных внеклеточными бактериями. • 3. Инфекциях, вызванных внутриклеточными бактериями.
Особенности иммунного ответа при: • 1. Токсикозах и токсикоинфекциях. • 2. Инфекциях, вызванных внеклеточными бактериями. • 3. Инфекциях, вызванных внутриклеточными бактериями.
 Иммунитет к токсигенным бактериям. Clostridium spp. , Bacillus anthracis и др. • Элиминация бактерий, нейтрализациия токсина. • Процесс нейтрализации состоит в конкуренции между рецепторами и АТ за молекулу токсина. • Если токсин связывается с рецептором, АТ не могут разрушить этот комплекс.
Иммунитет к токсигенным бактериям. Clostridium spp. , Bacillus anthracis и др. • Элиминация бактерий, нейтрализациия токсина. • Процесс нейтрализации состоит в конкуренции между рецепторами и АТ за молекулу токсина. • Если токсин связывается с рецептором, АТ не могут разрушить этот комплекс.
 B. anthracis имеет и капсулу и экзотоксин. • Инкапсулированный микроорганизм ускользает от фагоцитоза и удлиняется период токсинообразования. • Антитоксический иммунитет протективный , но развивается медленно. • Результат – летальный исход невакцинированных животных. • Вакцинные штаммы токсигенны но бескапсульные, в споровой форме. • Бескапсульные бактерии удаляются фагоцитозом до того как накопятся опасные количества токсина, но не до того как разовьется антитоксический иммунитет.
B. anthracis имеет и капсулу и экзотоксин. • Инкапсулированный микроорганизм ускользает от фагоцитоза и удлиняется период токсинообразования. • Антитоксический иммунитет протективный , но развивается медленно. • Результат – летальный исход невакцинированных животных. • Вакцинные штаммы токсигенны но бескапсульные, в споровой форме. • Бескапсульные бактерии удаляются фагоцитозом до того как накопятся опасные количества токсина, но не до того как разовьется антитоксический иммунитет.
 Иммунитет к внеклеточным бактериям. • 1. Активация комплемента по альтернативному и лектиновому пути с образованием С 3 в – опсонинов. АТ: • 2. АТ к поверхностным О- АГ бактерий – это опсонины и активаторы классического пути активации комплемента. • 3. АТ против К-АГ (капсула) бактерий нейтрализуют ее антифагоцитарную активность. • 4. АТ против пилей или адгезивных АГ нейтрализуют их, влияют на экспрессию пилей и вызвают делецию генов, кодирующих адгезивные АГ в плазмидах. • Патогенность таких бактерий утрачивается.
Иммунитет к внеклеточным бактериям. • 1. Активация комплемента по альтернативному и лектиновому пути с образованием С 3 в – опсонинов. АТ: • 2. АТ к поверхностным О- АГ бактерий – это опсонины и активаторы классического пути активации комплемента. • 3. АТ против К-АГ (капсула) бактерий нейтрализуют ее антифагоцитарную активность. • 4. АТ против пилей или адгезивных АГ нейтрализуют их, влияют на экспрессию пилей и вызвают делецию генов, кодирующих адгезивные АГ в плазмидах. • Патогенность таких бактерий утрачивается.
 Иммунитет к внутриклеточным бактериям. Активированные МФ – основные эффекторные клетки против них. • Цитокины Т х1: ИФγ и ФНОα значительно увеличивают продукцию NO и NO 2 – в МФ. • Ответ неспецифичен, способны разрушать многие обычно резистентные бактерии, присутствующие в организме. • МФ животных переболевших, например, листериозом, развивают высокую устойчивость к M. tuberculosis.
Иммунитет к внутриклеточным бактериям. Активированные МФ – основные эффекторные клетки против них. • Цитокины Т х1: ИФγ и ФНОα значительно увеличивают продукцию NO и NO 2 – в МФ. • Ответ неспецифичен, способны разрушать многие обычно резистентные бактерии, присутствующие в организме. • МФ животных переболевших, например, листериозом, развивают высокую устойчивость к M. tuberculosis.
 Патогенез бактериальных болезней зависит от направленности иммунного ответа (клеточный или гуморальный). • Лепра у людей протекает в 2 -х формах: туберкулоидная и лепроматозная. • Туберкулоидная форма характеризуется интенсивным клеточный иммунитет. В поврежденных тканях содержится небольшое количество возбудителя. • Лепроматозная – высокий титр АТ к возбудителю, низкий клеточный ответ (Т-х2, ИЛ 4, 10), в очагах поражения большое количество возбудителя. Прогноз неблагоприятный
Патогенез бактериальных болезней зависит от направленности иммунного ответа (клеточный или гуморальный). • Лепра у людей протекает в 2 -х формах: туберкулоидная и лепроматозная. • Туберкулоидная форма характеризуется интенсивным клеточный иммунитет. В поврежденных тканях содержится небольшое количество возбудителя. • Лепроматозная – высокий титр АТ к возбудителю, низкий клеточный ответ (Т-х2, ИЛ 4, 10), в очагах поражения большое количество возбудителя. Прогноз неблагоприятный
 ИЛ 4 включает Т-х2 -гуморальный ответ и супрессирует Т -х1 клеточный ответ. • Животные могут синтезировать структурные варианты ИЛ 4: ИЛ 4 δ 2 и ИЛ 4 δ 3 путем альтернативного сплайсинга pre-m. RNA (телята). • Эти варианты могут связываться и блокировать рецепторы к ИЛ 4, в результате развивается клеточный иммунитет.
ИЛ 4 включает Т-х2 -гуморальный ответ и супрессирует Т -х1 клеточный ответ. • Животные могут синтезировать структурные варианты ИЛ 4: ИЛ 4 δ 2 и ИЛ 4 δ 3 путем альтернативного сплайсинга pre-m. RNA (телята). • Эти варианты могут связываться и блокировать рецепторы к ИЛ 4, в результате развивается клеточный иммунитет.
 • Иммунный ответ в начале бактериальных инфекций может колебаться между Т-х1 и Т-х2 ответом пока не установится окончательный вариант: • либо Т-х1, • либо Т-х2, • либо средний вариант.
• Иммунный ответ в начале бактериальных инфекций может колебаться между Т-х1 и Т-х2 ответом пока не установится окончательный вариант: • либо Т-х1, • либо Т-х2, • либо средний вариант.
 Осложнения при антибактериальном иммунитете. 1. Иммуносупрессия, вызываемая бактериями Механизм недостаточно изучен. • При хронических микобактериальных болезнях отмечается состояние анергии, лимфоциты не дифференцируются, увеличивается число клетоксупрессоров. • 2. Повреждения, вызываемые АТ к эпитопам, общим для возбудителя и хозяина. • 3. Белки теплового шока (БТШ) вызывают развитие аутоиммунных заболеваний. • Это стрессовые белки, экспрессируются на возбудителях и клетках хозяина, антигенно родственны.
Осложнения при антибактериальном иммунитете. 1. Иммуносупрессия, вызываемая бактериями Механизм недостаточно изучен. • При хронических микобактериальных болезнях отмечается состояние анергии, лимфоциты не дифференцируются, увеличивается число клетоксупрессоров. • 2. Повреждения, вызываемые АТ к эпитопам, общим для возбудителя и хозяина. • 3. Белки теплового шока (БТШ) вызывают развитие аутоиммунных заболеваний. • Это стрессовые белки, экспрессируются на возбудителях и клетках хозяина, антигенно родственны.
 • • • Иммунитет против патогенных грибов. Врожденный иммунитет 1. Активация комплемента по АП. 2. Основной защитный механизм – клеточный. РАМР ы грибов через TLR 2 или дектин 1 (поверхностный клеточный лектин), включают синтез ИЛ 23. ИЛ-23 Т х-17 ИЛ-17 активация нейтрофилов, эндотелиальных клеток, развитие острого воспаления. Нейтрофилы - внеклеточный цитолиз, освобождая ферменты наружу. МФ и НК могут поглощать и разрушать маленькие фрагменты грибов и споры. • Дрожжи вызывают продукцию ИЛ-12 и Тх1 ответ.
• • • Иммунитет против патогенных грибов. Врожденный иммунитет 1. Активация комплемента по АП. 2. Основной защитный механизм – клеточный. РАМР ы грибов через TLR 2 или дектин 1 (поверхностный клеточный лектин), включают синтез ИЛ 23. ИЛ-23 Т х-17 ИЛ-17 активация нейтрофилов, эндотелиальных клеток, развитие острого воспаления. Нейтрофилы - внеклеточный цитолиз, освобождая ферменты наружу. МФ и НК могут поглощать и разрушать маленькие фрагменты грибов и споры. • Дрожжи вызывают продукцию ИЛ-12 и Тх1 ответ.
 Адаптивный иммунитет. Некоторые грибы(Aspergillus)-факультативные внутриклеточные паразиты • Основным защитным механизмом служит Тх1 ответ. • Некоторые Т-л и НК могут развивать прямой цитотоксический эффект против криптококков и кандид. • Хронические и прогрессирующие микозы ассоциированы с недостаточностью Т-л (СПИД). • ГЗТ не развивается после перенесенных микозов.
Адаптивный иммунитет. Некоторые грибы(Aspergillus)-факультативные внутриклеточные паразиты • Основным защитным механизмом служит Тх1 ответ. • Некоторые Т-л и НК могут развивать прямой цитотоксический эффект против криптококков и кандид. • Хронические и прогрессирующие микозы ассоциированы с недостаточностью Т-л (СПИД). • ГЗТ не развивается после перенесенных микозов.
 Противопаразитарный иммунитет. Врожденный иммунитет. • 1. Разрушение одноклеточных и многоклеточных паразитов комплементом ( лизис и опсонизация). • • 2. Мелкие и внутриклеточные паразиты могут уничтожаться активированными макрофагами МФ, эозинофилы (главный основной белок и нейротоксин) • 3. Нейтрофилы, Эо и НК-клетки способны вести контактный цитолиз пораженной паразитами клетки.
Противопаразитарный иммунитет. Врожденный иммунитет. • 1. Разрушение одноклеточных и многоклеточных паразитов комплементом ( лизис и опсонизация). • • 2. Мелкие и внутриклеточные паразиты могут уничтожаться активированными макрофагами МФ, эозинофилы (главный основной белок и нейротоксин) • 3. Нейтрофилы, Эо и НК-клетки способны вести контактный цитолиз пораженной паразитами клетки.
 Адаптивный иммунитет. • 1. CTL осуществляют контактный киллинг клеток. • 2. Гельминты обладают уникальной способностью переключать иммунный ответ на Тх2 и вызывать продукцию Ig. E. • 3. В процессе паразитарных болезней часто развиваются аллергические и аутоиммунные заболевания ( ГНТ).
Адаптивный иммунитет. • 1. CTL осуществляют контактный киллинг клеток. • 2. Гельминты обладают уникальной способностью переключать иммунный ответ на Тх2 и вызывать продукцию Ig. E. • 3. В процессе паразитарных болезней часто развиваются аллергические и аутоиммунные заболевания ( ГНТ).
 АТ • 4. АТ усиливают механизмы фагоцитоза, • АТ запускают механизм активации комплемента по классическому пути на поверхности паразита. • АТ нейтрализуют токсины, выделяемые гельминтами, • АТ стерически блокируют рецепторы мелких паразитов.
АТ • 4. АТ усиливают механизмы фагоцитоза, • АТ запускают механизм активации комплемента по классическому пути на поверхности паразита. • АТ нейтрализуют токсины, выделяемые гельминтами, • АТ стерически блокируют рецепторы мелких паразитов.


