Иммунология опухолей нов.ppt
- Количество слайдов: 75
 ПРОТИВООПУХОЛЕВЫЙ ИММУНИТЕТ
ПРОТИВООПУХОЛЕВЫЙ ИММУНИТЕТ
 Что такое опухоль? Опухолью называют патологическую ткань, клетки которой генетически чужеродны для организма. Клетки опухоли не способны образовать нормальные тканевые структуры. В опухолевой ткани нарушено равновесие между клеточными и соединительнотканными структурами. В результате недостаточного кровоснабжения в опухолевой ткани развиваются очаги некроза, изъязвления. Опухоли делят на доброкачественные и злокачественные.
Что такое опухоль? Опухолью называют патологическую ткань, клетки которой генетически чужеродны для организма. Клетки опухоли не способны образовать нормальные тканевые структуры. В опухолевой ткани нарушено равновесие между клеточными и соединительнотканными структурами. В результате недостаточного кровоснабжения в опухолевой ткани развиваются очаги некроза, изъязвления. Опухоли делят на доброкачественные и злокачественные.
 Антигены опухоли Опухолевые антигены, или неоантигены - это такие антигены, которые презентируются молекулами МНС I или MHC II на поверхности опухолевых клеток. Такие антигены могут быть презентированы опухолевыми клетками, и никогда — нормальными клетками. В таком случае они называются опухоль-специфичными антигенами (tumor-specific antigen, TSA). Более распространенными являются антигены, которые презентируются и на поверхности здоровых, и на поверхности опухолевых клеток, их называют опухольассоциированными антигенами (tumor-associated antigen, TAA).
Антигены опухоли Опухолевые антигены, или неоантигены - это такие антигены, которые презентируются молекулами МНС I или MHC II на поверхности опухолевых клеток. Такие антигены могут быть презентированы опухолевыми клетками, и никогда — нормальными клетками. В таком случае они называются опухоль-специфичными антигенами (tumor-specific antigen, TSA). Более распространенными являются антигены, которые презентируются и на поверхности здоровых, и на поверхности опухолевых клеток, их называют опухольассоциированными антигенами (tumor-associated antigen, TAA).
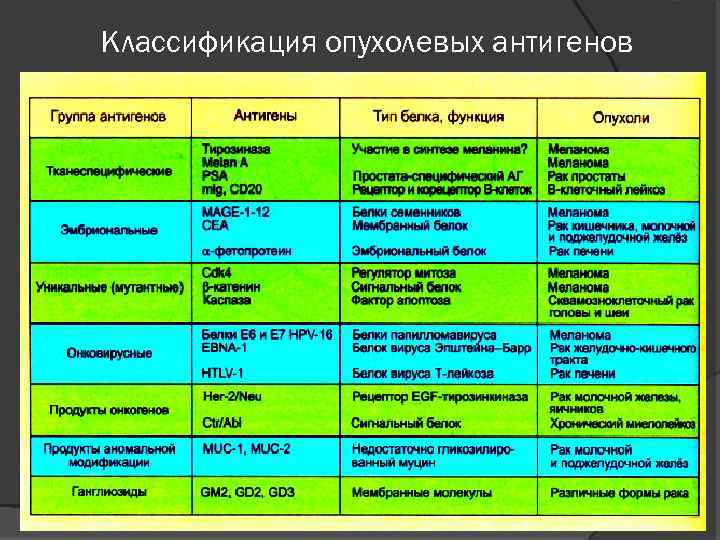 Классификация опухолевых антигенов
Классификация опухолевых антигенов
 Антигены опухоли В настоящее время выделяют четыре группы опухолевых антигенов, различающихся по своему происхождению: вирус-специфические антигены вирусов человека, вызывающих злокачественную трансформацию опухолевых клеток; специфические опухолевые антигены, синтезирующиеся преимущественно в опухолевой ткани; неоантигены, появляющиеся в результате соматических мутаций; клеточные белки, контролирующие пролиферацию опухолевых клеток - теломераза.
Антигены опухоли В настоящее время выделяют четыре группы опухолевых антигенов, различающихся по своему происхождению: вирус-специфические антигены вирусов человека, вызывающих злокачественную трансформацию опухолевых клеток; специфические опухолевые антигены, синтезирующиеся преимущественно в опухолевой ткани; неоантигены, появляющиеся в результате соматических мутаций; клеточные белки, контролирующие пролиферацию опухолевых клеток - теломераза.
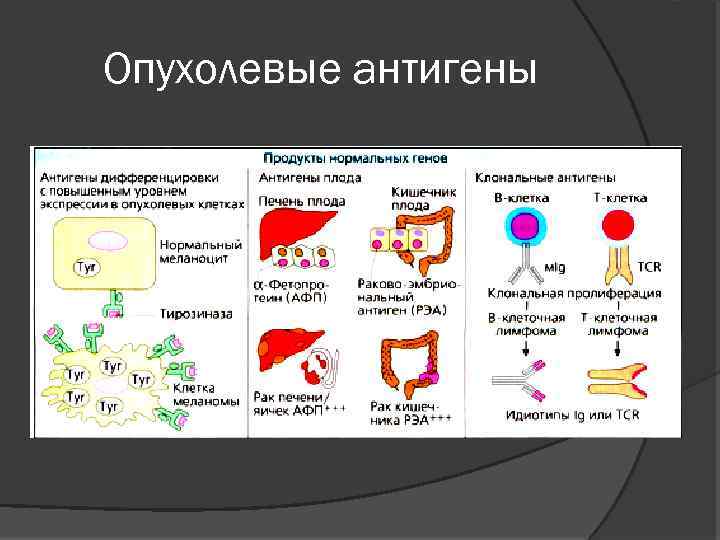 Опухолевые антигены
Опухолевые антигены
 Этиология опухолей 1. 2. 3. 4. 5. Физические факторы (УФО, Х и У-лучи) Химические канцерогены (ароматические амины, полициклические ароматические углеводороды) Вирусы (ДНК-содержащие: вирус Эпштейн. Барра, герпеса; РНК-содержащие: ВИЧ) Наследственная предрасположенность Старение (наибольшее количество злокачественных образований регистрируется в возрастном интервале 55 -74 лет)
Этиология опухолей 1. 2. 3. 4. 5. Физические факторы (УФО, Х и У-лучи) Химические канцерогены (ароматические амины, полициклические ароматические углеводороды) Вирусы (ДНК-содержащие: вирус Эпштейн. Барра, герпеса; РНК-содержащие: ВИЧ) Наследственная предрасположенность Старение (наибольшее количество злокачественных образований регистрируется в возрастном интервале 55 -74 лет)
 Онкоген и протоонкоген Онкоге н — это ген, кодирующий белок, который, в случае нарушения регуляции, может вызвать образование злокачественной опухоли. Протоонкоген — это обычный ген, который может стать онкогеном из-за мутаций или повышения экспрессии. Многие протоонкогены кодируют белки, которые регулируют клеточный рост и дифференцировку. Существует три основных пути активации протоонкогена: мутация внутри протоонкогена, которая меняет структуру белка; повышение концентрации белка ; транслокация (хромосомная перестройка).
Онкоген и протоонкоген Онкоге н — это ген, кодирующий белок, который, в случае нарушения регуляции, может вызвать образование злокачественной опухоли. Протоонкоген — это обычный ген, который может стать онкогеном из-за мутаций или повышения экспрессии. Многие протоонкогены кодируют белки, которые регулируют клеточный рост и дифференцировку. Существует три основных пути активации протоонкогена: мутация внутри протоонкогена, которая меняет структуру белка; повышение концентрации белка ; транслокация (хромосомная перестройка).
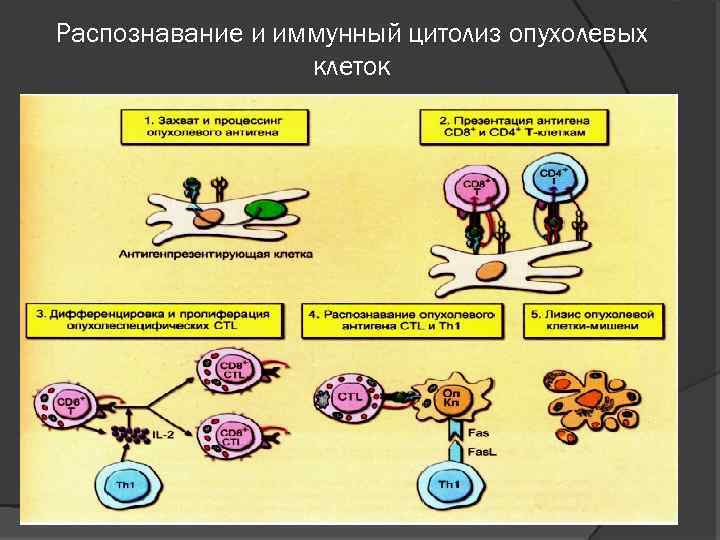 Распознавание и иммунный цитолиз опухолевых клеток
Распознавание и иммунный цитолиз опухолевых клеток
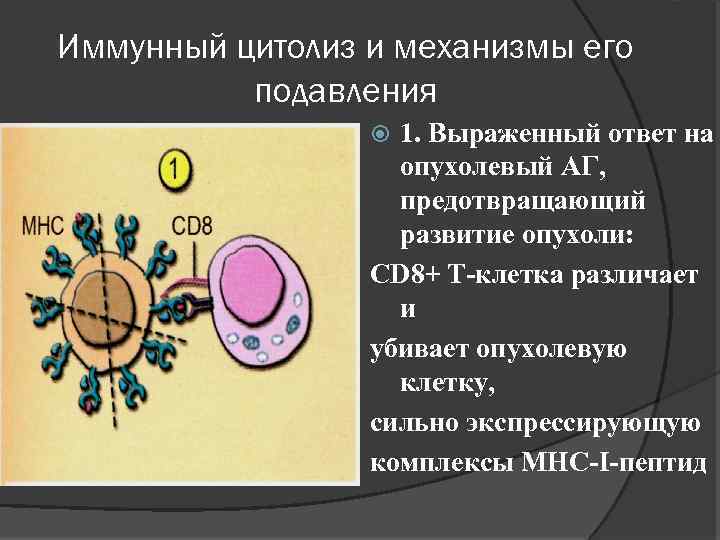 Иммунный цитолиз и механизмы его подавления 1. Выраженный ответ на опухолевый АГ, предотвращающий развитие опухоли: СD 8+ Т-клетка различает и убивает опухолевую клетку, сильно экспрессирующую комплексы МНС-I-пептид
Иммунный цитолиз и механизмы его подавления 1. Выраженный ответ на опухолевый АГ, предотвращающий развитие опухоли: СD 8+ Т-клетка различает и убивает опухолевую клетку, сильно экспрессирующую комплексы МНС-I-пептид
 Иммунный цитолиз и механизмы его подавления 2. СD 8+ Т-клетка игнорирует опухолевую клетку, слабо экспрессирующую комплексы МНС-Iпептид.
Иммунный цитолиз и механизмы его подавления 2. СD 8+ Т-клетка игнорирует опухолевую клетку, слабо экспрессирующую комплексы МНС-Iпептид.
 Иммунный цитолиз и механизмы его подавления 3. Экспрессия комплексов МНС-Iпептид ослабляется под влиянием антител к опухолевому АГ. В результате интернализации комплекса опухолевый АГ (красные кружки) – антитело, СD 8+ Тклетки не распознают опухолевую клетку.
Иммунный цитолиз и механизмы его подавления 3. Экспрессия комплексов МНС-Iпептид ослабляется под влиянием антител к опухолевому АГ. В результате интернализации комплекса опухолевый АГ (красные кружки) – антитело, СD 8+ Тклетки не распознают опухолевую клетку.
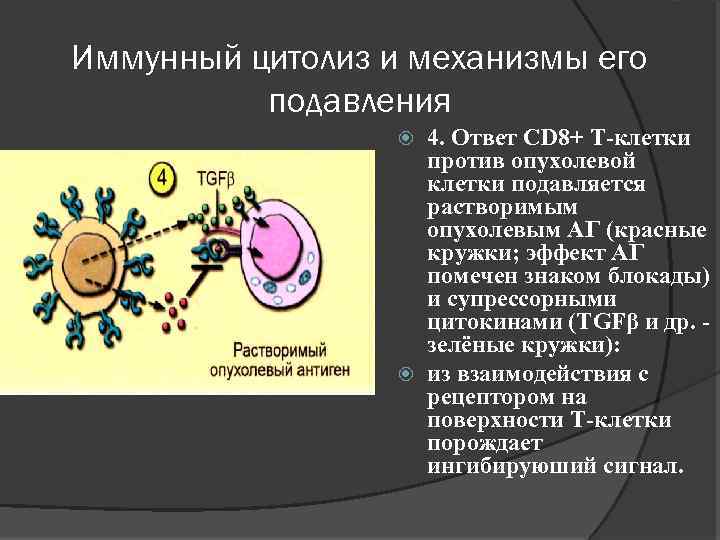 Иммунный цитолиз и механизмы его подавления 4. Ответ СD 8+ Т-клетки против опухолевой клетки подавляется растворимым опухолевым АГ (красные кружки; эффект АГ помечен знаком блокады) и супрессорными цитокинами (ТGFβ и др. зелёные кружки): из взаимодействия с рецептором на поверхности Т-клетки порождает ингибируюший сигнал.
Иммунный цитолиз и механизмы его подавления 4. Ответ СD 8+ Т-клетки против опухолевой клетки подавляется растворимым опухолевым АГ (красные кружки; эффект АГ помечен знаком блокады) и супрессорными цитокинами (ТGFβ и др. зелёные кружки): из взаимодействия с рецептором на поверхности Т-клетки порождает ингибируюший сигнал.
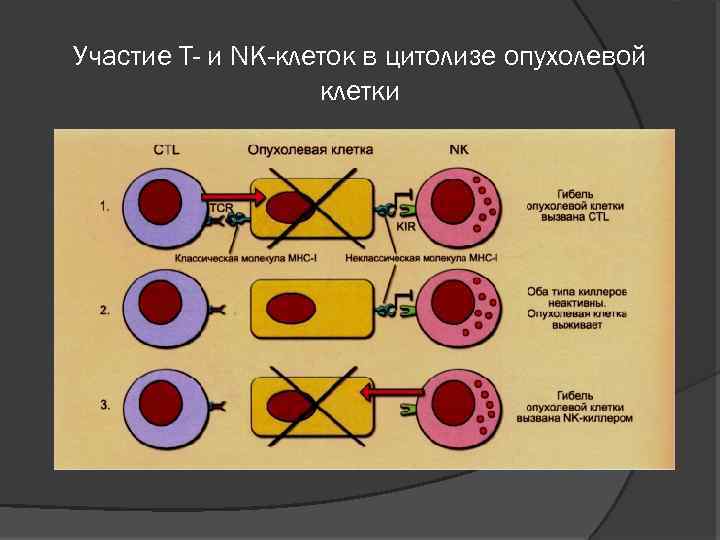 Участие Т- и NK-клеток в цитолизе опухолевой клетки
Участие Т- и NK-клеток в цитолизе опухолевой клетки
 Участие Т- и NK-клеток в цитолизе опухолевой клетки 1. 2. 3. Экспрессия классических молекул МНС класса 1 (у человека - НLА- А, В, С) опухолевой клеткой делает её мишенью цитотоксического действия СВ 8+ цитотоксических Т-лимфоцитов (СТL). Экспрессия неклассических молекул МНС (у чело века - НЕА- F, G, Н) защищает её от цитотоксического действия NK-клеток (запрет повреждения «своего» ). Отсутствие классических и наличие неклассических молекул МНС обеспечивает избегание опухолевой клеткой цитолиза. Отсутствие молекул МНС обоих типов делает клетку чувствительной к действию NK-киллеров.
Участие Т- и NK-клеток в цитолизе опухолевой клетки 1. 2. 3. Экспрессия классических молекул МНС класса 1 (у человека - НLА- А, В, С) опухолевой клеткой делает её мишенью цитотоксического действия СВ 8+ цитотоксических Т-лимфоцитов (СТL). Экспрессия неклассических молекул МНС (у чело века - НЕА- F, G, Н) защищает её от цитотоксического действия NK-клеток (запрет повреждения «своего» ). Отсутствие классических и наличие неклассических молекул МНС обеспечивает избегание опухолевой клеткой цитолиза. Отсутствие молекул МНС обоих типов делает клетку чувствительной к действию NK-киллеров.
 Узнавание опухолевых антигенов Т-клетки способны узнавать опухолевые Аг. После разрушения в клетке Аг (мутантные белки) могут быть представлены цитотоксическим СD 8+ Тклеткам в виде пептидов, связанных с молекулами МНС класса 1. Т-клеточный ответ является НLАзависимым, (подходит ли мутантный опухолевый пептид к участку связывания Аг на молекуле НLА).
Узнавание опухолевых антигенов Т-клетки способны узнавать опухолевые Аг. После разрушения в клетке Аг (мутантные белки) могут быть представлены цитотоксическим СD 8+ Тклеткам в виде пептидов, связанных с молекулами МНС класса 1. Т-клеточный ответ является НLАзависимым, (подходит ли мутантный опухолевый пептид к участку связывания Аг на молекуле НLА).
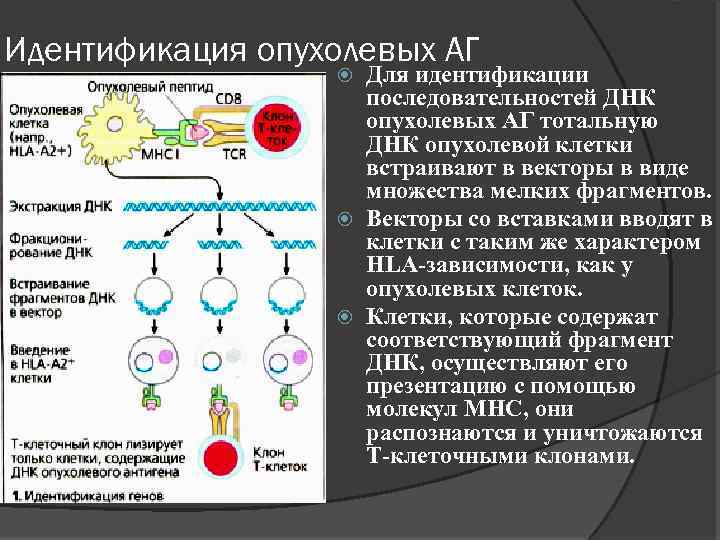 Идентификация опухолевых АГ Для идентификации последовательностей ДНК опухолевых АГ тотальную ДНК опухолевой клетки встраивают в векторы в виде множества мелких фрагментов. Векторы со вставками вводят в клетки с таким же характером НLА-зависимости, как у опухолевых клеток. Клетки, которые содержат соответствующий фрагмент ДНК, осуществляют его презентацию с помощью молекул МНС, они распознаются и уничтожаются Т-клеточными клонами.
Идентификация опухолевых АГ Для идентификации последовательностей ДНК опухолевых АГ тотальную ДНК опухолевой клетки встраивают в векторы в виде множества мелких фрагментов. Векторы со вставками вводят в клетки с таким же характером НLА-зависимости, как у опухолевых клеток. Клетки, которые содержат соответствующий фрагмент ДНК, осуществляют его презентацию с помощью молекул МНС, они распознаются и уничтожаются Т-клеточными клонами.
 Роль NK-клеток в иммунологии опухоли NK-клетка присоединяется к опухолевой клетке через антитела G класса на поверхности опухолевой клетки с участием CD 16. CD 158 молекулы (KIR) на поверхности NK-клеток исполняют роль рецепторов для молекул HLA I класса нормальных клеток. После плотного контакта натурального киллера с опухолевой клеткой осуществляется выброс NKклеткой белков – перфоринов. Взаимодействие CD 16 с Ig. G, активация NK-клеток IL-2, IL-12 приводит к усилению экспрессии FASлиганда (CD 178) на NK-клетках, и уничтожение опухолевой клетки происходит и через взаимодействие CD 178 с рецепторами апоптоза на ней.
Роль NK-клеток в иммунологии опухоли NK-клетка присоединяется к опухолевой клетке через антитела G класса на поверхности опухолевой клетки с участием CD 16. CD 158 молекулы (KIR) на поверхности NK-клеток исполняют роль рецепторов для молекул HLA I класса нормальных клеток. После плотного контакта натурального киллера с опухолевой клеткой осуществляется выброс NKклеткой белков – перфоринов. Взаимодействие CD 16 с Ig. G, активация NK-клеток IL-2, IL-12 приводит к усилению экспрессии FASлиганда (CD 178) на NK-клетках, и уничтожение опухолевой клетки происходит и через взаимодействие CD 178 с рецепторами апоптоза на ней.
 Особая роль натуральных киллеров в противоопухолевом иммунитете подтверждается не только прямыми наблюдениями in vitro, но и сравнительными данными по активности этих клеток у мышей инбредных линий. Различные линии этих животных характеризуются индивидуальным уровнем НК, и этот уровень коррелирует со способностью развивать антиопухолевую защиту. У мышей с высоким уровнем НК спонтанные или индуцируемые опухоли встречаются редко. У мышей с низким исходным уровнем НК частота спонтанных опухолей, напротив, высокая. Трансплантация клеток от линий мышей с высоким уровнем НК линиям с низким содержанием этих клеток обеспечивает защиту последних от некоторых форм опухолей. Клинические данные также демонстрируют связь между уровнем НК в периферичекой крови больных и интенсивностью роста опухоли.
Особая роль натуральных киллеров в противоопухолевом иммунитете подтверждается не только прямыми наблюдениями in vitro, но и сравнительными данными по активности этих клеток у мышей инбредных линий. Различные линии этих животных характеризуются индивидуальным уровнем НК, и этот уровень коррелирует со способностью развивать антиопухолевую защиту. У мышей с высоким уровнем НК спонтанные или индуцируемые опухоли встречаются редко. У мышей с низким исходным уровнем НК частота спонтанных опухолей, напротив, высокая. Трансплантация клеток от линий мышей с высоким уровнем НК линиям с низким содержанием этих клеток обеспечивает защиту последних от некоторых форм опухолей. Клинические данные также демонстрируют связь между уровнем НК в периферичекой крови больных и интенсивностью роста опухоли.
 Роль макрофагов Активированный Т-лимфоцит выделяет γ-IFN. Он подаёт сигнал, мишенью которого является ядро МФ. Этот сигнал вызывает образование синтазы окиси азота, превращающей аргинин в окись азота, которая разрушает опухолевые клетки, подавляя энергообразование в цикле Кребса и при транспорте электронов в митохондриях и синтез ДНК. Производные аргинина, особенно метильные, блокируют образование нитратов в МФ.
Роль макрофагов Активированный Т-лимфоцит выделяет γ-IFN. Он подаёт сигнал, мишенью которого является ядро МФ. Этот сигнал вызывает образование синтазы окиси азота, превращающей аргинин в окись азота, которая разрушает опухолевые клетки, подавляя энергообразование в цикле Кребса и при транспорте электронов в митохондриях и синтез ДНК. Производные аргинина, особенно метильные, блокируют образование нитратов в МФ.
 Опухолевые клетки синтезируют фактор, ингибирующий миграцию макрофагов (MIF). Под действием MIF макрофаги, пришедшие к опухоли, теряют свою подвижность и возможность передать информацию об обнаруженной опухоли другим ИКК. Обездвиженный МФ производит большое количество активатора плазминогена, благодаря чему опухолевые клетки приобретают способность проникать в кровеносное русло и распространяться по организму.
Опухолевые клетки синтезируют фактор, ингибирующий миграцию макрофагов (MIF). Под действием MIF макрофаги, пришедшие к опухоли, теряют свою подвижность и возможность передать информацию об обнаруженной опухоли другим ИКК. Обездвиженный МФ производит большое количество активатора плазминогена, благодаря чему опухолевые клетки приобретают способность проникать в кровеносное русло и распространяться по организму.
 Роль дендритных клеток Большие надежды возлагаются на иммунотерапию больных со злокачественными опухолями при помощи адаптивного переноса дендритных клеток (ДК), которые способны инициировать специфический противоопухолевый иммунный ответ, опосредованный цитотоксическими лимфоцитами. Уникальность функции ДК определяется их способностью к интернализации, процессингу и презентации антигенов наивным Т-лимфоцитам, то есть клеткам, ранее не подвергавшимся воздействию данного антигена. Этой способностью не обладают другие антигенпредставляющие клетки, такие как макрофаги или Влимфоциты. Обычно зрелые ДК получают in vitro из CD 34+ костномозговых предшественников или популяции моноцитов периферической крови. В настоящее время проводятся клинические испытания эффективности адаптивного переноса нагруженных опухолевыми антигенами ДК при метастазирующей меланоме, неходжкинской лимфоме и раке различных локализаций.
Роль дендритных клеток Большие надежды возлагаются на иммунотерапию больных со злокачественными опухолями при помощи адаптивного переноса дендритных клеток (ДК), которые способны инициировать специфический противоопухолевый иммунный ответ, опосредованный цитотоксическими лимфоцитами. Уникальность функции ДК определяется их способностью к интернализации, процессингу и презентации антигенов наивным Т-лимфоцитам, то есть клеткам, ранее не подвергавшимся воздействию данного антигена. Этой способностью не обладают другие антигенпредставляющие клетки, такие как макрофаги или Влимфоциты. Обычно зрелые ДК получают in vitro из CD 34+ костномозговых предшественников или популяции моноцитов периферической крови. В настоящее время проводятся клинические испытания эффективности адаптивного переноса нагруженных опухолевыми антигенами ДК при метастазирующей меланоме, неходжкинской лимфоме и раке различных локализаций.
 Роль В-лимфоцитов При взаимодействии опухолевого антигена и В- лимфоцита, рецептор которого соответствует данному антигену, происходит отбор реагирующих В-лимфоцитов. Они перерабатывают опухолевые антигены и активируются. У активированных Влимфоцитов процессированный Аг представлен на плазматической мембране в комплексе с белком MHC класса II. Зрелая Т-хелперная клетка, прошедшая антигенспецифичную активацию макрофагом с белком MHC класса II, связывается с активированным В-лимфоцитом. Это приводит к выделению Т-хелпером ИЛ-2, под действием которого В-клетка делится и дифференцируется, превращаясь в плазматическую клетку, секретирущую АТ. АТ связываются с антигенами опухоли, но она может терять свои поверхностные АГ. Комплекс АГ-АТ покидает опухолевую клетку раньше, чем происходит активация и полимеризация комплемента. Противоопухолевые АТ и циркулирующие иммунные комплексы усугубляют развитие болезни. Они блокируют антигены опухолевых клеток и рецепторы Т-киллеров.
Роль В-лимфоцитов При взаимодействии опухолевого антигена и В- лимфоцита, рецептор которого соответствует данному антигену, происходит отбор реагирующих В-лимфоцитов. Они перерабатывают опухолевые антигены и активируются. У активированных Влимфоцитов процессированный Аг представлен на плазматической мембране в комплексе с белком MHC класса II. Зрелая Т-хелперная клетка, прошедшая антигенспецифичную активацию макрофагом с белком MHC класса II, связывается с активированным В-лимфоцитом. Это приводит к выделению Т-хелпером ИЛ-2, под действием которого В-клетка делится и дифференцируется, превращаясь в плазматическую клетку, секретирущую АТ. АТ связываются с антигенами опухоли, но она может терять свои поверхностные АГ. Комплекс АГ-АТ покидает опухолевую клетку раньше, чем происходит активация и полимеризация комплемента. Противоопухолевые АТ и циркулирующие иммунные комплексы усугубляют развитие болезни. Они блокируют антигены опухолевых клеток и рецепторы Т-киллеров.
 Роль Т-лимфоцитов Главный элемент активной противоопухолевой защиты - цитотоксические Т-лимфоциты. Незрелой Т-клетке антиген представляет макрофаг с белком HLA класса I. Способность Т-киллеров отвечать на опухолевые клетки также зависит от молекул MHC опухолевой клетки. Т-киллер, связавшись своими рецепторами с опухолевой клеткой, вступает с ней в плотный контакт, для чего необходимы ионы магния, и выбрасывает белки перфорины. Перфорины встраиваются в мембрану опухолевой клетки и в присутствии кальция полимеризуются, образуя каналы, через которые в клетку входит избыточное количество воды, и опухолевая клетка разрывается. Т-киллер уничтожает лишь несколько опухолевых клеток, после чего в нём истощаются запасы энергии и перфоринов, и он погибает сам.
Роль Т-лимфоцитов Главный элемент активной противоопухолевой защиты - цитотоксические Т-лимфоциты. Незрелой Т-клетке антиген представляет макрофаг с белком HLA класса I. Способность Т-киллеров отвечать на опухолевые клетки также зависит от молекул MHC опухолевой клетки. Т-киллер, связавшись своими рецепторами с опухолевой клеткой, вступает с ней в плотный контакт, для чего необходимы ионы магния, и выбрасывает белки перфорины. Перфорины встраиваются в мембрану опухолевой клетки и в присутствии кальция полимеризуются, образуя каналы, через которые в клетку входит избыточное количество воды, и опухолевая клетка разрывается. Т-киллер уничтожает лишь несколько опухолевых клеток, после чего в нём истощаются запасы энергии и перфоринов, и он погибает сам.
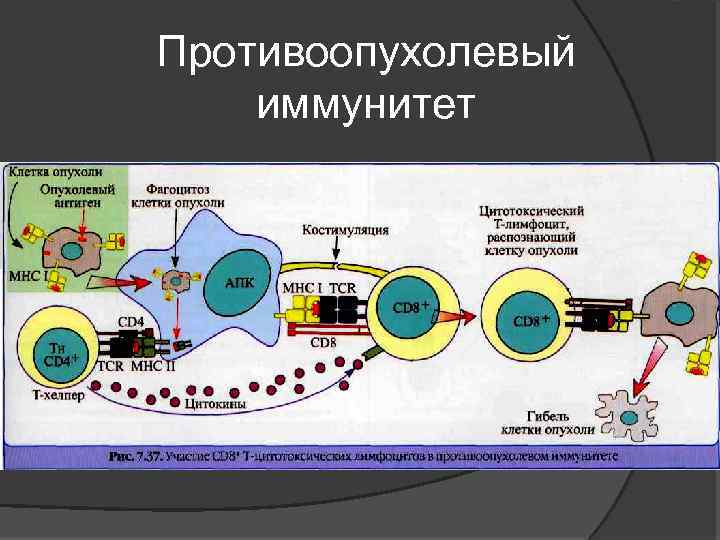 Противоопухолевый иммунитет
Противоопухолевый иммунитет
 Роль антител Противоопухолевые антитела не всегда играют защитную роль, а иногда даже стимулируют развитие опухоли. Это, видимо, связано с тем, что специфические иммуноглобулины связывают антигенные рецепторы опухолевой клетки, тем самым препятствуя контакту Т-лимфоцитовкиллеров с клеткой. Адоптивный перенос иммунных Т-лимфоцитов в интактный организм сообщает противоопухолевый иммунитет. Пассивный перенос противоопухолевых антител иммунитета не сообщает.
Роль антител Противоопухолевые антитела не всегда играют защитную роль, а иногда даже стимулируют развитие опухоли. Это, видимо, связано с тем, что специфические иммуноглобулины связывают антигенные рецепторы опухолевой клетки, тем самым препятствуя контакту Т-лимфоцитовкиллеров с клеткой. Адоптивный перенос иммунных Т-лимфоцитов в интактный организм сообщает противоопухолевый иммунитет. Пассивный перенос противоопухолевых антител иммунитета не сообщает.
 Причины «ускользания» опухоли от иммунного ответа • маскировка опухолевых антигенов избытком антител или иммунных комплексов, вырабатываемых иммунной системой хозяина опухоли; • снижение или полную блокаду Ткиллеров антителами иммунной системы хозяина опухоли к противоопухолевым антигенам; • снижение «уровня презентации» опухолевых антигенов макрофагами, приводящее к угнетению продукции противоопухолевых цитокинов (ФНО, интерфероны и т. д. ) макрофагами.
Причины «ускользания» опухоли от иммунного ответа • маскировка опухолевых антигенов избытком антител или иммунных комплексов, вырабатываемых иммунной системой хозяина опухоли; • снижение или полную блокаду Ткиллеров антителами иммунной системы хозяина опухоли к противоопухолевым антигенам; • снижение «уровня презентации» опухолевых антигенов макрофагами, приводящее к угнетению продукции противоопухолевых цитокинов (ФНО, интерфероны и т. д. ) макрофагами.
 Механизмы избегания опухолями иммунного отторжения
Механизмы избегания опухолями иммунного отторжения
 Опухоль избегает агрессии со стороны организма, используя следующие механизмы: синтез и секреция цитокинов, блокирующих функции лимфоцитов (TGF-β, IL-10); секреция ганглиозидов, блокирующих передачу сигнала в клетке, в интерстициальное пространство (GD la, GD 2, GD 3, GM 1, GM 2); синтез и секреция факторов периферической селекции Тh, «переключающих» иммунный ответ с клеточного пути на гуморальный (IL-4);
Опухоль избегает агрессии со стороны организма, используя следующие механизмы: синтез и секреция цитокинов, блокирующих функции лимфоцитов (TGF-β, IL-10); секреция ганглиозидов, блокирующих передачу сигнала в клетке, в интерстициальное пространство (GD la, GD 2, GD 3, GM 1, GM 2); синтез и секреция факторов периферической селекции Тh, «переключающих» иммунный ответ с клеточного пути на гуморальный (IL-4);
 Иммунодиагностика
Иммунодиагностика
 Иммунодиагностика опухолей основана на определении в крови опухолевых антигенов и антител, а также сенсибилизированных к опухолевым антигенам лимфоцитов. Таким способом уже диагностируют опухоли печени, рак желудка, кишечника и др. Качество диагностики возрастает при использовании моноклональных антител против антигенов опухолей.
Иммунодиагностика опухолей основана на определении в крови опухолевых антигенов и антител, а также сенсибилизированных к опухолевым антигенам лимфоцитов. Таким способом уже диагностируют опухоли печени, рак желудка, кишечника и др. Качество диагностики возрастает при использовании моноклональных антител против антигенов опухолей.
 Иммунодиагностика
Иммунодиагностика
 Биохимические сдвиги увеличение содержания мочевины при нормальной концентрации креатинина свидетельствует об интенсивном распаде опухоли, а при повышенной его концентрации - о нарушении функции почек; снижение содержания глюкозы; увеличение содержания общего белка (при снижении концентрации альбумина) - характерный признак миеломной болезни
Биохимические сдвиги увеличение содержания мочевины при нормальной концентрации креатинина свидетельствует об интенсивном распаде опухоли, а при повышенной его концентрации - о нарушении функции почек; снижение содержания глюкозы; увеличение содержания общего белка (при снижении концентрации альбумина) - характерный признак миеломной болезни
 Молекулярная диагностика опухолей повышение активности щелочной фосфатазы свидетельствует о нарушении функции печени, в частности, в результате появления в ней метастазов гипопротеинемия и гипоальбуминемия - показатель общего воздействия опухоли на организм как следствие снижения синтеза белка и усиленного его распада.
Молекулярная диагностика опухолей повышение активности щелочной фосфатазы свидетельствует о нарушении функции печени, в частности, в результате появления в ней метастазов гипопротеинемия и гипоальбуминемия - показатель общего воздействия опухоли на организм как следствие снижения синтеза белка и усиленного его распада.
 Молекулярная диагностика опухолей Опухолевые маркеры - это вещества, образующиеся в связи с измененным метаболизмом злокачественно трансформированной клетки, при возникновении опухоли их уровни повышаются. Определение опухолевых маркеров проводят в гистологическом материале или в биологических жидкостях (гормональные опухолевые маркеры).
Молекулярная диагностика опухолей Опухолевые маркеры - это вещества, образующиеся в связи с измененным метаболизмом злокачественно трансформированной клетки, при возникновении опухоли их уровни повышаются. Определение опухолевых маркеров проводят в гистологическом материале или в биологических жидкостях (гормональные опухолевые маркеры).
 Молекулярная диагностика опухолей Классификация опухолевых маркеров По химической природе: гликопротеины, полипептиды, углеводные детерминанты гликопротеинов, гликолипиды, белки, полиамины, иммуноглобулины и др. По биологической функции: онкофетальные антигены, энзимы (фукозилтрансфераза), гормоны (АКТГ, плацентарный лактоген, пролактин), рецепторы (прогестероновые, эстрогеновые) и др. соединения (ферритин, иммуноглобулины)
Молекулярная диагностика опухолей Классификация опухолевых маркеров По химической природе: гликопротеины, полипептиды, углеводные детерминанты гликопротеинов, гликолипиды, белки, полиамины, иммуноглобулины и др. По биологической функции: онкофетальные антигены, энзимы (фукозилтрансфераза), гормоны (АКТГ, плацентарный лактоген, пролактин), рецепторы (прогестероновые, эстрогеновые) и др. соединения (ферритин, иммуноглобулины)
 Молекулярная диагностика опухолей По современной классификации, опухолевые маркеры: первичные опухолево-ассоциированные; вторичные, продуцируемые опухолью (специфические и неспецифические); вторичные, индуцируемые опухолевым процессом.
Молекулярная диагностика опухолей По современной классификации, опухолевые маркеры: первичные опухолево-ассоциированные; вторичные, продуцируемые опухолью (специфические и неспецифические); вторичные, индуцируемые опухолевым процессом.
 Молекулярная диагностика опухолей Опухолевые маркеры используют в следующих случаях: A) скрининг Б) оценка эффективности терапии B) прогноз Г) длительное наблюдение с целью раннего выявления рецидивов и генерализации заболевания.
Молекулярная диагностика опухолей Опухолевые маркеры используют в следующих случаях: A) скрининг Б) оценка эффективности терапии B) прогноз Г) длительное наблюдение с целью раннего выявления рецидивов и генерализации заболевания.
 Молекулярная диагностика опухолей ДНК-диагностика Раннее выявление опухолей наиболее часто основывается на определении мутаций Ras и p 53, обнаружение которых позволяет в некоторых случаях судить о стадии опухолевого процесса. Микросателлитные маркеры высоко эффективны в ранней диагностике рака мочевого пузыря и простаты. Широкий спектр опухолей может быть диагностирован с использованием протоколов активности телоизомеразы. Широкое применение находит определение HPV вирусов при раке шейки матки и молекулярных тестов для выявления мутаций онкогенов непосредственно на гистологических срезах. ДНК-тестирование применяется при наследуемых опухолях: ретинобластоме, полипозе кишечника, множественных эндокринных опухолях второго типа (MEN 2), раке молочной железы и яичников (BRCA 1, BRCA 2).
Молекулярная диагностика опухолей ДНК-диагностика Раннее выявление опухолей наиболее часто основывается на определении мутаций Ras и p 53, обнаружение которых позволяет в некоторых случаях судить о стадии опухолевого процесса. Микросателлитные маркеры высоко эффективны в ранней диагностике рака мочевого пузыря и простаты. Широкий спектр опухолей может быть диагностирован с использованием протоколов активности телоизомеразы. Широкое применение находит определение HPV вирусов при раке шейки матки и молекулярных тестов для выявления мутаций онкогенов непосредственно на гистологических срезах. ДНК-тестирование применяется при наследуемых опухолях: ретинобластоме, полипозе кишечника, множественных эндокринных опухолях второго типа (MEN 2), раке молочной железы и яичников (BRCA 1, BRCA 2).
 Моноклональные АТ CEA (Carcino-embrional antigen) - ракоэмбриональный АГ; MUC-1 - муцин 1, СА-125, Lех - АГ группы крови Lех ; ЕGF-R — рецептор эпидермального фактора роста, тип 1; НЕR 2/Neu — продукт онкогена neu; IL-2 R — рецептор ИЛ- 2; FАРα (Fetal α-protein) — альфафетопротеин.
Моноклональные АТ CEA (Carcino-embrional antigen) - ракоэмбриональный АГ; MUC-1 - муцин 1, СА-125, Lех - АГ группы крови Lех ; ЕGF-R — рецептор эпидермального фактора роста, тип 1; НЕR 2/Neu — продукт онкогена neu; IL-2 R — рецептор ИЛ- 2; FАРα (Fetal α-protein) — альфафетопротеин.
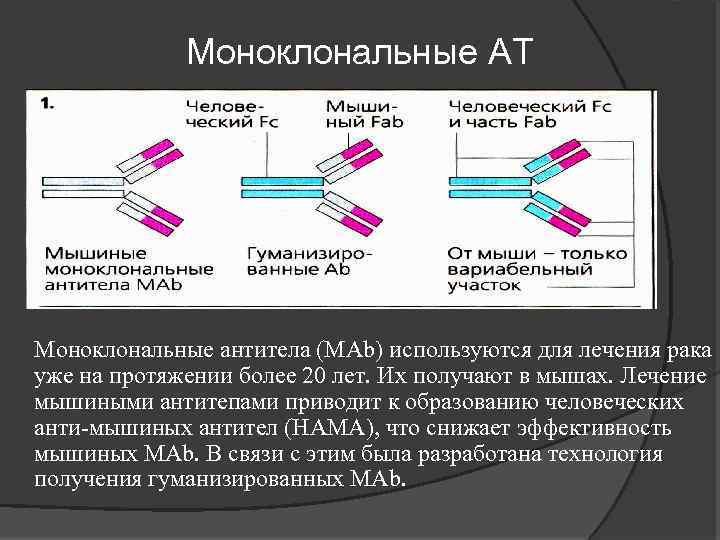 Моноклональные АТ n Моноклональные антитела (МAb) используются для лечения рака уже на протяжении более 20 лет. Их получают в мышах. Лечение мышиными антитепами приводит к образованию человеческих анти-мышиных антител (НАМА), что снижает эффективность мышиных МАb. В связи с этим была разработана технология получения гуманизированных МАb.
Моноклональные АТ n Моноклональные антитела (МAb) используются для лечения рака уже на протяжении более 20 лет. Их получают в мышах. Лечение мышиными антитепами приводит к образованию человеческих анти-мышиных антител (НАМА), что снижает эффективность мышиных МАb. В связи с этим была разработана технология получения гуманизированных МАb.
 моноклональные АТ Для устранения иммуногенности моноклональных Ат с помощью методов генной инженерии в их молекуле замещают наиболее иммуногенную часть * * — С-домены или С-домены и каркасную последовательность V-доменов (остаются лишь три гипервариабельных участка в Vдоменах Н- и L-цепей). Возможно лишь проявление иммуногенности идиотопов, которая свойственна и аутологичным антителам.
моноклональные АТ Для устранения иммуногенности моноклональных Ат с помощью методов генной инженерии в их молекуле замещают наиболее иммуногенную часть * * — С-домены или С-домены и каркасную последовательность V-доменов (остаются лишь три гипервариабельных участка в Vдоменах Н- и L-цепей). Возможно лишь проявление иммуногенности идиотопов, которая свойственна и аутологичным антителам.
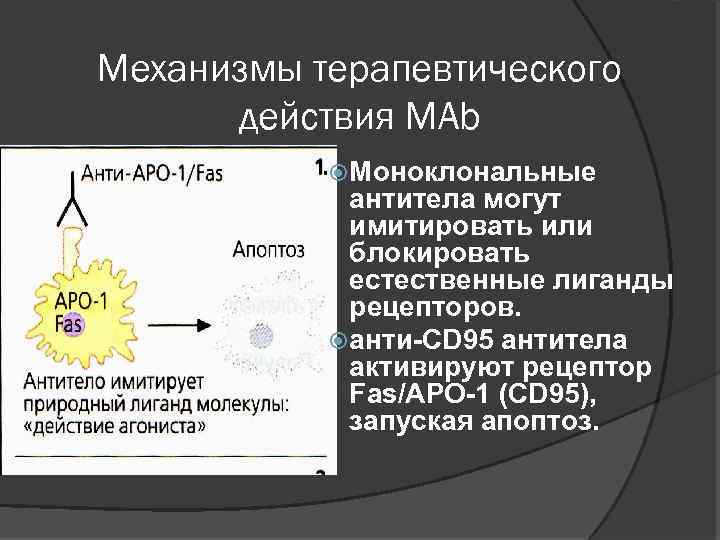 Механизмы терапевтического действия МАb Моноклональные антитела могут имитировать или блокировать естественные лиганды рецепторов. анти-CD 95 антитела активируют рецептор Fas/AРО-1 (CD 95), запуская апоптоз.
Механизмы терапевтического действия МАb Моноклональные антитела могут имитировать или блокировать естественные лиганды рецепторов. анти-CD 95 антитела активируют рецептор Fas/AРО-1 (CD 95), запуская апоптоз.
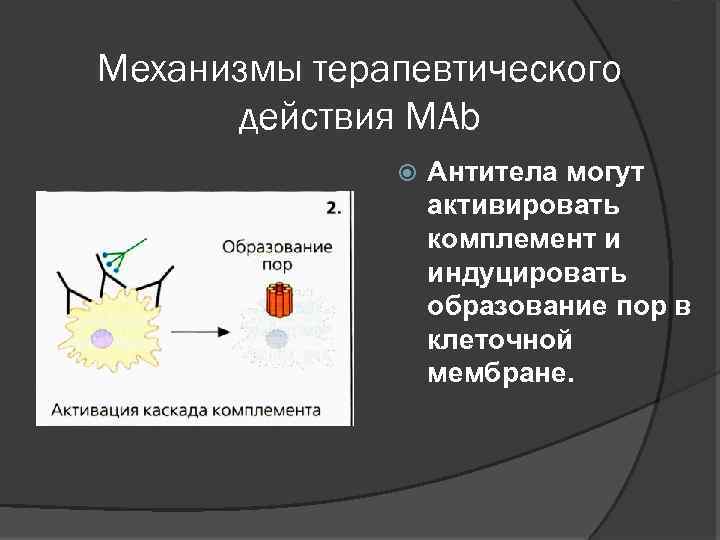 Механизмы терапевтического действия МАb Антитела могут активировать комплемент и индуцировать образование пор в клеточной мембране.
Механизмы терапевтического действия МАb Антитела могут активировать комплемент и индуцировать образование пор в клеточной мембране.
 Механизмы терапевтического действия МАb При АЗКЦ клеткикиллеры, несущие Fсрецепторы, узнают Fсфрагмент связанных с клеткой Ат, что приводит к высвобождению цитоплазматических гранул, содержащих цитотоксические перфорины и гранзимы
Механизмы терапевтического действия МАb При АЗКЦ клеткикиллеры, несущие Fсрецепторы, узнают Fсфрагмент связанных с клеткой Ат, что приводит к высвобождению цитоплазматических гранул, содержащих цитотоксические перфорины и гранзимы
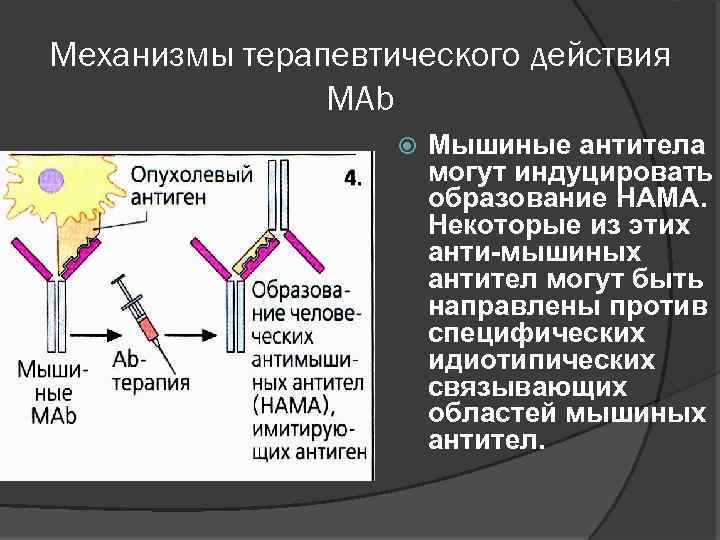 Механизмы терапевтического действия МАb Мышиные антитела могут индуцировать образование НАМА. Некоторые из этих анти-мышиных антител могут быть направлены против специфических идиотипических связывающих областей мышиных антител.
Механизмы терапевтического действия МАb Мышиные антитела могут индуцировать образование НАМА. Некоторые из этих анти-мышиных антител могут быть направлены против специфических идиотипических связывающих областей мышиных антител.
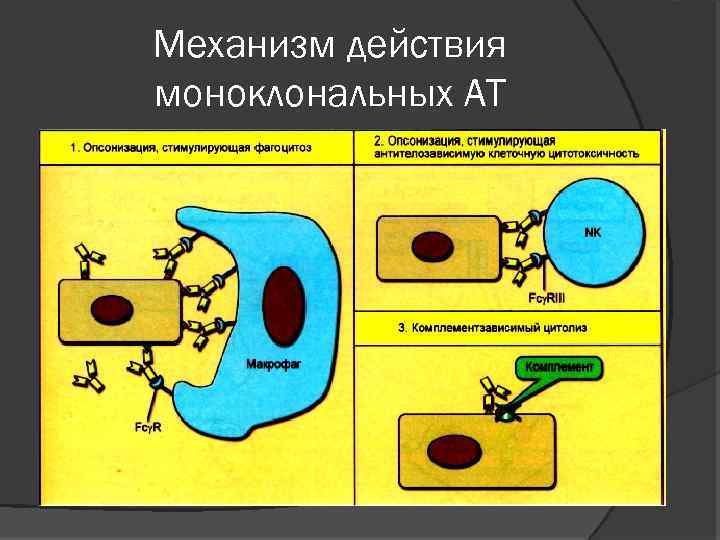 Механизм действия моноклональных АТ
Механизм действия моноклональных АТ
 Механизм действия моноклональных АТ Моноклональные антитела оказывают противоовухолевое действие по механизму антителозависимого клеточного цитолиза, опосредованного МФ (1) или NK-клетками (2). Оба типа эффекторных клеток распознают Fс-часть антител, связавшихся с опухолевым АГ, с помощью Fсрецепторов (FсγI, II и III на МФ и FсγIII на NKклетках). Для МФ это служит сигналом для фагоцитоза или внутриклеточного цитолиза клетки-мишени, для NK-клеток - для контактного цитолиза. Комллементзависимый цитолиз опухолевых клеток (3) не играет существенной роли в реализации лечебного действия антител, так как мембрана опухолевых клеток располагает факторами, инактивирующими компоненты С’.
Механизм действия моноклональных АТ Моноклональные антитела оказывают противоовухолевое действие по механизму антителозависимого клеточного цитолиза, опосредованного МФ (1) или NK-клетками (2). Оба типа эффекторных клеток распознают Fс-часть антител, связавшихся с опухолевым АГ, с помощью Fсрецепторов (FсγI, II и III на МФ и FсγIII на NKклетках). Для МФ это служит сигналом для фагоцитоза или внутриклеточного цитолиза клетки-мишени, для NK-клеток - для контактного цитолиза. Комллементзависимый цитолиз опухолевых клеток (3) не играет существенной роли в реализации лечебного действия антител, так как мембрана опухолевых клеток располагает факторами, инактивирующими компоненты С’.
 Иммунотерапия
Иммунотерапия
 Задачи иммунотерапии в онкологии Базисная иммунотерапия опухолей с целью получения непосредственного противоопухолевого эффекта. Снижение побочных эффектов традиционной противоопухолевой терапии: - лечение миелосупрессии - лечение иммуносупрессии - коррекция общетоксического действия - антиоксидантный эффект Профилактика рецидивов опухоли и возникновения новых других опухолей. Профилактика и лечение сопуствующих инфекционных осложнений (вирусные, бактериальные и грибковые инфекции).
Задачи иммунотерапии в онкологии Базисная иммунотерапия опухолей с целью получения непосредственного противоопухолевого эффекта. Снижение побочных эффектов традиционной противоопухолевой терапии: - лечение миелосупрессии - лечение иммуносупрессии - коррекция общетоксического действия - антиоксидантный эффект Профилактика рецидивов опухоли и возникновения новых других опухолей. Профилактика и лечение сопуствующих инфекционных осложнений (вирусные, бактериальные и грибковые инфекции).
 Виды иммунотерапии В зависимости от метода и механизма иммунологического действия иммунотерапию опухолей разделяют на: активную; пассивную; специфическую; неспецифическую; Комбинированную.
Виды иммунотерапии В зависимости от метода и механизма иммунологического действия иммунотерапию опухолей разделяют на: активную; пассивную; специфическую; неспецифическую; Комбинированную.
 Активная специфическая терапия Вакцины из инактивированных или модифицированных опухолевых клеток, опухолевые клеточные экстракты, очищенные или рекомбинантные опухолевые антигены, идиотипы, вирусные или бактериальные гены-векторы, внедряемые в опухоль. Вакцинация против онкогенных вирусов - гепатита В, вирусов папиломмы, Т-клеточного лейкоза человека (HTLV-1), вируса Эпштейн-Барра.
Активная специфическая терапия Вакцины из инактивированных или модифицированных опухолевых клеток, опухолевые клеточные экстракты, очищенные или рекомбинантные опухолевые антигены, идиотипы, вирусные или бактериальные гены-векторы, внедряемые в опухоль. Вакцинация против онкогенных вирусов - гепатита В, вирусов папиломмы, Т-клеточного лейкоза человека (HTLV-1), вируса Эпштейн-Барра.
 Активная неспецифическая терапия БЦЖ, "Имурон", Corynobacterium parvum, цитокины (альфа, бета, гамма ИФНы, ИЛ-1, ИЛ-2, ИЛ-12, ФНО), Леакадин, Левамизол (Декарис), препараты гормонов тимуса, мурамилдипептид, димеколат трегалозы, сополимер пирана, ДЭМА, поли-(I: C), пиримидины, MGN-3.
Активная неспецифическая терапия БЦЖ, "Имурон", Corynobacterium parvum, цитокины (альфа, бета, гамма ИФНы, ИЛ-1, ИЛ-2, ИЛ-12, ФНО), Леакадин, Левамизол (Декарис), препараты гормонов тимуса, мурамилдипептид, димеколат трегалозы, сополимер пирана, ДЭМА, поли-(I: C), пиримидины, MGN-3.
 Активная комбинированная терапия Сочетание вакцинотерапии с цитокинами или неспецифическими иммуностимуляторами.
Активная комбинированная терапия Сочетание вакцинотерапии с цитокинами или неспецифическими иммуностимуляторами.
 Пассивная специфическая терапия Антитела, чистые или конъюгированные с лекарственными средствами, пролекарствами, токсинами или радиоизотопами; биоспецифичные антитела; Тклетки, дендритные клетки.
Пассивная специфическая терапия Антитела, чистые или конъюгированные с лекарственными средствами, пролекарствами, токсинами или радиоизотопами; биоспецифичные антитела; Тклетки, дендритные клетки.
 Пассивная неспецифическая терапия ЛАК терапия, цитокины (ИЛ-1, ИЛ-2, ФНО, интерфероны), лектины (Iscador), белки теплового шока
Пассивная неспецифическая терапия ЛАК терапия, цитокины (ИЛ-1, ИЛ-2, ФНО, интерфероны), лектины (Iscador), белки теплового шока
 Пассивная комбинированная терапия ЛАК терапия совместно с биоспецифичными антителами
Пассивная комбинированная терапия ЛАК терапия совместно с биоспецифичными антителами
 Направления и средства иммунотерапии
Направления и средства иммунотерапии
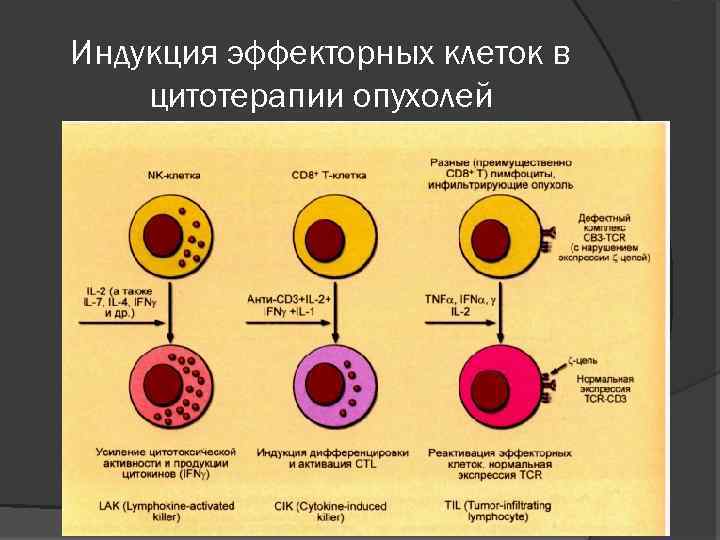 Индукция эффекторных клеток в цитотерапии опухолей
Индукция эффекторных клеток в цитотерапии опухолей
 Лечение онкологических больных радикальное хирургическое удаление опухоли химиотерапия (алкилирующие агенты, повреждающие ДНК, антиметаболиты, которые ингибируют синтез нуклеиновых кислот, антибиотики, гормоны и природные соединения) радиотерапия симптоматическое лечение Новые направления в лечении опухолей: фотодинамическая терапия направленная доставка лекарств в клетки-мишени подавление ангиогенеза генная терапия иммунотерапия
Лечение онкологических больных радикальное хирургическое удаление опухоли химиотерапия (алкилирующие агенты, повреждающие ДНК, антиметаболиты, которые ингибируют синтез нуклеиновых кислот, антибиотики, гормоны и природные соединения) радиотерапия симптоматическое лечение Новые направления в лечении опухолей: фотодинамическая терапия направленная доставка лекарств в клетки-мишени подавление ангиогенеза генная терапия иммунотерапия
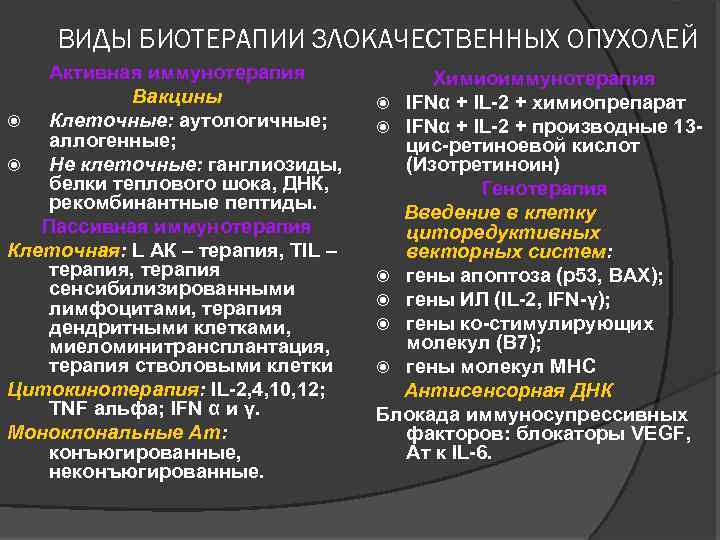 ВИДЫ БИОТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ Активная иммунотерапия Вакцины Клеточные: аутологичные; аллогенные; Не клеточные: ганглиозиды, белки теплового шока, ДНК, рекомбинантные пептиды. Пассивная иммунотерапия Клеточная: L АК – терапия, TIL – терапия, терапия сенсибилизированными лимфоцитами, терапия дендритными клетками, миеломинитрансплантация, терапия стволовыми клетки Цитокинотерапия: IL-2, 4, 10, 12; TNF альфа; IFN α и γ. Моноклональные Ат: конъюгированные, неконъюгированные. Химиоиммунотерапия IFNα + IL-2 + химиопрепарат IFNα + IL-2 + производные 13 цис-ретиноевой кислот (Изотретиноин) Генотерапия Введение в клетку циторедуктивных векторных систем: гены апоптоза (р53, ВАХ); гены ИЛ (IL-2, IFN-γ); гены ко-стимулирующих молекул (В 7); гены молекул МНС Антисенсорная ДНК Блокада иммуносупрессивных факторов: блокаторы VEGF, Ат к IL-6.
ВИДЫ БИОТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ Активная иммунотерапия Вакцины Клеточные: аутологичные; аллогенные; Не клеточные: ганглиозиды, белки теплового шока, ДНК, рекомбинантные пептиды. Пассивная иммунотерапия Клеточная: L АК – терапия, TIL – терапия, терапия сенсибилизированными лимфоцитами, терапия дендритными клетками, миеломинитрансплантация, терапия стволовыми клетки Цитокинотерапия: IL-2, 4, 10, 12; TNF альфа; IFN α и γ. Моноклональные Ат: конъюгированные, неконъюгированные. Химиоиммунотерапия IFNα + IL-2 + химиопрепарат IFNα + IL-2 + производные 13 цис-ретиноевой кислот (Изотретиноин) Генотерапия Введение в клетку циторедуктивных векторных систем: гены апоптоза (р53, ВАХ); гены ИЛ (IL-2, IFN-γ); гены ко-стимулирующих молекул (В 7); гены молекул МНС Антисенсорная ДНК Блокада иммуносупрессивных факторов: блокаторы VEGF, Ат к IL-6.
 Методы клеточной иммунотерапии LAK-терапия (Lymphokine–activated killers) - метод иммунотерапии, основанный на использовании полученных от больного лимфокинактивированных киллеров - лимфоцитов, большая часть из которых представлена NK, культивируемыми в присутствии интерлейкина-2. TIL-терапия (Tumor-infiltrating lymphocytes) - метод иммунотерапии, основанный на использовании полученных от больного лимфоцитов, которые инфильтрируют опухоль и содержат в своем составе разные субпопуляции клеток.
Методы клеточной иммунотерапии LAK-терапия (Lymphokine–activated killers) - метод иммунотерапии, основанный на использовании полученных от больного лимфокинактивированных киллеров - лимфоцитов, большая часть из которых представлена NK, культивируемыми в присутствии интерлейкина-2. TIL-терапия (Tumor-infiltrating lymphocytes) - метод иммунотерапии, основанный на использовании полученных от больного лимфоцитов, которые инфильтрируют опухоль и содержат в своем составе разные субпопуляции клеток.
 Методы клеточной иммунотерапии Терапия сенсибилизированными лимфоцитами - метод, основанный на использовании полученных от больного лимфоцитов, которые вне организма подвергаются ионизирующему облучению, воздействию ультрафиолетовых лучей или каких-либо других физических факторов, вызывающих активацию клеток. Терапия дендритными клетками - использование полученных от больного и культивируемых вне организма дендритных клеток.
Методы клеточной иммунотерапии Терапия сенсибилизированными лимфоцитами - метод, основанный на использовании полученных от больного лимфоцитов, которые вне организма подвергаются ионизирующему облучению, воздействию ультрафиолетовых лучей или каких-либо других физических факторов, вызывающих активацию клеток. Терапия дендритными клетками - использование полученных от больного и культивируемых вне организма дендритных клеток.
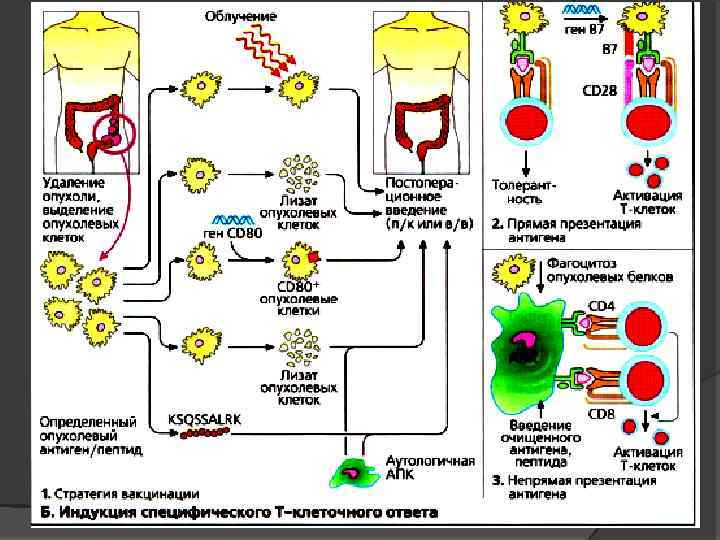
 Индукция специфического Т-клеточного ответа У многих пациентов хирургическое вмешательство в момент постановки диагноза может успешно уничтожить первичную опухоль. Однако у некоторых из этих пациентов через какое-то время будут образовываться отдаленные метастазы или произойдет повторное возникновение опухоли. Пациентам с факторами риска (тип опухоли, степень злокачественности, глубина проникновения опухоли, вовлечение лимфатических узлов и др. ) показано проведение адъювантной терапии. В большинстве случаев пока не удается индуцировать специфический Т-клеточный ответ на опухоль путем введения облученных аутологичных опухолевых клеток или лизатов опухолевых клеток. Вместе с лизатами опухолевых клеток, очищенными опухолевыми АГ или специфическими опухолевыми пептидами можно ввести дендритные клетки, образованные ех vivo.
Индукция специфического Т-клеточного ответа У многих пациентов хирургическое вмешательство в момент постановки диагноза может успешно уничтожить первичную опухоль. Однако у некоторых из этих пациентов через какое-то время будут образовываться отдаленные метастазы или произойдет повторное возникновение опухоли. Пациентам с факторами риска (тип опухоли, степень злокачественности, глубина проникновения опухоли, вовлечение лимфатических узлов и др. ) показано проведение адъювантной терапии. В большинстве случаев пока не удается индуцировать специфический Т-клеточный ответ на опухоль путем введения облученных аутологичных опухолевых клеток или лизатов опухолевых клеток. Вместе с лизатами опухолевых клеток, очищенными опухолевыми АГ или специфическими опухолевыми пептидами можно ввести дендритные клетки, образованные ех vivo.
 Цитокинотерапия
Цитокинотерапия
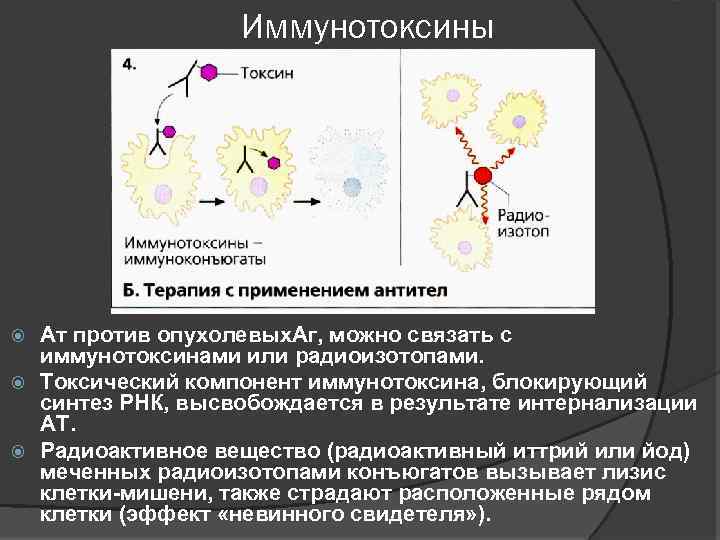 Иммунотоксины Ат против опухолевых. Аг, можно связать с иммунотоксинами или радиоизотопами. Токсический компонент иммунотоксина, блокирующий синтез РНК, высвобождается в результате интернализации АТ. Радиоактивное вещество (радиоактивный иттрий или йод) меченных радиоизотопами конъюгатов вызывает лизис клетки-мишени, также страдают расположенные рядом клетки (эффект «невинного свидетеля» ).
Иммунотоксины Ат против опухолевых. Аг, можно связать с иммунотоксинами или радиоизотопами. Токсический компонент иммунотоксина, блокирующий синтез РНК, высвобождается в результате интернализации АТ. Радиоактивное вещество (радиоактивный иттрий или йод) меченных радиоизотопами конъюгатов вызывает лизис клетки-мишени, также страдают расположенные рядом клетки (эффект «невинного свидетеля» ).
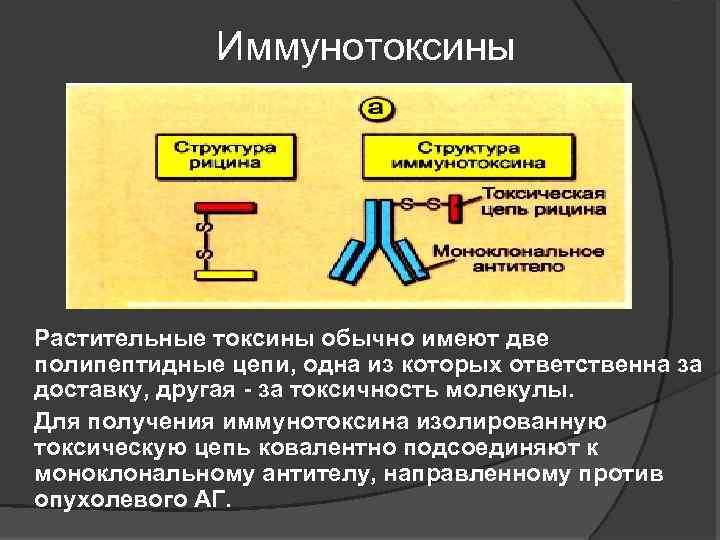 Иммунотоксины n n Растительные токсины обычно имеют две полипептидные цепи, одна из которых ответственна за доставку, другая - за токсичность молекулы. Для получения иммунотоксина изолированную токсическую цепь ковалентно подсоединяют к моноклональному антителу, направленному против опухолевого АГ.
Иммунотоксины n n Растительные токсины обычно имеют две полипептидные цепи, одна из которых ответственна за доставку, другая - за токсичность молекулы. Для получения иммунотоксина изолированную токсическую цепь ковалентно подсоединяют к моноклональному антителу, направленному против опухолевого АГ.
 Доставка токсина в клетку n n Связывание иммунотокисна с мембранным АГ Интернализация комплекса в составе эндосомы. Токсическая субъединица иммунотоксина поступает в цитозоль, Реализация токсического действия гибель клетки.
Доставка токсина в клетку n n Связывание иммунотокисна с мембранным АГ Интернализация комплекса в составе эндосомы. Токсическая субъединица иммунотоксина поступает в цитозоль, Реализация токсического действия гибель клетки.
 Специфический цитолиз n Иммунотоксин вызывает специфический цитолиз опухолевой клетки, несущей АГ, против которого направлены моноклональные антитела.
Специфический цитолиз n Иммунотоксин вызывает специфический цитолиз опухолевой клетки, несущей АГ, против которого направлены моноклональные антитела.
 Противоопухолевые вакцины Противоопухолевая вакцинация — это способ создания активного специфического противоопухолевого иммунитета в организме с помощью вакцины, содержащей иммуногенные антигены.
Противоопухолевые вакцины Противоопухолевая вакцинация — это способ создания активного специфического противоопухолевого иммунитета в организме с помощью вакцины, содержащей иммуногенные антигены.
 Противоопухолевые вакцины могут включать в свой состав целые опухолевые клетки либо только их антигены. В зависимости от их состава и, следовательно, механизма формирования иммунного ответа противоопухолевые вакцины классифицируются следующим образом: – Вакцины на основе целых клеток: - аутологичные; - аллогенные. – Антигенные вакцины: – белки или фрагменты белков опухолевых клеток; – ДНК и РНК-содержащие вакцины; – рекомбинантные вирусы; – антиидиотипические вакцины. – Вакцины на основе дендритных клеток.
Противоопухолевые вакцины могут включать в свой состав целые опухолевые клетки либо только их антигены. В зависимости от их состава и, следовательно, механизма формирования иммунного ответа противоопухолевые вакцины классифицируются следующим образом: – Вакцины на основе целых клеток: - аутологичные; - аллогенные. – Антигенные вакцины: – белки или фрагменты белков опухолевых клеток; – ДНК и РНК-содержащие вакцины; – рекомбинантные вирусы; – антиидиотипические вакцины. – Вакцины на основе дендритных клеток.
 В случае клеточных вакцин опухолевые клетки берутся непосредственно у пациента и выращиваются в специальных условиях. Существует два типа клеточных противоопухолевых вакцин. — Аутологичные клеточные вакцины содержат собственные клетки пациента (предварительно инактивированные). — Аллогенные клеточные вакцины изготовлены из целых инактивированных клеток другого пациента или представляют собой комбинацию из клеток нескольких пациентов.
В случае клеточных вакцин опухолевые клетки берутся непосредственно у пациента и выращиваются в специальных условиях. Существует два типа клеточных противоопухолевых вакцин. — Аутологичные клеточные вакцины содержат собственные клетки пациента (предварительно инактивированные). — Аллогенные клеточные вакцины изготовлены из целых инактивированных клеток другого пациента или представляют собой комбинацию из клеток нескольких пациентов.
 Антигенные вакцины не содержат в своем составе целых клеток, а только антигены опухолевых клеток. С лечебной целью используют как ДК, нагруженные опухолевым АГ in vitro (в этом случае индукция СТL происходит in vivo) или СТL, индуцированные in vitro. В обоих случаях именно СТL реализуют цитолиз опухолевых клеток.
Антигенные вакцины не содержат в своем составе целых клеток, а только антигены опухолевых клеток. С лечебной целью используют как ДК, нагруженные опухолевым АГ in vitro (в этом случае индукция СТL происходит in vivo) или СТL, индуцированные in vitro. В обоих случаях именно СТL реализуют цитолиз опухолевых клеток.
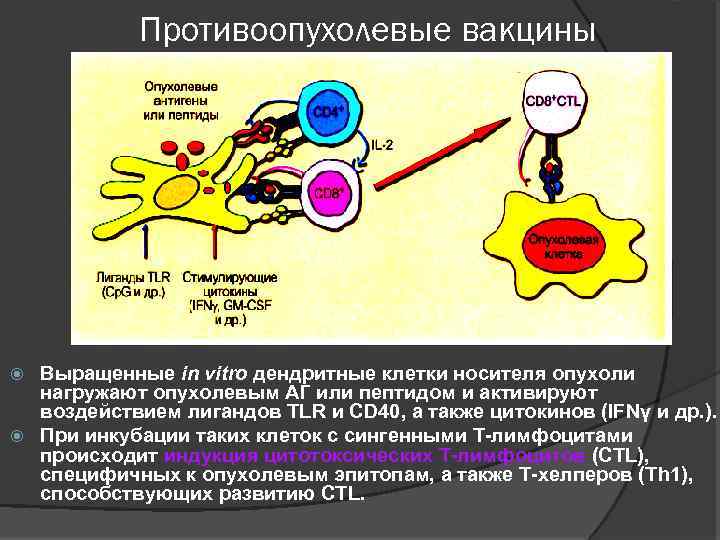 Противоопухолевые вакцины Выращенные in vitro дендритные клетки носителя опухоли нагружают опухолевым АГ или пептидом и активируют воздействием лигандов ТLR и СD 40, а также цитокинов (IFNγ и др. ). При инкубации таких клеток с сингенными Т-лимфоцитами происходит индукция цитотоксических Т-лимфоцитов (СТL), специфичных к опухолевым эпитопам, а также Т-хелперов (Тh 1), способствующих развитию СТL.
Противоопухолевые вакцины Выращенные in vitro дендритные клетки носителя опухоли нагружают опухолевым АГ или пептидом и активируют воздействием лигандов ТLR и СD 40, а также цитокинов (IFNγ и др. ). При инкубации таких клеток с сингенными Т-лимфоцитами происходит индукция цитотоксических Т-лимфоцитов (СТL), специфичных к опухолевым эпитопам, а также Т-хелперов (Тh 1), способствующих развитию СТL.


