2 стом противоопух.транспл иммунитет.ppt
- Количество слайдов: 108

Противоопухолевый и трансплантационный иммунитет профессор Бажукова Т. А. зав. каф. микробиологии, вирусологии и иммунологии
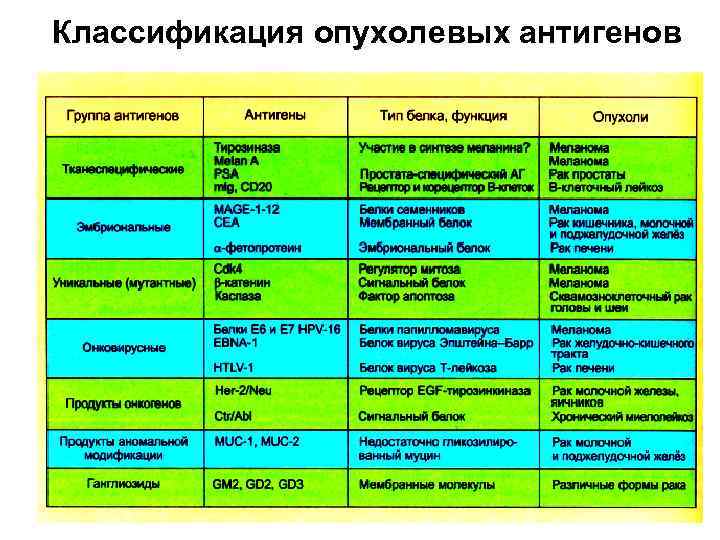
Классификация опухолевых антигенов
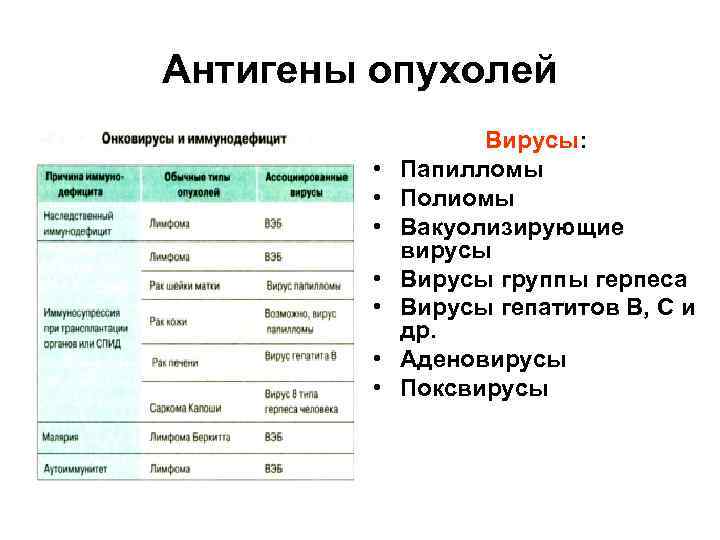
Антигены опухолей • • Вирусы: Папилломы Полиомы Вакуолизирующие вирусы Вирусы группы герпеса Вирусы гепатитов В, С и др. Аденовирусы Поксвирусы
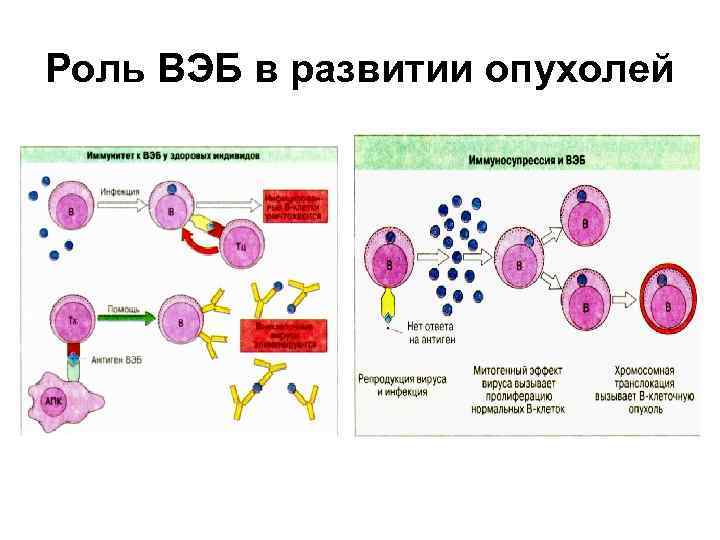
Роль ВЭБ в развитии опухолей

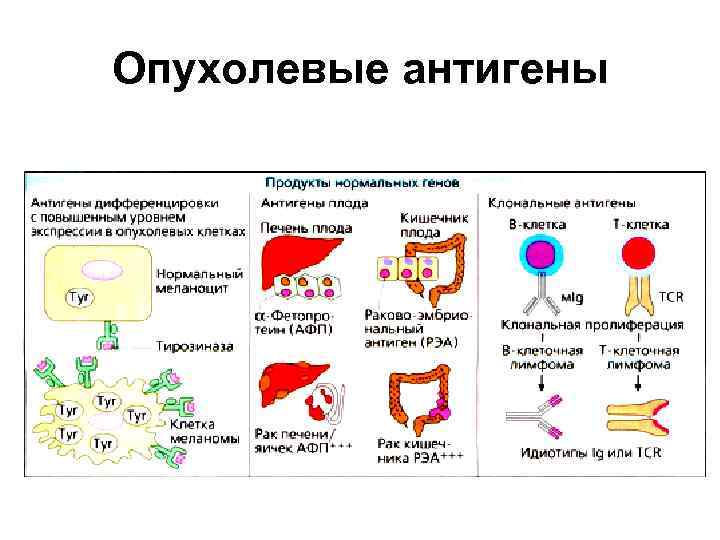
Опухолевые антигены
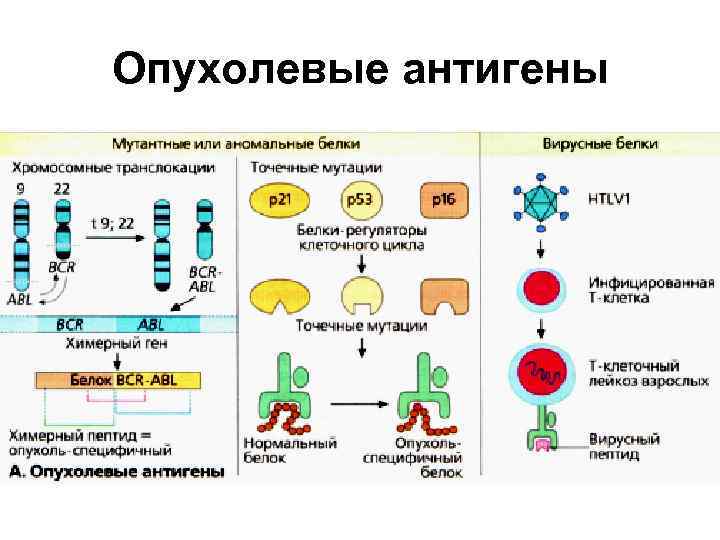
Опухолевые антигены

Узнавание опухолевых антигенов • Т-клетки способны узнавать опухолевые Аг. После разрушения в клетке Аг (мутантные белки) презентируются ТСD 8+ лимфоцитам в виде пептидов, связанных с молекулами МНС-1 класса. • Т-клеточный ответ является НLАзависимым. • Опухолевые клетки осуществляют презентацию антигена с низкой эффективностью, поскольку лишены важных ко-стимулирующих молекул.
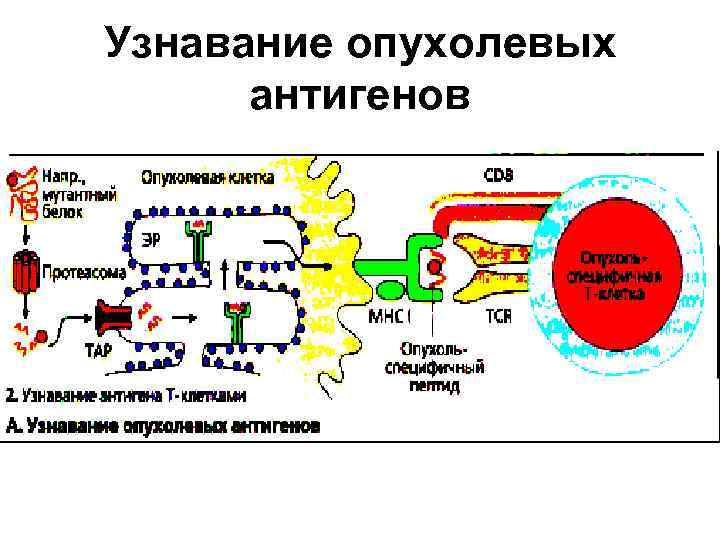
Узнавание опухолевых антигенов
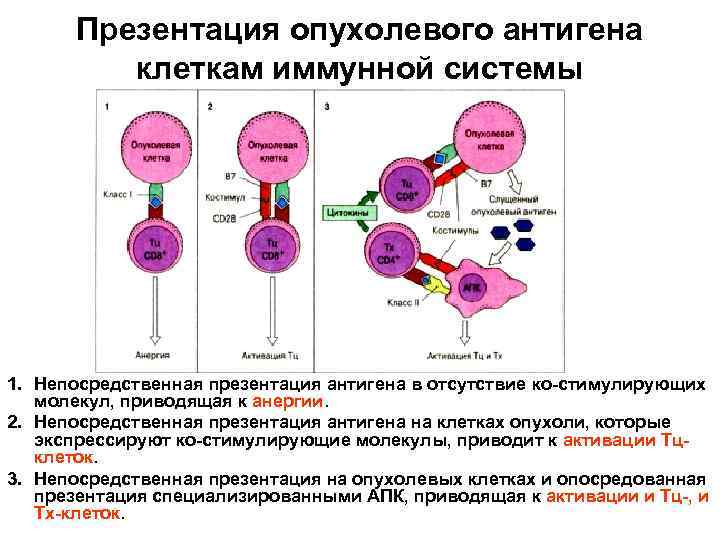
Презентация опухолевого антигена клеткам иммунной системы 1. Непосредственная презентация антигена в отсутствие ко-стимулирующих молекул, приводящая к анергии. 2. Непосредственная презентация антигена на клетках опухоли, которые экспрессируют ко-стимулирующие молекулы, приводит к активации Тцклеток. 3. Непосредственная презентация на опухолевых клетках и опосредованная презентация специализированными АПК, приводящая к активации и Тц-, и Тх-клеток.

Противоопухолевый иммунитет
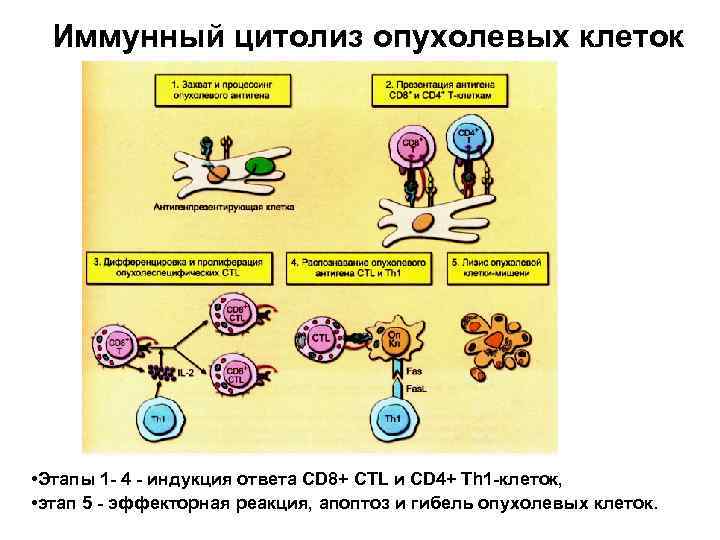
Иммунный цитолиз опухолевых клеток • Этапы 1 - 4 - индукция ответа CD 8+ CTL и СD 4+ Th 1 -клеток, • этап 5 - эффекторная реакция, апоптоз и гибель опухолевых клеток.
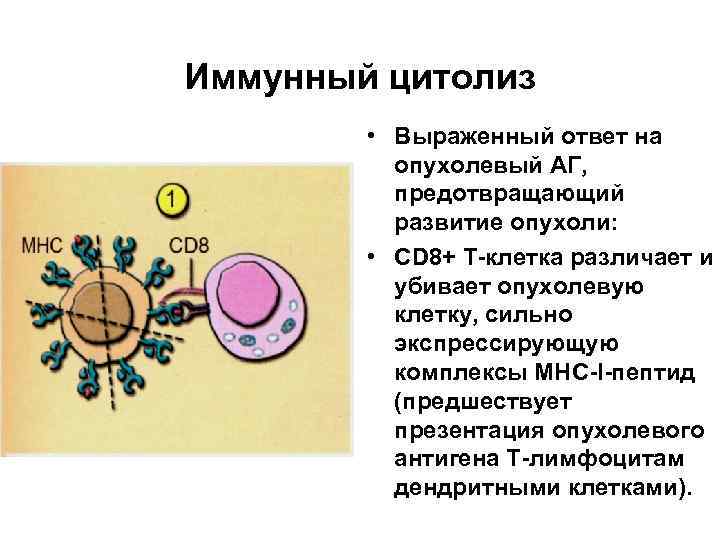
Иммунный цитолиз • Выраженный ответ на опухолевый АГ, предотвращающий развитие опухоли: • СD 8+ Т-клетка различает и убивает опухолевую клетку, сильно экспрессирующую комплексы МНС-I-пептид (предшествует презентация опухолевого антигена Т-лимфоцитам дендритными клетками).

Механизмы избегания опухолями иммунного ответа
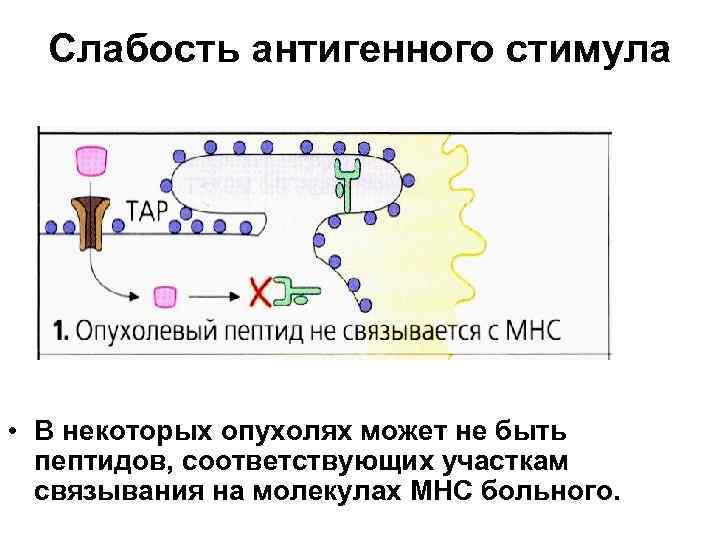
Слабость антигенного стимула • В некоторых опухолях может не быть пептидов, соответствующих участкам связывания на молекулах МНС больного.
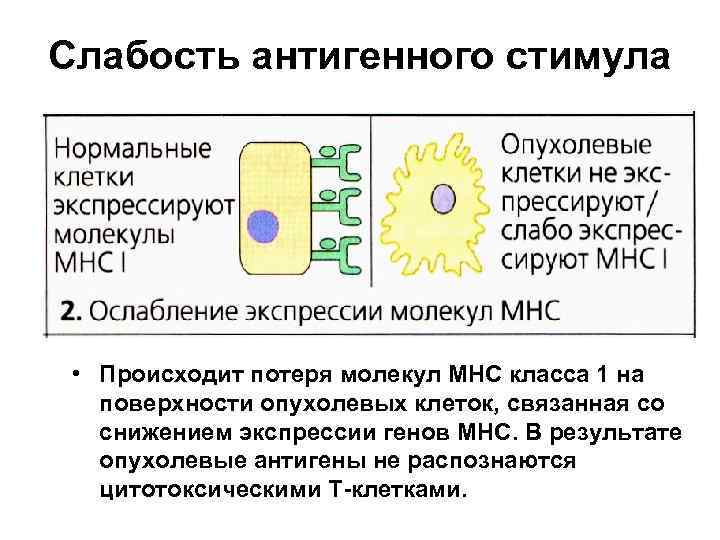
Слабость антигенного стимула • Происходит потеря молекул МНС класса 1 на поверхности опухолевых клеток, связанная со снижением экспрессии генов МНС. В результате опухолевые антигены не распознаются цитотоксическими Т-клетками.
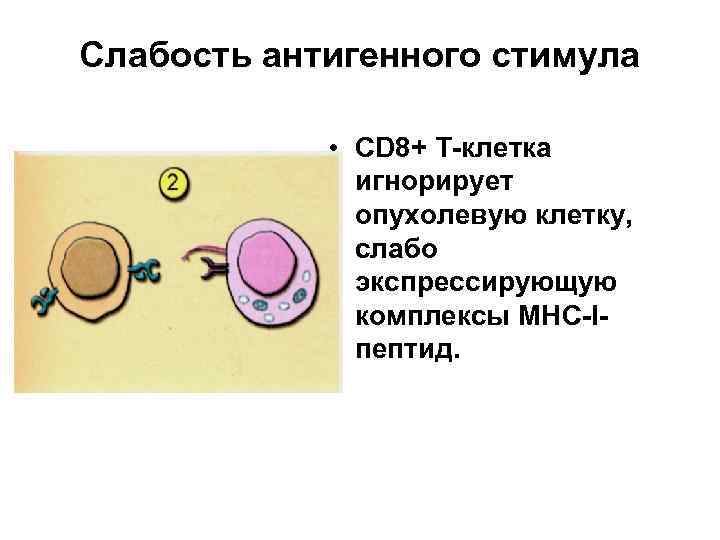
Слабость антигенного стимула • СD 8+ Т-клетка игнорирует опухолевую клетку, слабо экспрессирующую комплексы МНС-Iпептид.
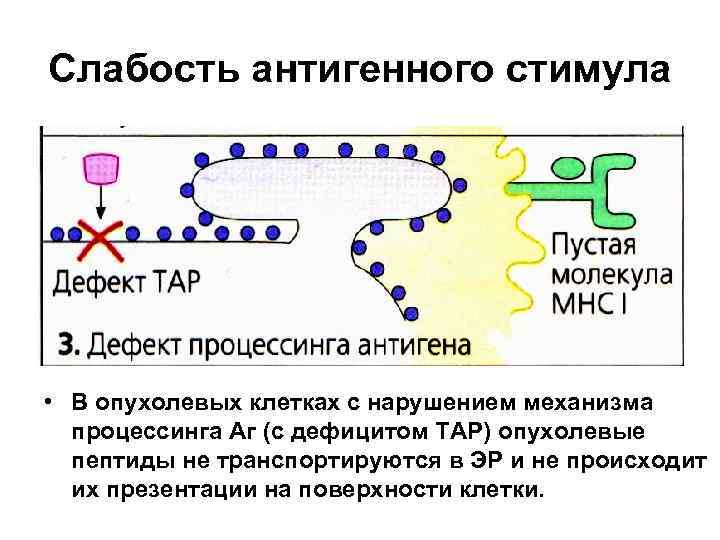
Слабость антигенного стимула • В опухолевых клетках с нарушением механизма процессинга Аг (с дефицитом ТАР) опухолевые пептиды не транспортируются в ЭР и не происходит их презентации на поверхности клетки.

Слабость антигенного стимула • Экспрессия комплексов МНС-Iпептид ослабляется под влиянием антител к опухолевому АГ. • В результате интернализации комплекса опухолевый АГ – антитело, СD 8+ Тклетки не распознают опухолевую клетку.
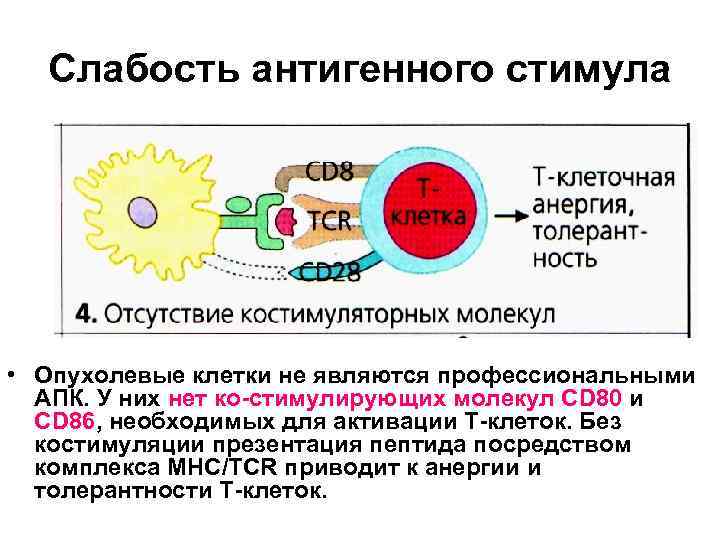
Слабость антигенного стимула • Опухолевые клетки не являются профессиональными АПК. У них нет ко-стимулирующих молекул СD 80 и СD 86, необходимых для активации Т-клеток. Без костимуляции презентация пептида посредством комплекса МНС/ТСR приводит к анергии и толерантности Т-клеток.
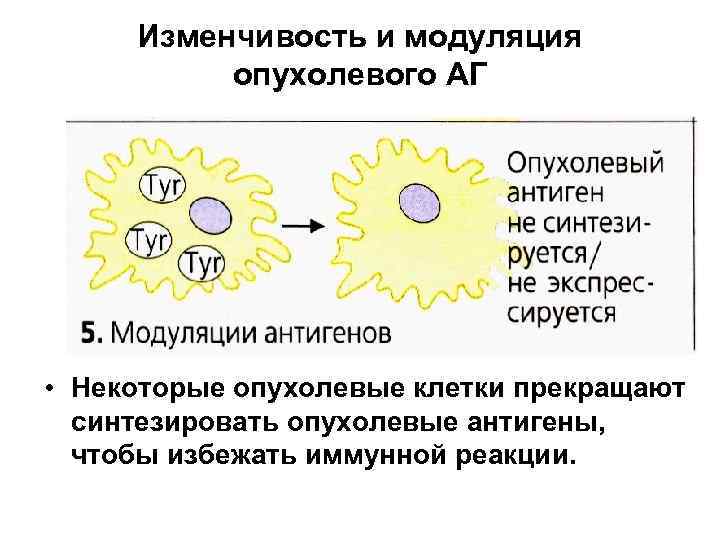
Изменчивость и модуляция опухолевого АГ • Некоторые опухолевые клетки прекращают синтезировать опухолевые антигены, чтобы избежать иммунной реакции.
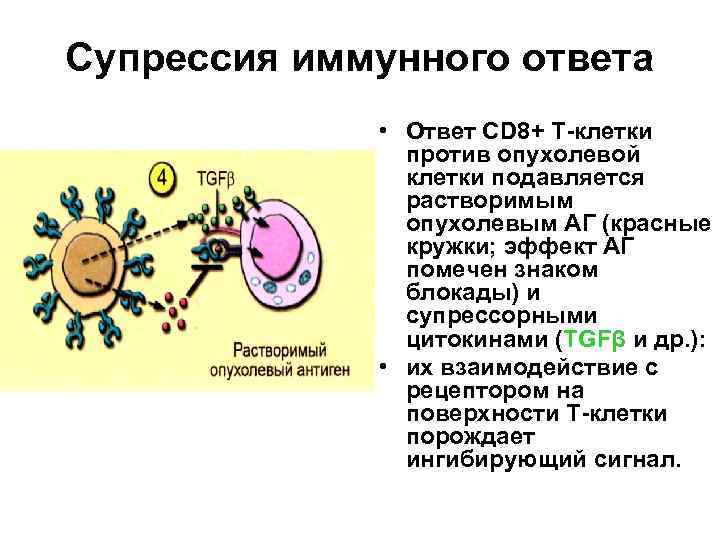
Супрессия иммунного ответа • Ответ СD 8+ Т-клетки против опухолевой клетки подавляется растворимым опухолевым АГ (красные кружки; эффект АГ помечен знаком блокады) и супрессорными цитокинами (ТGFβ и др. ): • их взаимодействие с рецептором на поверхности Т-клетки порождает ингибирующий сигнал.
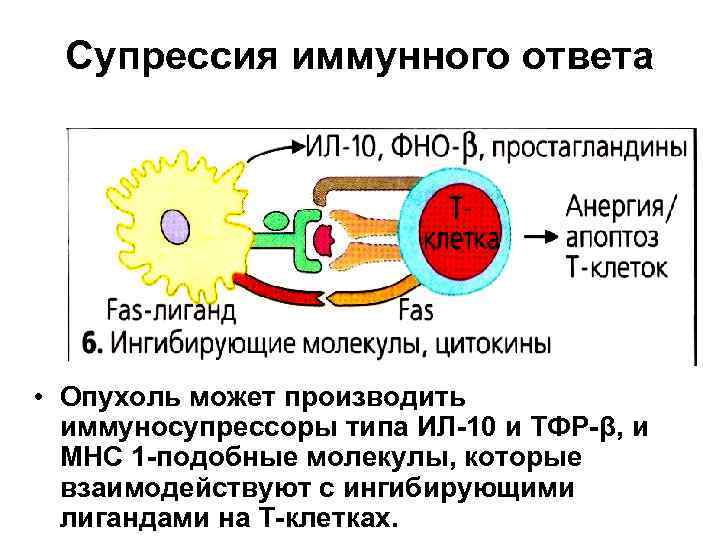
Супрессия иммунного ответа • Опухоль может производить иммуносупрессоры типа ИЛ-10 и ТФР-β, и МНС 1 -подобные молекулы, которые взаимодействуют с ингибирующими лигандами на Т-клетках.

Особенности противоопухолевого иммунитета • Низкая иммуногенность опухолевых клеток • Отсутствие воспалительной реакции в месте онкогенеза • Иммуносупрессивная активность ряда «негативных» цитокинов (βТФР) • Экранирование раковых клеток от антител

Особенности противоопухолевого иммунитета • Основную роль играют активированные макрофаги • Естественные киллеры • Образование антител анти-Fab, анти-Fc

Диагностика опухолей • Комплексная лабораторная биохимическая и иммунологическая диагностика строится на определении • опухолевых маркеров, • гормонов, • биологически активных соединений, • изоформ ферментов, • метаболитов костного ремоделирования в случае метастатического поражения костей.

Диагностика опухолей • Современные иммуноморфологические и цитологические исследования позволяют изучать биоптаты не только самой опухоли, но и различных выделений (мокроты, мочи, асцитической жидкости).

Диагностика опухолей Биохимические сдвиги • увеличение содержания мочевины при нормальной концентрации креатинина свидетельствует об интенсивном распаде опухоли, а при повышенной его концентрации - о нарушении функции почек; • снижение содержания глюкозы указывает на значительную утилизацию глюкозы опухолевыми клетками (при лимфосаркоме и некоторых быстро растущих опухолях у детей); • увеличение содержания общего белка (при снижении концентрации альбумина) - характерный признак миеломной болезни; снижение содержания общего белка и альбумина обнаруживается у онкологических больных при поражении печени метастазами и в ряде других случаев как отражение общего действия опухоли на организм;

Молекулярная диагностика опухолей • повышение активности щелочной фосфатазы свидетельствует о нарушении функции печени, в частности, в результате появления в ней метастазов (появление избыточных количеств фермента в крови может быть также следствием его гиперпродукции клетками остеогенной саркомы); • гипопротеинемия и гипоальбуминемия показатель общего воздействия опухоли на организм как следствие снижения синтеза белка и усиленного его распада.

Молекулярная диагностика опухолей • Опухолевые маркеры - это вещества, образующиеся в связи с измененным метаболизмом злокачественно трансформированной клетки, при возникновении опухоли их уровни повышаются. Определение опухолевых маркеров проводят в гистологическом материале или в биологических жидкостях (гормональные опухолевые маркеры). • Современные биохимические и иммунологические методы позволяют выявить новообразования, когда минимальный уровень секретируемого опухолью маркера — от одного до нескольких фемтомолей (в пересчете на 1 мл сыворотки крови). Большая эффективность использования опухолевых маркеров в клинике может быть достигнута путем комбинации разных тестов.

Молекулярная диагностика опухолей Классификация опухолевых маркеров • • По химической природе: гликопротеины, полипептиды, углеводные детерминанты гликопротеинов, гликолипиды, белки, полиамины, иммуноглобулины и др.

Классификация опухолевых маркеров • По биологической функции: • онкофетальные антигены (РЭА, α 1 -фетопротеин, ХГЧ, специфический β 1 -протеин беременности, СА 125, СА 153, СА 19 -9, СА 50, СА 72 -4), • энзимы (фукозилтрансфераза, кислая фосфатаза простаты, лактатдегидрогеназа, нейронспецифическая енолаза, тимидинкиназа, тимидилатсинтетаза, специфический антиген простаты), • гормоны (АКТГ, антидиуретический гормон, плацентарный лактоген, паратгормон, пролактин, кальцитонин), • рецепторы (прогестероновые, эстрогеновые) и • другие соединения (ферритин, β-2 -микроглобулин, иммуноглобулины, тканевой полипептидный специфический антиген, ЦИФРА 21 -1, тканевый полипептидный антиген)

Молекулярная диагностика опухолей Опухолевые маркеры используют в следующих случаях: A) скрининг Б) оценка эффективности терапии B) прогноз Г) длительное наблюдение с целью раннего выявления рецидивов и генерализации заболевания.

Молекулярная диагностика опухолей ДНК-диагностика • Раннее выявление опухолей наиболее часто основывается на определении мутаций Ras и p 53, обнаружение которых позволяет в некоторых случаях судить о стадии опухолевого процесса. • Информативным ранним маркером рака толстой кишки служат мутации гена АРС, обнаруживаемые более чем в 70% аденом. • Микросателлитные маркеры высоко эффективны в ранней диагностике рака мочевого пузыря и простаты. Широкий спектр опухолей может быть диагностирован с использованием протоколов активности телоизомеразы. • Широкое применение находит определение HPV вирусов при раке шейки матки и молекулярных тестов для выявления мутаций онкогенов непосредственно на гистологических срезах. • ДНК-тестирование применяется при наследуемых опухолях: ретинобластоме, полипозе кишечника, множественных эндокринных опухолях второго типа (MEN 2), раке молочной железы и яичников (BRCA 1, BRCA 2).

Направления и средства иммунотерапии

Направления и средства иммунотерапии • Первоначальные подходы основывались на традиционных методах вакцинации. • Современные подходы к иммунотерапии опухолей основываются на использовании клеточных и молекулярно-биологических технологий. • LAK (Lymphokine - activated killers) - киллеры, активированные лимфокинами; • СIК (Суtokine-induced killers) - киллеры, активированные цитокинами; • TIL (Tumor-infiltrating lymphocytes) лимфоциты, инфильтрирующие опухоль.
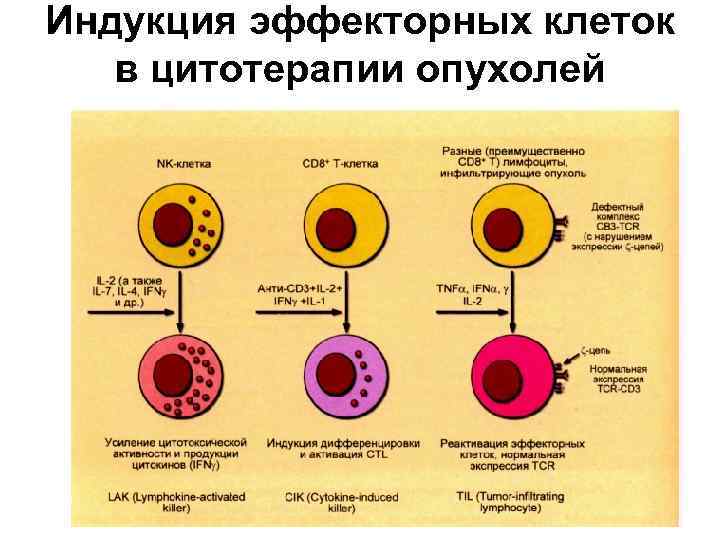
Индукция эффекторных клеток в цитотерапии опухолей

Методы клеточной иммунотерапии • LAK-терапия (Lymphokine–activated killers) метод иммунотерапии, основанный на использовании полученных от больного лимфокинактивированных киллеров лимфоцитов, большая часть из которых представлена NK, культивируемыми в присутствии интерлейкина-2. • TIL-терапия (Tumor-infiltrating lymphocytes) метод иммунотерапии, основанный на использовании полученных от больного лимфоцитов, которые инфильтрируют опухоль и содержат в своем составе разные субпопуляции клеток.

Методы клеточной иммунотерапии • Терапия сенсибилизированными лимфоцитами - метод, основанный на использовании полученных от больного лимфоцитов, которые вне организма подвергаются ионизирующему облучению, воздействию ультрафиолетовых лучей или каких-либо других физических факторов, вызывающих активацию клеток. • Терапия дендритными клетками использование полученных от больного и культивируемых вне организма дендритных клеток.

Усиление неспецифического иммунитета • В конце ХIХ в. американский хирург Уильям Колей вводил больным лизаты опухолевых клеток, которые были заражены бактериями из-за не разработанности методик стерильной работы. У некоторых пациентов лроисходила регрессия опухоли. • В ХХ в. опыт с противоопухолевой вакцинации был вновь повторен, использование немодифицированных опухолевых клеток не приводило к возникновению ощутимого иммунного ответа. • Вскоре в вакцину стали добавлять адъюванты. Сначала использовали ослабленные штаммы микобактерий: бациллу Кальметта-Герена (БЦЖ) и Corynebacterium parvum. В более поздних экспериментах для этой цели пытались использовать вирус ньюкастлской болезни. • Некоторые положительные данные указывают на возможность применения усовершенствованных методов вакцинации в будущем.

Усиление неспецифического иммунитета • В последние годы были проведены работы по генетической модификации опухолевых клеток с целью достичь селективной индукции Т-клеточного иммунного ответа. • Стимуляция локального роста Т-клеток или дендритных клеток путем секреции цитокинов (ИЛ-З, ИЛ-4, ИЛ- 7 и ГМ-КСФ) для активации специфичных к опухоли Т-клеток.
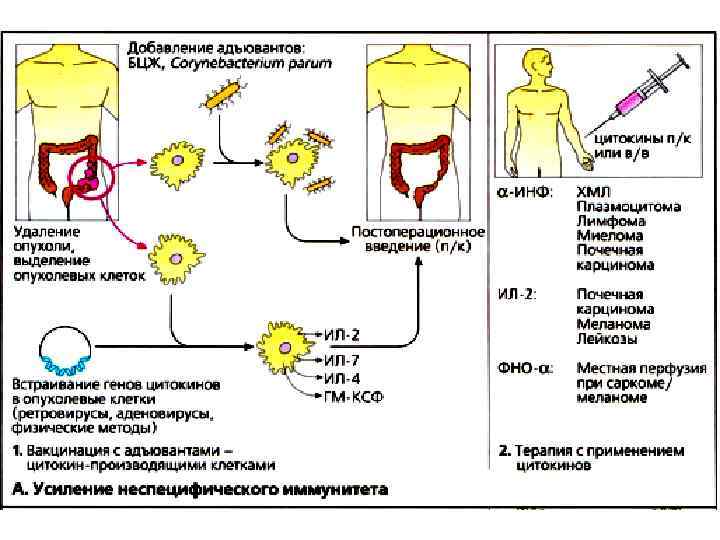

Усиление неспецифического иммунитета • В терапевтических целях можно использовать системное введение цитокинов. Однако на практике при отдельных видах олухолей используются только α -ИНФ и ИЛ-2. Кроме иммуностимулирующей активности, α -ИНФ обладает и прямым антиролиферативным действием, что может объяснять наблюдаемый терапевтический эффект. • Лучше остальных видов опухолей на иммунотерапию реагируют почечные карциномы и злокачественные меланомы. • При лечении пациентов с саркомами и меланомами при перфузии конечностей для усиления воздействия на опухолевые клетки используется также фактор некроза опухолей ФНО-α в сочетании с противоопухолевыми препаратами.

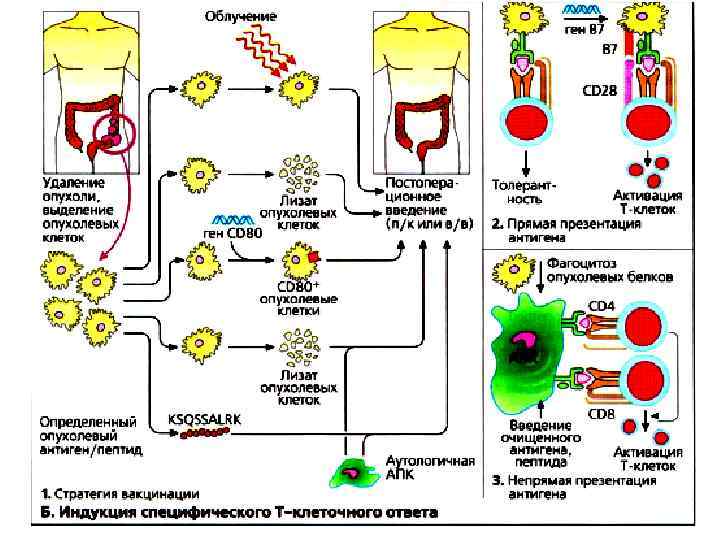
Индукция специфического Тклеточного ответа • У многих пациентов хирургическое вмешательство в момент постановки диагноза может успешно уничтожить первичную опухоль. Однако у некоторых из этих пациентов через какое-то время будут образовываться отдаленные метастазы или произойдет повторное возникновение опухоли. Пациентам с факторами риска (тип опухоли, степень злокачественности, глубина проникновения опухоли, вовлечение лимфатических узлов и др. ) показано проведение адъювантной терапии. • В большинстве случаев пока не удается индуцировать специфический Т-клеточный ответ на опухоль путем введения облученных аутологичных опухолевых клеток или лизатов опухолевых клеток.
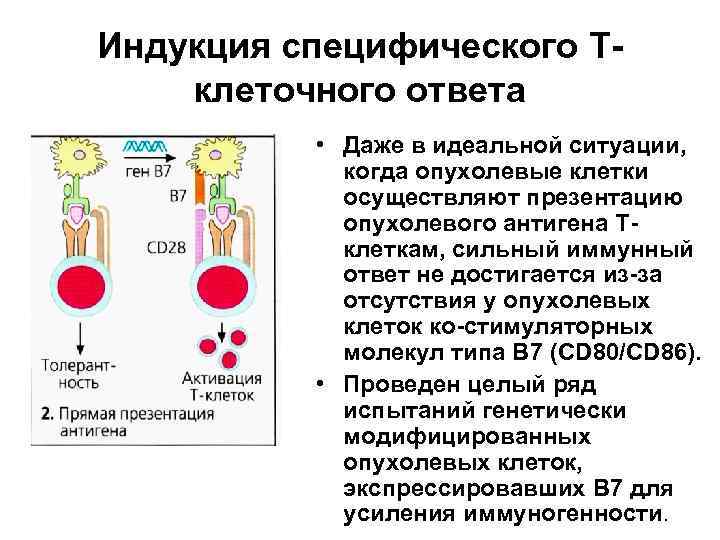
Индукция специфического Тклеточного ответа • Даже в идеальной ситуации, когда опухолевые клетки осуществляют презентацию опухолевого антигена Тклеткам, сильный иммунный ответ не достигается из-за отсутствия у опухолевых клеток ко-стимуляторных молекул типа В 7 (СD 80/СD 86). • Проведен целый ряд испытаний генетически модифицированных опухолевых клеток, экспрессировавших В 7 для усиления иммуногенности.
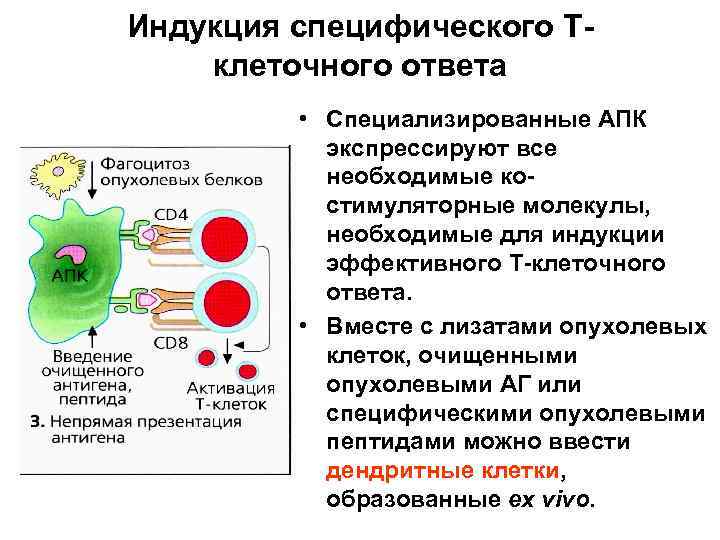
Индукция специфического Тклеточного ответа • Специализированные АПК экспрессируют все необходимые костимуляторные молекулы, необходимые для индукции эффективного Т-клеточного ответа. • Вместе с лизатами опухолевых клеток, очищенными опухолевыми АГ или специфическими опухолевыми пептидами можно ввести дендритные клетки, образованные ех vivo.
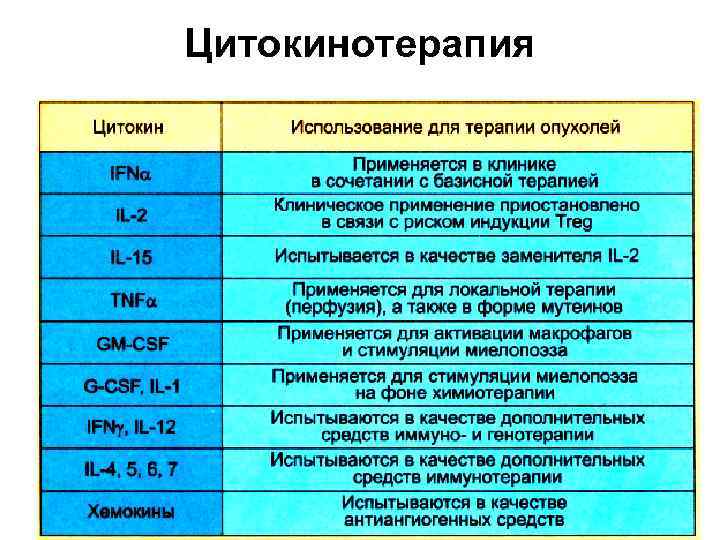
Цитокинотерапия

Цитокинотерапия • В качестве средства иммунотерапии используется IFNα. Его противоопухолевая активность обусловлена активирующим действием на эффекторные клетки (CTL, NK), усилением экспрессии МНС-I, антиангиогенным, антипролиферативным и дифференцирующим действием. • Применение препаратов на основе IL-2, ранее использовавшихся для иммунотерапии опухолей, приостановлено в связи со способностью этого цитокина поддерживать развитие и пролиферацию естественных регуляторных Т-клеток (Тreg).

Цитокинотерапия • В качестве аналогов эффективного, но токсичного цитокина ТNF используют его мутантные формы (с ослабленной токсичностью) - мутеины. • Цитокины с миелопоэтической активностью применяют для устранения цитопений, индуцированных химиотерапией. • Большинство других цитокинов или используется в ограниченном масштабе в специальных случаях, или находится на разных стадиях испытаний.

Моноклональные АТ • • • CEA (Carcino-embrional antigen) - ракоэмбриональный АГ; MUC-1 - муцин 1, СА-125, Lех - АГ группы крови Lех ; ЕGF-R — рецептор эпидермального фактора роста, тип 1; НЕR 2/Neu — продукт онкогена neu; IL-2 R — рецептор ИЛ- 2; FАРα (Fetal α-protein) — альфафетопротеин.
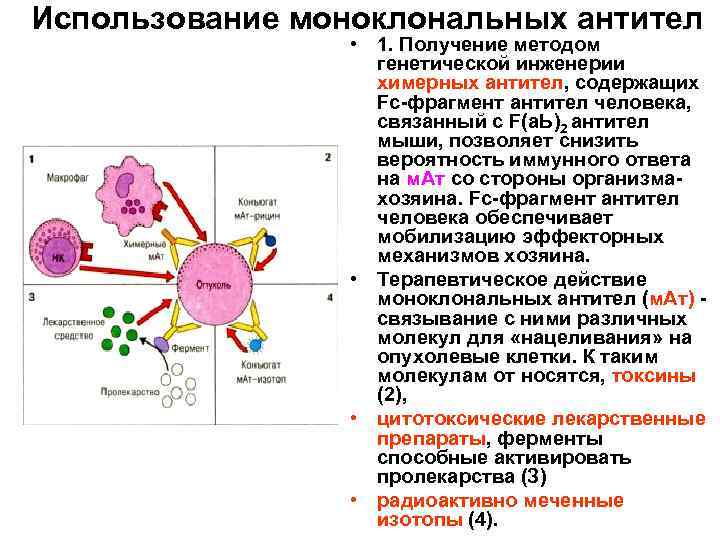
Использование моноклональных антител • 1. Получение методом генетической инженерии химерных антител, содержащих Fс-фрагмент антител человека, связанный с F(а. Ь)2 антител мыши, позволяет снизить вероятность иммунного ответа на м. Ат со стороны организмахозяина. Fс-фрагмент антител человека обеспечивает мобилизацию эффекторных механизмов хозяина. • Терапевтическое действие моноклональных антител (м. Ат) связывание с ними различных молекул для «нацеливания» на опухолевые клетки. К таким молекулам от носятся, токсины (2), • цитотоксические лекарственные препараты, ферменты способные активировать пролекарства (З) • радиоактивно меченные изотопы (4).
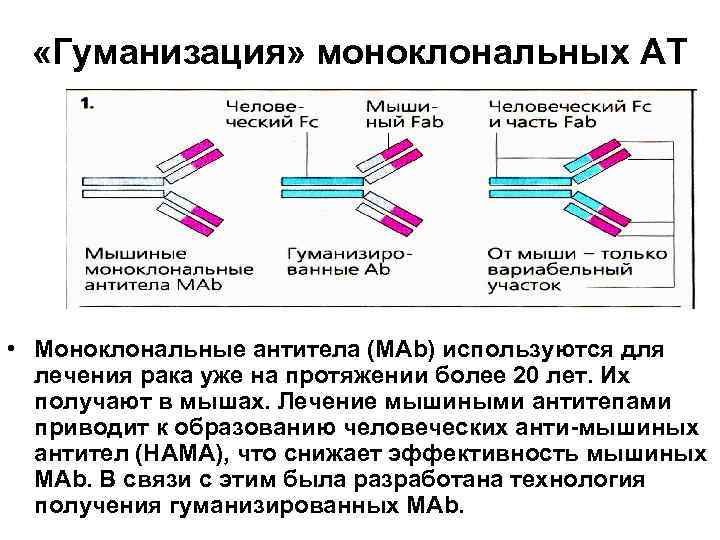
«Гуманизация» моноклональных АТ • Моноклональные антитела (МAb) используются для лечения рака уже на протяжении более 20 лет. Их получают в мышах. Лечение мышиными антитепами приводит к образованию человеческих анти-мышиных антител (НАМА), что снижает эффективность мышиных МАb. В связи с этим была разработана технология получения гуманизированных МАb.
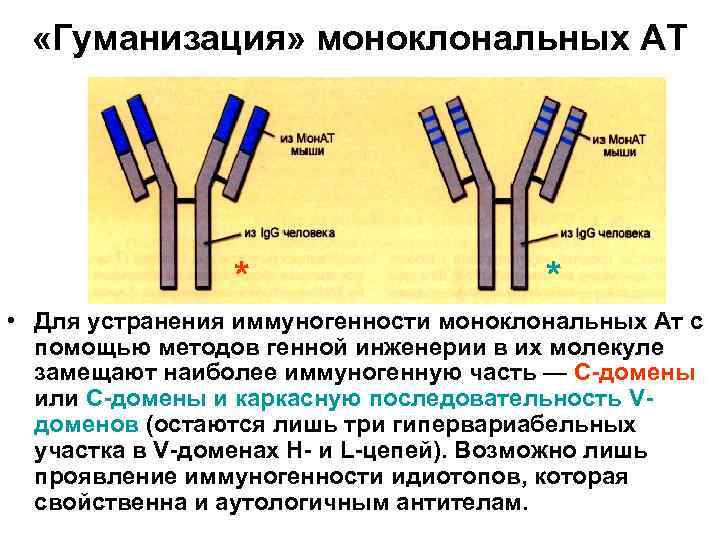
«Гуманизация» моноклональных АТ * * • Для устранения иммуногенности моноклональных Ат с помощью методов генной инженерии в их молекуле замещают наиболее иммуногенную часть — С-домены или С-домены и каркасную последовательность Vдоменов (остаются лишь три гипервариабельных участка в V-доменах Н- и L-цепей). Возможно лишь проявление иммуногенности идиотопов, которая свойственна и аутологичным антителам.
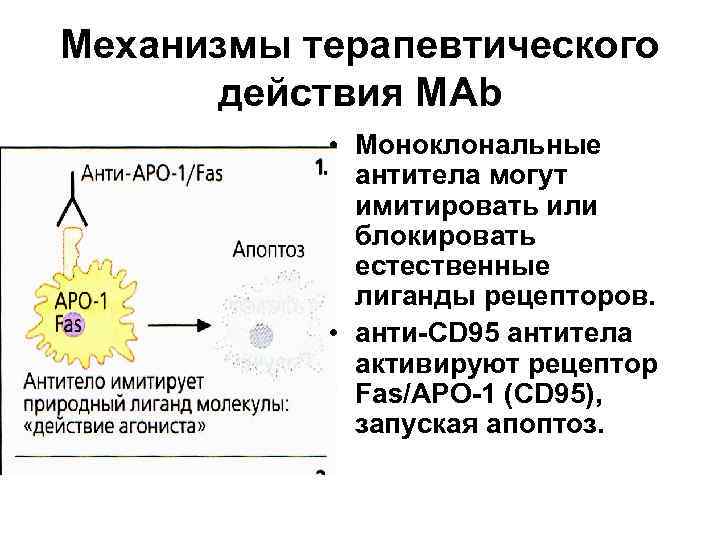
Механизмы терапевтического действия МАb • Моноклональные антитела могут имитировать или блокировать естественные лиганды рецепторов. • анти-CD 95 антитела активируют рецептор Fas/AРО-1 (CD 95), запуская апоптоз.
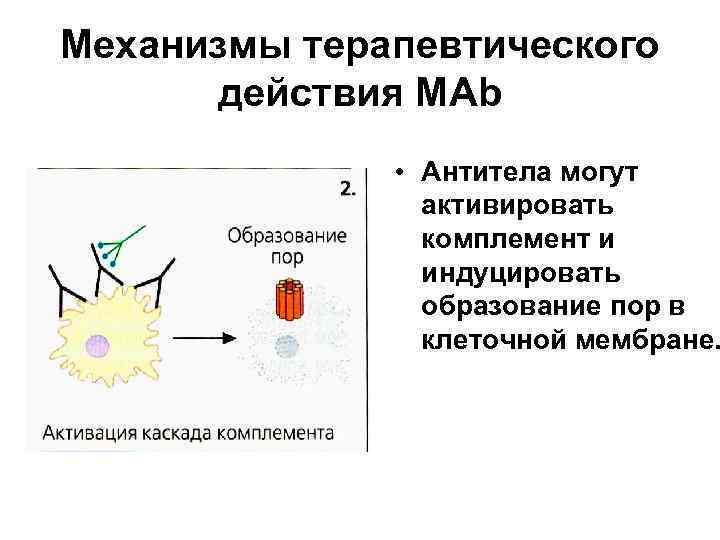
Механизмы терапевтического действия МАb • Антитела могут активировать комплемент и индуцировать образование пор в клеточной мембране.
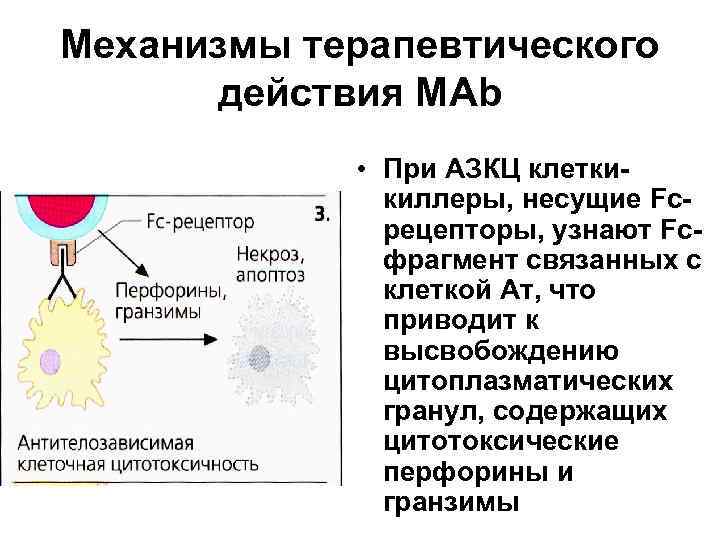
Механизмы терапевтического действия МАb • При АЗКЦ клеткикиллеры, несущие Fсрецепторы, узнают Fсфрагмент связанных с клеткой Ат, что приводит к высвобождению цитоплазматических гранул, содержащих цитотоксические перфорины и гранзимы
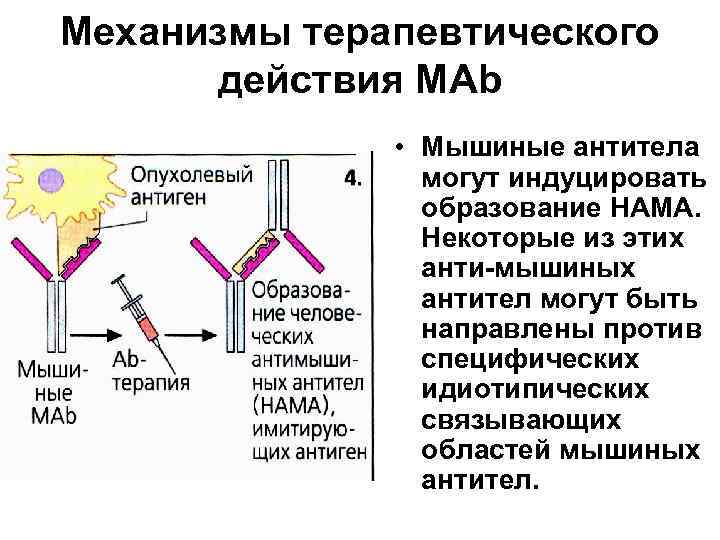
Механизмы терапевтического действия МАb • Мышиные антитела могут индуцировать образование НАМА. Некоторые из этих анти-мышиных антител могут быть направлены против специфических идиотипических связывающих областей мышиных антител.

Механизмы терапевтического действия МАb • Антиидиотипические антитела имитируют опухолевые антигены и могут служить опухолевыми суррогатами в вакцинах. • Они также могут приводить к образованию анти-идиотипических моноклональных антител, которые узнают опухолевый антиген, подобно мышиным МAb. В результате реализации этого каскада действие мышиных моноклональных антител усиливается.
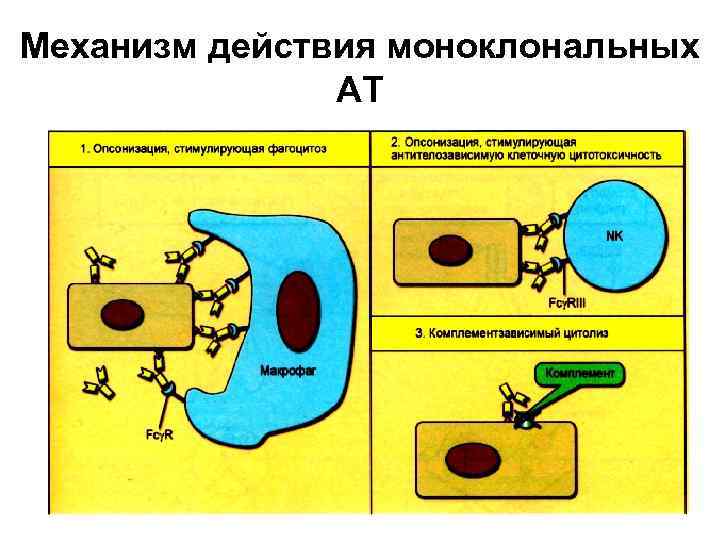
Механизм действия моноклональных АТ

Механизм действия моноклональных АТ • Моноклональные антитела оказывают противоовухолевое действие по механизму антителозависимого клеточного цитолиза, опосредованного МФ (1) или NK-клетками (2). Оба типа эффекторных клеток распознают Fс-часть антител, связавшихся с опухолевым АГ, с помощью Fсрецепторов (FсγI, II и III на МФ и FсγIII на NK-клетках). Для МФ это служит сигналом для фагоцитоза или внутриклеточного цитолиза клетки-мишени, для NKклеток - для контактного цитолиза. • Комллементзависимый цитолиз опухолевых клеток (3) не играет существенной роли в реализации лечебного действия антител, так как мембрана опухолевых клеток располагает факторами, инактивирующими компоненты С’.
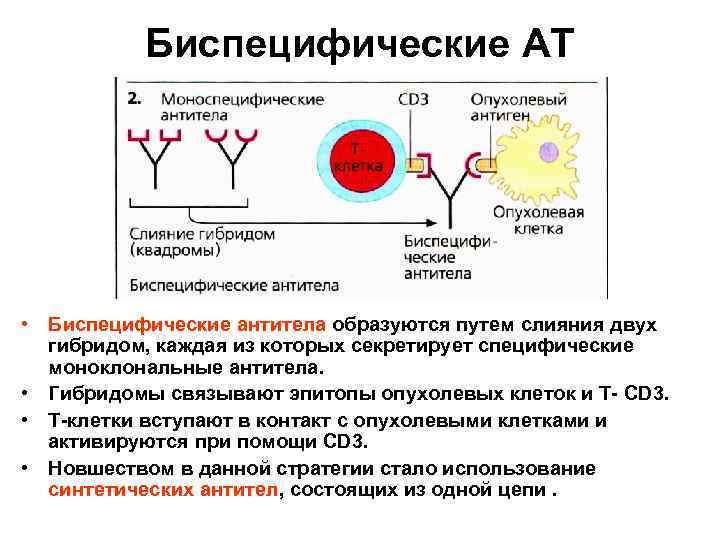
Биспецифические АТ • Биспецифические антитела образуются путем слияния двух гибридом, каждая из которых секретирует специфические моноклональные антитела. • Гибридомы связывают эпитопы опухолевых клеток и Т- CD 3. • Т-клетки вступают в контакт с опухолевыми клетками и активируются при помощи CD 3. • Новшеством в данной стратегии стало использование cинтетических антител, состоящих из одной цепи.
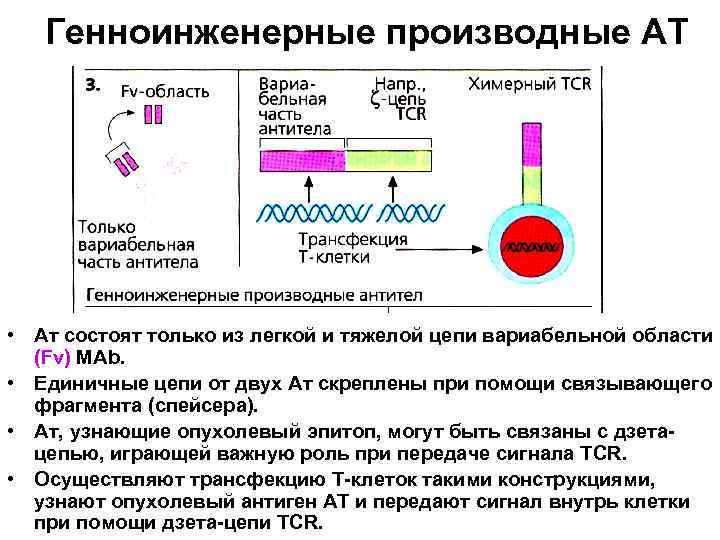
Генноинженерные производные АТ • Ат состоят только из легкой и тяжелой цепи вариабельной области (Fv) МАb. • Единичные цепи от двух Ат скреплены при помощи связывающего фрагмента (спейсера). • Ат, узнающие опухолевый эпитоп, могут быть связаны с дзетацепью, играющей важную роль при передаче сигнала ТCR. • Осуществляют трансфекцию Т-клеток такими конструкциями, узнают опухолевый антиген АТ и передают сигнал внутрь клетки при помощи дзета-цепи ТCR.
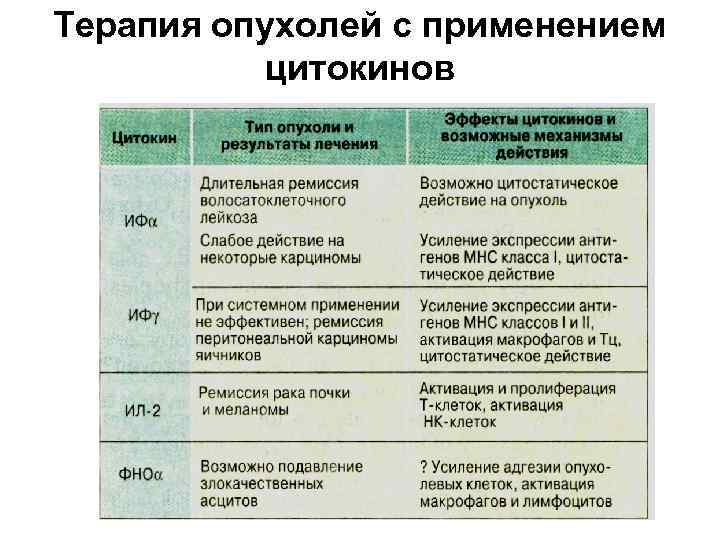
Терапия опухолей с применением цитокинов
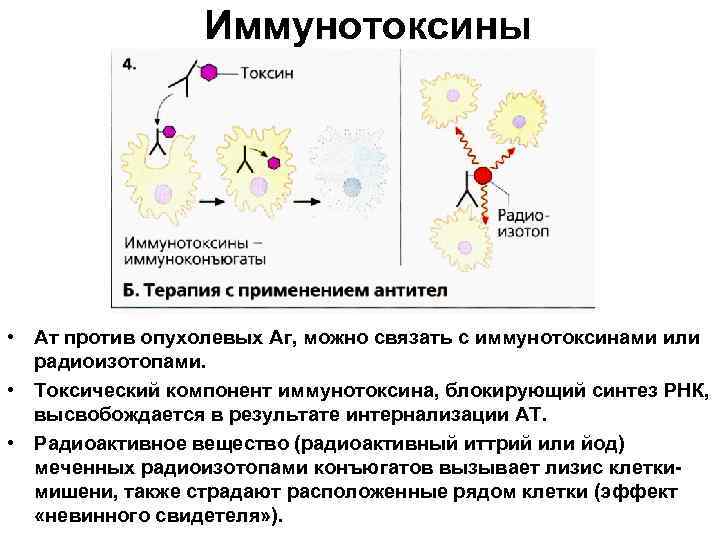
Иммунотоксины • Ат против опухолевых Аг, можно связать с иммунотоксинами или радиоизотопами. • Токсический компонент иммунотоксина, блокирующий синтез РНК, высвобождается в результате интернализации АТ. • Радиоактивное вещество (радиоактивный иттрий или йод) меченных радиоизотопами конъюгатов вызывает лизис клеткимишени, также страдают расположенные рядом клетки (эффект «невинного свидетеля» ).

Иммунотоксины • Растительные токсины обычно имеют две полипептидные цепи, одна из которых ответственна за доставку, другая - за токсичность молекулы. • Для получения иммунотоксина изолированную токсическую цепь ковалентно подсоединяют к моноклональному антителу, направленному против опухолевого АГ.

Доставка токсина в клетку • Связывание иммунотоксина с мембранным АГ • Интернализация комплекса в составе эндосомы. • Токсическая субъединица иммунотоксина поступает в цитозоль, • Реализация токсического действия - гибель клетки.

Специфический цитолиз • Иммунотоксин вызывает специфический цитолиз опухолевой клетки, несущей АГ, против которого направлены моноклональные антитела.
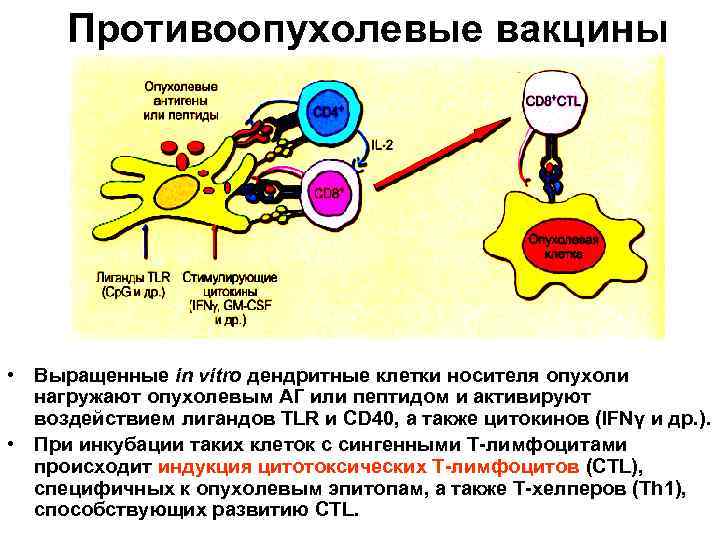
Противоопухолевые вакцины • Выращенные in vitro дендритные клетки носителя опухоли нагружают опухолевым АГ или пептидом и активируют воздействием лигандов ТLR и СD 40, а также цитокинов (IFNγ и др. ). • При инкубации таких клеток с сингенными Т-лимфоцитами происходит индукция цитотоксических Т-лимфоцитов (СТL), специфичных к опухолевым эпитопам, а также Т-хелперов (Тh 1), способствующих развитию СТL.

Создание противоопухолевых вакцин • С лечебной целью используют как ДК, нагруженные опухолевым АГ in vitro (в этом случае индукция СТL происходит in vivo) или СТL, индуцированные in vitro. В обоих случаях именно СТL реализуют цитолиз опухолевых клеток. • Возникают препятствия на пути реализации указанной программы (одно из них отсутствие эффективной доставки СТL к опухоли).

Генноинженерные опухоль-специфичные Т -клеточные рецепторы • Были предприняты попытки выделять инфильтрующие опухоль лимфоциты ТIL из удаленных опухолей и вновь переливать их пациенту. • Возможно определить последовательность ДНК вариабельных доменов α- и β-цепей ТCR TIL. • С помощью вирусных векторов можно получить генетически измененные Тлимфоциты, специфическим образом реагирующие с опухолевыми клетками. • Затем следует осуществить адаптивную терапию, вводя пациенту эти размноженные ех vivo клетки.
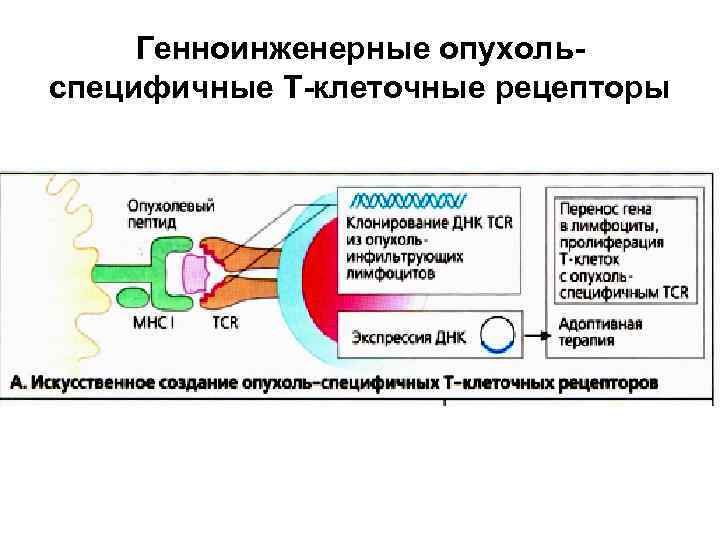
Генноинженерные опухольспецифичные Т-клеточные рецепторы

Клиническая трансплантация
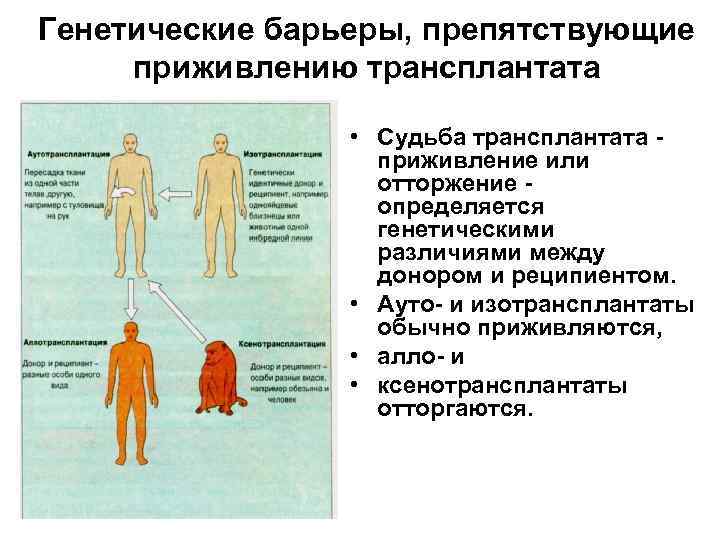
Генетические барьеры, препятствующие приживлению трансплантата • Судьба трансплантата приживление или отторжение определяется генетическими различиями между донором и реципиентом. • Ауто- и изотрансплантаты обычно приживляются, • алло- и • ксенотрансплантаты отторгаются.

Наследование гаплотипов МНС • МНС человека (HLA) расположен в коротком плече хромосомы 6. • Комплекс генов НLА класса 1 (HLA-А, HLA-В и HLA-C и класса II (HLA-D), локализованных в одной хромосоме (гаплотип), наследуется целиком, и любой индивид имеет два HLA-гаплотипа, каждый из которых унаследован от одного из родителей.
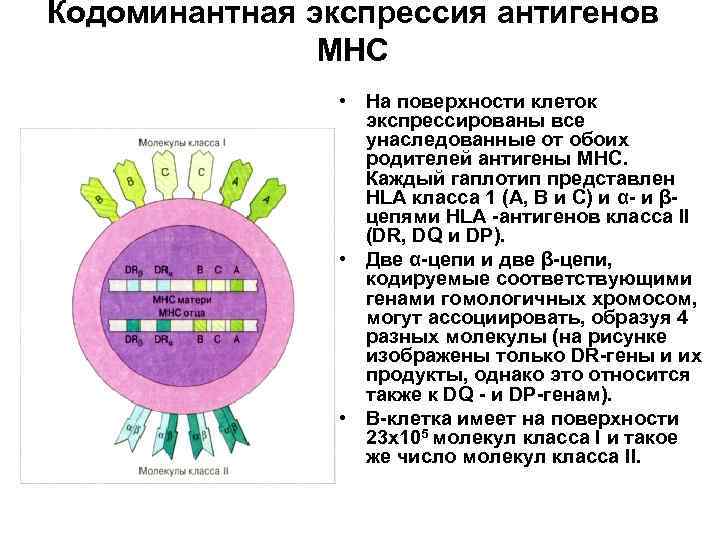
Кодоминантная экспрессия антигенов МНС • На поверхности клеток экспрессированы все унаследованные от обоих родителей антигены МНС. Каждый гаплотип представлен HLA класса 1 (А, В и С) и α- и βцепями HLA -антигенов класса II (DR, DQ и DP). • Две α-цепи и две β-цепи, кодируемые соответствующими генами гомологичных хромосом, могут ассоциировать, образуя 4 разных молекулы (на рисунке изображены только DR-гены и их продукты, однако это относится также к DQ - и DP-генам). • В-клетка имеет на поверхности 23 x 105 молекул класса I и такое же число молекул класса II.

Генетические законы трансплантации • 1. Трансплантация внутри одной инбредной линии ( сингенная трансплантация) всегда успешна: между донором и реципиентом отсутствуют генетические, а следовательно, и антигенные различия.

Генетические законы трансплантации • 2. Трансплантация между особями разных инбредных линий ( аллогенная трансплантация) терпит неудачу: между донором и реципиентом имеются различия по комплексу МНС и по контролируемым им молекулам (антигенам) гистосовместимости. В результате у реципиента развивается иммунный ответ на чужеродные антигены донора, что приводит к отторжению трансплантата.

Генетические законы трансплантации • 3. Трансплантаты родительских линий Р 1 или Р 2 приживаются у гибридов первого поколения (Р 1*Р 2)F 1. Поскольку антигены гистосовместимости наследуются по кодоминантному типу, гибриды F 1 имеют полный набор антигенов обоих родителей. Трансплантаты родителей не несут чужеродной информации для гибрида F 1, и в результате трансплантат приживается. В то же время трансплантат гибрида F 1 отторгается у мышей родительских линий, так как реципиенты (Р 1 или Р 2) реагируют на антигены второго родителя (Р 2 или Р 1), представленные у гибрида F 1.

Генетические законы трансплантации • 4. Трансплантаты гибридов второго поколения F 2 приживаются у гибридов F 1. У гибридов F 2 происходит расщепление признака по антигенам гистосовместимости на гомозиготы и гетерозиготы, и они не имеют каких- либо антигенов, которые не были бы представлены у F 1. В итоге наблюдается приживление трансплантатов.

Генетические законы трансплантации • 5. Трансплантаты родительских линий Р 1 и Р 2 приживаются у одних особей F 2, но отторгаются у других. Поскольку гибриды F 2 включают как гомозиготы, так и гетерозиготы, трансплантация ткани одного из гомозиготных родителей на гомозиготную особь F 2, имеющую иной генотип, приводит к отторжению трансплантата. • Аналогичные отношения существуют и при пересадке родительских трансплантатов на гибрид возвратного скрещивания.
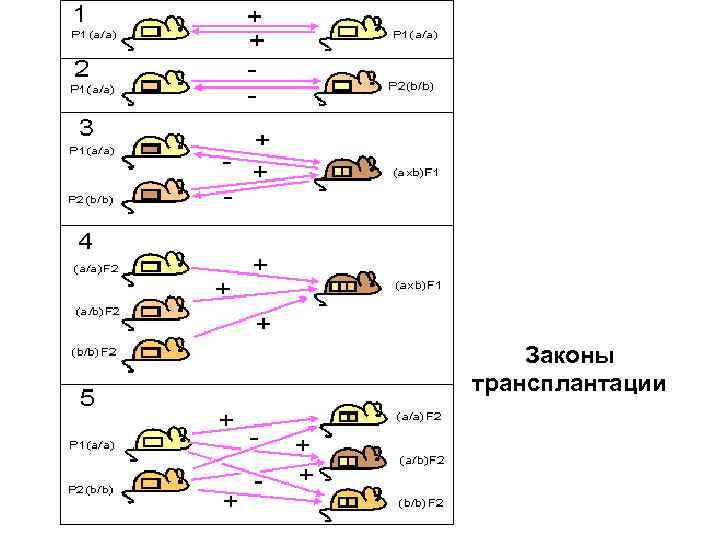
Законы трансплантации
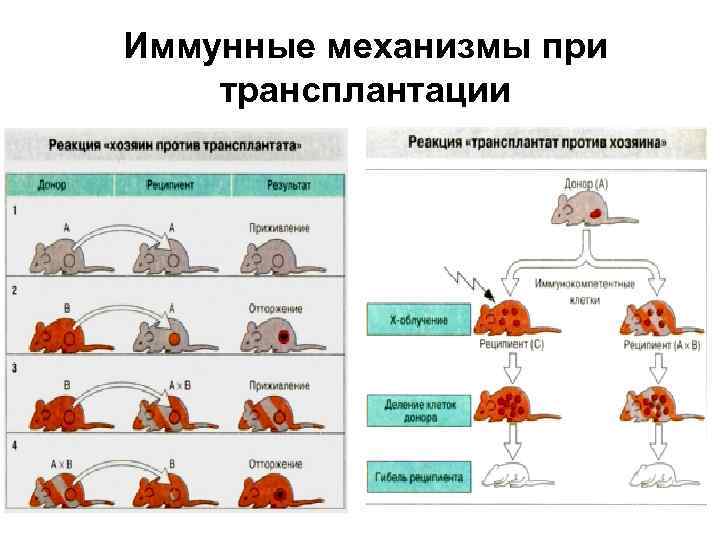
Иммунные механизмы при трансплантации
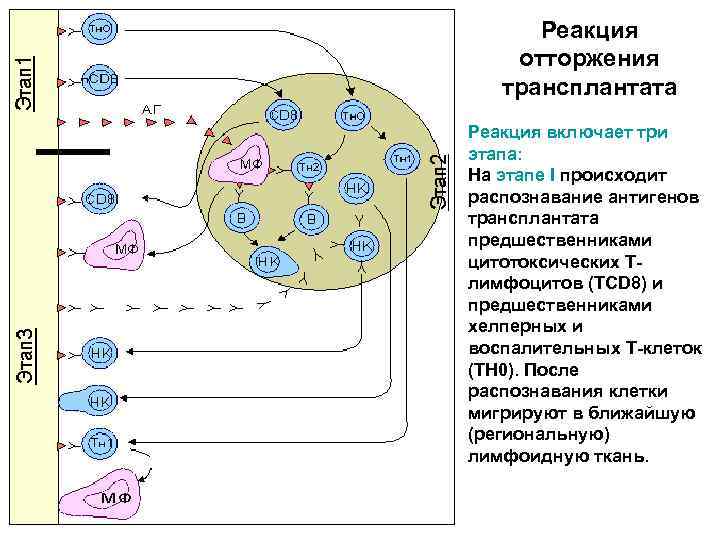
Реакция отторжения трансплантата Реакция включает три этапа: На этапе I происходит распознавание антигенов трансплантата предшественниками цитотоксических Тлимфоцитов (ТCD 8) и предшественниками хелперных и воспалительных Т-клеток (ТН 0). После распознавания клетки мигрируют в ближайшую (региональную) лимфоидную ткань.
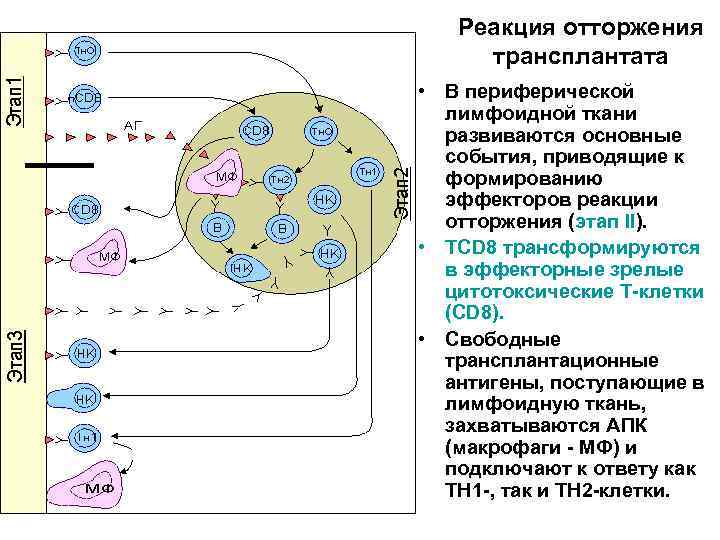
Реакция отторжения трансплантата • В периферической лимфоидной ткани развиваются основные события, приводящие к формированию эффекторов реакции отторжения (этап II). • TCD 8 трансформируются в эффекторные зрелые цитотоксические Т-клетки (CD 8). • Свободные трансплантационные антигены, поступающие в лимфоидную ткань, захватываются АПК (макрофаги - МФ) и подключают к ответу как ТН 1 -, так и ТН 2 -клетки.
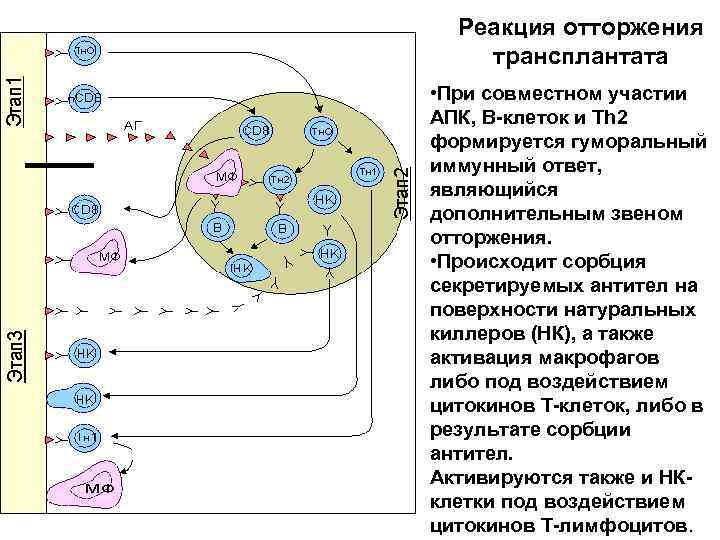
Реакция отторжения трансплантата • При совместном участии АПК, В-клеток и Тh 2 формируется гуморальный иммунный ответ, являющийся дополнительным звеном отторжения. • Происходит сорбция секретируемых антител на поверхности натуральных киллеров (НК), а также активация макрофагов либо под воздействием цитокинов Т-клеток, либо в результате сорбции антител. Активируются также и НКклетки под воздействием цитокинов Т-лимфоцитов.
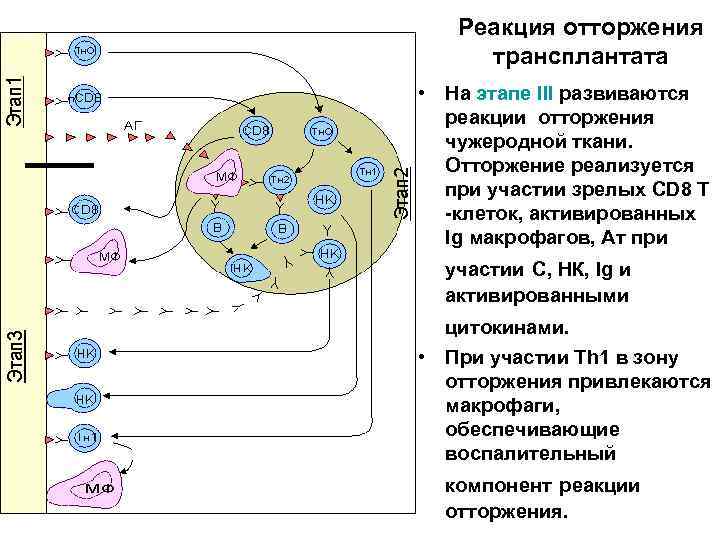
Реакция отторжения трансплантата • На этапе III развиваются реакции отторжения чужеродной ткани. Отторжение реализуется при участии зрелых CD 8 Т -клеток, активированных Ig макрофагов, Ат при участии С, НК, Ig и активированными цитокинами. • При участии Тh 1 в зону отторжения привлекаются макрофаги, обеспечивающие воспалительный компонент реакции отторжения.
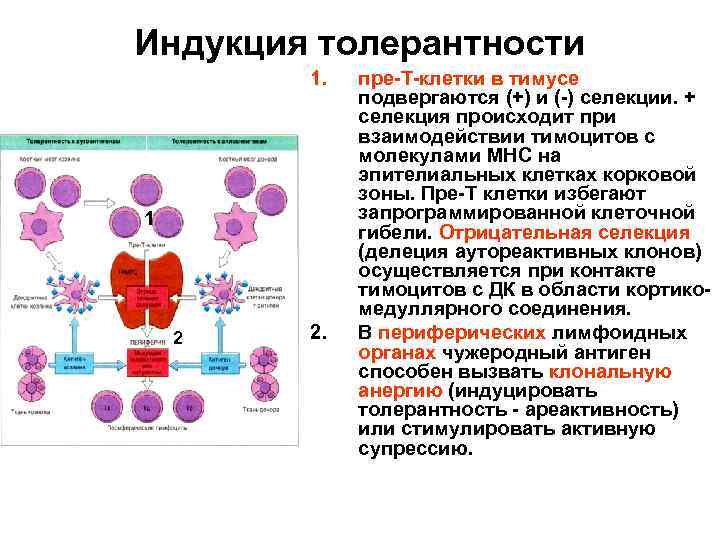
Индукция толерантности 1. 1 2 2. пре-Т-клетки в тимусе подвергаются (+) и (-) селекции. + селекция происходит при взаимодействии тимоцитов с молекулами МНС на эпителиальных клетках корковой зоны. Пре-Т клетки избегают запрограммированной клеточной гибели. Отрицательная селекция (делеция аутореактивных клонов) осуществляется при контакте тимоцитов с ДК в области кортикомедуллярного соединения. В периферических лимфоидных органах чужеродный антиген способен вызвать клональную анергию (индуцировать толерантность - ареактивность) или стимулировать активную супрессию.
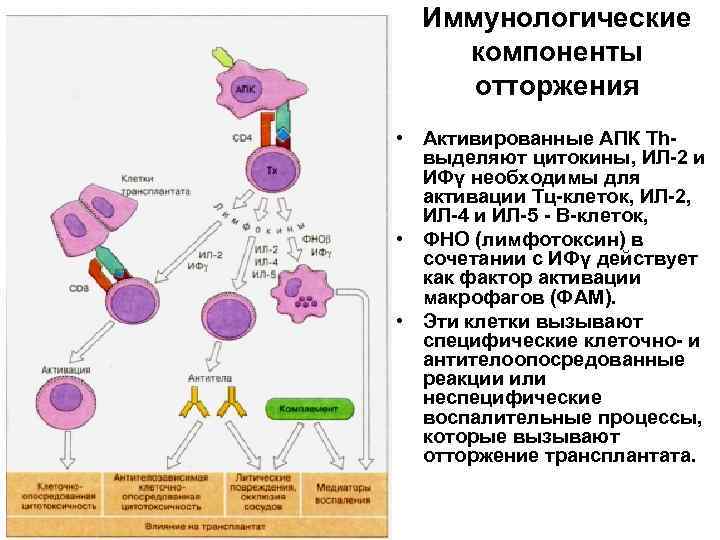
Иммунологические компоненты отторжения • Активированные АПК Тhвыделяют цитокины, ИЛ-2 и ИФγ необходимы для активации Тц-клеток, ИЛ-2, ИЛ-4 и ИЛ-5 - В-клеток, • ФНО (лимфотоксин) в сочетании с ИФγ действует как фактор активации макрофагов (ФАМ). • Эти клетки вызывают специфические клеточно- и антителоопосредованные реакции или неспецифические воспалительные процессы, которые вызывают отторжение трансплантата.

Трансплантационный иммунитет • Антигены гистосовместимости HLA – антигены I класса (А, В. С) • Реакция отторжения трансплантата (Тцитотоксические киллеры и антитела) • Ат-зависимая клеточно-опосредованная цитотоксичность • Ат –опосредованный цитолиз трансплантата (гемагглютинины, гемолизины, лейкотоксины, цитотоксины)
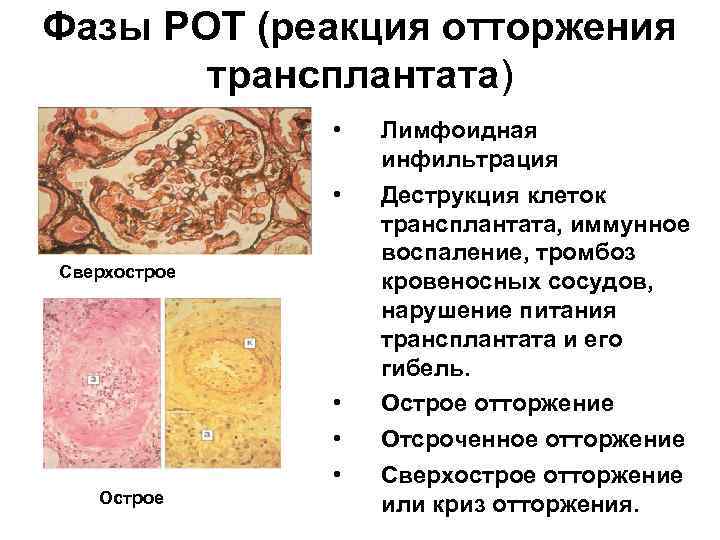
Фазы РОТ (реакция отторжения трансплантата) • • Сверхострое Острое • • • Лимфоидная инфильтрация Деструкция клеток трансплантата, иммунное воспаление, тромбоз кровеносных сосудов, нарушение питания трансплантата и его гибель. Острое отторжение Отсроченное отторжение Сверхострое отторжение или криз отторжения.
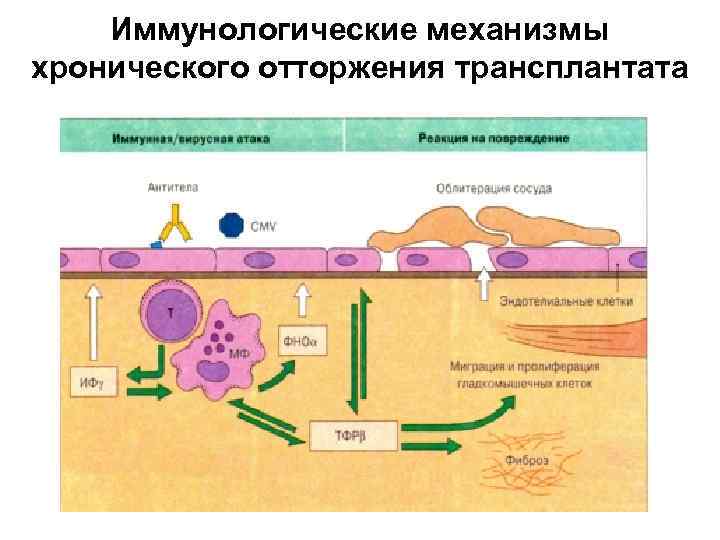
Иммунологические механизмы хронического отторжения трансплантата
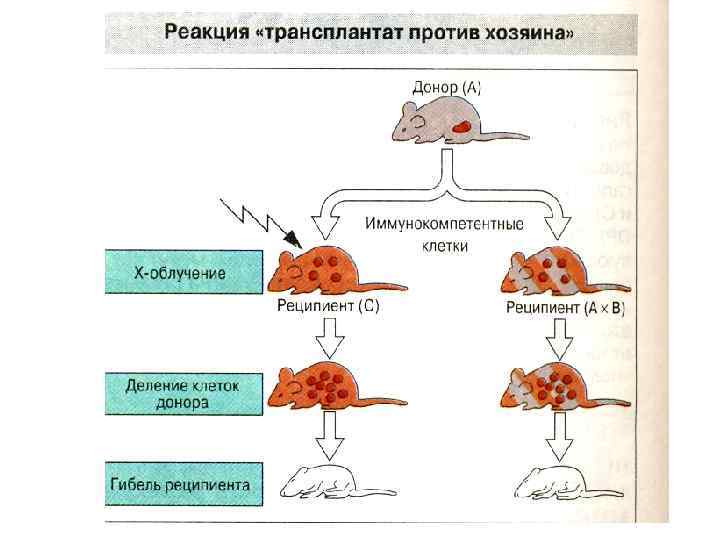

Болезнь «трансплантат против хозяина» • Тяжелая острая реакция "трансплантат против хозяина" сопровождается иммунодефицитом и склонностью к инфекциям. • Легкая острая реакция "трансплантат против хозяина", как ни странно, приносит пользу - за счет реакции "трансплантат против опухоли".

Болезнь «трансплантат против хозяина» • Хроническая реакция "трансплантат против хозяина" развивается через 3 мес. и более после трансплантации и проявляется высыпаниями по типу красного плоского лишая на коже, высыпаниями по типу красного плоского лишая на слизистой рта, склерозом кожи, алопецией, нарушением функции печени, сухостью рта, сухостью глаз (как при синдроме Шегрена). • Возможны облитерирующий бронхиолит и нарушения моторики ЖКТ

Болезнь «трансплантат против хозяина» • Болезнь запускается Т-лимфоцитами донора, распознающими антигены малых комплексов гистосовместимости реципиента. • Обнаруживаются аутореактивные донорские Тлимфоциты, распознающие общие для донора и реципиента антигены. • Активированные Т-лимфоциты секретируют ряд цитокинов, из которых важнейшим для развития болезни считается ИЛ-4. Болезнь лечится иммунодепрессантами. • Наибольшую угрозу для жизни представляют оппортунистические инфекции, связанные как с аутоиммунным конфликтом, так и с его лечением. Из -за слабой выработки антител к полисахаридным антигенам больные подвержены бактериальным инфекциям.

Методы диагностики • 1) Серологические методы определения • Основной серологический метод типирования антигенов HLA лимфоцитотоксический тест. Метод заключается в следующем: - К сывороткам против разных антигенов HLA добавляют по 2000 исследуемых лимфоцитов. - После инкубации добавляют комплемент (его источником может служить кроличья сыворотка). - Лимфоциты, несущие антиген, против которого направлена сыворотка, под действием комплемента разрушаются. - Затем к лимфоцитам добавляют краситель, который окрашивает только живые клетки. Результат оценивают по относительному числу погибших лимфоцитов.

Методы диагностики • 2) Молекулярно-генетические методы определения • Эти методы основаны на исследовании ДНК. Они лишены недостатков серологических методов. Генетическое типирование стало возможным после расшифровки нуклеотидной последовательности генов HLA и выявления различий между аллелями этих генов. В настоящее время молекулярно- генетические методы используются только для типирования генов HLA класса II. • Метод основан на способности бактериальных эндонуклеаз расщеплять ДНК в тех участках, в которых сосредоточены специфические для определенной эндонуклеазы последовательности нуклеотидов - сайты рестрикции. Сайты рестрикции для данной эндонуклеазы в разных аллелях одного гена располагаются на разном расстоянии друг от друга, поэтому длина рестрикционных фрагментов у разных аллелей разная. Применение эндонуклеаз позволило выявить полиморфизм длин рестрикционных фрагментов ДНК, подобный полиморфизму HLA, определяемому серологически.

Методы диагностики • Полимеразная цепная реакция - метод, предназначенный для получения большого количества копий фрагментов ДНК с определенной нуклеотидной последовательностью. Основное достоинство метода - высокая чувствительность, он позволяет создать множество копий фрагмента ДНК при минимальном исходном ее количестве. Реакция включает следующие стадии: - денатурация ДНК с получением двух однонитевых фрагментов; гибридизация олигонуклеотидов с 5'-концевыми участками этих фрагментов; - синтез комплементарной последовательности нуклеотидов. • Реакцию проводят циклично, последовательно повторяя все ее стадии до получения достаточного количества копий исходного фрагмента ДНК.
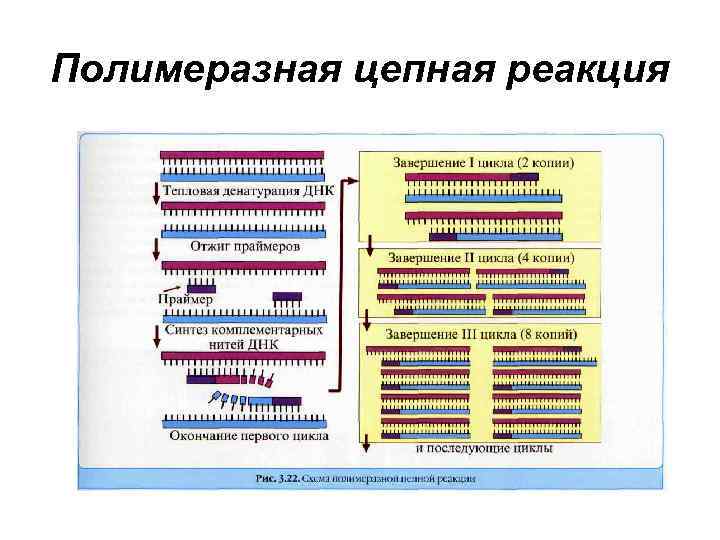
Полимеразная цепная реакция

Методы диагностики Клеточные методы определения • После распознавания чужеродного антигена начинается пролиферация Т-лимфоцитов. Этот процесс можно воспроизвести in vitro в смешанной культуре лимфоцитов, состоящей из лимфоцитов донора и реципиента. Если донор и реципиент несут разные антигены HLA класса II, в смешанной культуре отмечается пролиферация. • Чтобы оценить иммунный ответ лимфоцитов только одного из исследуемых (отвечающих клеток), лимфоциты другого (стимулирующие клетки) инактивируют облучением или митомицином. • Смешанная культура лимфоцитов позволяет выявить различия по антигенам HLA, которые нельзя обнаружить серологическими методами, например различия по антигенам HLA-DP и HLA-DQ.

Методы диагностики • Смешанная культура лимфоцитов. Равное количество лимфоцитов донора и реципиента смешивают и инкубируют в течение 5 суток при температуре 37 о. С, затем добавляют 3 Н-тимидин, который встраивается в ДНК пролиферирующих клеток. В присутствии 3 Нтимидина лимфоциты инкубируют еще 1 сутки, после чего определяют радиоактивность отвечающих клеток. • В качестве отрицательного контроля используются культуры, состоящие только из отвечающих клеток, в качестве положительного - культура отвечающих клеток, стимулированных смесью лимфоцитов от разных доноров. • Если радиоактивность в смешанной культуре превышает радиоактивность в отрицательном контроле не более чем на 20% или составляет не более 20% от радиоактивности в положительном контроле, считают, что донор и реципиент совместимы по антигенам HLA класса II.
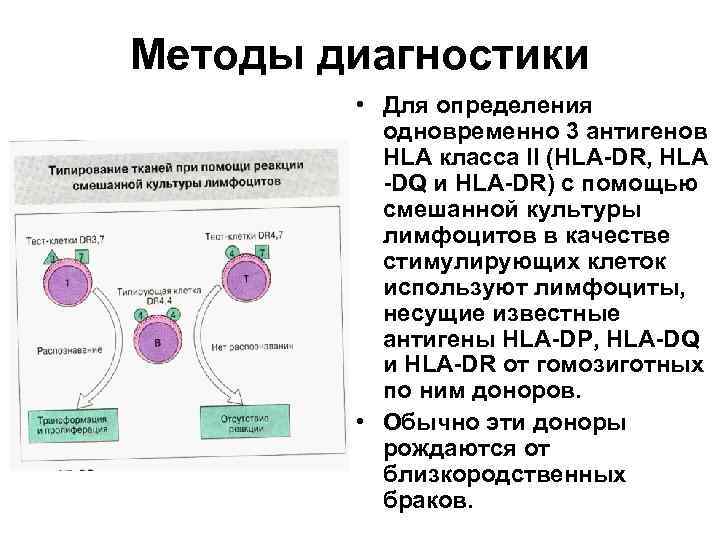
Методы диагностики • Для определения одновременно 3 антигенов HLA класса II (HLA-DR, HLA -DQ и HLA-DR) с помощью смешанной культуры лимфоцитов в качестве стимулирующих клеток используют лимфоциты, несущие известные антигены HLA-DP, HLA-DQ и HLA-DR от гомозиготных по ним доноров. • Обычно эти доноры рождаются от близкородственных браков.
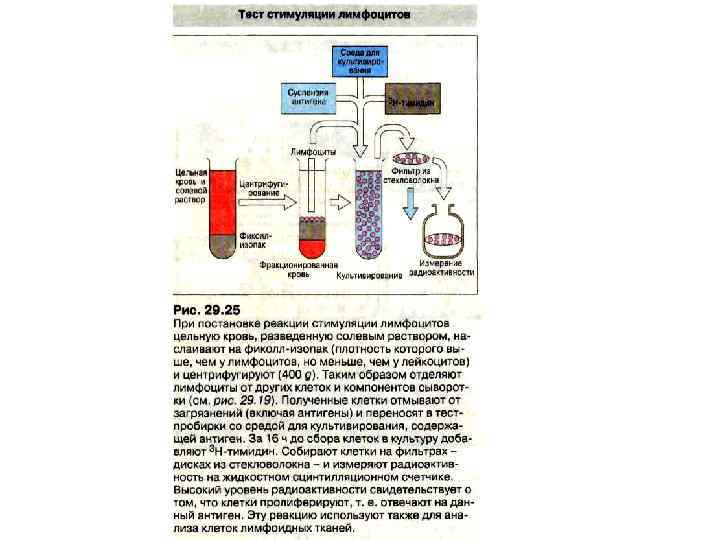

Методы диагностики • Реакция клеточной цитотоксичности. При совместном культивировании лимфоцитов реципиента (отвечающих клеток) и отличающихся от них по антигенам HLA класса II стимулирующих клеток среди отвечающих клеток появляются цитотксические Т-лимфоциты. Они способны разрушать клеткимишени, несущие антигены, которые присутствуют на стимулирующих клетках. • Изучение клеточной цитотоксичности в смешанной культуре лимфоцитов в ряде случаев позволяет предсказать, будет трансплантат стимулировать образование цитотоксических Тлимфоцитов или нет. • Для этого готовится смешанная культура лимфоцитов, где отвечающими клетками служат лимфоциты реципиента, а стимулирующими - инактивированные лимфоциты донора. • После 6 суток инкубации смешанной культуре лимфоцитов к отвечающим клеткам добавляют свежие клетки того же донора, меченные 51 Cr.
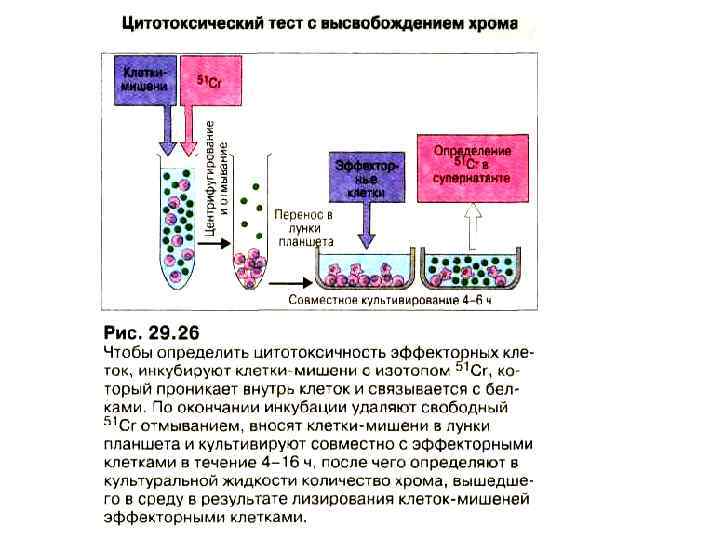

Предотвращение отторжения трансплантата • Cтероиды, циклоспорин и азатиоприн - подавляют реакцию отторжения разными путями. • Стероиды обладают противовоспалительными свойствами - угнетают функции макрофагов и АПК, снижая также экспрессию антигенов МНС. • Циклоспорин блокирует продукцию цитокинов; • азатиоприн подавляет пролиферацию активированных клеток.
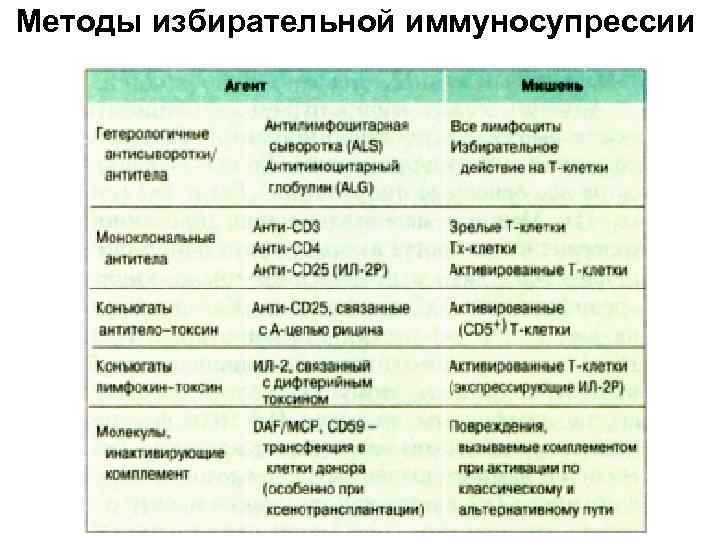
Методы избирательной иммуносупрессии
2 стом противоопух.транспл иммунитет.ppt