3 Простые вещества.ppt
- Количество слайдов: 17

Простые вещества

Особенности • Отсутствуют эффекты, связанные с разностью электроотрицательностей, реализуются либо металлические, либо неполярные ковалентные связи • Отсутствует понятие «состав» элемент простое вещество кислород – O 2 углерод – С алмаз – С, графит – С железо – Fe • Граница Цинтля проходит между IIIA и IVA группами, отделяет элементы с дефицитом электронов от элементов с их достаточным количеством. • Кристаллохимическое правило Юм-Розери 8 – N 2
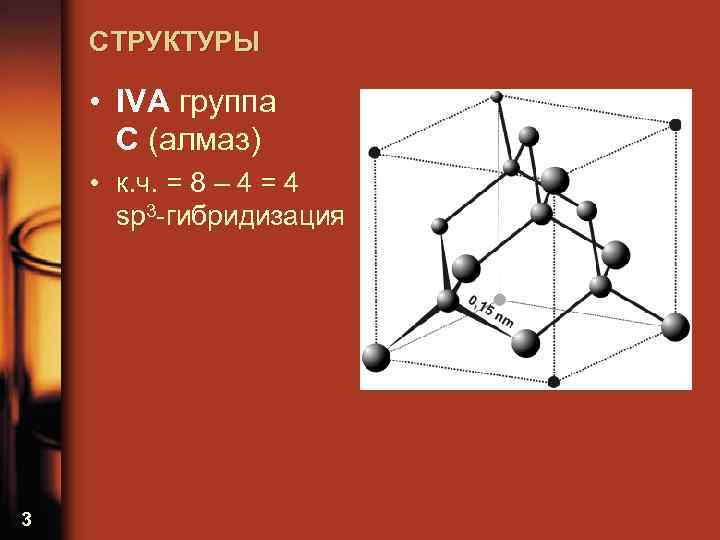
СТРУКТУРЫ • IVА группа С (алмаз) • к. ч. = 8 – 4 = 4 sp 3 -гибридизация 3
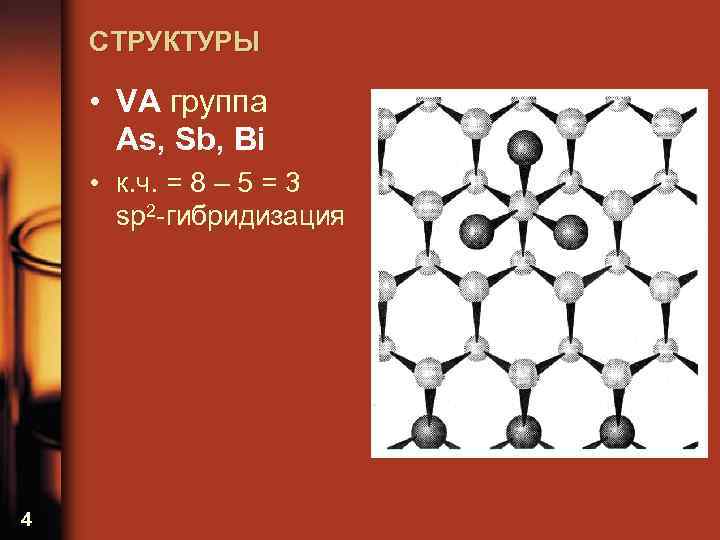
СТРУКТУРЫ • VА группа As, Sb, Bi • к. ч. = 8 – 5 = 3 sp 2 -гибридизация 4
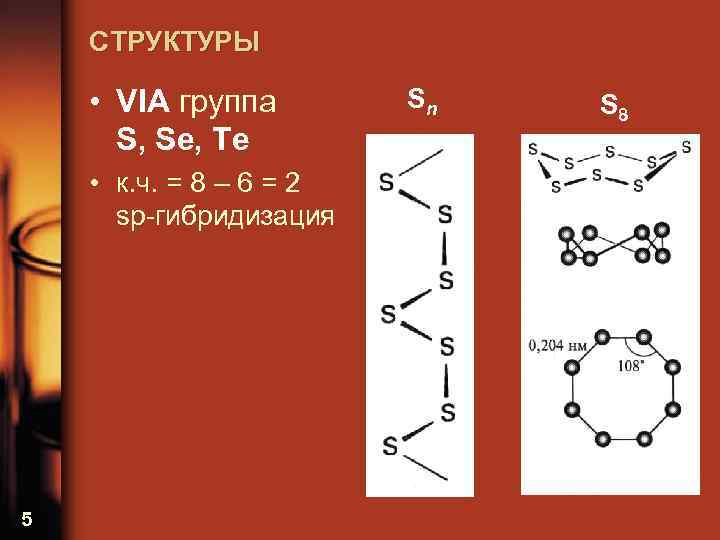
СТРУКТУРЫ • VIА группа S, Se, Te • к. ч. = 8 – 6 = 2 sp-гибридизация 5 Sn S 8

СТРУКТУРЫ • VIIА группа Cl 2, Br 2, I 2 • к. ч. = 8 – 7 = 1 молекулярная решетка 6

СТРУКТУРЫ • VIIIА группа кристаллы благородных газов • к. ч. = 8 – 8 = 0 одноатомные молекулы 7
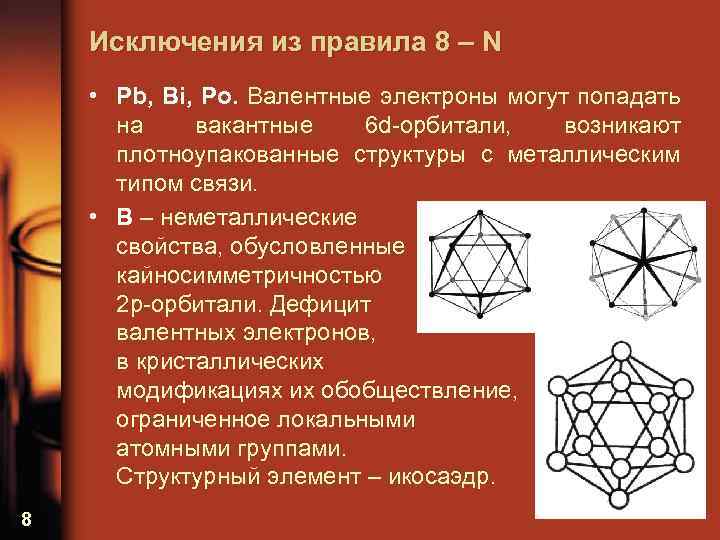
Исключения из правила 8 – N • Pb, Bi, Po. Валентные электроны могут попадать на вакантные 6 d-орбитали, возникают плотноупакованные структуры с металлическим типом связи. • B – неметаллические свойства, обусловленные кайносимметричностью 2 p-орбитали. Дефицит валентных электронов, в кристаллических модификациях их обобществление, ограниченное локальными атомными группами. Структурный элемент – икосаэдр. 8

• Диагональная граница между металлами и неметаллами проходит от B к At между элементами: B – Al, Si – Ge, As – Sb, Te – Po. 9 • Al, Ga, In, Sb, As – расположены вблизи диагональной границы и одними свойствами напоминают металлы, по другим – неметаллы.

Физические свойства простых веществ
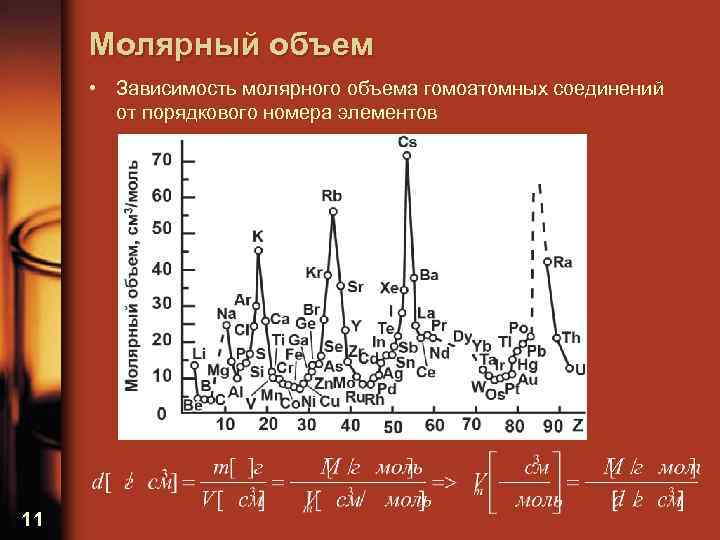
Молярный объем • Зависимость молярного объема гомоатомных соединений от порядкового номера элементов 11
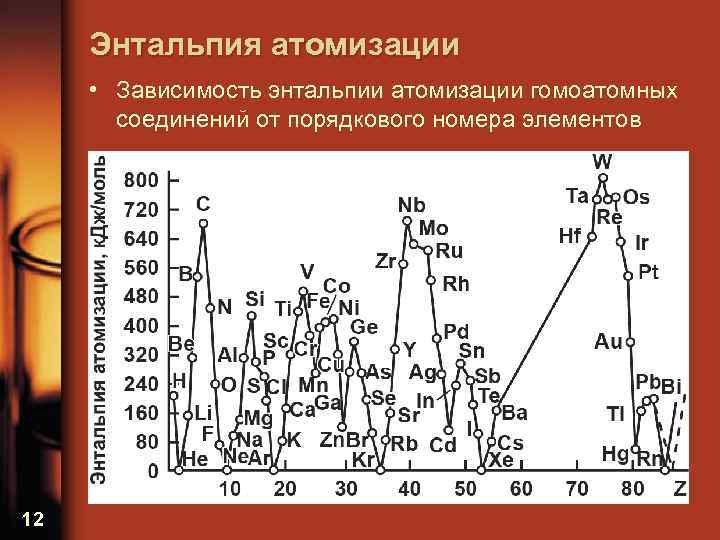
Энтальпия атомизации • Зависимость энтальпии атомизации гомоатомных соединений от порядкового номера элементов 12
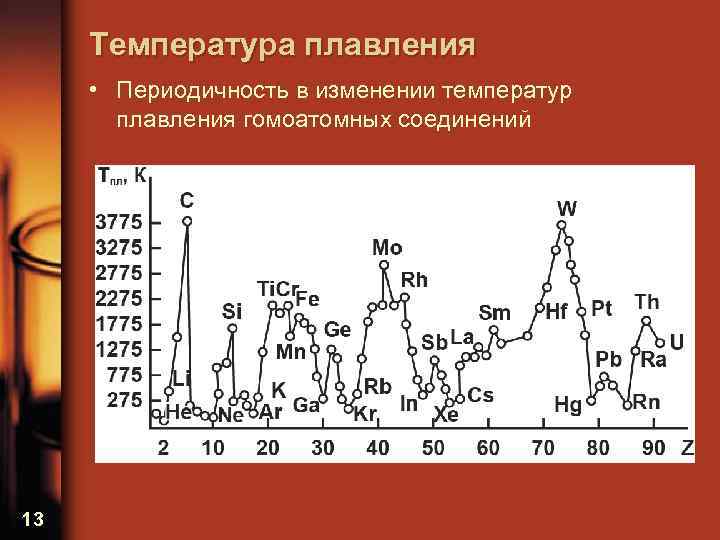
Температура плавления • Периодичность в изменении температур плавления гомоатомных соединений 13
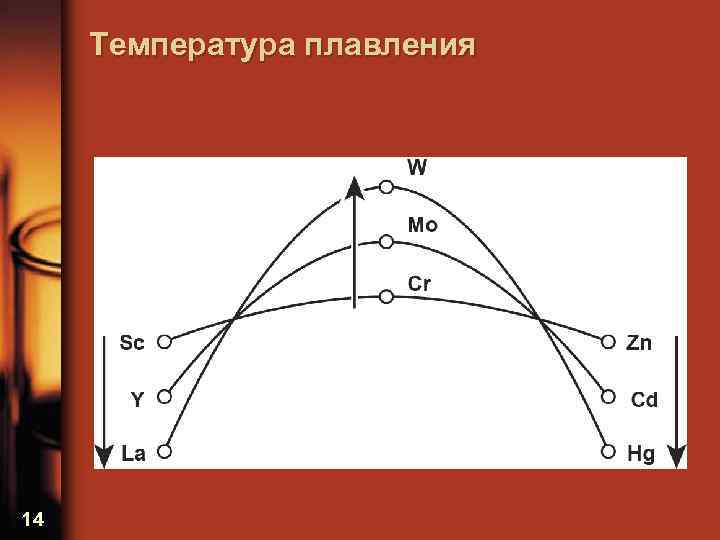
Температура плавления 14

Энергии диссоциации двухатомных молекул гомоатомных соединений 15

Химические свойства простых веществ
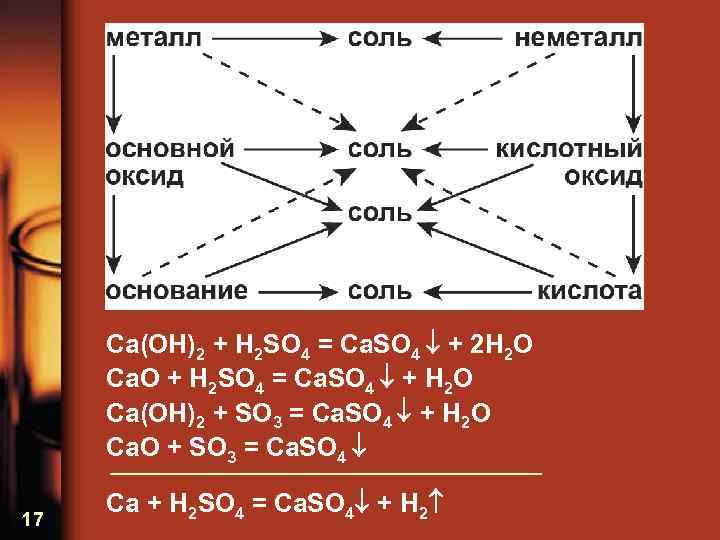
Ca(OH)2 + H 2 SO 4 = Ca. SO 4 + 2 H 2 O Ca. O + H 2 SO 4 = Ca. SO 4 + H 2 O Ca(OH)2 + SO 3 = Ca. SO 4 + H 2 O Ca. O + SO 3 = Ca. SO 4 17 Ca + H 2 SO 4 = Ca. SO 4 + H 2
3 Простые вещества.ppt