Лекция_04_изомерия КБ.ppt
- Количество слайдов: 35
 Пространственная изомерия органических соединений Лекция 4
Пространственная изомерия органических соединений Лекция 4
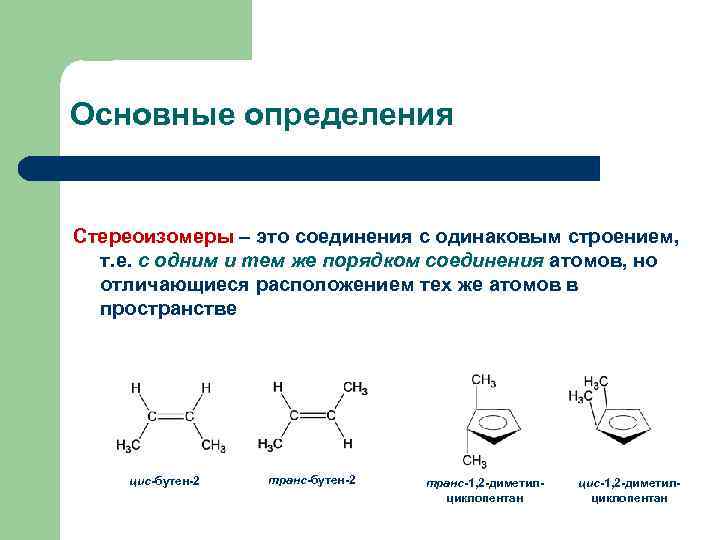 Основные определения Стереоизомеры – это соединения с одинаковым строением, т. е. с одним и тем же порядком соединения атомов, но отличающиеся расположением тех же атомов в пространстве цис-бутен-2 транс-1, 2 -диметилциклопентан цис-1, 2 -диметилциклопентан
Основные определения Стереоизомеры – это соединения с одинаковым строением, т. е. с одним и тем же порядком соединения атомов, но отличающиеся расположением тех же атомов в пространстве цис-бутен-2 транс-1, 2 -диметилциклопентан цис-1, 2 -диметилциклопентан
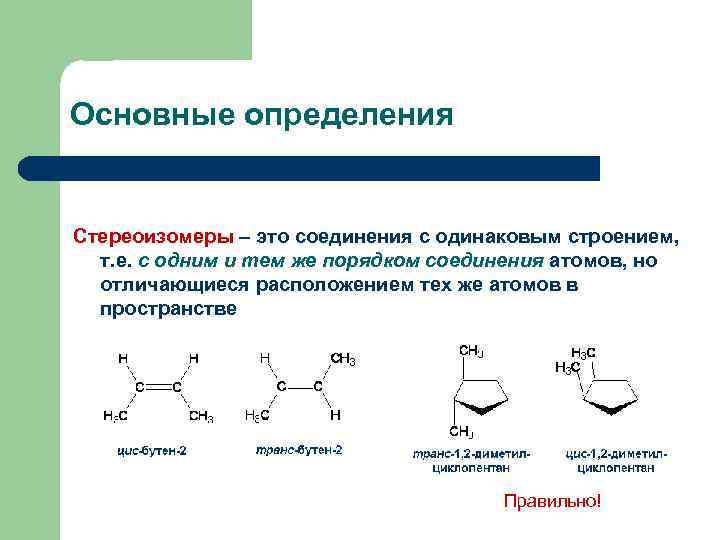 Основные определения Стереоизомеры – это соединения с одинаковым строением, т. е. с одним и тем же порядком соединения атомов, но отличающиеся расположением тех же атомов в пространстве Правильно!
Основные определения Стереоизомеры – это соединения с одинаковым строением, т. е. с одним и тем же порядком соединения атомов, но отличающиеся расположением тех же атомов в пространстве Правильно!
 Основные определения Стереоизомеры Конфигурационные • Могут существовать в виде индивидуальных форм • Могут быть выделены в виде самостоятельно существующих веществ • Каждый изомер обладает определенными физическими и химическими свойствами Конформационные (конформации, конформеры) • Существуют все вместе в виде единого множества геометрических форм молекул • Возникают в результате вращения отдельных фрагментов молекул вокруг простых связей • Взаимопревращение конформеров не сопровождается разрывом связей Конформация – пространственное расположение атомов в молекуле, которое может изменяться при вращении и изгибе связей Конфигурация – пространственное расположение атомов в молекуле, которое не может изменяться при вращении и изгибе связей
Основные определения Стереоизомеры Конфигурационные • Могут существовать в виде индивидуальных форм • Могут быть выделены в виде самостоятельно существующих веществ • Каждый изомер обладает определенными физическими и химическими свойствами Конформационные (конформации, конформеры) • Существуют все вместе в виде единого множества геометрических форм молекул • Возникают в результате вращения отдельных фрагментов молекул вокруг простых связей • Взаимопревращение конформеров не сопровождается разрывом связей Конформация – пространственное расположение атомов в молекуле, которое может изменяться при вращении и изгибе связей Конфигурация – пространственное расположение атомов в молекуле, которое не может изменяться при вращении и изгибе связей
 Внутримолекулярное вращение по σсвязям http: // www. chemistry. ssu. samara. ru
Внутримолекулярное вращение по σсвязям http: // www. chemistry. ssu. samara. ru
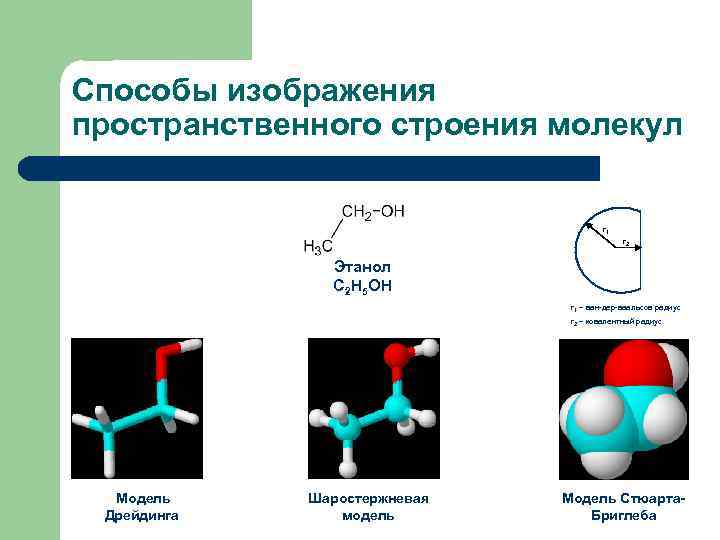 Способы изображения пространственного строения молекул r 1 r 2 Этанол С 2 Н 5 ОН r 1 – ван-дер-ваальсов радиус r 2 – ковалентный радиус Модель Дрейдинга Шаростержневая модель Модель Стюарта. Бриглеба
Способы изображения пространственного строения молекул r 1 r 2 Этанол С 2 Н 5 ОН r 1 – ван-дер-ваальсов радиус r 2 – ковалентный радиус Модель Дрейдинга Шаростержневая модель Модель Стюарта. Бриглеба
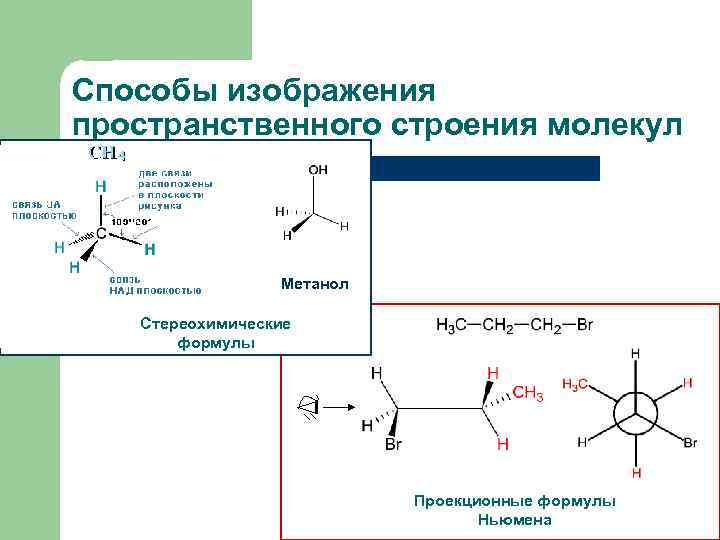 Способы изображения пространственного строения молекул Метанол Стереохимические формулы Проекционные формулы Ньюмена
Способы изображения пространственного строения молекул Метанол Стереохимические формулы Проекционные формулы Ньюмена
 Проекционные формулы Фишера Молекулы, имеющие в своем составе ассиметрические атомы углерода (тетраэдрические атомы с четырьмя разными заместителями) Структура молекулы изображается в виде двухмерного скелета с горизонтальными и вертикальными линиями Молочная кислота Перестановка двух заместителей = переход к другому энантиомеру Поворот на 90° = переход к другому энантиомеру Поворот на 180° = тот же самый энантиомер
Проекционные формулы Фишера Молекулы, имеющие в своем составе ассиметрические атомы углерода (тетраэдрические атомы с четырьмя разными заместителями) Структура молекулы изображается в виде двухмерного скелета с горизонтальными и вертикальными линиями Молочная кислота Перестановка двух заместителей = переход к другому энантиомеру Поворот на 90° = переход к другому энантиомеру Поворот на 180° = тот же самый энантиомер
 Стереохимическая номенклатура: R, Sсистема (Р. Кан, К. Ингольд, В. Прелог (1951)) Правила последовательности Кана-Ингольда-Прелога – определение старшинства заместителей 2 -гидроксипропановая кислота Старшинство заместителей убывает по часовой стрелке (лат. rectus – правый) Старшинство заместителей убывает против часовой стрелки (лат. sinister – левый) Младший заместитель (Н) направлен за плоскость рисунка, от нас
Стереохимическая номенклатура: R, Sсистема (Р. Кан, К. Ингольд, В. Прелог (1951)) Правила последовательности Кана-Ингольда-Прелога – определение старшинства заместителей 2 -гидроксипропановая кислота Старшинство заместителей убывает по часовой стрелке (лат. rectus – правый) Старшинство заместителей убывает против часовой стрелки (лат. sinister – левый) Младший заместитель (Н) направлен за плоскость рисунка, от нас
 Правила старшинства заместителей Кана-Прелога-Ингольда Учитывается: 1) 2) 3) 4) 5) 6) Атомный номер Атомная масса (в случае изотопов) Неподеленная электронная пара – самый младший заместитель Если у ближайшего атома показатели совпадают, старшинство определяют по второму, третьему и т. д. слоям атомов Наличие кратных связей Стереохимия заместителей и пр.
Правила старшинства заместителей Кана-Прелога-Ингольда Учитывается: 1) 2) 3) 4) 5) 6) Атомный номер Атомная масса (в случае изотопов) Неподеленная электронная пара – самый младший заместитель Если у ближайшего атома показатели совпадают, старшинство определяют по второму, третьему и т. д. слоям атомов Наличие кратных связей Стереохимия заместителей и пр.
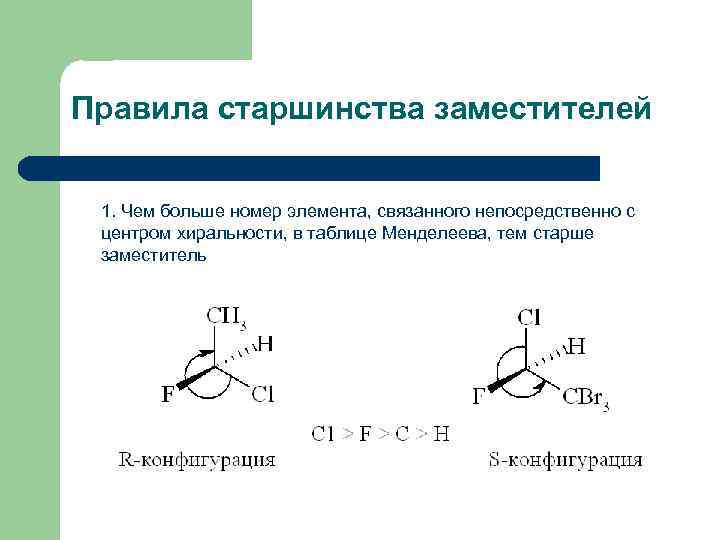 Правила старшинства заместителей 1. Чем больше номер элемента, связанного непосредственно с центром хиральности, в таблице Менделеева, тем старше заместитель
Правила старшинства заместителей 1. Чем больше номер элемента, связанного непосредственно с центром хиральности, в таблице Менделеева, тем старше заместитель
 Правила старшинства заместителей 2. Неподеленная пара электронов (НПЭ) - самый младший заместитель
Правила старшинства заместителей 2. Неподеленная пара электронов (НПЭ) - самый младший заместитель
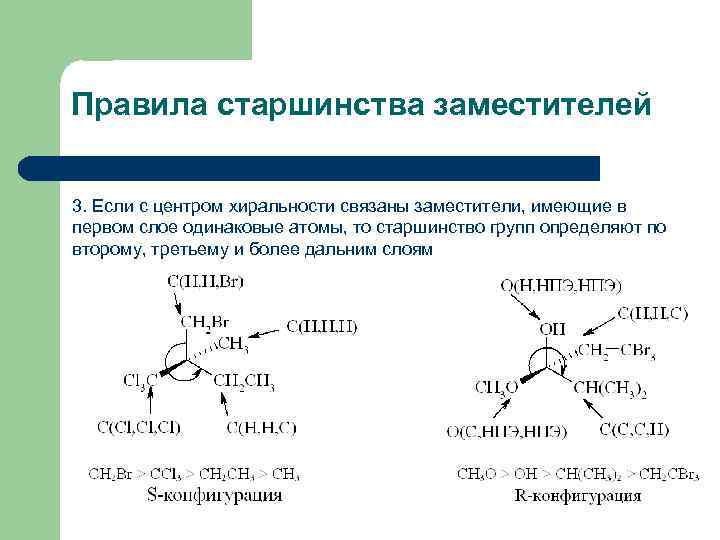 Правила старшинства заместителей 3. Если с центром хиральности связаны заместители, имеющие в первом слое одинаковые атомы, то старшинство групп определяют по второму, третьему и более дальним слоям
Правила старшинства заместителей 3. Если с центром хиральности связаны заместители, имеющие в первом слое одинаковые атомы, то старшинство групп определяют по второму, третьему и более дальним слоям
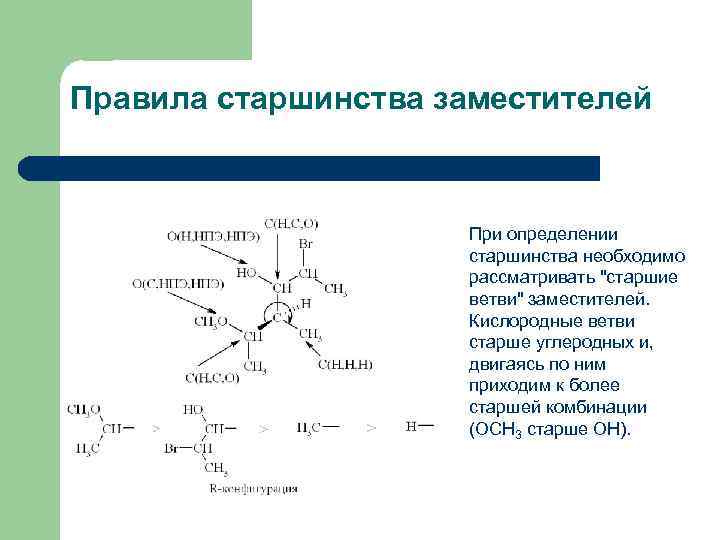 Правила старшинства заместителей При определении старшинства необходимо рассматривать "старшие ветви" заместителей. Кислородные ветви старше углеродных и, двигаясь по ним приходим к более старшей комбинации (ОСН 3 старше ОН).
Правила старшинства заместителей При определении старшинства необходимо рассматривать "старшие ветви" заместителей. Кислородные ветви старше углеродных и, двигаясь по ним приходим к более старшей комбинации (ОСН 3 старше ОН).
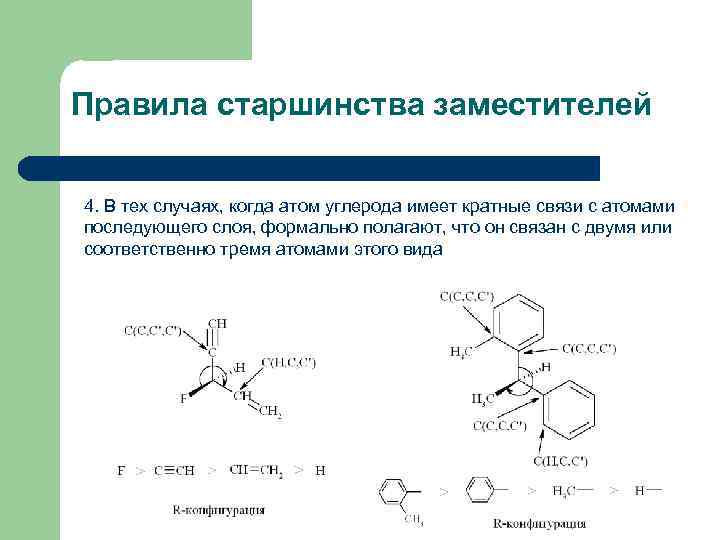 Правила старшинства заместителей 4. В тех случаях, когда атом углерода имеет кратные связи с атомами последующего слоя, формально полагают, что он связан с двумя или соответственно тремя атомами этого вида
Правила старшинства заместителей 4. В тех случаях, когда атом углерода имеет кратные связи с атомами последующего слоя, формально полагают, что он связан с двумя или соответственно тремя атомами этого вида
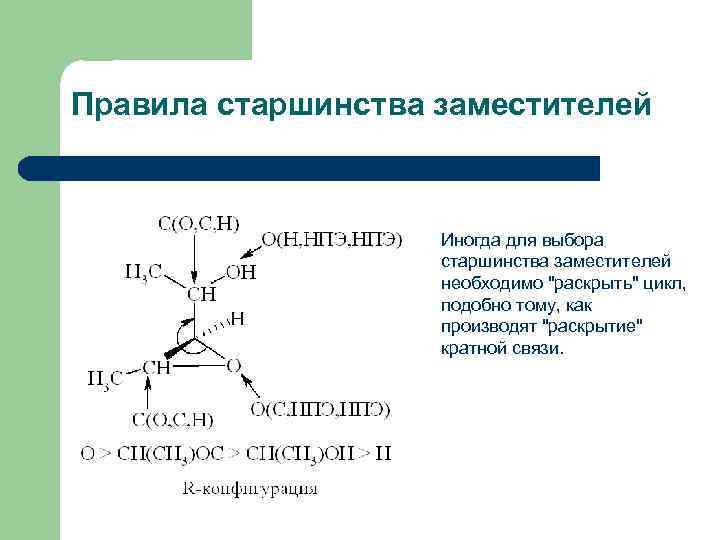 Правила старшинства заместителей Иногда для выбора старшинства заместителей необходимо "раскрыть" цикл, подобно тому, как производят "раскрытие" кратной связи.
Правила старшинства заместителей Иногда для выбора старшинства заместителей необходимо "раскрыть" цикл, подобно тому, как производят "раскрытие" кратной связи.
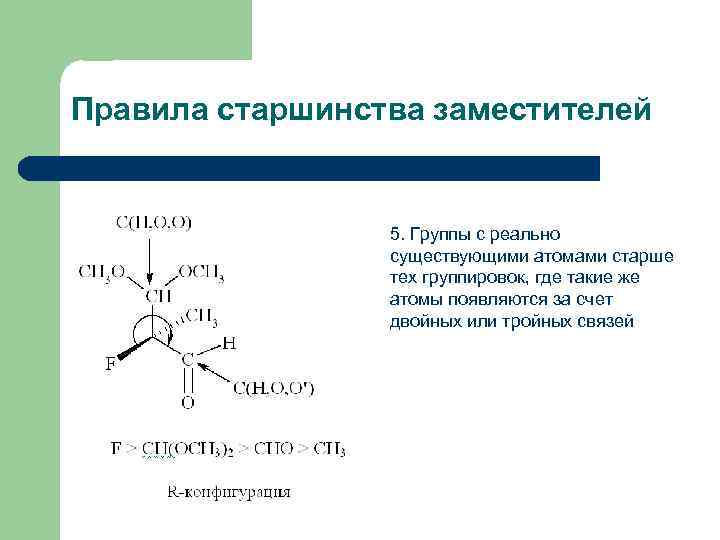 Правила старшинства заместителей 5. Группы с реально существующими атомами старше тех группировок, где такие же атомы появляются за счет двойных или тройных связей
Правила старшинства заместителей 5. Группы с реально существующими атомами старше тех группировок, где такие же атомы появляются за счет двойных или тройных связей
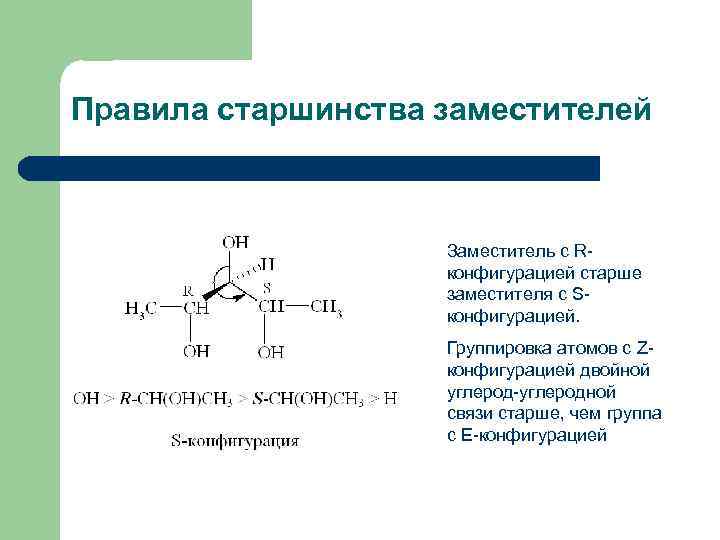 Правила старшинства заместителей Заместитель с Rконфигурацией старше заместителя с Sконфигурацией. Группировка атомов с Zконфигурацией двойной углерод-углеродной связи старше, чем группа с Е-конфигурацией
Правила старшинства заместителей Заместитель с Rконфигурацией старше заместителя с Sконфигурацией. Группировка атомов с Zконфигурацией двойной углерод-углеродной связи старше, чем группа с Е-конфигурацией
 D, L-номенклатура (М. А. Розанов (1906)) L(-)-глицериновый альдегид левовращающий L-молочная кислота D(+)-глицериновый альдегид правовращающий L-аланин D-манноза L-манноза
D, L-номенклатура (М. А. Розанов (1906)) L(-)-глицериновый альдегид левовращающий L-молочная кислота D(+)-глицериновый альдегид правовращающий L-аланин D-манноза L-манноза
 Хиральность - отсутствие симметрии относительно правой и левой стороны. если отражение объекта в идеальном плоском зеркале отличается от самого объекта, то объекту присуща хиральность:
Хиральность - отсутствие симметрии относительно правой и левой стороны. если отражение объекта в идеальном плоском зеркале отличается от самого объекта, то объекту присуща хиральность:
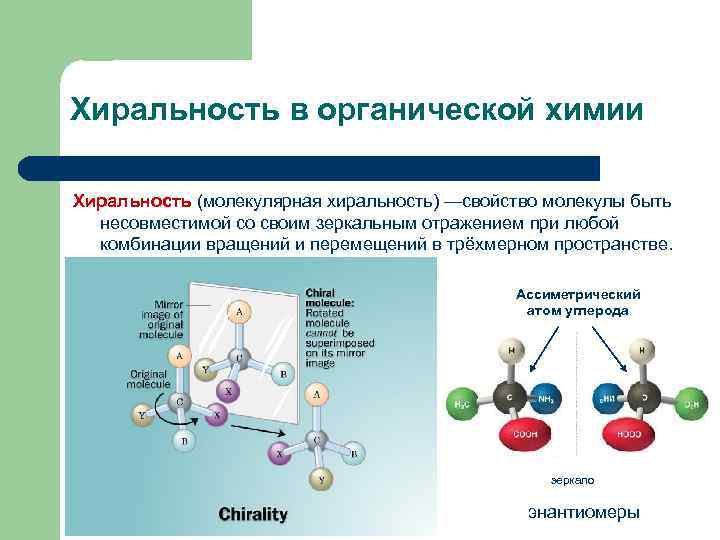 Хиральность в органической химии Хиральность (молекулярная хиральность) —свойство молекулы быть несовместимой со своим зеркальным отражением при любой комбинации вращений и перемещений в трёхмерном пространстве. Ассиметрический атом углерода зеркало энантиомеры
Хиральность в органической химии Хиральность (молекулярная хиральность) —свойство молекулы быть несовместимой со своим зеркальным отражением при любой комбинации вращений и перемещений в трёхмерном пространстве. Ассиметрический атом углерода зеркало энантиомеры
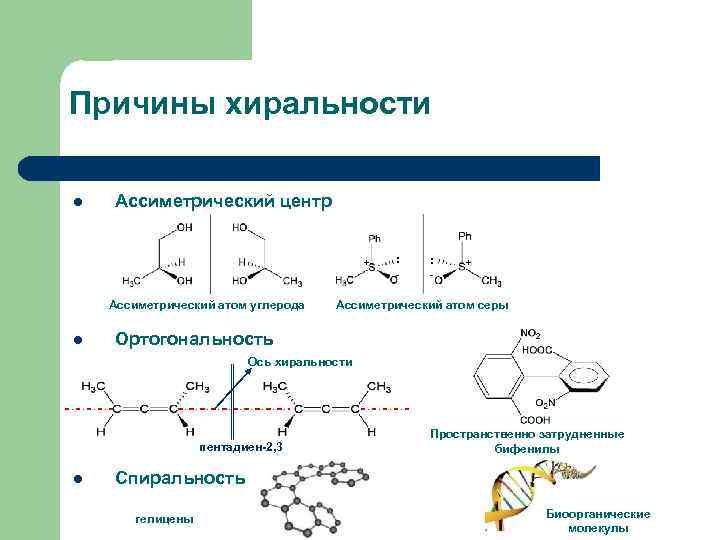 Причины хиральности l Ассиметрический центр Ассиметрический атом углерода l : : - + Ассиметрический атом серы Ортогональность Ось хиральности пентадиен-2, 3 l Пространственно затрудненные бифенилы Спиральность гелицены Биоорганические молекулы
Причины хиральности l Ассиметрический центр Ассиметрический атом углерода l : : - + Ассиметрический атом серы Ортогональность Ось хиральности пентадиен-2, 3 l Пространственно затрудненные бифенилы Спиральность гелицены Биоорганические молекулы
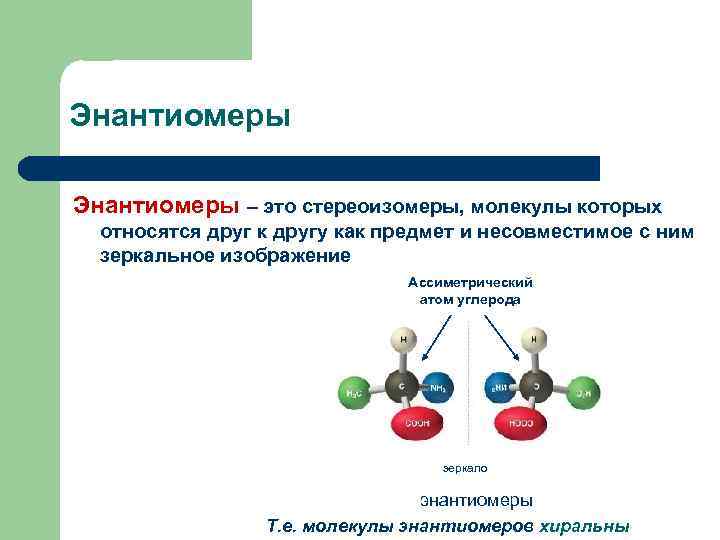 Энантиомеры – это стереоизомеры, молекулы которых относятся друг к другу как предмет и несовместимое с ним зеркальное изображение Ассиметрический атом углерода зеркало энантиомеры Т. е. молекулы энантиомеров хиральны
Энантиомеры – это стереоизомеры, молекулы которых относятся друг к другу как предмет и несовместимое с ним зеркальное изображение Ассиметрический атом углерода зеркало энантиомеры Т. е. молекулы энантиомеров хиральны
 Свойства энантиомеров • Одинаковые физические свойства - температура плавления, температура кипения - плотность - растворимость (в ахиральной среде) - показатель преломления • Одинаковые химические свойства в ахиральном окружении • Различная оптическая активность (способность отклонять плоскость плоскополяризованного света) - правовращающие (+) - левовращающие (-)
Свойства энантиомеров • Одинаковые физические свойства - температура плавления, температура кипения - плотность - растворимость (в ахиральной среде) - показатель преломления • Одинаковые химические свойства в ахиральном окружении • Различная оптическая активность (способность отклонять плоскость плоскополяризованного света) - правовращающие (+) - левовращающие (-)
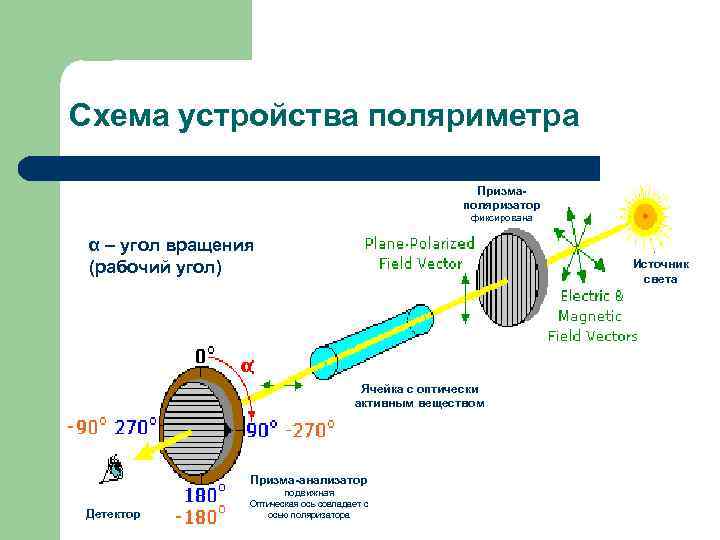 Схема устройства поляриметра Призмаполяризатор фиксирована α – угол вращения (рабочий угол) Источник света Ячейка с оптически активным веществом Призма-анализатор подвижная Детектор Оптическая ось совпадает с осью поляризатора
Схема устройства поляриметра Призмаполяризатор фиксирована α – угол вращения (рабочий угол) Источник света Ячейка с оптически активным веществом Призма-анализатор подвижная Детектор Оптическая ось совпадает с осью поляризатора
![Удельное вращение [α] - Сравнение оптической активности образцов Определение ЭИ Показатель качества природных компонентов Удельное вращение [α] - Сравнение оптической активности образцов Определение ЭИ Показатель качества природных компонентов](https://present5.com/presentation/3/49503650_275383598.pdf-img/49503650_275383598.pdf-26.jpg) Удельное вращение [α] - Сравнение оптической активности образцов Определение ЭИ Показатель качества природных компонентов (например, эфирных масел) Удельное вращение: α – наблюдаемое вращение образца, град С – концентрация l – длина кюветы, дм При температуре t ºC и λ = 589, 3 нм Энантиомерный избыток: %
Удельное вращение [α] - Сравнение оптической активности образцов Определение ЭИ Показатель качества природных компонентов (например, эфирных масел) Удельное вращение: α – наблюдаемое вращение образца, град С – концентрация l – длина кюветы, дм При температуре t ºC и λ = 589, 3 нм Энантиомерный избыток: %
 Рацемические смеси Рацемическая смесь (±) – смесь равных количеств двух энантиомеров Не обладает оптической активностью Энантиомерный избыток (ЭИ) = (доля энантиомера А - доля энантиомера В)× 100% R (+) S (-) Нерацемическая смесь: 80% (R)-1 -фенилэтиламина + 20% (S)-1 -фенилэтиламина = 60% ЭИ Рацемическая смесь: 50% (R)-1 -фенилэтиламина + 50% (S)-1 -фенилэтиламина = 0% ЭИ
Рацемические смеси Рацемическая смесь (±) – смесь равных количеств двух энантиомеров Не обладает оптической активностью Энантиомерный избыток (ЭИ) = (доля энантиомера А - доля энантиомера В)× 100% R (+) S (-) Нерацемическая смесь: 80% (R)-1 -фенилэтиламина + 20% (S)-1 -фенилэтиламина = 60% ЭИ Рацемическая смесь: 50% (R)-1 -фенилэтиламина + 50% (S)-1 -фенилэтиламина = 0% ЭИ
 Диастереомеры – это стереоизомеры, молекулы которых не относятся друг к другу как предмет и несовместимое с ним зеркальное отражение Соединения, молекулы которых имеют два и более центра хиральности Диастереомеры различаются по физико-химическим свойствам (температуры плавления, растворимость, теплоты образования, реакционная способность)
Диастереомеры – это стереоизомеры, молекулы которых не относятся друг к другу как предмет и несовместимое с ним зеркальное отражение Соединения, молекулы которых имеют два и более центра хиральности Диастереомеры различаются по физико-химическим свойствам (температуры плавления, растворимость, теплоты образования, реакционная способность)
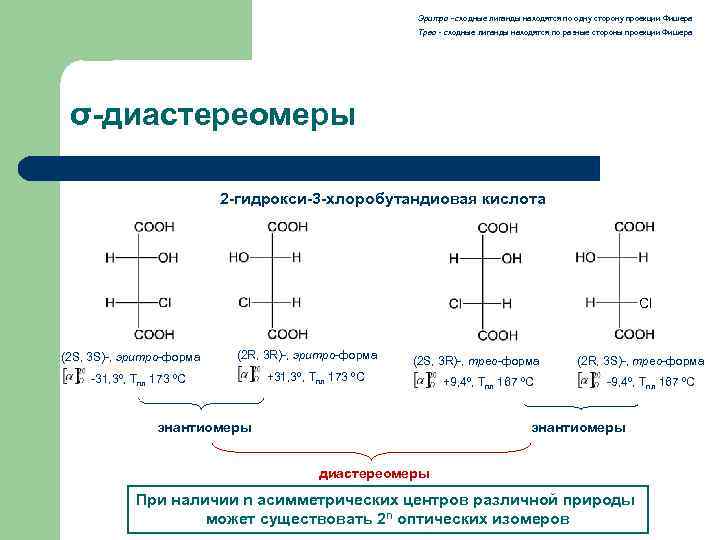 Эритро - сходные лиганды находятся по одну сторону проекции Фишера Трео - сходные лиганды находятся по разные стороны проекции Фишера σ-диастереомеры 2 -гидрокси-3 -хлоробутандиовая кислота Cl (2 S, 3 S)-, эритро-форма (2 R, 3 R)-, эритро-форма -31, 3º, Тпл 173 ºС (2 S, 3 R)-, трео-форма +31, 3º, Тпл 173 ºС энантиомеры +9, 4º, Тпл 167 ºС (2 R, 3 S)-, трео-форма -9, 4º, Тпл 167 ºС энантиомеры диастереомеры При наличии n асимметрических центров различной природы может существовать 2 n оптических изомеров
Эритро - сходные лиганды находятся по одну сторону проекции Фишера Трео - сходные лиганды находятся по разные стороны проекции Фишера σ-диастереомеры 2 -гидрокси-3 -хлоробутандиовая кислота Cl (2 S, 3 S)-, эритро-форма (2 R, 3 R)-, эритро-форма -31, 3º, Тпл 173 ºС (2 S, 3 R)-, трео-форма +31, 3º, Тпл 173 ºС энантиомеры +9, 4º, Тпл 167 ºС (2 R, 3 S)-, трео-форма -9, 4º, Тпл 167 ºС энантиомеры диастереомеры При наличии n асимметрических центров различной природы может существовать 2 n оптических изомеров
 мезо-Формы (2 R, 3 R)-винная кислота +12º, Тпл 170 ºС (2 S, 3 S)-винная кислота -12º, Тпл 170 ºС (2 R, 3 S)-винная кислота (2 S, 3 R)-винная кислота мезовинная кислота 0º, Тпл 140 ºС Оптически неактивна (ассиметрические атомы углерода обладают противоположной конфигурацией) Если возможно существование мезо-форм, то число стереоизомеров равно (2 n/2 -1)(2 n/2+1), если n – четное и 2 n-1, если n – нечетное число; n – число ассиметрических атомов углерода
мезо-Формы (2 R, 3 R)-винная кислота +12º, Тпл 170 ºС (2 S, 3 S)-винная кислота -12º, Тпл 170 ºС (2 R, 3 S)-винная кислота (2 S, 3 R)-винная кислота мезовинная кислота 0º, Тпл 140 ºС Оптически неактивна (ассиметрические атомы углерода обладают противоположной конфигурацией) Если возможно существование мезо-форм, то число стереоизомеров равно (2 n/2 -1)(2 n/2+1), если n – четное и 2 n-1, если n – нечетное число; n – число ассиметрических атомов углерода
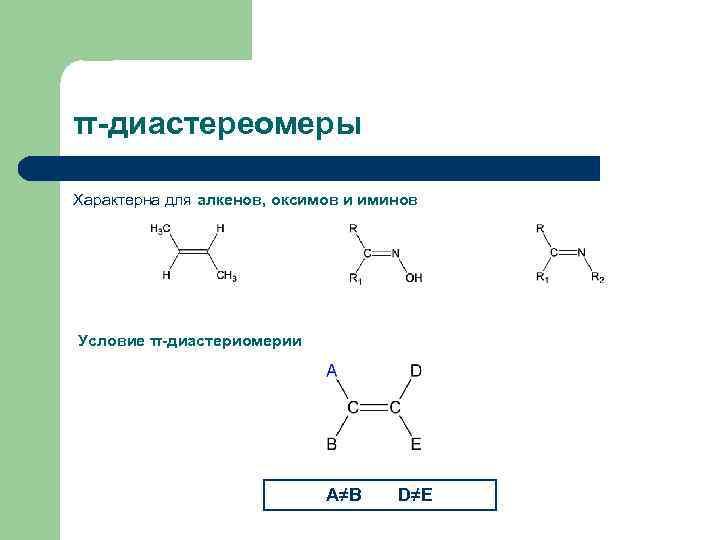 π-диастереомеры Характерна для алкенов, оксимов и иминов Условие π-диастериомерии A≠B D≠E
π-диастереомеры Характерна для алкенов, оксимов и иминов Условие π-диастериомерии A≠B D≠E
 π-диастереомеры В молекулах алкенов свободное вращение вокруг π-связи не происходит Вопрос: Возможна ли цис- транс-изомерия в молекулах алкинов?
π-диастереомеры В молекулах алкенов свободное вращение вокруг π-связи не происходит Вопрос: Возможна ли цис- транс-изомерия в молекулах алкинов?
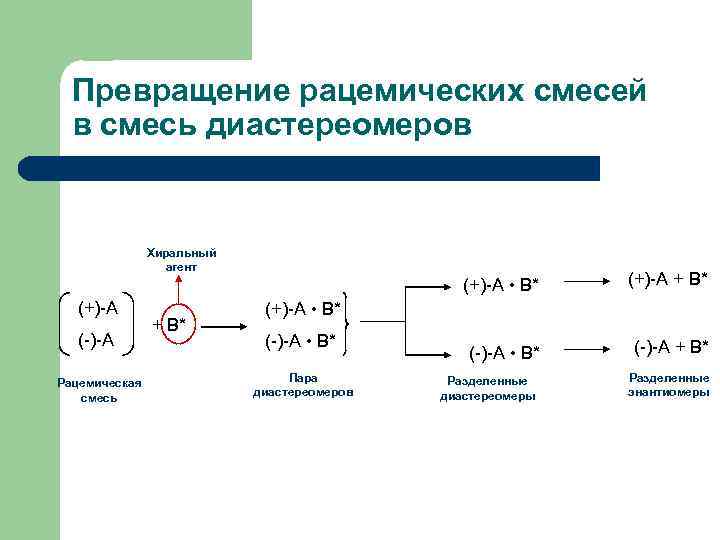 Превращение рацемических смесей в смесь диастереомеров Хиральный агент (+)-А • В* (+)-А (-)-А Рацемическая смесь + В* (+)-А + В* (-)-А • В* (-)-А + В* (+)-А • В* (-)-А • В* Пара диастереомеров Разделенные диастереомеры Разделенные энантиомеры
Превращение рацемических смесей в смесь диастереомеров Хиральный агент (+)-А • В* (+)-А (-)-А Рацемическая смесь + В* (+)-А + В* (-)-А • В* (-)-А + В* (+)-А • В* (-)-А • В* Пара диастереомеров Разделенные диастереомеры Разделенные энантиомеры
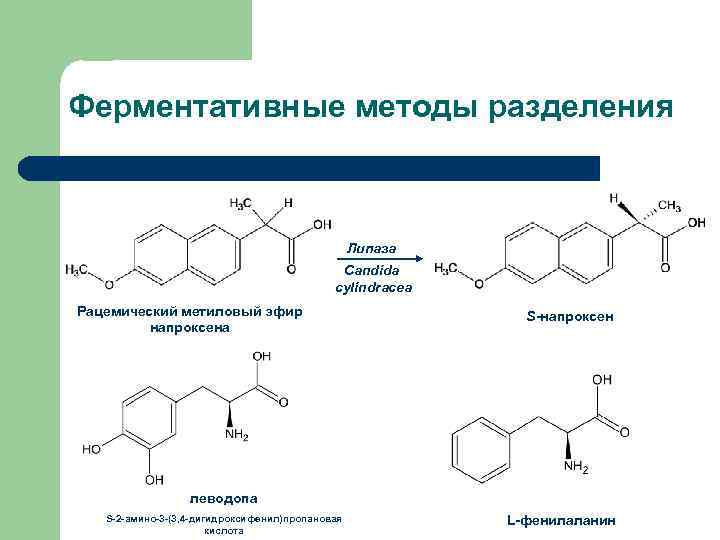 Ферментативные методы разделения Липаза Candida cylindracea Рацемический метиловый эфир напроксена S-напроксен леводопа S-2 -амино-3 -(3, 4 -дигидроксифенил)пропановая кислота L-фенилаланин
Ферментативные методы разделения Липаза Candida cylindracea Рацемический метиловый эфир напроксена S-напроксен леводопа S-2 -амино-3 -(3, 4 -дигидроксифенил)пропановая кислота L-фенилаланин
 Благодарю за внимание!
Благодарю за внимание!


