05 - Молекулы-2.pptx
- Количество слайдов: 75
 Пространственная форма и симметрия МО
Пространственная форма и симметрия МО
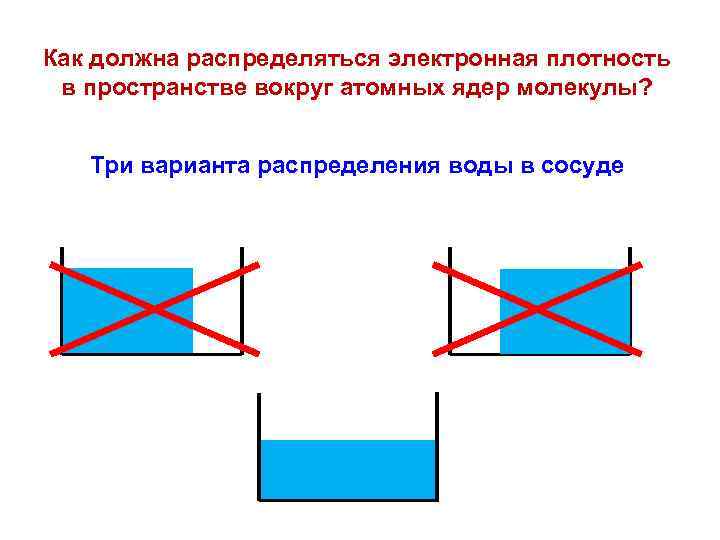 Как должна распределяться электронная плотность в пространстве вокруг атомных ядер молекулы? Три варианта распределения воды в сосуде
Как должна распределяться электронная плотность в пространстве вокруг атомных ядер молекулы? Три варианта распределения воды в сосуде
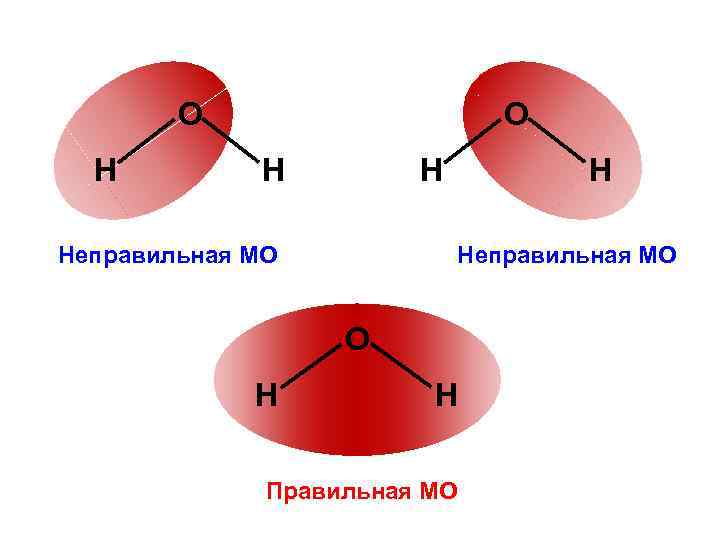 О Н Н Неправильная МО О Н Н Правильная МО
О Н Н Неправильная МО О Н Н Правильная МО
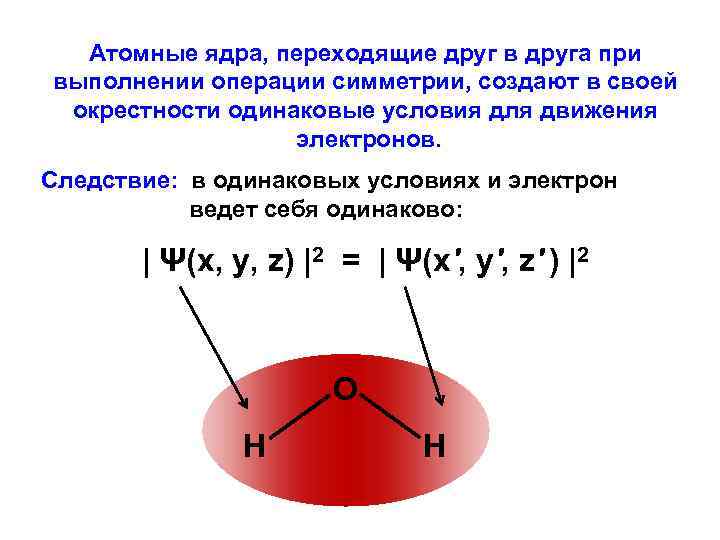 Атомные ядра, переходящие друг в друга при выполнении операции симметрии, создают в своей окрестности одинаковые условия для движения электронов. Следствие: в одинаковых условиях и электрон ведет себя одинаково: | Ψ(x, y, z) |2 = | Ψ(x', y', z' ) |2 О Н Н
Атомные ядра, переходящие друг в друга при выполнении операции симметрии, создают в своей окрестности одинаковые условия для движения электронов. Следствие: в одинаковых условиях и электрон ведет себя одинаково: | Ψ(x, y, z) |2 = | Ψ(x', y', z' ) |2 О Н Н
 21. 10. 15
21. 10. 15
 1. Пространственная форма МО не может быть произвольной и все допустимые варианты обусловлены формой самой молекулы. 2. Любая МО имеет определенную пространственную ФОРМУ и СИММЕТРИЮ. Пространственная симметрия МО Точечные группы симметрии Теория групп и их неприводимых представлений
1. Пространственная форма МО не может быть произвольной и все допустимые варианты обусловлены формой самой молекулы. 2. Любая МО имеет определенную пространственную ФОРМУ и СИММЕТРИЮ. Пространственная симметрия МО Точечные группы симметрии Теория групп и их неприводимых представлений
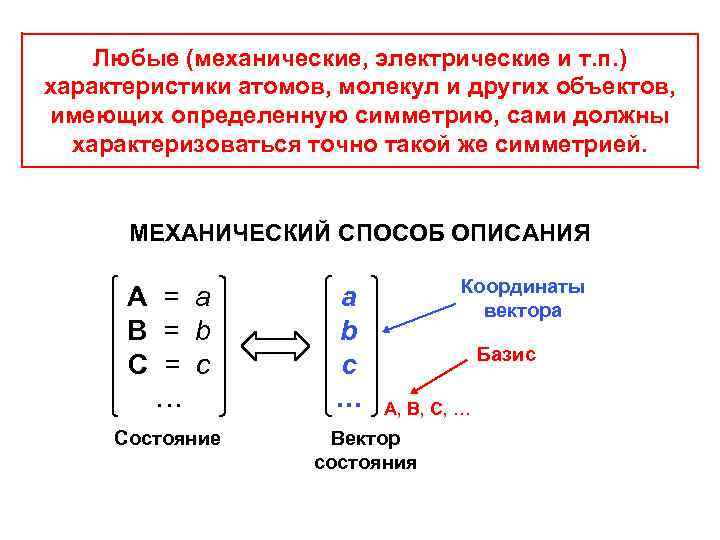 Любые (механические, электрические и т. п. ) характеристики атомов, молекул и других объектов, имеющих определенную симметрию, сами должны характеризоваться точно такой же симметрией. МЕХАНИЧЕСКИЙ СПОСОБ ОПИСАНИЯ А = а В = b C = c … Состояние а b c … Координаты вектора Базис А, В, C, … Вектор состояния
Любые (механические, электрические и т. п. ) характеристики атомов, молекул и других объектов, имеющих определенную симметрию, сами должны характеризоваться точно такой же симметрией. МЕХАНИЧЕСКИЙ СПОСОБ ОПИСАНИЯ А = а В = b C = c … Состояние а b c … Координаты вектора Базис А, В, C, … Вектор состояния
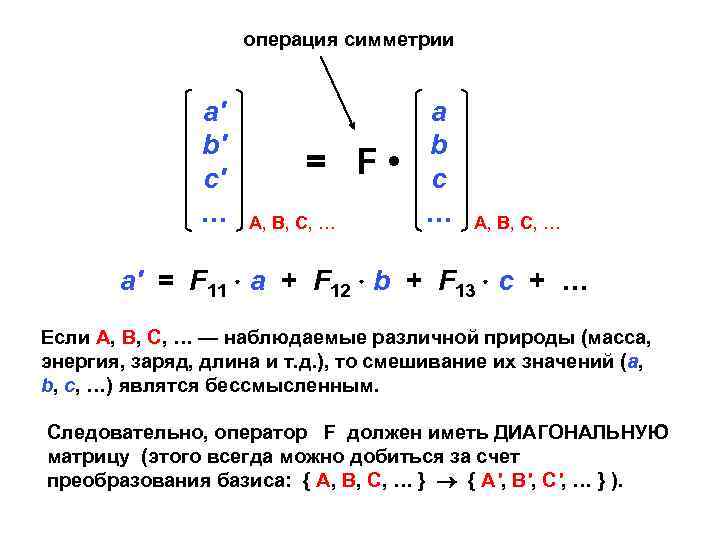 операция симметрии а′ b′ c′ … = F • А, В, C, … а b c … А, В, C, … a′ = F 11 a + F 12 b + F 13 c + … Если А, В, С, … — наблюдаемые различной природы (масса, энергия, заряд, длина и т. д. ), то смешивание их значений (a, b, c, …) являтся бессмысленным. Следовательно, оператор F должен иметь ДИАГОНАЛЬНУЮ матрицу (этого всегда можно добиться за счет преобразования базиса: { А, В, С, … } { А′, В′, С′, … } ).
операция симметрии а′ b′ c′ … = F • А, В, C, … а b c … А, В, C, … a′ = F 11 a + F 12 b + F 13 c + … Если А, В, С, … — наблюдаемые различной природы (масса, энергия, заряд, длина и т. д. ), то смешивание их значений (a, b, c, …) являтся бессмысленным. Следовательно, оператор F должен иметь ДИАГОНАЛЬНУЮ матрицу (этого всегда можно добиться за счет преобразования базиса: { А, В, С, … } { А′, В′, С′, … } ).
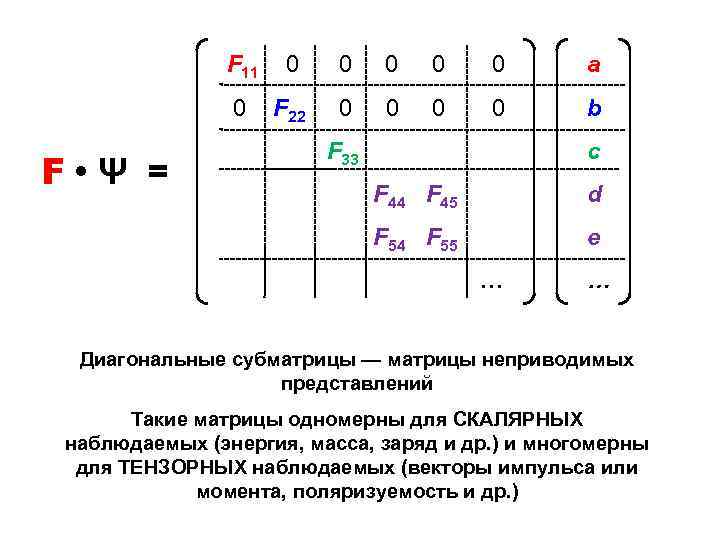 F 11 0 0 a 0 F • Ψ = 0 F 22 0 0 b F 33 c F 44 F 45 d F 54 F 55 e … … Диагональные субматрицы — матрицы неприводимых представлений Такие матрицы одномерны для СКАЛЯРНЫХ наблюдаемых (энергия, масса, заряд и др. ) и многомерны для ТЕНЗОРНЫХ наблюдаемых (векторы импульса или момента, поляризуемость и др. )
F 11 0 0 a 0 F • Ψ = 0 F 22 0 0 b F 33 c F 44 F 45 d F 54 F 55 e … … Диагональные субматрицы — матрицы неприводимых представлений Такие матрицы одномерны для СКАЛЯРНЫХ наблюдаемых (энергия, масса, заряд и др. ) и многомерны для ТЕНЗОРНЫХ наблюдаемых (векторы импульса или момента, поляризуемость и др. )
 Правило: каждая наблюдаемая «принадлежит» (относится, описывается) к одному из НП ТГС или «типов симметрии» Ψ НП ТГС Используя НП ТГС, можно решать два типа задач: • классификация наблюдаемых по типам симметрии (НП ТГС), • построение или выбор правильных в физическом отношении фундаментальных наборов наблюдаемых (базисов): такая процедура называется «симметризацией базиса» .
Правило: каждая наблюдаемая «принадлежит» (относится, описывается) к одному из НП ТГС или «типов симметрии» Ψ НП ТГС Используя НП ТГС, можно решать два типа задач: • классификация наблюдаемых по типам симметрии (НП ТГС), • построение или выбор правильных в физическом отношении фундаментальных наборов наблюдаемых (базисов): такая процедура называется «симметризацией базиса» .
 Классификация и построение МО
Классификация и построение МО
 Общие возможности Полный набор АО или МО всегда разбивается на группы, в соответствии с размерностями НП: • каждая орбиталь, описываемая одномерным НП, преобразуется операторами симметрии сама в себя и имеет свою индивидуальную энергию, • две орбитали, описываемые двумерными НП, преобразуются друг в друга и образуют дважды вырожденный энергетический уровень, • три орбитали, принадлежащие трехмерному НП, образуют трижды вырожденный уровень и т. д.
Общие возможности Полный набор АО или МО всегда разбивается на группы, в соответствии с размерностями НП: • каждая орбиталь, описываемая одномерным НП, преобразуется операторами симметрии сама в себя и имеет свою индивидуальную энергию, • две орбитали, описываемые двумерными НП, преобразуются друг в друга и образуют дважды вырожденный энергетический уровень, • три орбитали, принадлежащие трехмерному НП, образуют трижды вырожденный уровень и т. д.
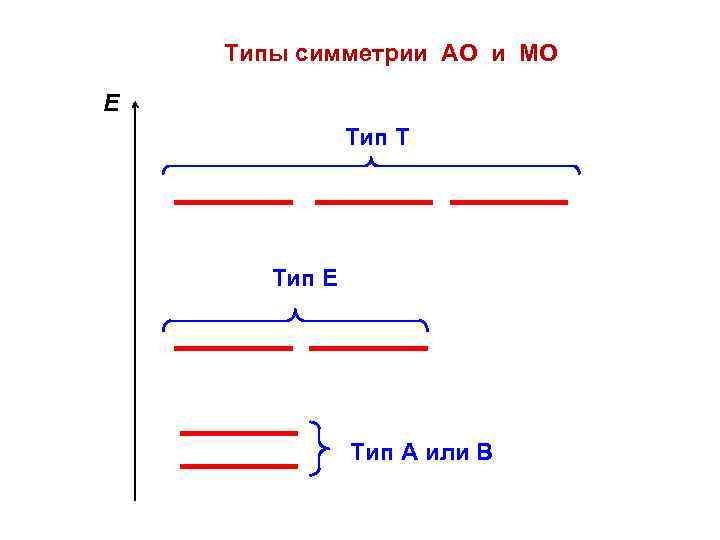 Типы симметрии АО и МО Е Тип Т Тип Е Тип А или В
Типы симметрии АО и МО Е Тип Т Тип Е Тип А или В
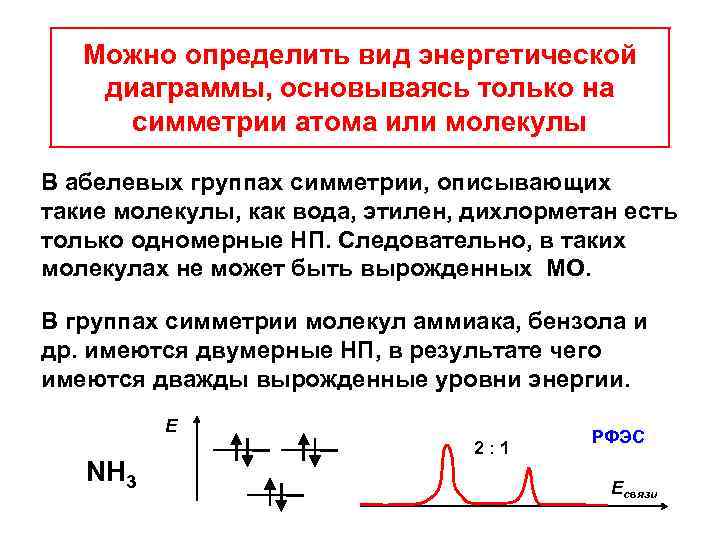 Можно определить вид энергетической диаграммы, основываясь только на симметрии атома или молекулы В абелевых группах симметрии, описывающих такие молекулы, как вода, этилен, дихлорметан есть только одномерные НП. Следовательно, в таких молекулах не может быть вырожденных МО. В группах симметрии молекул аммиака, бензола и др. имеются двумерные НП, в результате чего имеются дважды вырожденные уровни энергии. Е NH 3 2: 1 РФЭС Есвязи
Можно определить вид энергетической диаграммы, основываясь только на симметрии атома или молекулы В абелевых группах симметрии, описывающих такие молекулы, как вода, этилен, дихлорметан есть только одномерные НП. Следовательно, в таких молекулах не может быть вырожденных МО. В группах симметрии молекул аммиака, бензола и др. имеются двумерные НП, в результате чего имеются дважды вырожденные уровни энергии. Е NH 3 2: 1 РФЭС Есвязи
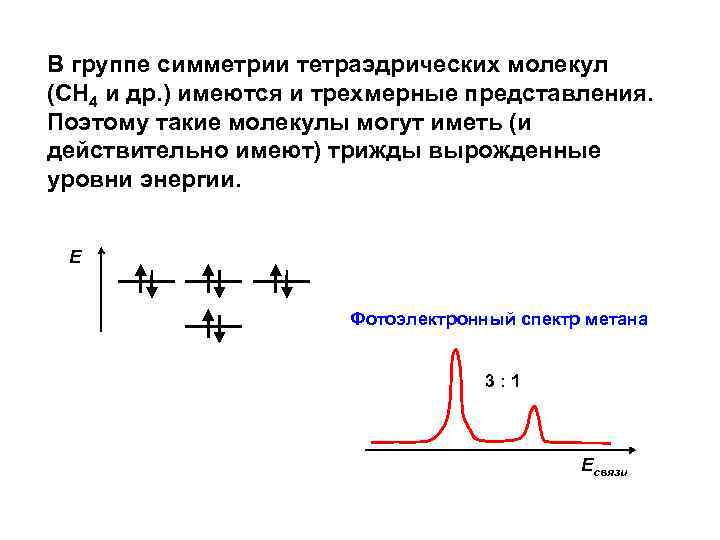 В группе симметрии тетраэдрических молекул (CH 4 и др. ) имеются и трехмерные представления. Поэтому такие молекулы могут иметь (и действительно имеют) трижды вырожденные уровни энергии. Е Фотоэлектронный спектр метана 3: 1 Есвязи
В группе симметрии тетраэдрических молекул (CH 4 и др. ) имеются и трехмерные представления. Поэтому такие молекулы могут иметь (и действительно имеют) трижды вырожденные уровни энергии. Е Фотоэлектронный спектр метана 3: 1 Есвязи
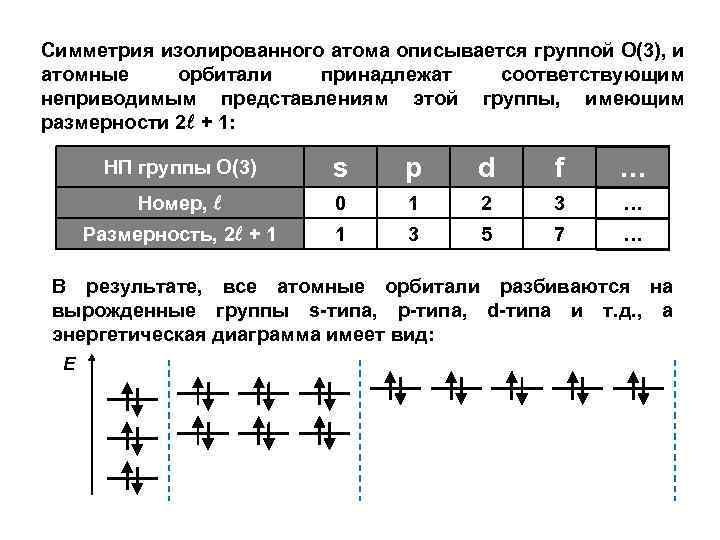 Симметрия изолированного атома описывается группой О(3), и атомные орбитали принадлежат соответствующим неприводимым представлениям этой группы, имеющим размерности 2 + 1: НП группы О(3) s p d f … Номер, 0 1 2 3 … Размерность, 2 + 1 1 3 5 7 … В результате, все атомные орбитали разбиваются на вырожденные группы s-типа, р-типа, d-типа и т. д. , а энергетическая диаграмма имеет вид: Е
Симметрия изолированного атома описывается группой О(3), и атомные орбитали принадлежат соответствующим неприводимым представлениям этой группы, имеющим размерности 2 + 1: НП группы О(3) s p d f … Номер, 0 1 2 3 … Размерность, 2 + 1 1 3 5 7 … В результате, все атомные орбитали разбиваются на вырожденные группы s-типа, р-типа, d-типа и т. д. , а энергетическая диаграмма имеет вид: Е
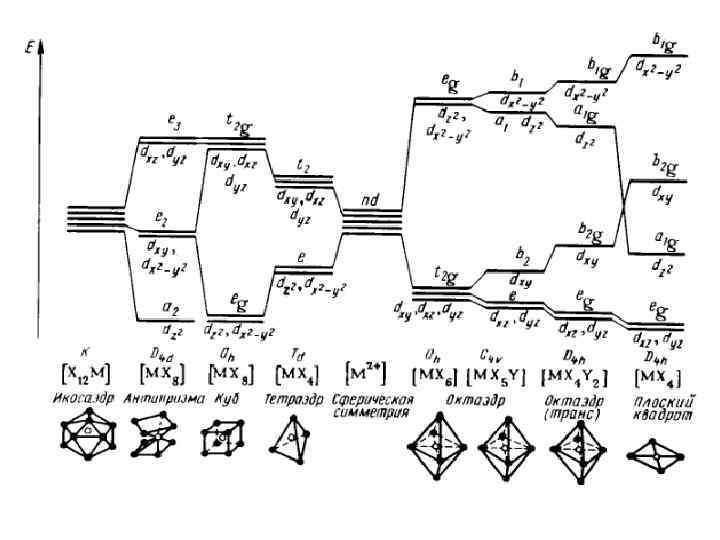
 Если окружить атом другими атомами, т. е. включить его в состав молекулы, то симметрия, очевидно, станет другой. Соответственно изменится и распределение АО по энергетическим уровням. Обычно симметрия понижается и сильно вырожденные группы АО расщепляются на более мелкие. Типичным примером являются комплексы переходных металлов (КПМ), в которых характер расщепления d-орбиталей полностью определяется симметрией окружения центрального иона. Теория кристаллического поля
Если окружить атом другими атомами, т. е. включить его в состав молекулы, то симметрия, очевидно, станет другой. Соответственно изменится и распределение АО по энергетическим уровням. Обычно симметрия понижается и сильно вырожденные группы АО расщепляются на более мелкие. Типичным примером являются комплексы переходных металлов (КПМ), в которых характер расщепления d-орбиталей полностью определяется симметрией окружения центрального иона. Теория кристаллического поля
 Построение волновых функций I. Метод ВС (валентных схем) Ψ = С 1 Ψ 1 + С 2 Ψ 2 + … + С n Ψn Базисный набор (волновые функции «резонансных форм» ) Резонансная форма (РФ) — особое состояние молекулы, приготавливаемое специальным прибором, «измеряющим» принадлежность электронов химическим атомам молекулы
Построение волновых функций I. Метод ВС (валентных схем) Ψ = С 1 Ψ 1 + С 2 Ψ 2 + … + С n Ψn Базисный набор (волновые функции «резонансных форм» ) Резонансная форма (РФ) — особое состояние молекулы, приготавливаемое специальным прибором, «измеряющим» принадлежность электронов химическим атомам молекулы
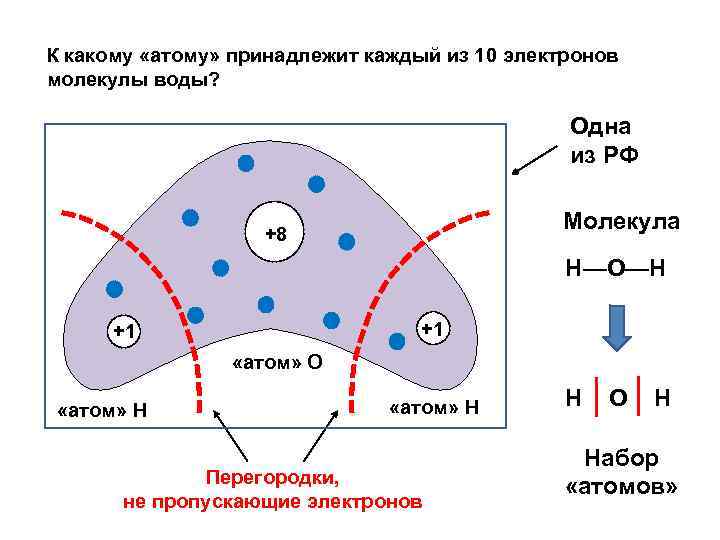 К какому «атому» принадлежит каждый из 10 электронов молекулы воды? Одна из РФ Молекула +8 Н—О—Н +1 +1 «атом» О «атом» Н Перегородки, не пропускающие электронов Н О Н Набор «атомов»
К какому «атому» принадлежит каждый из 10 электронов молекулы воды? Одна из РФ Молекула +8 Н—О—Н +1 +1 «атом» О «атом» Н Перегородки, не пропускающие электронов Н О Н Набор «атомов»
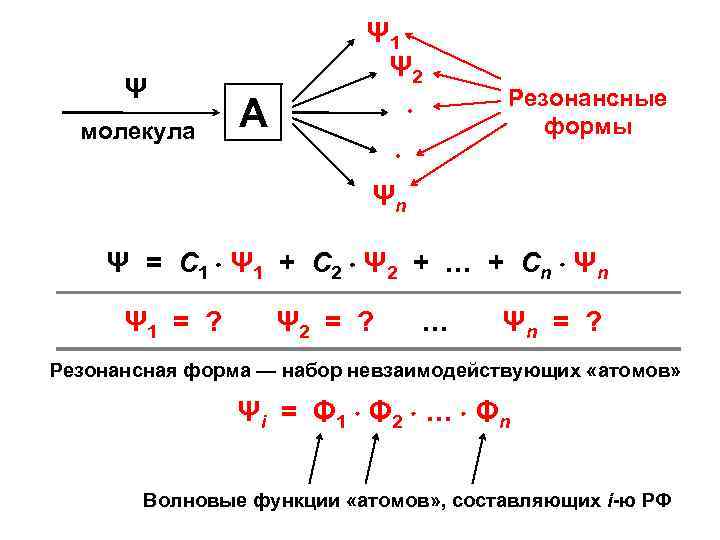 Ψ молекула Ψ 1 Ψ 2 А • Резонансные формы • Ψn Ψ = С 1 Ψ 1 + С 2 Ψ 2 + … + С n Ψn Ψ 1 = ? Ψ 2 = ? … Ψn = ? Резонансная форма — набор невзаимодействующих «атомов» Ψi = Φ 1 Φ 2 … Φ n Волновые функции «атомов» , составляющих i-ю РФ
Ψ молекула Ψ 1 Ψ 2 А • Резонансные формы • Ψn Ψ = С 1 Ψ 1 + С 2 Ψ 2 + … + С n Ψn Ψ 1 = ? Ψ 2 = ? … Ψn = ? Резонансная форма — набор невзаимодействующих «атомов» Ψi = Φ 1 Φ 2 … Φ n Волновые функции «атомов» , составляющих i-ю РФ
 Построение волновой функции молекулы в методе ВС 1) определение набора РФ (всех возможных способов распределения электронов молекулы по «атомам» ); 2) составление для каждого «атома» атомной волновой функции и ее оптимизация, например, методом самосогласованного поля Хартри-Фока; 3) построение волновых функций РФ в виде произведений атомных волновых функций; 4) составление линейной комбинации общего вида из волновых функций РФ; 5) оптимизация набора коэффициентов (С 1, С 2, . . . , Cn) построенной линейной комбинации.
Построение волновой функции молекулы в методе ВС 1) определение набора РФ (всех возможных способов распределения электронов молекулы по «атомам» ); 2) составление для каждого «атома» атомной волновой функции и ее оптимизация, например, методом самосогласованного поля Хартри-Фока; 3) построение волновых функций РФ в виде произведений атомных волновых функций; 4) составление линейной комбинации общего вида из волновых функций РФ; 5) оптимизация набора коэффициентов (С 1, С 2, . . . , Cn) построенной линейной комбинации.
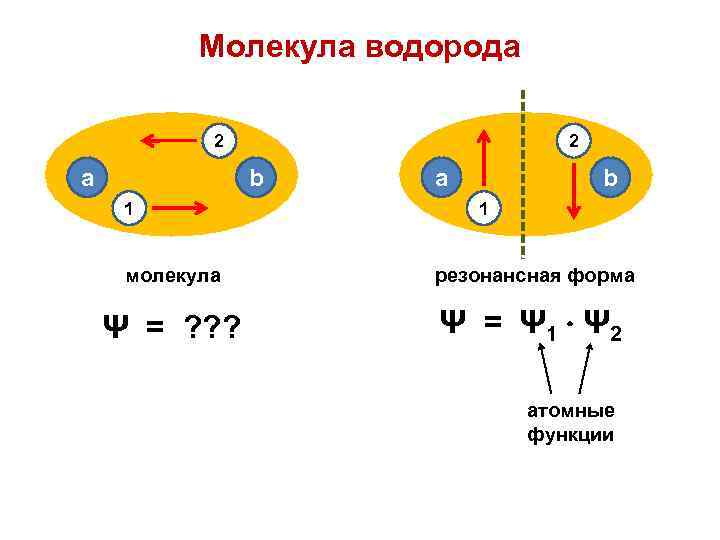 Молекула водорода 2 a 2 b 1 a b 1 молекула резонансная форма Ψ = ? ? ? Ψ = Ψ 1 Ψ 2 атомные функции
Молекула водорода 2 a 2 b 1 a b 1 молекула резонансная форма Ψ = ? ? ? Ψ = Ψ 1 Ψ 2 атомные функции
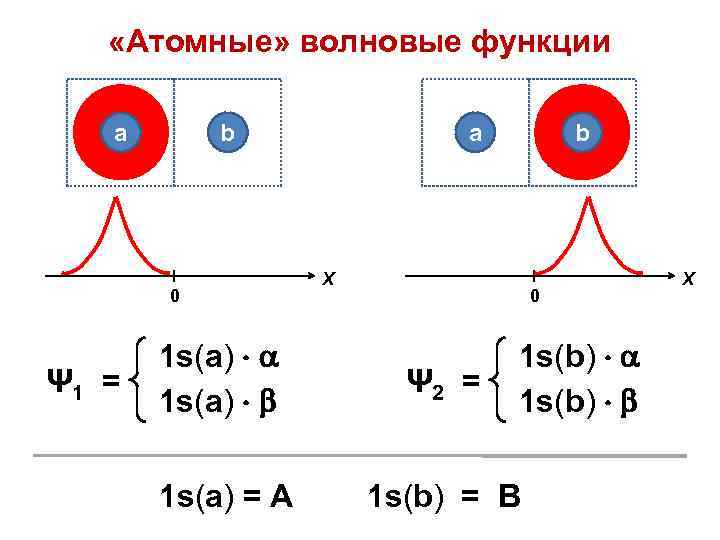 «Атомные» волновые функции a b 0 Ψ 1 = a b Х 0 1 s(a) 1 s(b) Ψ 2 = 1 s(a) = A 1 s(b) = B Х
«Атомные» волновые функции a b 0 Ψ 1 = a b Х 0 1 s(a) 1 s(b) Ψ 2 = 1 s(a) = A 1 s(b) = B Х
 Резонансные формы Ковалентные формы 1 2 Ψ 1 = A B 1 2 Ψ 5 = A B 1 2 Ψ 2 = A B 1 2 Ψ 6 = A B 2 1 Ψ 3 = B A 2 1 Ψ 7 = B A 2 1 Ψ 4 = B A 2 1 Ψ 8 = B A Ионные формы A A Ψ 9 = A A 1 2 = A A – A A Ψ 10 = B B = B B – B B
Резонансные формы Ковалентные формы 1 2 Ψ 1 = A B 1 2 Ψ 5 = A B 1 2 Ψ 2 = A B 1 2 Ψ 6 = A B 2 1 Ψ 3 = B A 2 1 Ψ 7 = B A 2 1 Ψ 4 = B A 2 1 Ψ 8 = B A Ионные формы A A Ψ 9 = A A 1 2 = A A – A A Ψ 10 = B B = B B – B B
 Волновые функции резонансных форм Ψ 1 = A B = AB Ψ 5 = A B = AB Ψ 2 = A B = AB Ψ 6 = A B = AB Ψ 3 = B A = BA Ψ 7 = B A = BA Ψ 4 = B A = BA Ψ 8 = B A = BA Ψ 9 = A A – A A = AA[ – ] Ψ 10 = B B – B B = BB[ – ] Ψ = С 1 Ψ 1 + С 2 Ψ 2 + … + С 10 Ψ 10
Волновые функции резонансных форм Ψ 1 = A B = AB Ψ 5 = A B = AB Ψ 2 = A B = AB Ψ 6 = A B = AB Ψ 3 = B A = BA Ψ 7 = B A = BA Ψ 4 = B A = BA Ψ 8 = B A = BA Ψ 9 = A A – A A = AA[ – ] Ψ 10 = B B – B B = BB[ – ] Ψ = С 1 Ψ 1 + С 2 Ψ 2 + … + С 10 Ψ 10
 Проверка перестановочной симметрии Электронная оболочка молекулы — фермионная система и должна удовлетворять принципу Паули: Ψ( pq ) = – Ψ( qp ) Ψas = С 1(Ψ 1)as + С 2(Ψ 2)as + … + С 10(Ψ 10)as Ψ 1 = A(1)B(2) (1) (2) P 12 Ψ 1 = A(2)B(1) (2) (1) = B(1)A(2) (1) (2) ≠ – Ψ 1 Функция Ψ 1 не является собственной для оператора Р 12 и, следовательно, ее нельзя считать ни симметричной, ни антисимметричной
Проверка перестановочной симметрии Электронная оболочка молекулы — фермионная система и должна удовлетворять принципу Паули: Ψ( pq ) = – Ψ( qp ) Ψas = С 1(Ψ 1)as + С 2(Ψ 2)as + … + С 10(Ψ 10)as Ψ 1 = A(1)B(2) (1) (2) P 12 Ψ 1 = A(2)B(1) (2) (1) = B(1)A(2) (1) (2) ≠ – Ψ 1 Функция Ψ 1 не является собственной для оператора Р 12 и, следовательно, ее нельзя считать ни симметричной, ни антисимметричной
 P 12 Ψ 1 = B(1)A(2) (1) (2) = BA = Ψ 3 Ψ 1 СИММЕТРИЗАЦИЯ Ψ 1 Ψ 3 P P Ψ 3 Ψ+ = Ψ 1 + Ψ 3 Ψ– = Ψ 1 – Ψ 3 P Ψ+ = P (AB + BA ) = (BA + AB ) = = (AB + BA ) = (+1) Ψ+ P Ψ– = P (AB – BA ) = (BA – AB ) = = – (AB – BA ) = (– 1) Ψ– Ψ+ — симметричная, Ψ– — антисимметричная
P 12 Ψ 1 = B(1)A(2) (1) (2) = BA = Ψ 3 Ψ 1 СИММЕТРИЗАЦИЯ Ψ 1 Ψ 3 P P Ψ 3 Ψ+ = Ψ 1 + Ψ 3 Ψ– = Ψ 1 – Ψ 3 P Ψ+ = P (AB + BA ) = (BA + AB ) = = (AB + BA ) = (+1) Ψ+ P Ψ– = P (AB – BA ) = (BA – AB ) = = – (AB – BA ) = (– 1) Ψ– Ψ+ — симметричная, Ψ– — антисимметричная
 Ψ = С 1Ψ 1 + С 2Ψ 2 + С 3Ψ 3 + … + С 10Ψ 10 Если С 3 = – С 1 , тогда Ψ = С 1Ψ 1 + С 2Ψ 2 – С 1Ψ 3 + … + С 10Ψ 10 = = С 1(Ψ 1 – Ψ 3)as + С 2Ψ 2 + … + С 10Ψ 10 С 3 С 4 С 7 С 8 = = – С 1 – С 2 – С 5 – С 6 Ψ = + + + С 1(Ψ 1 – Ψ 3)as + С 2(Ψ 2 – Ψ 4)as + С 5(Ψ 5 – Ψ 7)as + С 6(Ψ 6 – Ψ 8)as + С 9Ψ 9 + С 10Ψ 10
Ψ = С 1Ψ 1 + С 2Ψ 2 + С 3Ψ 3 + … + С 10Ψ 10 Если С 3 = – С 1 , тогда Ψ = С 1Ψ 1 + С 2Ψ 2 – С 1Ψ 3 + … + С 10Ψ 10 = = С 1(Ψ 1 – Ψ 3)as + С 2Ψ 2 + … + С 10Ψ 10 С 3 С 4 С 7 С 8 = = – С 1 – С 2 – С 5 – С 6 Ψ = + + + С 1(Ψ 1 – Ψ 3)as + С 2(Ψ 2 – Ψ 4)as + С 5(Ψ 5 – Ψ 7)as + С 6(Ψ 6 – Ψ 8)as + С 9Ψ 9 + С 10Ψ 10
 28. 10. 15
28. 10. 15
 СИММЕТРИЗАЦИЯ Ψ 1 Ψ 2 Ψ 3 Ψ 4 Ψ 5 Ψ 6 Ψ 7 Ψ 8 Φ 1 = Ψ 1 – Ψ 3 = AB – BA Φ 2 = Ψ 2 – Ψ 4 = AB – BA Φ 3 = Ψ 5 – Ψ 7 = AB – BA Φ 4 = Ψ 6 – Ψ 8 = AB – BA Φ 5 = Ψ 9 = AА – АA Φ 6 = Ψ 10 = ВВ – ВВ Ψ 9 Ψ 10 Ψ as = С 1 Φ 1 + С 2 Φ 2 + … + С 6 Φ 6
СИММЕТРИЗАЦИЯ Ψ 1 Ψ 2 Ψ 3 Ψ 4 Ψ 5 Ψ 6 Ψ 7 Ψ 8 Φ 1 = Ψ 1 – Ψ 3 = AB – BA Φ 2 = Ψ 2 – Ψ 4 = AB – BA Φ 3 = Ψ 5 – Ψ 7 = AB – BA Φ 4 = Ψ 6 – Ψ 8 = AB – BA Φ 5 = Ψ 9 = AА – АA Φ 6 = Ψ 10 = ВВ – ВВ Ψ 9 Ψ 10 Ψ as = С 1 Φ 1 + С 2 Φ 2 + … + С 6 Φ 6
 Φ 1 Φ 2 Φ 3 Φ 4 = = AB AB – – BA BA BA = (AB – BA) Φ 5 = AА – АA = AA [ – ] Φ 6 = ВВ – ВВ = BB [ – ] ПРОСТРАНСТВЕННАЯ симметрия — волновая функция должна принадлежать одному из неприводимых представлений (типов симметрии) ТГС, т. е. быть собственной для операторов симметрии, входящих в ТГС. Ф НП ТГС или F Ф = (± 1)Ф
Φ 1 Φ 2 Φ 3 Φ 4 = = AB AB – – BA BA BA = (AB – BA) Φ 5 = AА – АA = AA [ – ] Φ 6 = ВВ – ВВ = BB [ – ] ПРОСТРАНСТВЕННАЯ симметрия — волновая функция должна принадлежать одному из неприводимых представлений (типов симметрии) ТГС, т. е. быть собственной для операторов симметрии, входящих в ТГС. Ф НП ТГС или F Ф = (± 1)Ф
 ПРОСТРАНСТВЕННАЯ симметрия Операция инверсии ( Pab ) — меняет местами ядра a и b Pab Φ = (± 1) Φ Φ 1 = AB – BA P Φ 1 = P (AB – BA ) = (BA – AB ) – Φ 2 = Pab Φ 1 ≠ (± 1)Φ 1 СИММЕТРИЗАЦИЯ Φ 1 Φ 2 Φ+ = Φ 1 + Φ 2 Φ– = Φ 1 – Φ 2
ПРОСТРАНСТВЕННАЯ симметрия Операция инверсии ( Pab ) — меняет местами ядра a и b Pab Φ = (± 1) Φ Φ 1 = AB – BA P Φ 1 = P (AB – BA ) = (BA – AB ) – Φ 2 = Pab Φ 1 ≠ (± 1)Φ 1 СИММЕТРИЗАЦИЯ Φ 1 Φ 2 Φ+ = Φ 1 + Φ 2 Φ– = Φ 1 – Φ 2
 Φ+ = = AB – BA + BA – AB = AB + BA – AB = (AB + BA) – (BA + AB) = (AB + BA) [ – ] Φ– = = AB – BA + AB = (AB – BA) – (BA – AB) = (AB – BA) [ + ] P Φ+ = P (AB + BA) = (BA + AB) = (+1) Φ+ P Φ– = P (AB – BA) = (BA – AB) = (– 1) Φ– Φ+ — «четная» функция (симметричная относительно Pab ) Φ– — «нечетная» функция (антисимметричная относительно Pab )
Φ+ = = AB – BA + BA – AB = AB + BA – AB = (AB + BA) – (BA + AB) = (AB + BA) [ – ] Φ– = = AB – BA + AB = (AB – BA) – (BA – AB) = (AB – BA) [ + ] P Φ+ = P (AB + BA) = (BA + AB) = (+1) Φ+ P Φ– = P (AB – BA) = (BA – AB) = (– 1) Φ– Φ+ — «четная» функция (симметричная относительно Pab ) Φ– — «нечетная» функция (антисимметричная относительно Pab )
 Φ 3 = (AB – BA) Φ 4 = (AB – BA) «нечетная» Φ 5 = AA [ – ] ? ? ? Φ 6 = BB [ – ] ? ? ? СИММЕТРИЗАЦИЯ Φ 5 Φ 6 Φ+′ = (АА + ВВ) [ – ] Φ–′ = (АА – ВВ) [ – ] Φ+′ = Φ 5 + Φ 6 Φ–′ = Φ 5 – Φ 6 «четная» «нечетная»
Φ 3 = (AB – BA) Φ 4 = (AB – BA) «нечетная» Φ 5 = AA [ – ] ? ? ? Φ 6 = BB [ – ] ? ? ? СИММЕТРИЗАЦИЯ Φ 5 Φ 6 Φ+′ = (АА + ВВ) [ – ] Φ–′ = (АА – ВВ) [ – ] Φ+′ = Φ 5 + Φ 6 Φ–′ = Φ 5 – Φ 6 «четная» «нечетная»
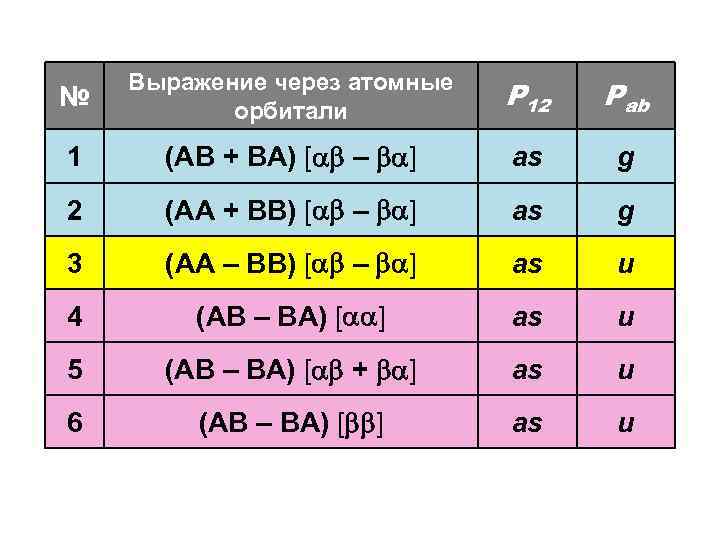 № Выражение через атомные орбитали Р 12 Рab 1 (AB + BA) [ – ] as g 2 (AA + BB) [ – ] as g 3 (AA – BB) [ – ] as u 4 (АВ – BA) [ ] as u 5 (AB – BA) [ + ] as u 6 (АВ – BA) [ ] as u
№ Выражение через атомные орбитали Р 12 Рab 1 (AB + BA) [ – ] as g 2 (AA + BB) [ – ] as g 3 (AA – BB) [ – ] as u 4 (АВ – BA) [ ] as u 5 (AB – BA) [ + ] as u 6 (АВ – BA) [ ] as u
 Глобальная волновая функция молекулы Четная синглетная ( ) Φg = { C 1(AB + BA) + C 2(AA + BB) } [ – ] Нечетная триплетная ( ) Φu = (AB – BA) [ D 1( ) + D 2( + ) + D 3( ) ] Нечетная синглетная ( ) z ( ) Φ′u = (AA – BB) [ – ] ( + ) ( )
Глобальная волновая функция молекулы Четная синглетная ( ) Φg = { C 1(AB + BA) + C 2(AA + BB) } [ – ] Нечетная триплетная ( ) Φu = (AB – BA) [ D 1( ) + D 2( + ) + D 3( ) ] Нечетная синглетная ( ) z ( ) Φ′u = (AA – BB) [ – ] ( + ) ( )
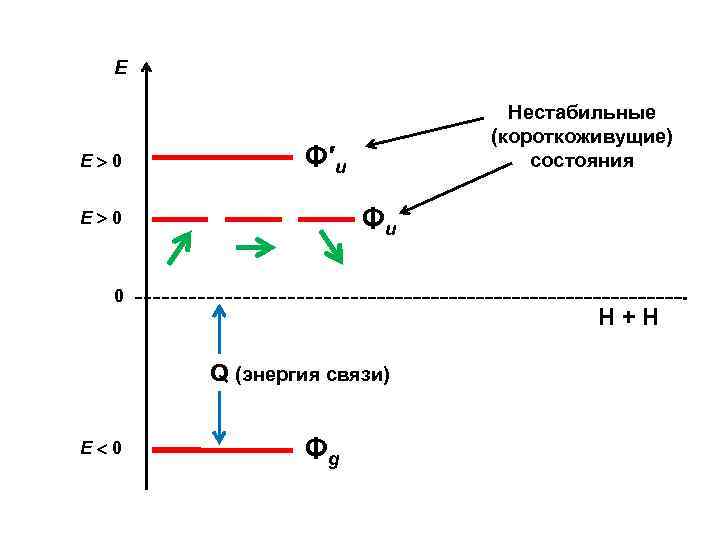 Е Е 0 Нестабильные (короткоживущие) состояния Φ′u Φu Е 0 0 H+H Q (энергия связи) Е 0 Φg
Е Е 0 Нестабильные (короткоживущие) состояния Φ′u Φu Е 0 0 H+H Q (энергия связи) Е 0 Φg
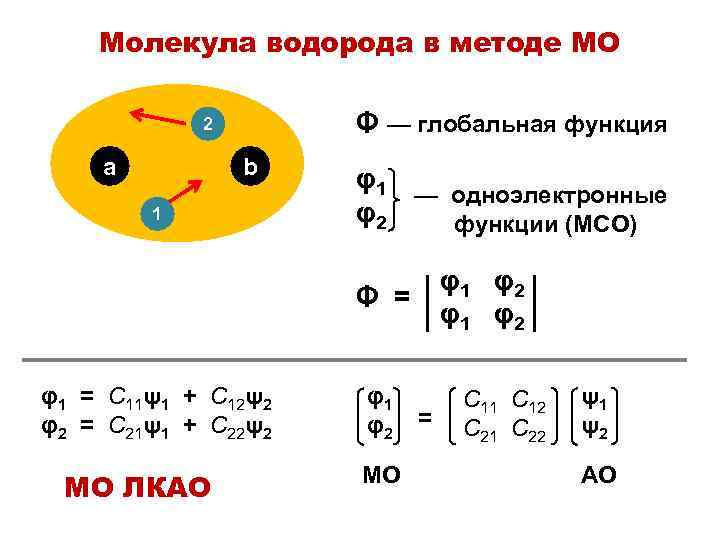 Молекула водорода в методе МО Φ — глобальная функция 2 a b 1 φ1 — одноэлектронные φ2 функции (МСО) φ1 φ2 Φ = φ1 = С 11ψ1 + С 12ψ2 φ2 = С 21ψ1 + С 22ψ2 МО ЛКАО φ1 φ2 МО = С 11 С 12 С 21 С 22 ψ1 ψ2 АО
Молекула водорода в методе МО Φ — глобальная функция 2 a b 1 φ1 — одноэлектронные φ2 функции (МСО) φ1 φ2 Φ = φ1 = С 11ψ1 + С 12ψ2 φ2 = С 21ψ1 + С 22ψ2 МО ЛКАО φ1 φ2 МО = С 11 С 12 С 21 С 22 ψ1 ψ2 АО
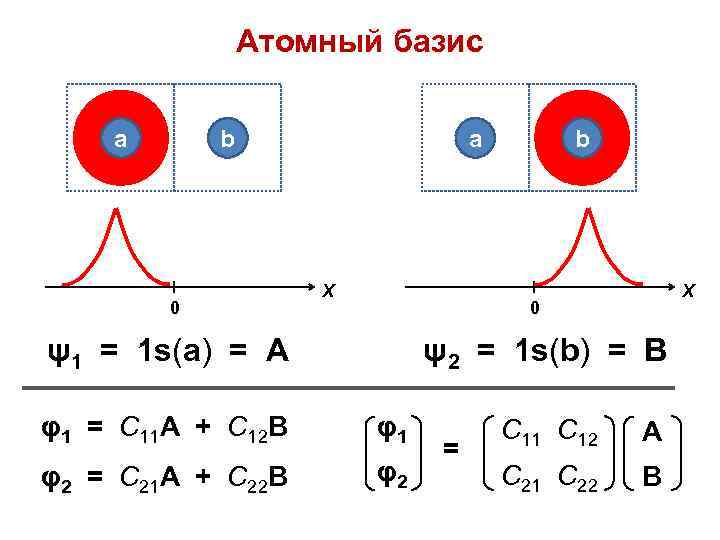 Атомный базис a b 0 a Х b Х 0 ψ1 = 1 s(a) = A ψ2 = 1 s(b) = B φ1 = С 11 A + С 12 B φ1 φ2 = С 21 A + С 22 B φ2 = С 11 С 12 А С 21 С 22 В
Атомный базис a b 0 a Х b Х 0 ψ1 = 1 s(a) = A ψ2 = 1 s(b) = B φ1 = С 11 A + С 12 B φ1 φ2 = С 21 A + С 22 B φ2 = С 11 С 12 А С 21 С 22 В
 Пространственная симметрия МО Оба атомных ядра в молекуле Н—Н одинаковы и поэтому переводятся друг в друга посредством операций симметрии ТГС |С 1|2 = |С 2|2 С 11 = + С 12 четная нечетная С 21 = – С 22 G = Сg (А + В) U = Сu (А – В)
Пространственная симметрия МО Оба атомных ядра в молекуле Н—Н одинаковы и поэтому переводятся друг в друга посредством операций симметрии ТГС |С 1|2 = |С 2|2 С 11 = + С 12 четная нечетная С 21 = – С 22 G = Сg (А + В) U = Сu (А – В)
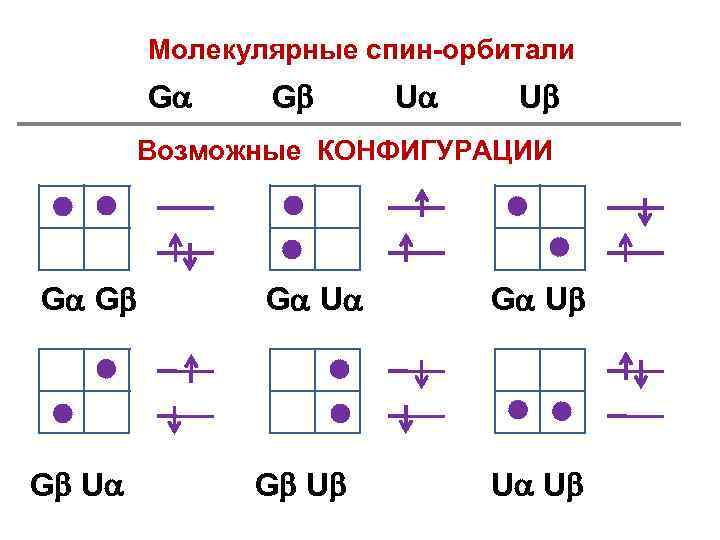 Молекулярные спин-орбитали G G U U Возможные КОНФИГУРАЦИИ G G G U U U
Молекулярные спин-орбитали G G U U Возможные КОНФИГУРАЦИИ G G G U U U
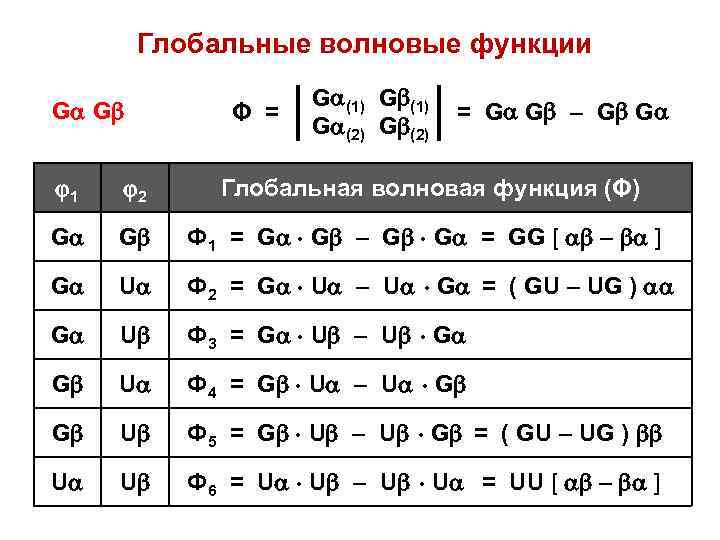 Глобальные волновые функции G G Φ = G (1) G (2) = G G – G G 1 2 Глобальная волновая функция (Φ) G G Ф 1 = G G – G G = GG [ – ] G U Ф 2 = G U – U G = ( GU – UG ) G U Ф 3 = G U – U G G U Ф 4 = G U – U G G U Ф 5 = G U – U G = ( GU – UG ) U U Ф 6 = U U – U U = UU [ – ]
Глобальные волновые функции G G Φ = G (1) G (2) = G G – G G 1 2 Глобальная волновая функция (Φ) G G Ф 1 = G G – G G = GG [ – ] G U Ф 2 = G U – U G = ( GU – UG ) G U Ф 3 = G U – U G G U Ф 4 = G U – U G G U Ф 5 = G U – U G = ( GU – UG ) U U Ф 6 = U U – U U = UU [ – ]
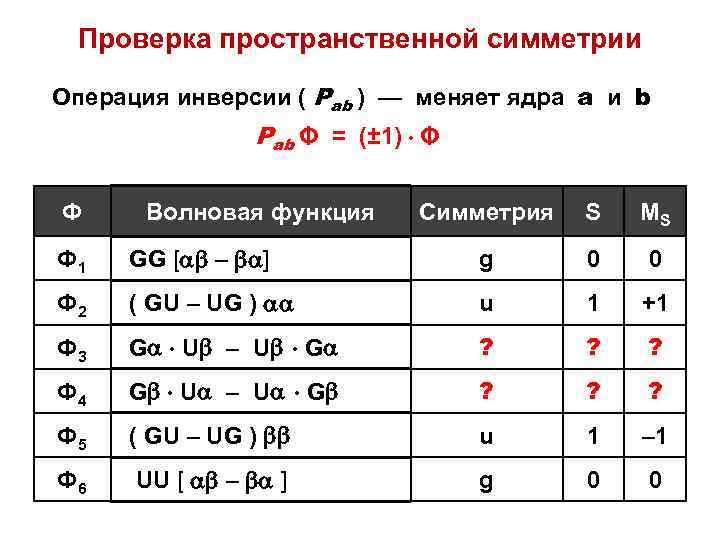 Проверка пространственной симметрии Операция инверсии ( Pab ) — меняет ядра a и b Pab Φ = (± 1) Φ Ф Волновая функция Симметрия S MS Ф 1 GG [ – ] g 0 0 Ф 2 ( GU – UG ) u 1 +1 Ф 3 G U – U G ? ? ? Ф 4 G U – U G ? ? ? Ф 5 ( GU – UG ) u 1 – 1 Ф 6 UU [ – ] g 0 0
Проверка пространственной симметрии Операция инверсии ( Pab ) — меняет ядра a и b Pab Φ = (± 1) Φ Ф Волновая функция Симметрия S MS Ф 1 GG [ – ] g 0 0 Ф 2 ( GU – UG ) u 1 +1 Ф 3 G U – U G ? ? ? Ф 4 G U – U G ? ? ? Ф 5 ( GU – UG ) u 1 – 1 Ф 6 UU [ – ] g 0 0
 Функции Φ 3 и Φ 4 не являются собственными для операторов инверсии (I) спина (S 2) и проекции спина (SZ) СИММЕТРИЗАЦИЯ Φ 3 Φ 4 Φ+ = Φ 3 + Φ 4 Φ– = Φ 3 – Φ 4 Φ+ = G U – U G + G U – U G = = G U + G U – U G = = GU [ + ] – UG [ + ] = = (GU – UG) [ + ] Φ– = (GU + UG) [ – ]
Функции Φ 3 и Φ 4 не являются собственными для операторов инверсии (I) спина (S 2) и проекции спина (SZ) СИММЕТРИЗАЦИЯ Φ 3 Φ 4 Φ+ = Φ 3 + Φ 4 Φ– = Φ 3 – Φ 4 Φ+ = G U – U G + G U – U G = = G U + G U – U G = = GU [ + ] – UG [ + ] = = (GU – UG) [ + ] Φ– = (GU + UG) [ – ]
![Глобальные волновые функции Ф Волновая функция Симметрия S MS Фg GG [ – ] Глобальные волновые функции Ф Волновая функция Симметрия S MS Фg GG [ – ]](https://present5.com/presentation/1/26667163_437005611.pdf-img/26667163_437005611.pdf-46.jpg) Глобальные волновые функции Ф Волновая функция Симметрия S MS Фg GG [ – ] g 0 0 Ф′g UU [ – ] g 0 0 Фu(+) (GU – UG) u 1 +1 Фu(0) (GU – UG) [ + ] u 1 0 Фu(–) (GU – UG) u 1 – 1 Ф′u (GU + UG) [ – ] u 0 0 Фg = С 1(GG) + С 2(UU) [ – ] Фu = (GU – UG) [С 1( ) + С 2( ) + С 3( + )]
Глобальные волновые функции Ф Волновая функция Симметрия S MS Фg GG [ – ] g 0 0 Ф′g UU [ – ] g 0 0 Фu(+) (GU – UG) u 1 +1 Фu(0) (GU – UG) [ + ] u 1 0 Фu(–) (GU – UG) u 1 – 1 Ф′u (GU + UG) [ – ] u 0 0 Фg = С 1(GG) + С 2(UU) [ – ] Фu = (GU – UG) [С 1( ) + С 2( ) + С 3( + )]
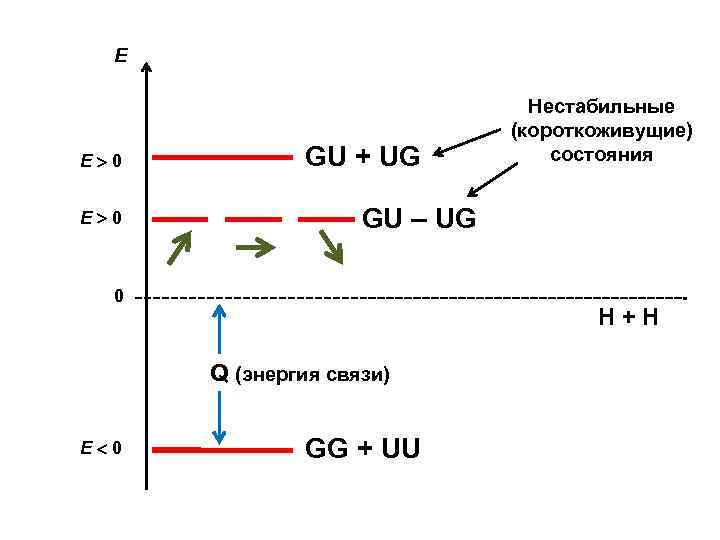 Е Е 0 GU + UG GU – UG 0 H+H Q (энергия связи) Е 0 Нестабильные (короткоживущие) состояния GG + UU
Е Е 0 GU + UG GU – UG 0 H+H Q (энергия связи) Е 0 Нестабильные (короткоживущие) состояния GG + UU
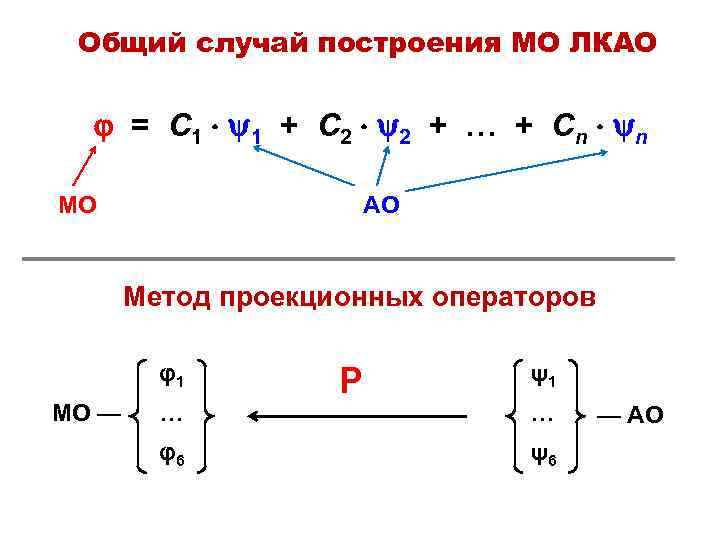 Общий случай построения МО ЛКАО = С 1 1 + С 2 2 + … + С n n МО АО Метод проекционных операторов φ1 МО — … φ6 P ψ1 … ψ6 — АО
Общий случай построения МО ЛКАО = С 1 1 + С 2 2 + … + С n n МО АО Метод проекционных операторов φ1 МО — … φ6 P ψ1 … ψ6 — АО
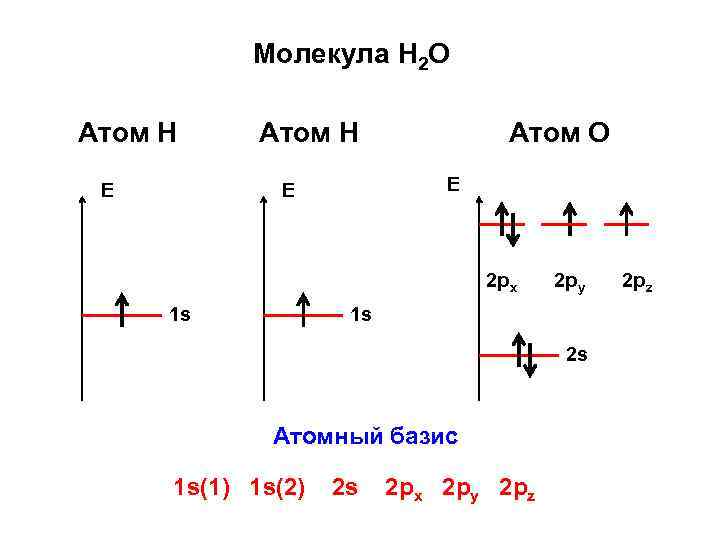 Молекула Н 2 О Атом Н Е Атом Н Атом О Е Е 2 px 1 s 2 py 1 s 2 s Атомный базис 1 s(1) 1 s(2) 2 s 2 px 2 py 2 pz
Молекула Н 2 О Атом Н Е Атом Н Атом О Е Е 2 px 1 s 2 py 1 s 2 s Атомный базис 1 s(1) 1 s(2) 2 s 2 px 2 py 2 pz
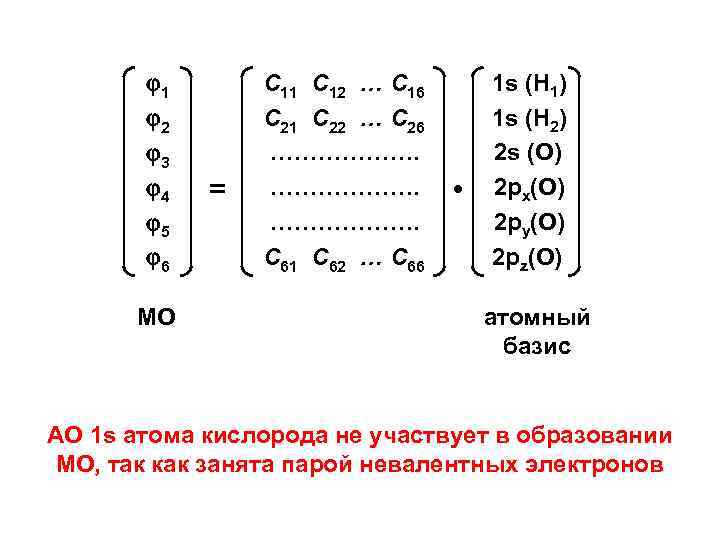 1 2 3 4 5 6 МО = С 11 С 12 … С 16 С 21 С 22 … С 26 ………………. С 61 С 62 … С 66 • 1 s (H 1) 1 s (H 2) 2 s (O) 2 px(O) 2 py(O) 2 pz(O) атомный базис АО 1 s атома кислорода не участвует в образовании МО, так как занята парой невалентных электронов
1 2 3 4 5 6 МО = С 11 С 12 … С 16 С 21 С 22 … С 26 ………………. С 61 С 62 … С 66 • 1 s (H 1) 1 s (H 2) 2 s (O) 2 px(O) 2 py(O) 2 pz(O) атомный базис АО 1 s атома кислорода не участвует в образовании МО, так как занята парой невалентных электронов
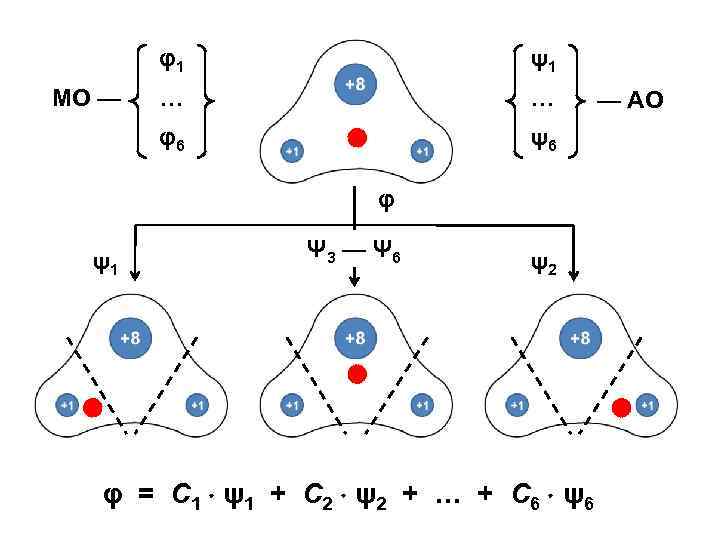 φ1 … … φ6 МО — ψ1 ψ6 φ ψ1 Ψ 3 — Ψ 6 ψ2 φ = С 1 ψ 1 + С 2 ψ 2 + … + С 6 ψ 6 — АО
φ1 … … φ6 МО — ψ1 ψ6 φ ψ1 Ψ 3 — Ψ 6 ψ2 φ = С 1 ψ 1 + С 2 ψ 2 + … + С 6 ψ 6 — АО
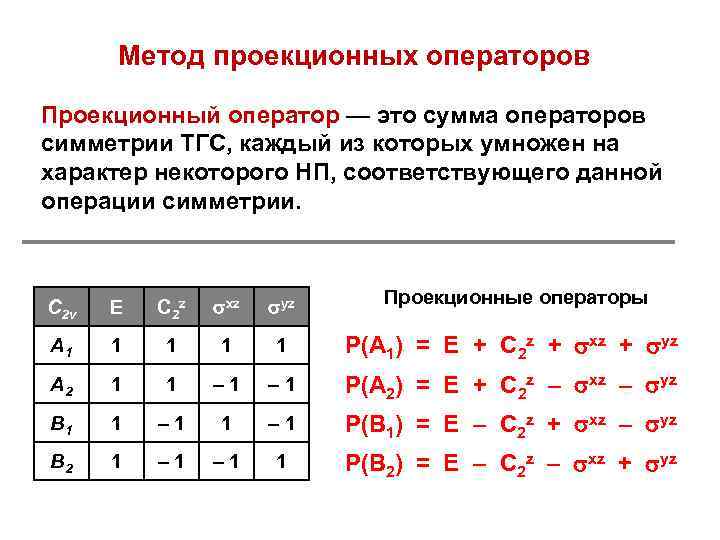 Метод проекционных операторов Проекционный оператор — это сумма операторов симметрии ТГС, каждый из которых умножен на характер некоторого НП, соответствующего данной операции симметрии. C 2 v Е C 2 z xz yz Проекционные операторы А 1 1 1 Р(А 1) = Е + C 2 z + xz + yz A 2 1 1 – 1 Р(А 2) = Е + C 2 z – xz – yz B 1 1 – 1 Р(В 1) = Е – C 2 z + xz – yz B 2 1 – 1 1 Р(В 2) = Е – C 2 z – xz + yz
Метод проекционных операторов Проекционный оператор — это сумма операторов симметрии ТГС, каждый из которых умножен на характер некоторого НП, соответствующего данной операции симметрии. C 2 v Е C 2 z xz yz Проекционные операторы А 1 1 1 Р(А 1) = Е + C 2 z + xz + yz A 2 1 1 – 1 Р(А 2) = Е + C 2 z – xz – yz B 1 1 – 1 Р(В 1) = Е – C 2 z + xz – yz B 2 1 – 1 1 Р(В 2) = Е – C 2 z – xz + yz
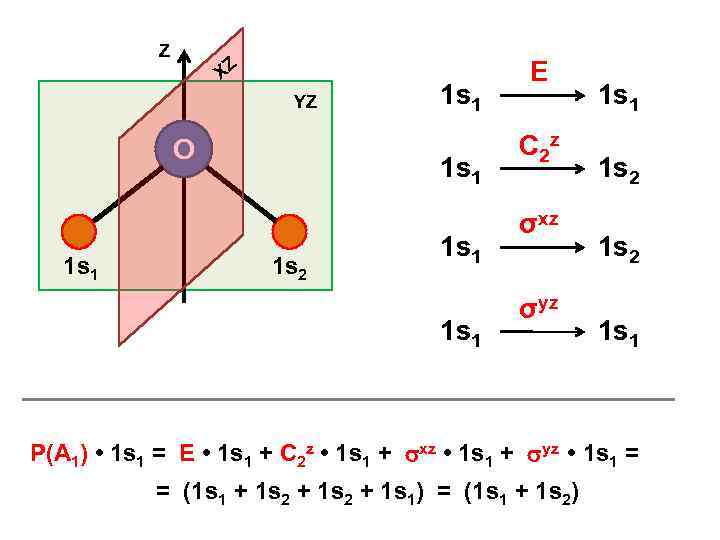 Z XZ YZ О 1 s 1 1 s 2 1 s 1 E C 2 z σxz σyz 1 s 1 1 s 2 1 s 1 Р(А 1) • 1 s 1 = Е • 1 s 1 + C 2 z • 1 s 1 + xz • 1 s 1 + yz • 1 s 1 = = (1 s 1 + 1 s 2 + 1 s 1) = (1 s 1 + 1 s 2)
Z XZ YZ О 1 s 1 1 s 2 1 s 1 E C 2 z σxz σyz 1 s 1 1 s 2 1 s 1 Р(А 1) • 1 s 1 = Е • 1 s 1 + C 2 z • 1 s 1 + xz • 1 s 1 + yz • 1 s 1 = = (1 s 1 + 1 s 2 + 1 s 1) = (1 s 1 + 1 s 2)
 = С 1(1 s 1) + С 2(1 s 2) + С 3(2 s) + С 4(2 px) + С 5(2 py) + С 6(2 pz) Р(А 1) = С 1(1 s 1 + 1 s 2 + 1 s 1) + С 2(1 s 2 + 1 s 1 + 1 s 2) + + С 3(2 s + 2 s) + С 4(2 px – 2 px + 2 px – 2 px) + + С 5(2 py – 2 py + 2 py) + С 6(2 pz + 2 pz) = = 2(C 1 + C 2)(1 s 1 + 1 s 2) + 4 C 3(2 s) + 4 С 6(2 pz) = = D 1(1 s 1 + 1 s 2) + D 2(2 s) + D 3(2 pz) Р(А 2) = С 1(1 s 1 + 1 s 2 – 1 s 1) + С 2(1 s 2 + 1 s 1 – 1 s 2) + + С 3(2 s + 2 s – 2 s) + С 4(2 px – 2 px + 2 px) + + С 5(2 py – 2 py + 2 py – 2 py) + С 6(2 pz + 2 pz – 2 pz) = = 0
= С 1(1 s 1) + С 2(1 s 2) + С 3(2 s) + С 4(2 px) + С 5(2 py) + С 6(2 pz) Р(А 1) = С 1(1 s 1 + 1 s 2 + 1 s 1) + С 2(1 s 2 + 1 s 1 + 1 s 2) + + С 3(2 s + 2 s) + С 4(2 px – 2 px + 2 px – 2 px) + + С 5(2 py – 2 py + 2 py) + С 6(2 pz + 2 pz) = = 2(C 1 + C 2)(1 s 1 + 1 s 2) + 4 C 3(2 s) + 4 С 6(2 pz) = = D 1(1 s 1 + 1 s 2) + D 2(2 s) + D 3(2 pz) Р(А 2) = С 1(1 s 1 + 1 s 2 – 1 s 1) + С 2(1 s 2 + 1 s 1 – 1 s 2) + + С 3(2 s + 2 s – 2 s) + С 4(2 px – 2 px + 2 px) + + С 5(2 py – 2 py + 2 py – 2 py) + С 6(2 pz + 2 pz – 2 pz) = = 0
 = С 1(1 s 1) + С 2(1 s 2) + С 3(2 s) + С 4(2 px) + С 5(2 py) + С 6(2 pz) Р(B 1) = С 1(1 s 1 – 1 s 2 + 1 s 2 – 1 s 1) + С 2(1 s 2 – 1 s 1 + 1 s 1 – 1 s 2) + + С 3(2 s – 2 s + 2 s – 2 s) + С 4(2 px + 2 px) + + С 5(2 py + 2 py – 2 py) + С 6(2 pz – 2 pz + 2 pz – 2 pz) = = 2 C 4(2 px) = D 1(2 px) Р(В 2) = С 1(1 s 1 – 1 s 2 + 1 s 1) + С 2(1 s 2 – 1 s 1 + 1 s 2) + + С 3(2 s – 2 s + 2 s) + С 4(2 px + 2 px – 2 px) + + С 5(2 py + 2 py) + С 6(2 pz – 2 pz + 2 pz) = = 2(C 1 – C 2)(1 s 1 – 1 s 2) + 4 C 5(2 py) = = D 1(1 s 1 – 1 s 2) + D 2(2 py)
= С 1(1 s 1) + С 2(1 s 2) + С 3(2 s) + С 4(2 px) + С 5(2 py) + С 6(2 pz) Р(B 1) = С 1(1 s 1 – 1 s 2 + 1 s 2 – 1 s 1) + С 2(1 s 2 – 1 s 1 + 1 s 1 – 1 s 2) + + С 3(2 s – 2 s + 2 s – 2 s) + С 4(2 px + 2 px) + + С 5(2 py + 2 py – 2 py) + С 6(2 pz – 2 pz + 2 pz – 2 pz) = = 2 C 4(2 px) = D 1(2 px) Р(В 2) = С 1(1 s 1 – 1 s 2 + 1 s 1) + С 2(1 s 2 – 1 s 1 + 1 s 2) + + С 3(2 s – 2 s + 2 s) + С 4(2 px + 2 px – 2 px) + + С 5(2 py + 2 py) + С 6(2 pz – 2 pz + 2 pz) = = 2(C 1 – C 2)(1 s 1 – 1 s 2) + 4 C 5(2 py) = = D 1(1 s 1 – 1 s 2) + D 2(2 py)
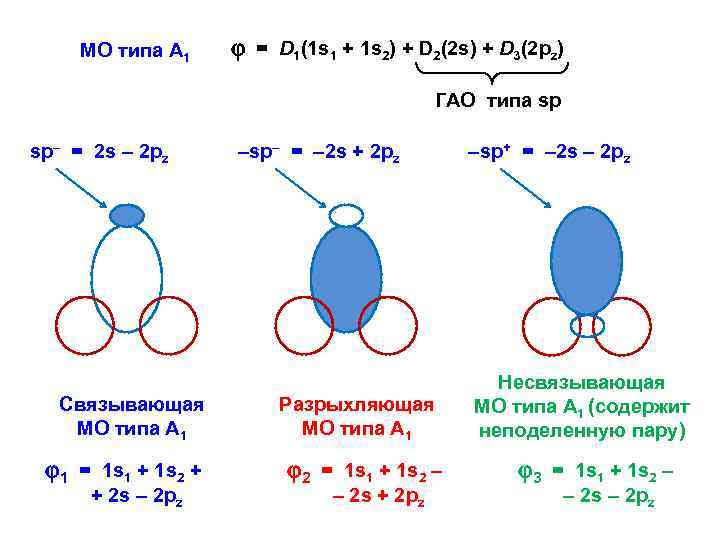 МО типа А 1 = D 1(1 s 1 + 1 s 2) + D 2(2 s) + D 3(2 pz) ГАО типа sp sp– = 2 s – 2 pz Связывающая МО типа А 1 1 = 1 s 1 + 1 s 2 + + 2 s – 2 pz –sp– = – 2 s + 2 pz Разрыхляющая МО типа А 1 2 = 1 s 1 + 1 s 2 – – 2 s + 2 pz –sp+ = – 2 s – 2 pz Несвязывающая МО типа А 1 (содержит неподеленную пару) 3 = 1 s 1 + 1 s 2 – – 2 s – 2 pz
МО типа А 1 = D 1(1 s 1 + 1 s 2) + D 2(2 s) + D 3(2 pz) ГАО типа sp sp– = 2 s – 2 pz Связывающая МО типа А 1 1 = 1 s 1 + 1 s 2 + + 2 s – 2 pz –sp– = – 2 s + 2 pz Разрыхляющая МО типа А 1 2 = 1 s 1 + 1 s 2 – – 2 s + 2 pz –sp+ = – 2 s – 2 pz Несвязывающая МО типа А 1 (содержит неподеленную пару) 3 = 1 s 1 + 1 s 2 – – 2 s – 2 pz
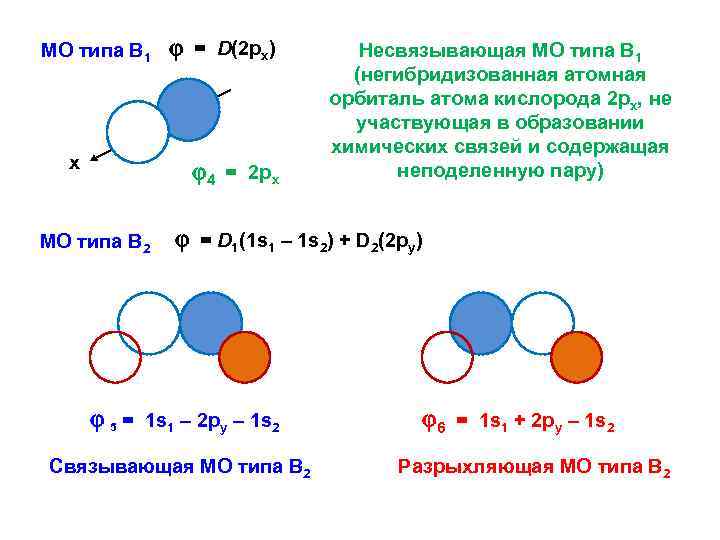 МО типа В 1 х = D(2 рх) 4 = 2 рх МО типа В 2 Несвязывающая МО типа В 1 (негибридизованная атомная орбиталь атома кислорода 2 pх, не участвующая в образовании химических связей и содержащая неподеленную пару) = D 1(1 s 1 – 1 s 2) + D 2(2 py) 5 = 1 s 1 – 2 ру – 1 s 2 Связывающая МО типа В 2 6 = 1 s 1 + 2 ру – 1 s 2 Разрыхляющая МО типа В 2
МО типа В 1 х = D(2 рх) 4 = 2 рх МО типа В 2 Несвязывающая МО типа В 1 (негибридизованная атомная орбиталь атома кислорода 2 pх, не участвующая в образовании химических связей и содержащая неподеленную пару) = D 1(1 s 1 – 1 s 2) + D 2(2 py) 5 = 1 s 1 – 2 ру – 1 s 2 Связывающая МО типа В 2 6 = 1 s 1 + 2 ру – 1 s 2 Разрыхляющая МО типа В 2
 1 = 1 s 1 + 1 s 2 + 2 s – 2 pz 2 = 1 s 1 + 1 s 2 – 2 s + 2 pz 3 = 1 s 1 + 1 s 2 – 2 s – 2 pz 4 = 2 рх 5 = 1 s 1 – 2 ру – 1 s 2 6 = 1 s 1 + 2 ру – 1 s 2 Атомно-молекулярная матрица 1 2 3 4 5 6 = 1 1 1 – 1 0 0 0 1 – 1 0 0 0 – 1 1 0 0 0 – 1 0 0 1 s 1 1 s 2 2 s 2 px 2 py 2 pz
1 = 1 s 1 + 1 s 2 + 2 s – 2 pz 2 = 1 s 1 + 1 s 2 – 2 s + 2 pz 3 = 1 s 1 + 1 s 2 – 2 s – 2 pz 4 = 2 рх 5 = 1 s 1 – 2 ру – 1 s 2 6 = 1 s 1 + 2 ру – 1 s 2 Атомно-молекулярная матрица 1 2 3 4 5 6 = 1 1 1 – 1 0 0 0 1 – 1 0 0 0 – 1 1 0 0 0 – 1 0 0 1 s 1 1 s 2 2 s 2 px 2 py 2 pz
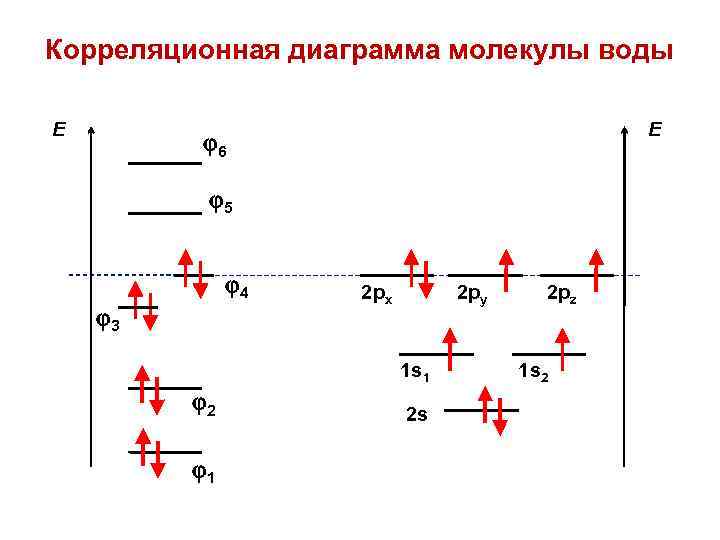 Корреляционная диаграмма молекулы воды E E 6 5 4 3 2 px 2 py 1 s 1 2 1 2 s 2 pz 1 s 2
Корреляционная диаграмма молекулы воды E E 6 5 4 3 2 px 2 py 1 s 1 2 1 2 s 2 pz 1 s 2
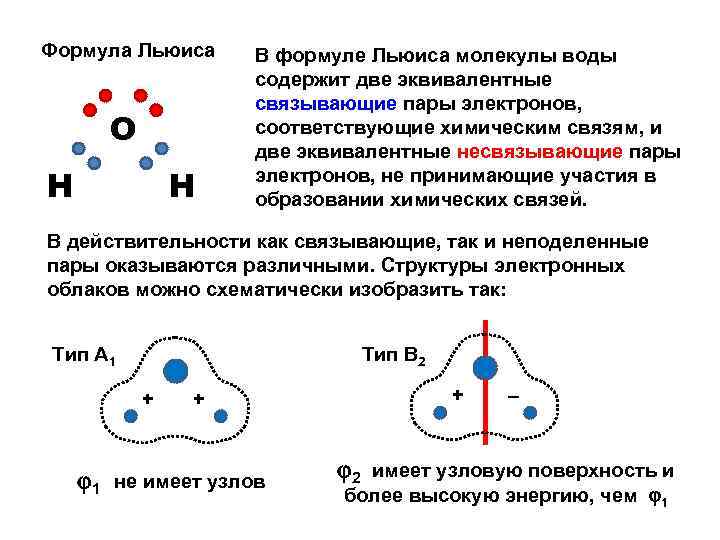 Формула Льюиса О Н Н В формуле Льюиса молекулы воды содержит две эквивалентные связывающие пары электронов, соответствующие химическим связям, и две эквивалентные несвязывающие пары электронов, не принимающие участия в образовании химических связей. В действительности как связывающие, так и неподеленные пары оказываются различными. Структуры электронных облаков можно схематически изобразить так: Тип А 1 Тип В 2 + + 1 не имеет узлов + – 2 имеет узловую поверхность и более высокую энергию, чем 1
Формула Льюиса О Н Н В формуле Льюиса молекулы воды содержит две эквивалентные связывающие пары электронов, соответствующие химическим связям, и две эквивалентные несвязывающие пары электронов, не принимающие участия в образовании химических связей. В действительности как связывающие, так и неподеленные пары оказываются различными. Структуры электронных облаков можно схематически изобразить так: Тип А 1 Тип В 2 + + 1 не имеет узлов + – 2 имеет узловую поверхность и более высокую энергию, чем 1
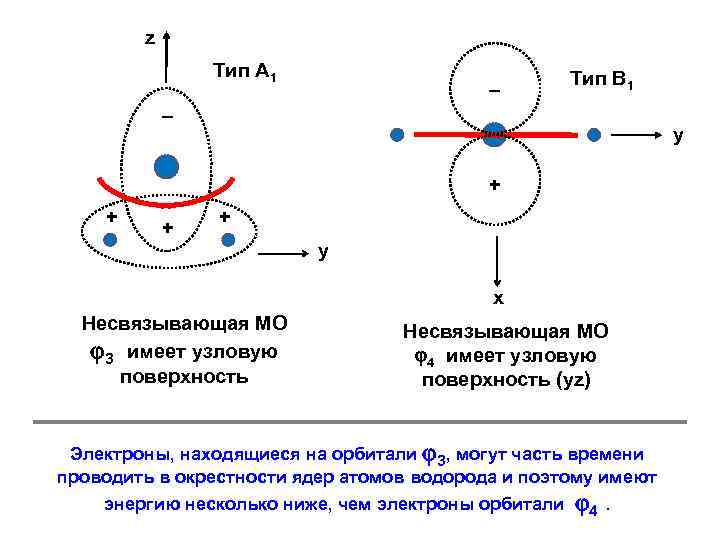 z Тип А 1 – Тип В 1 – у + + у х Несвязывающая МО 3 имеет узловую поверхность Несвязывающая МО 4 имеет узловую поверхность (yz) Электроны, находящиеся на орбитали 3, могут часть времени проводить в окрестности ядер атомов водорода и поэтому имеют энергию несколько ниже, чем электроны орбитали 4.
z Тип А 1 – Тип В 1 – у + + у х Несвязывающая МО 3 имеет узловую поверхность Несвязывающая МО 4 имеет узловую поверхность (yz) Электроны, находящиеся на орбитали 3, могут часть времени проводить в окрестности ядер атомов водорода и поэтому имеют энергию несколько ниже, чем электроны орбитали 4.
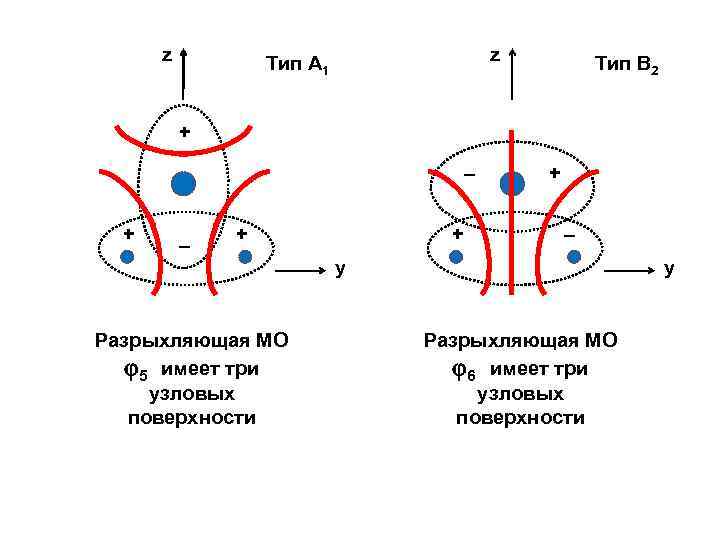 z z Тип А 1 Тип В 2 + – + + + – у у Разрыхляющая МО 5 имеет три узловых поверхности Разрыхляющая МО 6 имеет три узловых поверхности
z z Тип А 1 Тип В 2 + – + + + – у у Разрыхляющая МО 5 имеет три узловых поверхности Разрыхляющая МО 6 имеет три узловых поверхности
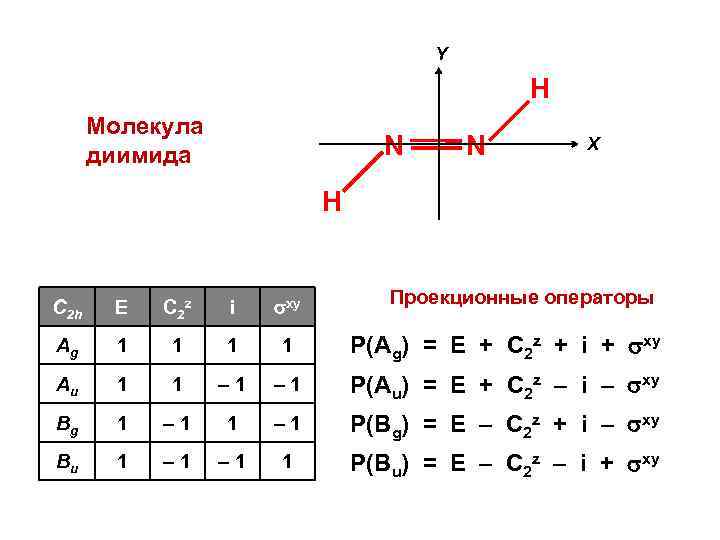 Y H Молекула диимида N N X H Проекционные операторы C 2 h Е C 2 z i xy Аg 1 1 Р(Аg) = Е + C 2 z + i + xy Au 1 1 – 1 Р(Аu) = Е + C 2 z – i – xy Bg 1 – 1 Р(Вg) = Е – C 2 z + i – xy Bu 1 – 1 1 Р(Вu) = Е – C 2 z – i + xy
Y H Молекула диимида N N X H Проекционные операторы C 2 h Е C 2 z i xy Аg 1 1 Р(Аg) = Е + C 2 z + i + xy Au 1 1 – 1 Р(Аu) = Е + C 2 z – i – xy Bg 1 – 1 Р(Вg) = Е – C 2 z + i – xy Bu 1 – 1 1 Р(Вu) = Е – C 2 z – i + xy
 Атомный базис молекулы диимида ( 1 s 1 1 s 2 )Н ( 2 s 1 2 px 1 2 py 1 2 pz 1 )N 1 ( 2 s 2 2 px 2 2 py 2 2 pz 2 )N 2 МО молекулы диимида = С 1(1 s 1) + С 2(1 s 2) + С 3(2 s 1) + С 4(2 px 1) + С 5(2 py 1) + + С 6(2 pz 1) + С 7(2 s 2) + С 8(2 px 2) + С 9(2 py 2) + С 10(2 pz 2)
Атомный базис молекулы диимида ( 1 s 1 1 s 2 )Н ( 2 s 1 2 px 1 2 py 1 2 pz 1 )N 1 ( 2 s 2 2 px 2 2 py 2 2 pz 2 )N 2 МО молекулы диимида = С 1(1 s 1) + С 2(1 s 2) + С 3(2 s 1) + С 4(2 px 1) + С 5(2 py 1) + + С 6(2 pz 1) + С 7(2 s 2) + С 8(2 px 2) + С 9(2 py 2) + С 10(2 pz 2)
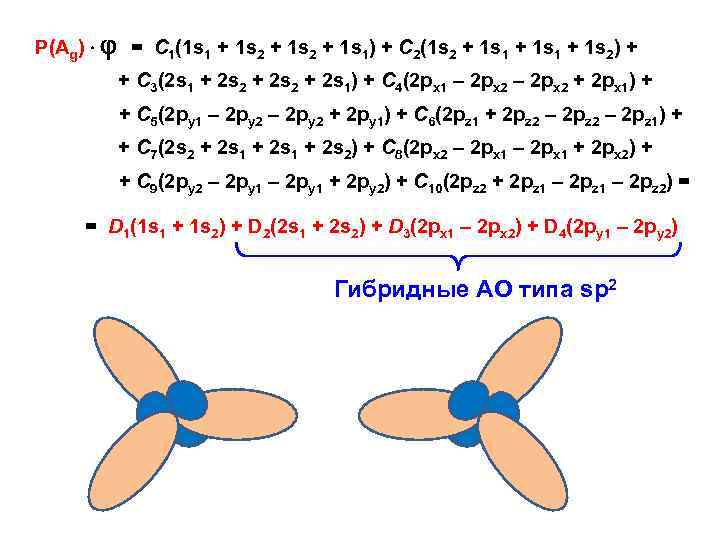 Р(Аg) = С 1(1 s 1 + 1 s 2 + 1 s 1) + С 2(1 s 2 + 1 s 1 + 1 s 2) + + С 3(2 s 1 + 2 s 2 + 2 s 1) + С 4(2 px 1 – 2 px 2 + 2 px 1) + + С 5(2 py 1 – 2 py 2 + 2 py 1) + С 6(2 pz 1 + 2 pz 2 – 2 pz 1) + + С 7(2 s 2 + 2 s 1 + 2 s 2) + С 8(2 px 2 – 2 px 1 + 2 px 2) + + С 9(2 py 2 – 2 py 1 + 2 py 2) + С 10(2 pz 2 + 2 pz 1 – 2 pz 2) = = D 1(1 s 1 + 1 s 2) + D 2(2 s 1 + 2 s 2) + D 3(2 px 1 – 2 px 2) + D 4(2 py 1 – 2 py 2) Гибридные АО типа sp 2
Р(Аg) = С 1(1 s 1 + 1 s 2 + 1 s 1) + С 2(1 s 2 + 1 s 1 + 1 s 2) + + С 3(2 s 1 + 2 s 2 + 2 s 1) + С 4(2 px 1 – 2 px 2 + 2 px 1) + + С 5(2 py 1 – 2 py 2 + 2 py 1) + С 6(2 pz 1 + 2 pz 2 – 2 pz 1) + + С 7(2 s 2 + 2 s 1 + 2 s 2) + С 8(2 px 2 – 2 px 1 + 2 px 2) + + С 9(2 py 2 – 2 py 1 + 2 py 2) + С 10(2 pz 2 + 2 pz 1 – 2 pz 2) = = D 1(1 s 1 + 1 s 2) + D 2(2 s 1 + 2 s 2) + D 3(2 px 1 – 2 px 2) + D 4(2 py 1 – 2 py 2) Гибридные АО типа sp 2
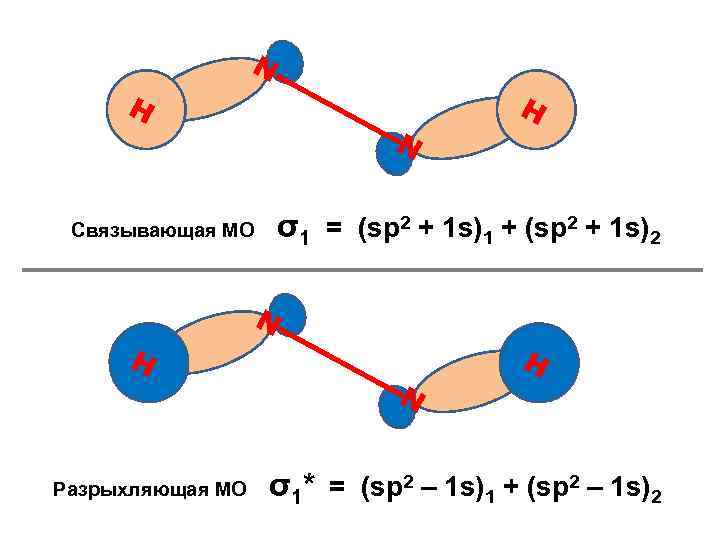 N H σ1 = (sp 2 + 1 s)1 + (sp 2 + 1 s)2 Связывающая МО N H Разрыхляющая МО N H σ1* = (sp 2 – 1 s)1 + (sp 2 – 1 s)2
N H σ1 = (sp 2 + 1 s)1 + (sp 2 + 1 s)2 Связывающая МО N H Разрыхляющая МО N H σ1* = (sp 2 – 1 s)1 + (sp 2 – 1 s)2
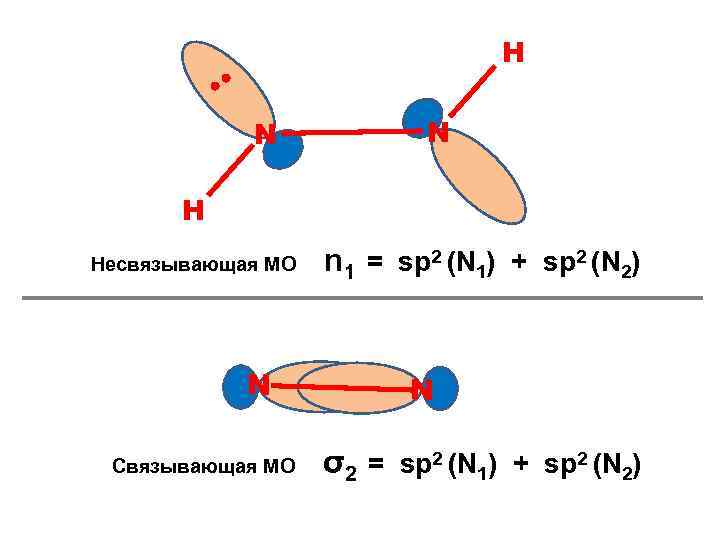 Н • • N N Н Несвязывающая МО N Связывающая МО n 1 = sp 2 (N 1) + sp 2 (N 2) N σ2 = sp 2 (N 1) + sp 2 (N 2)
Н • • N N Н Несвязывающая МО N Связывающая МО n 1 = sp 2 (N 1) + sp 2 (N 2) N σ2 = sp 2 (N 1) + sp 2 (N 2)
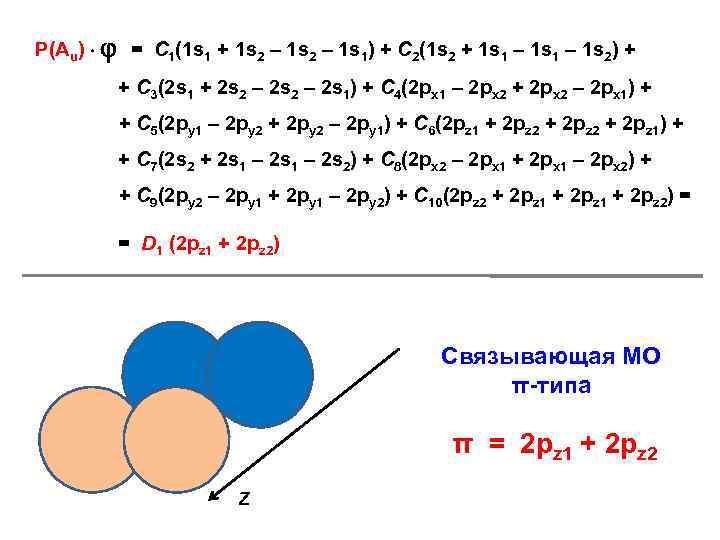 Р(Аu) = С 1(1 s 1 + 1 s 2 – 1 s 1) + С 2(1 s 2 + 1 s 1 – 1 s 2) + + С 3(2 s 1 + 2 s 2 – 2 s 1) + С 4(2 px 1 – 2 px 2 + 2 px 2 – 2 px 1) + + С 5(2 py 1 – 2 py 2 + 2 py 2 – 2 py 1) + С 6(2 pz 1 + 2 pz 2 + 2 pz 1) + + С 7(2 s 2 + 2 s 1 – 2 s 2) + С 8(2 px 2 – 2 px 1 + 2 px 1 – 2 px 2) + + С 9(2 py 2 – 2 py 1 + 2 py 1 – 2 py 2) + С 10(2 pz 2 + 2 pz 1 + 2 pz 2) = = D 1 (2 pz 1 + 2 pz 2) Связывающая МО π-типа π = 2 pz 1 + 2 pz 2 Z
Р(Аu) = С 1(1 s 1 + 1 s 2 – 1 s 1) + С 2(1 s 2 + 1 s 1 – 1 s 2) + + С 3(2 s 1 + 2 s 2 – 2 s 1) + С 4(2 px 1 – 2 px 2 + 2 px 2 – 2 px 1) + + С 5(2 py 1 – 2 py 2 + 2 py 2 – 2 py 1) + С 6(2 pz 1 + 2 pz 2 + 2 pz 1) + + С 7(2 s 2 + 2 s 1 – 2 s 2) + С 8(2 px 2 – 2 px 1 + 2 px 1 – 2 px 2) + + С 9(2 py 2 – 2 py 1 + 2 py 1 – 2 py 2) + С 10(2 pz 2 + 2 pz 1 + 2 pz 2) = = D 1 (2 pz 1 + 2 pz 2) Связывающая МО π-типа π = 2 pz 1 + 2 pz 2 Z
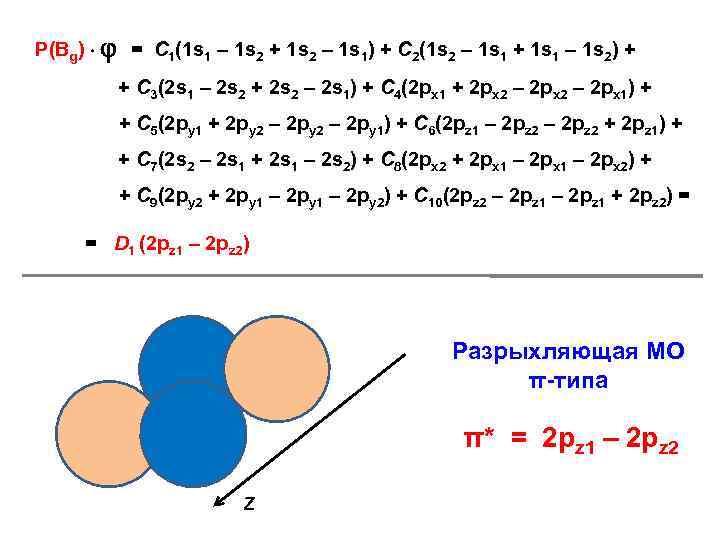 Р(Вg) = С 1(1 s 1 – 1 s 2 + 1 s 2 – 1 s 1) + С 2(1 s 2 – 1 s 1 + 1 s 1 – 1 s 2) + + С 3(2 s 1 – 2 s 2 + 2 s 2 – 2 s 1) + С 4(2 px 1 + 2 px 2 – 2 px 1) + + С 5(2 py 1 + 2 py 2 – 2 py 1) + С 6(2 pz 1 – 2 pz 2 + 2 pz 1) + + С 7(2 s 2 – 2 s 1 + 2 s 1 – 2 s 2) + С 8(2 px 2 + 2 px 1 – 2 px 2) + + С 9(2 py 2 + 2 py 1 – 2 py 2) + С 10(2 pz 2 – 2 pz 1 + 2 pz 2) = = D 1 (2 pz 1 – 2 pz 2) Разрыхляющая МО π-типа π* = 2 pz 1 – 2 pz 2 Z
Р(Вg) = С 1(1 s 1 – 1 s 2 + 1 s 2 – 1 s 1) + С 2(1 s 2 – 1 s 1 + 1 s 1 – 1 s 2) + + С 3(2 s 1 – 2 s 2 + 2 s 2 – 2 s 1) + С 4(2 px 1 + 2 px 2 – 2 px 1) + + С 5(2 py 1 + 2 py 2 – 2 py 1) + С 6(2 pz 1 – 2 pz 2 + 2 pz 1) + + С 7(2 s 2 – 2 s 1 + 2 s 1 – 2 s 2) + С 8(2 px 2 + 2 px 1 – 2 px 2) + + С 9(2 py 2 + 2 py 1 – 2 py 2) + С 10(2 pz 2 – 2 pz 1 + 2 pz 2) = = D 1 (2 pz 1 – 2 pz 2) Разрыхляющая МО π-типа π* = 2 pz 1 – 2 pz 2 Z
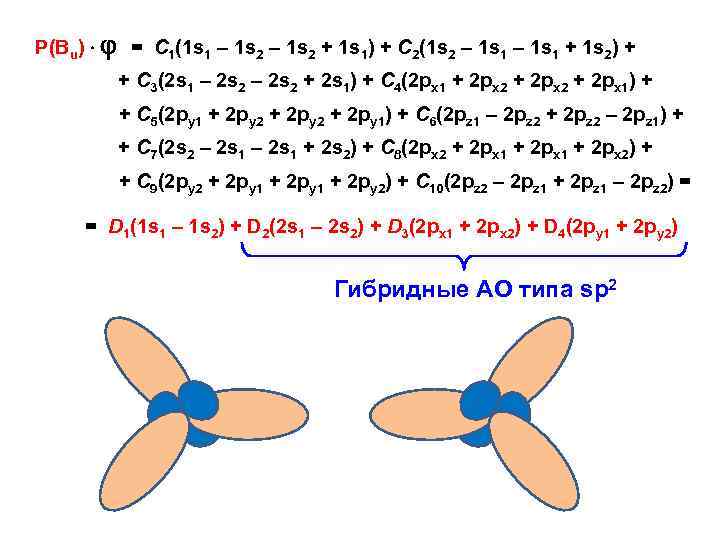 Р(Bu) = С 1(1 s 1 – 1 s 2 + 1 s 1) + С 2(1 s 2 – 1 s 1 + 1 s 2) + + С 3(2 s 1 – 2 s 2 + 2 s 1) + С 4(2 px 1 + 2 px 2 + 2 px 1) + + С 5(2 py 1 + 2 py 2 + 2 py 1) + С 6(2 pz 1 – 2 pz 2 + 2 pz 2 – 2 pz 1) + + С 7(2 s 2 – 2 s 1 + 2 s 2) + С 8(2 px 2 + 2 px 1 + 2 px 2) + + С 9(2 py 2 + 2 py 1 + 2 py 2) + С 10(2 pz 2 – 2 pz 1 + 2 pz 1 – 2 pz 2) = = D 1(1 s 1 – 1 s 2) + D 2(2 s 1 – 2 s 2) + D 3(2 px 1 + 2 px 2) + D 4(2 py 1 + 2 py 2) Гибридные АО типа sp 2
Р(Bu) = С 1(1 s 1 – 1 s 2 + 1 s 1) + С 2(1 s 2 – 1 s 1 + 1 s 2) + + С 3(2 s 1 – 2 s 2 + 2 s 1) + С 4(2 px 1 + 2 px 2 + 2 px 1) + + С 5(2 py 1 + 2 py 2 + 2 py 1) + С 6(2 pz 1 – 2 pz 2 + 2 pz 2 – 2 pz 1) + + С 7(2 s 2 – 2 s 1 + 2 s 2) + С 8(2 px 2 + 2 px 1 + 2 px 2) + + С 9(2 py 2 + 2 py 1 + 2 py 2) + С 10(2 pz 2 – 2 pz 1 + 2 pz 1 – 2 pz 2) = = D 1(1 s 1 – 1 s 2) + D 2(2 s 1 – 2 s 2) + D 3(2 px 1 + 2 px 2) + D 4(2 py 1 + 2 py 2) Гибридные АО типа sp 2
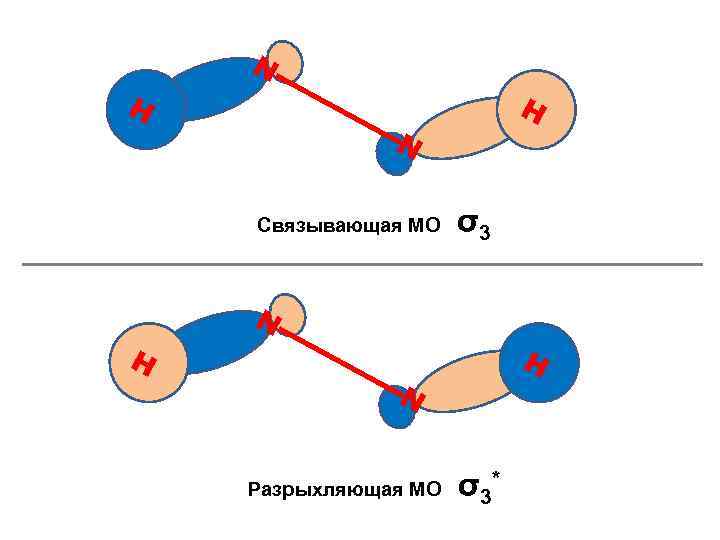 N H H N Связывающая МО σ3 N H H N Разрыхляющая МО σ3*
N H H N Связывающая МО σ3 N H H N Разрыхляющая МО σ3*
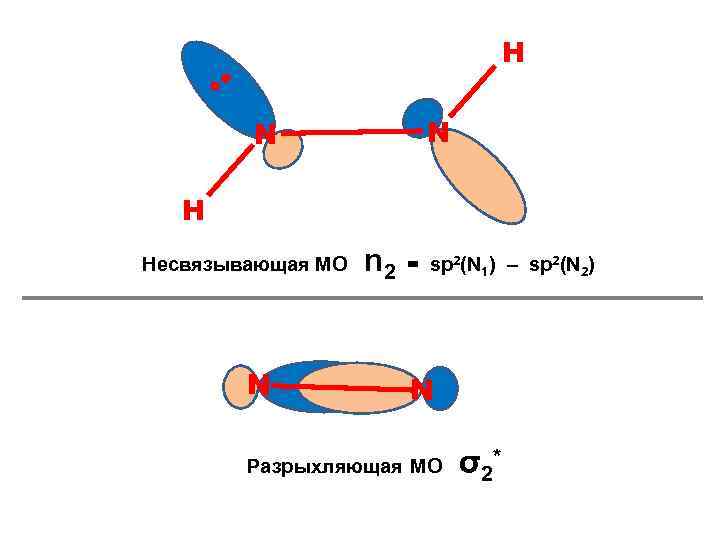 Н • • N N Н Несвязывающая МО N n 2 = sp 2(N 1) – sp 2(N 2) N Разрыхляющая МО σ2*
Н • • N N Н Несвязывающая МО N n 2 = sp 2(N 1) – sp 2(N 2) N Разрыхляющая МО σ2*
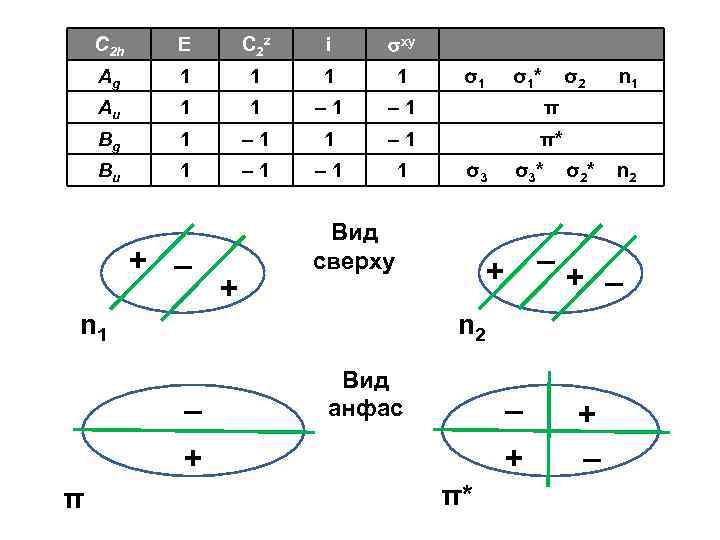 C 2 h Е C 2 z i xy Аg 1 1 Au 1 1 – 1 π Bg 1 – 1 π* Bu 1 – 1 1 + – + σ1 σ3 Вид сверху n 1 σ2 σ3 * + – n 1 σ2 * n 2 + – n 2 – Вид анфас – + + π σ1 * π* + –
C 2 h Е C 2 z i xy Аg 1 1 Au 1 1 – 1 π Bg 1 – 1 π* Bu 1 – 1 1 + – + σ1 σ3 Вид сверху n 1 σ2 σ3 * + – n 1 σ2 * n 2 + – n 2 – Вид анфас – + + π σ1 * π* + –
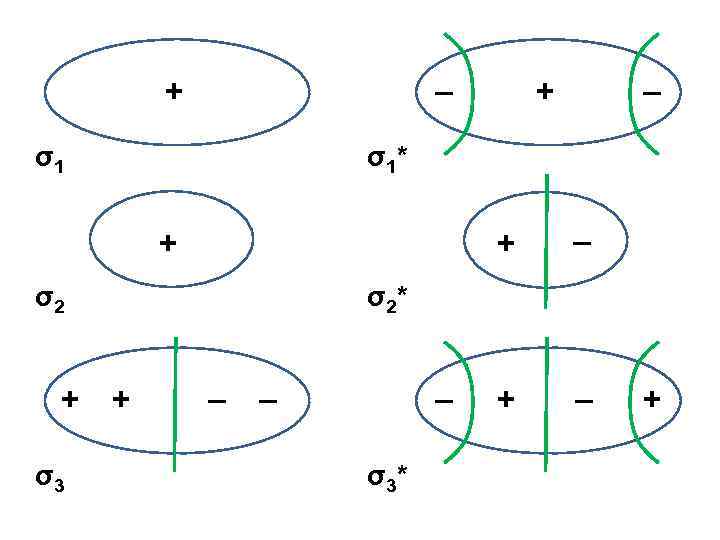 + – σ1 + σ2 σ3 – σ1* + + + – σ2* + – – – σ3* +
+ – σ1 + σ2 σ3 – σ1* + + + – σ2* + – – – σ3* +
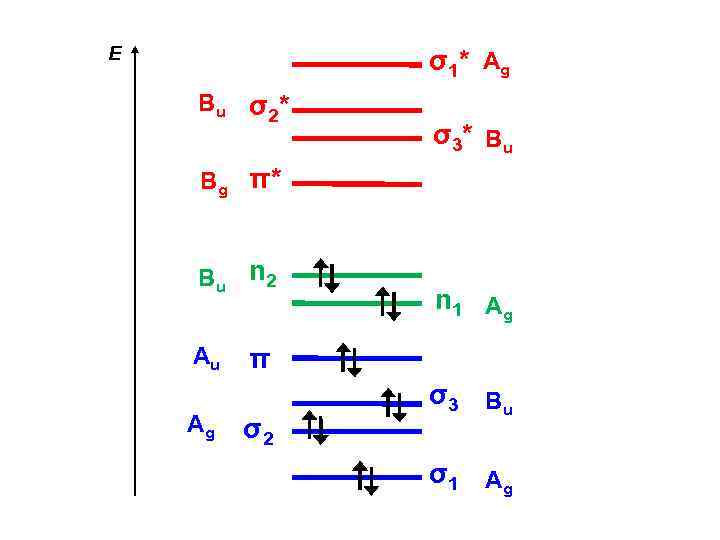 E σ1* A g B u σ2* σ3* B u Bg π* Bu n 2 Au Ag n 1 Ag π σ2 σ3 B u σ1 A g
E σ1* A g B u σ2* σ3* B u Bg π* Bu n 2 Au Ag n 1 Ag π σ2 σ3 B u σ1 A g


