НК_2012-13.ppt
- Количество слайдов: 46
 ПРООКСИДАНТНАЯ и АНТИОКСИДАНТНАЯ системы организма старший преподаватель кафедры биологии, к. б. н. Московцева О. М. Кафедра Биологии ГБОУ ВПО Ниж. ГМА Минздрав 2011
ПРООКСИДАНТНАЯ и АНТИОКСИДАНТНАЯ системы организма старший преподаватель кафедры биологии, к. б. н. Московцева О. М. Кафедра Биологии ГБОУ ВПО Ниж. ГМА Минздрав 2011
 организм АО СР АО
организм АО СР АО
 Свободнорадикальное окисление непрерывно протекает в норме во всех тканях живых организмов интенсификация СРО может быть следствием недостаточность антиоксидантной системы гиперпродукция свободных радикалов СР АО АО СР «окислительный стресс» универсальный механизм клеточных повреждений и общее патогенетическое звено в механизме воздействия на организм факторов среды Владимиров Ю. А. , Арчаков А. И. Перекисное окисление липидов в биомембранах. М. : Наука, 1972
Свободнорадикальное окисление непрерывно протекает в норме во всех тканях живых организмов интенсификация СРО может быть следствием недостаточность антиоксидантной системы гиперпродукция свободных радикалов СР АО АО СР «окислительный стресс» универсальный механизм клеточных повреждений и общее патогенетическое звено в механизме воздействия на организм факторов среды Владимиров Ю. А. , Арчаков А. И. Перекисное окисление липидов в биомембранах. М. : Наука, 1972
 СВОБОДНЫЕ РАДИКАЛЫ АКТИВНЫЕ ФОРМЫ КИСЛОРОДА КЛАССИФИКАЦИЯ ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ИСТОЧНИКИ ОБРАЗОВАНИЯ В ОРГАНИЗМЕ
СВОБОДНЫЕ РАДИКАЛЫ АКТИВНЫЕ ФОРМЫ КИСЛОРОДА КЛАССИФИКАЦИЯ ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ИСТОЧНИКИ ОБРАЗОВАНИЯ В ОРГАНИЗМЕ
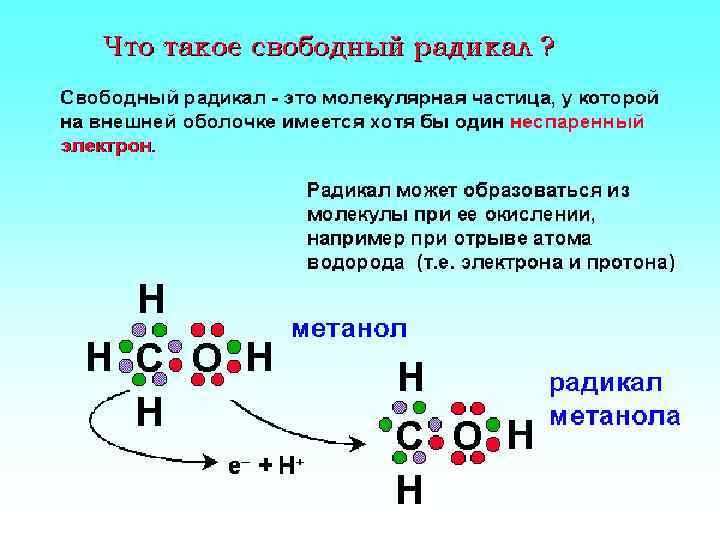
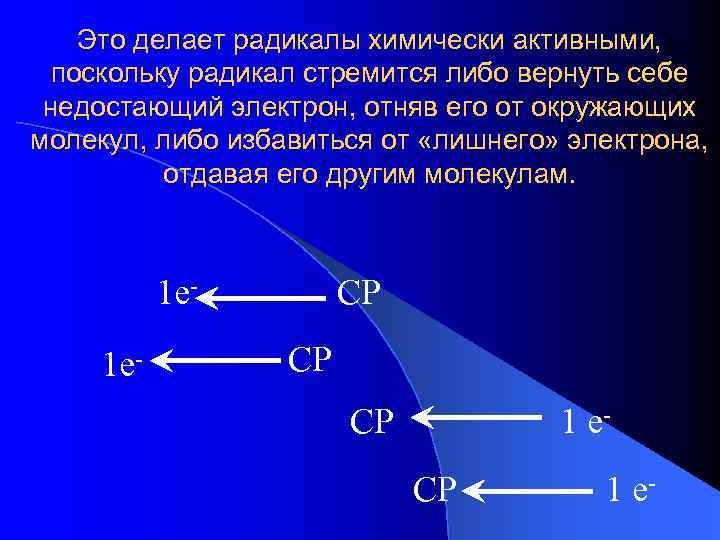 Это делает радикалы химически активными, поскольку радикал стремится либо вернуть себе недостающий электрон, отняв его от окружающих молекул, либо избавиться от «лишнего» электрона, отдавая его другим молекулам. 1 е 1 е- СР СР СР 1 е-
Это делает радикалы химически активными, поскольку радикал стремится либо вернуть себе недостающий электрон, отняв его от окружающих молекул, либо избавиться от «лишнего» электрона, отдавая его другим молекулам. 1 е 1 е- СР СР СР 1 е-
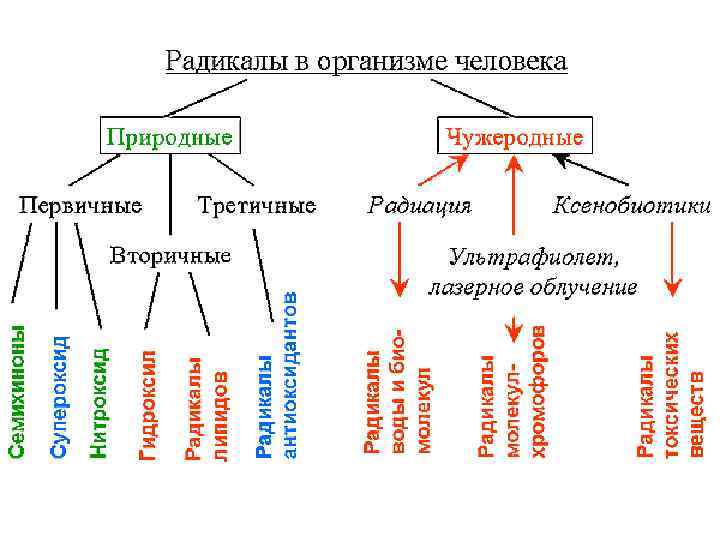
 СР Общая особенность АКМ – малые значения времен жизни в биологических субстратах, что в некоторой степени компенсирует их высокую реакционную способность. Зенков Н. К. , Ланкин В. З. , Меньщикова Е. Б. , 2001
СР Общая особенность АКМ – малые значения времен жизни в биологических субстратах, что в некоторой степени компенсирует их высокую реакционную способность. Зенков Н. К. , Ланкин В. З. , Меньщикова Е. Б. , 2001
 СР Активные формы кислорода (АФК) – высокореакционные, преимущественно радикальные кислородные соединения, образующиеся в живых организмах в результате неполного восстановления молекулярного кислорода или изменения спина одного из электронов, находящихся на внешних орбиталях
СР Активные формы кислорода (АФК) – высокореакционные, преимущественно радикальные кислородные соединения, образующиеся в живых организмах в результате неполного восстановления молекулярного кислорода или изменения спина одного из электронов, находящихся на внешних орбиталях
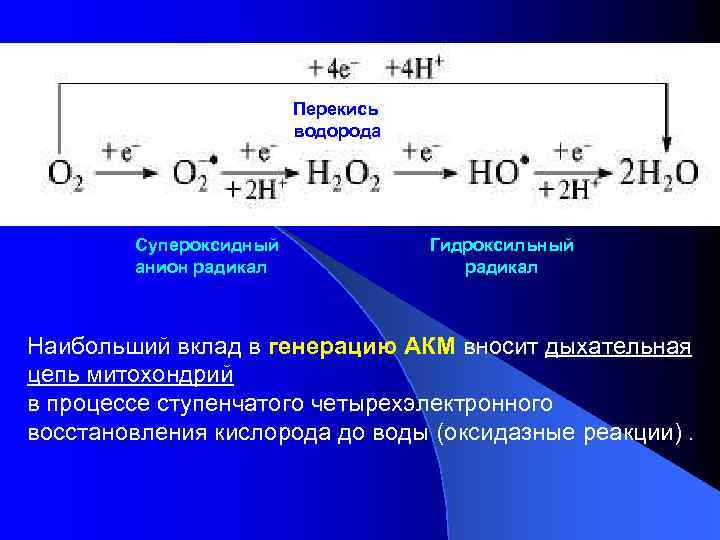 Перекись водорода Супероксидный анион радикал Гидроксильный радикал Наибольший вклад в генерацию АКМ вносит дыхательная цепь митохондрий в процессе ступенчатого четырехэлектронного восстановления кислорода до воды (оксидазные реакции).
Перекись водорода Супероксидный анион радикал Гидроксильный радикал Наибольший вклад в генерацию АКМ вносит дыхательная цепь митохондрий в процессе ступенчатого четырехэлектронного восстановления кислорода до воды (оксидазные реакции).
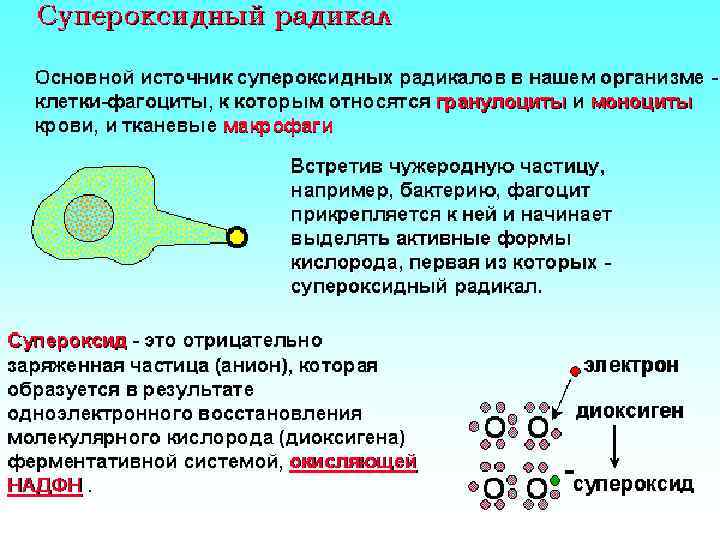
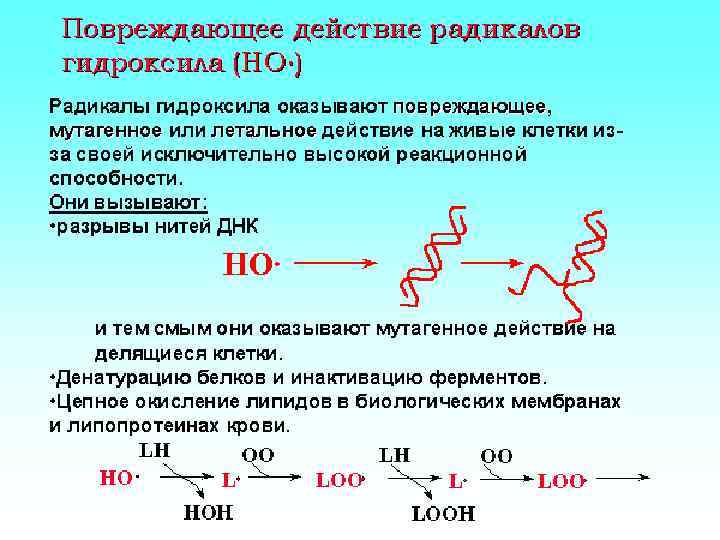
 Другие виды АФК НО 2* - гидроперекисный радикал (время жизни 10 -3) * Ингибирует перекисное окисление липидов * Переходит в Н 2 О 2 RО* NО* - алкоксильный радикал (время жизни 10 -6) * Ингибирует перекисное окисление липидов * Обладает цитотоксическим и канцерогенным действием - нитроксильный радикал (время жизни 10 -1) * Релаксация гладкомышечных клеток * Обладает цитотоксическим действием * Ингибирование пролиферации лимфоцитов * Нейрорегуляция
Другие виды АФК НО 2* - гидроперекисный радикал (время жизни 10 -3) * Ингибирует перекисное окисление липидов * Переходит в Н 2 О 2 RО* NО* - алкоксильный радикал (время жизни 10 -6) * Ингибирует перекисное окисление липидов * Обладает цитотоксическим и канцерогенным действием - нитроксильный радикал (время жизни 10 -1) * Релаксация гладкомышечных клеток * Обладает цитотоксическим действием * Ингибирование пролиферации лимфоцитов * Нейрорегуляция
 Другие виды АФК RО 2 О 21 - перекисный радикал (время жизни 10 -2 -10) * Взаимодействует с ненасыщенными липидами * Реакция рекомбинации сопровождается свечением - синглетный кислород (время жизни 10 -6) * Индуцирует реакции перекисного окисления липидов * Обладает цитотоксическим и мутагенным действием ОBr- OCl- -галогеновые производные - (время жизни зависит от субстрата) OI ОСN * Индуцируют реакции перекисного окисления липидов * Обладают цитотоксическим и мутагенным действием
Другие виды АФК RО 2 О 21 - перекисный радикал (время жизни 10 -2 -10) * Взаимодействует с ненасыщенными липидами * Реакция рекомбинации сопровождается свечением - синглетный кислород (время жизни 10 -6) * Индуцирует реакции перекисного окисления липидов * Обладает цитотоксическим и мутагенным действием ОBr- OCl- -галогеновые производные - (время жизни зависит от субстрата) OI ОСN * Индуцируют реакции перекисного окисления липидов * Обладают цитотоксическим и мутагенным действием
 Источники образования АФК 1. Оксидазные реакции на внутренней мембране митохондрий (четырехэлектронное восстановление кислорода до воды)
Источники образования АФК 1. Оксидазные реакции на внутренней мембране митохондрий (четырехэлектронное восстановление кислорода до воды)
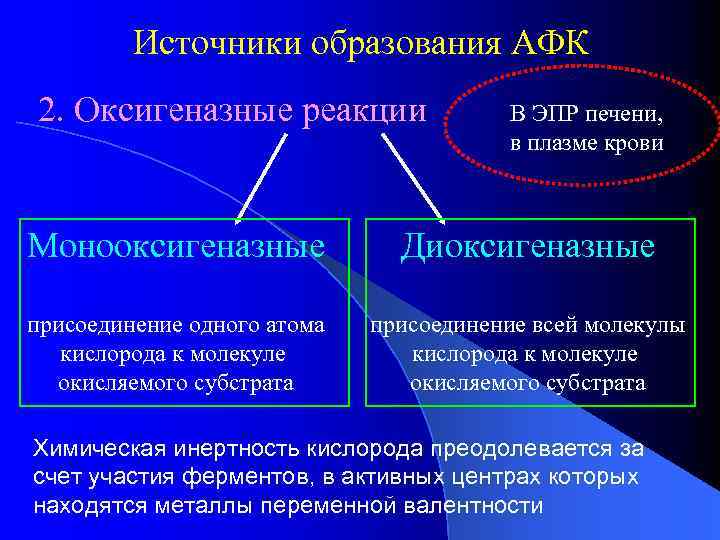 Источники образования АФК 2. Оксигеназные реакции В ЭПР печени, в плазме крови Монооксигеназные Диоксигеназные присоединение одного атома кислорода к молекуле окисляемого субстрата присоединение всей молекулы кислорода к молекуле окисляемого субстрата Химическая инертность кислорода преодолевается за счет участия ферментов, в активных центрах которых находятся металлы переменной валентности
Источники образования АФК 2. Оксигеназные реакции В ЭПР печени, в плазме крови Монооксигеназные Диоксигеназные присоединение одного атома кислорода к молекуле окисляемого субстрата присоединение всей молекулы кислорода к молекуле окисляемого субстрата Химическая инертность кислорода преодолевается за счет участия ферментов, в активных центрах которых находятся металлы переменной валентности
 Источники образования АФК 3. Комплексирование кислорода ионами металлов переменной валентности В живом организме большое количество Ме перементной валентности (железо, медь, магний, марганец) Fe 2+ + ROOH → Fe 3+ + RO* + OH*
Источники образования АФК 3. Комплексирование кислорода ионами металлов переменной валентности В живом организме большое количество Ме перементной валентности (железо, медь, магний, марганец) Fe 2+ + ROOH → Fe 3+ + RO* + OH*
 Источники образования АФК 4. Аутоокисление гемоглобина Hb + O 2 → Hb…. . O 2 →Met Hb + O 25. Реакция гипоксантин - ксантиноксидаза в большинстве органов Ксантиноксидаза Ксантиндегидрогеназа * участие в окислительных процессах * участие в метаболизме пуринов * участие в окислении пиримидинов, жирных кислот глутатиона, адреналина
Источники образования АФК 4. Аутоокисление гемоглобина Hb + O 2 → Hb…. . O 2 →Met Hb + O 25. Реакция гипоксантин - ксантиноксидаза в большинстве органов Ксантиноксидаза Ксантиндегидрогеназа * участие в окислительных процессах * участие в метаболизме пуринов * участие в окислении пиримидинов, жирных кислот глутатиона, адреналина
 Источники образования АФК 6. Пероксисомы Содержат Н 2 О 2 -генерирующие ферменты: Оксидаза L-α-оксикислот Оксидаза D-аминокислот Глицилоксидаза и др. Один из главных источников Генерации перекиси водорода До 35%
Источники образования АФК 6. Пероксисомы Содержат Н 2 О 2 -генерирующие ферменты: Оксидаза L-α-оксикислот Оксидаза D-аминокислот Глицилоксидаза и др. Один из главных источников Генерации перекиси водорода До 35%
 Источники образования АФК 6. Система фагоцитоза – совокупность клеток и гуморальных факторов, обеспечивающих основной уровень структурного гомеостаза фагоциты микрофаги Нейтрофилы Эозинофилы Базофилы крови макрофаги Клетки тканей (селезенки, лимфоузлов) Монобласты Моноциты (предшественники)
Источники образования АФК 6. Система фагоцитоза – совокупность клеток и гуморальных факторов, обеспечивающих основной уровень структурного гомеостаза фагоциты микрофаги Нейтрофилы Эозинофилы Базофилы крови макрофаги Клетки тканей (селезенки, лимфоузлов) Монобласты Моноциты (предшественники)
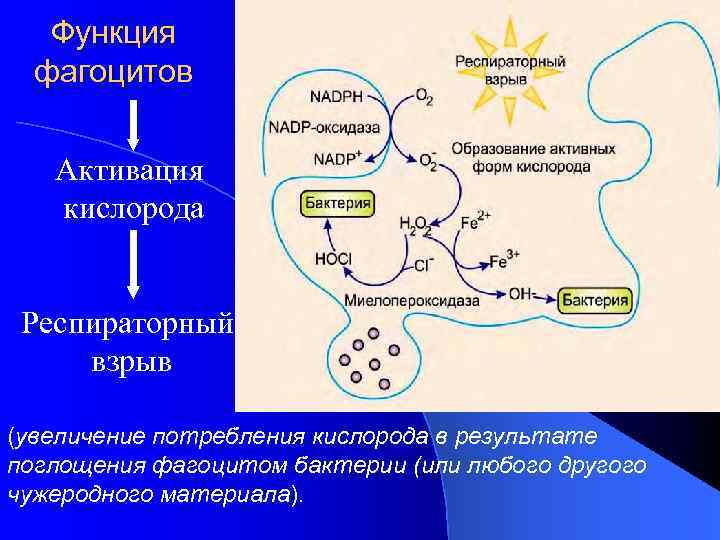 Функция фагоцитов Активация кислорода Респираторный взрыв (увеличение потребления кислорода в результате поглощения фагоцитом бактерии (или любого другого чужеродного материала).
Функция фагоцитов Активация кислорода Респираторный взрыв (увеличение потребления кислорода в результате поглощения фагоцитом бактерии (или любого другого чужеродного материала).
 СР Повреждающее действие АКМ (АФК) Липиды Белки ДНК
СР Повреждающее действие АКМ (АФК) Липиды Белки ДНК
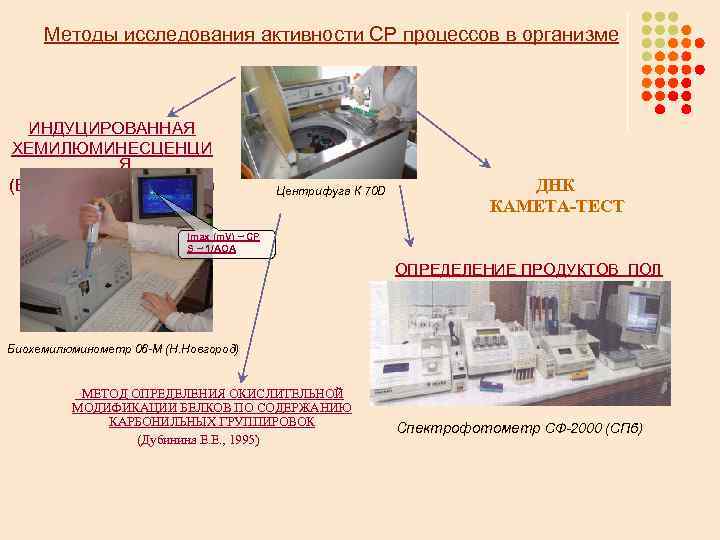 Методы исследования активности СР процессов в организме ИНДУЦИРОВАННАЯ ХЕМИЛЮМИНЕСЦЕНЦИ Я (Ермолин С. В. и др. , 1990) Центрифуга К 70 D ДНК КАМЕТА-ТЕСТ Imax (m. V) ~ СР S ~ 1/АОА ОПРЕДЕЛЕНИЕ ПРОДУКТОВ ПОЛ Биохемилюминометр 06 -М (Н. Новгород) МЕТОД ОПРЕДЕЛЕНИЯ ОКИСЛИТЕЛЬНОЙ МОДИФИКАЦИИ БЕЛКОВ ПО СОДЕРЖАНИЮ КАРБОНИЛЬНЫХ ГРУППИРОВОК (Дубинина Е. Е. , 1995) Спектрофотометр СФ-2000 (СПб)
Методы исследования активности СР процессов в организме ИНДУЦИРОВАННАЯ ХЕМИЛЮМИНЕСЦЕНЦИ Я (Ермолин С. В. и др. , 1990) Центрифуга К 70 D ДНК КАМЕТА-ТЕСТ Imax (m. V) ~ СР S ~ 1/АОА ОПРЕДЕЛЕНИЕ ПРОДУКТОВ ПОЛ Биохемилюминометр 06 -М (Н. Новгород) МЕТОД ОПРЕДЕЛЕНИЯ ОКИСЛИТЕЛЬНОЙ МОДИФИКАЦИИ БЕЛКОВ ПО СОДЕРЖАНИЮ КАРБОНИЛЬНЫХ ГРУППИРОВОК (Дубинина Е. Е. , 1995) Спектрофотометр СФ-2000 (СПб)
 Антиоксидантная система защиты организма
Антиоксидантная система защиты организма
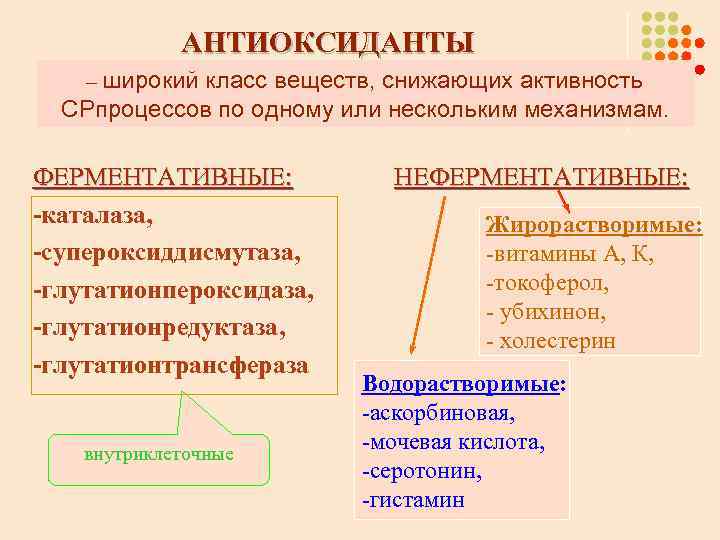 АНТИОКСИДАНТЫ – широкий класс веществ, снижающих активность СРпроцессов по одному или нескольким механизмам. ФЕРМЕНТАТИВНЫЕ: -каталаза, -супероксиддисмутаза, -глутатионпероксидаза, -глутатионредуктаза, -глутатионтрансфераза внутриклеточные НЕФЕРМЕНТАТИВНЫЕ: Жирорастворимые: -витамины А, К, -токоферол, - убихинон, - холестерин Водорастворимые: -аскорбиновая, -мочевая кислота, -серотонин, -гистамин
АНТИОКСИДАНТЫ – широкий класс веществ, снижающих активность СРпроцессов по одному или нескольким механизмам. ФЕРМЕНТАТИВНЫЕ: -каталаза, -супероксиддисмутаза, -глутатионпероксидаза, -глутатионредуктаза, -глутатионтрансфераза внутриклеточные НЕФЕРМЕНТАТИВНЫЕ: Жирорастворимые: -витамины А, К, -токоферол, - убихинон, - холестерин Водорастворимые: -аскорбиновая, -мочевая кислота, -серотонин, -гистамин
 Природные антиоксиданты Антиоксиданты Локализация Функция Ферменты, белки СОД Каталаза Пероксидазы Ферритин Трансферин Лактоферин Церулоплазмин Альбумин Низкомолекуляр ные вещества Витамин Е Плазма крови, клетки Пероксисомы Клеточные мембраны, митохондрии Цитоплазма Внеклеточная жидкость То же ~ ~ Дисмутация О 12 Деградация Н 2 О 2 Связывание Fе То же ~ Связывание Fе, Cu, дисмутация О 12 То же Клеточные мембраны Каротиноиды Витамин С Мочевая кислота Билирубин Клеточные мембраны Цитоплазма Кровь То же Нейтрализация жирорастворимых радикалов То же Нейтрализация О 2 -, ОН· То же ~
Природные антиоксиданты Антиоксиданты Локализация Функция Ферменты, белки СОД Каталаза Пероксидазы Ферритин Трансферин Лактоферин Церулоплазмин Альбумин Низкомолекуляр ные вещества Витамин Е Плазма крови, клетки Пероксисомы Клеточные мембраны, митохондрии Цитоплазма Внеклеточная жидкость То же ~ ~ Дисмутация О 12 Деградация Н 2 О 2 Связывание Fе То же ~ Связывание Fе, Cu, дисмутация О 12 То же Клеточные мембраны Каротиноиды Витамин С Мочевая кислота Билирубин Клеточные мембраны Цитоплазма Кровь То же Нейтрализация жирорастворимых радикалов То же Нейтрализация О 2 -, ОН· То же ~
 АНТИОКСИДАНТЫ – широкий класс веществ, снижающих активность СРпроцессов по одному или нескольким механизмам. ПО МЕХАНИЗМУ ДЕЙСТВИЯ: 1) Антирадикальные ингибиторы (перехватчики органических радикалов); 2) Антиокислители (взаимодействуют с органическими перекисями); 3) Хелаторы (связывают ионы Me переменной валентности); 4) Тушители (безизлучательно инактивируют синглетный кислород) ЗАЙЦЕВ В. Г. , ОСТРОВСКИЙ О. В. , ЗАКРЕВСКИЙ В. И. , 2003
АНТИОКСИДАНТЫ – широкий класс веществ, снижающих активность СРпроцессов по одному или нескольким механизмам. ПО МЕХАНИЗМУ ДЕЙСТВИЯ: 1) Антирадикальные ингибиторы (перехватчики органических радикалов); 2) Антиокислители (взаимодействуют с органическими перекисями); 3) Хелаторы (связывают ионы Me переменной валентности); 4) Тушители (безизлучательно инактивируют синглетный кислород) ЗАЙЦЕВ В. Г. , ОСТРОВСКИЙ О. В. , ЗАКРЕВСКИЙ В. И. , 2003
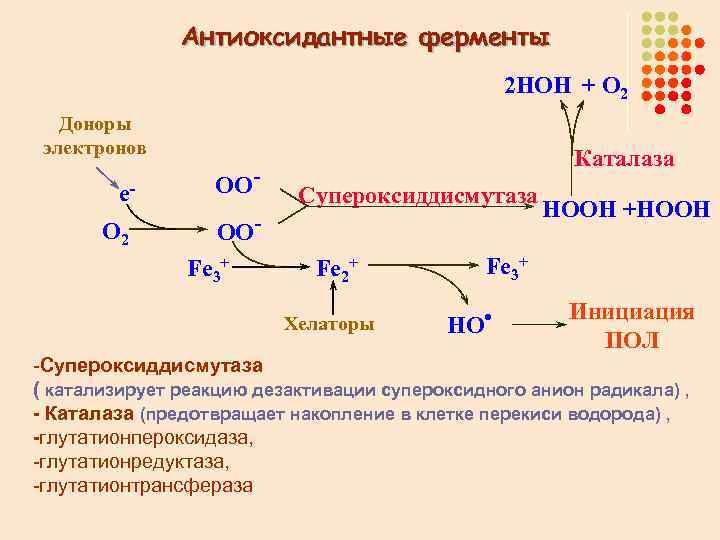 Антиоксидантные ферменты 2 НОН + О 2 Доноры электронов е- ОО- О 2 Каталаза ООFe 3+ Супероксиддисмутаза Fe 2+ Хелаторы НООН +НООН Fe 3+ НО • Инициация ПОЛ -Супероксиддисмутаза ( катализирует реакцию дезактивации супероксидного анион радикала) , - Каталаза (предотвращает накопление в клетке перекиси водорода) , -глутатионпероксидаза, -глутатионредуктаза, -глутатионтрансфераза
Антиоксидантные ферменты 2 НОН + О 2 Доноры электронов е- ОО- О 2 Каталаза ООFe 3+ Супероксиддисмутаза Fe 2+ Хелаторы НООН +НООН Fe 3+ НО • Инициация ПОЛ -Супероксиддисмутаза ( катализирует реакцию дезактивации супероксидного анион радикала) , - Каталаза (предотвращает накопление в клетке перекиси водорода) , -глутатионпероксидаза, -глутатионредуктаза, -глутатионтрансфераза
 Супероксиддисмутаза (СОД) - единственный известный в настоящее время фермент, субстратом которого являются свободные радикалы. Формы СОД отличаются по содержанию металлов: -Сu, Zn-СОД, -Mn – COD, -Fe -СОД. Фермент, обнаруженный Мак. Кордом и Фридовичем имеет молекулярную массу 32 к. Д и состоит из двух субъединиц, каждая из которых содержит по одному атому Сu и одному атому Zn: Сu 2+ Zn 2+
Супероксиддисмутаза (СОД) - единственный известный в настоящее время фермент, субстратом которого являются свободные радикалы. Формы СОД отличаются по содержанию металлов: -Сu, Zn-СОД, -Mn – COD, -Fe -СОД. Фермент, обнаруженный Мак. Кордом и Фридовичем имеет молекулярную массу 32 к. Д и состоит из двух субъединиц, каждая из которых содержит по одному атому Сu и одному атому Zn: Сu 2+ Zn 2+
 Супероксиддисмутаза (СОД) Катализирует реакцию дезактивации супероксидного анион радикала -заключается в переносе электрона с одного супероксидного радикала на другой. -промежуточный акцептор этого электрона - атом меди, входящий в активный центр СОД: 1. СОД-Сu 2+ + HO 2 • 2. СОД-Сu+ + O 2 + 2 H+ СОД-Сu+ + O 2 СОД-Сu 2+ + Н 2 О 2 Zn 2+ не участвует в каталитическом цикле, хотя и входит в активный центр. Ионы металлов защищают молекулу СОД от воздействий различных протеаз.
Супероксиддисмутаза (СОД) Катализирует реакцию дезактивации супероксидного анион радикала -заключается в переносе электрона с одного супероксидного радикала на другой. -промежуточный акцептор этого электрона - атом меди, входящий в активный центр СОД: 1. СОД-Сu 2+ + HO 2 • 2. СОД-Сu+ + O 2 + 2 H+ СОД-Сu+ + O 2 СОД-Сu 2+ + Н 2 О 2 Zn 2+ не участвует в каталитическом цикле, хотя и входит в активный центр. Ионы металлов защищают молекулу СОД от воздействий различных протеаз.
 Деактивация перекиси водорода Перекись водорода (Н 2 О 2) - основной источник самых токсичных радикалов в живых системах - НО* радикалов. Следовательно, снижение уровня Н 2 О 2 приведет к снижению концентрации НО* радикалов. Удаление Н 2 О 2 осуществляют два класса ферментов: каталаза 2 Н 2 О 2 каталаза 2 Н 2 О + О 2 Каталаза представляет собой гемовый фермент, состоящий из четырех субъединиц с общей молекулярной массой около 240 к. Д. пероксидазы Н 2 О 2 + АН 2 пероксидаза 2 Н 2 О + А Пероксидазы также являются ферментами, разрушающими Н 2 О 2 нерадикальным путем и образующими Н 2 О; при этом окислению подвергается не вторая молекула Н 2 О 2, как в случае каталазы, а другие субстраты (АН 2).
Деактивация перекиси водорода Перекись водорода (Н 2 О 2) - основной источник самых токсичных радикалов в живых системах - НО* радикалов. Следовательно, снижение уровня Н 2 О 2 приведет к снижению концентрации НО* радикалов. Удаление Н 2 О 2 осуществляют два класса ферментов: каталаза 2 Н 2 О 2 каталаза 2 Н 2 О + О 2 Каталаза представляет собой гемовый фермент, состоящий из четырех субъединиц с общей молекулярной массой около 240 к. Д. пероксидазы Н 2 О 2 + АН 2 пероксидаза 2 Н 2 О + А Пероксидазы также являются ферментами, разрушающими Н 2 О 2 нерадикальным путем и образующими Н 2 О; при этом окислению подвергается не вторая молекула Н 2 О 2, как в случае каталазы, а другие субстраты (АН 2).
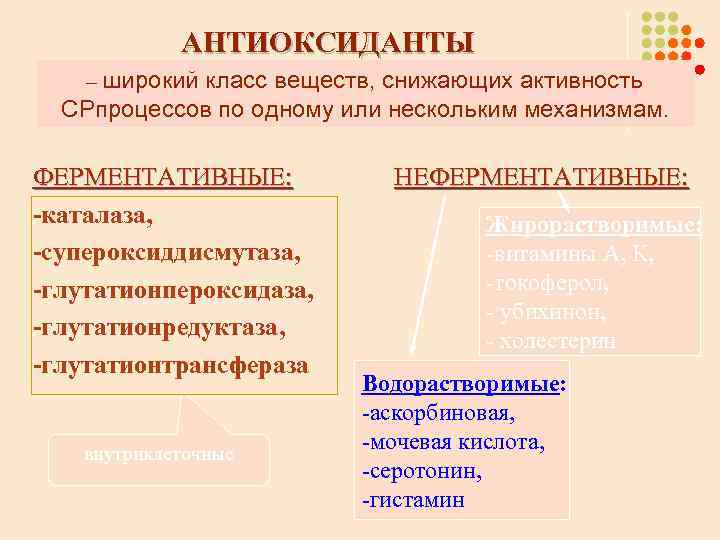 АНТИОКСИДАНТЫ – широкий класс веществ, снижающих активность СРпроцессов по одному или нескольким механизмам. ФЕРМЕНТАТИВНЫЕ: -каталаза, -супероксиддисмутаза, -глутатионпероксидаза, -глутатионредуктаза, -глутатионтрансфераза внутриклеточные НЕФЕРМЕНТАТИВНЫЕ: Жирорастворимые: -витамины А, К, -токоферол, - убихинон, - холестерин Водорастворимые: -аскорбиновая, -мочевая кислота, -серотонин, -гистамин
АНТИОКСИДАНТЫ – широкий класс веществ, снижающих активность СРпроцессов по одному или нескольким механизмам. ФЕРМЕНТАТИВНЫЕ: -каталаза, -супероксиддисмутаза, -глутатионпероксидаза, -глутатионредуктаза, -глутатионтрансфераза внутриклеточные НЕФЕРМЕНТАТИВНЫЕ: Жирорастворимые: -витамины А, К, -токоферол, - убихинон, - холестерин Водорастворимые: -аскорбиновая, -мочевая кислота, -серотонин, -гистамин
 Антирадикальные ингибиторы T l Аскорбиновая кислота (витамин С, аскорбат) Защитный эффект аскорбата основан на том, что образующиеся в результате его окисления промежуточные радикалы и молекулы менее активны, чем НО* радикалы.
Антирадикальные ингибиторы T l Аскорбиновая кислота (витамин С, аскорбат) Защитный эффект аскорбата основан на том, что образующиеся в результате его окисления промежуточные радикалы и молекулы менее активны, чем НО* радикалы.
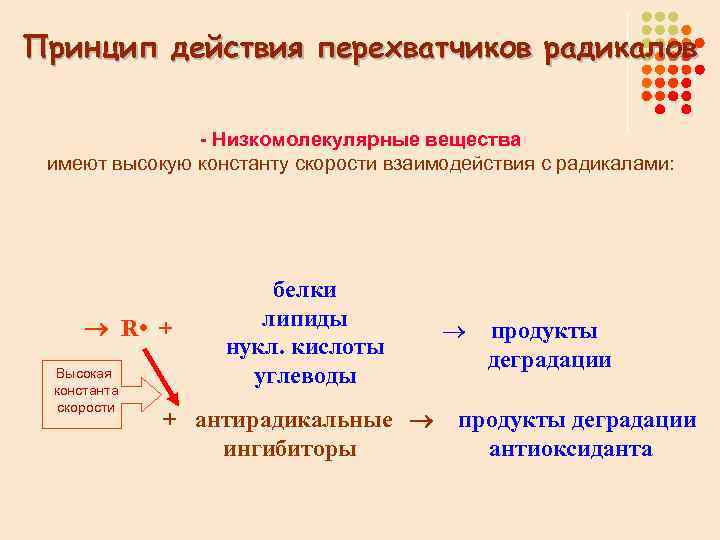 Принцип действия перехватчиков радикалов - Низкомолекулярные вещества имеют высокую константу скорости взаимодействия с радикалами: R • + Высокая константа скорости белки липиды нукл. кислоты углеводы + антирадикальные ингибиторы ® продукты деградации антиоксиданта
Принцип действия перехватчиков радикалов - Низкомолекулярные вещества имеют высокую константу скорости взаимодействия с радикалами: R • + Высокая константа скорости белки липиды нукл. кислоты углеводы + антирадикальные ингибиторы ® продукты деградации антиоксиданта
 Аскорбиновая кислота (витамин С) -В защите липидов от перекисного окисления превосходит по своей активности все АО плазмы, - нейтрализует окислители, поступающие с загрязненным воздухом (NO, свободные радикалы сигаретного дыма), - редуцирует канцерогенные нитроамины, - является синергистом b-каротина и токоферола. Однако, в присутствии Fe или Cu становится мощным прооксидантом.
Аскорбиновая кислота (витамин С) -В защите липидов от перекисного окисления превосходит по своей активности все АО плазмы, - нейтрализует окислители, поступающие с загрязненным воздухом (NO, свободные радикалы сигаретного дыма), - редуцирует канцерогенные нитроамины, - является синергистом b-каротина и токоферола. Однако, в присутствии Fe или Cu становится мощным прооксидантом.
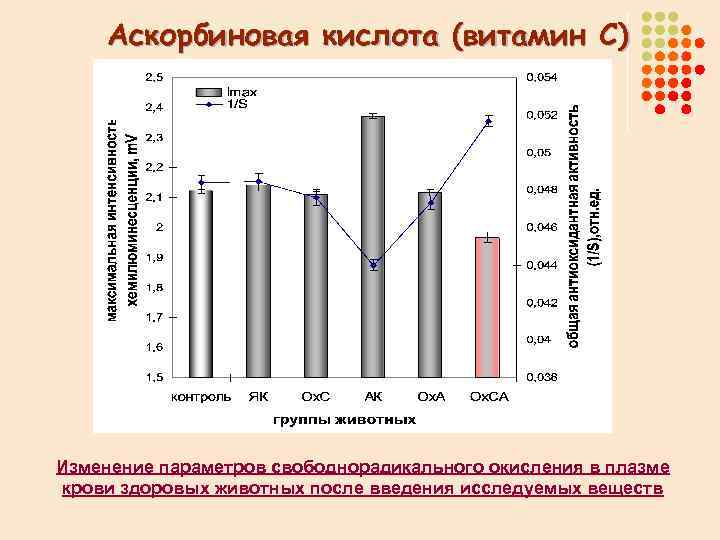 Аскорбиновая кислота (витамин С) Изменение параметров свободнорадикального окисления в плазме крови здоровых животных после введения исследуемых веществ
Аскорбиновая кислота (витамин С) Изменение параметров свободнорадикального окисления в плазме крови здоровых животных после введения исследуемых веществ
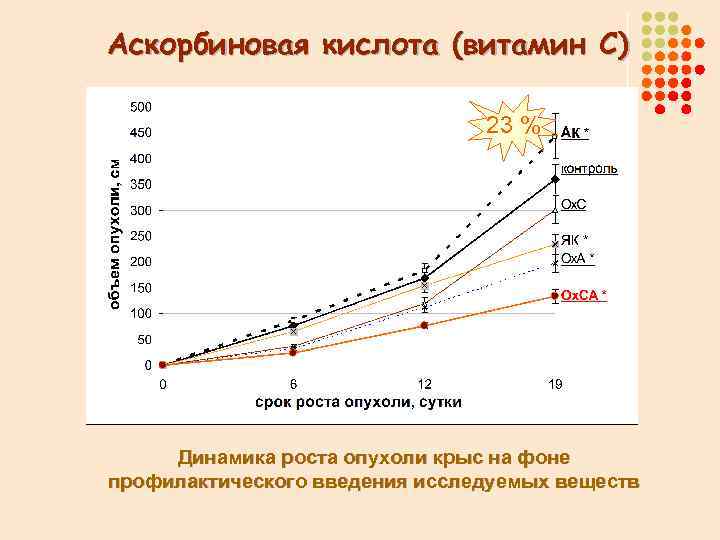 Аскорбиновая кислота (витамин С) 23 % Динамика роста опухоли крыс на фоне профилактического введения исследуемых веществ
Аскорбиновая кислота (витамин С) 23 % Динамика роста опухоли крыс на фоне профилактического введения исследуемых веществ
 ? ? ? ? ?
? ? ? ? ?
 Свободнорадикальное окисление непрерывно протекает в норме во всех тканях живых организмов интенсификация СРО может быть следствием недостаточность антиоксидантной системы гиперпродукция свободных радикалов СР АО АО СР «окислительный стресс» универсальный механизм клеточных повреждений и общее патогенетическое звено в механизме воздействия на организм факторов среды Владимиров Ю. А. , Арчаков А. И. Перекисное окисление липидов в биомембранах. М. : Наука, 1972
Свободнорадикальное окисление непрерывно протекает в норме во всех тканях живых организмов интенсификация СРО может быть следствием недостаточность антиоксидантной системы гиперпродукция свободных радикалов СР АО АО СР «окислительный стресс» универсальный механизм клеточных повреждений и общее патогенетическое звено в механизме воздействия на организм факторов среды Владимиров Ю. А. , Арчаков А. И. Перекисное окисление липидов в биомембранах. М. : Наука, 1972


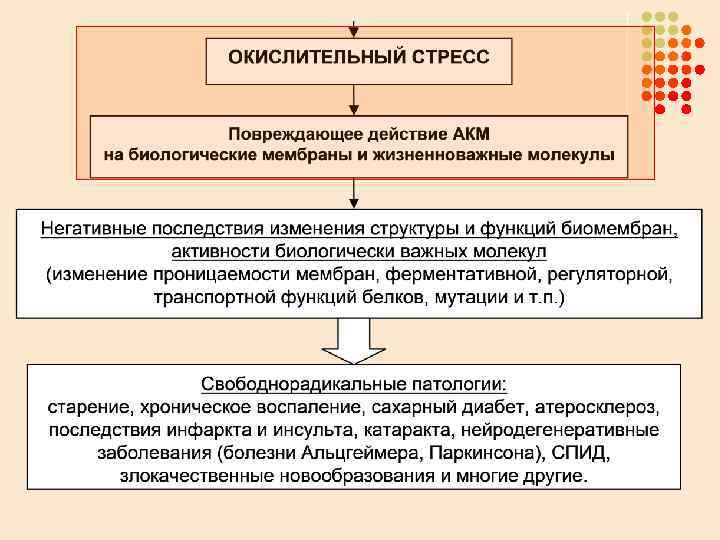
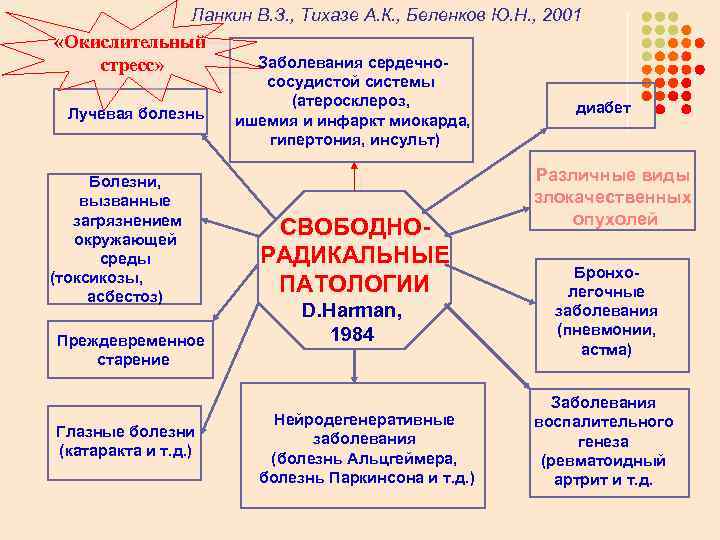 Ланкин В. З. , Тихазе А. К. , Беленков Ю. Н. , 2001 «Окислительный стресс» Лучевая болезнь Болезни, вызванные загрязнением окружающей среды (токсикозы, асбестоз) Преждевременное старение Глазные болезни (катаракта и т. д. ) Заболевания сердечнососудистой системы (атеросклероз, ишемия и инфаркт миокарда, гипертония, инсульт) СВОБОДНОРАДИКАЛЬНЫЕ ПАТОЛОГИИ D. Harman, 1984 Нейродегенеративные заболевания (болезнь Альцгеймера, болезнь Паркинсона и т. д. ) диабет Различные виды злокачественных опухолей Бронхолегочные заболевания (пневмонии, астма) Заболевания воспалительного генеза (ревматоидный артрит и т. д.
Ланкин В. З. , Тихазе А. К. , Беленков Ю. Н. , 2001 «Окислительный стресс» Лучевая болезнь Болезни, вызванные загрязнением окружающей среды (токсикозы, асбестоз) Преждевременное старение Глазные болезни (катаракта и т. д. ) Заболевания сердечнососудистой системы (атеросклероз, ишемия и инфаркт миокарда, гипертония, инсульт) СВОБОДНОРАДИКАЛЬНЫЕ ПАТОЛОГИИ D. Harman, 1984 Нейродегенеративные заболевания (болезнь Альцгеймера, болезнь Паркинсона и т. д. ) диабет Различные виды злокачественных опухолей Бронхолегочные заболевания (пневмонии, астма) Заболевания воспалительного генеза (ревматоидный артрит и т. д.
 1956 Семенов Н. Н. - открытие разветвленных цепных реакций 1954 Б. Н. Тарусов- новый тип патогенетических факторов: инициированное внешними воздействиями и резко активированное свободно-радикальное окисление 1957 Н. М. Эмануэль, 1962 А. И. Журавлев, 1963 Е. А. Нейфах, 1970 Е. Б. Бурлакова, 1972 Ю. А. Владимиров, 1989 Е. П. Сидорик, Е. А. Баглей AO tumor СР СР ОРГАНИЗМ АО
1956 Семенов Н. Н. - открытие разветвленных цепных реакций 1954 Б. Н. Тарусов- новый тип патогенетических факторов: инициированное внешними воздействиями и резко активированное свободно-радикальное окисление 1957 Н. М. Эмануэль, 1962 А. И. Журавлев, 1963 Е. А. Нейфах, 1970 Е. Б. Бурлакова, 1972 Ю. А. Владимиров, 1989 Е. П. Сидорик, Е. А. Баглей AO tumor СР СР ОРГАНИЗМ АО
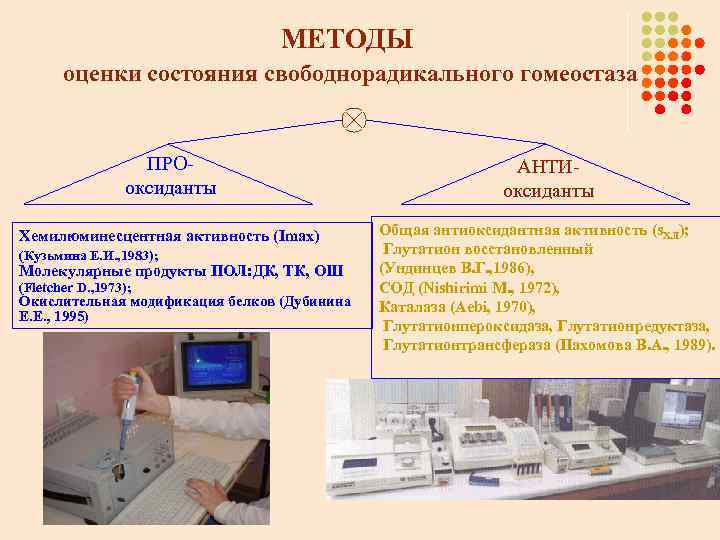 МЕТОДЫ оценки состояния свободнорадикального гомеостаза ПРОоксиданты АНТИоксиданты Хемилюминесцентная активность (Imax) Общая антиоксидантная активность (s. ХЛ); Глутатион восстановленный (Ундинцев В. Г. , 1986), СОД (Nishirimi M. , 1972), Каталаза (Aebi, 1970), Глутатионпероксидаза, Глутатионредуктаза, Глутатионтрансфераза (Пахомова В. А. , 1989). (Кузьмина Е. И. , 1983); Молекулярные продукты ПОЛ: ДК, ТК, ОШ (Fletcher D. , 1973); Окислительная модификация белков (Дубинина Е. Е. , 1995)
МЕТОДЫ оценки состояния свободнорадикального гомеостаза ПРОоксиданты АНТИоксиданты Хемилюминесцентная активность (Imax) Общая антиоксидантная активность (s. ХЛ); Глутатион восстановленный (Ундинцев В. Г. , 1986), СОД (Nishirimi M. , 1972), Каталаза (Aebi, 1970), Глутатионпероксидаза, Глутатионредуктаза, Глутатионтрансфераза (Пахомова В. А. , 1989). (Кузьмина Е. И. , 1983); Молекулярные продукты ПОЛ: ДК, ТК, ОШ (Fletcher D. , 1973); Окислительная модификация белков (Дубинина Е. Е. , 1995)


