Производство серной кислоты.ppt
- Количество слайдов: 26

Производство серной кислоты.

Особенности серной кислоты: ü самая дешевая из всех кислот ü не дымит ü в концентрированном виде не разрушает черные металлы ü является одной из самых сильных кислот ü в широком диапазоне температур находится в жидком состоянии.
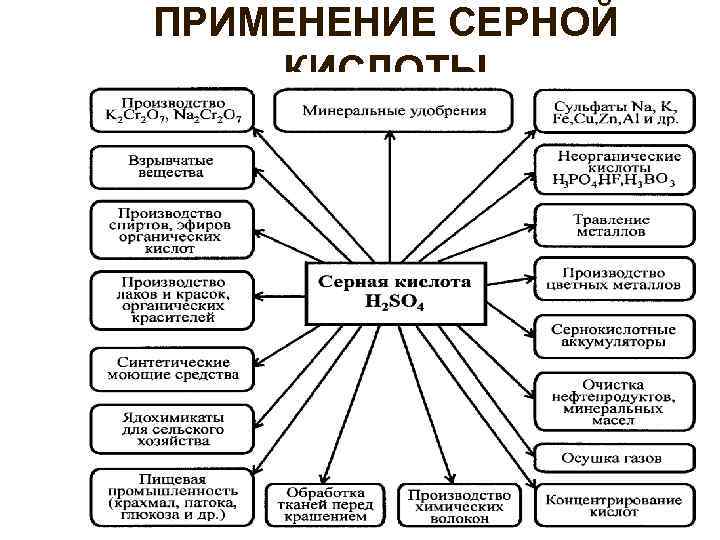
ПРИМЕНЕНИЕ СЕРНОЙ КИСЛОТЫ

СЕРНАЯ КИСЛОТА МОЖЕТ СУЩЕСТВОВАТЬ: ü как самостоятельное химическое соединение H 2 SO 4 ü в виде соединений с водой H 2 SO 4 • 2 Н 2 О, H 2 SO 4 • 4 Н 2 О и с триоксидом серы H 2 SO 4 • 2 SО 3 В технике серной кислотой называют: безводную H 2 SO 4 ü ее водные растворы ü растворы триоксида серы в безводной H 2 SO 4 - олеум (смесь H 2 SO 4 и соединений ü

Безводная серная кислота — тяжелая маслянистая бесцветная жидкость, смешивающаяся с водой и триоксидом серы в любом соотношении. Физические свойства серной кислоты (плотность, температура кристаллизации, температура кипения) зависят от ее состава. ü Безводная 100%-ная серная кислота имеет сравнительно высокую температуру кристаллизации 10, 7 °С. ü

Промышленность выпускает три вида товарной серной кислоты. Концентрация Температура кристаллизации, °C Башенная кислота 75% 29, 5 Контактная кислота 92, 5% 22, 0 Олеум 20% своб. S 0 з +2 -

СЫРЬЁ ДЛЯ ПРОИЗВОДСТВА СЕРНОЙ КИСЛОТЫ Исходные реагенты : ü элементная сера ü серосодержащие соединения, из которых можно получить либо серу, либо диоксид серы: • сульфиды железа • сульфиды цветных металлов (меди, цинка и др. ) • сероводород и др. ТРАДИЦИОННЫЕ ОСНОВНЫЕ ИСТОЧНИКИ СЫРЬЯ : § сера и железный (серный) колчедан. § отходящие газы цветной металлургии, получаемые при обжиге сульфидов цветных металлов и содержащие диоксид

Химическая схема включает реакции: обжиг серного колчедана 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 +8 SO 2 или серы S 2 + 2 O 2 = 2 SO 2; ü окисление диоксида серы SO 2 + 1/2 O 2 = SO 3; ü абсорбция триоксида серы SO 3 + H 2 O = H 2 SO 4. ü
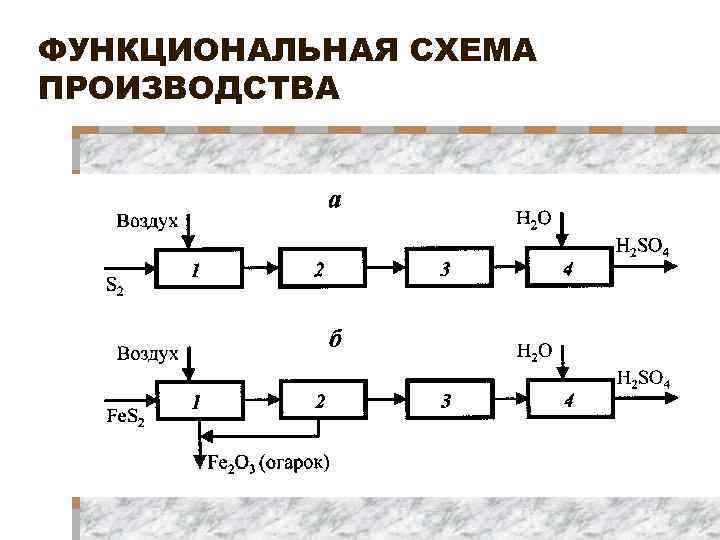
ФУНКЦИОНАЛЬНАЯ СХЕМА ПРОИЗВОДСТВА

Обжиг серосодержащего сырья n ü ü ü Обжиг колчедана (пирита) : термическая диссоциация 2 Fe. S 2 = 2 Fe. S + S 2, газофазное горение серы S 2 + 2 O 2 = 2 SO 2, горение пирротина 4 Fe. S + 7 O 2 = 2 Fe 2 O 3 + 4 SO 2 Суммарная реакция: 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 (1) При небольшом избытке или недостатке кислорода образуется смешанный оксид железа: 3 Fe. S 2 + 8 O 2 = Fe 3 O 4 + 6 SO 2

Термическое разложение пирита начинается при 200°С и воспламеняется сера. n При t > 680°С интенсивно протекают все три реакции. n В промышленности обжиг ведут при 850 -900°С. n Лимитирующая стадия процесса массоперенос окислителя к месту реакции и продуктов разложения в газовую фазу. n
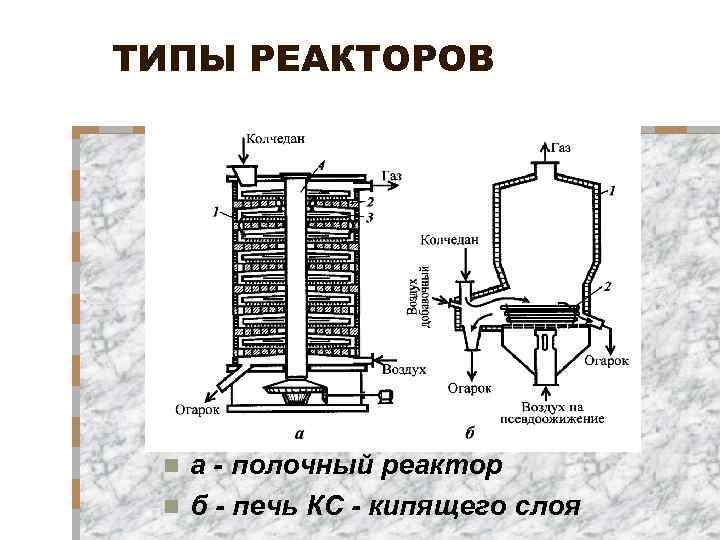
ТИПЫ РЕАКТОРОВ а - полочный реактор n б - печь КС - кипящего слоя n

Полочный реактор Печи КС Недостатки: Преимущества: n n n движущиеся скребки в высокотемпературной зоне усложняют его конструкцию неодинаковый температурный режим по полкам трудно организовать отвод тепла из зоны реакции нельзя получить обжиговый газ с концентрацией SO 2 более 8 -9%. невозможность использования мелких частиц. n n n можно перерабатывать мелкие частицы хороший контакт твёрдых частиц с газом выравнивание температурного слоя по всему полю высокая интенсивность концентрация SO 2 в обжиговом газе - до 13 -15%. Недостатки : n повышенная запыленность обжигового газа из-за механической эрозии подвижных твердых частиц.
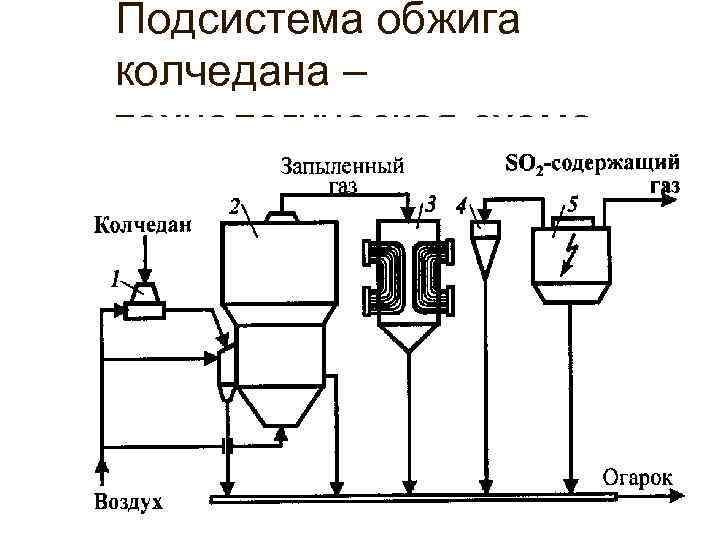
Подсистема обжига колчедана – технологическая схема.

Состав обжигового газа определяется из стехиометрического уравнения (1). N 2 O 2 SO 2 Vн 1 - С 0 Vк 1 - С 0(1 - x) m. C 0 x n С 0 - начальная концентрация кислорода n m - соотношение стехиометрических коэффициентов перед SO 2 и О 2 в уравнении реакции окисления [для реакции (1) m = 8/11]. n Концентрация диоксида серы а в обжиговом газе равна n (2)

n Связь концентраций кислорода b и диоксида серы а: (3) При обжиге колчедана в избытке воздуха уравнение (3) примет вид b = 0, 21 - 1, 3 a. (4) n В действительности содержание кислорода меньше, чем по уравнению (4). Практически можно использовать уравнение b = 0, 21 1, 4 a. n

Сжигание серы. При горении серы по реакции 1/2 S 2 + O 2 = SO 2 часть кислорода эквимолярно переходит в диоксид серы, и потому суммарная концентрация O 2 и SO 2 равна концентрации кислорода С 0 в исходном газе (a + b = C 0), так что при сжигании серы в воздухе b = 0, 21 a (5) n Газ от сжигания серы богаче кислородом, чем от сжигания колчедана. n

Промывка газа после обжига. Примеси: • соединения фтора, селена, теллура, мышьяка. • естественная влага сырья • SO 3 • оксиды азота. Примеси приводят: • к коррозии аппаратуры • к отравлению катализатора • сказываются на качестве серной кислоты.
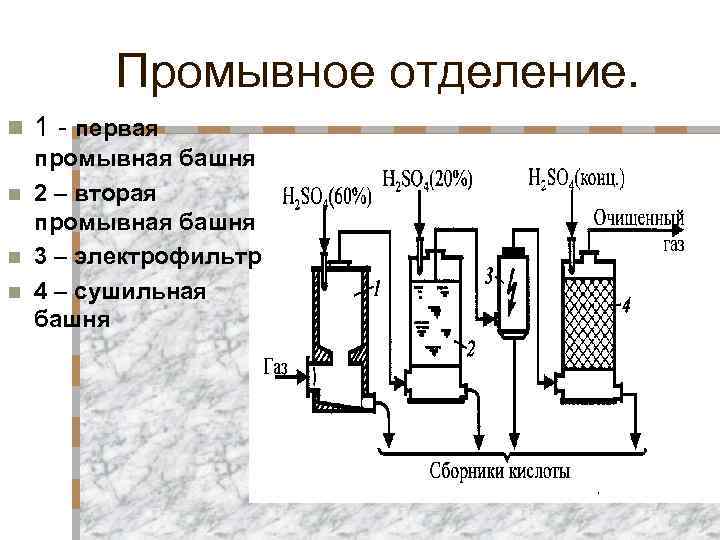
Промывное отделение. n 1 - первая промывная башня n 2 – вторая промывная башня n 3 – электрофильтр n 4 – сушильная башня

Окисление диоксида серы. Физико-химические свойства процесса. SO 2 + 1/2 O 2 = SO 3 (6) n Реакция - обратимая, экзотермическая, протекает на катализаторе с уменьшением объема. При t= 500°С Qр = 94, 2 к. Дж/моль. Константа равновесия Кр [атм-0, 5] зависит от температуры и в интервале 400 -700°С lg. Кр = 4905/T 4, 6455 (7) n Согласно закону действующих масс, при равновесии n

n Равновесную степень превращения диоксида серы xр получим из стехиометрического уравнения (6) и условия равновесия (8): (9) ü 0, 5 axp показывает относительное изменение (уменьшение) объема реакционной смеси. n Скорость реакции r описывается уравнением Борескова-Иванова: (10) ü где k = koexp(-E/RT) - константа скорости реакции, A' = 0, 8 - константа, парциальные давления соответствующих компонентов, атм.
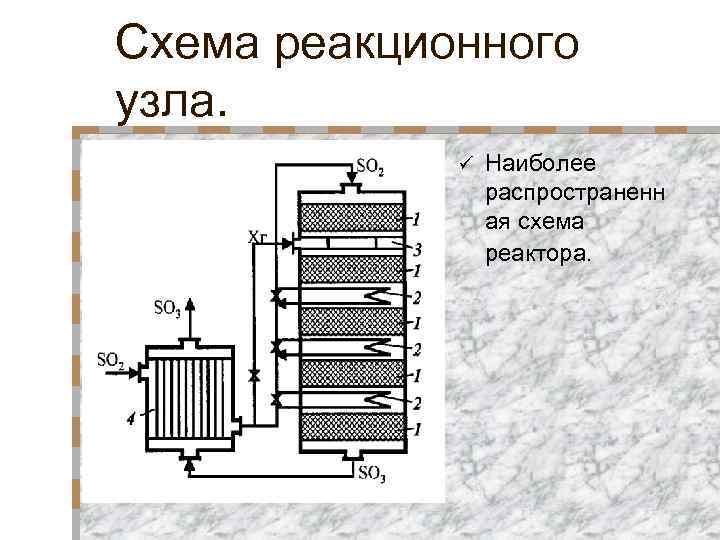
Схема реакционного узла. ü Наиболее распространенн ая схема реактора.
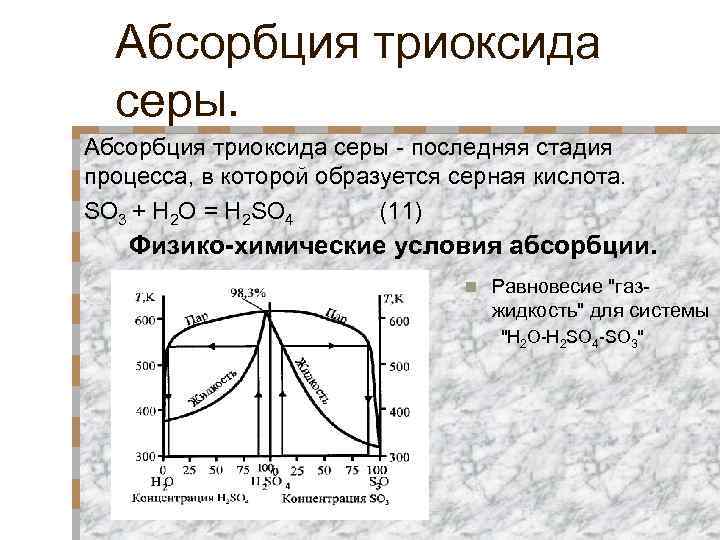
Абсорбция триоксида серы - последняя стадия процесса, в которой образуется серная кислота. SO 3 + H 2 O = H 2 SO 4 (11) Физико-химические условия абсорбции. n Равновесие "газжидкость" для системы "H 2 O-H 2 SO 4 -SO 3"
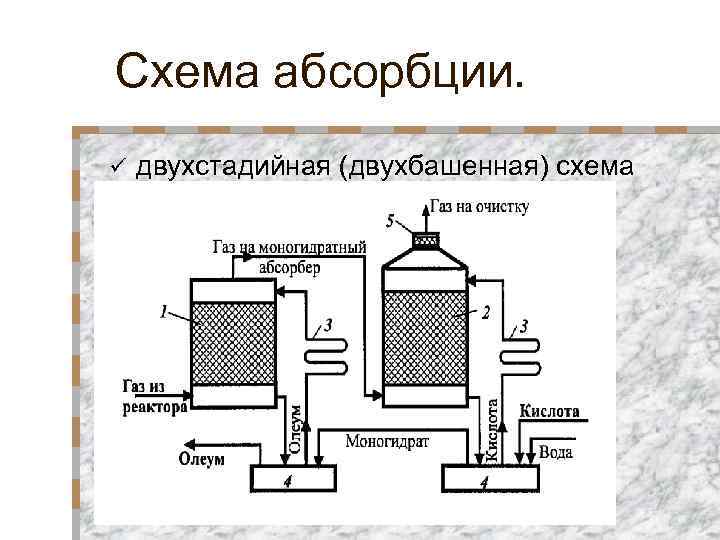
Схема абсорбции. ü двухстадийная (двухбашенная) схема абсорбции
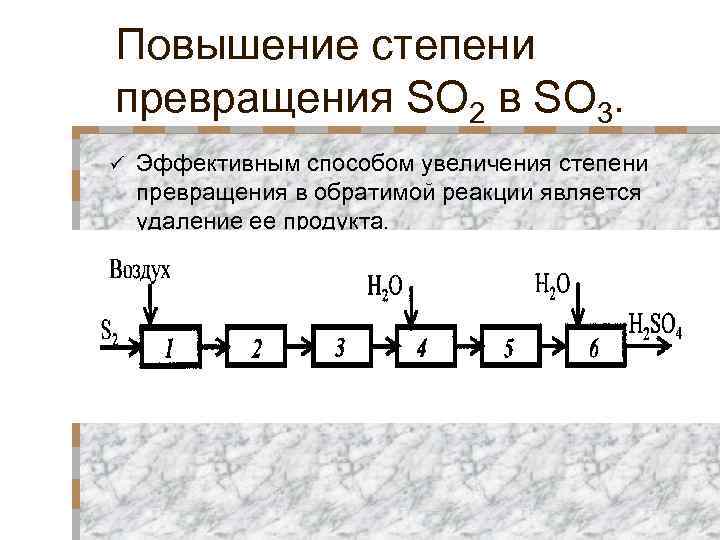
Повышение степени превращения SO 2 в SO 3. ü Эффективным способом увеличения степени превращения в обратимой реакции является удаление ее продукта.
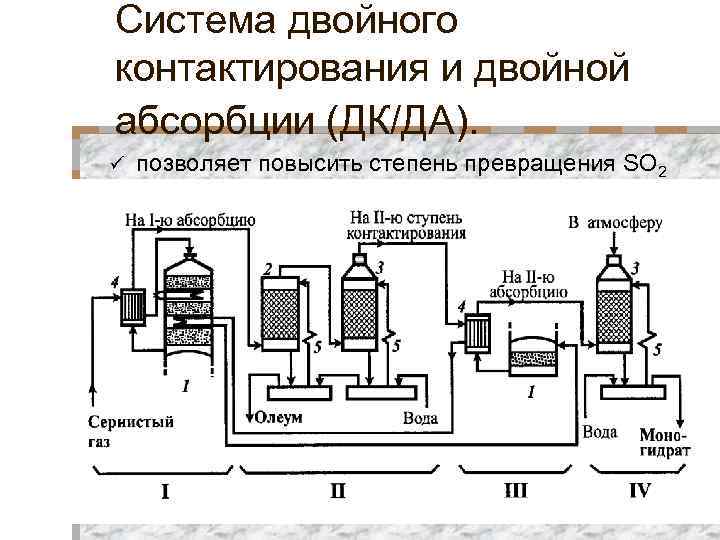
Система двойного контактирования и двойной абсорбции (ДК/ДА). ü позволяет повысить степень превращения SO 2 в SO 3
Производство серной кислоты.ppt