Никель.ppt
- Количество слайдов: 35
 Производство никеля Металлургические технологии Лекция 6
Производство никеля Металлургические технологии Лекция 6
 История открытия Никель впервые попавший в руки человека, – небесного происхождения: содержащее этот элемент прочное и стойкое к ржавлению метеоритное железо шло не только на талисманы, но и на оружие. Уже с 17 в. рудокопам Саксонии (Германия) была известна руда, которая по внешнему виду напоминала медные руды, но меди при выплавке не давала. Ее называли купферникель (нем. Kupfer — медь, а Nickel — имя гнома). Как оказалось впоследствии, купферникель — соединения никеля и мышьяка - Ni. As.
История открытия Никель впервые попавший в руки человека, – небесного происхождения: содержащее этот элемент прочное и стойкое к ржавлению метеоритное железо шло не только на талисманы, но и на оружие. Уже с 17 в. рудокопам Саксонии (Германия) была известна руда, которая по внешнему виду напоминала медные руды, но меди при выплавке не давала. Ее называли купферникель (нем. Kupfer — медь, а Nickel — имя гнома). Как оказалось впоследствии, купферникель — соединения никеля и мышьяка - Ni. As.
 Первым вывод о присутствии в купферникеле нового металла сделал шведский металлург А. Ф. Кронстедт в 1751 г. В 1775 г. , через 10 лет после смерти Кронстедта, швед Т. Бергман выполнил исследования, позволявшие заключить, что никель — это простое вещество. Окончательно никель как элемент утвердился в начале 19 -го века, в 1804 году, после скрупулезных исследований немецкого химика И. Рихтера, который для очистки провел 32 перекристаллизации никелевого купороса (сульфата никеля) и в результате восстановления получил чистый металл.
Первым вывод о присутствии в купферникеле нового металла сделал шведский металлург А. Ф. Кронстедт в 1751 г. В 1775 г. , через 10 лет после смерти Кронстедта, швед Т. Бергман выполнил исследования, позволявшие заключить, что никель — это простое вещество. Окончательно никель как элемент утвердился в начале 19 -го века, в 1804 году, после скрупулезных исследований немецкого химика И. Рихтера, который для очистки провел 32 перекристаллизации никелевого купороса (сульфата никеля) и в результате восстановления получил чистый металл.
 Физические свойства Металлический никель имеет серебристый цвет с желтоватым оттенком, - очень тверд, - вязкий и ковкий, - хорошо полируется, - проявляет магнитные свойства при температурах ниже 340° C. Не разрушается при сильных нагрузках и вибрации. Ø Тпл=1455 о С Ткип=2900 о С
Физические свойства Металлический никель имеет серебристый цвет с желтоватым оттенком, - очень тверд, - вязкий и ковкий, - хорошо полируется, - проявляет магнитные свойства при температурах ниже 340° C. Не разрушается при сильных нагрузках и вибрации. Ø Тпл=1455 о С Ткип=2900 о С
 Химические свойства Высокая коррозионная стойкость — устойчив на воздухе, в воде, в щелочах, в ряде кислот. Склонен к пассивированию — образованию на его поверхности плотной оксидной пленки. Активно растворяется в азотной кислоте. Степень окисления +2 и +3. Наиболее устойчивы соединения +2 (большое количество обычных и комплексных соединений). Ni 2 O 3 - сильный окислитель. С CO никель легко образует летучий и весьма ядовитый карбонил Ni(CO)4.
Химические свойства Высокая коррозионная стойкость — устойчив на воздухе, в воде, в щелочах, в ряде кислот. Склонен к пассивированию — образованию на его поверхности плотной оксидной пленки. Активно растворяется в азотной кислоте. Степень окисления +2 и +3. Наиболее устойчивы соединения +2 (большое количество обычных и комплексных соединений). Ni 2 O 3 - сильный окислитель. С CO никель легко образует летучий и весьма ядовитый карбонил Ni(CO)4.
 Тонкодисперсный порошок никеля пирофорный самовоспламеняется на воздухе. Образует оксиды (Ni. O, Ni 2 О 3 ) и гидроксиды (Ni(OH)2 , Ni(OH)3 ). Важнейшие растворимые соли – ацетат, хлорид, нитрат и сульфат. Растворы окрашены обычно в зеленый цвет, а безводные соли – желтые или коричнево-желтые. Нерастворимые соли – оксалат и фосфат (зеленые), сульфиды: Ni. S (черный), Ni 2 S 3 (желтовато-бронзовый) и Ni 3 S 4 (черный). Никель образует координационные и комплексные соединения. Например, диметилглиоксимат никеля Ni(HC 4 H 6 N 2 O 2)2, дающий четкую красную окраску в кислой среде, используется в качественном анализе на никель.
Тонкодисперсный порошок никеля пирофорный самовоспламеняется на воздухе. Образует оксиды (Ni. O, Ni 2 О 3 ) и гидроксиды (Ni(OH)2 , Ni(OH)3 ). Важнейшие растворимые соли – ацетат, хлорид, нитрат и сульфат. Растворы окрашены обычно в зеленый цвет, а безводные соли – желтые или коричнево-желтые. Нерастворимые соли – оксалат и фосфат (зеленые), сульфиды: Ni. S (черный), Ni 2 S 3 (желтовато-бронзовый) и Ni 3 S 4 (черный). Никель образует координационные и комплексные соединения. Например, диметилглиоксимат никеля Ni(HC 4 H 6 N 2 O 2)2, дающий четкую красную окраску в кислой среде, используется в качественном анализе на никель.
 Физиологические свойства Ni - основная причина аллергии (контактного дерматина) на металлы, контактирующие с кожей (украшения, часы, джинсовые заклепки). Пыль, пары никеля и его соединений токсичны. Cпособен накапливаться в роговице, что может привести к значительному ухудшению зрения. Никель — канцерогенное вещество. ПДК [Ni (CO)4] в воздухе производственных помещений 0, 0005 мг/м 3.
Физиологические свойства Ni - основная причина аллергии (контактного дерматина) на металлы, контактирующие с кожей (украшения, часы, джинсовые заклепки). Пыль, пары никеля и его соединений токсичны. Cпособен накапливаться в роговице, что может привести к значительному ухудшению зрения. Никель — канцерогенное вещество. ПДК [Ni (CO)4] в воздухе производственных помещений 0, 0005 мг/м 3.
 Установлено, что поджелудочная железа очень богата никелем. При введении вслед за инсулином продлевает действие инсулина и тем самым повышается гипогликемическая активность. Ni оказывает влияние на ферментативные процессы. Ni может угнетать действие адреналина и снижать артериальное давления. Избыточное поступление в организм вызывает витилиго (лат. vitilus — теленок) - нарушение пигментации, выражающееся в исчезновении пигмента меланина на отдельных участках кожи. Причины возникновения витилиго неизвестны, предполагают, что имеют значение нервно эндокринные расстройства.
Установлено, что поджелудочная железа очень богата никелем. При введении вслед за инсулином продлевает действие инсулина и тем самым повышается гипогликемическая активность. Ni оказывает влияние на ферментативные процессы. Ni может угнетать действие адреналина и снижать артериальное давления. Избыточное поступление в организм вызывает витилиго (лат. vitilus — теленок) - нарушение пигментации, выражающееся в исчезновении пигмента меланина на отдельных участках кожи. Причины возникновения витилиго неизвестны, предполагают, что имеют значение нервно эндокринные расстройства.
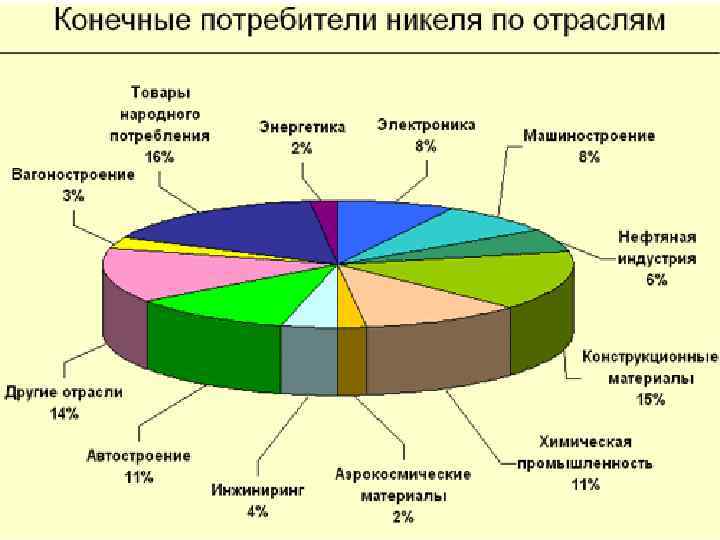
 Применение Основная доля выплавляемого Ni (до 80%) расходуется на приготовление сплавов. Добавление Ni в стали повышает химическую стойкость. Сплавы характеризуются высокой вязкостью и используются при изготовлении прочной брони. Сплав железа и никеля (инвар), содержащий 36 -38% Ni, обладает низким коэффициентом термического расширения, его применяют при изготовлении ответственных деталей различных приборов.
Применение Основная доля выплавляемого Ni (до 80%) расходуется на приготовление сплавов. Добавление Ni в стали повышает химическую стойкость. Сплавы характеризуются высокой вязкостью и используются при изготовлении прочной брони. Сплав железа и никеля (инвар), содержащий 36 -38% Ni, обладает низким коэффициентом термического расширения, его применяют при изготовлении ответственных деталей различных приборов.
 При изготовлении сердечников электромагнитов широкое применение находят сплавы под общим названием пермаллои (Fe - 40÷ 80 % Ni). Общеизвестны применяемые в различных нагревателях нихромовые спирали (Ni - 10 ÷ 30 % Cr). Общее число различных сплавов Ni достигает нескольких тысяч. Высокая коррозионная стойкость никелевых покрытий позволяет использовать тонкие никелевые слои для защиты различных металлов от коррозии путем их никелирования. Никелирование придает изделиям красивый внешний вид. В этом случае для проведения электролиза используют водный раствор двойного сульфата аммония и никеля (NH 4)2 Ni(SO 4)2.
При изготовлении сердечников электромагнитов широкое применение находят сплавы под общим названием пермаллои (Fe - 40÷ 80 % Ni). Общеизвестны применяемые в различных нагревателях нихромовые спирали (Ni - 10 ÷ 30 % Cr). Общее число различных сплавов Ni достигает нескольких тысяч. Высокая коррозионная стойкость никелевых покрытий позволяет использовать тонкие никелевые слои для защиты различных металлов от коррозии путем их никелирования. Никелирование придает изделиям красивый внешний вид. В этом случае для проведения электролиза используют водный раствор двойного сульфата аммония и никеля (NH 4)2 Ni(SO 4)2.
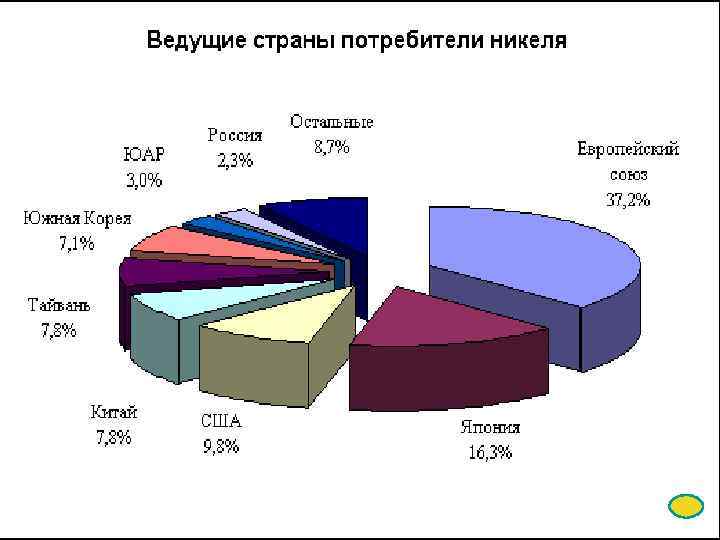
 В России добычу и переработку руд Ni осуществляют: Ø «Норильская горно-рудная компания» , Ø «Кольская горно-металлургическая компания» (оба предприятия входят в состав РАО «Норильский никель» ), Ø «Уфалейникель» Ø «Южуралникель» . Крупнейшее – РАО «Норильский никель» , в составе которого рудники Норильского ГМК и комбинат «Печенганикель» , разрабатывающие сульфидные медно-никелевые руды месторождений Норильского района и Кольского полуострова. На долю этих руд приходится 92— 93% общероссийской добычи никеля и кобальта.
В России добычу и переработку руд Ni осуществляют: Ø «Норильская горно-рудная компания» , Ø «Кольская горно-металлургическая компания» (оба предприятия входят в состав РАО «Норильский никель» ), Ø «Уфалейникель» Ø «Южуралникель» . Крупнейшее – РАО «Норильский никель» , в составе которого рудники Норильского ГМК и комбинат «Печенганикель» , разрабатывающие сульфидные медно-никелевые руды месторождений Норильского района и Кольского полуострова. На долю этих руд приходится 92— 93% общероссийской добычи никеля и кобальта.

 Нахождение в природе Запасы никеля — около 17· 1019 т — заключены в ядре Земли, которое по одной из гипотез состоит из железоникелевого сплава. Земля примерно на 3 % состоит из Ni, а среди составляющих планету элементов Ni занимает пятое место Кларк 8· 10– 3 %.
Нахождение в природе Запасы никеля — около 17· 1019 т — заключены в ядре Земли, которое по одной из гипотез состоит из железоникелевого сплава. Земля примерно на 3 % состоит из Ni, а среди составляющих планету элементов Ni занимает пятое место Кларк 8· 10– 3 %.
 Важнейшие минералы: никелин (купферникель) Ni. As пентландит (Fe, Ni)9 S 8 миллерит Ni. S гарниерит (Ni, Mg)6 Si 4 O 10(OH)2 бунзеит Ni. O Никелевые руды: - сульфидные - окисленные В морской воде содержание никеля 1· 10– 8– 5· 10– 8 %.
Важнейшие минералы: никелин (купферникель) Ni. As пентландит (Fe, Ni)9 S 8 миллерит Ni. S гарниерит (Ni, Mg)6 Si 4 O 10(OH)2 бунзеит Ni. O Никелевые руды: - сульфидные - окисленные В морской воде содержание никеля 1· 10– 8– 5· 10– 8 %.
 Общие запасы никеля в рудах на начало 2010 г. оцениваются в количестве 145 млн. т. , в том числе достоверные — 59 млн. т. Основные руды содержат: Co, Cu, Fe, S, Cd, As, Au, Ag, Re, Pt, Hg, Bi, Zn, Mo, Al, Cr, Mg, Si, Ca, Pb, Sn и другие (до 30) химические элементы.
Общие запасы никеля в рудах на начало 2010 г. оцениваются в количестве 145 млн. т. , в том числе достоверные — 59 млн. т. Основные руды содержат: Co, Cu, Fe, S, Cd, As, Au, Ag, Re, Pt, Hg, Bi, Zn, Mo, Al, Cr, Mg, Si, Ca, Pb, Sn и другие (до 30) химические элементы.
 От 40 до 66 % Ni находится в окисленных рудах (ОНР), 33 % —в сульфидных, 0, 7 % —в прочих. По состоянию на 2008 г. доля Ni, произведённого переработкой ОНР, составила порядка 40 % от общемирового объёма производства.
От 40 до 66 % Ni находится в окисленных рудах (ОНР), 33 % —в сульфидных, 0, 7 % —в прочих. По состоянию на 2008 г. доля Ni, произведённого переработкой ОНР, составила порядка 40 % от общемирового объёма производства.
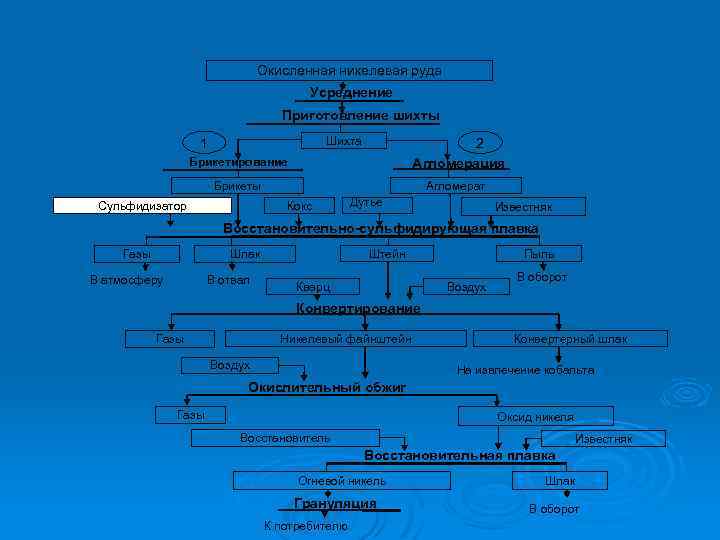 Окисленная никелевая руда Усреднение Приготовление шихты Шихта 1 Брикетирование 2 Агломерация Брикеты Агломерат Сульфидизатор Кокс Дутье Известняк Восстановительно-сульфидирующая плавка Газы В атмосферу В отвал Пыль Штейн Шлак Кварц Воздух В оборот Конвертирование Никелевый файнштейн Газы Воздух Конвертерный шлак На извлечение кобальта Окислительный обжиг Газы Оксид никеля Восстановитель Известняк Восстановительная плавка Огневой никель Грануляция К потребителю Шлак В оборот
Окисленная никелевая руда Усреднение Приготовление шихты Шихта 1 Брикетирование 2 Агломерация Брикеты Агломерат Сульфидизатор Кокс Дутье Известняк Восстановительно-сульфидирующая плавка Газы В атмосферу В отвал Пыль Штейн Шлак Кварц Воздух В оборот Конвертирование Никелевый файнштейн Газы Воздух Конвертерный шлак На извлечение кобальта Окислительный обжиг Газы Оксид никеля Восстановитель Известняк Восстановительная плавка Огневой никель Грануляция К потребителю Шлак В оборот
 Особенности переработки ОНР Предварительная подготовка (брикетирование, агломерация) Ø Плавка на штейн (сульфидизатор) Ø Конвертирование (полный перевод Fe и maximum Со в шлак) Ø Переработка шлака на Со Ø Многостадийность переработки файнштейна Ø Потеря до 15% Со с товарным Ni Ø Н-4 (Ni≥ 98%) , Н-3 (Ni≥ 98, 6%, Cu≤ 0, 6%) Ø
Особенности переработки ОНР Предварительная подготовка (брикетирование, агломерация) Ø Плавка на штейн (сульфидизатор) Ø Конвертирование (полный перевод Fe и maximum Со в шлак) Ø Переработка шлака на Со Ø Многостадийность переработки файнштейна Ø Потеря до 15% Со с товарным Ni Ø Н-4 (Ni≥ 98%) , Н-3 (Ni≥ 98, 6%, Cu≤ 0, 6%) Ø
 В промышленных условиях ОНР делят на два типа. l l Тугоплавкие магнезиальные руды подвергают электроплавке на ферроникель (5 -50 % Ni+Co, в зависимости от состава сырья и технологических особенностей). Латеритовые руды перерабатывают гидрометаллургическими методами с применением аммиачно-карбонатного выщелачивания или сернокислотного автоклавного выщелачивания.
В промышленных условиях ОНР делят на два типа. l l Тугоплавкие магнезиальные руды подвергают электроплавке на ферроникель (5 -50 % Ni+Co, в зависимости от состава сырья и технологических особенностей). Латеритовые руды перерабатывают гидрометаллургическими методами с применением аммиачно-карбонатного выщелачивания или сернокислотного автоклавного выщелачивания.
 Особенность переработки окисленных никелевых руд Ø Окисленные никелевые руды (ОНР), в отличие от сульфидного сырья, не имеют в своем составе горючих составляющих и характеризуются низким содержанием никеля (около 1%) и высокой влажностью. Эти обстоятельства определяют технологические и конструктивные особенности печи Ванюкова.
Особенность переработки окисленных никелевых руд Ø Окисленные никелевые руды (ОНР), в отличие от сульфидного сырья, не имеют в своем составе горючих составляющих и характеризуются низким содержанием никеля (около 1%) и высокой влажностью. Эти обстоятельства определяют технологические и конструктивные особенности печи Ванюкова.
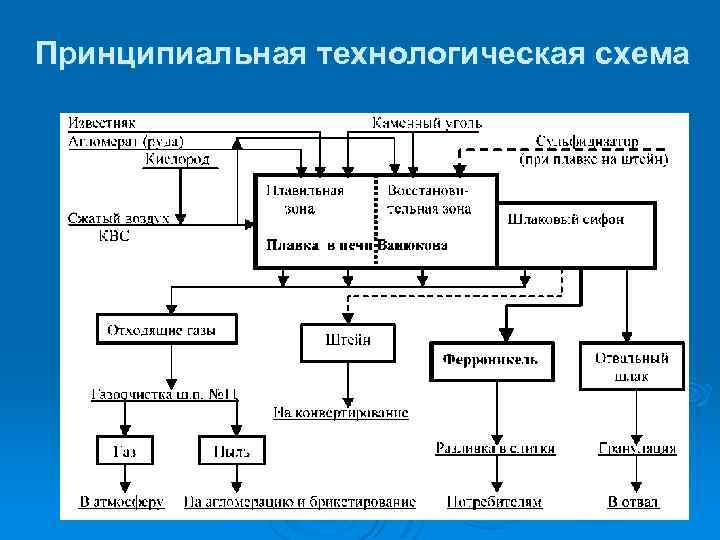 Принципиальная технологическая схема
Принципиальная технологическая схема
 Руда, уголь и флюсы из расходных бункеров, оборудованных ленточными весовыми дозаторами, непрерывно ленточными конвейерами подаются в ванну расплава плавильной камеры печи.
Руда, уголь и флюсы из расходных бункеров, оборудованных ленточными весовыми дозаторами, непрерывно ленточными конвейерами подаются в ванну расплава плавильной камеры печи.
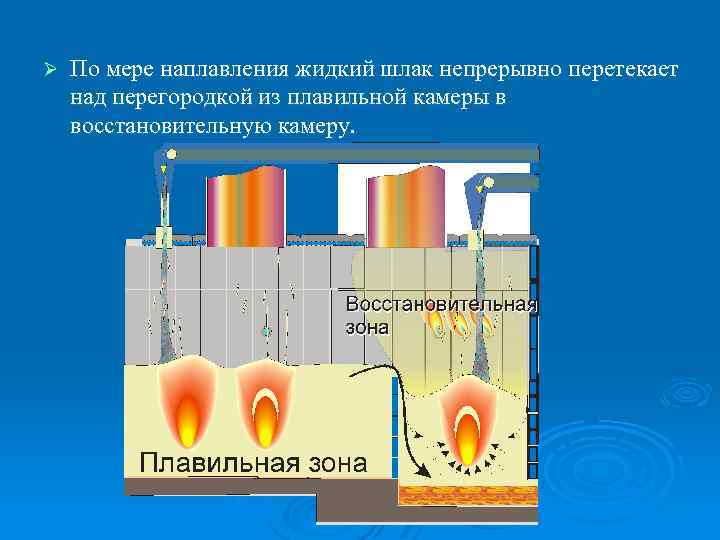 Ø По мере наплавления жидкий шлак непрерывно перетекает над перегородкой из плавильной камеры в восстановительную камеру.
Ø По мере наплавления жидкий шлак непрерывно перетекает над перегородкой из плавильной камеры в восстановительную камеру.
 Процесс жидкофазного восстановления Восстановление оксидов осуществляется при температуре расплава 1300 -1650°С. Для создания восстановительных условий в расплав подается уголь и кислородновоздушное дутье. При этом протекают следующие реакции: Ø 2 С + O 2 2 CO + Q Ø Fe 3 O 4 + C 3 Fe. O + CO - Q Ø Ni. O + C Ni + CO - Q Ø Co. O + C Co + CO - Q Ø Fe. O + C Fe + CO - Q Кроме того, восстановителем может служить и часть СО газовой фазы: Ø Fe. O + CO Fe + CO 2 - Q Ø Ni. O + CO Ni + CO 2 - Q Ø Co. O + CO Co + CO 2 - Q В результате образуются капли металла, которые, укрупняясь, осаждаются и формируют донную фазу - ферроникель.
Процесс жидкофазного восстановления Восстановление оксидов осуществляется при температуре расплава 1300 -1650°С. Для создания восстановительных условий в расплав подается уголь и кислородновоздушное дутье. При этом протекают следующие реакции: Ø 2 С + O 2 2 CO + Q Ø Fe 3 O 4 + C 3 Fe. O + CO - Q Ø Ni. O + C Ni + CO - Q Ø Co. O + C Co + CO - Q Ø Fe. O + C Fe + CO - Q Кроме того, восстановителем может служить и часть СО газовой фазы: Ø Fe. O + CO Fe + CO 2 - Q Ø Ni. O + CO Ni + CO 2 - Q Ø Co. O + CO Co + CO 2 - Q В результате образуются капли металла, которые, укрупняясь, осаждаются и формируют донную фазу - ферроникель.
 Ø Восстановительная камера для поддержания температурного баланса и перемешивания расплава также оборудована фурмами бокового дутья. Ø Шлаковый расплав с капельками металла перетекает в сифон, где под действием силы тяжести происходит естественное расслоение по плотности металла и шлака.
Ø Восстановительная камера для поддержания температурного баланса и перемешивания расплава также оборудована фурмами бокового дутья. Ø Шлаковый расплав с капельками металла перетекает в сифон, где под действием силы тяжести происходит естественное расслоение по плотности металла и шлака.
 Шлак, как более легкий компонент, непрерывно выпускается через шлаковую летку на грануляцию
Шлак, как более легкий компонент, непрерывно выпускается через шлаковую летку на грануляцию
 металл, по мере накопления, периодически сливается в ковш
металл, по мере накопления, периодически сливается в ковш
 и затем, ковшом разливается в изложницы.
и затем, ковшом разливается в изложницы.
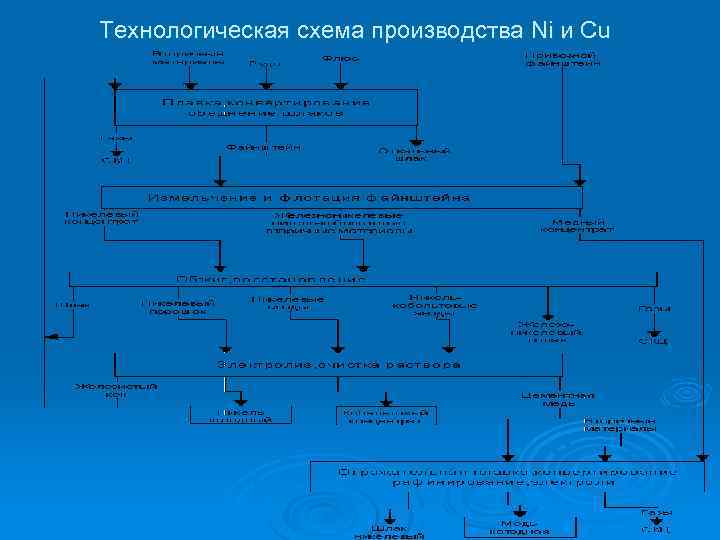 Технологическая схема производства Ni и Cu
Технологическая схема производства Ni и Cu
 Особенности переработки сульфидных никелевых руд (СНР) Ø Предварительная подготовка (обогащение, обжиг) Ø Плавка концентрата на штейн Ø Конвертирование (неполный перевод Fe из штейна в шлак, maximum концентрирование Со в файнштейне)
Особенности переработки сульфидных никелевых руд (СНР) Ø Предварительная подготовка (обогащение, обжиг) Ø Плавка концентрата на штейн Ø Конвертирование (неполный перевод Fe из штейна в шлак, maximum концентрирование Со в файнштейне)
 Особенности переработки СНР Разделение меди и никеля в файнштейне - флотацией (конц. Ni с благородными Ме, конц. Сu) - карбонильным способом Ø Ø Переработка Ni концентрата на черновой Ni (обжиг и восстановительная анодная плавка) Черновой никель: Ni – 88 -89% Fe – 2 -4% Ø Co – 1 -2% S – до 2, 5 % Cu – 4 -6%
Особенности переработки СНР Разделение меди и никеля в файнштейне - флотацией (конц. Ni с благородными Ме, конц. Сu) - карбонильным способом Ø Ø Переработка Ni концентрата на черновой Ni (обжиг и восстановительная анодная плавка) Черновой никель: Ni – 88 -89% Fe – 2 -4% Ø Co – 1 -2% S – до 2, 5 % Cu – 4 -6%
 Особенности переработки СНР Электролитическое рафинирования Т= 70 -75 о С i = 260 -360 А/м 2 U =2, 5 B Ŋ= 96 % Wуд =3300 к. Вт • час/т Ni Ø Ø Н-1, Н-0, НОЧ (99, 93 – 99, 99%)
Особенности переработки СНР Электролитическое рафинирования Т= 70 -75 о С i = 260 -360 А/м 2 U =2, 5 B Ŋ= 96 % Wуд =3300 к. Вт • час/т Ni Ø Ø Н-1, Н-0, НОЧ (99, 93 – 99, 99%)
 Товарная продукция
Товарная продукция


