Производство лекарственных средств — серийное


































Предмет ОРГАНИЗАЦИЯ.ppt
- Количество слайдов: 40
 Производство лекарственных средств - серийное получение лекарственных средств предприятиями - изготовителями, имеющими лицензии на производство лекарственных средств, в соответствии с правилами организации производства и контроля качества лекарственных средств, утвержденными федеральным органом контроля качества лекарственных средств. СЕРИЯ - определенное количество лекарственного средства, полученного в результате одного технологического цикла. Основным требованием к серии является ее однородность. ПРОИЗВОДСТВО – все операции по производству конечной продукции, начиная от приобретения сырья, вспомогательных, упаковочных и маркировочных материалов, получения полупродуктов, до изготовления и упаковки, включая валидацию и обеспечение качества готового продукта, выдачи разрешения на реализацию, а также хранение, собственно реализацию и транспортирование готовой продукции (ОСТ 64 -02 -003 -2002) Валидация (Validation) - документированная процедура, дающая высокую степень уверенности в том, что конкретный процесс, метод или система будет последовательно приводить к результатам, отвечающим заранее установленным критериям приемлемости.
Производство лекарственных средств - серийное получение лекарственных средств предприятиями - изготовителями, имеющими лицензии на производство лекарственных средств, в соответствии с правилами организации производства и контроля качества лекарственных средств, утвержденными федеральным органом контроля качества лекарственных средств. СЕРИЯ - определенное количество лекарственного средства, полученного в результате одного технологического цикла. Основным требованием к серии является ее однородность. ПРОИЗВОДСТВО – все операции по производству конечной продукции, начиная от приобретения сырья, вспомогательных, упаковочных и маркировочных материалов, получения полупродуктов, до изготовления и упаковки, включая валидацию и обеспечение качества готового продукта, выдачи разрешения на реализацию, а также хранение, собственно реализацию и транспортирование готовой продукции (ОСТ 64 -02 -003 -2002) Валидация (Validation) - документированная процедура, дающая высокую степень уверенности в том, что конкретный процесс, метод или система будет последовательно приводить к результатам, отвечающим заранее установленным критериям приемлемости.
 Характерные признаки производства ЛС массовость, ограниченная номенклатура и узкая специализация; стабильность лекарственных препаратов и длительный срок хранения; жесткая регламентация; высокая степень механизации технологических процессов. Фармацевтические заводы Фармацевтические фабрики сравнительно малые объемы; простые лекарственные формы; отдельные этапы производства (фасовка)
Характерные признаки производства ЛС массовость, ограниченная номенклатура и узкая специализация; стабильность лекарственных препаратов и длительный срок хранения; жесткая регламентация; высокая степень механизации технологических процессов. Фармацевтические заводы Фармацевтические фабрики сравнительно малые объемы; простые лекарственные формы; отдельные этапы производства (фасовка)
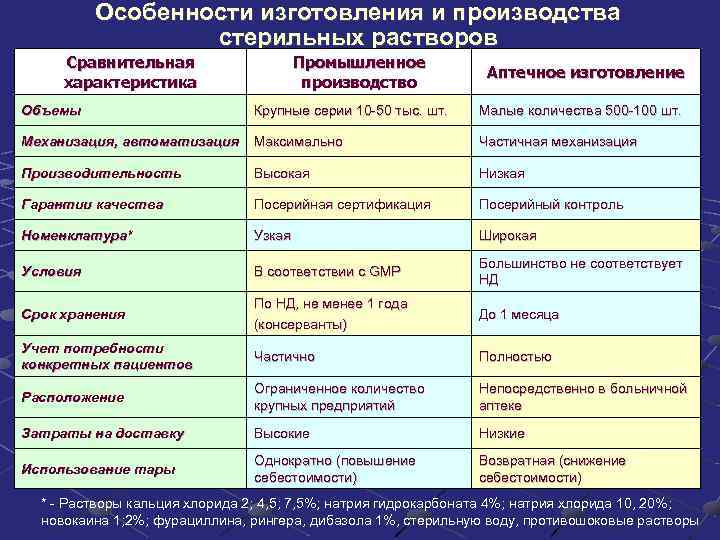
 Особенности изготовления и производства стерильных растворов Сравнительная Промышленное Аптечное изготовление характеристика производство Объемы Крупные серии 10 -50 тыс. шт. Малые количества 500 -100 шт. Механизация, автоматизация Максимально Частичная механизация Производительность Высокая Низкая Гарантии качества Посерийная сертификация Посерийный контроль Номенклатура* Узкая Широкая Большинство не соответствует Условия В соответствии с GMP НД По НД, не менее 1 года Срок хранения До 1 месяца (консерванты) Учет потребности Частично Полностью конкретных пациентов Ограниченное количество Непосредственно в больничной Расположение крупных предприятий аптеке Затраты на доставку Высокие Низкие Однократно (повышение Возвратная (снижение Использование тары себестоимости) * - Растворы кальция хлорида 2; 4, 5; 7, 5%; натрия гидрокарбоната 4%; натрия хлорида 10, 20%; новокаина 1; 2%; фурациллина, рингера, дибазола 1%, стерильную воду, противошоковые растворы
Особенности изготовления и производства стерильных растворов Сравнительная Промышленное Аптечное изготовление характеристика производство Объемы Крупные серии 10 -50 тыс. шт. Малые количества 500 -100 шт. Механизация, автоматизация Максимально Частичная механизация Производительность Высокая Низкая Гарантии качества Посерийная сертификация Посерийный контроль Номенклатура* Узкая Широкая Большинство не соответствует Условия В соответствии с GMP НД По НД, не менее 1 года Срок хранения До 1 месяца (консерванты) Учет потребности Частично Полностью конкретных пациентов Ограниченное количество Непосредственно в больничной Расположение крупных предприятий аптеке Затраты на доставку Высокие Низкие Однократно (повышение Возвратная (снижение Использование тары себестоимости) * - Растворы кальция хлорида 2; 4, 5; 7, 5%; натрия гидрокарбоната 4%; натрия хлорида 10, 20%; новокаина 1; 2%; фурациллина, рингера, дибазола 1%, стерильную воду, противошоковые растворы
 Федеральный закон РФ № 86 О ЛЕКАРСТВЕННЫХ СРЕДСТВАХ» Глава IX Разработка, доклинические исследования лек. средств Глава IV Производство и изготовление лекарственных средств Глава VII Оптовая торговля лекарственными средствами Глава VIII Розничная торговля лекарственными средствами Федеральный закон РФ № 184 О ТЕХНИЧЕСКОМ РЕГУЛИРОВАНИИ» Принят Государственной Думой 5 декабря 2002 года Одобрен Советом Федерации 18 декабря 2002 года регулирует отношения, возникающие при: разработке, принятии, применении и исполнении обязательных требований к продукции, процессам производства, эксплуатации, хранения, перевозки, реализации и утилизации; разработке, принятии, применении и исполнении на добровольной основе требований к продукции, процессам производства, эксплуатации, хранении, реализации и утилизации, выполнению работ или оказанию услуг; оценке соответствия.
Федеральный закон РФ № 86 О ЛЕКАРСТВЕННЫХ СРЕДСТВАХ» Глава IX Разработка, доклинические исследования лек. средств Глава IV Производство и изготовление лекарственных средств Глава VII Оптовая торговля лекарственными средствами Глава VIII Розничная торговля лекарственными средствами Федеральный закон РФ № 184 О ТЕХНИЧЕСКОМ РЕГУЛИРОВАНИИ» Принят Государственной Думой 5 декабря 2002 года Одобрен Советом Федерации 18 декабря 2002 года регулирует отношения, возникающие при: разработке, принятии, применении и исполнении обязательных требований к продукции, процессам производства, эксплуатации, хранения, перевозки, реализации и утилизации; разработке, принятии, применении и исполнении на добровольной основе требований к продукции, процессам производства, эксплуатации, хранении, реализации и утилизации, выполнению работ или оказанию услуг; оценке соответствия.
 Техническое регулирование - правовое регулирование отношений в области установления, применения и исполнения обязательных требований к продукции, процессам производства, эксплуатации, хранения, перевозки, реализации и утилизации, а также в области установления и применения на добровольной основе требований к продукции, процессам производства, эксплуатации, хранения, перевозки, реализации и утилизации, выполнению работ или оказанию услуг и правовое регулирование отношений в области оценки соответствия; технический регламент - документ, который принят международным договором Российской Федерации, ратифицированным в порядке, установленном законодательством Российской Федерации, или федеральным законом, или указом Президента Российской Федерации, или постановлением Правительства Российской Федерации, и устанавливает обязательные для применения и исполнения требования к объектам технического регулирования (продукции, в том числе зданиям, строениям и сооружениям, процессам производства, эксплуатации, хранения, перевозки, реализации и утилизации).
Техническое регулирование - правовое регулирование отношений в области установления, применения и исполнения обязательных требований к продукции, процессам производства, эксплуатации, хранения, перевозки, реализации и утилизации, а также в области установления и применения на добровольной основе требований к продукции, процессам производства, эксплуатации, хранения, перевозки, реализации и утилизации, выполнению работ или оказанию услуг и правовое регулирование отношений в области оценки соответствия; технический регламент - документ, который принят международным договором Российской Федерации, ратифицированным в порядке, установленном законодательством Российской Федерации, или федеральным законом, или указом Президента Российской Федерации, или постановлением Правительства Российской Федерации, и устанавливает обязательные для применения и исполнения требования к объектам технического регулирования (продукции, в том числе зданиям, строениям и сооружениям, процессам производства, эксплуатации, хранения, перевозки, реализации и утилизации).
 Лицензионными требованиями и условиями при осуществлении производства лекарственных средств являются Государственная регистрация в Российской Федерации в установленном порядке лекарственных средств, заявленных соискателем лицензии для производства; Соблюдение правил организации производства и контроля качества лекарственных средств (GMP), утвержденных в установленном порядке; Соответствие производственных помещений оборудования техническим нормам и требованиям; Наличие у соискателя лицензии и лицензиата принадлежащих им на праве собственности или на ином законном основании зданий, помещений и оборудования, необходимых для осуществления лицензируемой деятельности; Наличие в штате юридического лица работников, ответственных за производство, качество и маркировку ЛС, имеющих высшее или среднее специальное образование (химико-технологичекое, биотехнологическое, фармацевтическое или медицинское) и стаж работы по специальности не менее 3 лет; Повышение не реже 1 раза в 5 лет квалификации специалистов, отвечающих за производство, качество и маркировку лекарственных средств; Соблюдение требований Федерального закона «О лекарственных средствах» к продаже произведенных лицензиатом лекарственных средств. Постановление Правительства РФ от 04. 07. 02 № 500
Лицензионными требованиями и условиями при осуществлении производства лекарственных средств являются Государственная регистрация в Российской Федерации в установленном порядке лекарственных средств, заявленных соискателем лицензии для производства; Соблюдение правил организации производства и контроля качества лекарственных средств (GMP), утвержденных в установленном порядке; Соответствие производственных помещений оборудования техническим нормам и требованиям; Наличие у соискателя лицензии и лицензиата принадлежащих им на праве собственности или на ином законном основании зданий, помещений и оборудования, необходимых для осуществления лицензируемой деятельности; Наличие в штате юридического лица работников, ответственных за производство, качество и маркировку ЛС, имеющих высшее или среднее специальное образование (химико-технологичекое, биотехнологическое, фармацевтическое или медицинское) и стаж работы по специальности не менее 3 лет; Повышение не реже 1 раза в 5 лет квалификации специалистов, отвечающих за производство, качество и маркировку лекарственных средств; Соблюдение требований Федерального закона «О лекарственных средствах» к продаже произведенных лицензиатом лекарственных средств. Постановление Правительства РФ от 04. 07. 02 № 500
 "Good Manufacturing Practice for Medicinal Products “ - Правила производства лекарственных средств Национальный стандарт Российской Федерации ГОСТ Р 52249 -2004 система требований к производству и контролю качества лекарственных средств для человека и животных
"Good Manufacturing Practice for Medicinal Products “ - Правила производства лекарственных средств Национальный стандарт Российской Федерации ГОСТ Р 52249 -2004 система требований к производству и контролю качества лекарственных средств для человека и животных
 Основополагающие принципы GMP Четкая регламентация всех производственных процессов, периодически пересматриваемых с учетом приобретенного опыта; Валидация производства; Наличие квалифицированного персонала; Разработка четких и однозначных технологических регламентов и инструкций; Обучение персонала надлежащему выполнению технологических операций; Регистрация всех этапов производства и отклонений; Надлежащее хранение, регистрация готового продукта
Основополагающие принципы GMP Четкая регламентация всех производственных процессов, периодически пересматриваемых с учетом приобретенного опыта; Валидация производства; Наличие квалифицированного персонала; Разработка четких и однозначных технологических регламентов и инструкций; Обучение персонала надлежащему выполнению технологических операций; Регистрация всех этапов производства и отклонений; Надлежащее хранение, регистрация готового продукта
 ГОСТ Р 52249 -2004 Национальный стандарт Р Ф «Правила производства и контроля качества лекарственных средств» Good Manufacturing Practice For Medicinal Products (GMP) Принципы. Обеспечение качества. Требования к производству 1. УПРАВЛЕНИЕ КАЧЕСТВОМ и контролю качества ЛС. Основные требования. Контроль качества. Основные требования к контролю качества Принципы. Общие положения. Руководящие работники. Обязанности 2. ПЕРСОНАЛ Уполномоченных лиц, Обязанности руководителя производства. Обязанности руководителя службы контроля качества. Обучение. Гигиена персонала Принцип. Помещения. Производственная зона. Зоны 3. ПОМЕЩЕНИЯ И ОБОРУДОВАНИЕ складирования. Зоны контроля качества Вспомогательные зоны. Оборудование Принципы. Общие положения. Обязательная документация. Спецификации на исходные и упаковочные материалы, на промежуточную и 4. ДОКУМЕНТАЦИЯ нерасфасованную продукцию, на готовую продукцию. Промышленный регламент и технологические инструкции. Инструкции по упаковке. Протоколы на серию продукции, на упаковку серии продукции. Приемка. Отбор проб. Проведение испытаний. Прочее. перекрестного загрязнения Принципы. Общие положения Предотвращение 5. ПРОИЗВОДСТВО при производстве. Аттестация (валидация). Исходные материалы. Промежуточная и нерасфасованная продукция. Упаковочные материалы. Операции по упаковке. Готовая продукция. Отклоненные, повторно использованные и возвращенные материалы 6. КОНТРОЛЬ КАЧЕСТВА Принципы. Общие положения. Организация работы контрольных лабораторий. Документация. Отбор проб. Проведение испытаний 7. РАБОТА ПО КОНТРАКТАМ Принципы. Общие положения. Заказчик. Исполнитель. Контракт 8. РЕКЛАМАЦИЯ И ОТЗЫВ ПРОДУКЦИИ Принципы. Рекламации. Отзыв продукции 9. САМОИНСПЕКЦИЯ Принципы.
ГОСТ Р 52249 -2004 Национальный стандарт Р Ф «Правила производства и контроля качества лекарственных средств» Good Manufacturing Practice For Medicinal Products (GMP) Принципы. Обеспечение качества. Требования к производству 1. УПРАВЛЕНИЕ КАЧЕСТВОМ и контролю качества ЛС. Основные требования. Контроль качества. Основные требования к контролю качества Принципы. Общие положения. Руководящие работники. Обязанности 2. ПЕРСОНАЛ Уполномоченных лиц, Обязанности руководителя производства. Обязанности руководителя службы контроля качества. Обучение. Гигиена персонала Принцип. Помещения. Производственная зона. Зоны 3. ПОМЕЩЕНИЯ И ОБОРУДОВАНИЕ складирования. Зоны контроля качества Вспомогательные зоны. Оборудование Принципы. Общие положения. Обязательная документация. Спецификации на исходные и упаковочные материалы, на промежуточную и 4. ДОКУМЕНТАЦИЯ нерасфасованную продукцию, на готовую продукцию. Промышленный регламент и технологические инструкции. Инструкции по упаковке. Протоколы на серию продукции, на упаковку серии продукции. Приемка. Отбор проб. Проведение испытаний. Прочее. перекрестного загрязнения Принципы. Общие положения Предотвращение 5. ПРОИЗВОДСТВО при производстве. Аттестация (валидация). Исходные материалы. Промежуточная и нерасфасованная продукция. Упаковочные материалы. Операции по упаковке. Готовая продукция. Отклоненные, повторно использованные и возвращенные материалы 6. КОНТРОЛЬ КАЧЕСТВА Принципы. Общие положения. Организация работы контрольных лабораторий. Документация. Отбор проб. Проведение испытаний 7. РАБОТА ПО КОНТРАКТАМ Принципы. Общие положения. Заказчик. Исполнитель. Контракт 8. РЕКЛАМАЦИЯ И ОТЗЫВ ПРОДУКЦИИ Принципы. Рекламации. Отзыв продукции 9. САМОИНСПЕКЦИЯ Принципы.
 ГОСТ Р 52249 -2004 Национальный стандарт Р Ф «Правила производства и контроля качества лекарственных средств» Good Manufacturing Practice For Medicinal Products (GMP) Специфические требования GMP (приложения): 1. ПРОИЗВОДСТВО СТЕРИЛЬНЫХ ЛЕКАРСТВЕННЫХ СРЕД 2. ПРОИЗВОДСТВО МЕДИЦИНСКИХ БИОЛОГИЧЕСКИХ ПРЕПАРАТОВ СТВ 3. ПРОИЗВОДСТВО РАДИОФАРМАЦЕВТИЧЕСКИХ ПРЕПАРАТОВ 4. ПРОИЗВОДСТВО ЛЕКАРСТВЕННЫХ СРЕДСТВ ДЛЯ ЖИВОТНЫХ (КРОМЕ ИММУННЫХ ПРЕПАРАТОВ) 5. ПРОИЗВОДСТВО ИММУННЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ ДЛЯ ЖИВОТНЫХ 6. ПРОИЗВОДСТВО МЕДИЦИНСКИХ ГАЗОВ 7. ПРОИЗВОДСТВО ЛЕКАРСТВЕННЫХ СРЕДСТВ ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ 8. ОТБОР ПРОБ ИСХОДНЫХ И УПАКОВОЧНЫХ МАТЕРИАЛОВ 9. ПРОИЗВОДСТВО ЖИДКОСТЕЙ, КРЕМОВ И МАЗЕЙ 10. ПРОИЗВОДСТВО АЭРОЗОЛЕЙ ДЛЯ ИНГАЛЯЦИЙ 11. СИСТЕМЫ С КОМПЬЮТЕРНЫМ УПРАВЛЕНИЕМ И КОНТРОЛЕМ 12. ИСПОЛЬЗОВАНИЕ ИОНИЗИРУЮЩЕГО ИЗЛУЧЕНИЯ В ПРОИЗВОДСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ 13. ПРОИЗВОДСТВО ЛЕКАРСТВЕННЫХ СРЕДСТВ ДЛЯ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ 14. ПРОИЗВОДСТВО ЛЕКАРСТВЕННЫХ СРЕДСТВ ИЗ КРОВИ ИЛИ ПЛАЗМЫ ЧЕЛОВЕКА 15. АТТЕСТАЦИЯ ПРОЦЕССОВ И ОБОРУДОВАНИЯ 16. ПОДТВЕРЖДЕНИЕ СООТВЕТСТВИЯ СЕРИИ ПРОДУКЦИИ С ЦЕЛЬЮ ЕЕ ВЫПУСКА, ВЫПОЛНЯЕМОЕ УПОЛНОМОЧЕННЫМ ЛИЦОМ 17. ВЫПУСК ПО ПАРАМЕТРАМ 18. РУКОВОДСТВО ПО ПРОИЗВОДСТВУ АКТИВНЫХ ФАРМАЦЕВТИЧЕСКИХ
ГОСТ Р 52249 -2004 Национальный стандарт Р Ф «Правила производства и контроля качества лекарственных средств» Good Manufacturing Practice For Medicinal Products (GMP) Специфические требования GMP (приложения): 1. ПРОИЗВОДСТВО СТЕРИЛЬНЫХ ЛЕКАРСТВЕННЫХ СРЕД 2. ПРОИЗВОДСТВО МЕДИЦИНСКИХ БИОЛОГИЧЕСКИХ ПРЕПАРАТОВ СТВ 3. ПРОИЗВОДСТВО РАДИОФАРМАЦЕВТИЧЕСКИХ ПРЕПАРАТОВ 4. ПРОИЗВОДСТВО ЛЕКАРСТВЕННЫХ СРЕДСТВ ДЛЯ ЖИВОТНЫХ (КРОМЕ ИММУННЫХ ПРЕПАРАТОВ) 5. ПРОИЗВОДСТВО ИММУННЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ ДЛЯ ЖИВОТНЫХ 6. ПРОИЗВОДСТВО МЕДИЦИНСКИХ ГАЗОВ 7. ПРОИЗВОДСТВО ЛЕКАРСТВЕННЫХ СРЕДСТВ ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ 8. ОТБОР ПРОБ ИСХОДНЫХ И УПАКОВОЧНЫХ МАТЕРИАЛОВ 9. ПРОИЗВОДСТВО ЖИДКОСТЕЙ, КРЕМОВ И МАЗЕЙ 10. ПРОИЗВОДСТВО АЭРОЗОЛЕЙ ДЛЯ ИНГАЛЯЦИЙ 11. СИСТЕМЫ С КОМПЬЮТЕРНЫМ УПРАВЛЕНИЕМ И КОНТРОЛЕМ 12. ИСПОЛЬЗОВАНИЕ ИОНИЗИРУЮЩЕГО ИЗЛУЧЕНИЯ В ПРОИЗВОДСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ 13. ПРОИЗВОДСТВО ЛЕКАРСТВЕННЫХ СРЕДСТВ ДЛЯ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ 14. ПРОИЗВОДСТВО ЛЕКАРСТВЕННЫХ СРЕДСТВ ИЗ КРОВИ ИЛИ ПЛАЗМЫ ЧЕЛОВЕКА 15. АТТЕСТАЦИЯ ПРОЦЕССОВ И ОБОРУДОВАНИЯ 16. ПОДТВЕРЖДЕНИЕ СООТВЕТСТВИЯ СЕРИИ ПРОДУКЦИИ С ЦЕЛЬЮ ЕЕ ВЫПУСКА, ВЫПОЛНЯЕМОЕ УПОЛНОМОЧЕННЫМ ЛИЦОМ 17. ВЫПУСК ПО ПАРАМЕТРАМ 18. РУКОВОДСТВО ПО ПРОИЗВОДСТВУ АКТИВНЫХ ФАРМАЦЕВТИЧЕСКИХ
 1. Управление качеством Ø ГОСТ Р ИСО 19011 -2003 « Руководящие указания по аудиту систем менеджмента качества и/или систем экологического менеджмента Ø ОСТ 91500. 05. 001 -00 «Стандарты качества лекарственных средств. Основные положения» Ø ОСТ 64 -02 -001 -2002 «Контрольные лаборатории отделов контроля качества предприятий-производителей лекарственных средств. Требования и порядок аккредитации на техническую компетентность» 2. Персонал Ø МУ 42 -51 -10 -93 «Методические указания. Требования к персоналу» Ø МУ 42 -51 -11 -93 «Методические указания. Подготовка персонала к работе» Ø МУ 42 -51 -12 -93 «Методические указания. Подготовка технологической одежды и перчаток» Ø МУ 42 -51 -13 -93 «Методические указания. Обработка рук персонала»
1. Управление качеством Ø ГОСТ Р ИСО 19011 -2003 « Руководящие указания по аудиту систем менеджмента качества и/или систем экологического менеджмента Ø ОСТ 91500. 05. 001 -00 «Стандарты качества лекарственных средств. Основные положения» Ø ОСТ 64 -02 -001 -2002 «Контрольные лаборатории отделов контроля качества предприятий-производителей лекарственных средств. Требования и порядок аккредитации на техническую компетентность» 2. Персонал Ø МУ 42 -51 -10 -93 «Методические указания. Требования к персоналу» Ø МУ 42 -51 -11 -93 «Методические указания. Подготовка персонала к работе» Ø МУ 42 -51 -12 -93 «Методические указания. Подготовка технологической одежды и перчаток» Ø МУ 42 -51 -13 -93 «Методические указания. Обработка рук персонала»
 2. Персонал (продолжение) Ø МУ 42 -51 -14 -93 «Методические указания. Контроль микробной контаминации рук персонала» Ø МУ 42 -51 -15 -93 «Методические указания. Контроль микробной контаминации технологической одежды» Ø МУ 42 -51 -16 -93 «Методические указания. Контроль степени выделения частиц тканью технологической одежды» Ø РДИ 64 -28 -84 «Инструкция. Соблюдение и контроль личной гигиены персонала производственных помещений на предприятиях и в организациях химико - фармацевтической промышленности» Ø ОСТ 64 -028 -87 «ССБТ. Порядок обеспечения рабочих и служащих средствами индивидуальной защиты. Выбор, эксплуатация и уход за ними» Ø ОСТ 64 -038 -87 «ССБТ. Классификация лекарственных препаратов для выбора средств индивидуальной защиты» Ø МУ 64 -09 -001 -2002 «Производство лекарственных средств. Персонал фармацевтических предприятий»
2. Персонал (продолжение) Ø МУ 42 -51 -14 -93 «Методические указания. Контроль микробной контаминации рук персонала» Ø МУ 42 -51 -15 -93 «Методические указания. Контроль микробной контаминации технологической одежды» Ø МУ 42 -51 -16 -93 «Методические указания. Контроль степени выделения частиц тканью технологической одежды» Ø РДИ 64 -28 -84 «Инструкция. Соблюдение и контроль личной гигиены персонала производственных помещений на предприятиях и в организациях химико - фармацевтической промышленности» Ø ОСТ 64 -028 -87 «ССБТ. Порядок обеспечения рабочих и служащих средствами индивидуальной защиты. Выбор, эксплуатация и уход за ними» Ø ОСТ 64 -038 -87 «ССБТ. Классификация лекарственных препаратов для выбора средств индивидуальной защиты» Ø МУ 64 -09 -001 -2002 «Производство лекарственных средств. Персонал фармацевтических предприятий»
 3. Помещения и оборудование Ø ГОСТ 12. 2. 020 -76 «ССБТ. Электрооборудование взрывозащищенное. Классификация. Маркировка» Ø ГОСТ 12. 2. 016 -81 «ССБТ. Оборудование компрессорное. Общие требования безопасности» Ø ГОСТ 12. 2. 003 -91 «ССБТ. Оборудование производственное. Общие требования безопасности» Ø ГОСТ Р 50766 -95 «Помещения чистые. Классификация, методы аттестации. Основные требования» Ø ГОСТ Р ИСО 14644 -1 -2000 «Чистые помещения и связанные с ними контролируемые среды. Ч. 1 Классификация чистоты воздуха» Ø ГОСТ Р ИСО 14644 -2 -2000 «Чистые помещения и связанные с ними контролируемые среды. Ч. 2 Требования к контролю и мониторингу для подтверждения постоянного соответствия ГОСТ Р ИСО 14644 -1» Ø ГОСТ Р ИСО 14644 -4 -2002 «Чистые помещения и связанные с ними контролируемые среды. Ч. 4 Проектирование, строительство и ввод в эксплуатацию»
3. Помещения и оборудование Ø ГОСТ 12. 2. 020 -76 «ССБТ. Электрооборудование взрывозащищенное. Классификация. Маркировка» Ø ГОСТ 12. 2. 016 -81 «ССБТ. Оборудование компрессорное. Общие требования безопасности» Ø ГОСТ 12. 2. 003 -91 «ССБТ. Оборудование производственное. Общие требования безопасности» Ø ГОСТ Р 50766 -95 «Помещения чистые. Классификация, методы аттестации. Основные требования» Ø ГОСТ Р ИСО 14644 -1 -2000 «Чистые помещения и связанные с ними контролируемые среды. Ч. 1 Классификация чистоты воздуха» Ø ГОСТ Р ИСО 14644 -2 -2000 «Чистые помещения и связанные с ними контролируемые среды. Ч. 2 Требования к контролю и мониторингу для подтверждения постоянного соответствия ГОСТ Р ИСО 14644 -1» Ø ГОСТ Р ИСО 14644 -4 -2002 «Чистые помещения и связанные с ними контролируемые среды. Ч. 4 Проектирование, строительство и ввод в эксплуатацию»
 3. Помещения и оборудование (продолжение) Ø МУ 42 -51 -5 -93 «Методические указания. Подготовка производственных помещений» Ø МУ 42 -51 -6 -93 «Методические указания. Подготовка технологического оборудования» Ø МУ 42 -51 -9 -93 «Методические указания. Контроль микробной контаминации производственных помещений и оборудования» Ø МУ 64 -02 -005 -2002 «Классификация и организация помещений для производства нестерильных лекарственных средств» Ø ОСТ 64 -043 -87 «Технологическое оборудование, используемое в химфармпромышленности. Обозначения условные графические» Ø ОСТ 64 -057 -88 «ССБТ. Оборудование для таблетирования лекарственных средств. Требования безопасности»
3. Помещения и оборудование (продолжение) Ø МУ 42 -51 -5 -93 «Методические указания. Подготовка производственных помещений» Ø МУ 42 -51 -6 -93 «Методические указания. Подготовка технологического оборудования» Ø МУ 42 -51 -9 -93 «Методические указания. Контроль микробной контаминации производственных помещений и оборудования» Ø МУ 64 -02 -005 -2002 «Классификация и организация помещений для производства нестерильных лекарственных средств» Ø ОСТ 64 -043 -87 «Технологическое оборудование, используемое в химфармпромышленности. Обозначения условные графические» Ø ОСТ 64 -057 -88 «ССБТ. Оборудование для таблетирования лекарственных средств. Требования безопасности»
 По соответствию производственных помещений и оборудования техническим нормам и требованиям В РФ имеется около 200 СНи. Пов, Сан. Пи. Нов, рекомендаций Госгортехнадзора и Пожарного надзора: СНи. П 11 -01 -95 «Инструкция о порядке разработки, согласования, утверждения и составе проектной документации на строительство предприятий, зданий и сооружений» . СНи. П 2. 09. 02 -85 «Производственные здания» , 1991 г. СНи. П 2. 01. 02 -85 «Противопожарные нормы» СНи. П 21 -01 -97 «Пожарная безопасность зданий и сооружений» «Санитарные правила для предприятий по производству лекарственных препаратов» НПБ 105 -95 «Определение категорий помещений и зданий по взрывопожароопасной и пожарной опасности» НПБ 110 -96 «Перечень зданий, сооружений, помещений и оборудования, подлежащих защите автоматическими установками тушения и обнаружения пожара» СНи. П 3. 05 -84 «Технологическое оборудование и технологические трубопроводы» «Инструкция о порядке рассмотрения, согласования и экспертизы воздухоохранных мероприятий и выдачи разрешений на выброс загрязняющих веществ по проектным решениям» [ОНД 1 -84] МУ 64 -01 -003 -2002 Порядок составления и выдачи исходных данных на проектирование новых, расширение, реконструкцию и техническое перевооружение предприятий и производственных объектов медицинской промышленности
По соответствию производственных помещений и оборудования техническим нормам и требованиям В РФ имеется около 200 СНи. Пов, Сан. Пи. Нов, рекомендаций Госгортехнадзора и Пожарного надзора: СНи. П 11 -01 -95 «Инструкция о порядке разработки, согласования, утверждения и составе проектной документации на строительство предприятий, зданий и сооружений» . СНи. П 2. 09. 02 -85 «Производственные здания» , 1991 г. СНи. П 2. 01. 02 -85 «Противопожарные нормы» СНи. П 21 -01 -97 «Пожарная безопасность зданий и сооружений» «Санитарные правила для предприятий по производству лекарственных препаратов» НПБ 105 -95 «Определение категорий помещений и зданий по взрывопожароопасной и пожарной опасности» НПБ 110 -96 «Перечень зданий, сооружений, помещений и оборудования, подлежащих защите автоматическими установками тушения и обнаружения пожара» СНи. П 3. 05 -84 «Технологическое оборудование и технологические трубопроводы» «Инструкция о порядке рассмотрения, согласования и экспертизы воздухоохранных мероприятий и выдачи разрешений на выброс загрязняющих веществ по проектным решениям» [ОНД 1 -84] МУ 64 -01 -003 -2002 Порядок составления и выдачи исходных данных на проектирование новых, расширение, реконструкцию и техническое перевооружение предприятий и производственных объектов медицинской промышленности
 4. Документация Ø ГОСТ 2. 105 -95 «ЕСКД. Общие требования к текстовым документам» Ø ГОСТ Р 6. 30 -2003 «Унифицированные системы документации. Унифицированная система организационно-распорядительной документации. Требования к оформлению документов» Ø ОСТ 64 -02 -003 -2002 «Продукция медицинской промышленности. Технологические регламенты производства. Содержание. Порядок разработки, согласования и утверждения» Ø МУ 64 -04 -002 -2002 «Производство лекарственных средств. Документация» Ø МУ 64 -04 -003 -2002 «Производство лекарственных средств. Документация. Общие требования. Примерные формы и рекомендации по их заполнению»
4. Документация Ø ГОСТ 2. 105 -95 «ЕСКД. Общие требования к текстовым документам» Ø ГОСТ Р 6. 30 -2003 «Унифицированные системы документации. Унифицированная система организационно-распорядительной документации. Требования к оформлению документов» Ø ОСТ 64 -02 -003 -2002 «Продукция медицинской промышленности. Технологические регламенты производства. Содержание. Порядок разработки, согласования и утверждения» Ø МУ 64 -04 -002 -2002 «Производство лекарственных средств. Документация» Ø МУ 64 -04 -003 -2002 «Производство лекарственных средств. Документация. Общие требования. Примерные формы и рекомендации по их заполнению»
 5. Производство Ø ГОСТ 17768 -90 «Средства лекарственные. Упаковка, маркировка, транспортирование и хранение» Ø МУ 42 -51 -1 -93 и МУ 42 -51 -26 -93 «Методические указания. Организация и контроль производства лекарственных средств. Стерильные лекарственные средства» Ø МУ 64 -04 -001 -2002 «Производство лекарственных средств. Валидация. Основные положения» Ø МУ 64 -01 -001 -2002 «Производство лекарственных средств. Термины и определения» Ø МУ 64 -801 -00 «Организация процесса упаковки лекарственных средств. Основные положения и требования»
5. Производство Ø ГОСТ 17768 -90 «Средства лекарственные. Упаковка, маркировка, транспортирование и хранение» Ø МУ 42 -51 -1 -93 и МУ 42 -51 -26 -93 «Методические указания. Организация и контроль производства лекарственных средств. Стерильные лекарственные средства» Ø МУ 64 -04 -001 -2002 «Производство лекарственных средств. Валидация. Основные положения» Ø МУ 64 -01 -001 -2002 «Производство лекарственных средств. Термины и определения» Ø МУ 64 -801 -00 «Организация процесса упаковки лекарственных средств. Основные положения и требования»
 6. Контроль качества Ø ГОСТ Р ИСО 9001 -2001 «Системы менеджмента качества. Требования» Ø МУ 2. 1. 4. 1057 -01 «Организация внутреннего контроля качества санитарно-микробиологических исследований воды. Методические указания» Ø ОСТ 42 -504 -96 «Контроль качества лекарственных средств на промышленных предприятиях и в организациях. Основные положения» Ø ОСТ 64 -02 -001 -2002 «Контрольные лаборатории отделов контроля качества предприятий-производителей лекарственных средств. Требования и порядок аккредитации на техническую компетентность»
6. Контроль качества Ø ГОСТ Р ИСО 9001 -2001 «Системы менеджмента качества. Требования» Ø МУ 2. 1. 4. 1057 -01 «Организация внутреннего контроля качества санитарно-микробиологических исследований воды. Методические указания» Ø ОСТ 42 -504 -96 «Контроль качества лекарственных средств на промышленных предприятиях и в организациях. Основные положения» Ø ОСТ 64 -02 -001 -2002 «Контрольные лаборатории отделов контроля качества предприятий-производителей лекарственных средств. Требования и порядок аккредитации на техническую компетентность»
 1. Удостоверьтесь в наличии письменного руководства (инструкции) перед началом любого вида работ. 2. Следуйте инструкции методично, выполняя всё до мельчайших деталей (консультируйтесь, если Вы чего-нибудь не понимаете). 3. Проследите, чтобы используемый материал был именно тот, который необходим. 4. Убедитесь, что используемое оборудование именно то, которое необходимо, и что оно чистое. 5. Предотвращайте загрязнение и смешивание. 6. Остерегайтесь ошибок в маркировке. 7. Будьте аккуратны и точны в своих действиях. 8. Чистота и опрятность Вашего рабочего места - вот Ваш закон. 9. Помните о возможности ошибок, недосмотра и неправильной производственной практики и докладывайте о подобных случаях немедленно, так как умалчивание может стоить кому-то жизни. 10. Аккуратно документируйте все Ваши действия и процесс тестирования.
1. Удостоверьтесь в наличии письменного руководства (инструкции) перед началом любого вида работ. 2. Следуйте инструкции методично, выполняя всё до мельчайших деталей (консультируйтесь, если Вы чего-нибудь не понимаете). 3. Проследите, чтобы используемый материал был именно тот, который необходим. 4. Убедитесь, что используемое оборудование именно то, которое необходимо, и что оно чистое. 5. Предотвращайте загрязнение и смешивание. 6. Остерегайтесь ошибок в маркировке. 7. Будьте аккуратны и точны в своих действиях. 8. Чистота и опрятность Вашего рабочего места - вот Ваш закон. 9. Помните о возможности ошибок, недосмотра и неправильной производственной практики и докладывайте о подобных случаях немедленно, так как умалчивание может стоить кому-то жизни. 10. Аккуратно документируйте все Ваши действия и процесс тестирования.
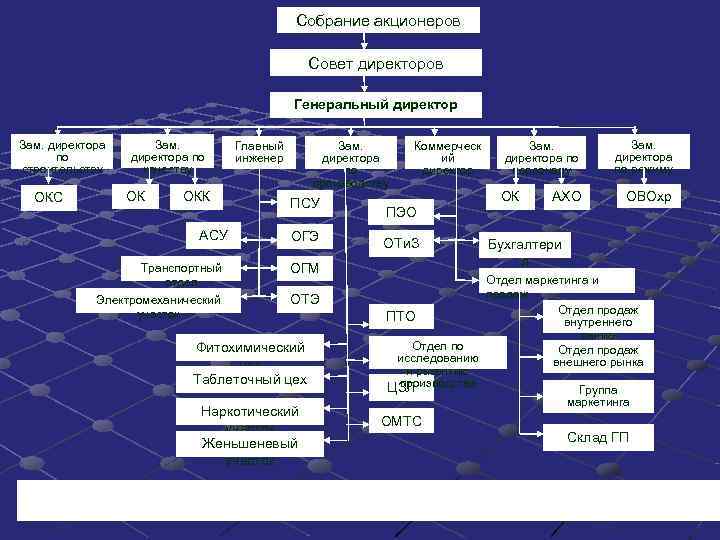
 Собрание акционеров Совет директоров Генеральный директор Зам. директора Зам. Главный Зам. Коммерческ Зам. по директора по инженер директора ий директора по директора строительству качеству по директор персоналу по режиму производству ОКС ОК ОКК ПСУ ОК АХО ОВОхр ПЭО АСУ ОГЭ ОТи. З Бухгалтери Транспортный я ОГМ отдел Отдел маркетинга и Электромеханический ОТЭ продаж участок Отдел продаж ПТО внутреннего рынка Фитохимический Отдел по Отдел продаж исследованию внешнего рынка цех и развитию Таблеточный цех производства ЦЗЛ Группа маркетинга Наркотический ОМТС участок Женьшеневый Склад ГП участок Организационная структура химико-фармацевтического завода
Собрание акционеров Совет директоров Генеральный директор Зам. директора Зам. Главный Зам. Коммерческ Зам. по директора по инженер директора ий директора по директора строительству качеству по директор персоналу по режиму производству ОКС ОК ОКК ПСУ ОК АХО ОВОхр ПЭО АСУ ОГЭ ОТи. З Бухгалтери Транспортный я ОГМ отдел Отдел маркетинга и Электромеханический ОТЭ продаж участок Отдел продаж ПТО внутреннего рынка Фитохимический Отдел по Отдел продаж исследованию внешнего рынка цех и развитию Таблеточный цех производства ЦЗЛ Группа маркетинга Наркотический ОМТС участок Женьшеневый Склад ГП участок Организационная структура химико-фармацевтического завода
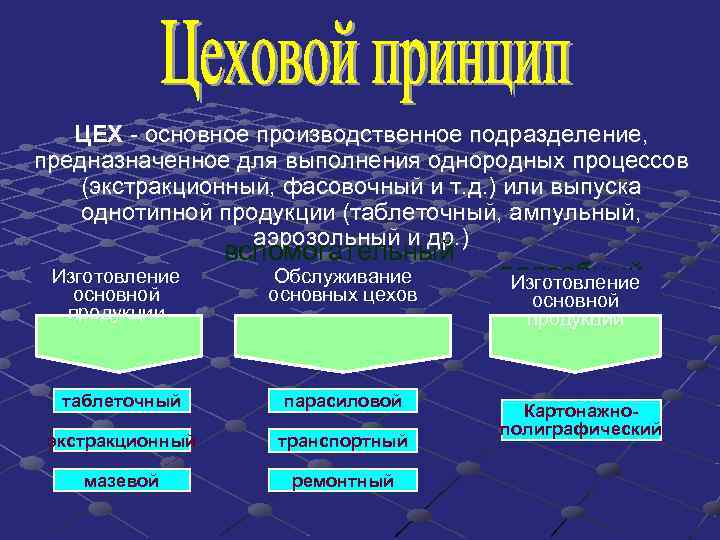
 ЦЕХ - основное производственное подразделение, предназначенное для выполнения однородных процессов (экстракционный, фасовочный и т. д. ) или выпуска однотипной продукции (таблеточный, ампульный, аэрозольный и др. ) вспомогательный основной Изготовление Обслуживание подсобный Изготовление основной основных цехов основной продукции продукции таблеточный парасиловой Картонажно- полиграфический экстракционный транспортный мазевой ремонтный
ЦЕХ - основное производственное подразделение, предназначенное для выполнения однородных процессов (экстракционный, фасовочный и т. д. ) или выпуска однотипной продукции (таблеточный, ампульный, аэрозольный и др. ) вспомогательный основной Изготовление Обслуживание подсобный Изготовление основной основных цехов основной продукции продукции таблеточный парасиловой Картонажно- полиграфический экстракционный транспортный мазевой ремонтный
 Лекарственное средство (лекарственная субстанция) - вещества, применяемые для профилактики, диагностики, лечения болезни, предотвращения беременности, полученные из крови, плазмы крови, а также органов, тканей человека или животного, растений, минералов, методами синтеза или с применением биологических технологий. К лекарственным средствам относятся также вещества растительного, животного или синтетического происхождения, обладающие фармакологической активностью и предназначенные для производства и изготовления лекарственных средств (фармацевтические субстанции) Лекарственный препарат – дозированное лекарственное средство, готовое к применению Лекарственная форма − форма, придаваемая лекарственному средству или растительному сырью, удобная для употребления и обеспечивающая необходимый лечебный эффект
Лекарственное средство (лекарственная субстанция) - вещества, применяемые для профилактики, диагностики, лечения болезни, предотвращения беременности, полученные из крови, плазмы крови, а также органов, тканей человека или животного, растений, минералов, методами синтеза или с применением биологических технологий. К лекарственным средствам относятся также вещества растительного, животного или синтетического происхождения, обладающие фармакологической активностью и предназначенные для производства и изготовления лекарственных средств (фармацевтические субстанции) Лекарственный препарат – дозированное лекарственное средство, готовое к применению Лекарственная форма − форма, придаваемая лекарственному средству или растительному сырью, удобная для употребления и обеспечивающая необходимый лечебный эффект
 патентованные лекарственные средства - лекарственные средства, право на производство и продажу которых охраняется патентным законодательством Российской Федерации; незаконные копии лекарственных средств - лекарственные средства, поступившие в обращение с нарушением патентного законодательства Российской Федерации; оригинальные лекарственные средства - лекарственные средства, поступившие в обращение с зарегистрированными собственными названиями; воспроизведенные лекарственные средства - лекарственные средства, поступившие в обращение после истечения срока действия исключительных патентных прав на оригинальные лекарственные средства;
патентованные лекарственные средства - лекарственные средства, право на производство и продажу которых охраняется патентным законодательством Российской Федерации; незаконные копии лекарственных средств - лекарственные средства, поступившие в обращение с нарушением патентного законодательства Российской Федерации; оригинальные лекарственные средства - лекарственные средства, поступившие в обращение с зарегистрированными собственными названиями; воспроизведенные лекарственные средства - лекарственные средства, поступившие в обращение после истечения срока действия исключительных патентных прав на оригинальные лекарственные средства;
 Вспомогательное вещество − относительно индифферентное вещество органической или неорганической природы, разрешенное для медицинского применения с целью получения лекарственной формы, придания или сохранения определенных свойств лекарственного препарата. Перечень вспомогательных веществ обширен: в зависимости от вида лекарственной формы это могут быть вещества, увеличивающие вязкость, поверхностно - активные и буферные, корригенты, консерванты, стабилизаторы, наполнители, разрыхлители, скользящие и др. качество лекарственных средств - соответствие лекарственных средств государственному стандарту качества лекарственных средств; безопасность лекарственных средств - характеристика лекарственных средств, основанная на сравнительном анализе их эффективности и оценки риска причинения вреда здоровью; эффективность лекарственных средств - характеристика степени положительного влияния лекарственных средств на течение болезни; сертификат качества лекарственного средства - документ, подтверждающий соответствие качества лекарственного средства государственному стандарту качества лекарственных средств;
Вспомогательное вещество − относительно индифферентное вещество органической или неорганической природы, разрешенное для медицинского применения с целью получения лекарственной формы, придания или сохранения определенных свойств лекарственного препарата. Перечень вспомогательных веществ обширен: в зависимости от вида лекарственной формы это могут быть вещества, увеличивающие вязкость, поверхностно - активные и буферные, корригенты, консерванты, стабилизаторы, наполнители, разрыхлители, скользящие и др. качество лекарственных средств - соответствие лекарственных средств государственному стандарту качества лекарственных средств; безопасность лекарственных средств - характеристика лекарственных средств, основанная на сравнительном анализе их эффективности и оценки риска причинения вреда здоровью; эффективность лекарственных средств - характеристика степени положительного влияния лекарственных средств на течение болезни; сертификат качества лекарственного средства - документ, подтверждающий соответствие качества лекарственного средства государственному стандарту качества лекарственных средств;
 Нормативно-техническая (нормативная) документация документы, устанавливающие правила, общие принципы или характеристики, касающиеся разных видов деятельности или их результатов : 1. Государственный реестр лекарственных сердств 2. Государственная фармакопея (ГФ). 3. Фармакопейные статьи (ФС). 4. Фармакопейная статья предприятия (ФСП) 5. Государственные (национальные)стандарты (ГОСТ). 6. Технические регламенты 7. Технологические регламенты 8. Отраслевые стандарты (ОСТ). 9. Технические условия (ТУ). 10. Руководящий нормативный документ (РД). 11. Производственные и технологические инструкции.
Нормативно-техническая (нормативная) документация документы, устанавливающие правила, общие принципы или характеристики, касающиеся разных видов деятельности или их результатов : 1. Государственный реестр лекарственных сердств 2. Государственная фармакопея (ГФ). 3. Фармакопейные статьи (ФС). 4. Фармакопейная статья предприятия (ФСП) 5. Государственные (национальные)стандарты (ГОСТ). 6. Технические регламенты 7. Технологические регламенты 8. Отраслевые стандарты (ОСТ). 9. Технические условия (ТУ). 10. Руководящий нормативный документ (РД). 11. Производственные и технологические инструкции.
 Регистрационный номер – кодовое обозначение, присваиваемое лекарственному средству при государственной регистрации ГОСУДАРСТВЕННАЯ ФАРМАКОПЕЯ (ГФ) – сборник государственных стандартов качества лекарственных средств (ФC), имеющий законодательный характер. ФАРМАКОПЕЙНАЯ СТАТЬЯ (ФС) - Государственный стандарт качества лекарственного средства на лекарственное средство под МНН (если оно имеется ), содержащий обязательный перечень показателей и методов контроля качества с учетом его лекарственной формы. ФАРМАКОПЕЙНАЯ СТАТЬЯ ПРЕДПРИЯТИЯ (ФСП) - стандарт качества лекарственного средства на лекарственное средство под торговым названием, содержащий перечень показателей и методов контроля качества лекарственного средства производства конкретного предприятия, учитывающий конкретную технологию данного предприятия и прошедший экспертизу и регистрацию в установленном порядке.
Регистрационный номер – кодовое обозначение, присваиваемое лекарственному средству при государственной регистрации ГОСУДАРСТВЕННАЯ ФАРМАКОПЕЯ (ГФ) – сборник государственных стандартов качества лекарственных средств (ФC), имеющий законодательный характер. ФАРМАКОПЕЙНАЯ СТАТЬЯ (ФС) - Государственный стандарт качества лекарственного средства на лекарственное средство под МНН (если оно имеется ), содержащий обязательный перечень показателей и методов контроля качества с учетом его лекарственной формы. ФАРМАКОПЕЙНАЯ СТАТЬЯ ПРЕДПРИЯТИЯ (ФСП) - стандарт качества лекарственного средства на лекарственное средство под торговым названием, содержащий перечень показателей и методов контроля качества лекарственного средства производства конкретного предприятия, учитывающий конкретную технологию данного предприятия и прошедший экспертизу и регистрацию в установленном порядке.
 технический регламент - документ, который принят международным договором Российской Федерации, ратифицированным в порядке, установленном законодательством Российской Федерации, или федеральным законом, или указом Президента Российской Федерации, или постановлением Правительства Российской Федерации, и устанавливает обязательные для применения и исполнения требования к объектам технического регулирования (продукции, в том числе зданиям, строениям и сооружениям, процессам производства, эксплуатации, хранения, перевозки, реализации и утилизации). Отраслевой стандарт (ОСТ) - нормативный документ устанавливающий дополнительные технические требования и групповые характеристики, необходимые для изготовления и поставки ЛС (научно- технические термины и обозначения, общетехническая документация, технологические нормы, правила приемки, маркировка, упаковка, хранение, транспортирование, общие правила и т. д. ) Производственная инструкция - нормативный документ, имеющий статус стандарта предприятия, который регламентирует определенную часть производственного процесса.
технический регламент - документ, который принят международным договором Российской Федерации, ратифицированным в порядке, установленном законодательством Российской Федерации, или федеральным законом, или указом Президента Российской Федерации, или постановлением Правительства Российской Федерации, и устанавливает обязательные для применения и исполнения требования к объектам технического регулирования (продукции, в том числе зданиям, строениям и сооружениям, процессам производства, эксплуатации, хранения, перевозки, реализации и утилизации). Отраслевой стандарт (ОСТ) - нормативный документ устанавливающий дополнительные технические требования и групповые характеристики, необходимые для изготовления и поставки ЛС (научно- технические термины и обозначения, общетехническая документация, технологические нормы, правила приемки, маркировка, упаковка, хранение, транспортирование, общие правила и т. д. ) Производственная инструкция - нормативный документ, имеющий статус стандарта предприятия, который регламентирует определенную часть производственного процесса.
 Технологический регламент производства - нормативный документ, устанавливающий методы производства, технологические нормативы, технические средства, условия и порядок проведения технологического процесса в производстве фармацевтической продукции, обеспечивающий получение лекарственного средства с показателями качества, отвечающими требованиям ФСП (ТУ), а также устанавливающий безопасность ведения работ и достижение оптимальных технико-экономических показателей конкретного производства. лабораторный регламент (ЛР) опытно-промышленный регламент (ОПР) пусковые (временные) регламенты (ПУР) ОСТ 64 -03 -003 -2002 «Продукция медицинской промышленности. Технологические регламенты производства. промышленный регламент (ПР) Содержание, порядок разработки, согласования и утверждения»
Технологический регламент производства - нормативный документ, устанавливающий методы производства, технологические нормативы, технические средства, условия и порядок проведения технологического процесса в производстве фармацевтической продукции, обеспечивающий получение лекарственного средства с показателями качества, отвечающими требованиям ФСП (ТУ), а также устанавливающий безопасность ведения работ и достижение оптимальных технико-экономических показателей конкретного производства. лабораторный регламент (ЛР) опытно-промышленный регламент (ОПР) пусковые (временные) регламенты (ПУР) ОСТ 64 -03 -003 -2002 «Продукция медицинской промышленности. Технологические регламенты производства. промышленный регламент (ПР) Содержание, порядок разработки, согласования и утверждения»
 1. Характеристика готового продукта 2. Химическая схема производства 3. Технологическая схема производства 4. Аппаратурная схема производства и спецификация оборудования 5. Характеристика сырья, вспомогательных материалов и полупродуктов 6. Изложение технологического процесса 7. Материальный баланс 8. Переработка и обезвреживание отходов производства 9. Контроль производства 10. Безопасная эксплуатация производства 11. Охрана окружающей среды 12. Перечень производственных инструкций 13. Технико-экономические нормативы 14. Информационные материалы
1. Характеристика готового продукта 2. Химическая схема производства 3. Технологическая схема производства 4. Аппаратурная схема производства и спецификация оборудования 5. Характеристика сырья, вспомогательных материалов и полупродуктов 6. Изложение технологического процесса 7. Материальный баланс 8. Переработка и обезвреживание отходов производства 9. Контроль производства 10. Безопасная эксплуатация производства 11. Охрана окружающей среды 12. Перечень производственных инструкций 13. Технико-экономические нормативы 14. Информационные материалы
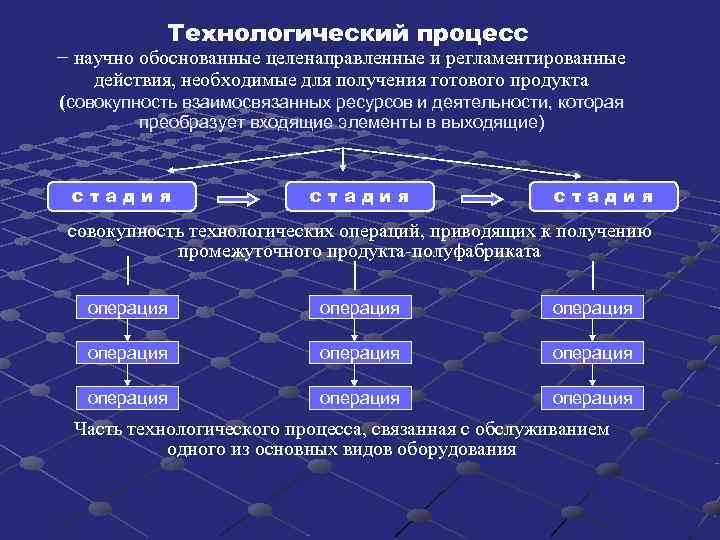
 Технологический процесс − научно обоснованные целенаправленные и регламентированные действия, необходимые для получения готового продукта (совокупность взаимосвязанных ресурсов и деятельности, которая преобразует входящие элементы в выходящие) стадия стадия совокупность технологических операций, приводящих к получению промежуточного продукта-полуфабриката операция операция операция Часть технологического процесса, связанная с обслуживанием одного из основных видов оборудования
Технологический процесс − научно обоснованные целенаправленные и регламентированные действия, необходимые для получения готового продукта (совокупность взаимосвязанных ресурсов и деятельности, которая преобразует входящие элементы в выходящие) стадия стадия совокупность технологических операций, приводящих к получению промежуточного продукта-полуфабриката операция операция операция Часть технологического процесса, связанная с обслуживанием одного из основных видов оборудования
 Готовая продукция - продукция, прошедшая все последовательные стадии технологического процесса, включая упаковку, маркировку, контроль качества, и готовая к реализации Серия готовой продукции – определенное количество готовой продукции, полученное в условиях, гарантирующих ее однородность Серия готового лекарственного средства - совокупность единиц лекарственного препарата, которая изготовлена из одних и тех же серий исходного сырья, материалов и полуфабрикатов, на одном технологическом оборудовании, в одном технологическом процессе, в одинаковых условиях Полупродукт - частично обработанное сырье, получаемый на любой стадии технологического процесса, исключая конечную стадию, и предназначенная для дальнейшей обработки, прежде чем он станет готовой продукцией. Технические средства - совокупность орудий производства, необходимых для осуществления технологического процесса.
Готовая продукция - продукция, прошедшая все последовательные стадии технологического процесса, включая упаковку, маркировку, контроль качества, и готовая к реализации Серия готовой продукции – определенное количество готовой продукции, полученное в условиях, гарантирующих ее однородность Серия готового лекарственного средства - совокупность единиц лекарственного препарата, которая изготовлена из одних и тех же серий исходного сырья, материалов и полуфабрикатов, на одном технологическом оборудовании, в одном технологическом процессе, в одинаковых условиях Полупродукт - частично обработанное сырье, получаемый на любой стадии технологического процесса, исключая конечную стадию, и предназначенная для дальнейшей обработки, прежде чем он станет готовой продукцией. Технические средства - совокупность орудий производства, необходимых для осуществления технологического процесса.
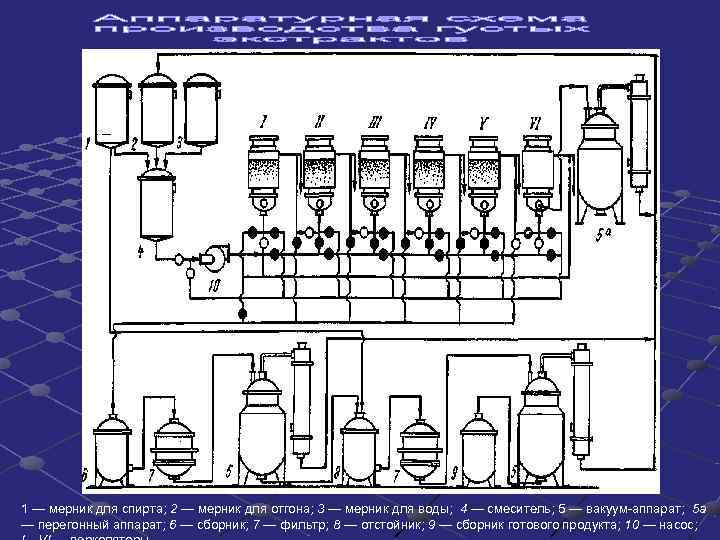
 1 — мерник для спирта; 2 — мерник для отгона; 3 — мерник для воды; 4 — смеситель; 5 — вакуум-аппарат; 5 а — перегонный аппарат; 6 — сборник; 7 — фильтр; 8 — отстойник; 9 — сборник готового продукта; 10 — насос;
1 — мерник для спирта; 2 — мерник для отгона; 3 — мерник для воды; 4 — смеситель; 5 — вакуум-аппарат; 5 а — перегонный аппарат; 6 — сборник; 7 — фильтр; 8 — отстойник; 9 — сборник готового продукта; 10 — насос;
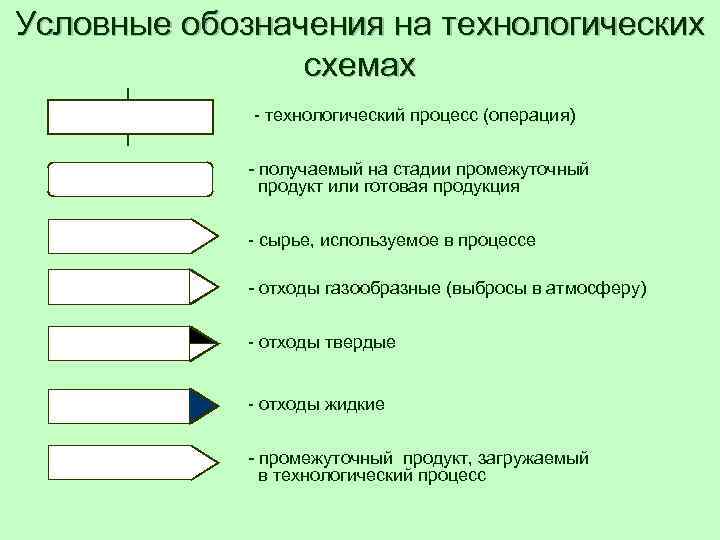
 Условные обозначения на технологических схемах - технологический процесс (операция) - получаемый на стадии промежуточный продукт или готовая продукция - сырье, используемое в процессе - отходы газообразные (выбросы в атмосферу) - отходы твердые - отходы жидкие - промежуточный продукт, загружаемый в технологический процесс
Условные обозначения на технологических схемах - технологический процесс (операция) - получаемый на стадии промежуточный продукт или готовая продукция - сырье, используемое в процессе - отходы газообразные (выбросы в атмосферу) - отходы твердые - отходы жидкие - промежуточный продукт, загружаемый в технологический процесс
 ОСТ 64 -03 -003 -2002 «Продукция медицинской промышленности. Технологические регламенты производства. Содержание, порядок разработки, согласования и утверждения» “ВР” – стадии вспомогательных работ “ТП” – стадии основного технологического процесса “ПО” – стадии переработки используемых отходов “ОБО” – стадии обезвреживания отходов “ОБВ” – стадии обезвреживания технологических и вентиляционных выбросов в атмосферу “УМО” – стадии упаковывания, маркировки и отгрузки готового продукта
ОСТ 64 -03 -003 -2002 «Продукция медицинской промышленности. Технологические регламенты производства. Содержание, порядок разработки, согласования и утверждения» “ВР” – стадии вспомогательных работ “ТП” – стадии основного технологического процесса “ПО” – стадии переработки используемых отходов “ОБО” – стадии обезвреживания отходов “ОБВ” – стадии обезвреживания технологических и вентиляционных выбросов в атмосферу “УМО” – стадии упаковывания, маркировки и отгрузки готового продукта
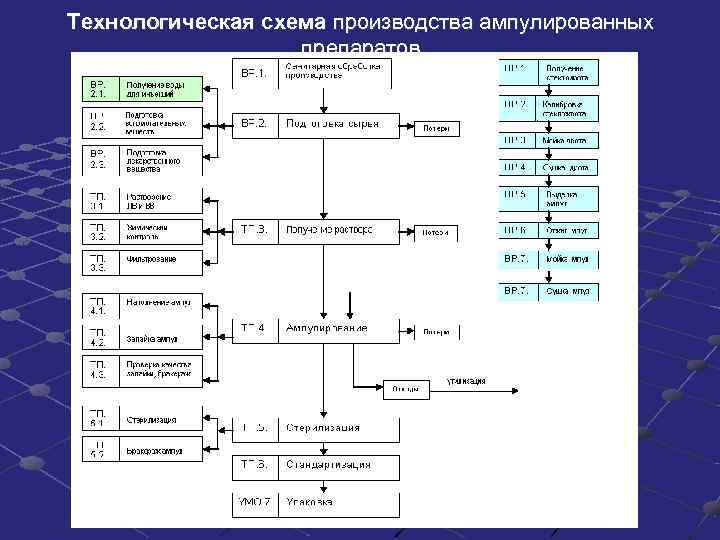
 Технологическая схема производства ампулированных препаратов
Технологическая схема производства ампулированных препаратов
 Отходы - модифицированные или некондиционные остатки исходного сырья, материалов или полуфабрикатов, которые без соответствующей переработки не могут быть использованы для приготовления готового продукта. Отбросы - отходы производства, которые не подлежат дальнейшей переработке и не представляют потребительской стоимости Материальные потери : 1. Механические − при недостаточной механизации процесса перемещения перерабатываемых материалов (пролив жидкости, бой); 2. Физико-химические − в случае проведения процесса без учета физико-химических свойств лекарственных веществ (неполнота экстрагирования веществ, потеря эфирного масла при выпаривании); 3. Химические – в следствие неполноты протекания реакции.
Отходы - модифицированные или некондиционные остатки исходного сырья, материалов или полуфабрикатов, которые без соответствующей переработки не могут быть использованы для приготовления готового продукта. Отбросы - отходы производства, которые не подлежат дальнейшей переработке и не представляют потребительской стоимости Материальные потери : 1. Механические − при недостаточной механизации процесса перемещения перерабатываемых материалов (пролив жидкости, бой); 2. Физико-химические − в случае проведения процесса без учета физико-химических свойств лекарственных веществ (неполнота экстрагирования веществ, потеря эфирного масла при выпаривании); 3. Химические – в следствие неполноты протекания реакции.
 Исправимый Окончательный Требует дополнительных затрат Приводит к безвозвратным на его переработку потерям в производстве
Исправимый Окончательный Требует дополнительных затрат Приводит к безвозвратным на его переработку потерям в производстве
 - сравнение теоретически возможного и практически полученного выхода готового продукта - сравнение теоретически возможного и практически полученного выхода готового продукта С 1=(С 2+С 3+С 4)+С 5 (С 1) - количество исходного сырья, материалов, полупродуктов и промежуточной продукции использованных в производстве; (С 2) - количество фактически полученной готовой продукции; (С 3) - отходы; (С 4) - отбросы; (С 5) - потери, т. е. сравнение теоретически возможного и практически полученного выхода продукции
- сравнение теоретически возможного и практически полученного выхода готового продукта - сравнение теоретически возможного и практически полученного выхода готового продукта С 1=(С 2+С 3+С 4)+С 5 (С 1) - количество исходного сырья, материалов, полупродуктов и промежуточной продукции использованных в производстве; (С 2) - количество фактически полученной готовой продукции; (С 3) - отходы; (С 4) - отбросы; (С 5) - потери, т. е. сравнение теоретически возможного и практически полученного выхода продукции
 С 2 Выход продукта (ŋ) = — • 100% ( ) • 100% С 1 -(C 3+C 4) С 2 – количество фактически полученной готовой продукции ; С 1 – количество исходного сырья. С 5 Трата (ε) = • 100% С 1 -(C 3+C 4) С 5 -потери С 1 – количество исходного сырья
С 2 Выход продукта (ŋ) = — • 100% ( ) • 100% С 1 -(C 3+C 4) С 2 – количество фактически полученной готовой продукции ; С 1 – количество исходного сырья. С 5 Трата (ε) = • 100% С 1 -(C 3+C 4) С 5 -потери С 1 – количество исходного сырья
 С 1 К расходный = — С 2 Если регламентом предусматривается возврат сырья и регенерация, то: С 1 − (кол-во возвращенного исх. вещ. ) К расходный = ————— С 2 Норма расхода (расходная норма) – максимально допустимое количество сырья, материалов, полуфабрикатов, необходимое для приготовления единицы продукции.
С 1 К расходный = — С 2 Если регламентом предусматривается возврат сырья и регенерация, то: С 1 − (кол-во возвращенного исх. вещ. ) К расходный = ————— С 2 Норма расхода (расходная норма) – максимально допустимое количество сырья, материалов, полуфабрикатов, необходимое для приготовления единицы продукции.

