 Производство аммиака 1 ЗАО СТК "ЦЕОСИТ"
Производство аммиака 1 ЗАО СТК "ЦЕОСИТ"
 Формы существования азота в литосфере 2
Формы существования азота в литосфере 2
 методы связывания азота • Азотфиксирующими бактериями • Дуговой проводиться под действием электрической дуги при температуре 1500 -2000 градусов по Цельсию. Q 1 = 179, 2 к. Дж/моль • Цианамидный проводиться при температуре 1000 градусов по Цельсию по уравнению: Ca C 2 + N 2 = Ca CN 2 + C + Q 2 = 301, 5 к. Дж/моль • аммиачный способ N 2 + 3 H 2 = 2 NH 3 + Q экзо Q = 14, 2 ккал/моль = 60 к. Дж/моль 3
методы связывания азота • Азотфиксирующими бактериями • Дуговой проводиться под действием электрической дуги при температуре 1500 -2000 градусов по Цельсию. Q 1 = 179, 2 к. Дж/моль • Цианамидный проводиться при температуре 1000 градусов по Цельсию по уравнению: Ca C 2 + N 2 = Ca CN 2 + C + Q 2 = 301, 5 к. Дж/моль • аммиачный способ N 2 + 3 H 2 = 2 NH 3 + Q экзо Q = 14, 2 ккал/моль = 60 к. Дж/моль 3
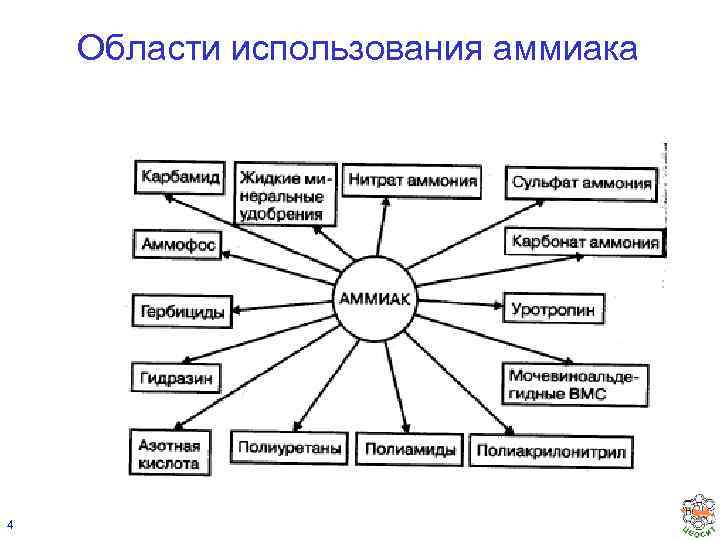 Области использования аммиака 4
Области использования аммиака 4
 Сырьё для производства аммиака 5
Сырьё для производства аммиака 5
 Очистка АВС -адсорбция твёрдыми сорбентами -абсорбция жидкими сорбентами -конденсация примесей глубоким охлаждением - каталитическое гидрирование 6
Очистка АВС -адсорбция твёрдыми сорбентами -абсорбция жидкими сорбентами -конденсация примесей глубоким охлаждением - каталитическое гидрирование 6
 Термодинамика качественно 7 • N 2 + 3 H 2 = 2 NH 3 + Q экзо Q = 14, 2 ккал/моль = 60 к. Дж/моль Задача термодинамики – сдвинуть равновесие системы направо, в сторону образования продукта реакции – аммиака. На качественном уровне влияние условий проведения реакции на равновесие определяется принципом Ле-Шателье. • Если на систему, находящуюся в равновесии, оказывается внешнее воздействие, то в системе происходят процессы, уменьшающие это внешнее воздействие. • Равновесие направо смещают: 1. Отвод тепла – Q → + Q Понижение температуры, которое связано с отводом тепла: -Т→+Т 2. В результате реакции объем газов уменьшается вдвое. При проведении реакции в замкнутом объеме реактора Vр = Const. Это равнозначно уменьшению давления в системе. Поэтому повышение давления смещает равновесие направо: + P → - P 3. Теоретически можно было бы взять избыток азота или водорода против стехиометрии. Но так как у нас нет источника для получения отдельно азота и водорода, а сразу при конверсии метана получается азотоводородная смесь, приходится соотношение реагентов поддерживать строго стехиометрическим
Термодинамика качественно 7 • N 2 + 3 H 2 = 2 NH 3 + Q экзо Q = 14, 2 ккал/моль = 60 к. Дж/моль Задача термодинамики – сдвинуть равновесие системы направо, в сторону образования продукта реакции – аммиака. На качественном уровне влияние условий проведения реакции на равновесие определяется принципом Ле-Шателье. • Если на систему, находящуюся в равновесии, оказывается внешнее воздействие, то в системе происходят процессы, уменьшающие это внешнее воздействие. • Равновесие направо смещают: 1. Отвод тепла – Q → + Q Понижение температуры, которое связано с отводом тепла: -Т→+Т 2. В результате реакции объем газов уменьшается вдвое. При проведении реакции в замкнутом объеме реактора Vр = Const. Это равнозначно уменьшению давления в системе. Поэтому повышение давления смещает равновесие направо: + P → - P 3. Теоретически можно было бы взять избыток азота или водорода против стехиометрии. Но так как у нас нет источника для получения отдельно азота и водорода, а сразу при конверсии метана получается азотоводородная смесь, приходится соотношение реагентов поддерживать строго стехиометрическим
 Термодинамика количественно • Из изобары Вант-Гоффа в интегральной форме • По термодинамической системе присвоения знаков для экзотермической реакции ∆H отрицательно, поэтому выражение константы равновесия принимает вид: • Отсюда: 1. С понижением температуры константа равновесия увеличивается, т. е. равновесие смещается направо. 2. Отвод тепла, связанного с температурой, также смещает равновесие направо. 3. Концентрационyю зависимость константы равновесия можно представить уравнением: • • При t=const, Kp =Const. • 1 С увеличением аммиака увеличивается. • 2 С повышением общего давления в системе равновесная мольная доля аммиака увеличивается в квадрате. Поэтому рекцию проводят при давлении около 30 МПа • 8 т. е. с увеличением чистоты азото-водородной смеси равновесная доля
Термодинамика количественно • Из изобары Вант-Гоффа в интегральной форме • По термодинамической системе присвоения знаков для экзотермической реакции ∆H отрицательно, поэтому выражение константы равновесия принимает вид: • Отсюда: 1. С понижением температуры константа равновесия увеличивается, т. е. равновесие смещается направо. 2. Отвод тепла, связанного с температурой, также смещает равновесие направо. 3. Концентрационyю зависимость константы равновесия можно представить уравнением: • • При t=const, Kp =Const. • 1 С увеличением аммиака увеличивается. • 2 С повышением общего давления в системе равновесная мольная доля аммиака увеличивается в квадрате. Поэтому рекцию проводят при давлении около 30 МПа • 8 т. е. с увеличением чистоты азото-водородной смеси равновесная доля
 кинетика В отсуствие катализатора формальное уравнение скорости реакции выражается: Суммарный порядок по реагентам n = 1 + 3 = 4. Реакции 4 -го порядка мало вероятны, кроме того очень высокой является энергия активации реакции. Поэтому в отсутствие катализатора реакция не протекает. В присутствии промышленного железного катализатора снижается суммарный порядок по реагентам до полуторного и энергия активации снижается до Е = 39, 6 ккал/моль или 165 к. Дж/моль. • • , • где: k 1 k -константа скорости каталитической реакции, • X N 2 –мольная доля азота в смеси, • X H 2 - мольная доля водорода в смеси, • Po - общее давление в смеси, • F- удельная поверхность катализатора. 9
кинетика В отсуствие катализатора формальное уравнение скорости реакции выражается: Суммарный порядок по реагентам n = 1 + 3 = 4. Реакции 4 -го порядка мало вероятны, кроме того очень высокой является энергия активации реакции. Поэтому в отсутствие катализатора реакция не протекает. В присутствии промышленного железного катализатора снижается суммарный порядок по реагентам до полуторного и энергия активации снижается до Е = 39, 6 ккал/моль или 165 к. Дж/моль. • • , • где: k 1 k -константа скорости каталитической реакции, • X N 2 –мольная доля азота в смеси, • X H 2 - мольная доля водорода в смеси, • Po - общее давление в смеси, • F- удельная поверхность катализатора. 9
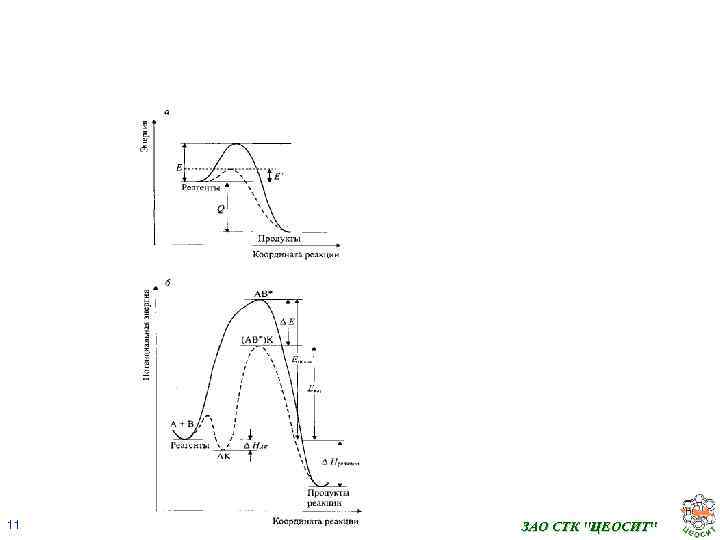
 Катализом называется изменение скорости химических реак ций или возбуждение их в присутствии веществ — катализаторов, которые участвуют в реакции, вступая в промежуточное химическое взаимодействие с реагентами, но восстанавливают свой химический состав при окончании каталитического акта. • A+B=P В присутствии катализатора К • A + K = AK • AK + B = P + K. 10 ЗАО СТК "ЦЕОСИТ"
Катализом называется изменение скорости химических реак ций или возбуждение их в присутствии веществ — катализаторов, которые участвуют в реакции, вступая в промежуточное химическое взаимодействие с реагентами, но восстанавливают свой химический состав при окончании каталитического акта. • A+B=P В присутствии катализатора К • A + K = AK • AK + B = P + K. 10 ЗАО СТК "ЦЕОСИТ"
 11 ЗАО СТК "ЦЕОСИТ"
11 ЗАО СТК "ЦЕОСИТ"
 Активность катализатора (А) – это мера ускоряющего воздействия по отношению к данному процессу 12 . ЗАО СТК "ЦЕОСИТ"
Активность катализатора (А) – это мера ускоряющего воздействия по отношению к данному процессу 12 . ЗАО СТК "ЦЕОСИТ"
 Все химические Классификация каталитических реакций - гомогенные, т. е. протекающие в однородной системе - газовой фазе или растворе - гетерогенные - те, которые происходят на поверхности раздела между веществами. - ферментативные реакции, происходящие под действием биологических катализаторов ферментов. 13 ЗАО СТК "ЦЕОСИТ"
Все химические Классификация каталитических реакций - гомогенные, т. е. протекающие в однородной системе - газовой фазе или растворе - гетерогенные - те, которые происходят на поверхности раздела между веществами. - ферментативные реакции, происходящие под действием биологических катализаторов ферментов. 13 ЗАО СТК "ЦЕОСИТ"
 катализаторы Катализатор ГИАП 14
катализаторы Катализатор ГИАП 14
 • Катализатор получают при добавке в расплав Fe 3 O 4 при температуре 1500 0 С промоторов Al 2 O 3 и K 2 O. • Al 2 O 3 - предохраняет от спекания Fe 2 O 3 и Fe O. • K 2 O– дезактивирует кислотные центры Al 2 O 3 и облегчает десорбцию NH 3 с катализатора. При реакции с азота с водородом окислы железа восстанавливаются до металлического состояния. Таким образом, синтез аммиака происходит на поверхности металлического железа. • Катализатор применяют в виде гранул размером от 2 до 10 мм, и удельной поверхностью Sуд = 10 – 20 м 2 / г. • Катализатор отравляется влагой и CO. Поэтому азото-водородную смесь очищают от паров воды и оксида углерода. 15
• Катализатор получают при добавке в расплав Fe 3 O 4 при температуре 1500 0 С промоторов Al 2 O 3 и K 2 O. • Al 2 O 3 - предохраняет от спекания Fe 2 O 3 и Fe O. • K 2 O– дезактивирует кислотные центры Al 2 O 3 и облегчает десорбцию NH 3 с катализатора. При реакции с азота с водородом окислы железа восстанавливаются до металлического состояния. Таким образом, синтез аммиака происходит на поверхности металлического железа. • Катализатор применяют в виде гранул размером от 2 до 10 мм, и удельной поверхностью Sуд = 10 – 20 м 2 / г. • Катализатор отравляется влагой и CO. Поэтому азото-водородную смесь очищают от паров воды и оксида углерода. 15
 • Из кинетического уравнения видно, что увеличения скорости реакции можно добиться : • • • С увеличением общего давления в реакторе Po скорость реакции увеличивается в степени 1, 5. Увеличением мольных долей азота и водорода за счет тщательной очистки азото – водородной смеси от углекислоты щелочью или содой. Увеличением константы скорости реакции : – С увеличением температуры логарифм константы скорости увеличивается, а следовательно константа скорости увеличивается в еще большей степени. – С понижением энергии активации Ек константа скорости существенно увеличивается. Понижение энергии активации достигается применением катализатора. • 16 В уравнении скорости реакции в знаменателе дроби присутствует мольная доля аммиака. Это говорит о том, что аммиак сильнее адсорбируется на катализаторе по сравнению с исходными азотом и водородом, поэтому уменьшает скорость химической реакции.
• Из кинетического уравнения видно, что увеличения скорости реакции можно добиться : • • • С увеличением общего давления в реакторе Po скорость реакции увеличивается в степени 1, 5. Увеличением мольных долей азота и водорода за счет тщательной очистки азото – водородной смеси от углекислоты щелочью или содой. Увеличением константы скорости реакции : – С увеличением температуры логарифм константы скорости увеличивается, а следовательно константа скорости увеличивается в еще большей степени. – С понижением энергии активации Ек константа скорости существенно увеличивается. Понижение энергии активации достигается применением катализатора. • 16 В уравнении скорости реакции в знаменателе дроби присутствует мольная доля аммиака. Это говорит о том, что аммиак сильнее адсорбируется на катализаторе по сравнению с исходными азотом и водородом, поэтому уменьшает скорость химической реакции.
 Выбор условий проведения реакции • Противоречие требований термодинамики и кинетики Температура выбирается из требований кинетики. Для повышения константы скорости до приемлимых значений необходимо повысить температуру до 420 град. С. При этом равновесие смещается налево и равновесная степень превращения ограничивается значением Xp=15% • Повышение давления способствует сдвигу равновесия в сторону образования аммиака и увеличению скорости реакции. Поэтому реакцию проводят при максимально возможном высоком давлении P=300 600 Атмосфер. Величина давления ограничивается только техническими возможностями. Выше 600 ат. резко возрастает цена аппарата. • Увеличение чистоты азото-водородной смеси выгодно как с точки зрения термодинамики , так и кинетики. Поэтому смесь тщательно очищают от CO 2 щелочью или содой. • Катализатор применяют для увеличения скорости реакции. Является чисто кинетическим фактором воздействия на реакцию. 17
Выбор условий проведения реакции • Противоречие требований термодинамики и кинетики Температура выбирается из требований кинетики. Для повышения константы скорости до приемлимых значений необходимо повысить температуру до 420 град. С. При этом равновесие смещается налево и равновесная степень превращения ограничивается значением Xp=15% • Повышение давления способствует сдвигу равновесия в сторону образования аммиака и увеличению скорости реакции. Поэтому реакцию проводят при максимально возможном высоком давлении P=300 600 Атмосфер. Величина давления ограничивается только техническими возможностями. Выше 600 ат. резко возрастает цена аппарата. • Увеличение чистоты азото-водородной смеси выгодно как с точки зрения термодинамики , так и кинетики. Поэтому смесь тщательно очищают от CO 2 щелочью или содой. • Катализатор применяют для увеличения скорости реакции. Является чисто кинетическим фактором воздействия на реакцию. 17
 Технологические приемы • • 18 Степень превращения азото-водородной смеси за один проход через ректор ограничивается равновесием и составляет 15 -20%. Поэтому применяется возврат азото-водородной смеси после выделения полученного аммиака. Реакция идет с выделением тепла, тепловой эффект 14, 2 ккал/моль или 60 к. Дж/моль. Поэтому требуется применение реакционного устройства с отводом тепла. В слой катализатора помещаются двойные трубки, играющие роль теплообменников. По трубкам проходит холодный синтез-газ, на нагрев которого расходуется тепло реакции.
Технологические приемы • • 18 Степень превращения азото-водородной смеси за один проход через ректор ограничивается равновесием и составляет 15 -20%. Поэтому применяется возврат азото-водородной смеси после выделения полученного аммиака. Реакция идет с выделением тепла, тепловой эффект 14, 2 ккал/моль или 60 к. Дж/моль. Поэтому требуется применение реакционного устройства с отводом тепла. В слой катализатора помещаются двойные трубки, играющие роль теплообменников. По трубкам проходит холодный синтез-газ, на нагрев которого расходуется тепло реакции.
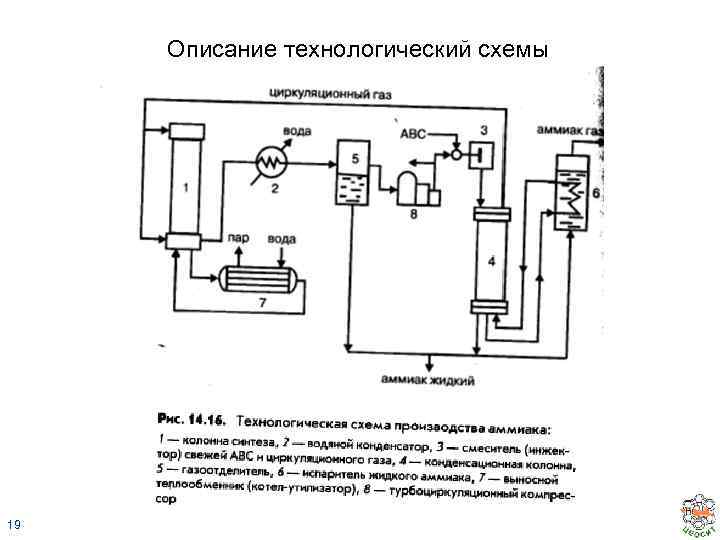 Описание технологический схемы 19
Описание технологический схемы 19


