3Производство и рафинирование алюминия.ppt
- Количество слайдов: 32
 Производство алюминия электролизом криолито-глиноземного расплава
Производство алюминия электролизом криолито-глиноземного расплава
 Производство алюминия – ведущая подотрасль цветной металлургии • по объему производства и потребления • по уровню рентабельности • по величине получаемой прибыли
Производство алюминия – ведущая подотрасль цветной металлургии • по объему производства и потребления • по уровню рентабельности • по величине получаемой прибыли
 История До конца XIX века алюминий в промышленных масштабах не производился. 1854 год Анри Сент-Клер Девиль изобрёл первый способ промышленного производства алюминия, основанный на вытеснении Аl металлическим Na из двойного хлорида натрия и алюминия Na. Cl·Al. Cl 3. В 1855 году был получен первый слиток металла массой 6— 8 кг. За 36 лет применения, с 1855 по 1890 год, способом Сент-Клер Девиля было получено 200 тонн металлического алюминия. В 1856 году он же получил алюминий электролизом расплава хлорида натрия-алюминия.
История До конца XIX века алюминий в промышленных масштабах не производился. 1854 год Анри Сент-Клер Девиль изобрёл первый способ промышленного производства алюминия, основанный на вытеснении Аl металлическим Na из двойного хлорида натрия и алюминия Na. Cl·Al. Cl 3. В 1855 году был получен первый слиток металла массой 6— 8 кг. За 36 лет применения, с 1855 по 1890 год, способом Сент-Клер Девиля было получено 200 тонн металлического алюминия. В 1856 году он же получил алюминий электролизом расплава хлорида натрия-алюминия.
 История В 1885 году, основываясь на технологии, предложенной Николаем Бекетовым, построен завод по производству алюминия в немецком городе Гмелингеме. Технология Бекетова мало чем отличалась от способа Девиля, но была проще и заключалась во взаимодействии между криолитом (Na 3 Al. F 6) и магнием. За пять лет на этом заводе было получено около 58 т алюминия — более четверти всего мирового производства металла химическим путем в период с 1854 по 1890 год.
История В 1885 году, основываясь на технологии, предложенной Николаем Бекетовым, построен завод по производству алюминия в немецком городе Гмелингеме. Технология Бекетова мало чем отличалась от способа Девиля, но была проще и заключалась во взаимодействии между криолитом (Na 3 Al. F 6) и магнием. За пять лет на этом заводе было получено около 58 т алюминия — более четверти всего мирового производства металла химическим путем в период с 1854 по 1890 год.
 История Метод, изобретённый почти одновременно Чарльзом Холлом во Франции и Полем Эру в США в 1886 году, основан на получении алюминия электролизом глинозема, растворённого в расплавленном криолите, положил начало современному способу производства алюминия. 1892 – первый завод в Швейцарии 1929 – получен первый Al в России 1932 – первый алюминиевый завод в России
История Метод, изобретённый почти одновременно Чарльзом Холлом во Франции и Полем Эру в США в 1886 году, основан на получении алюминия электролизом глинозема, растворённого в расплавленном криолите, положил начало современному способу производства алюминия. 1892 – первый завод в Швейцарии 1929 – получен первый Al в России 1932 – первый алюминиевый завод в России
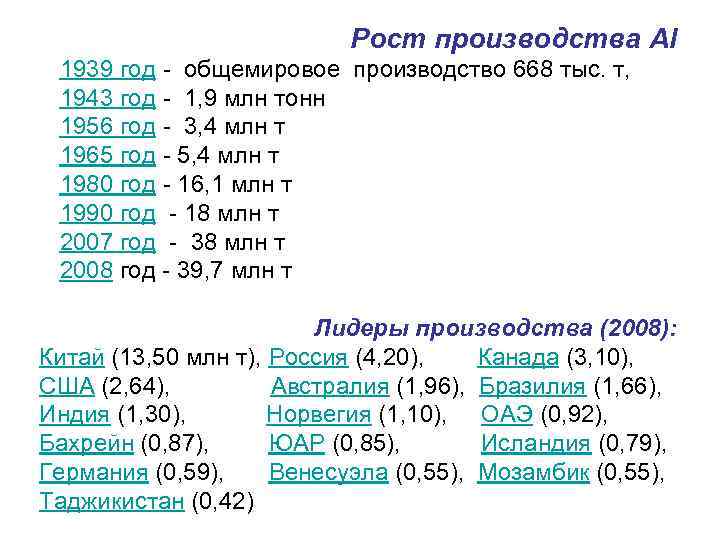 Рост производства Al 1939 год - общемировое производство 668 тыс. т, 1943 год - 1, 9 млн тонн 1956 год - 3, 4 млн т 1965 год - 5, 4 млн т 1980 год - 16, 1 млн т 1990 год - 18 млн т 2007 год - 38 млн т 2008 год - 39, 7 млн т Лидеры производства (2008): Китай (13, 50 млн т), Россия (4, 20), Канада (3, 10), США (2, 64), Австралия (1, 96), Бразилия (1, 66), Индия (1, 30), Норвегия (1, 10), ОАЭ (0, 92), Бахрейн (0, 87), ЮАР (0, 85), Исландия (0, 79), Германия (0, 59), Венесуэла (0, 55), Мозамбик (0, 55), Таджикистан (0, 42)
Рост производства Al 1939 год - общемировое производство 668 тыс. т, 1943 год - 1, 9 млн тонн 1956 год - 3, 4 млн т 1965 год - 5, 4 млн т 1980 год - 16, 1 млн т 1990 год - 18 млн т 2007 год - 38 млн т 2008 год - 39, 7 млн т Лидеры производства (2008): Китай (13, 50 млн т), Россия (4, 20), Канада (3, 10), США (2, 64), Австралия (1, 96), Бразилия (1, 66), Индия (1, 30), Норвегия (1, 10), ОАЭ (0, 92), Бахрейн (0, 87), ЮАР (0, 85), Исландия (0, 79), Германия (0, 59), Венесуэла (0, 55), Мозамбик (0, 55), Таджикистан (0, 42)
 Области применения Конструкционный материал Достоинства Al — лёгкость, податливость штамповке, коррозионная стойкость, высокая теплопроводность, нетоксичность соединений. Недостаток Al — малая прочность, поэтому его обычно сплавляют с небольшим количеством меди и магния (сплав дюралюминий).
Области применения Конструкционный материал Достоинства Al — лёгкость, податливость штамповке, коррозионная стойкость, высокая теплопроводность, нетоксичность соединений. Недостаток Al — малая прочность, поэтому его обычно сплавляют с небольшим количеством меди и магния (сплав дюралюминий).
 Области применения • Электропроводность Al всего в 1, 7 раза меньше, чем у Cu, при этом Al приблизительно в 2 раза дешевле – применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при изготовлении проводников в чипах. Недостаток - наличие прочной оксидной плёнки, затрудняющей пайку. • Аl и его сплавы сохраняют прочность при сверхнизких температурах – используется в криогенной технике. • Высокий коэффициент отражения в сочетании с дешевизной и лёгкостью напыления делает Al идеальным материалом для изготовления зеркал. • В производстве строительных материалов как газообразующий агент.
Области применения • Электропроводность Al всего в 1, 7 раза меньше, чем у Cu, при этом Al приблизительно в 2 раза дешевле – применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при изготовлении проводников в чипах. Недостаток - наличие прочной оксидной плёнки, затрудняющей пайку. • Аl и его сплавы сохраняют прочность при сверхнизких температурах – используется в криогенной технике. • Высокий коэффициент отражения в сочетании с дешевизной и лёгкостью напыления делает Al идеальным материалом для изготовления зеркал. • В производстве строительных материалов как газообразующий агент.
 Сплавы на основе Al • Al-Mg сплавы обладают высокой коррозионной стойкостью и хорошо свариваются; из них делают корпуса быстроходных судов. • Al-Mn сплавы во многом аналогичны алюминиево-магниевым. • Al-Cu сплавы ( дюралюминий) можно подвергать термообработке, что намного повышает их прочность. Но - термообработанные материалы нельзя сваривать, поэтому детали самолётов до сих пор соединяют заклёпками. Сплав с бо льшим содержанием меди по цвету внешне очень похож на золото, и его иногда применяют для имитации Au. • Al-Si сплавы (силумины) лучше всего подходят для литья. Из них часто отливают корпуса разных механизмов. • Комплексные сплавы на основе алюминия: авиаль. • Al переходит в сверхпроводящее состояние при температуре 1, 2 Кельвина.
Сплавы на основе Al • Al-Mg сплавы обладают высокой коррозионной стойкостью и хорошо свариваются; из них делают корпуса быстроходных судов. • Al-Mn сплавы во многом аналогичны алюминиево-магниевым. • Al-Cu сплавы ( дюралюминий) можно подвергать термообработке, что намного повышает их прочность. Но - термообработанные материалы нельзя сваривать, поэтому детали самолётов до сих пор соединяют заклёпками. Сплав с бо льшим содержанием меди по цвету внешне очень похож на золото, и его иногда применяют для имитации Au. • Al-Si сплавы (силумины) лучше всего подходят для литья. Из них часто отливают корпуса разных механизмов. • Комплексные сплавы на основе алюминия: авиаль. • Al переходит в сверхпроводящее состояние при температуре 1, 2 Кельвина.
 Области применения • Al - важный компонент многих сплавов: - в алюминиевых бронзах основные компоненты — медь и алюминий. - в магниевых сплавах чаще всего используется алюминий. - для спиралей в электронагревательных приборах используют фехраль (Fe, Cr, Al) • Al иногда используют в производстве бижутерии • В стекловарении используются фторид, фосфат и оксид Al • Al зарегистрирован в качестве пищевой добавки Е 173 • Al и его соединения используются в качестве ракетного горючего в двухкомпонентных ракетных топливах и в качестве горючего компонента в твёрдых ракетных топливах.
Области применения • Al - важный компонент многих сплавов: - в алюминиевых бронзах основные компоненты — медь и алюминий. - в магниевых сплавах чаще всего используется алюминий. - для спиралей в электронагревательных приборах используют фехраль (Fe, Cr, Al) • Al иногда используют в производстве бижутерии • В стекловарении используются фторид, фосфат и оксид Al • Al зарегистрирован в качестве пищевой добавки Е 173 • Al и его соединения используются в качестве ракетного горючего в двухкомпонентных ракетных топливах и в качестве горючего компонента в твёрдых ракетных топливах.
 Токсичность Al • Al отличается незначительным токсическим действием, но многие растворимые в воде неорганические соединения алюминия сохраняются в растворённом состоянии длительное время и могут оказывать вредное воздействие на человека и теплокровных животных через питьевую воду. • Наиболее ядовиты хлориды, нитраты, ацетаты, сульфаты и др. Для человека токсическое действие при попадании внутрь оказывают следующие дозы соединений алюминия (мг/кг массы тела): ацетат алюминия — 0, 2 -0, 4; гидроксид алюминия — 3, 7 -7, 3; алюминиевые квасцы — 2, 9. • В первую очередь действует на нервную систему (накапливается в нервной ткани, приводя к тяжёлым расстройствам функции ЦНС). • ПДК в воде хозяйственно-питьевого использования составляет 0, 2 мг/дм 3.
Токсичность Al • Al отличается незначительным токсическим действием, но многие растворимые в воде неорганические соединения алюминия сохраняются в растворённом состоянии длительное время и могут оказывать вредное воздействие на человека и теплокровных животных через питьевую воду. • Наиболее ядовиты хлориды, нитраты, ацетаты, сульфаты и др. Для человека токсическое действие при попадании внутрь оказывают следующие дозы соединений алюминия (мг/кг массы тела): ацетат алюминия — 0, 2 -0, 4; гидроксид алюминия — 3, 7 -7, 3; алюминиевые квасцы — 2, 9. • В первую очередь действует на нервную систему (накапливается в нервной ткани, приводя к тяжёлым расстройствам функции ЦНС). • ПДК в воде хозяйственно-питьевого использования составляет 0, 2 мг/дм 3.
 Состав электролита • Na 3 Al. F 6 – основа электролита – растворитель Al 2 O 3 • Na. F, Al. F 3 – для корректировки состава электролита • Ca. F 2, Mg. F 2 – для ↓ Тплав электролита • Na. Cl, Ba. Cl 2 – для корректировки вязкости электролита
Состав электролита • Na 3 Al. F 6 – основа электролита – растворитель Al 2 O 3 • Na. F, Al. F 3 – для корректировки состава электролита • Ca. F 2, Mg. F 2 – для ↓ Тплав электролита • Na. Cl, Ba. Cl 2 – для корректировки вязкости электролита
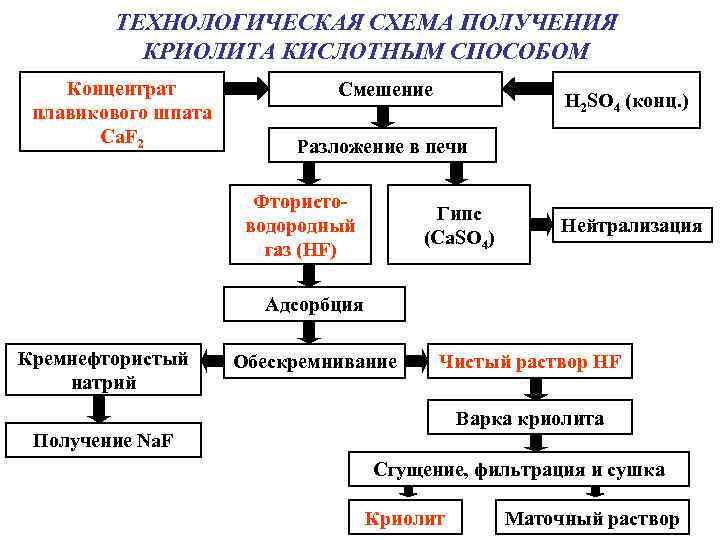 ТЕХНОЛОГИЧЕСКАЯ СХЕМА ПОЛУЧЕНИЯ КРИОЛИТА КИСЛОТНЫМ СПОСОБОМ Концентрат плавикового шпата Ca. F 2 Смешение H 2 SO 4 (конц. ) Разложение в печи Фтористоводородный газ (HF) Гипс (Ca. SO 4) Нейтрализация Адсорбция Кремнефтористый натрий Обескремнивание Чистый раствор HF Варка криолита Получение Na. F Сгущение, фильтрация и сушка Криолит Маточный раствор
ТЕХНОЛОГИЧЕСКАЯ СХЕМА ПОЛУЧЕНИЯ КРИОЛИТА КИСЛОТНЫМ СПОСОБОМ Концентрат плавикового шпата Ca. F 2 Смешение H 2 SO 4 (конц. ) Разложение в печи Фтористоводородный газ (HF) Гипс (Ca. SO 4) Нейтрализация Адсорбция Кремнефтористый натрий Обескремнивание Чистый раствор HF Варка криолита Получение Na. F Сгущение, фильтрация и сушка Криолит Маточный раствор
 КО – криолитовое отношение КО = (Na. F) / (Al. F 3) (мольн. ) КО = 3 – электролит нейтральный КО > 3 – электролит щелочной КО < 3 – электролит кислый На практике КО = 2, 5÷ 2, 8
КО – криолитовое отношение КО = (Na. F) / (Al. F 3) (мольн. ) КО = 3 – электролит нейтральный КО > 3 – электролит щелочной КО < 3 – электролит кислый На практике КО = 2, 5÷ 2, 8
 Разновидности электролизеров • По типу анодов - обожженные - непрерывно самообжигающиеся • По принципу токоподвода - с верхним токоподводом - с боковым токоподводом • По рабочей мощности - малой мощности (100 -130 к. А) - средней мощности (150 -175 к. А) - большой мощности (255 -500 к. А)
Разновидности электролизеров • По типу анодов - обожженные - непрерывно самообжигающиеся • По принципу токоподвода - с верхним токоподводом - с боковым токоподводом • По рабочей мощности - малой мощности (100 -130 к. А) - средней мощности (150 -175 к. А) - большой мощности (255 -500 к. А)
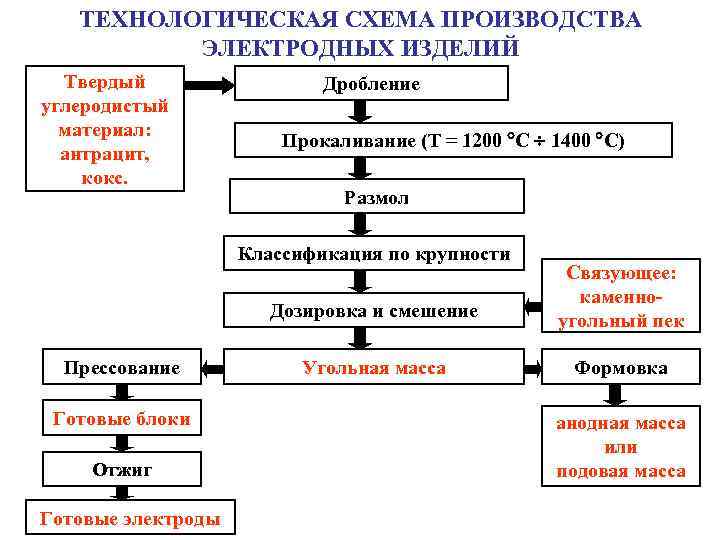 ТЕХНОЛОГИЧЕСКАЯ СХЕМА ПРОИЗВОДСТВА ЭЛЕКТРОДНЫХ ИЗДЕЛИЙ Твердый углеродистый материал: антрацит, кокс. Дробление Прокаливание (Т = 1200 С 1400 С) Размол Классификация по крупности Дозировка и смешение Прессование Готовые блоки Отжиг Готовые электроды Связующее: каменноугольный пек Угольная масса Формовка анодная масса или подовая масса
ТЕХНОЛОГИЧЕСКАЯ СХЕМА ПРОИЗВОДСТВА ЭЛЕКТРОДНЫХ ИЗДЕЛИЙ Твердый углеродистый материал: антрацит, кокс. Дробление Прокаливание (Т = 1200 С 1400 С) Размол Классификация по крупности Дозировка и смешение Прессование Готовые блоки Отжиг Готовые электроды Связующее: каменноугольный пек Угольная масса Формовка анодная масса или подовая масса
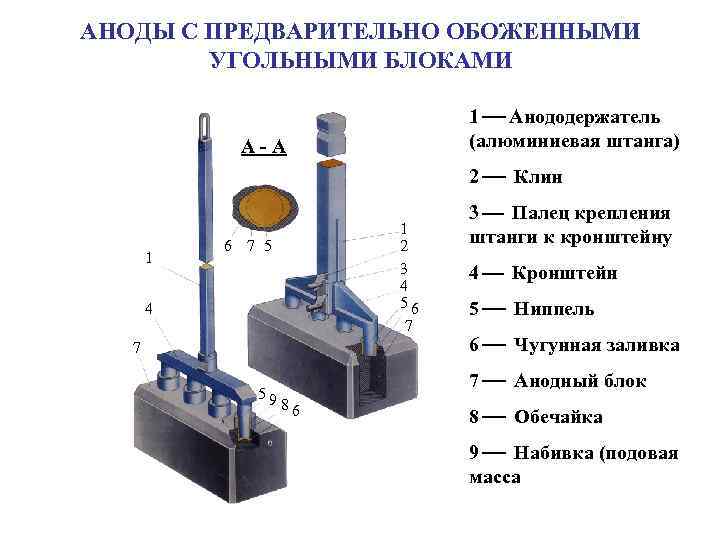 АНОДЫ С ПРЕДВАРИТЕЛЬНО ОБОЖЕННЫМИ УГОЛЬНЫМИ БЛОКАМИ 1 Анододержатель (алюминиевая штанга) А-А 2 Клин 1 1 2 3 4 56 7 5 4 7 59 3 Палец крепления штанги к кронштейну 4 Кронштейн 5 Ниппель 6 Чугунная заливка 7 Анодный блок 86 8 Обечайка 9 Набивка (подовая масса
АНОДЫ С ПРЕДВАРИТЕЛЬНО ОБОЖЕННЫМИ УГОЛЬНЫМИ БЛОКАМИ 1 Анододержатель (алюминиевая штанга) А-А 2 Клин 1 1 2 3 4 56 7 5 4 7 59 3 Палец крепления штанги к кронштейну 4 Кронштейн 5 Ниппель 6 Чугунная заливка 7 Анодный блок 86 8 Обечайка 9 Набивка (подовая масса
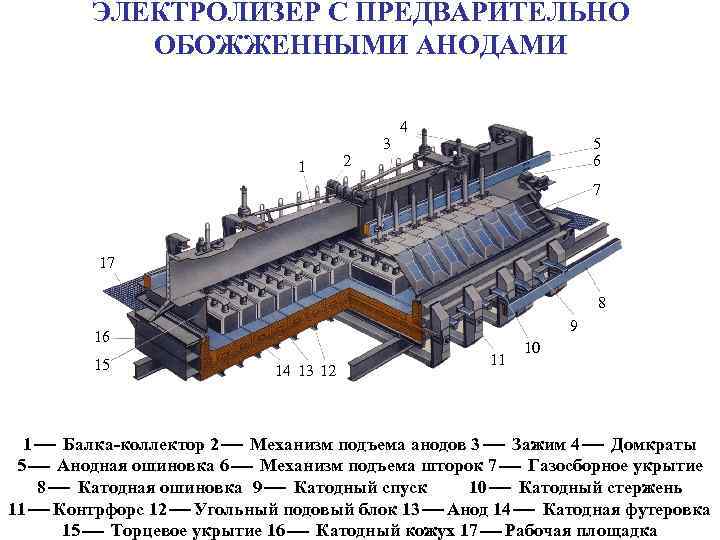 ЭЛЕКТРОЛИЗЕР С ПРЕДВАРИТЕЛЬНО ОБОЖЖЕННЫМИ АНОДАМИ 1 2 3 4 5 6 7 17 8 9 16 15 14 13 12 11 10 1 Балка-коллектор 2 Механизм подъема анодов 3 Зажим 4 Домкраты 5 Анодная ошиновка 6 Механизм подъема шторок 7 Газосборное укрытие 8 Катодная ошиновка 9 Катодный спуск 10 Катодный стержень 11 Контрфорс 12 Угольный подовый блок 13 Анод 14 Катодная футеровка 15 Торцевое укрытие 16 Катодный кожух 17 Рабочая площадка
ЭЛЕКТРОЛИЗЕР С ПРЕДВАРИТЕЛЬНО ОБОЖЖЕННЫМИ АНОДАМИ 1 2 3 4 5 6 7 17 8 9 16 15 14 13 12 11 10 1 Балка-коллектор 2 Механизм подъема анодов 3 Зажим 4 Домкраты 5 Анодная ошиновка 6 Механизм подъема шторок 7 Газосборное укрытие 8 Катодная ошиновка 9 Катодный спуск 10 Катодный стержень 11 Контрфорс 12 Угольный подовый блок 13 Анод 14 Катодная футеровка 15 Торцевое укрытие 16 Катодный кожух 17 Рабочая площадка
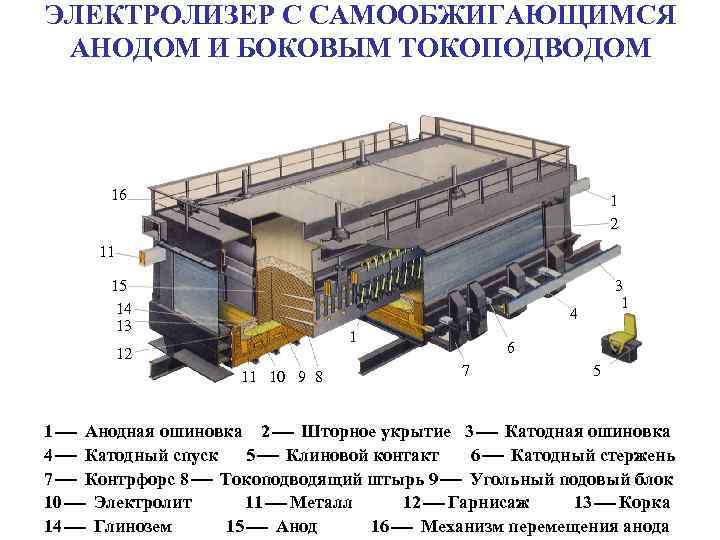 ЭЛЕКТРОЛИЗЕР С САМООБЖИГАЮЩИМСЯ АНОДОМ И БОКОВЫМ ТОКОПОДВОДОМ 16 1 2 11 15 14 13 3 1 4 1 12 11 10 9 8 6 7 5 1 Анодная ошиновка 2 Шторное укрытие 3 Катодная ошиновка 4 Катодный спуск 5 Клиновой контакт 6 Катодный стержень 7 Контрфорс 8 Токоподводящий штырь 9 Угольный подовый блок 10 Электролит 11 Металл 12 Гарнисаж 13 Корка 14 Глинозем 15 Анод 16 Механизм перемещения анода
ЭЛЕКТРОЛИЗЕР С САМООБЖИГАЮЩИМСЯ АНОДОМ И БОКОВЫМ ТОКОПОДВОДОМ 16 1 2 11 15 14 13 3 1 4 1 12 11 10 9 8 6 7 5 1 Анодная ошиновка 2 Шторное укрытие 3 Катодная ошиновка 4 Катодный спуск 5 Клиновой контакт 6 Катодный стержень 7 Контрфорс 8 Токоподводящий штырь 9 Угольный подовый блок 10 Электролит 11 Металл 12 Гарнисаж 13 Корка 14 Глинозем 15 Анод 16 Механизм перемещения анода
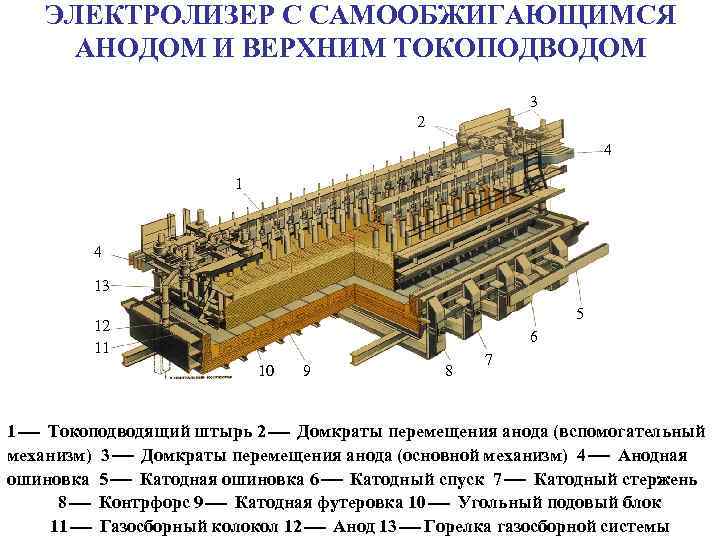 ЭЛЕКТРОЛИЗЕР С САМООБЖИГАЮЩИМСЯ АНОДОМ И ВЕРХНИМ ТОКОПОДВОДОМ 3 2 4 13 5 12 11 6 10 9 8 7 1 Токоподводящий штырь 2 Домкраты перемещения анода (вспомогательный механизм) 3 Домкраты перемещения анода (основной механизм) 4 Анодная ошиновка 5 Катодная ошиновка 6 Катодный спуск 7 Катодный стержень 8 Контрфорс 9 Катодная футеровка 10 Угольный подовый блок 11 Газосборный колокол 12 Анод 13 Горелка газосборной системы
ЭЛЕКТРОЛИЗЕР С САМООБЖИГАЮЩИМСЯ АНОДОМ И ВЕРХНИМ ТОКОПОДВОДОМ 3 2 4 13 5 12 11 6 10 9 8 7 1 Токоподводящий штырь 2 Домкраты перемещения анода (вспомогательный механизм) 3 Домкраты перемещения анода (основной механизм) 4 Анодная ошиновка 5 Катодная ошиновка 6 Катодный спуск 7 Катодный стержень 8 Контрфорс 9 Катодная футеровка 10 Угольный подовый блок 11 Газосборный колокол 12 Анод 13 Горелка газосборной системы
 Химизм процесса Растворение глинозема в электролите Na 3 ALF 6 + Al 2 O 3 = 3 Na. Al. OF 2 Диссоциация Na. Al. OF 2 = Na+ + Al. OF 2 Реакции на электродах K: 2 Al 3+ + 6ē = 2 Alo А: 3 O 2 - - 6ē = 1, 5 O 2 + C → CO + CO 2 Суммарная химическая реакция 2 Al 2 O 3 + 3 С = 4 Al + 3 CO 2 Al 2 O 3 + 3 С = 2 Al + 3 CO
Химизм процесса Растворение глинозема в электролите Na 3 ALF 6 + Al 2 O 3 = 3 Na. Al. OF 2 Диссоциация Na. Al. OF 2 = Na+ + Al. OF 2 Реакции на электродах K: 2 Al 3+ + 6ē = 2 Alo А: 3 O 2 - - 6ē = 1, 5 O 2 + C → CO + CO 2 Суммарная химическая реакция 2 Al 2 O 3 + 3 С = 4 Al + 3 CO 2 Al 2 O 3 + 3 С = 2 Al + 3 CO
 Основные показатели процесса Выход по току Масса теоретическая Электрохимический эквивалент , г/А час , к. Вт час/т Удельный расход энергии , к. Вт час/т
Основные показатели процесса Выход по току Масса теоретическая Электрохимический эквивалент , г/А час , к. Вт час/т Удельный расход энергии , к. Вт час/т
 Основные показатели процесса • • Выход по току 88÷ 90 % Удельный расход энергии 13900 к. Вт*час/т Al Uраб= 4 ÷ 4, 5 В Q= 550 ÷ 1200 кг/сутки • к. Al = 0, 3355 г/А*час
Основные показатели процесса • • Выход по току 88÷ 90 % Удельный расход энергии 13900 к. Вт*час/т Al Uраб= 4 ÷ 4, 5 В Q= 550 ÷ 1200 кг/сутки • к. Al = 0, 3355 г/А*час
 Факторы, влияющие на показатели процесса • Плотность тока iа > iк iа = 0, 7÷ 1, 0 А/см 2 • Состав электролита КО = 2, 5 ÷ 2, 8 содержание Al 2 O 3 = 4 ÷ 8 % • Температура электролиза Т = 930 ÷ 960 о. С • Межполюсное расстояние L = 3 ÷ 5 см
Факторы, влияющие на показатели процесса • Плотность тока iа > iк iа = 0, 7÷ 1, 0 А/см 2 • Состав электролита КО = 2, 5 ÷ 2, 8 содержание Al 2 O 3 = 4 ÷ 8 % • Температура электролиза Т = 930 ÷ 960 о. С • Межполюсное расстояние L = 3 ÷ 5 см
 Анодный эффект Признаки • Повышение напряжения • Искровой разряд • Несмачиваемость анода • Изменение состава анодных газов Причина Обеднение электролита глиноземом
Анодный эффект Признаки • Повышение напряжения • Искровой разряд • Несмачиваемость анода • Изменение состава анодных газов Причина Обеднение электролита глиноземом
 Качество алюминия • Первичный алюминий - сырец А 85, А 8, А 7 Е, А 7 Э, А 6, А 5 Е, А 0 • Алюминий высокой чистоты (АВЧ) А 995, А 99, А 97, А 95 • Алюминий особой чистоты (АОЧ) А 999 – 99, 999% Al
Качество алюминия • Первичный алюминий - сырец А 85, А 8, А 7 Е, А 7 Э, А 6, А 5 Е, А 0 • Алюминий высокой чистоты (АВЧ) А 995, А 99, А 97, А 95 • Алюминий особой чистоты (АОЧ) А 999 – 99, 999% Al
 Примесей в первичном Al • Неметаллические • Механические • Металлические • Газообразные
Примесей в первичном Al • Неметаллические • Механические • Металлические • Газообразные
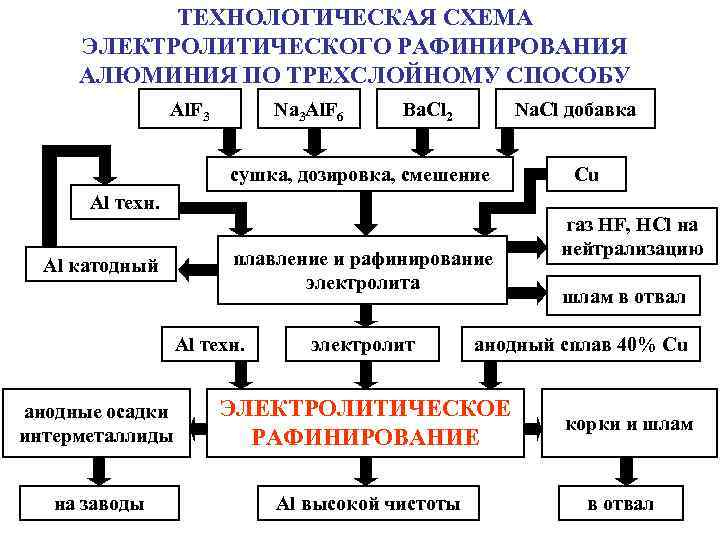 ТЕХНОЛОГИЧЕСКАЯ СХЕМА ЭЛЕКТРОЛИТИЧЕСКОГО РАФИНИРОВАНИЯ АЛЮМИНИЯ ПО ТРЕХСЛОЙНОМУ СПОСОБУ Al. F 3 Na 3 Al. F 6 Ba. Cl 2 Na. Cl добавка сушка, дозировка, смешение Al техн. Al катодный плавление и рафинирование электролита Al техн. электролит Cu газ HF, HCl на нейтрализацию шлам в отвал анодный сплав 40% Cu анодные осадки интерметаллиды ЭЛЕКТРОЛИТИЧЕСКОЕ РАФИНИРОВАНИЕ на заводы Al высокой чистоты корки и шлам в отвал
ТЕХНОЛОГИЧЕСКАЯ СХЕМА ЭЛЕКТРОЛИТИЧЕСКОГО РАФИНИРОВАНИЯ АЛЮМИНИЯ ПО ТРЕХСЛОЙНОМУ СПОСОБУ Al. F 3 Na 3 Al. F 6 Ba. Cl 2 Na. Cl добавка сушка, дозировка, смешение Al техн. Al катодный плавление и рафинирование электролита Al техн. электролит Cu газ HF, HCl на нейтрализацию шлам в отвал анодный сплав 40% Cu анодные осадки интерметаллиды ЭЛЕКТРОЛИТИЧЕСКОЕ РАФИНИРОВАНИЕ на заводы Al высокой чистоты корки и шлам в отвал
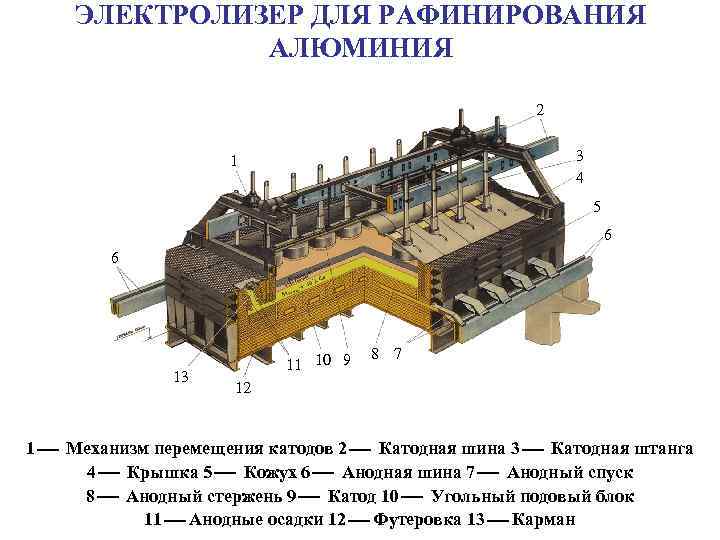 ЭЛЕКТРОЛИЗЕР ДЛЯ РАФИНИРОВАНИЯ АЛЮМИНИЯ 2 3 4 1 5 6 6 13 11 10 9 8 7 12 1 Механизм перемещения катодов 2 Катодная шина 3 Катодная штанга 4 Крышка 5 Кожух 6 Анодная шина 7 Анодный спуск 8 Анодный стержень 9 Катод 10 Угольный подовый блок 11 Анодные осадки 12 Футеровка 13 Карман
ЭЛЕКТРОЛИЗЕР ДЛЯ РАФИНИРОВАНИЯ АЛЮМИНИЯ 2 3 4 1 5 6 6 13 11 10 9 8 7 12 1 Механизм перемещения катодов 2 Катодная шина 3 Катодная штанга 4 Крышка 5 Кожух 6 Анодная шина 7 Анодный спуск 8 Анодный стержень 9 Катод 10 Угольный подовый блок 11 Анодные осадки 12 Футеровка 13 Карман
 Состав электролита • Na 3 Al. F 6 – основа электролита (40÷ 45%) • Na. F, Al. F 3 – для корректировки состава электролита (КО=1, 5÷ 2, 2) • Ba. Cl 2 - для увеличения плотности электролита (55÷ 60%) • Na. Cl – для увеличения электропроводности электролита (2÷ 4%)
Состав электролита • Na 3 Al. F 6 – основа электролита (40÷ 45%) • Na. F, Al. F 3 – для корректировки состава электролита (КО=1, 5÷ 2, 2) • Ba. Cl 2 - для увеличения плотности электролита (55÷ 60%) • Na. Cl – для увеличения электропроводности электролита (2÷ 4%)
 Состав анодного сплава Alпервичный+ 30÷ 40 % Cu Реакции на электродах А: Alо - 3ē = Al 3+ K: Al 3+ + 3ē = Alo Примеси • В электролите – Na, K, Ca, Mg, Ti • В анодном сплаве – интерметаллиды (Al-Cu-Fe-Si-Ga)
Состав анодного сплава Alпервичный+ 30÷ 40 % Cu Реакции на электродах А: Alо - 3ē = Al 3+ K: Al 3+ + 3ē = Alo Примеси • В электролите – Na, K, Ca, Mg, Ti • В анодном сплаве – интерметаллиды (Al-Cu-Fe-Si-Ga)
 Основные показатели процесса • Выход по току 95÷ 97 % • Удельный расход энергии 18000 к. Вт*час/т Al • • Uраб= 5, 5 ÷ 6, 0 В Т = 750÷ 810 о. С i = 0, 5 ÷ 0, 6 А/см 2 L = 11÷ 13 см
Основные показатели процесса • Выход по току 95÷ 97 % • Удельный расход энергии 18000 к. Вт*час/т Al • • Uраб= 5, 5 ÷ 6, 0 В Т = 750÷ 810 о. С i = 0, 5 ÷ 0, 6 А/см 2 L = 11÷ 13 см


