8. пр.фурана- для заоч. 9 сем..ppt
- Количество слайдов: 63
 Производные фурана 1
Производные фурана 1
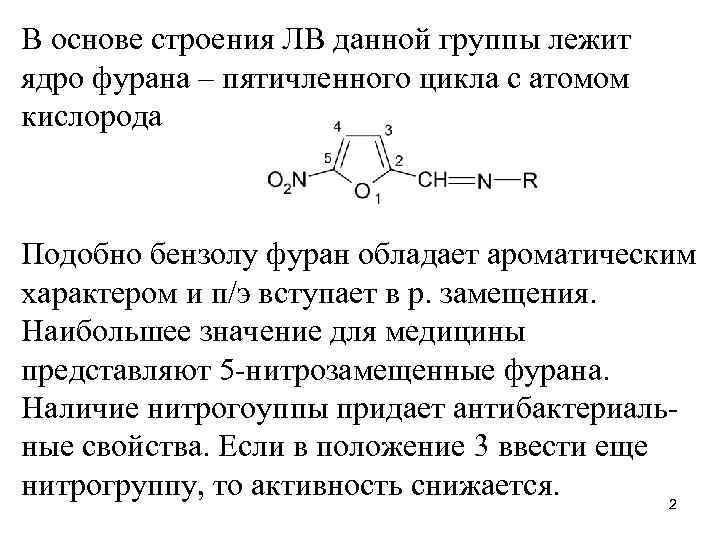 В основе строения ЛВ данной группы лежит ядро фурана – пятичленного цикла с атомом кислорода Подобно бензолу фуран обладает ароматическим характером и п/э вступает в р. замещения. Наибольшее значение для медицины представляют 5 -нитрозамещенные фурана. Наличие нитрогоуппы придает антибактериальные свойства. Если в положение 3 ввести еще нитрогруппу, то активность снижается. 2
В основе строения ЛВ данной группы лежит ядро фурана – пятичленного цикла с атомом кислорода Подобно бензолу фуран обладает ароматическим характером и п/э вступает в р. замещения. Наибольшее значение для медицины представляют 5 -нитрозамещенные фурана. Наличие нитрогоуппы придает антибактериальные свойства. Если в положение 3 ввести еще нитрогруппу, то активность снижается. 2
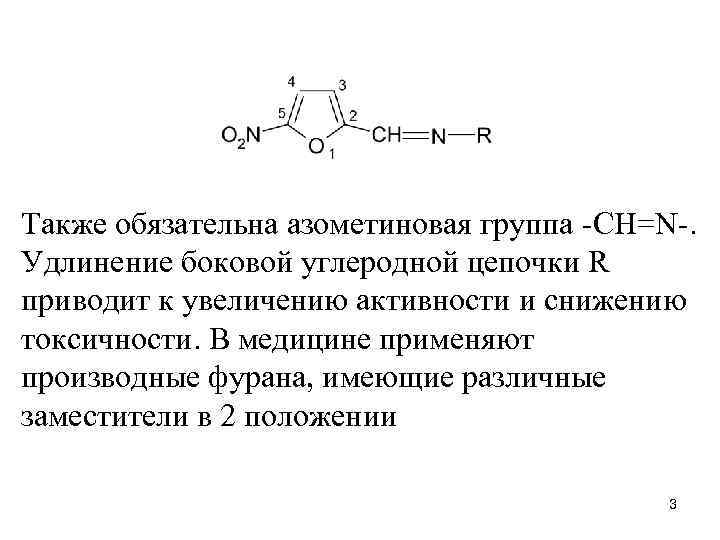 Также обязательна азометиновая группа -CH=N-. Удлинение боковой углеродной цепочки R приводит к увеличению активности и снижению токсичности. В медицине применяют производные фурана, имеющие различные заместители в 2 положении 3
Также обязательна азометиновая группа -CH=N-. Удлинение боковой углеродной цепочки R приводит к увеличению активности и снижению токсичности. В медицине применяют производные фурана, имеющие различные заместители в 2 положении 3
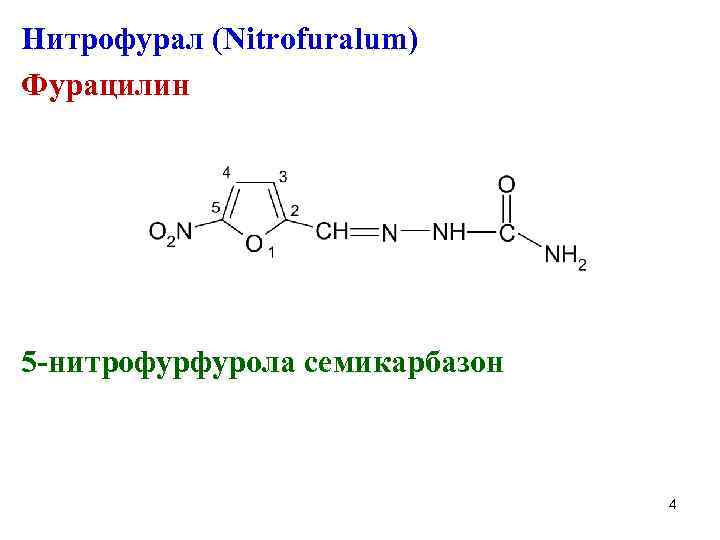 Нитрофурал (Nitrofuralum) Фурацилин 5 -нитрофурфурола семикарбазон 4
Нитрофурал (Nitrofuralum) Фурацилин 5 -нитрофурфурола семикарбазон 4
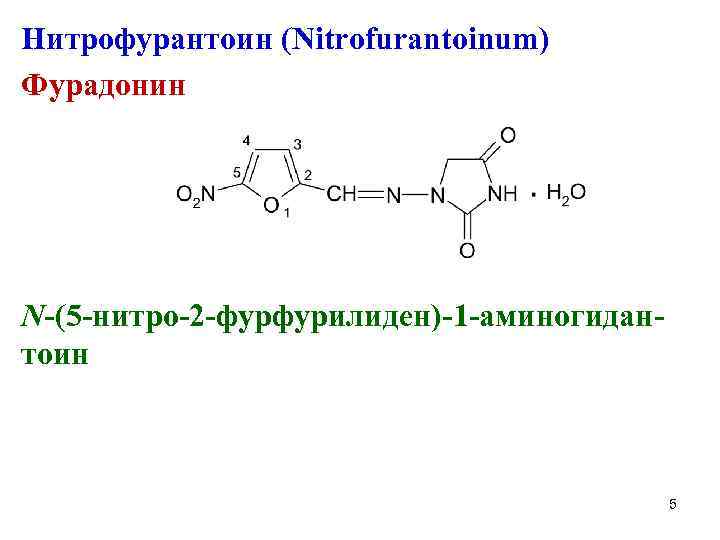 Нитрофурантоин (Nitrofurantoinum) Фурадонин N-(5 -нитро-2 -фурфурилиден)-1 -аминогидантоин 5
Нитрофурантоин (Nitrofurantoinum) Фурадонин N-(5 -нитро-2 -фурфурилиден)-1 -аминогидантоин 5
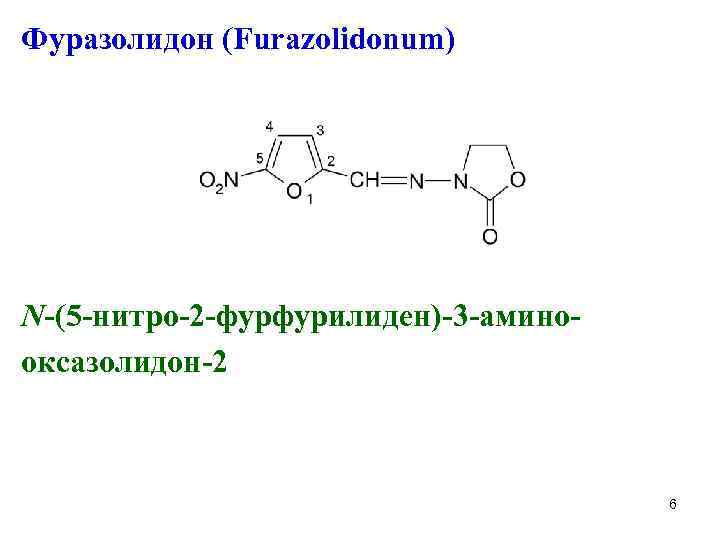 Фуразолидон (Furazolidonum) N-(5 -нитро-2 -фурфурилиден)-3 -аминооксазолидон-2 6
Фуразолидон (Furazolidonum) N-(5 -нитро-2 -фурфурилиден)-3 -аминооксазолидон-2 6
![Фуразидин (Furazidinum) Фурагин 1 -[3 -(5 -нитро-2 -фурил)аллилиденамино]гидантоин 7 Фуразидин (Furazidinum) Фурагин 1 -[3 -(5 -нитро-2 -фурил)аллилиденамино]гидантоин 7](https://present5.com/presentation/45652853_429696002/image-7.jpg) Фуразидин (Furazidinum) Фурагин 1 -[3 -(5 -нитро-2 -фурил)аллилиденамино]гидантоин 7
Фуразидин (Furazidinum) Фурагин 1 -[3 -(5 -нитро-2 -фурил)аллилиденамино]гидантоин 7
 Это желтые с зеленоватым (нитрофурал, нитрофрантоин, фуразолидон) или оранжевым оттенком (фуразидин) кристаллические вещества, без запаха, горького вкуса, о. м. р. воде и спирте. Ввиду наличия нитро и амидной групп нитрофурал имеет в растворах кислую реакцию и лучше других растворяется в щелочах Фуразидин растворимый содержит 10% калиевой соли фуразидина и 90% Na. Cl 8
Это желтые с зеленоватым (нитрофурал, нитрофрантоин, фуразолидон) или оранжевым оттенком (фуразидин) кристаллические вещества, без запаха, горького вкуса, о. м. р. воде и спирте. Ввиду наличия нитро и амидной групп нитрофурал имеет в растворах кислую реакцию и лучше других растворяется в щелочах Фуразидин растворимый содержит 10% калиевой соли фуразидина и 90% Na. Cl 8
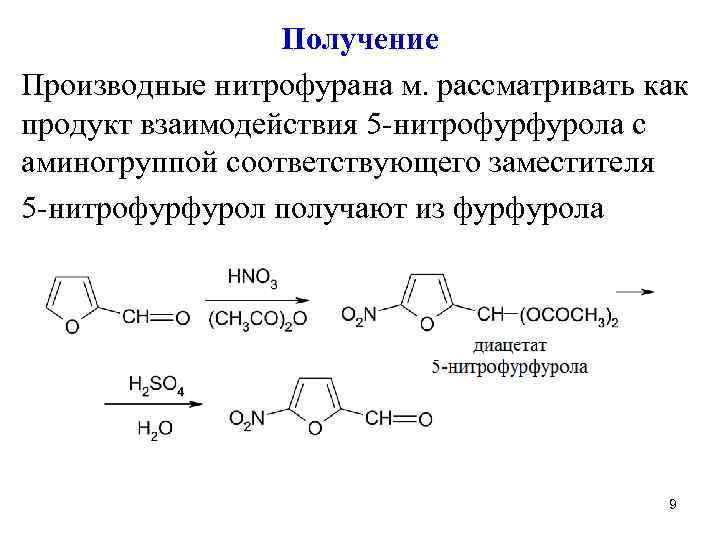 Получение Производные нитрофурана м. рассматривать как продукт взаимодействия 5 -нитрофурфурола с аминогруппой соответствующего заместителя 5 -нитрофурфурол получают из фурфурола 9
Получение Производные нитрофурана м. рассматривать как продукт взаимодействия 5 -нитрофурфурола с аминогруппой соответствующего заместителя 5 -нитрофурфурол получают из фурфурола 9
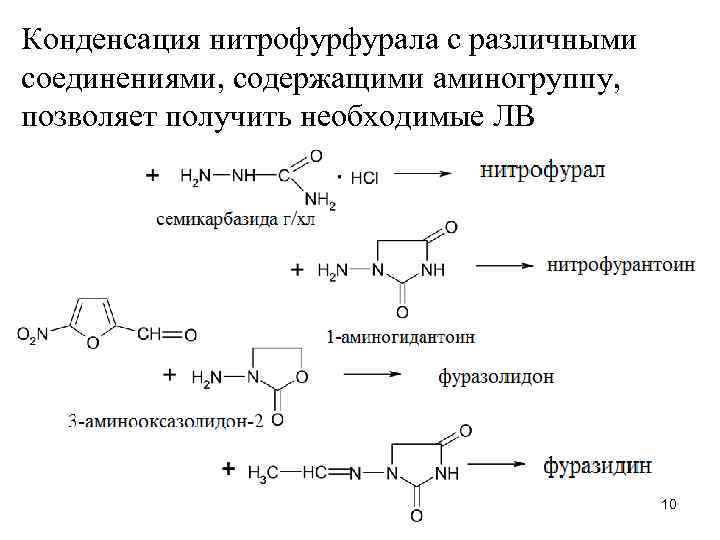 Конденсация нитрофурфурала с различными соединениями, содержащими аминогруппу, позволяет получить необходимые ЛВ 10
Конденсация нитрофурфурала с различными соединениями, содержащими аминогруппу, позволяет получить необходимые ЛВ 10
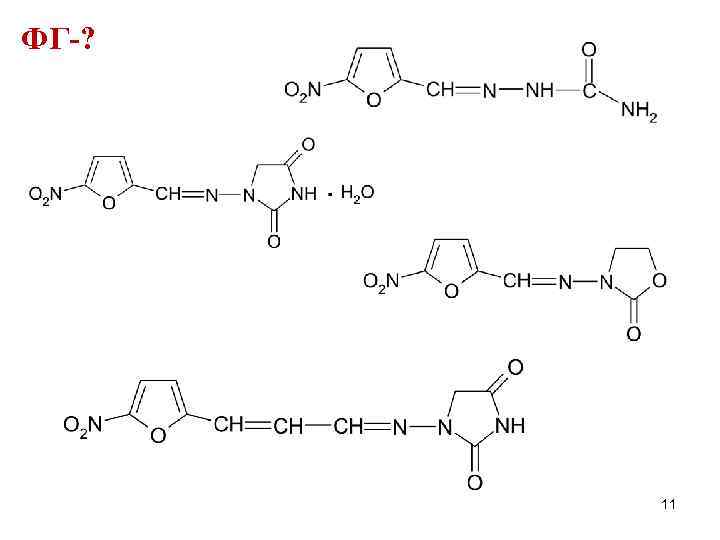 ФГ-? 11
ФГ-? 11
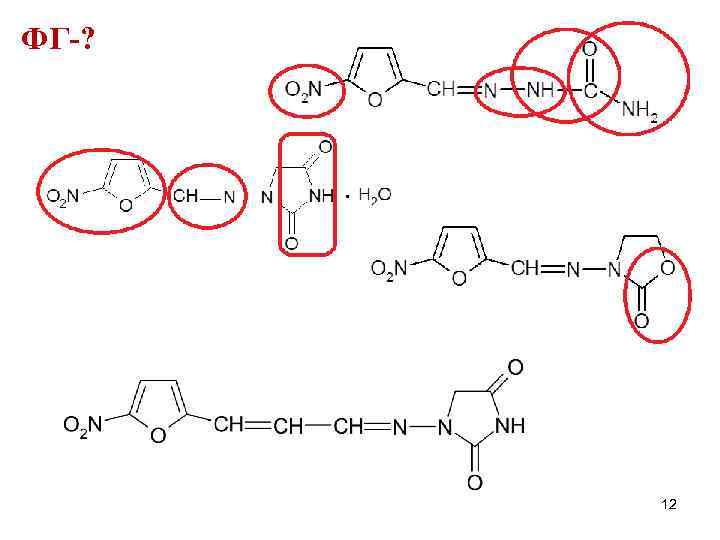 ФГ-? 12
ФГ-? 12
 ФГ ядро нитофурана нитрогруппа азометиновая группа -CH=Nамидные группы (замещ-я и незамещ-я) гидразиновая связь =N-NHимидная группа -СO-NH-CO- у нитрофурантоина и фуразидина сложноэфирная группа в лактамном кольце фуразолидона 13
ФГ ядро нитофурана нитрогруппа азометиновая группа -CH=Nамидные группы (замещ-я и незамещ-я) гидразиновая связь =N-NHимидная группа -СO-NH-CO- у нитрофурантоина и фуразидина сложноэфирная группа в лактамном кольце фуразолидона 13
 Качественный анализ 1. Определяют Т плавления (нитрофурантоин и фуразолидон плавятся с разложением) 2. СПФ в УФ- и видимой области спектра (NO 2 -гр. , двойные связи – наличие сопряженных связей в структуре данных ЛВ обуславливает их окраску) 3. ИК-спектроскопия 14
Качественный анализ 1. Определяют Т плавления (нитрофурантоин и фуразолидон плавятся с разложением) 2. СПФ в УФ- и видимой области спектра (NO 2 -гр. , двойные связи – наличие сопряженных связей в структуре данных ЛВ обуславливает их окраску) 3. ИК-спектроскопия 14
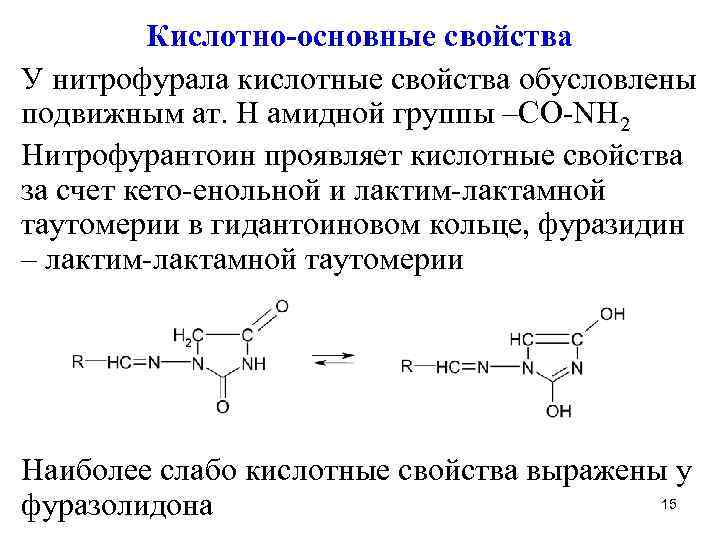 Кислотно-основные свойства У нитрофурала кислотные свойства обусловлены подвижным ат. H амидной группы –CO-NH 2 Нитрофурантоин проявляет кислотные свойства за счет кето-енольной и лактим-лактамной таутомерии в гидантоиновом кольце, фуразидин – лактим-лактамной таутомерии Наиболее слабо кислотные свойства выражены у 15 фуразолидона
Кислотно-основные свойства У нитрофурала кислотные свойства обусловлены подвижным ат. H амидной группы –CO-NH 2 Нитрофурантоин проявляет кислотные свойства за счет кето-енольной и лактим-лактамной таутомерии в гидантоиновом кольце, фуразидин – лактим-лактамной таутомерии Наиболее слабо кислотные свойства выражены у 15 фуразолидона
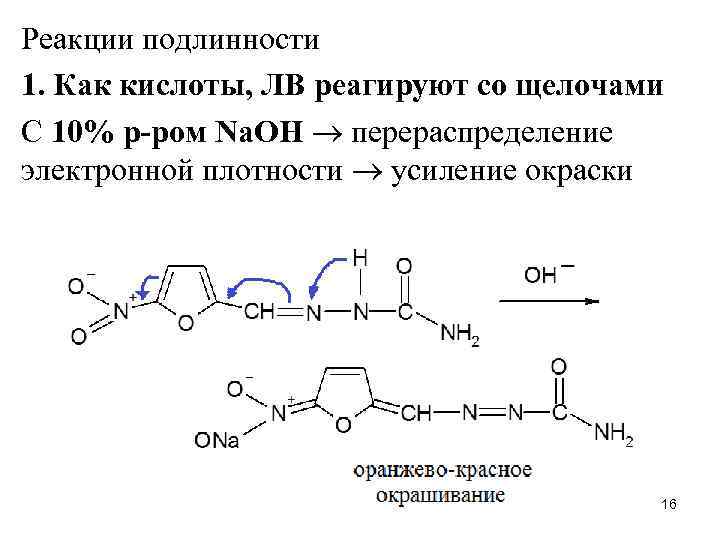 Реакции подлинности 1. Как кислоты, ЛВ реагируют со щелочами С 10% р-ром Na. OH перераспределение электронной плотности усиление окраски 16
Реакции подлинности 1. Как кислоты, ЛВ реагируют со щелочами С 10% р-ром Na. OH перераспределение электронной плотности усиление окраски 16
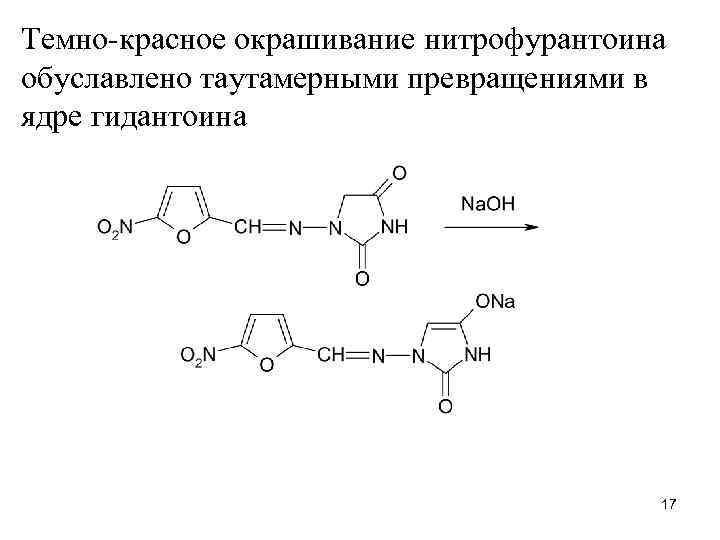 Темно-красное окрашивание нитрофурантоина обуславлено таутамерными превращениями в ядре гидантоина 17
Темно-красное окрашивание нитрофурантоина обуславлено таутамерными превращениями в ядре гидантоина 17
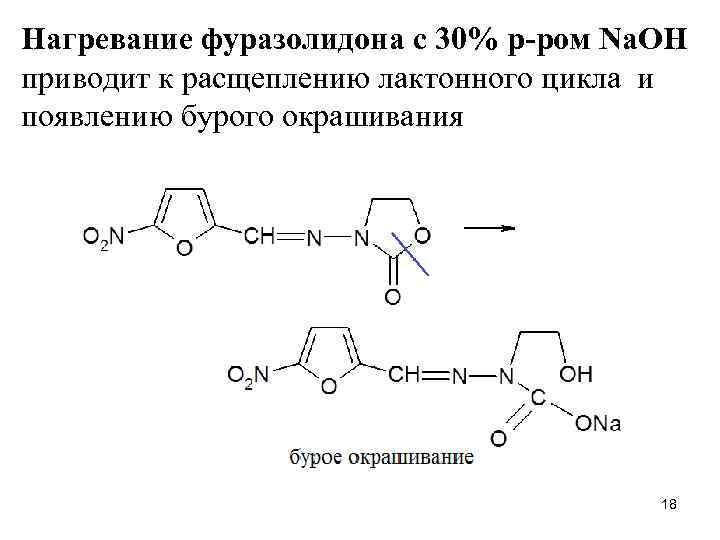 Нагревание фуразолидона с 30% р-ром Na. OH приводит к расщеплению лактонного цикла и появлению бурого окрашивания 18
Нагревание фуразолидона с 30% р-ром Na. OH приводит к расщеплению лактонного цикла и появлению бурого окрашивания 18
 2. За счет кислотных свойств все пр-ные фурана растворяются в протофильных растворителях (пиридин, ДМФА), образуя окрашенные анионы, которые с катионами щелочных металлов образуют соли различной окраски Нитрофурантоин + ДМФА + сп. р-р KOH коричнево-желтое окрашивание Фуразолидон + ДМФА + сп. р-р KOH фиолетовое окрашивание 19
2. За счет кислотных свойств все пр-ные фурана растворяются в протофильных растворителях (пиридин, ДМФА), образуя окрашенные анионы, которые с катионами щелочных металлов образуют соли различной окраски Нитрофурантоин + ДМФА + сп. р-р KOH коричнево-желтое окрашивание Фуразолидон + ДМФА + сп. р-р KOH фиолетовое окрашивание 19
 Отличить производные нитрофурана друг от друга можно по окраске со спиртовым раствором KOH в сочетании с ацетоном нитрофурал темно-красное окрашивание нитрофурантоин зеленовато-желтое, переходящее в бурое, затем в бурый осадок фуразолидон постепенно появляющееся красное окрашивание, переходящее в бурое фуразидин красное окрашивание, затем красный осадок 20
Отличить производные нитрофурана друг от друга можно по окраске со спиртовым раствором KOH в сочетании с ацетоном нитрофурал темно-красное окрашивание нитрофурантоин зеленовато-желтое, переходящее в бурое, затем в бурый осадок фуразолидон постепенно появляющееся красное окрашивание, переходящее в бурое фуразидин красное окрашивание, затем красный осадок 20
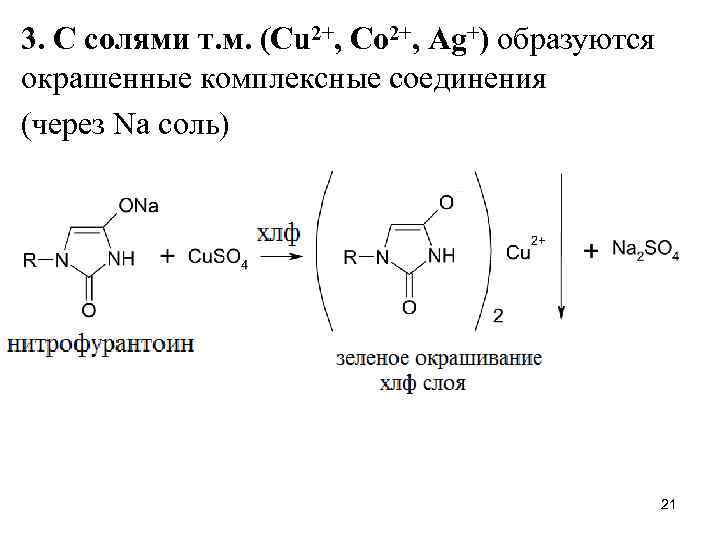 3. С солями т. м. (Cu 2+, Co 2+, Ag+) образуются окрашенные комплексные соединения (через Na соль) 21
3. С солями т. м. (Cu 2+, Co 2+, Ag+) образуются окрашенные комплексные соединения (через Na соль) 21
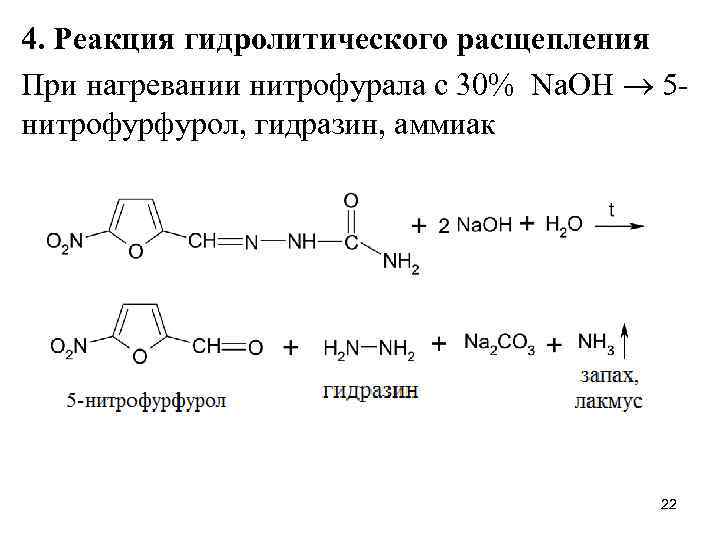 4. Реакция гидролитического расщепления При нагревании нитрофурала с 30% Na. OH 5 нитрофурфурол, гидразин, аммиак 22
4. Реакция гидролитического расщепления При нагревании нитрофурала с 30% Na. OH 5 нитрофурфурол, гидразин, аммиак 22
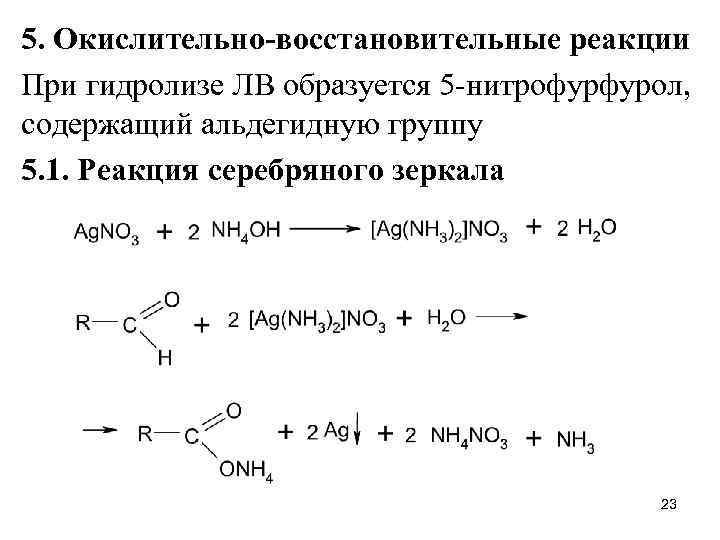 5. Окислительно-восстановительные реакции При гидролизе ЛВ образуется 5 -нитрофурфурол, содержащий альдегидную группу 5. 1. Реакция серебряного зеркала 23
5. Окислительно-восстановительные реакции При гидролизе ЛВ образуется 5 -нитрофурфурол, содержащий альдегидную группу 5. 1. Реакция серебряного зеркала 23
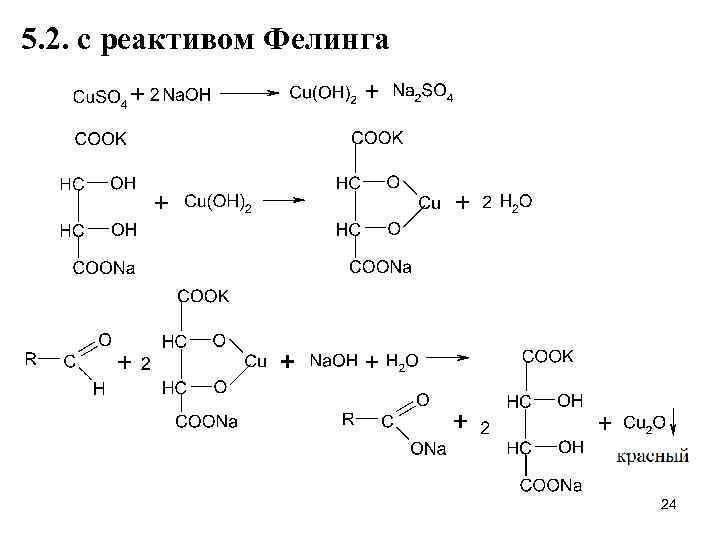 5. 2. с реактивом Фелинга 24
5. 2. с реактивом Фелинга 24
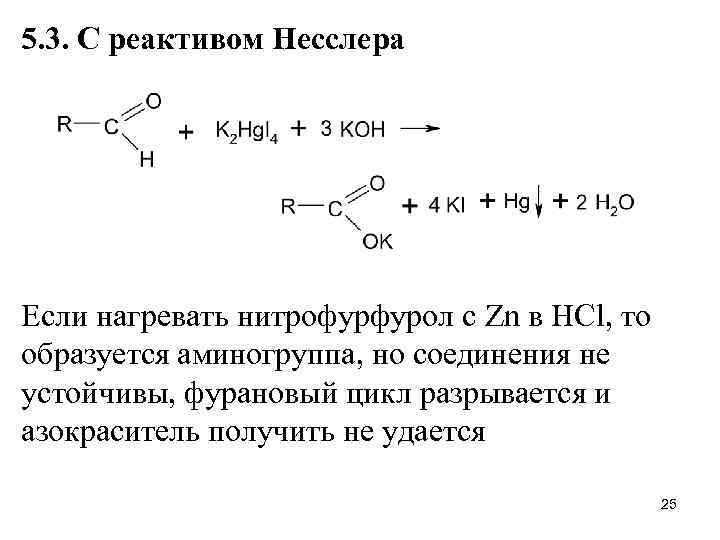 5. 3. С реактивом Несслера Если нагревать нитрофурфурол с Zn в HCl, то образуется аминогруппа, но соединения не устойчивы, фурановый цикл разрывается и азокраситель получить не удается 25
5. 3. С реактивом Несслера Если нагревать нитрофурфурол с Zn в HCl, то образуется аминогруппа, но соединения не устойчивы, фурановый цикл разрывается и азокраситель получить не удается 25
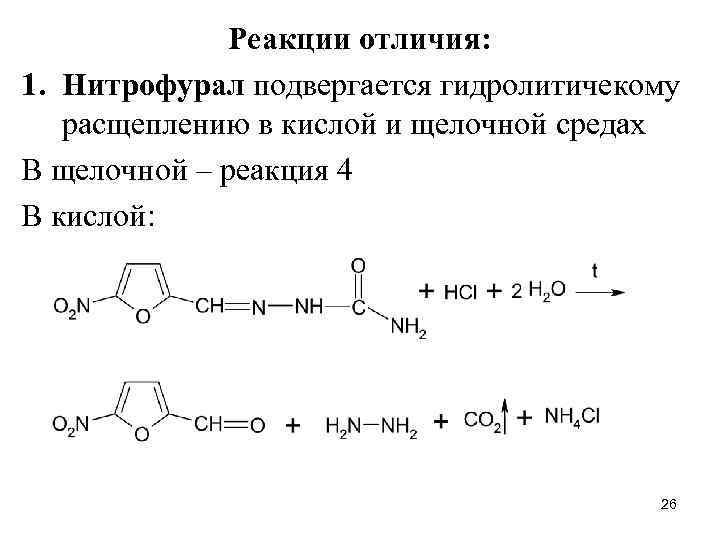 Реакции отличия: 1. Нитрофурал подвергается гидролитичекому расщеплению в кислой и щелочной средах В щелочной – реакция 4 В кислой: 26
Реакции отличия: 1. Нитрофурал подвергается гидролитичекому расщеплению в кислой и щелочной средах В щелочной – реакция 4 В кислой: 26
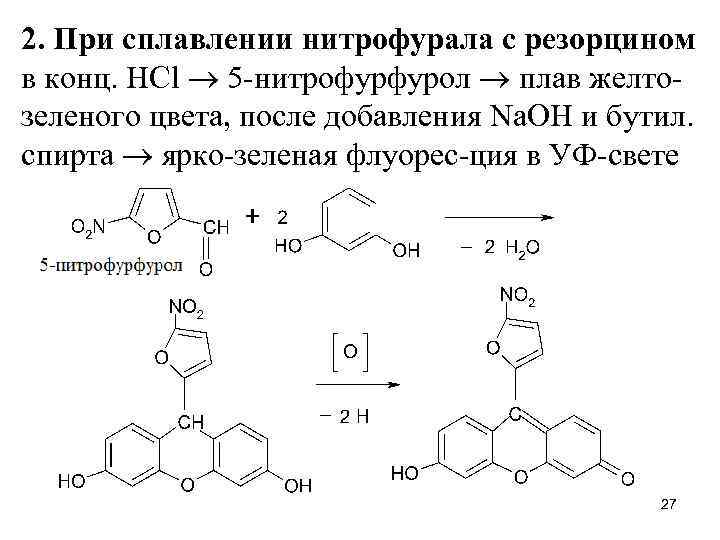 2. При сплавлении нитрофурала с резорцином в конц. HCl 5 -нитрофурфурол плав желтозеленого цвета, после добавления Na. OH и бутил. спирта ярко-зеленая флуорес-ция в УФ-свете 27
2. При сплавлении нитрофурала с резорцином в конц. HCl 5 -нитрофурфурол плав желтозеленого цвета, после добавления Na. OH и бутил. спирта ярко-зеленая флуорес-ция в УФ-свете 27
 Примеси В ЛВ устанавливают содержание посторонних примесей – ТСХ (доп) В фуразидине определяют отсутствие легкообугливающихся (при 250 о. С) примесей 28
Примеси В ЛВ устанавливают содержание посторонних примесей – ТСХ (доп) В фуразидине определяют отсутствие легкообугливающихся (при 250 о. С) примесей 28
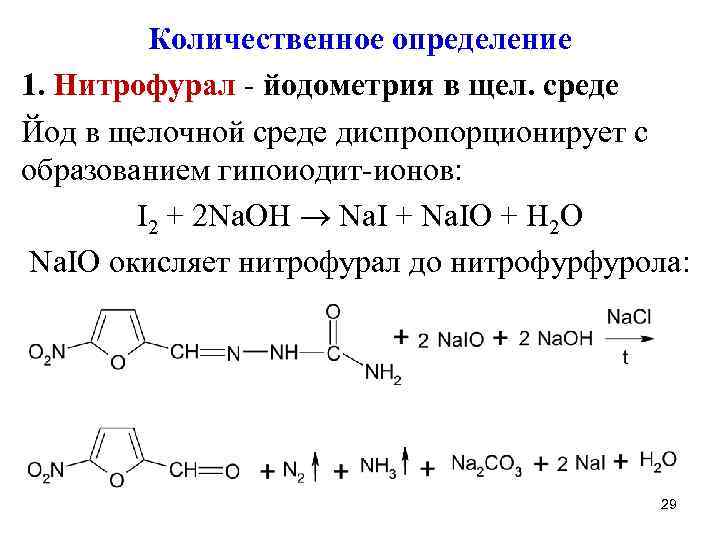 Количественное определение 1. Нитрофурал - йодометрия в щел. среде Йод в щелочной среде диспропорционирует с образованием гипоиодит-ионов: I 2 + 2 Na. OH Na. I + Na. IO + H 2 O Na. IO окисляет нитрофурал до нитрофурфурола: 29
Количественное определение 1. Нитрофурал - йодометрия в щел. среде Йод в щелочной среде диспропорционирует с образованием гипоиодит-ионов: I 2 + 2 Na. OH Na. I + Na. IO + H 2 O Na. IO окисляет нитрофурал до нитрофурфурола: 29
 Растворимость нитрофурала в воде улучшают добавлением Na. Cl и нагреванием Далее р-р подкисляют и выделившийся йод титруют тиосульфатом натрия Na. I + Na. IO + H 2 SO 4 I 2 + Na 2 SO 4 + H 2 O I 2 + Na 2 S 2 O 3 2 Na. I + Na 2 S 4 O 6 Ind – крахмал, || к. о. fэкв(нитрофурала) = ? 30
Растворимость нитрофурала в воде улучшают добавлением Na. Cl и нагреванием Далее р-р подкисляют и выделившийся йод титруют тиосульфатом натрия Na. I + Na. IO + H 2 SO 4 I 2 + Na 2 SO 4 + H 2 O I 2 + Na 2 S 2 O 3 2 Na. I + Na 2 S 4 O 6 Ind – крахмал, || к. о. fэкв(нитрофурала) = ? 30
 малое количество щелочи и короткое время действия реактива (1 -2 мин) обусловливают окисление только гидразина, не затрагивая при этом альдегидную группу 5 -нитрофурфурола N 2 -2 – 2 2 e N 20 fэкв(нитрофурала) = 1/4 31
малое количество щелочи и короткое время действия реактива (1 -2 мин) обусловливают окисление только гидразина, не затрагивая при этом альдегидную группу 5 -нитрофурфурола N 2 -2 – 2 2 e N 20 fэкв(нитрофурала) = 1/4 31
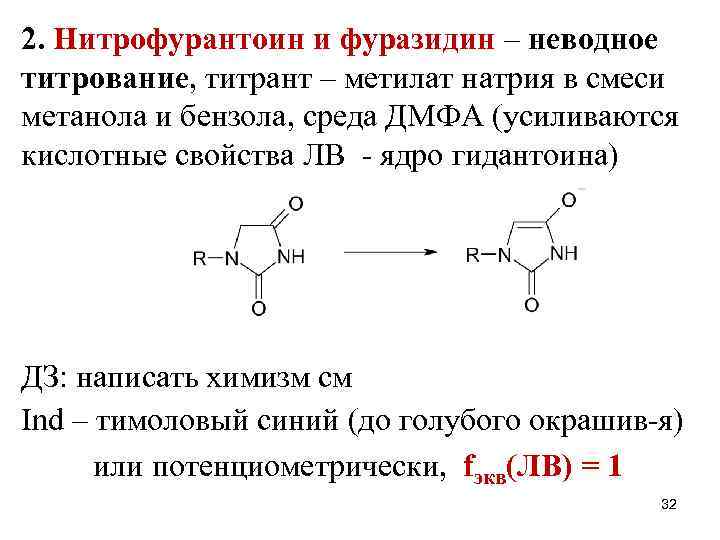 2. Нитрофурантоин и фуразидин – неводное титрование, титрант – метилат натрия в смеси метанола и бензола, среда ДМФА (усиливаются кислотные свойства ЛВ - ядро гидантоина) ДЗ: написать химизм см Ind – тимоловый синий (до голубого окрашив-я) или потенциометрически, fэкв(ЛВ) = 1 32
2. Нитрофурантоин и фуразидин – неводное титрование, титрант – метилат натрия в смеси метанола и бензола, среда ДМФА (усиливаются кислотные свойства ЛВ - ядро гидантоина) ДЗ: написать химизм см Ind – тимоловый синий (до голубого окрашив-я) или потенциометрически, fэкв(ЛВ) = 1 32
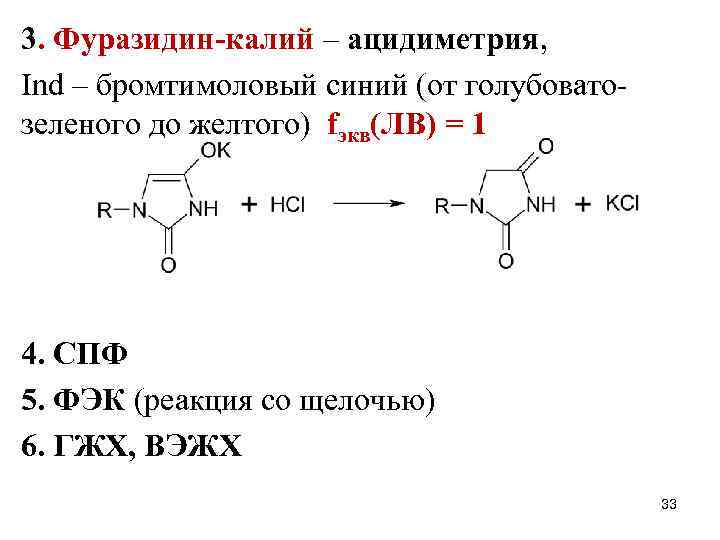 3. Фуразидин-калий – ацидиметрия, Ind – бромтимоловый синий (от голубоватозеленого до желтого) fэкв(ЛВ) = 1 4. СПФ 5. ФЭК (реакция со щелочью) 6. ГЖХ, ВЭЖХ 33
3. Фуразидин-калий – ацидиметрия, Ind – бромтимоловый синий (от голубоватозеленого до желтого) fэкв(ЛВ) = 1 4. СПФ 5. ФЭК (реакция со щелочью) 6. ГЖХ, ВЭЖХ 33
 Хранение Список, в ХУТ в банках темного стекла, в прохладном месте Под действием света происходит необратимое разрушение фуранового цикла (фотодеструкция), Под действием влаги легко гидролизуются Применение Антибактериальные средства Фуразолидон – антибактериальное и антипротозойное средство 34
Хранение Список, в ХУТ в банках темного стекла, в прохладном месте Под действием света происходит необратимое разрушение фуранового цикла (фотодеструкция), Под действием влаги легко гидролизуются Применение Антибактериальные средства Фуразолидон – антибактериальное и антипротозойное средство 34
 ЛФ: нитрофурал – таблетки, мазь Нитрофурантоин, фуразолидон и фуразидин – таблетки Фуразидин растворимый – таблетки, капсулы, смесь для приготовления р-ра местного применения 35
ЛФ: нитрофурал – таблетки, мазь Нитрофурантоин, фуразолидон и фуразидин – таблетки Фуразидин растворимый – таблетки, капсулы, смесь для приготовления р-ра местного применения 35
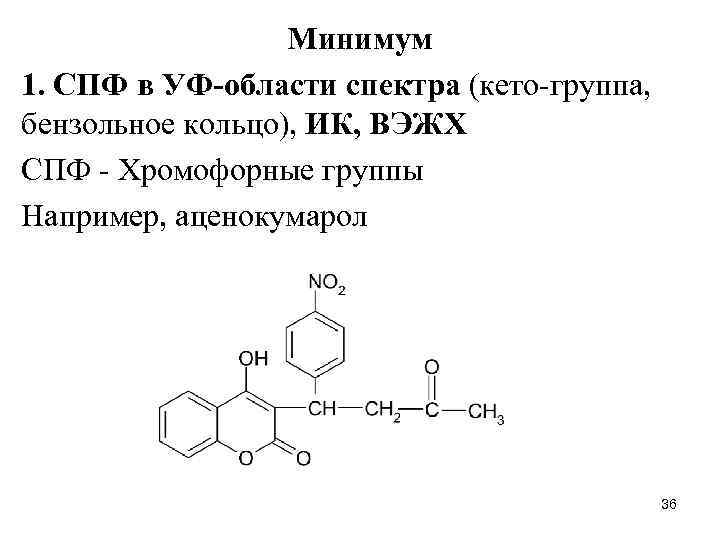 Минимум 1. СПФ в УФ-области спектра (кето-группа, бензольное кольцо), ИК, ВЭЖХ СПФ - Хромофорные группы Например, аценокумарол 36
Минимум 1. СПФ в УФ-области спектра (кето-группа, бензольное кольцо), ИК, ВЭЖХ СПФ - Хромофорные группы Например, аценокумарол 36
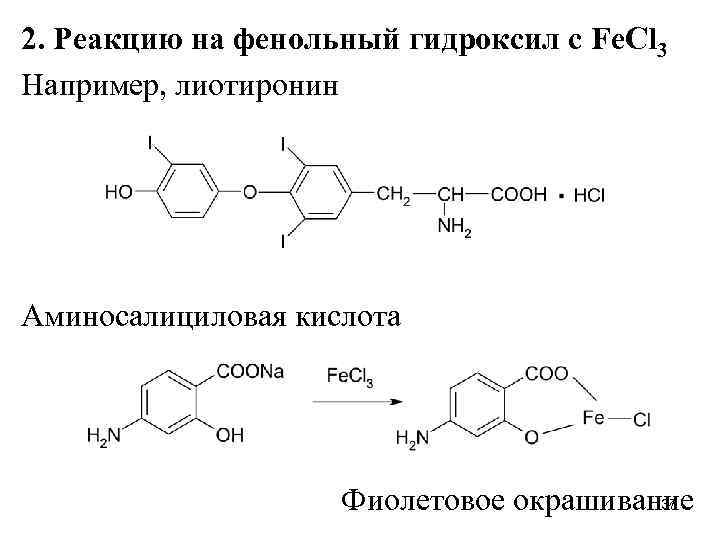 2. Реакцию на фенольный гидроксил с Fe. Cl 3 Например, лиотиронин Аминосалициловая кислота 37 Фиолетовое окрашивание
2. Реакцию на фенольный гидроксил с Fe. Cl 3 Например, лиотиронин Аминосалициловая кислота 37 Фиолетовое окрашивание
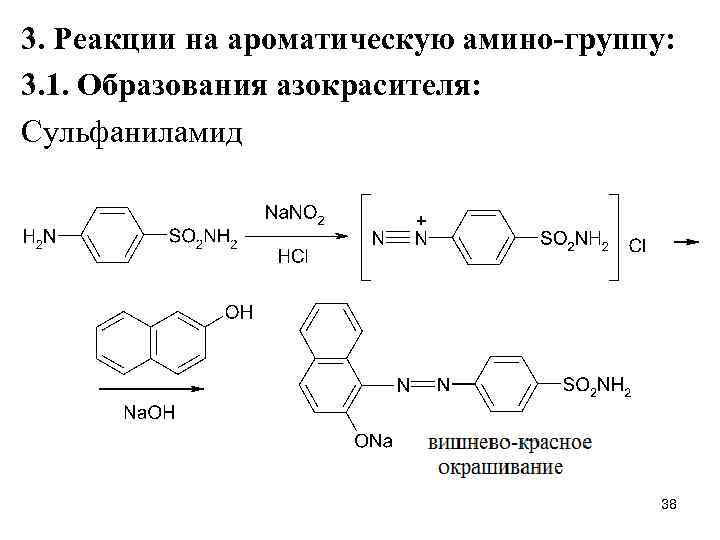 3. Реакции на ароматическую амино-группу: 3. 1. Образования азокрасителя: Сульфаниламид 38
3. Реакции на ароматическую амино-группу: 3. 1. Образования азокрасителя: Сульфаниламид 38
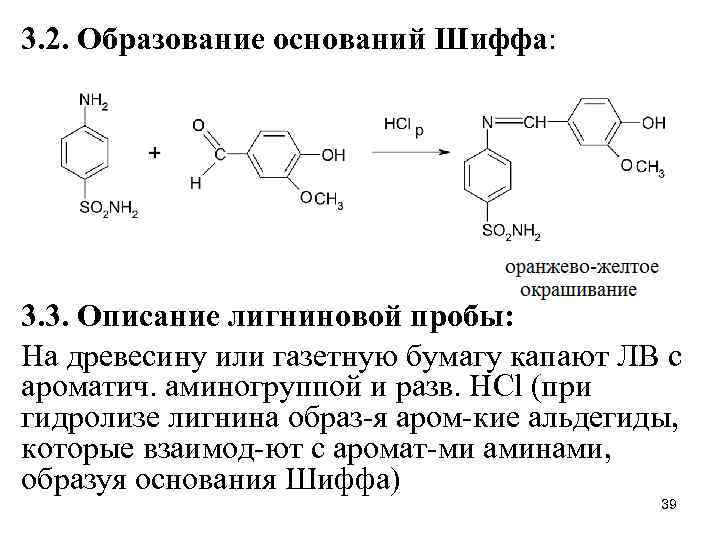 3. 2. Образование оснований Шиффа: 3. 3. Описание лигниновой пробы: На древесину или газетную бумагу капают ЛВ с ароматич. аминогруппой и разв. HCl (при гидролизе лигнина образ-я аром-кие альдегиды, которые взаимод-ют с аромат-ми аминами, образуя основания Шиффа) 39
3. 2. Образование оснований Шиффа: 3. 3. Описание лигниновой пробы: На древесину или газетную бумагу капают ЛВ с ароматич. аминогруппой и разв. HCl (при гидролизе лигнина образ-я аром-кие альдегиды, которые взаимод-ют с аромат-ми аминами, образуя основания Шиффа) 39
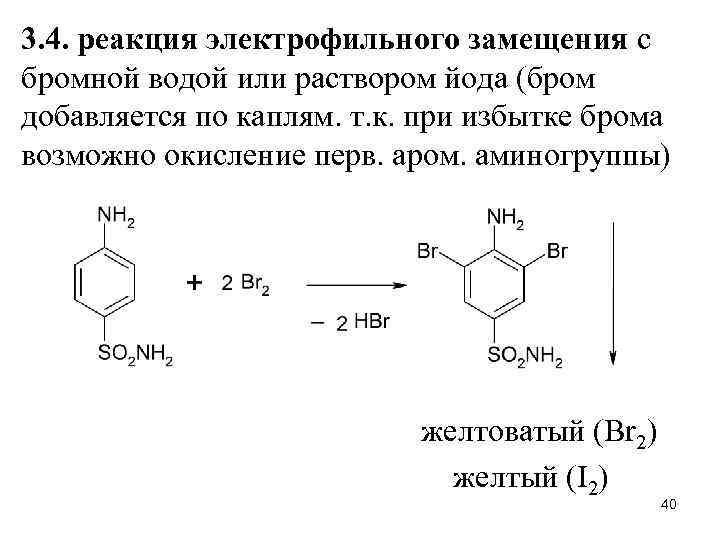 3. 4. реакция электрофильного замещения с бромной водой или раствором йода (бром добавляется по каплям. т. к. при избытке брома возможно окисление перв. аром. аминогруппы) желтоватый (Br 2) желтый (I 2) 40
3. 4. реакция электрофильного замещения с бромной водой или раствором йода (бром добавляется по каплям. т. к. при избытке брома возможно окисление перв. аром. аминогруппы) желтоватый (Br 2) желтый (I 2) 40
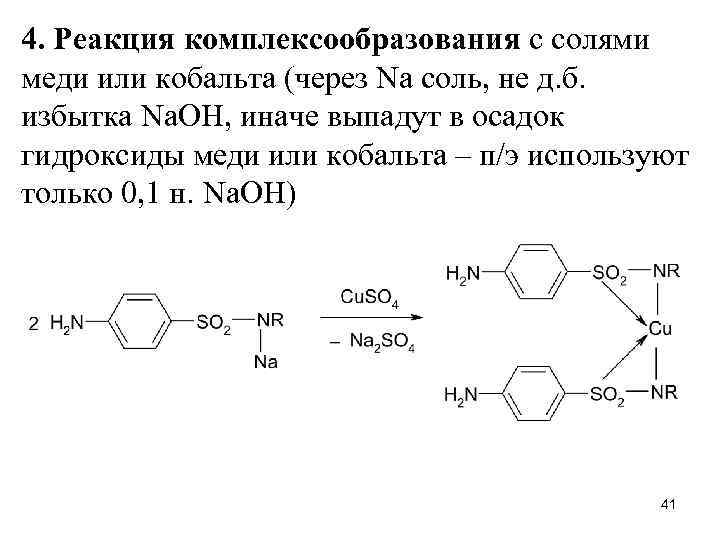 4. Реакция комплексообразования с солями меди или кобальта (через Na соль, не д. б. избытка Na. OH, иначе выпадут в осадок гидроксиды меди или кобальта – п/э используют только 0, 1 н. Na. OH) 41
4. Реакция комплексообразования с солями меди или кобальта (через Na соль, не д. б. избытка Na. OH, иначе выпадут в осадок гидроксиды меди или кобальта – п/э используют только 0, 1 н. Na. OH) 41
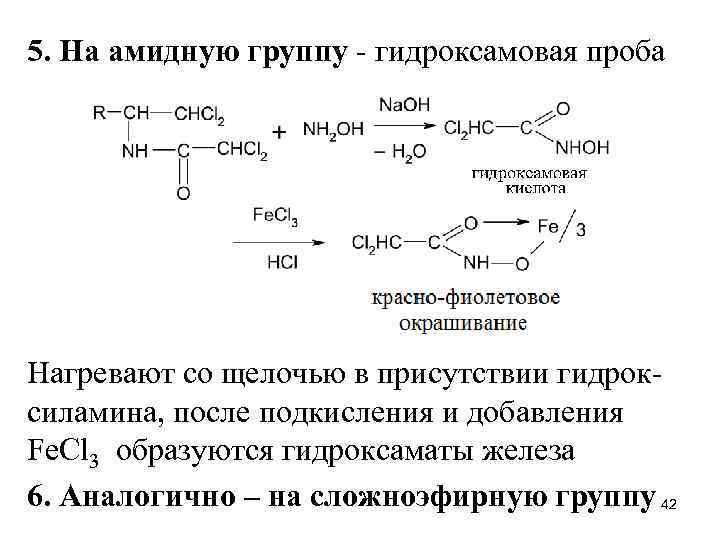 5. На амидную группу - гидроксамовая проба Нагревают со щелочью в присутствии гидроксиламина, после подкисления и добавления Fe. Cl 3 образуются гидроксаматы железа 6. Аналогично – на сложноэфирную группу 42
5. На амидную группу - гидроксамовая проба Нагревают со щелочью в присутствии гидроксиламина, после подкисления и добавления Fe. Cl 3 образуются гидроксаматы железа 6. Аналогично – на сложноэфирную группу 42
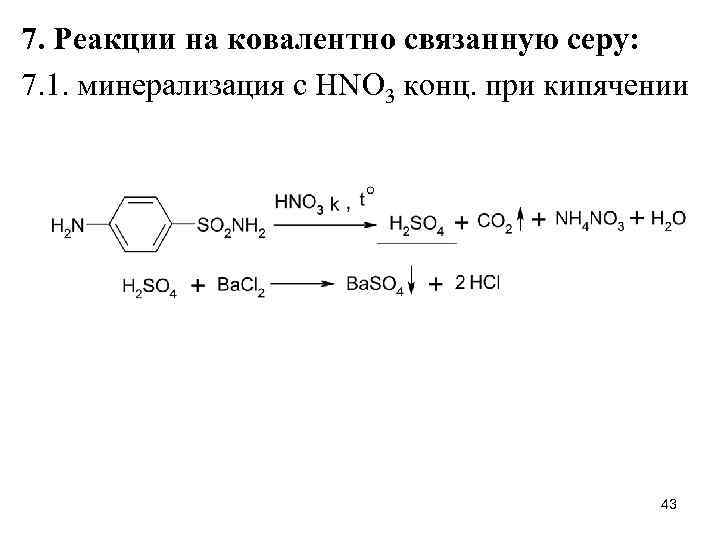 7. Реакции на ковалентно связанную серу: 7. 1. минерализация с HNO 3 конц. при кипячении 43
7. Реакции на ковалентно связанную серу: 7. 1. минерализация с HNO 3 конц. при кипячении 43
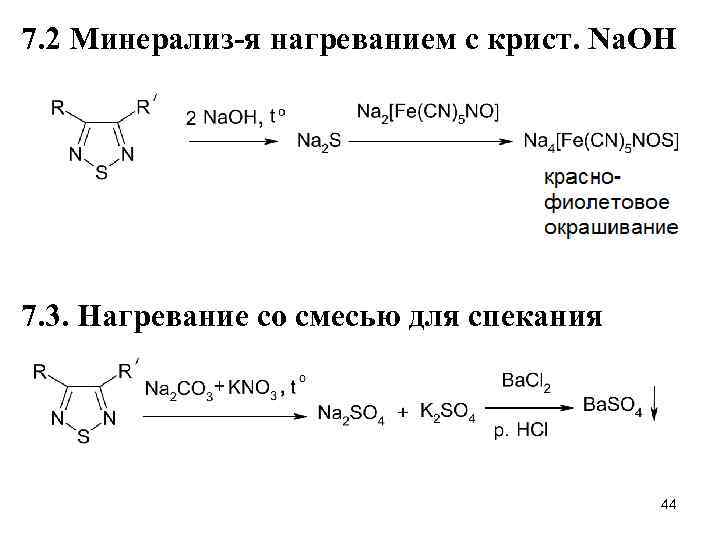 7. 2 Минерализ-я нагреванием с крист. Na. OH 7. 3. Нагревание со смесью для спекания 44
7. 2 Минерализ-я нагреванием с крист. Na. OH 7. 3. Нагревание со смесью для спекания 44
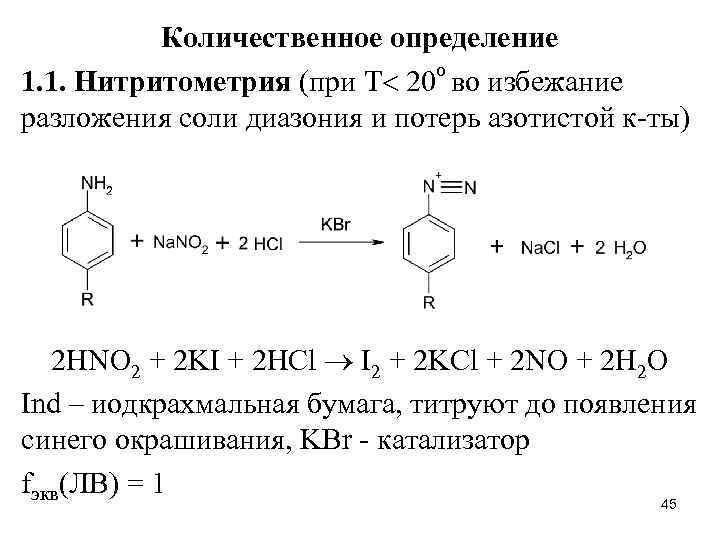 Количественное определение о 1. 1. Нитритометрия (при Т 20 во избежание разложения соли диазония и потерь азотистой к-ты) 2 HNO 2 + 2 KI + 2 HCl I 2 + 2 KCl + 2 NO + 2 H 2 O Ind – иодкрахмальная бумага, титруют до появления синего окрашивания, KBr - катализатор fэкв(ЛВ) = 1 45
Количественное определение о 1. 1. Нитритометрия (при Т 20 во избежание разложения соли диазония и потерь азотистой к-ты) 2 HNO 2 + 2 KI + 2 HCl I 2 + 2 KCl + 2 NO + 2 H 2 O Ind – иодкрахмальная бумага, титруют до появления синего окрашивания, KBr - катализатор fэкв(ЛВ) = 1 45
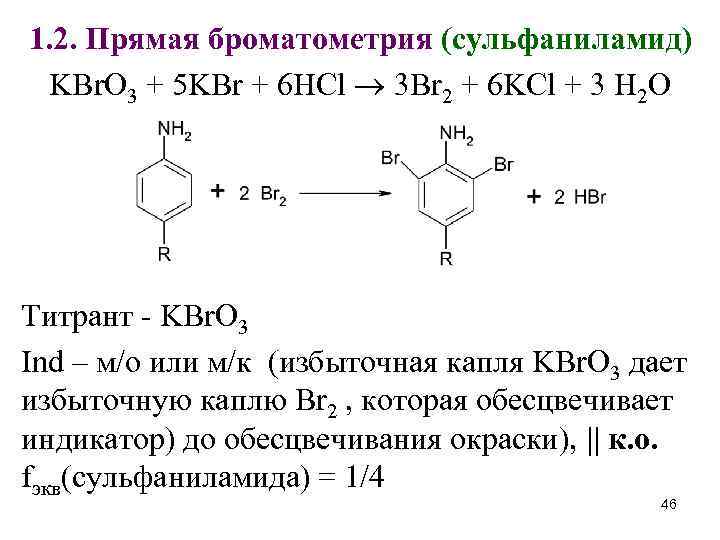 1. 2. Прямая броматометрия (сульфаниламид) KBr. O 3 + 5 KBr + 6 HCl 3 Br 2 + 6 KCl + 3 H 2 O Титрант - KBr. O 3 Ind – м/о или м/к (избыточная капля KBr. O 3 дает избыточную каплю Br 2 , которая обесцвечивает индикатор) до обесцвечивания окраски), || к. о. fэкв(сульфаниламида) = 1/4 46
1. 2. Прямая броматометрия (сульфаниламид) KBr. O 3 + 5 KBr + 6 HCl 3 Br 2 + 6 KCl + 3 H 2 O Титрант - KBr. O 3 Ind – м/о или м/к (избыточная капля KBr. O 3 дает избыточную каплю Br 2 , которая обесцвечивает индикатор) до обесцвечивания окраски), || к. о. fэкв(сульфаниламида) = 1/4 46
 Обратная броматометрия (сульфацетамид натрия, сульфадиметоксин, сульфален) KBr. O 3 + 5 KBr + 6 HCl 3 Br 2 + 6 KCl + 3 H 2 O Br 2 + 2 KI I 2 + 2 KBr I 2 + Na 2 S 2 O 3 2 Na. I + Na 2 S 4 O 6 Ind – крахмал, || к. о. fэкв(ЛВ) = 1/4 47
Обратная броматометрия (сульфацетамид натрия, сульфадиметоксин, сульфален) KBr. O 3 + 5 KBr + 6 HCl 3 Br 2 + 6 KCl + 3 H 2 O Br 2 + 2 KI I 2 + 2 KBr I 2 + Na 2 S 2 O 3 2 Na. I + Na 2 S 4 O 6 Ind – крахмал, || к. о. fэкв(ЛВ) = 1/4 47
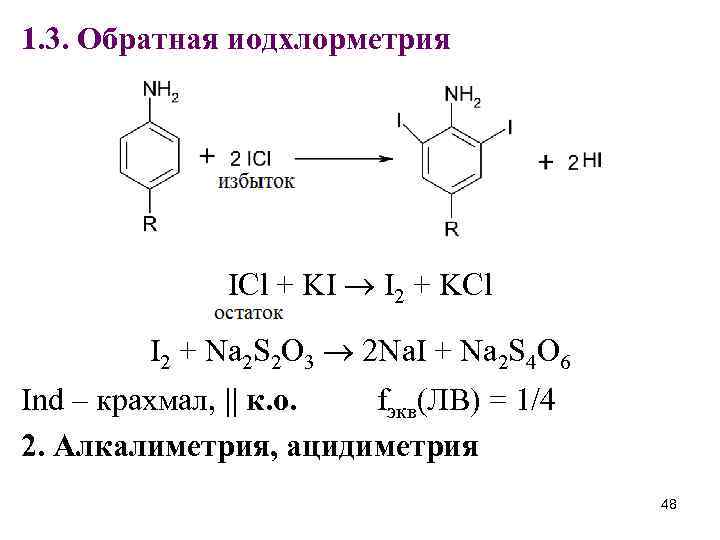 1. 3. Обратная иодхлорметрия ICl + KI I 2 + KCl I 2 + Na 2 S 2 O 3 2 Na. I + Na 2 S 4 O 6 Ind – крахмал, || к. о. fэкв(ЛВ) = 1/4 2. Алкалиметрия, ацидиметрия 48
1. 3. Обратная иодхлорметрия ICl + KI I 2 + KCl I 2 + Na 2 S 2 O 3 2 Na. I + Na 2 S 4 O 6 Ind – крахмал, || к. о. fэкв(ЛВ) = 1/4 2. Алкалиметрия, ацидиметрия 48
 2. Алкалиметрия, ацидиметрия 49
2. Алкалиметрия, ацидиметрия 49
 в 50
в 50
 в 51
в 51
 в 52
в 52
 в 53
в 53
 в 54
в 54
 в 55
в 55
 в 56
в 56
 в 57
в 57
 в 58
в 58
 в 59
в 59
 в 60
в 60
 в 61
в 61
 в 62
в 62
 в 63
в 63


