L-Proektir-6.ppt
- Количество слайдов: 22

Проектирование и оборудование предприятий нефтехимии (6)
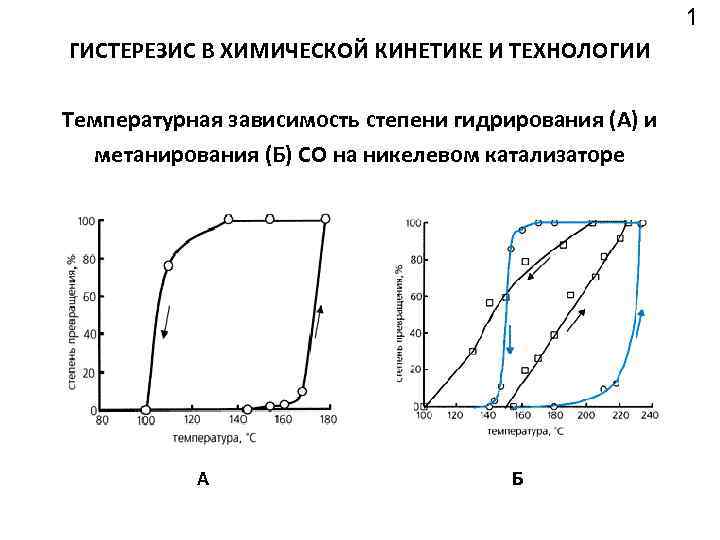
1 ГИСТЕРЕЗИС В ХИМИЧЕСКОЙ КИНЕТИКЕ И ТЕХНОЛОГИИ Температурная зависимость степени гидрирования (А) и метанирования (Б) СО на никелевом катализаторе А Б
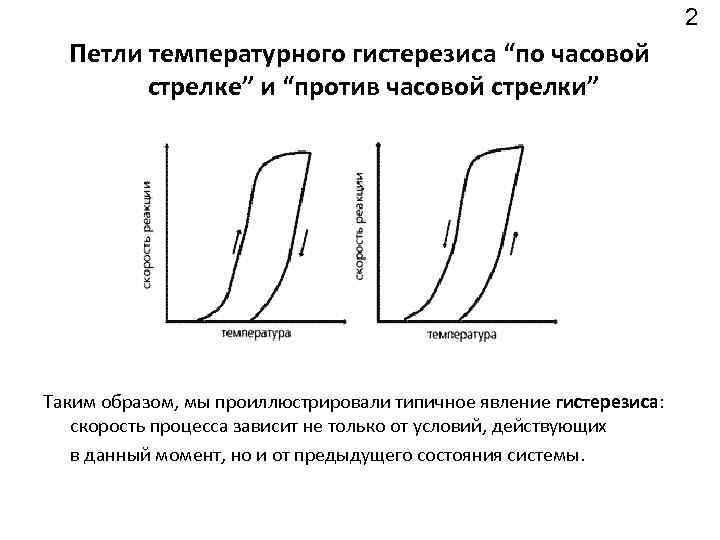
2 Петли температурного гистерезиса “по часовой стрелке” и “против часовой стрелки” Таким образом, мы проиллюстрировали типичное явление гистерезиса: скорость процесса зависит не только от условий, действующих в данный момент, но и от предыдущего состояния системы.

3 Возможные стационарные состояния проточного адиабатического РИС Пусть протекает экзотермическая реакция первого порядка: A R; W(CA, T)=k(T) CA=k(T) A Тогда уравнения материального и теплового балансов имеют вид: (AO-A)=VP W(A, T)= VP k(T) A; CP (T-TO)=QP VP Где VP – объем реактора, - объемная скорость подачи. Отношение VP/ = К – времени контакта. Поделив первое уравнение на VP, а второе на VP СP, получим новые уравнения МБ и ТБ: (AO-A)/ К=k(T) A; (T-TO)/ К=(QP/СP) k(T) A Мы уже видели на примере РИС-П, что в реакторе в зависимости от значения параметров возможны три стационарных состояния. Общая методика определения устойчивости стационарных состояний включает выполнение следующих этапов.
![4 1. Математическое описание нестационарного процесса. d. A/dt = [(AO-A)/ К] -W(A, T); d. 4 1. Математическое описание нестационарного процесса. d. A/dt = [(AO-A)/ К] -W(A, T); d.](https://present5.com/presentation/146109693_335156104/image-5.jpg)
4 1. Математическое описание нестационарного процесса. d. A/dt = [(AO-A)/ К] -W(A, T); d. T/dt = [(T-TO)/ К] -QP W(T, A)/CP. 2. Математическое описание стационарного процесса. d. AS/dt=0 = [(AO-AS)/ К] -W(AS, TS); d. TS/dt =0= [(TS-TO)/ К] -QP W(AS, TS)/CP. Где AS и TS – концентрация реагента и температура при стационарном состоянии системы, соответственно. 3. Математическое описание изменения отклонений от стационарного состояния во времени. d(A-AS)/dt = - (A-AS)/ К – [W(A, T)-W(AS, TS)]; d(T-TS)/dt = (T-TS)/ К -QP [W(A, T) - W(AS, TS)]/CP
![5 4. Линеаризация уравнений математического описания. [W(A, T) - W(AS, TS)]=(d. W/d. A)S (A-AS) 5 4. Линеаризация уравнений математического описания. [W(A, T) - W(AS, TS)]=(d. W/d. A)S (A-AS)](https://present5.com/presentation/146109693_335156104/image-6.jpg)
5 4. Линеаризация уравнений математического описания. [W(A, T) - W(AS, TS)]=(d. W/d. A)S (A-AS) - (d. W/d. T)S (T-TS); Выберем в качестве новых переменных отклонения от концентрации х= A-AS и температуру у= T-TS. Тогда с учетом равенства выше получим Или

6 5. Общее решение этой системы линейных дифференциальных уравнений имеет вид: x=A 1 exp( 1 t)+A 2 exp( 2 t); y=B 1 exp( 1 t)+B 2 exp( 2 t). Где А 1, А 2, В 1, В 2 – постоянные, 1, 2 – корни характеристического уравнения: = 2 – (а 11+а 22) + (а 11 а 22 -а 12 а 21), которые определяются выражением 6. Исследование корней характеристического уравнения. Фактически, как увидим далее, определение устойчивости сводится к определению условий, при которых 1+ 2 0; 1 2 > 0. Корни могут быть действительными числами или комплексносопряженными мнимыми: 1= + i, 2 = - i.
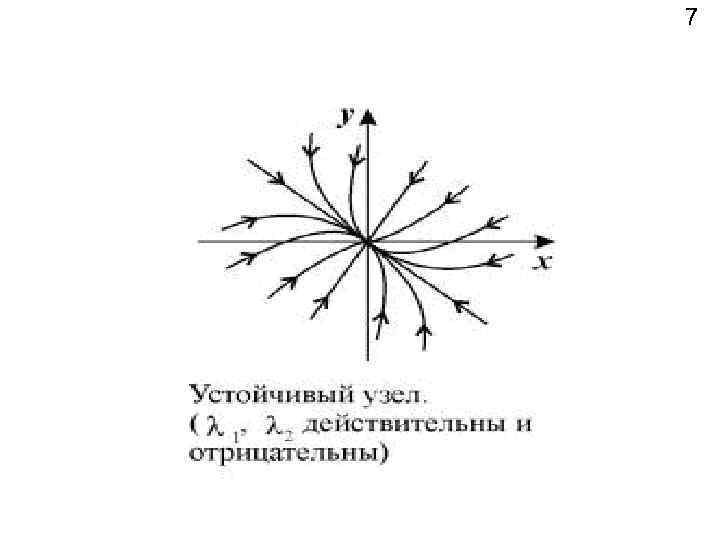
7
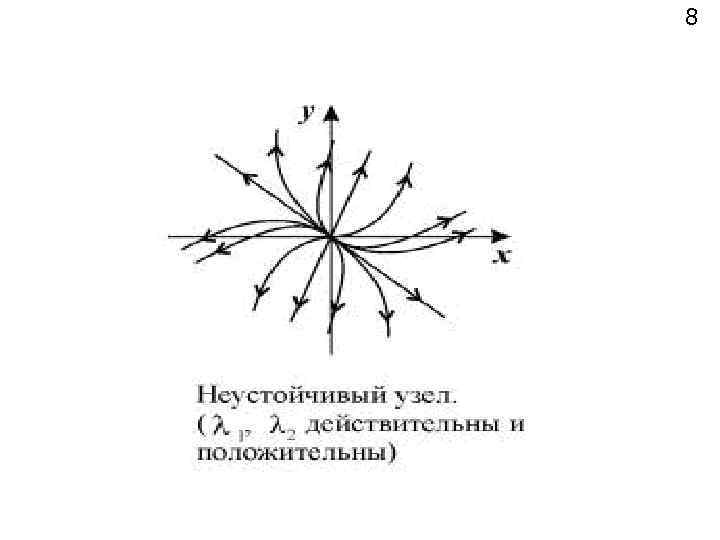
8
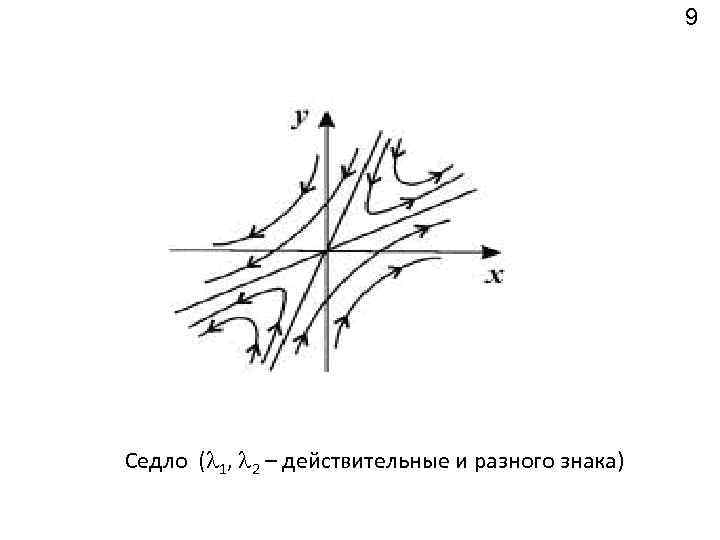
9 Седло ( 1, 2 – действительные и разного знака)

10

11
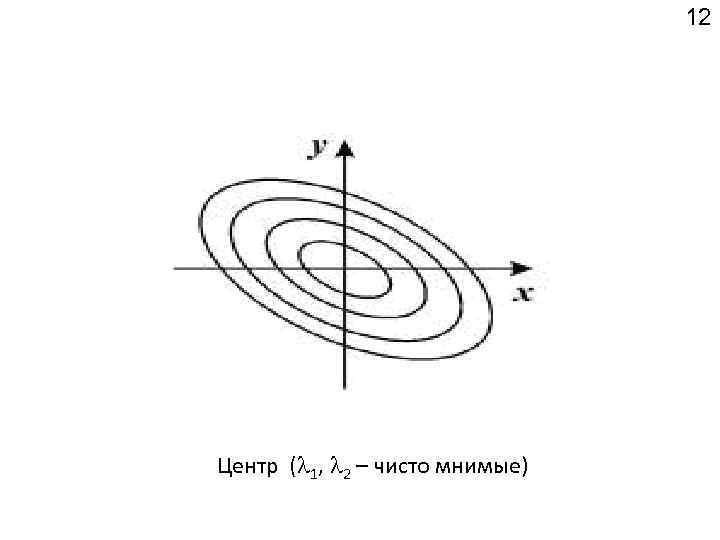
12 Центр ( 1, 2 – чисто мнимые)

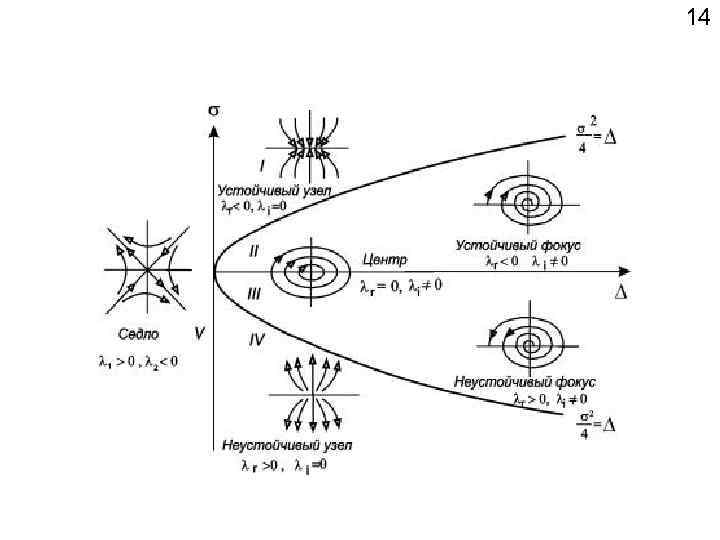
13 Введем для простоты записи обозначения: =– (а 11+а 22); =(а 11 а 22 -а 12 а 21); det= 2 -4 Тогда получим следующее характеристическое уравнение: 2 + + = 0
14

Материальный баланс реактора идеального смешения периодического действия (РИС-П) для i-того компонента представляется уравнениями: (1) с начальными условиями – t = 0: Сi=Сiо. Материальный баланс реактора идеального вытеснения (РИВ) для i-того компонента представляется уравнениями: (2) с начальными условиями – l = 0: Сi=Сiо. При численном решении уравнений математического описания, представленными обыкновенными дифференциальными уравнениями (1) или (3), используются, как правило, методы Рунге-Кутты различного порядка. Рассмотрим наиболее простой алгоритм решения методом Эйлера (метод Рунге-Кутты первого порядка). В этом методе ось решения (по времени или по длине) сканируется с постоянным шагом изменения аргумента Тогда разностные аналоги производных в уравнениях (1) и (2) будут иметь вид: 15

16 m=1…M (3) t=0…t. K =t. K /N, l=0…LP h=LP /(M-1) t – аргумент интегрирования по времени, t. K – время пребывания в реакторе, – шаг интегрирования по времени (N – число временных интервалов интегрирования); l – аргумент интегрирования по длине реактора, LP – длина реактора, h – шаг интегрирования по длине (M – число точек разбиения длины реактора), – значение концентраций на предыдущем временном шаге интегрирования. (Для простоты записи индекс i у концентраций Сi опущен). Граничные и начальные условия для уравнений (3) и уравнений (1), (2) аналогичны. Численное решение любого из уравнений (3) зависит от интерпретации правых частей. Существуют два метода численного решения: явный и неявный. В первом из них правые части являются функциями переменных, вычисленных на предыдущем шаге интегрирования (т. е. ), во вором методе функции переменных W=W(C). Рассмотрим простую реакцию первого порядка А В. Тогда разностный аналог уравнения (1) будет иметь следующий вид для явной и неявной схем (C=[A]): и

17 Получим следующие решения. Для явной схемы: С= (1 -k ) С= /(1+k ) Для неявной схемы: Видно, что решение по явной схеме накладывает ограничение на шаг интегрирования 1/k, т. к. отрицательных значений концентраций не существует. Поэтому в дальнейшем будем придерживаться неявных схем или полунеявных для сложных химических реакций, т. е. будем представлять правые части в виде: ij. Wj = – i. Ci+ i Где переменные и являются функциями концентраций компонентов. Тогда решение разностного уравнения для РИС-П имеет вид: Если компоненты только расходуются, то коэффициенты равны нулю, если только образуются, то равны нулю коэффициенты ; в остальных случаях отличны от нуля оба коэффициента. Например, для обратимой реакции А В с кинетическим уравнением W=k 1 A-k 2 B получим следующие решения: (4)

Как видно из формул (4), решения нуждаются в корректировке, т. к. содержат решения с предыдущего временного шага. Для устранения неточности решения необходимо использовать итерационную процедуру, приняв решение за значение на n-том шаге 18 итерации, а решение Y за значение на (n+1)-вом шаге итерации. Итерации продолжать до тех пор, пока разность l Y- l не станет меньше некоторой малой величины. Разностный аналог уравнения материального баланса для РИВ имеет вид: m=1…M Решение этого уравнения находится по рекуррентной формуле (5): (5) Рассмотрим некоторые реакции, кроме уже проанализированных необратимых и обратимых реакций первого порядка. Последовательные реакции. А В С; W 1=k 1 A, W 2=k 2 B A=k 1, B=k 2, C=0; A=0, B=k 1 A, C=k 2 B А В С; W 1=k 1 A-k 3 B, W 2=k 2 B-k 4 C A=k 1, B=k 2, C=k 4; A=k 3 B, B=k 1 A+k 4 C, C=k 2 B

19 А В 2 С; W 1=k 1 A, W 2=k 2 B-k 3 C 2 A=k 1, B=k 2, C=k 3 С(n); A=0, B=k 3 С(n)C(n), C=k 2 B(n+1) При определении по формуле (7) концентрации компонента «С» используется метод Зайделя, т. е. в числитель формулы входит уже найденное на (n+1)-ом шаге итерации значение «B(n+1)» . Итерации проводятся по концентрациями двух компонентов: «В» и «С» . Параллельные реакции. В А С; W 1=k 1 A, W 2=k 2 А A=k 1, B=0, C=0; A=0, B=k 1 A, C=k 2 А В А С; W 1=k 1 A-k 3 B, W 2=k 2 А-k 4 C A=k 1+k 2, B=k 3, C=k 4; A=k 3 B+k 4 C, B=k 3 A, C=k 4 С А + B 2 С; W 1=k 1 A, W 2=k 2 B-k 3 C 2 A=k 1, B=k 2, C=k 3 С(n); A=0, B=k 3 С(n)C(n), C=k 2 B(n+1) Вновь для расчета концентрации компонента «С» используется метод Зайделя. Итерации проводятся только по концентрации компонента «В» .

20 Анализируя балансные уравнения для РИС-П и РИВ, можно легко получить уравнения для нестационарной модели реактора идеального вытеснения: (6) с начальными условиями – при t = 0: Сi=Сiо, и граничными условиями – при l = 0: Сi=Сiо. Разностными аналогами уравнений материального баланса (6) является уравнение (7): (7) Начальные и граничные условия те же, что и для уравнения (6). Решение уравнений (7) представляется рекуррентными соотношениями (8): (8)

L-Proektir-6.ppt