Процессы технологии ПЭН.ppt
- Количество слайдов: 19
 Процессы технологии природных энергоносителей и углеродных материалов Преподаватель Дучко Мария Александровна, ассистент кафедры ХТТ
Процессы технологии природных энергоносителей и углеродных материалов Преподаватель Дучко Мария Александровна, ассистент кафедры ХТТ
 Основные процессы технологии природных энергоносителей 1. Термические процессы 2. Каталитические процессы 3. Процессы, связанные с переносом водорода 4. Окисление 5. Газификация 6. Синтезы на основе углерода и водорода
Основные процессы технологии природных энергоносителей 1. Термические процессы 2. Каталитические процессы 3. Процессы, связанные с переносом водорода 4. Окисление 5. Газификация 6. Синтезы на основе углерода и водорода
 1. Термические процессы • • • Термический крекинг Термический пиролиз Сажеобразование Полукоксование ТГИ Коксование ТГИ
1. Термические процессы • • • Термический крекинг Термический пиролиз Сажеобразование Полукоксование ТГИ Коксование ТГИ
 Термический крекинг и пиролиз углеводородов осуществляется в отсутствии катализаторов при повышенной t (крекинг – 450 -5000 С, пиролиз – 700 -9000 С) в отсутствии воздуха. • При крекинге происходит разрыв С-С связей, а при пиролизе рвутся С-С и С -Н связи. • Механизм реакций – свободно-радикальный. • Высшие парафины более склонны к расщеплению, чем низшие. • Разветвленные молекулы рвутся проще.
Термический крекинг и пиролиз углеводородов осуществляется в отсутствии катализаторов при повышенной t (крекинг – 450 -5000 С, пиролиз – 700 -9000 С) в отсутствии воздуха. • При крекинге происходит разрыв С-С связей, а при пиролизе рвутся С-С и С -Н связи. • Механизм реакций – свободно-радикальный. • Высшие парафины более склонны к расщеплению, чем низшие. • Разветвленные молекулы рвутся проще.
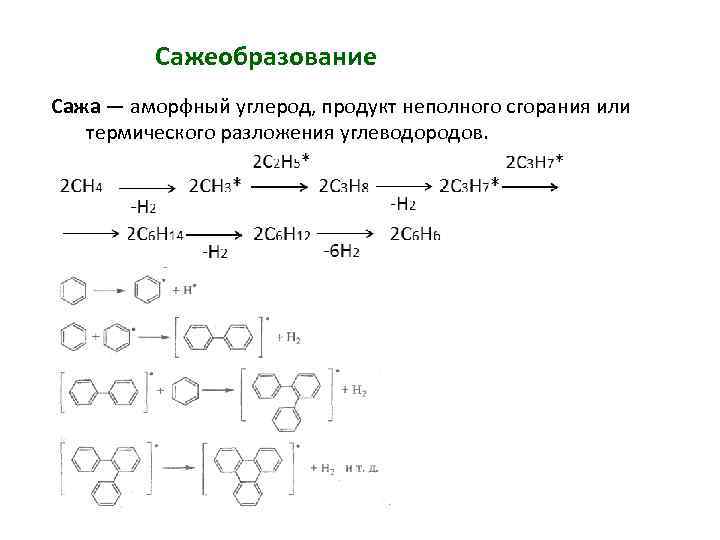 Сажеобразование Сажа — аморфный углерод, продукт неполного сгорания или термического разложения углеводородов.
Сажеобразование Сажа — аморфный углерод, продукт неполного сгорания или термического разложения углеводородов.
 Полукоксование и коксование ТГИ Полукоксование и коксование – это процессы термической деструкции твердых горючих ископаемых при нагревании без доступа воздуха: полукоксование проводят до 500 -5500 С, а коксование – до 11000 С. Технологические стадии процессов: 1. сушка (удаление влаги, 1000 С); 2. бертинирование (обработка сырья при t=2000 С с целью удаления летучих веществ; образуются CO, CO 2, H 2 O, CH 4); 3. полукоксование; 4. коксование. Полукоксование используется для получения жидких продуктов и искусственного жидкого топлива (ИЖТ). Сырьем является сапропели, некачественный бурый уголь, горючие сланцы, торф. Состав продуктов полукоксования: 1) Первичная смола – содержит несколько классов орг. соединений: основания, карбоновые кислоты, фенолы, у/в, асфальтены (число конденсированных ядер 110) и др. 2) Первичный газ – состоит в основном из СН 4, Н 2, непредельных у/в и летучих гетеросоединений. 3) Полукокс
Полукоксование и коксование ТГИ Полукоксование и коксование – это процессы термической деструкции твердых горючих ископаемых при нагревании без доступа воздуха: полукоксование проводят до 500 -5500 С, а коксование – до 11000 С. Технологические стадии процессов: 1. сушка (удаление влаги, 1000 С); 2. бертинирование (обработка сырья при t=2000 С с целью удаления летучих веществ; образуются CO, CO 2, H 2 O, CH 4); 3. полукоксование; 4. коксование. Полукоксование используется для получения жидких продуктов и искусственного жидкого топлива (ИЖТ). Сырьем является сапропели, некачественный бурый уголь, горючие сланцы, торф. Состав продуктов полукоксования: 1) Первичная смола – содержит несколько классов орг. соединений: основания, карбоновые кислоты, фенолы, у/в, асфальтены (число конденсированных ядер 110) и др. 2) Первичный газ – состоит в основном из СН 4, Н 2, непредельных у/в и летучих гетеросоединений. 3) Полукокс
 Коксование предназначено для получения высококачественных коксов. Сырьем являются коксуемые угли марок Г, К, ОС, входящие в состав шихты. Шихта — смесь исходных материалов, а в некоторых случаях (например, при выплавке чугуна в доменной печи) и топлива в определённой пропорции, подлежащая переработке в металлургических, химических и других агрегатах. Продукты коксования делят на 3 группы 1) Смола коксования – имеет более простой состав, чем первичная смола. Содержит незамещенные конденсированные ароматические соединения: 2)Коксовый газ 3)Кокс
Коксование предназначено для получения высококачественных коксов. Сырьем являются коксуемые угли марок Г, К, ОС, входящие в состав шихты. Шихта — смесь исходных материалов, а в некоторых случаях (например, при выплавке чугуна в доменной печи) и топлива в определённой пропорции, подлежащая переработке в металлургических, химических и других агрегатах. Продукты коксования делят на 3 группы 1) Смола коксования – имеет более простой состав, чем первичная смола. Содержит незамещенные конденсированные ароматические соединения: 2)Коксовый газ 3)Кокс
 2. Каталитические процессы Каталитический крекинг — термокаталитическая переработка нефтяных фракций с целью легких моторных топлив. Протекает в присутствии ионных катализаторов с кислотной функцией (алюмосиликаты, оксиды алюминия и др. ) при Т=450 -480 о. С при атмосферном давлении. Сn. H 2 n+MOH=Cn. H+2 n+1+MOМеханизм процесса – ионно-цепной. Алкилирование – введение алкильного заместителя в молекулу органического соединения. Типичными алкилирующими агентами являются алкилгалогениды, алкены, эпоксисоединения, спирты, реже альдегиды, кетоны, эфиры, сульфиды, диазоалканы. Протекает при низких температурах t<1000 С. Катализатор: H 2 SO 4 и безводная HF, Al. Cl 3. • Алкилирование парафинов олефинами • Алкилирование по ароматическому атому углерода.
2. Каталитические процессы Каталитический крекинг — термокаталитическая переработка нефтяных фракций с целью легких моторных топлив. Протекает в присутствии ионных катализаторов с кислотной функцией (алюмосиликаты, оксиды алюминия и др. ) при Т=450 -480 о. С при атмосферном давлении. Сn. H 2 n+MOH=Cn. H+2 n+1+MOМеханизм процесса – ионно-цепной. Алкилирование – введение алкильного заместителя в молекулу органического соединения. Типичными алкилирующими агентами являются алкилгалогениды, алкены, эпоксисоединения, спирты, реже альдегиды, кетоны, эфиры, сульфиды, диазоалканы. Протекает при низких температурах t<1000 С. Катализатор: H 2 SO 4 и безводная HF, Al. Cl 3. • Алкилирование парафинов олефинами • Алкилирование по ароматическому атому углерода.
 Алкилирование парафинов олефинами 1) н-бутилены легко протонируются кислотой и дают карбкатионы 2) вторичный карбкатион взаимодействует с изобутаном 3) третичный (наиболее стабильный) карбкатион атакует олефин 4) образующийся карбкатион изомеризуется в результате миграции водорода и метильных групп
Алкилирование парафинов олефинами 1) н-бутилены легко протонируются кислотой и дают карбкатионы 2) вторичный карбкатион взаимодействует с изобутаном 3) третичный (наиболее стабильный) карбкатион атакует олефин 4) образующийся карбкатион изомеризуется в результате миграции водорода и метильных групп
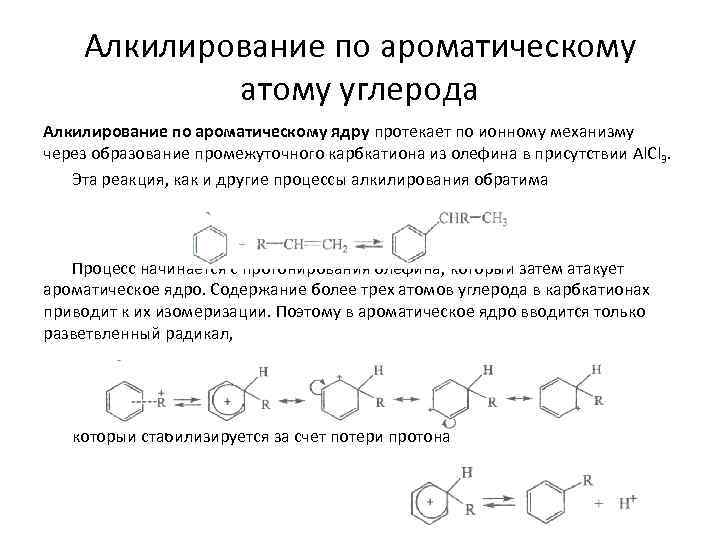 Алкилирование по ароматическому атому углерода Алкилирование по ароматическому ядру протекает по ионному механизму через образование промежуточного карбкатиона из олефина в присутствии Al. Cl 3. Эта реакция, как и другие процессы алкилирования обратима Процесс начинается с протонирования олефина, который затем атакует ароматическое ядро. Содержание более трех атомов углерода в карбкатионах приводит к их изомеризации. Поэтому в ароматическое ядро вводится только разветвленный радикал, который стабилизируется за счет потери протона
Алкилирование по ароматическому атому углерода Алкилирование по ароматическому ядру протекает по ионному механизму через образование промежуточного карбкатиона из олефина в присутствии Al. Cl 3. Эта реакция, как и другие процессы алкилирования обратима Процесс начинается с протонирования олефина, который затем атакует ароматическое ядро. Содержание более трех атомов углерода в карбкатионах приводит к их изомеризации. Поэтому в ароматическое ядро вводится только разветвленный радикал, который стабилизируется за счет потери протона
 3. Процессы, связанные с переносом водорода Гидрирование Риформинг Гидрокрекинг нефтяных остатков Деструктивно-гидрогенизационная переработка ТГИ • Гидроочистка • •
3. Процессы, связанные с переносом водорода Гидрирование Риформинг Гидрокрекинг нефтяных остатков Деструктивно-гидрогенизационная переработка ТГИ • Гидроочистка • •
 Гидрирование (гидрогенизация) — химическая реакция, включающая присоединение водорода к молекуле органического вещества. 1. Присоединение водорода по ненасыщенным связям Эти реакции широко используются для облагораживания топливных фракций. 2. Присоединение водорода к гетероатомному веществу Эти реакции применяют для очистки нефти от гетероатомов при подготовке ее к переработке. 3. Деструктивное гидрирование, гидрокрекинг – реакции, сопровождающиеся разрывом углерод-углеродных связей Эти реакции используются для увеличения выхода жидких продуктов при переработке некачественных ТГИ; для удаления коксовых продуктов при крекинге; для увеличения светлых фракций путем уменьшения молекулярной массы у/в
Гидрирование (гидрогенизация) — химическая реакция, включающая присоединение водорода к молекуле органического вещества. 1. Присоединение водорода по ненасыщенным связям Эти реакции широко используются для облагораживания топливных фракций. 2. Присоединение водорода к гетероатомному веществу Эти реакции применяют для очистки нефти от гетероатомов при подготовке ее к переработке. 3. Деструктивное гидрирование, гидрокрекинг – реакции, сопровождающиеся разрывом углерод-углеродных связей Эти реакции используются для увеличения выхода жидких продуктов при переработке некачественных ТГИ; для удаления коксовых продуктов при крекинге; для увеличения светлых фракций путем уменьшения молекулярной массы у/в
 Каталитический риформинг - это промышленный процесс переработки бензиновых и лигроиновых фракций нефти с целью получения высококачественных бензинов и ароматических углеводородов. Основные реакции: • изомеризация на кислотных центрах парафинов и нафтенов; • дегидрирование нафтеновых у/в; • дегидроциклизация парафинов; • ароматизация; • гидрокрекинг. Катализаторы: Pt, Pt+Re. Гидрокрекинг нефтяных остатков – это переработка высококипящих нефтяных фракций, мазута, вакуумного газойля или деасфальтизата для получения бензина, дизельного и реактивного топлива, смазочных масел, сырья для каталитического крекинга и др. Проводят действием водорода при 330— 450°С и давлении 5 -30 МПа в присутствии никель-молибденовых катализаторов. В процессе гидрокрекинга происходят следующие превращения: Основные реакции: • Гидроочистка — из сырья удаляются сера-азотсодержащие соединения; • Расщепление тяжелых молекул углеводорода на более мелкие; • Насыщение водородом непредельных углеводородов. Катализаторы: Ni-Mo.
Каталитический риформинг - это промышленный процесс переработки бензиновых и лигроиновых фракций нефти с целью получения высококачественных бензинов и ароматических углеводородов. Основные реакции: • изомеризация на кислотных центрах парафинов и нафтенов; • дегидрирование нафтеновых у/в; • дегидроциклизация парафинов; • ароматизация; • гидрокрекинг. Катализаторы: Pt, Pt+Re. Гидрокрекинг нефтяных остатков – это переработка высококипящих нефтяных фракций, мазута, вакуумного газойля или деасфальтизата для получения бензина, дизельного и реактивного топлива, смазочных масел, сырья для каталитического крекинга и др. Проводят действием водорода при 330— 450°С и давлении 5 -30 МПа в присутствии никель-молибденовых катализаторов. В процессе гидрокрекинга происходят следующие превращения: Основные реакции: • Гидроочистка — из сырья удаляются сера-азотсодержащие соединения; • Расщепление тяжелых молекул углеводорода на более мелкие; • Насыщение водородом непредельных углеводородов. Катализаторы: Ni-Mo.
 Деструктивно-гидрогенизационная переработка ТГИ Применяется для повышения топливной и химической ценности продуктов по сравнению с сырьем (за счет повышения отношения Н/С), для увеличения выхода жидких продуктов при переработке некачественных ТГИ; для удаления коксовых продуктов при крекинге; для увеличения светлых фракций путем уменьшения молекулярной массы у/в. • Экстракция углей • Деструктивная гидрогенизация и термическое растворение Катализаторы: оксиды и сульфиды металлов переменной валентности, Т=320420 о. С, Р=5 -15 МПа. Основные типы реакций деструкции. Гидроочистка Применяется для очистки нефти от гетероатомов при подготовке ее к переработке. Катализаторы: Al. Co. Mo, Al. Co. Ni
Деструктивно-гидрогенизационная переработка ТГИ Применяется для повышения топливной и химической ценности продуктов по сравнению с сырьем (за счет повышения отношения Н/С), для увеличения выхода жидких продуктов при переработке некачественных ТГИ; для удаления коксовых продуктов при крекинге; для увеличения светлых фракций путем уменьшения молекулярной массы у/в. • Экстракция углей • Деструктивная гидрогенизация и термическое растворение Катализаторы: оксиды и сульфиды металлов переменной валентности, Т=320420 о. С, Р=5 -15 МПа. Основные типы реакций деструкции. Гидроочистка Применяется для очистки нефти от гетероатомов при подготовке ее к переработке. Катализаторы: Al. Co. Mo, Al. Co. Ni
 4. Окисление углеродсодержащих веществ Процесс окисления углеродсодержащих веществ в технологических процессах аналогичен процессу окисления этих веществ в природных условиях. В природе эти процессы протекают в естественных условиях: атмосферное, давление, t окр. среды, в качестве окислителей выступают влажная среда и кислород воздуха. Это процесс тления, выветривания и т. п. В технологических процессах используются спец. окислители: HNO 3, KMn. O 4, K 2 Cr 2 O 7, H 2 O 2 и др. Давление от 1 до нескольких десятков атмосфер, температура: от t окр. среды до t горения у/в. Окисляемое вещество может быть жидким, твердым или газообразным, а окислитель – жидким или газообразным. • о Окисление алкилзамещенных аренов Окисление парафинов • Выветривание и самовозгорание углей • Окисление и стабилизация топлив и масел
4. Окисление углеродсодержащих веществ Процесс окисления углеродсодержащих веществ в технологических процессах аналогичен процессу окисления этих веществ в природных условиях. В природе эти процессы протекают в естественных условиях: атмосферное, давление, t окр. среды, в качестве окислителей выступают влажная среда и кислород воздуха. Это процесс тления, выветривания и т. п. В технологических процессах используются спец. окислители: HNO 3, KMn. O 4, K 2 Cr 2 O 7, H 2 O 2 и др. Давление от 1 до нескольких десятков атмосфер, температура: от t окр. среды до t горения у/в. Окисляемое вещество может быть жидким, твердым или газообразным, а окислитель – жидким или газообразным. • о Окисление алкилзамещенных аренов Окисление парафинов • Выветривание и самовозгорание углей • Окисление и стабилизация топлив и масел
 5. Газификация горючих ископаемых Газификация – это процесс высокотемпературного взаимодействия горючих ископаемых с парами воды, O 2, CO 2 или их смесями с целью получения горючих газов: H 2, CO, CH 4, которые в дальнейшем могут использоваться как топливо (синтез-газ) или как сырье для химической промышленности. • Воздушный газ: 2 С+O 2+3, 76 N 2=2 CO+3, 76 N 2 • Водяной газ: C+H 20=CO+H 2 • Полуводяной газ: 3, 65 C+O 2+1, 65 H 2 O+3, 76 N 2=3, 65 CO+1, 65 H 2+3, 76 N 2 • Оксиводяной газ: 3, 65 C+O 2+1, 65 H 2 O=3, 65 CO+1, 65 H 2 Получение синтез-газа: СН 4+Н 2 О=СО+3 Н 2 СН 4+СО 2=2 СО+2 Н 2 Т=800 -900 о. С СН 4+0, 5 О 2=СО+2 Н 2 Катализатор: Ni, нанесенный на Al 2 O 3
5. Газификация горючих ископаемых Газификация – это процесс высокотемпературного взаимодействия горючих ископаемых с парами воды, O 2, CO 2 или их смесями с целью получения горючих газов: H 2, CO, CH 4, которые в дальнейшем могут использоваться как топливо (синтез-газ) или как сырье для химической промышленности. • Воздушный газ: 2 С+O 2+3, 76 N 2=2 CO+3, 76 N 2 • Водяной газ: C+H 20=CO+H 2 • Полуводяной газ: 3, 65 C+O 2+1, 65 H 2 O+3, 76 N 2=3, 65 CO+1, 65 H 2+3, 76 N 2 • Оксиводяной газ: 3, 65 C+O 2+1, 65 H 2 O=3, 65 CO+1, 65 H 2 Получение синтез-газа: СН 4+Н 2 О=СО+3 Н 2 СН 4+СО 2=2 СО+2 Н 2 Т=800 -900 о. С СН 4+0, 5 О 2=СО+2 Н 2 Катализатор: Ni, нанесенный на Al 2 O 3
 6. Синтезы на основе CO и H 2 позволяют получать широкий спектр продуктов: углеводороды, спирты, карбоновые кислоты, альдегиды, кетоны, олефины. 1. Синтез Фишера-Тропша представляет собой каталитическое гидрирование оксида углерода с образованием смеси углеводородов; в зависимости от катализатора и условий, в которых осуществляется синтез, процесс преимущественно протекает по схеме (1) или (2):
6. Синтезы на основе CO и H 2 позволяют получать широкий спектр продуктов: углеводороды, спирты, карбоновые кислоты, альдегиды, кетоны, олефины. 1. Синтез Фишера-Тропша представляет собой каталитическое гидрирование оксида углерода с образованием смеси углеводородов; в зависимости от катализатора и условий, в которых осуществляется синтез, процесс преимущественно протекает по схеме (1) или (2):
 6. Синтезы на основе CO и H 2 2. Оксосинтез (гидроформилирование) – образование альдегидов, кетонов и т. п. из CO и H 2 и непредельных углеводородов. Катализаторы – карбонилы металлов VIII группы (например [HCo(CO)4]). Классификация процессов в зависимости от используемых реагентов Реагенты Название процесса Катализатор CO + H 2 + олефины гидроформилирование CO + H 2 О + олефины гидрокарбоксилирование карбонилы Ni CO + OCH 3 + олефины гидрометоксилирование карбонилы Rh карбонилы Co
6. Синтезы на основе CO и H 2 2. Оксосинтез (гидроформилирование) – образование альдегидов, кетонов и т. п. из CO и H 2 и непредельных углеводородов. Катализаторы – карбонилы металлов VIII группы (например [HCo(CO)4]). Классификация процессов в зависимости от используемых реагентов Реагенты Название процесса Катализатор CO + H 2 + олефины гидроформилирование CO + H 2 О + олефины гидрокарбоксилирование карбонилы Ni CO + OCH 3 + олефины гидрометоксилирование карбонилы Rh карбонилы Co
 Основные процессы технологии природных энергоносителей 1. Термические процессы • Крекинг и пиролиз • Сажеобразование • Полукоксование и коксование 2. Каталитические процессы • Каталитический крекинг • Алкилирование 3. Процессы, связанные с переносом водорода • Гидрирование • Каталитический риформинг • Гидрокрекинг • Гидроочистка • Деструктивно-гидрогенизационная переработка ТГИ 4. Окисление 5. Газификация 6. Синтезы на основе углерода и водорода • Синтез Фишера-Тропша • Оксосинтез
Основные процессы технологии природных энергоносителей 1. Термические процессы • Крекинг и пиролиз • Сажеобразование • Полукоксование и коксование 2. Каталитические процессы • Каталитический крекинг • Алкилирование 3. Процессы, связанные с переносом водорода • Гидрирование • Каталитический риформинг • Гидрокрекинг • Гидроочистка • Деструктивно-гидрогенизационная переработка ТГИ 4. Окисление 5. Газификация 6. Синтезы на основе углерода и водорода • Синтез Фишера-Тропша • Оксосинтез


