crystallization_4096.ppt
- Количество слайдов: 10

Процессы образования новой фазы Кристаллизация А. В. Шишкин, АЭТУ, НГТУ

1. Кристаллизация в однокомпонентной системе n n Процесс кристаллизации представляет собой фазовое превращение 1 -го рода, в результате которого выделяется теплота кристаллизации. При кристаллизации однокомпонентной системы (чистого вещества) условия фазового равновесия упрощаются – остаются только термическое равновесие: T (I) = T (j) и механическое равновесие: p (i) = p (j). Поэтому протекание неравновесной кристаллизации в однокомпонентной системе может быть только при нарушении термического или механического равновесия. Время релаксации системы к термическому T и механическому p равновесиям может быть оценено из следующих соотношений: T = r 2 / a; p = r / vs, где r – характерный размер системы; a – коэффициент температуропроводности; vs – скорость звука. Величины a и vs не очень сильно изменяются при фазовом 2/17/2018 А. В. Шишкин, АЭТУ, НГТУ 2 превращении и переохлаждении. Значения и для твердой и

2. Кристаллизация в многокомпонентной системе n n При кристаллизации бинарной или многокомпонентной системы в соответствии с условиями должно также соблюдаться равенство химических потенциалов компонентов в различных фазах (равновесие относительно диффузии). Время диффузионной релаксации системы D может быть оценено из выражения: D = r 2 / D, где D – коэффициент взаимной диффузии (для бинарной системы). Коэффициент диффузии существенно зависит от агрегатного состояния вещества и температуры. С переходом в твердое состояние и с понижением температуры коэффициент диффузии может понизиться на несколько порядков, что приведет к существенному росту времени диффузионной релаксации ( D >> T >> p). Поэтому неравновесная кристаллизация в многокомпонентной системе связана в первую очередь с отсутствием равновесия относительно диффузии. 2/17/2018 А. В. Шишкин, АЭТУ, НГТУ 3

2. 1. Режимы кристаллизации n n Диффузия успевает происходить и в жидкой фазе, и в твердой, и между ними, т. е. D L D S D L S, где индексы L и S относятся к жидкой и твердой фазам соответственно, реализуется равновесный режим кристаллизации. Диффузия в твердой фазе отсутствует или происходит слабо, однако проходит в жидкой фазе и между фазами, D S << (D L S), а следовательно, полное равновесие относительно диффузии не устанавливается, квазиравновесный режим кристаллизации. Диффузия в твердой фазе и между фазами не происходит или происходит слабо, D L >> (D S D L S), диффузионнокинетический режим кристаллизации. Диффузия в процессе кристаллизации не успевает происходить ни в жидкой, ни в твердой фазах; причина этого не только в том, что мал коэффициент диффузии, но и в том, что скорость проведения процесса (скорость кристаллизации, скорость охлаждения) велика, время проведения процесса мало кинетический режим кристаллизации, закалка. 2/17/2018 А. В. Шишкин, АЭТУ, НГТУ 4
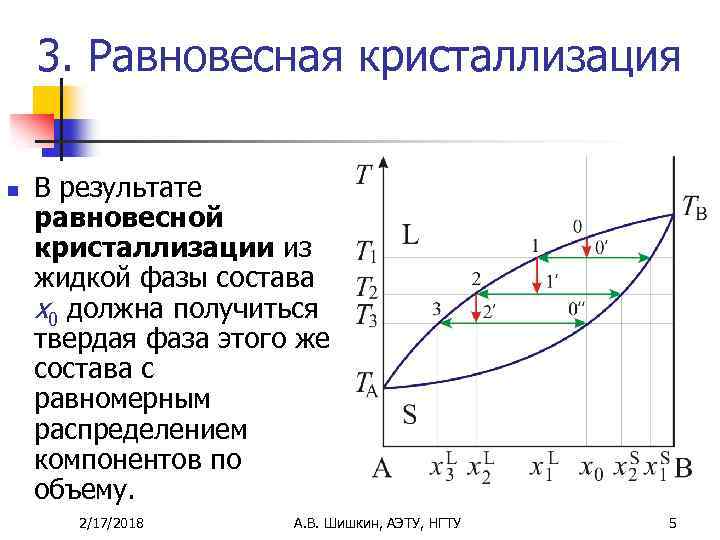
3. Равновесная кристаллизация n В результате равновесной кристаллизации из жидкой фазы состава x 0 должна получиться твердая фаза этого же состава с равномерным распределением компонентов по объему. 2/17/2018 А. В. Шишкин, АЭТУ, НГТУ 5

4. Неравновесная кристаллизация n n n При той же температуре D L >> D S ввиду различия механизмов диффузии в жидкой и твердой фазах. Ослабление диффузии между фазами объясняется: n относительным уменьшением границы раздела фаз в сравнении с растущим объемом твердой фазы; n гравитационной ликвацией, т. е. пространственным разделением фаз разной плотности в гравитационном поле; n обеднением поверхностного слоя твердой фазы тугоплавким компонентом в результате плохой диффузии в твердой фазе. Поэтому чаще реализуется диффузионно-кинетический режим кристаллизации: D L >> (D S D L S). 2/17/2018 А. В. Шишкин, АЭТУ, НГТУ 6
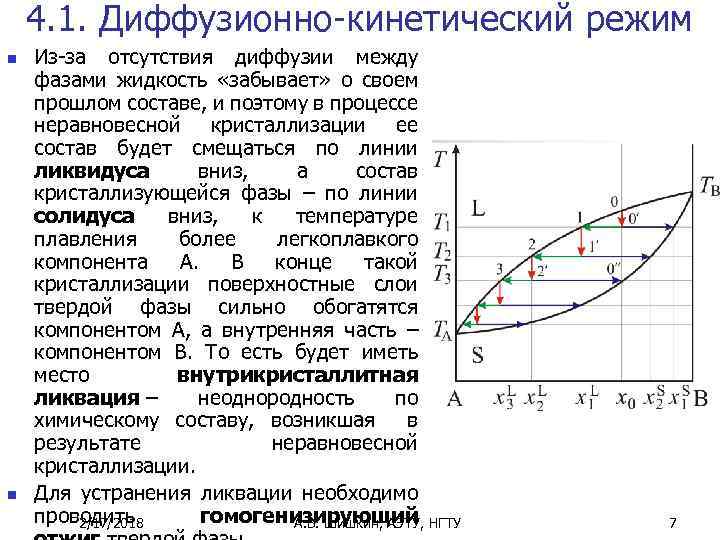
4. 1. Диффузионно-кинетический режим n n Из-за отсутствия диффузии между фазами жидкость «забывает» о своем прошлом составе, и поэтому в процессе неравновесной кристаллизации ее состав будет смещаться по линии ликвидуса вниз, а состав кристаллизующейся фазы – по линии солидуса вниз, к температуре плавления более легкоплавкого компонента A. В конце такой кристаллизации поверхностные слои твердой фазы сильно обогатятся компонентом A, а внутренняя часть – компонентом B. То есть будет иметь место внутрикристаллитная ликвация – неоднородность по химическому составу, возникшая в результате неравновесной кристаллизации. Для устранения ликвации необходимо проводить гомогенизирующий 2/17/2018 А. В. Шишкин, АЭТУ, НГТУ 7

4. 2. Кинетический режим n n При неполном прохождении разделительной диффузии в жидкой фазе в процессе кристаллизации фазовое равновесие нарушится, фазовая диаграмма уже не будет отвечать равновесному случаю, и кристаллизующаяся фаза станет в большей степени обогащаться на начальных стадиях более тугоплавким компонентом B. Качественно результат останется тем же – наличие ликвации. 2/17/2018 А. В. Шишкин, АЭТУ, НГТУ 8

4. 3. Бездиффузионная кристаллизация n n Бездиффузионная кристаллизация имеет место лишь в том случае, когда термодинамически разрешен процесс кристаллизации, но диффузия ни в одной из фаз произойти не успевает. Разделительная диффузия в процессе кристаллизации не успевает произойти только в том случае, когда скорость диффузии меньше скорости кристаллизации или длина диффузионного перемещения l. D меньше размера закристаллизовавшейся за это время области. То есть при бездиффузионной кристаллизации происходит захват растворенного компонента. Время элементарного акта диффузии: D = l. D 2 / D. Скорость кристаллизации: vc = v. T / (d. T / d. N), где v. T – скорость охлаждения; N – нормаль к поверхности кристаллизации; T – температура. Тогда время кристаллизации области с размером l. D может быть оценено так: c = l. D / vc = (l. D / v. T)(d. T / d. N). Тогда из неравенства c << D получим выражение для скорости охлаждения при бездиффузионной кристаллизации: v. T >> (D / l. D)(d. T / d. N). 2/17/2018 9 2 А. В. Шишкин, АЭТУ, НГТУ – 10 2 9
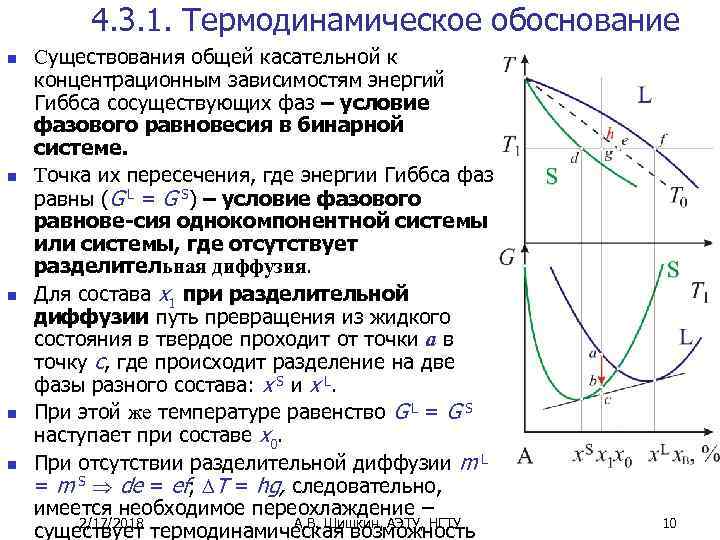
4. 3. 1. Термодинамическое обоснование n n n Существования общей касательной к концентрационным зависимостям энергий Гиббса сосуществующих фаз – условие фазового равновесия в бинарной системе. Точка их пересечения, где энергии Гиббса фаз равны (G L = G S) – условие фазового равнове-сия однокомпонентной системы или системы, где отсутствует разделительная диффузия. Для состава x 1 при разделительной диффузии путь превращения из жидкого состояния в твердое проходит от точки a в точку c, где происходит разделение на две фазы разного состава: x S и x L. При этой же температуре равенство G L = G S наступает при составе x 0. При отсутствии разделительной диффузии m L = m S de = ef; T = hg, следовательно, имеется необходимое переохлаждение – 2/17/2018 А. В. Шишкин, АЭТУ, НГТУ существует термодинамическая возможность 10
crystallization_4096.ppt