ЛК НТ-10 25.11.13.pptx
- Количество слайдов: 54
 Процессы на поверхности раздела ж-т НТ-10
Процессы на поверхности раздела ж-т НТ-10
 Смачиваемость поверхности Уравнение Венцеля – Смачивание шероховатой поверхности в статических условиях
Смачиваемость поверхности Уравнение Венцеля – Смачивание шероховатой поверхности в статических условиях
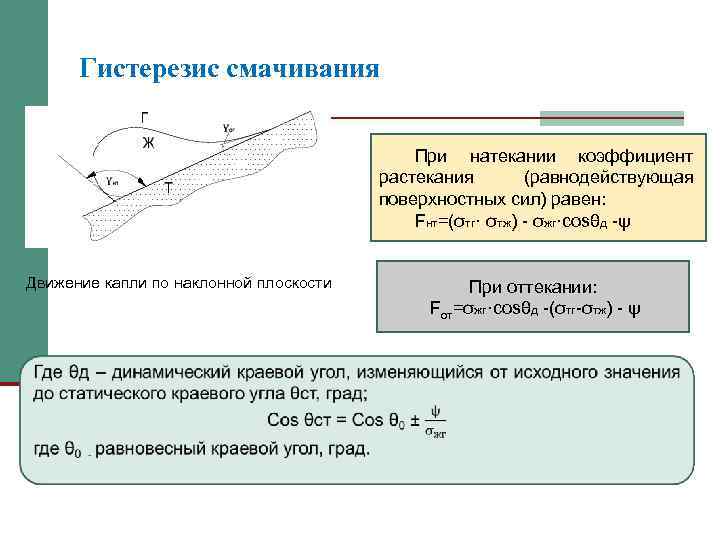 Гистерезис смачивания При натекании коэффициент растекания (равнодействующая поверхностных сил) равен: Fнт=(σтг· σтж) - σжг·сosθд -ψ Движение капли по наклонной плоскости При оттекании: Fот=σжг·cosθд -(σтг-σтж) - ψ
Гистерезис смачивания При натекании коэффициент растекания (равнодействующая поверхностных сил) равен: Fнт=(σтг· σтж) - σжг·сosθд -ψ Движение капли по наклонной плоскости При оттекании: Fот=σжг·cosθд -(σтг-σтж) - ψ
 Гистерезис смачивания n Под действием гравитационной силы, помимо шероховатости, скорость смачивания снижается с увеличением пористости поверхности, так как этому способствует физико-химический гистерезис смачивания как результат отпитывания жидкости в поры Краевой угол при смачивании пористой поверхности определяется по формуле: Cosθп = fт· Cosθ – fп где θ-равновесный краевой угол смачивания твердой поверхности, град; fт, fп- доли поверхности, занятые соответственно сплошным материалом и Смачивание пористой поверхности порами
Гистерезис смачивания n Под действием гравитационной силы, помимо шероховатости, скорость смачивания снижается с увеличением пористости поверхности, так как этому способствует физико-химический гистерезис смачивания как результат отпитывания жидкости в поры Краевой угол при смачивании пористой поверхности определяется по формуле: Cosθп = fт· Cosθ – fп где θ-равновесный краевой угол смачивания твердой поверхности, град; fт, fп- доли поверхности, занятые соответственно сплошным материалом и Смачивание пористой поверхности порами
 Гистерезис смачивания Кинетическим гистерезисом смачивания принято называть изменение угла смачивания при передвижении по твердой поверхности трехфазного периметра смачивания. Величина гистерезиса зависит от: - направления движения периметра смачивания, то есть от того, происходит ли вытеснение с твердой поверхности воды; - скорости перемещения трехфазной границы раздела фаз по твердой поверхности; - - шероховатости твердой поверхности; - адсорбции на поверхности веществ.
Гистерезис смачивания Кинетическим гистерезисом смачивания принято называть изменение угла смачивания при передвижении по твердой поверхности трехфазного периметра смачивания. Величина гистерезиса зависит от: - направления движения периметра смачивания, то есть от того, происходит ли вытеснение с твердой поверхности воды; - скорости перемещения трехфазной границы раздела фаз по твердой поверхности; - - шероховатости твердой поверхности; - адсорбции на поверхности веществ.
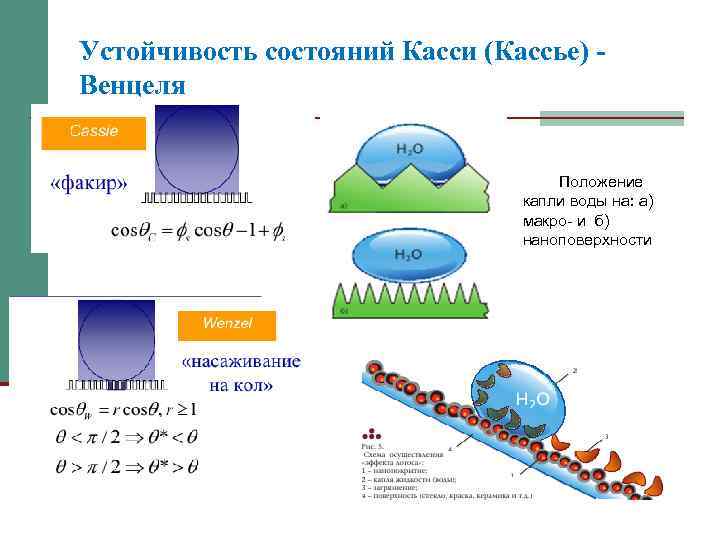 Устойчивость состояний Касси (Кассье) Венцеля Положение капли воды на: а) макро- и б) наноповерхности
Устойчивость состояний Касси (Кассье) Венцеля Положение капли воды на: а) макро- и б) наноповерхности
 Линейное натяжение Избыточную энергию линии трехфазного контакта по сравнению с энергией поверхности жидкости (для одинакового числа молекул) называют линейным натяжением (χ). 1 Дж= 1 н·м- линейное натяжение имеет размерность силы – ньютон (Н). p Эта сила направлена вдоль линии смачивания, она создает двумерное давление: p р*=к/r (уравнение Веселовского- Перцова (1936) p p С учетом (χ) равновесный краевой угол θ определяет уравнение Шелудко-Тошева-Платиканова (1980): Cos θ* = Cos θ – k/σr
Линейное натяжение Избыточную энергию линии трехфазного контакта по сравнению с энергией поверхности жидкости (для одинакового числа молекул) называют линейным натяжением (χ). 1 Дж= 1 н·м- линейное натяжение имеет размерность силы – ньютон (Н). p Эта сила направлена вдоль линии смачивания, она создает двумерное давление: p р*=к/r (уравнение Веселовского- Перцова (1936) p p С учетом (χ) равновесный краевой угол θ определяет уравнение Шелудко-Тошева-Платиканова (1980): Cos θ* = Cos θ – k/σr
 Краевой угол на фрактальной поверхности n Фрактальные поверхности- сильно шероховатые поверхности, поэтому краевой угол на подложке с фрактальной структурой будет отличаться от краевого угла для гладкой подложки. n Для фрактальных поверхностей площадь будет определяться размером молекул.
Краевой угол на фрактальной поверхности n Фрактальные поверхности- сильно шероховатые поверхности, поэтому краевой угол на подложке с фрактальной структурой будет отличаться от краевого угла для гладкой подложки. n Для фрактальных поверхностей площадь будет определяться размером молекул.
 Краевой угол на фрактальной поверхности Выражение для равновесного краевого угла на фрактальной поверхности : Cos θf = (γsv – γsl )/γlv {[(1 - (γsv/ γsl)·(d 2/d 1)2 -df /(1 - γsv/γsl)](d 1/ Δ 0) 2 -df } = = Cos θ 0 {[(1 - (γsv/ γsl)·(d 2/d 1)2 -df /(1 - γsv/ γsl)](d 1/ Δ 0) 2 -df } (1) Примем, что фрактальная структура поверхности начнет проявляться с масштаба δ 0 и ограничена сверху масштабом Δ 0. Пусть d 1 – размер молекул жидкости, а d 2 – размер молекул газа (или эквивалентной ему фазы), df – фрактальная размерность поверхности. Из формулы видно, что краевой угол на фрактальной поверхности определяется не только величиной межфазного натяжения, но и размерами молекул. А также масштабом , отвечающим верхнему пределу фрактального поведения поверхности. Если нижний предел δ 0 превышает размеры молекул, то формула(1) существенно упрощается. В этом случае, площадь межфазной поверхности, измеренная на масштабах δ 0, d 1 и d 2 имеет одну и ту же величину, поэтому в формуле (1) можно заменить d 1 и d 2 на δ 0, что приводит к достаточно простому выражению: Cos θ f = Cos θ 0 ·( δ 0/ Δ 0) 2 -df
Краевой угол на фрактальной поверхности Выражение для равновесного краевого угла на фрактальной поверхности : Cos θf = (γsv – γsl )/γlv {[(1 - (γsv/ γsl)·(d 2/d 1)2 -df /(1 - γsv/γsl)](d 1/ Δ 0) 2 -df } = = Cos θ 0 {[(1 - (γsv/ γsl)·(d 2/d 1)2 -df /(1 - γsv/ γsl)](d 1/ Δ 0) 2 -df } (1) Примем, что фрактальная структура поверхности начнет проявляться с масштаба δ 0 и ограничена сверху масштабом Δ 0. Пусть d 1 – размер молекул жидкости, а d 2 – размер молекул газа (или эквивалентной ему фазы), df – фрактальная размерность поверхности. Из формулы видно, что краевой угол на фрактальной поверхности определяется не только величиной межфазного натяжения, но и размерами молекул. А также масштабом , отвечающим верхнему пределу фрактального поведения поверхности. Если нижний предел δ 0 превышает размеры молекул, то формула(1) существенно упрощается. В этом случае, площадь межфазной поверхности, измеренная на масштабах δ 0, d 1 и d 2 имеет одну и ту же величину, поэтому в формуле (1) можно заменить d 1 и d 2 на δ 0, что приводит к достаточно простому выражению: Cos θ f = Cos θ 0 ·( δ 0/ Δ 0) 2 -df
 Статический краевой угол n При статическом методе размер капли не меняется в течение всего измерения, но это не означает, что угол контакта всегда остается постоянным. n Наоборот, воздействие внешних факторов может привести к изменению угла контакта со временем. n Из-за седиментации, испарения и аналогичных химических или физических взаимодействий краевой угол будет самопроизвольно изменяться со временем. n С одной стороны, статический краевой угол не может абсолютно оценить свободную энергию твердой поверхности, а с другой, он позволяет охарактеризовать временную зависимость таких процессов как высыхание чернил, нанесение клея, абсорбцию и адсорбцию жидкостей на бумаге.
Статический краевой угол n При статическом методе размер капли не меняется в течение всего измерения, но это не означает, что угол контакта всегда остается постоянным. n Наоборот, воздействие внешних факторов может привести к изменению угла контакта со временем. n Из-за седиментации, испарения и аналогичных химических или физических взаимодействий краевой угол будет самопроизвольно изменяться со временем. n С одной стороны, статический краевой угол не может абсолютно оценить свободную энергию твердой поверхности, а с другой, он позволяет охарактеризовать временную зависимость таких процессов как высыхание чернил, нанесение клея, абсорбцию и адсорбцию жидкостей на бумаге.
 Динамический краевой угол n Динамический угол контакта описывает процессы на границе твердое тело/жидкость во время увеличения объема капли (наступающий угол) или при уменьшении капли (отступающий угол), т. е. во время смачивания и осушения. n Граница не образуется мгновенно, для достижения динамического равновесия требуется время. n Из практики рекомендуется устанавливать поток жидкости 5 - 15 мл/мин, более высокая скорость потока будет только имитировать динамические методы.
Динамический краевой угол n Динамический угол контакта описывает процессы на границе твердое тело/жидкость во время увеличения объема капли (наступающий угол) или при уменьшении капли (отступающий угол), т. е. во время смачивания и осушения. n Граница не образуется мгновенно, для достижения динамического равновесия требуется время. n Из практики рекомендуется устанавливать поток жидкости 5 - 15 мл/мин, более высокая скорость потока будет только имитировать динамические методы.
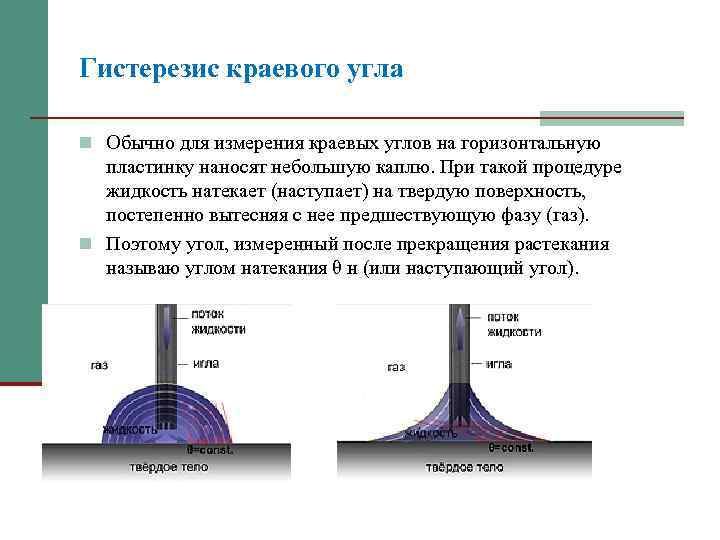 Гистерезис краевого угла n Обычно для измерения краевых углов на горизонтальную пластинку наносят небольшую каплю. При такой процедуре жидкость натекает (наступает) на твердую поверхность, постепенно вытесняя с нее предшествующую фазу (газ). n Поэтому угол, измеренный после прекращения растекания называю углом натекания θ н (или наступающий угол).
Гистерезис краевого угла n Обычно для измерения краевых углов на горизонтальную пластинку наносят небольшую каплю. При такой процедуре жидкость натекает (наступает) на твердую поверхность, постепенно вытесняя с нее предшествующую фазу (газ). n Поэтому угол, измеренный после прекращения растекания называю углом натекания θ н (или наступающий угол).
 Различные виды структуры переходной зоны вблизи линии трехфазного контакта n Для реальных тел: равновесный угол смачивания равен полусумме предельных углов натекания и оттекания: n cos(θ) = [cos(θ нт) + сos(θ от)]/2
Различные виды структуры переходной зоны вблизи линии трехфазного контакта n Для реальных тел: равновесный угол смачивания равен полусумме предельных углов натекания и оттекания: n cos(θ) = [cos(θ нт) + сos(θ от)]/2
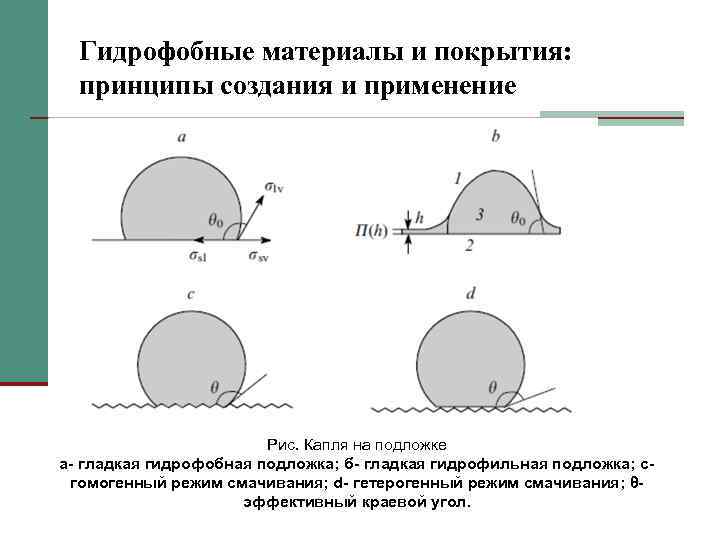 Гидрофобные материалы и покрытия: принципы создания и применение Рис. Капля на подложке а- гладкая гидрофобная подложка; б- гладкая гидрофильная подложка; сгомогенный режим смачивания; d- гетерогенный режим смачивания; θэффективный краевой угол.
Гидрофобные материалы и покрытия: принципы создания и применение Рис. Капля на подложке а- гладкая гидрофобная подложка; б- гладкая гидрофильная подложка; сгомогенный режим смачивания; d- гетерогенный режим смачивания; θэффективный краевой угол.
 Адгезия – взаимодействие между разнородными конденсированными телами при их молекулярном контакте. Причина адгезии – молекулярное притяжение контактирующих веществ или их химическое взаимодействие. Работа адгезии (WА) – работа, которую необходимо совершить для разделения двух контактирующих фаз. Уравнение Дюпре:
Адгезия – взаимодействие между разнородными конденсированными телами при их молекулярном контакте. Причина адгезии – молекулярное притяжение контактирующих веществ или их химическое взаимодействие. Работа адгезии (WА) – работа, которую необходимо совершить для разделения двух контактирующих фаз. Уравнение Дюпре:
 Межмолекулярные и межфазные взаимодействия Когезия – притяжение атомов или молекул внутри отдельной фазы, обусловленное межмолекулярными и межатомными взаимодействиями различной природы. Работа когезии (Wк) - работа, затрачиваемая на разрыв тела по сечению, равному единице площади.
Межмолекулярные и межфазные взаимодействия Когезия – притяжение атомов или молекул внутри отдельной фазы, обусловленное межмолекулярными и межатомными взаимодействиями различной природы. Работа когезии (Wк) - работа, затрачиваемая на разрыв тела по сечению, равному единице площади.
 Растекание жидкости Правило Гаркинса - растекание одной жидкости по поверхности другой происходит, если прилипание между двумя жидкостями больше, чем сцепление молекул растекающейся жидкости (WA > WK). Коэффициент растекания φ = WА – WК, φ >0 растекание, φ <0, растекание не происходит. Способность к растеканию зависит от когезии наносимой жидкости. Многие органические вещества растекаются по поверхности воды, а вода, как правило, не растекается на поверхности органических веществ. 17
Растекание жидкости Правило Гаркинса - растекание одной жидкости по поверхности другой происходит, если прилипание между двумя жидкостями больше, чем сцепление молекул растекающейся жидкости (WA > WK). Коэффициент растекания φ = WА – WК, φ >0 растекание, φ <0, растекание не происходит. Способность к растеканию зависит от когезии наносимой жидкости. Многие органические вещества растекаются по поверхности воды, а вода, как правило, не растекается на поверхности органических веществ. 17
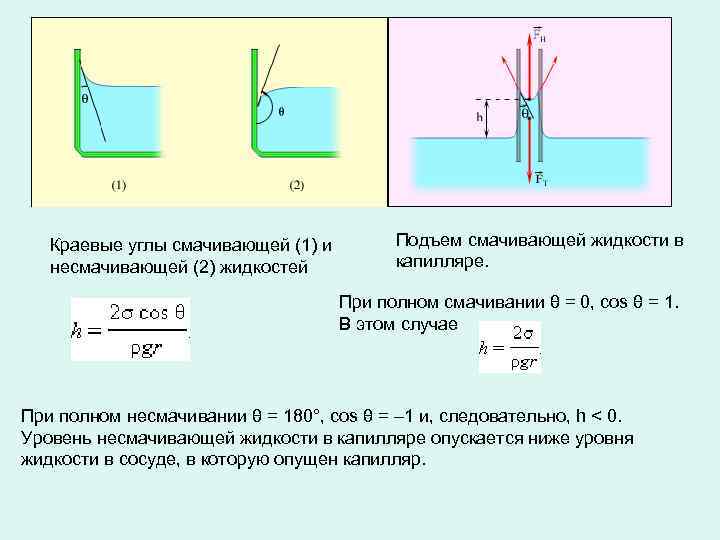 Краевые углы смачивающей (1) и несмачивающей (2) жидкостей Подъем смачивающей жидкости в капилляре. При полном смачивании θ = 0, cos θ = 1. В этом случае При полном несмачивании θ = 180°, cos θ = – 1 и, следовательно, h < 0. Уровень несмачивающей жидкости в капилляре опускается ниже уровня жидкости в сосуде, в которую опущен капилляр.
Краевые углы смачивающей (1) и несмачивающей (2) жидкостей Подъем смачивающей жидкости в капилляре. При полном смачивании θ = 0, cos θ = 1. В этом случае При полном несмачивании θ = 180°, cos θ = – 1 и, следовательно, h < 0. Уровень несмачивающей жидкости в капилляре опускается ниже уровня жидкости в сосуде, в которую опущен капилляр.
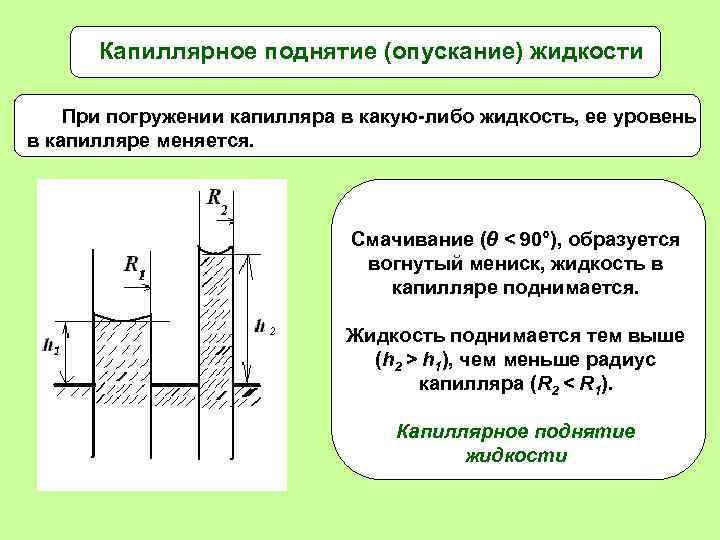 Капиллярное поднятие (опускание) жидкости При погружении капилляра в какую-либо жидкость, ее уровень в капилляре меняется. Смачивание (θ < 90°), образуется вогнутый мениск, жидкость в капилляре поднимается. Жидкость поднимается тем выше (h 2 > h 1), чем меньше радиус капилляра (R 2 < R 1). Капиллярное поднятие жидкости
Капиллярное поднятие (опускание) жидкости При погружении капилляра в какую-либо жидкость, ее уровень в капилляре меняется. Смачивание (θ < 90°), образуется вогнутый мениск, жидкость в капилляре поднимается. Жидкость поднимается тем выше (h 2 > h 1), чем меньше радиус капилляра (R 2 < R 1). Капиллярное поднятие жидкости
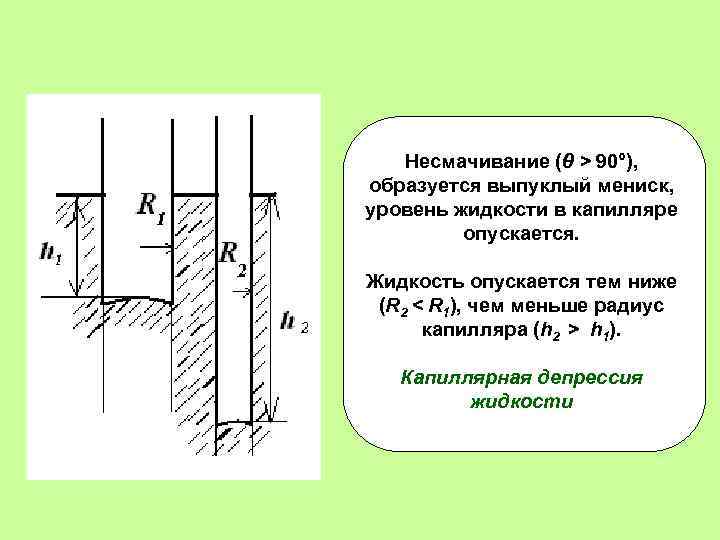 Несмачивание (θ > 90°), образуется выпуклый мениск, уровень жидкости в капилляре опускается. Жидкость опускается тем ниже (R 2 < R 1), чем меньше радиус капилляра (h 2 > h 1). Капиллярная депрессия жидкости
Несмачивание (θ > 90°), образуется выпуклый мениск, уровень жидкости в капилляре опускается. Жидкость опускается тем ниже (R 2 < R 1), чем меньше радиус капилляра (h 2 > h 1). Капиллярная депрессия жидкости
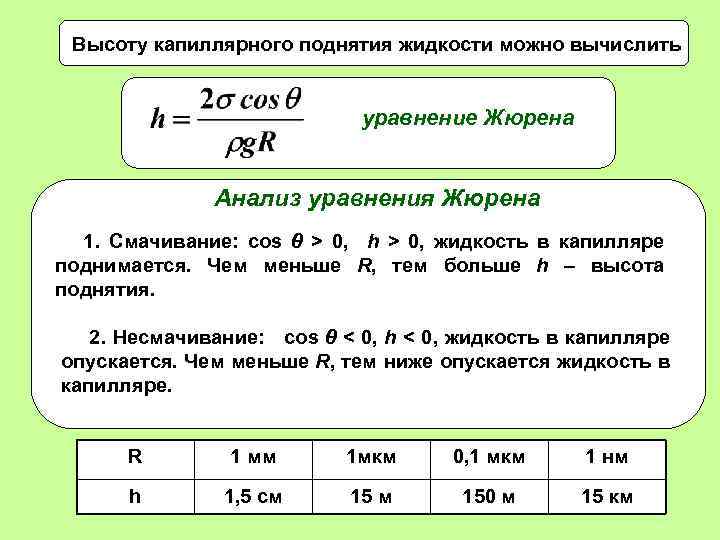 Высоту капиллярного поднятия жидкости можно вычислить уравнение Жюрена Анализ уравнения Жюрена 1. Смачивание: cos θ > 0, h > 0, жидкость в капилляре поднимается. Чем меньше R, тем больше h – высота поднятия. 2. Несмачивание: cos θ < 0, h < 0, жидкость в капилляре опускается. Чем меньше R, тем ниже опускается жидкость в капилляре. R 1 мм 1 мкм 0, 1 мкм 1 нм h 1, 5 см 150 м 15 км
Высоту капиллярного поднятия жидкости можно вычислить уравнение Жюрена Анализ уравнения Жюрена 1. Смачивание: cos θ > 0, h > 0, жидкость в капилляре поднимается. Чем меньше R, тем больше h – высота поднятия. 2. Несмачивание: cos θ < 0, h < 0, жидкость в капилляре опускается. Чем меньше R, тем ниже опускается жидкость в капилляре. R 1 мм 1 мкм 0, 1 мкм 1 нм h 1, 5 см 150 м 15 км
 Высокогидрофобное состояние поверхностей материалов и гистерезис смачивания n Путем изменения химического состава материала либо применения различных гидрофобизирующих агентов на гладких поверхностях можно достичь краевых углов < 120 о. n Для получения материалов с большими краевыми углами необходимо использовать совместное влияние шероховатости поверхности и химической структуры. n Именно подбором поверхностной текстуры можно достичь супергидрофобных состояний
Высокогидрофобное состояние поверхностей материалов и гистерезис смачивания n Путем изменения химического состава материала либо применения различных гидрофобизирующих агентов на гладких поверхностях можно достичь краевых углов < 120 о. n Для получения материалов с большими краевыми углами необходимо использовать совместное влияние шероховатости поверхности и химической структуры. n Именно подбором поверхностной текстуры можно достичь супергидрофобных состояний
 Методы создания текстурированных супергидрофобных поверхностей
Методы создания текстурированных супергидрофобных поверхностей
 Методы создания текстурированных супергидрофобных поверхностей
Методы создания текстурированных супергидрофобных поверхностей
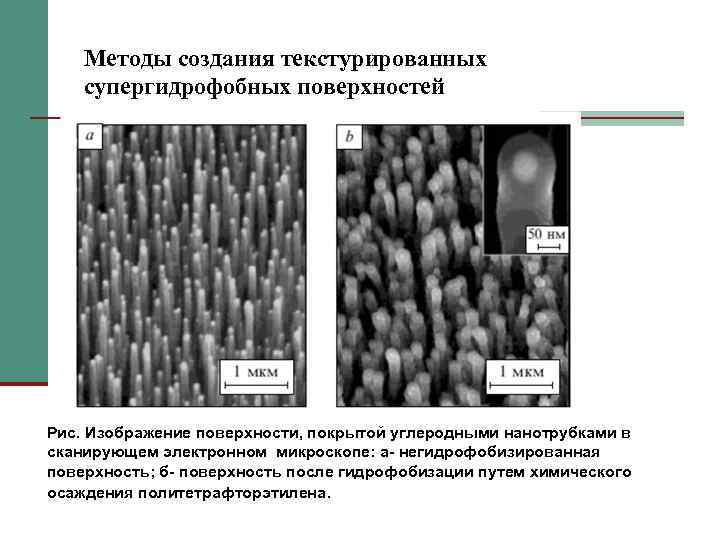 Методы создания текстурированных супергидрофобных поверхностей Рис. Изображение поверхности, покрытой углеродными нанотрубками в сканирующем электронном микроскопе: а- негидрофобизированная поверхность; б- поверхность после гидрофобизации путем химического осаждения политетрафторэтилена.
Методы создания текстурированных супергидрофобных поверхностей Рис. Изображение поверхности, покрытой углеродными нанотрубками в сканирующем электронном микроскопе: а- негидрофобизированная поверхность; б- поверхность после гидрофобизации путем химического осаждения политетрафторэтилена.
 Методы создания текстурированных супергидрофобных поверхностей Рис. Изображения в атомно-силовом микроскопе поверхности полибутадиеновой пленки после плазменного травления в течение 5 мин в атмосфере тетрафторида углерода.
Методы создания текстурированных супергидрофобных поверхностей Рис. Изображения в атомно-силовом микроскопе поверхности полибутадиеновой пленки после плазменного травления в течение 5 мин в атмосфере тетрафторида углерода.
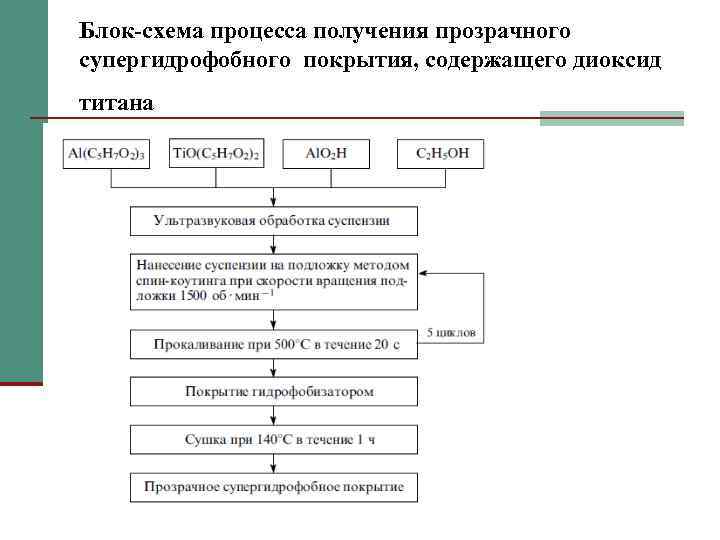 Блок-схема процесса получения прозрачного супергидрофобного покрытия, содержащего диоксид титана
Блок-схема процесса получения прозрачного супергидрофобного покрытия, содержащего диоксид титана

 Нанесение гидрофобных агентов на гладкие и текстурированные поверхности n Поверхностная энергия и смачиваемость зависят не n n n только от химического строения поверхности и ее текстуры. В значительной степени проявляется зависимость краевого угла от ориентации молекул на поверхности и степени их упорядочения. Для нанесения гидрофобизирующих монослоев чаще всего используют следующие методы: дип-коутинга (Dip-Coating), спин-коутинга (Spin- Coating), адсорбции из растворов или паров и испаряющейся капли.
Нанесение гидрофобных агентов на гладкие и текстурированные поверхности n Поверхностная энергия и смачиваемость зависят не n n n только от химического строения поверхности и ее текстуры. В значительной степени проявляется зависимость краевого угла от ориентации молекул на поверхности и степени их упорядочения. Для нанесения гидрофобизирующих монослоев чаще всего используют следующие методы: дип-коутинга (Dip-Coating), спин-коутинга (Spin- Coating), адсорбции из растворов или паров и испаряющейся капли.
 Нанесение гидрофобных агентов на гладкие и текстурированные поверхности n Метод дип-коутинга, или погружения, заключается в предварительном погружении и последующем извлечении образца из раствора, содержащего фобизирующий агент либо дисперсию гидрофобных частиц. n При нанесении покрытия из раствора его равномерность по толщине определяется возможностью поддержания постоянной скорости погружения и извлечения подложки, n в то время как толщина покрытия зависит от скорости движения отступающего (наступающего) мениска жидкости, концентрации гидрофобизирующего агента и вязкости раствора.
Нанесение гидрофобных агентов на гладкие и текстурированные поверхности n Метод дип-коутинга, или погружения, заключается в предварительном погружении и последующем извлечении образца из раствора, содержащего фобизирующий агент либо дисперсию гидрофобных частиц. n При нанесении покрытия из раствора его равномерность по толщине определяется возможностью поддержания постоянной скорости погружения и извлечения подложки, n в то время как толщина покрытия зависит от скорости движения отступающего (наступающего) мениска жидкости, концентрации гидрофобизирующего агента и вязкости раствора.
 Нанесение гидрофобных агентов на гладкие и текстурированные поверхности n Помимо указанных выше факторов при нанесении покрытий из дисперсий важное значение имеет также и диаметр частиц. n Наконец, качество и структура покрытия в значительной степени определяются характером взаимодействия гидрофобизирующих компонентов с подложкой, с растворителем и между собой. n В методе спин-коутинга, или центрифугирования капли раствора (либо дисперсии) на вращающейся подложке, для получения однородного по толщине покрытия большое значение имеют частота вращения и вязкость раствора. n Крме того, немаловажную роль играет летучесть растворителя, определяющая как равновесность структуры покрытия, так и его однордность по толщине.
Нанесение гидрофобных агентов на гладкие и текстурированные поверхности n Помимо указанных выше факторов при нанесении покрытий из дисперсий важное значение имеет также и диаметр частиц. n Наконец, качество и структура покрытия в значительной степени определяются характером взаимодействия гидрофобизирующих компонентов с подложкой, с растворителем и между собой. n В методе спин-коутинга, или центрифугирования капли раствора (либо дисперсии) на вращающейся подложке, для получения однородного по толщине покрытия большое значение имеют частота вращения и вязкость раствора. n Крме того, немаловажную роль играет летучесть растворителя, определяющая как равновесность структуры покрытия, так и его однордность по толщине.
 Нанесение гидрофобных агентов на гладкие и текстурированные поверхности n Метод адсорбции из растворов или паров используют в основном для получения монослойных гидрофобных покрытий, например, на основе самоорганизованных монослоев.
Нанесение гидрофобных агентов на гладкие и текстурированные поверхности n Метод адсорбции из растворов или паров используют в основном для получения монослойных гидрофобных покрытий, например, на основе самоорганизованных монослоев.
 Суперпокрытия n Наименьший гистерезис контактного угла, который удалось достигнуть в работе, составляет 4˚ и 6˚ градусов для «гидро-» и «олео-» соответственно. Материал под электронным микроскопом представляет собой полимерные ячейки, покрытые нанокристаллами Zn. O.
Суперпокрытия n Наименьший гистерезис контактного угла, который удалось достигнуть в работе, составляет 4˚ и 6˚ градусов для «гидро-» и «олео-» соответственно. Материал под электронным микроскопом представляет собой полимерные ячейки, покрытые нанокристаллами Zn. O.
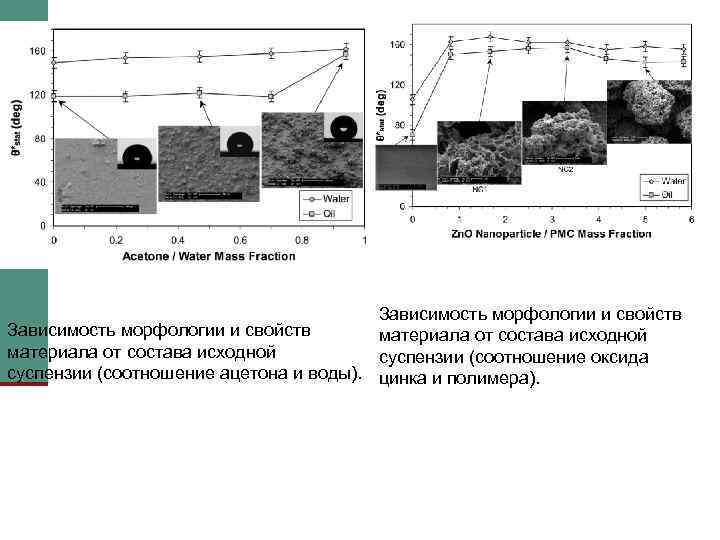 Зависимость морфологии и свойств материала от состава исходной суспензии (соотношение оксида суспензии (соотношение ацетона и воды). цинка и полимера).
Зависимость морфологии и свойств материала от состава исходной суспензии (соотношение оксида суспензии (соотношение ацетона и воды). цинка и полимера).
 Суперпокрытия
Суперпокрытия
 Высокоэнергетические и низкоэнергетические поверхности n Рассмотрим природу сил взаимодействия между жидкостью n n n и поверхностью твердого вещества. В расчете на 1 моль вещества твердого тела энергия U(тж) такого взаимодействия равна: U(тж) = Wa·NA/nт nт - число молекул (атомов, ионов) на единице площади твердого тела. Примем, что толщина слоя (δ) соответствует мономолекулярному слою, тогда nт = (ρт·NA/Мт)2/3 где ρт, Мт – соответственно, плотность и молекулярная масса твердого вещества.
Высокоэнергетические и низкоэнергетические поверхности n Рассмотрим природу сил взаимодействия между жидкостью n n n и поверхностью твердого вещества. В расчете на 1 моль вещества твердого тела энергия U(тж) такого взаимодействия равна: U(тж) = Wa·NA/nт nт - число молекул (атомов, ионов) на единице площади твердого тела. Примем, что толщина слоя (δ) соответствует мономолекулярному слою, тогда nт = (ρт·NA/Мт)2/3 где ρт, Мт – соответственно, плотность и молекулярная масса твердого вещества.
 Высокоэнергетические и низкоэнергетические поверхности. p p p При этих упрощениях энергия взаимодействия равна: U(тж) = Wa·( Мт/ρт)2/3·NA 1/3 (1) Уравнение (19) приводит к следующему выводу. Для жидкостей со сравнительно небольшим (σ<100 м. Дж/м 2) поверхностным натяжением необходимое условие смачивания Wa>σж может выполняться при сравнительно небольших энергиях взаимодействия U(тж)1 -10 к. Дж/моль. Такие небольшие энергии характерны для молекулярных сил, в том числе и для дисперсионных взаимодействий.
Высокоэнергетические и низкоэнергетические поверхности. p p p При этих упрощениях энергия взаимодействия равна: U(тж) = Wa·( Мт/ρт)2/3·NA 1/3 (1) Уравнение (19) приводит к следующему выводу. Для жидкостей со сравнительно небольшим (σ<100 м. Дж/м 2) поверхностным натяжением необходимое условие смачивания Wa>σж может выполняться при сравнительно небольших энергиях взаимодействия U(тж)1 -10 к. Дж/моль. Такие небольшие энергии характерны для молекулярных сил, в том числе и для дисперсионных взаимодействий.
 Высокоэнергетические и низкоэнергетические поверхности. p p p Другая ситуация возникает при контакте твердых тел с жидкостями, поверхностное натяжение которых велико – 10 -102 м. Дж/м 2. К ним относятся жидкие металлы, расплавы солей и оксидов и т. п. Для смачивания такими жидкостями необходимы большие энергии взаимодействия U(тж)- 101 -102 к. Дж/моль. Такие энергии характерны для химических взаимодействий с образованием ионных, ковалентных и металлических связей.
Высокоэнергетические и низкоэнергетические поверхности. p p p Другая ситуация возникает при контакте твердых тел с жидкостями, поверхностное натяжение которых велико – 10 -102 м. Дж/м 2. К ним относятся жидкие металлы, расплавы солей и оксидов и т. п. Для смачивания такими жидкостями необходимы большие энергии взаимодействия U(тж)- 101 -102 к. Дж/моль. Такие энергии характерны для химических взаимодействий с образованием ионных, ковалентных и металлических связей.
 Высокоэнергетические и низкоэнергетические поверхности. p p p На основе этих представлений проводится классификация твердых тел в зависимости от их поверхностной энергии σтг на границе с газом. Различают две группы поверхностей: низкоэнергетические (σ тг ≤ 100 м. Дж/м 2); высокоэнергетические (σтг > 100 м. Дж/м 2); При смачивании низкоэнергетических поверхностей преобладают дисперсионные взаимодействия между жидкостью и твердым телом. При смачивании высокоэнергетических поверхностей большую роль могут играть взаимодействия другой природы, особенно при контакте с жидкостями с высоким поверхностным натяжением.
Высокоэнергетические и низкоэнергетические поверхности. p p p На основе этих представлений проводится классификация твердых тел в зависимости от их поверхностной энергии σтг на границе с газом. Различают две группы поверхностей: низкоэнергетические (σ тг ≤ 100 м. Дж/м 2); высокоэнергетические (σтг > 100 м. Дж/м 2); При смачивании низкоэнергетических поверхностей преобладают дисперсионные взаимодействия между жидкостью и твердым телом. При смачивании высокоэнергетических поверхностей большую роль могут играть взаимодействия другой природы, особенно при контакте с жидкостями с высоким поверхностным натяжением.
 Высокоэнергетические и низкоэнергетические поверхности n Низкоэнергетические поверхности - это такие n n поверхности, которые смачиваются не полностью и реализуют определенный краевой угол. На низкоэнергетических поверхностях в результате их олеофобизации и повышения краевого угла уменьшается работа адгезии. Поэтому капля масла будет слабо удерживаться на поверхности. Поверхностное натяжение низкоэнергетических поверхностей не должно быть больше критического поверхностного натяжения. Полное смачивание - есть рубеж перехода низкоэнергетических поверхностей в высокоэнергетические.
Высокоэнергетические и низкоэнергетические поверхности n Низкоэнергетические поверхности - это такие n n поверхности, которые смачиваются не полностью и реализуют определенный краевой угол. На низкоэнергетических поверхностях в результате их олеофобизации и повышения краевого угла уменьшается работа адгезии. Поэтому капля масла будет слабо удерживаться на поверхности. Поверхностное натяжение низкоэнергетических поверхностей не должно быть больше критического поверхностного натяжения. Полное смачивание - есть рубеж перехода низкоэнергетических поверхностей в высокоэнергетические.
 Растекание n Основную фундаментальную проблему в растекании составляет противоречие между очевидным движением линии трехфазного контакта (периметра смачивания) и отвечающим жидкостям в гидродинамике граничным условию прилипания. n Для объяснения этого противоречия были предложены различные механизмы растекания. Наиболее известные из них два- механизм «расстилающегося ковра» или «гусеницы» , впервые предложенный Френкелем и Гегузиным и механизм скольжения молекул. n В соответствии с первым механизмом, жидкость накатывается на несмоченную твердую поверхность подобно гусенице трактора или расстилающемуся ковру, тогда как растекание полимерных жидкостей связано со скольжением цепных молекул.
Растекание n Основную фундаментальную проблему в растекании составляет противоречие между очевидным движением линии трехфазного контакта (периметра смачивания) и отвечающим жидкостям в гидродинамике граничным условию прилипания. n Для объяснения этого противоречия были предложены различные механизмы растекания. Наиболее известные из них два- механизм «расстилающегося ковра» или «гусеницы» , впервые предложенный Френкелем и Гегузиным и механизм скольжения молекул. n В соответствии с первым механизмом, жидкость накатывается на несмоченную твердую поверхность подобно гусенице трактора или расстилающемуся ковру, тогда как растекание полимерных жидкостей связано со скольжением цепных молекул.
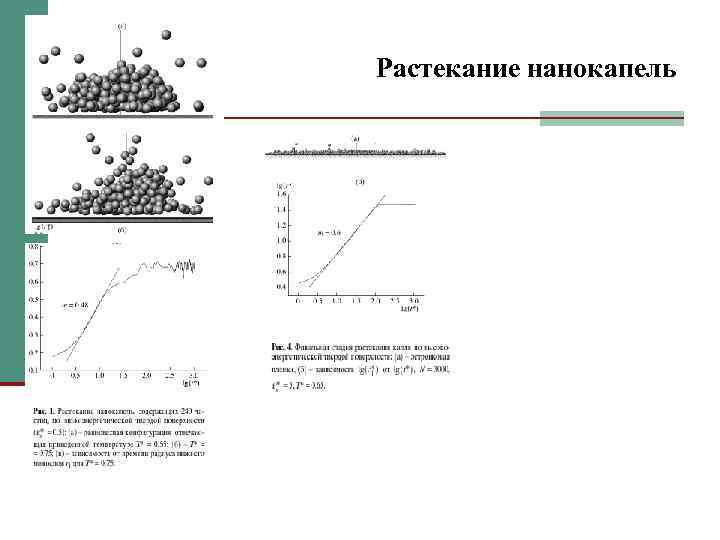 Растекание нанокапель
Растекание нанокапель
 Эффект кофейных колец n Эффект кофейных колец заключается в том, что при высыхании капли некоторой взвеси (например, кофе) частицы располагаются не равномерно по поверхности, которую занимала капля, а концентрируются к границам. Этот эффект учитывается, например, при создании струйных принтеров. n Ученые установили, что причины эффекта скрываются в форме частиц. Дело в том, что при высыхании капли площадь ее соприкосновения с поверхностью не уменьшается, а поверхность просто сплющивается. При этом сферические частицы (именно такую форму имеют частицы кофе) двигаются к границе капли.
Эффект кофейных колец n Эффект кофейных колец заключается в том, что при высыхании капли некоторой взвеси (например, кофе) частицы располагаются не равномерно по поверхности, которую занимала капля, а концентрируются к границам. Этот эффект учитывается, например, при создании струйных принтеров. n Ученые установили, что причины эффекта скрываются в форме частиц. Дело в том, что при высыхании капли площадь ее соприкосновения с поверхностью не уменьшается, а поверхность просто сплющивается. При этом сферические частицы (именно такую форму имеют частицы кофе) двигаются к границе капли.
 Эффект кофейных колец n Появление темной границы по краям можно наблюдать при высыхании капель практически всех типов растворов, содержащих микроскопические твердые частицы. n Кольца возникает из-за разной скорости испарения - по краям это происходит быстрее, и жидкость из центра перетекает к краям капли под действием силы поверхностного натяжения. n Вода увлекает нерастворимые частицы, и они собираются у края капли, что и приводит к образованию концентрических "кофейных колец".
Эффект кофейных колец n Появление темной границы по краям можно наблюдать при высыхании капель практически всех типов растворов, содержащих микроскопические твердые частицы. n Кольца возникает из-за разной скорости испарения - по краям это происходит быстрее, и жидкость из центра перетекает к краям капли под действием силы поверхностного натяжения. n Вода увлекает нерастворимые частицы, и они собираются у края капли, что и приводит к образованию концентрических "кофейных колец".
 Эффект кофейных колец n Используя так называемый эффект «кофейных колец» ( «coffee ring effect» ), израильские ученые нашли новый способ для создания сенсорных экранов, солнечных панелей и микросхем.
Эффект кофейных колец n Используя так называемый эффект «кофейных колец» ( «coffee ring effect» ), израильские ученые нашли новый способ для создания сенсорных экранов, солнечных панелей и микросхем.
 Эффект кофейных колец n Высохшие пятна от кофе продолжают контактировать друг с другом и сохраняют проводимость, при этом пропускают 95 процентов света через отверстие в центре, и, таким образом, модель экрана получилась практически прозрачной. n Обод отдельных колец менее 10 мкм по ширине и меньше чем 300 нм в высоте, при этом диаметр отверстия порядка 150 мкм; поэтому целое множество связанных колец почти невидимо невооруженным глазом. n Массивы колец имеют прозрачность 95%; удельное сопротивление: на 0. 5 см 2 – 4 ± 0. 5 Ом.
Эффект кофейных колец n Высохшие пятна от кофе продолжают контактировать друг с другом и сохраняют проводимость, при этом пропускают 95 процентов света через отверстие в центре, и, таким образом, модель экрана получилась практически прозрачной. n Обод отдельных колец менее 10 мкм по ширине и меньше чем 300 нм в высоте, при этом диаметр отверстия порядка 150 мкм; поэтому целое множество связанных колец почти невидимо невооруженным глазом. n Массивы колец имеют прозрачность 95%; удельное сопротивление: на 0. 5 см 2 – 4 ± 0. 5 Ом.
 Эффект кофейных колец Группа американских ученых выяснила, как предотвратить появление "кофейных колец", возникающих при высыхании по краям капель коллоидных растворов, например кофе или акварельной краски; это открытие поможет создать идеальные струйные принтеры, улучшить технологии расшифровки ДНК и окраски нанопленок.
Эффект кофейных колец Группа американских ученых выяснила, как предотвратить появление "кофейных колец", возникающих при высыхании по краям капель коллоидных растворов, например кофе или акварельной краски; это открытие поможет создать идеальные струйные принтеры, улучшить технологии расшифровки ДНК и окраски нанопленок.
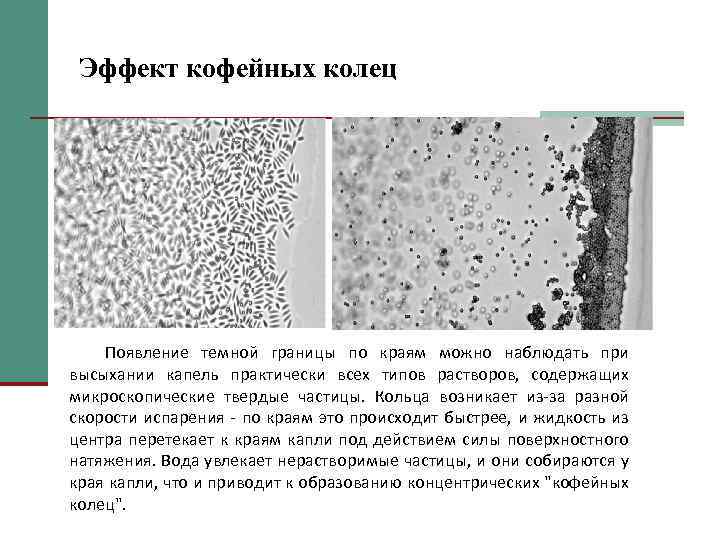 Эффект кофейных колец Появление темной границы по краям можно наблюдать при высыхании капель практически всех типов растворов, содержащих микроскопические твердые частицы. Кольца возникает из-за разной скорости испарения - по краям это происходит быстрее, и жидкость из центра перетекает к краям капли под действием силы поверхностного натяжения. Вода увлекает нерастворимые частицы, и они собираются у края капли, что и приводит к образованию концентрических "кофейных колец".
Эффект кофейных колец Появление темной границы по краям можно наблюдать при высыхании капель практически всех типов растворов, содержащих микроскопические твердые частицы. Кольца возникает из-за разной скорости испарения - по краям это происходит быстрее, и жидкость из центра перетекает к краям капли под действием силы поверхностного натяжения. Вода увлекает нерастворимые частицы, и они собираются у края капли, что и приводит к образованию концентрических "кофейных колец".
 Эффект кофейных колец Они подготовили несколько видов полистирольных сфер и эллипсоидов размером от 1 до 5 микрон и наблюдали за тем, как высыхают капли взвеси из этих частиц. Оказалось, что сферические частицы образуют идеальные "кофейные кольца". Однако вытянутые эллипсоиды не скапливались по краям пятна и распределялись равномерно по всей площади капли. Как оказалось, эллипсоиды образуют в капле единую структуру под действием так называемого "эффекта мюсли" (cheerio effect) - взаимодействие поверхности жидкости и воздуха вынуждает нерастворимые частицы притягиваться друг к другу. Пленка из частиц-эллипсоидов искривляет поверхность капли, прижимая ее края и выпячивая середину. В результате при высыхании капля "стягивается", что обеспечивает равномерное осаждение твердых частиц по всей ее площади. Добавление даже небольшого количества эллиптических частиц во взвесь из микроскопических сфер и воды оказалось достаточным для подавления эффекта "кофейного кольца".
Эффект кофейных колец Они подготовили несколько видов полистирольных сфер и эллипсоидов размером от 1 до 5 микрон и наблюдали за тем, как высыхают капли взвеси из этих частиц. Оказалось, что сферические частицы образуют идеальные "кофейные кольца". Однако вытянутые эллипсоиды не скапливались по краям пятна и распределялись равномерно по всей площади капли. Как оказалось, эллипсоиды образуют в капле единую структуру под действием так называемого "эффекта мюсли" (cheerio effect) - взаимодействие поверхности жидкости и воздуха вынуждает нерастворимые частицы притягиваться друг к другу. Пленка из частиц-эллипсоидов искривляет поверхность капли, прижимая ее края и выпячивая середину. В результате при высыхании капля "стягивается", что обеспечивает равномерное осаждение твердых частиц по всей ее площади. Добавление даже небольшого количества эллиптических частиц во взвесь из микроскопических сфер и воды оказалось достаточным для подавления эффекта "кофейного кольца".
 «Жемчужные» капли
«Жемчужные» капли
 «Жемчужные» капли
«Жемчужные» капли
 Эффект «розовых лепестков» Смысл «эффекта розовых лепестков» в обратном: в удержании капель воды на поверхности бутона. И хотя внешне он – прямая противоположность «эффекту лотоса» , первопричины и у того, и у другого явления одинаковые. Есть у розы и воскоподобные нанокристаллы, которые заставляют воду «сворачиваться» в шарики, есть и знаменитые шишечки, причем того же размера, что и у лотоса, но вот форма их и расстояние между ними другие. Эта особенность как раз и изменила эффект на противоположный. У лотоса расстояние между шишечками слишком мало, чтобы обеспечить полный контакт капли с поверхностью. А слегка конусообразные шишечки розовых лепестков, находящиеся на большем расстоянии друг от друга, справляются с этой задачей прекрасно и надежно удерживают каплю на лепестке.
Эффект «розовых лепестков» Смысл «эффекта розовых лепестков» в обратном: в удержании капель воды на поверхности бутона. И хотя внешне он – прямая противоположность «эффекту лотоса» , первопричины и у того, и у другого явления одинаковые. Есть у розы и воскоподобные нанокристаллы, которые заставляют воду «сворачиваться» в шарики, есть и знаменитые шишечки, причем того же размера, что и у лотоса, но вот форма их и расстояние между ними другие. Эта особенность как раз и изменила эффект на противоположный. У лотоса расстояние между шишечками слишком мало, чтобы обеспечить полный контакт капли с поверхностью. А слегка конусообразные шишечки розовых лепестков, находящиеся на большем расстоянии друг от друга, справляются с этой задачей прекрасно и надежно удерживают каплю на лепестке.
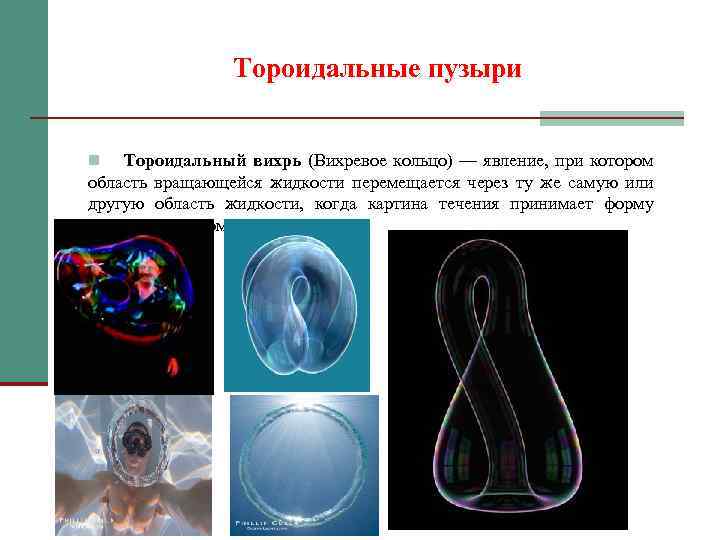 Тороидальные пузыри Тороидальный вихрь (Вихревое кольцо) — явление, при котором область вращающейся жидкости перемещается через ту же самую или другую область жидкости, когда картина течения принимает форму тороида или форму бублика. n
Тороидальные пузыри Тороидальный вихрь (Вихревое кольцо) — явление, при котором область вращающейся жидкости перемещается через ту же самую или другую область жидкости, когда картина течения принимает форму тороида или форму бублика. n
 Спасибо за внимание!
Спасибо за внимание!


