ПНТ_Лекция-12-1_pres.ppt
- Количество слайдов: 28
 Процессы и агрегаты нефтегазовых технологий Лекция 12: Термокаталитические процессы вторичной переработки нефти. Каталитические процессы – введение в теорию и аппаратурное оформление (2) Введение 12. 1. Каталитические процессы – введение в теорию 12. 1. 1. Учет внутренней диффузии в гетерогенно-каталитических процессах 12. 2. Способы отвода и подвода тепла в каталитических реакторах 12. 2. 1. Реакторы с встроенными теплообменными элементами 12. 2. 1. Реакторы с адиабатическими слоями и выносными теплообменниками 12. 3. Реакторные схемы каталитического риформинга 12. 3. 1. Схема с неподвижным слоем катализатора а) с осевым вводом б) с радиальным вводом 12. 3. 2. Схема с подвижным слоем катализатора 12. 4. Математические модели реакторных узлов риформинга при различном движении реагентов. 12. 4. 1. Кинетическая модель процесса риформинга 12. 4. 2. Моделирование процесса риформинга
Процессы и агрегаты нефтегазовых технологий Лекция 12: Термокаталитические процессы вторичной переработки нефти. Каталитические процессы – введение в теорию и аппаратурное оформление (2) Введение 12. 1. Каталитические процессы – введение в теорию 12. 1. 1. Учет внутренней диффузии в гетерогенно-каталитических процессах 12. 2. Способы отвода и подвода тепла в каталитических реакторах 12. 2. 1. Реакторы с встроенными теплообменными элементами 12. 2. 1. Реакторы с адиабатическими слоями и выносными теплообменниками 12. 3. Реакторные схемы каталитического риформинга 12. 3. 1. Схема с неподвижным слоем катализатора а) с осевым вводом б) с радиальным вводом 12. 3. 2. Схема с подвижным слоем катализатора 12. 4. Математические модели реакторных узлов риформинга при различном движении реагентов. 12. 4. 1. Кинетическая модель процесса риформинга 12. 4. 2. Моделирование процесса риформинга
 12. 1. Каталитические процессы 12. 1. 1. Основные стадии и область протекания каталитических процессов Каталитические процессы - протекают с участием катализаторов. Катализаторы образуют с одним из реагентов промежуточное соединение, которое затем реагирует с другим реагентом с образованием конечного продукта и выделением катализатора в неизменном виде. Различают гомогенные и гетерогенные катализаторы. При гетерогенном катализе катализатор и регенты находятся в разных фазах. Катализатор, как правило, находится на поверхности твердой фаз ы, а реагенты находятся в газовой или жидкой фазе. На поверхности твердого катализатора находятся так называемые активные центры. Реагент сорбируется на поверхности катализатора, образуя с активным центром промежуточное соединение, которое либо реагирует с другим реагентом, образуя продукт реакции и освобождая активный центр для следующих актов взаимодействия, либо просто распадается с выделением продукта реакции. Типичный гетерогенный катализатор представляет собой пористый твердый материал с сильно развитой внутренней поверхностью пор.
12. 1. Каталитические процессы 12. 1. 1. Основные стадии и область протекания каталитических процессов Каталитические процессы - протекают с участием катализаторов. Катализаторы образуют с одним из реагентов промежуточное соединение, которое затем реагирует с другим реагентом с образованием конечного продукта и выделением катализатора в неизменном виде. Различают гомогенные и гетерогенные катализаторы. При гетерогенном катализе катализатор и регенты находятся в разных фазах. Катализатор, как правило, находится на поверхности твердой фаз ы, а реагенты находятся в газовой или жидкой фазе. На поверхности твердого катализатора находятся так называемые активные центры. Реагент сорбируется на поверхности катализатора, образуя с активным центром промежуточное соединение, которое либо реагирует с другим реагентом, образуя продукт реакции и освобождая активный центр для следующих актов взаимодействия, либо просто распадается с выделением продукта реакции. Типичный гетерогенный катализатор представляет собой пористый твердый материал с сильно развитой внутренней поверхностью пор.
 При гетерогенном катализе можно выделить следующие основные стадии процесса: 1) транспорт реагентов из объема сплошной фазы к поверхности раздела фаз, называемой также интерфейсом ( «внешний» и «внутренний» ); 2) адсорбция реагента на поверхности твердой фазы, на ее активных центрах, с образованием промежуточных соединений; 3) химическое превращение промежуточного соединения в продукты реакции. 4) десорбция продукта реакции с поверхности катализатора; 5) диффузия продукта от поверхности раздела фаз в объем сплошной фазы. В зависимости от соотношения скоростей отдельных стадий гетерогенного каталитического процесса общая скорость процесса лимитируется, или определяется скоростью наиболее медленной стадии. Принято выделять транспорт реагентов к внешней поверхности частиц катализатора. Этот процесс называется внешней диффузией. Далее происходит транспорт реагентов внутрь пористых частиц катализатора. Этот процесс называется внутренней диффузией. Если наиболее медленной стадией является транспорт реагента к внешней поверхности частиц катализатора, то процесс происходит во внешне-диффузионной области. Если наиболее медленной стадией является транспорт реагента внутри пористой частицы катализатора, то считают, что процесс происходит во внутри-диффузионной области. Если наиболее медленной стадией является сама химическая реакция, то считают, что процесс происходит в кинетической области, так как общая скорость процесса лимитируется скоростью химической реакции на поверхности катализатора.
При гетерогенном катализе можно выделить следующие основные стадии процесса: 1) транспорт реагентов из объема сплошной фазы к поверхности раздела фаз, называемой также интерфейсом ( «внешний» и «внутренний» ); 2) адсорбция реагента на поверхности твердой фазы, на ее активных центрах, с образованием промежуточных соединений; 3) химическое превращение промежуточного соединения в продукты реакции. 4) десорбция продукта реакции с поверхности катализатора; 5) диффузия продукта от поверхности раздела фаз в объем сплошной фазы. В зависимости от соотношения скоростей отдельных стадий гетерогенного каталитического процесса общая скорость процесса лимитируется, или определяется скоростью наиболее медленной стадии. Принято выделять транспорт реагентов к внешней поверхности частиц катализатора. Этот процесс называется внешней диффузией. Далее происходит транспорт реагентов внутрь пористых частиц катализатора. Этот процесс называется внутренней диффузией. Если наиболее медленной стадией является транспорт реагента к внешней поверхности частиц катализатора, то процесс происходит во внешне-диффузионной области. Если наиболее медленной стадией является транспорт реагента внутри пористой частицы катализатора, то считают, что процесс происходит во внутри-диффузионной области. Если наиболее медленной стадией является сама химическая реакция, то считают, что процесс происходит в кинетической области, так как общая скорость процесса лимитируется скоростью химической реакции на поверхности катализатора.
 12. 1. Учет внутренней диффузии в гетерогенных каталитических процессах Катализаторы для каталитических процессов изготавливают в виде частиц различной формы, чаще всего в виде таблеток цилиндрической или сферической формы. Эти таблетки имеют развитую пористую структуру, что позволяет создавать катализаторы, имеющие внутреннюю поверхность пор, достигающих нескольких сотен м 2 на грамм. При такой структуре гранул большая часть химических превращений протекает внутри частицы катализатора. Рассмотрим вывод уравнения математической модели каталитического процесса, протекающего внутри пористой частицы катализатора. Для анализа процессов и вывода уравнений математической модели чаще всего используют так называемую квазигомогенную модель частицы катализатора. В соответствии с этой моделью частицу рассматривают как некую изотропную среду, обладающую проницаемостью для реагентов и продуктов реакции и обладающую каталитическими свойствами к превращению исходного реагента в продукты реакции. При этих допущениях можно считать, что транспорт вещества внутри пористой частицы катализатора подчинятся закону диффузии Фика, а скорость гетерогенной реакции на внутренней поверхности катализатора может быть отнесена к единице объема катализатора при введении так называемой удельной поверхности, т. е. поверхности, отнесенной к единице объема катализатора.
12. 1. Учет внутренней диффузии в гетерогенных каталитических процессах Катализаторы для каталитических процессов изготавливают в виде частиц различной формы, чаще всего в виде таблеток цилиндрической или сферической формы. Эти таблетки имеют развитую пористую структуру, что позволяет создавать катализаторы, имеющие внутреннюю поверхность пор, достигающих нескольких сотен м 2 на грамм. При такой структуре гранул большая часть химических превращений протекает внутри частицы катализатора. Рассмотрим вывод уравнения математической модели каталитического процесса, протекающего внутри пористой частицы катализатора. Для анализа процессов и вывода уравнений математической модели чаще всего используют так называемую квазигомогенную модель частицы катализатора. В соответствии с этой моделью частицу рассматривают как некую изотропную среду, обладающую проницаемостью для реагентов и продуктов реакции и обладающую каталитическими свойствами к превращению исходного реагента в продукты реакции. При этих допущениях можно считать, что транспорт вещества внутри пористой частицы катализатора подчинятся закону диффузии Фика, а скорость гетерогенной реакции на внутренней поверхности катализатора может быть отнесена к единице объема катализатора при введении так называемой удельной поверхности, т. е. поверхности, отнесенной к единице объема катализатора.
 В этом случае, частица катализатора может характеризоваться эффективным коэффициентом диффузии, Deff и константой скорости, отнесенной к единице объема катализатора kv. С учетом введенных понятий, можно записать: (12. 1) Где - коэффициент молекулярной диффузии, м 2/сек - «пористость» катализатора, отношение свободного объема пор объему катализатора Vкат, м 3/ м 3. Vпор к - коэффициент извилистости пор, отношение средней длины транспортной поры к радиусу частицы катализатора , м/м. - константа скорости гетерогенного процесса, отнесенная к единице объема пористой частицы катализатора, 1/сек (для реакции первого порядка) khet - константа скорости гетерогенного процесса, м/сек (для реакции первого порядка); Sуд - удельная поверхность катализатора, отнесенная к единице объема твердой фазы, м 2/м 3.
В этом случае, частица катализатора может характеризоваться эффективным коэффициентом диффузии, Deff и константой скорости, отнесенной к единице объема катализатора kv. С учетом введенных понятий, можно записать: (12. 1) Где - коэффициент молекулярной диффузии, м 2/сек - «пористость» катализатора, отношение свободного объема пор объему катализатора Vкат, м 3/ м 3. Vпор к - коэффициент извилистости пор, отношение средней длины транспортной поры к радиусу частицы катализатора , м/м. - константа скорости гетерогенного процесса, отнесенная к единице объема пористой частицы катализатора, 1/сек (для реакции первого порядка) khet - константа скорости гетерогенного процесса, м/сек (для реакции первого порядка); Sуд - удельная поверхность катализатора, отнесенная к единице объема твердой фазы, м 2/м 3.
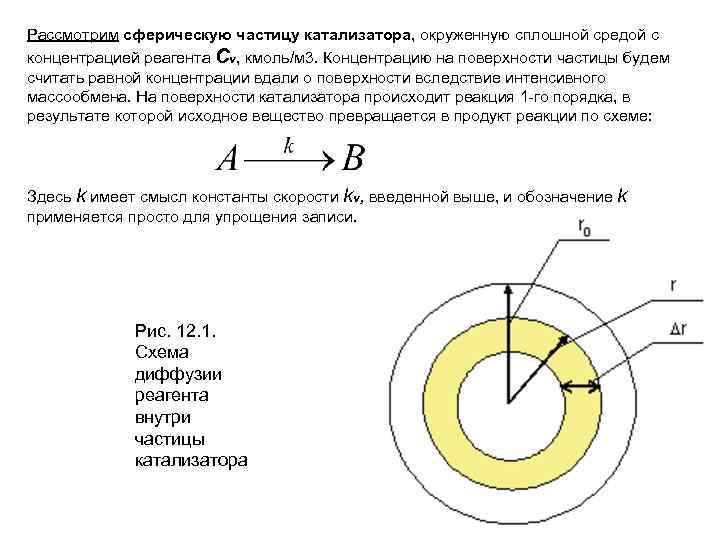 Рассмотрим сферическую частицу катализатора, окруженную сплошной средой с концентрацией реагента Сv, кмоль/м 3. Концентрацию на поверхности частицы будем считать равной концентрации вдали о поверхности вследствие интенсивного массообмена. На поверхности катализатора происходит реакция 1 -го порядка, в результате которой исходное вещество превращается в продукт реакции по схеме: Здесь k имеет смысл константы скорости kv, введенной выше, и обозначение k применяется просто для упрощения записи. Рис. 12. 1. Схема диффузии реагента внутри частицы катализатора
Рассмотрим сферическую частицу катализатора, окруженную сплошной средой с концентрацией реагента Сv, кмоль/м 3. Концентрацию на поверхности частицы будем считать равной концентрации вдали о поверхности вследствие интенсивного массообмена. На поверхности катализатора происходит реакция 1 -го порядка, в результате которой исходное вещество превращается в продукт реакции по схеме: Здесь k имеет смысл константы скорости kv, введенной выше, и обозначение k применяется просто для упрощения записи. Рис. 12. 1. Схема диффузии реагента внутри частицы катализатора
 Рассмотрим сферическую частицу катализатора. Выделим внутри частицы объем толщиной r, ограниченный радиусом r r- r (на Рис. 12. 1 выделен цветом). Составим уравнение материального баланса для выделенного объема по реагенту A. Приход реагента в выделенную область: (12. 2) Расход реагента в выделенной области: (12. 3) Рассмотрим величину элементарного объема V и площади, ограничивающий элементарный объем F: Накопление массы в элементарном объеме V будет равно интегралу от нуля до рассматриваемого времени t от разности между потоками прихода и расхода. (12. 4)
Рассмотрим сферическую частицу катализатора. Выделим внутри частицы объем толщиной r, ограниченный радиусом r r- r (на Рис. 12. 1 выделен цветом). Составим уравнение материального баланса для выделенного объема по реагенту A. Приход реагента в выделенную область: (12. 2) Расход реагента в выделенной области: (12. 3) Рассмотрим величину элементарного объема V и площади, ограничивающий элементарный объем F: Накопление массы в элементарном объеме V будет равно интегралу от нуля до рассматриваемого времени t от разности между потоками прихода и расхода. (12. 4)
 Разделим обе части уравнения (13. 4) на V и продифференцируем обе части уравнения по t. Учитывая, что мы рассматриваем процесс от нуля до текущего времени t, мы получим в левой части уравнения производную от концентрации по времени. В правой части мы получим подинтегральное выражение. (12. 5) Рассмотрим предел 1 -го слагаемого правой части уравнения (12. 17): (12. 6) Подставив полученное выражение предела в уравнение (2. 17) получим окончательное уравнение материального баланса для любой точки внутри частицы катализатора: (12. 7)
Разделим обе части уравнения (13. 4) на V и продифференцируем обе части уравнения по t. Учитывая, что мы рассматриваем процесс от нуля до текущего времени t, мы получим в левой части уравнения производную от концентрации по времени. В правой части мы получим подинтегральное выражение. (12. 5) Рассмотрим предел 1 -го слагаемого правой части уравнения (12. 17): (12. 6) Подставив полученное выражение предела в уравнение (2. 17) получим окончательное уравнение материального баланса для любой точки внутри частицы катализатора: (12. 7)
 В уравнении (12. 7) содержатся знаки частных производных, так концентрация с является функцией радиуса частицы r и времени t. Уравнение (12. 7), будучи уравнением в частных производных 2 -го порядка требует для своего однозначного решения задания начальных условий и двух граничных условий. В качестве начальных условий обычно задают профиль концентрации по радиусу в начальный момент времени, а в качестве граничных условий задают значения концентраций и ее производных на границах частицы и внутри. Поэтому начальные и граничные условия для уравнения (12. 7) будут выглядеть следующим образом: (12. 8) Граничные условия записываются из условия симметрии свойств частицы в центре и исходя из значения концентрации на внешней поверхности частицы при интенсивном массообмене в объеме: (12. 9). Рассмотрим решение уравнения (12. 7) с граничными условиями (13. 9) при стационарном режиме работы катализатора, т. е. при условии, что (12. 10) При этих условиях уравнение математической модели процесса (12. 7) может быть записано следующим образом: (12. 11)
В уравнении (12. 7) содержатся знаки частных производных, так концентрация с является функцией радиуса частицы r и времени t. Уравнение (12. 7), будучи уравнением в частных производных 2 -го порядка требует для своего однозначного решения задания начальных условий и двух граничных условий. В качестве начальных условий обычно задают профиль концентрации по радиусу в начальный момент времени, а в качестве граничных условий задают значения концентраций и ее производных на границах частицы и внутри. Поэтому начальные и граничные условия для уравнения (12. 7) будут выглядеть следующим образом: (12. 8) Граничные условия записываются из условия симметрии свойств частицы в центре и исходя из значения концентрации на внешней поверхности частицы при интенсивном массообмене в объеме: (12. 9). Рассмотрим решение уравнения (12. 7) с граничными условиями (13. 9) при стационарном режиме работы катализатора, т. е. при условии, что (12. 10) При этих условиях уравнение математической модели процесса (12. 7) может быть записано следующим образом: (12. 11)
 Преобразуем уравнение (12. 11) следующим образом: разделим правую и левую части уравнения на коэффициент диффузии и введем безразмерный радиус частицы: (12. 12) После подстановки соотношений (12. 12) в уравнение (13. 11), деления на D и введения нового обозначения, получим следующее выражение уравнения (12. 11): (12. 13) Где - модуль Тиле, безразмерный параметр, характеризующий отношение интенсивности транспорта вещества внутри частицы к интенсивности его расходования его за счет химической реакции. Для решения уравнения (12. 12) с граничными условиями (12. 9) введем новую переменную: Подставим полученное значение 2 -й производной и функции с в исходное уравнение (12. 12):
Преобразуем уравнение (12. 11) следующим образом: разделим правую и левую части уравнения на коэффициент диффузии и введем безразмерный радиус частицы: (12. 12) После подстановки соотношений (12. 12) в уравнение (13. 11), деления на D и введения нового обозначения, получим следующее выражение уравнения (12. 11): (12. 13) Где - модуль Тиле, безразмерный параметр, характеризующий отношение интенсивности транспорта вещества внутри частицы к интенсивности его расходования его за счет химической реакции. Для решения уравнения (12. 12) с граничными условиями (12. 9) введем новую переменную: Подставим полученное значение 2 -й производной и функции с в исходное уравнение (12. 12):
 После сокращения подобных членов и умножения обеих частей уравнения на величину безразмерного радиуса , получим: Характеристическое уравнение для полученного дифференциального уравнения имеет вид: В итоге решение дифференциального уравнения можно записать в виде: Выполним переход к исходной переменной с. В итоге получим окончательный вид решения уравнения (12. 12) (12. 13) Где А 1 и А 2 - постоянные интегрирования, определяемые из граничных условий (12. 9). Для их определения необходимо найти значения производной функции и подставить значения функции и её производной в заданные граничные условия.
После сокращения подобных членов и умножения обеих частей уравнения на величину безразмерного радиуса , получим: Характеристическое уравнение для полученного дифференциального уравнения имеет вид: В итоге решение дифференциального уравнения можно записать в виде: Выполним переход к исходной переменной с. В итоге получим окончательный вид решения уравнения (12. 12) (12. 13) Где А 1 и А 2 - постоянные интегрирования, определяемые из граничных условий (12. 9). Для их определения необходимо найти значения производной функции и подставить значения функции и её производной в заданные граничные условия.
 Получим систему из двух уравнений с двумя неизвестными А 1 и А 2 (12. 14) Умножим обе части уравнения (2. 26) на : (12. 15) Из первого граничного условия, подставляя в уравнение (2. 27) =0, получим: (12. 16) Подставим соотношение между постоянными интегрирования в (2. 25) и используем 2 -у граничное условие при =1: (12. 17) Подставим найденное значение произвольной постоянной в уравнение (12. 13), получим значение концентрации внутри частицы катализатора как функцию радиуса частицы. (12. 18)
Получим систему из двух уравнений с двумя неизвестными А 1 и А 2 (12. 14) Умножим обе части уравнения (2. 26) на : (12. 15) Из первого граничного условия, подставляя в уравнение (2. 27) =0, получим: (12. 16) Подставим соотношение между постоянными интегрирования в (2. 25) и используем 2 -у граничное условие при =1: (12. 17) Подставим найденное значение произвольной постоянной в уравнение (12. 13), получим значение концентрации внутри частицы катализатора как функцию радиуса частицы. (12. 18)
 Введем понятие коэффициента эффективности использования внутренней поверхности катализатора, или фактора эффективности. Эта величина будет равна отношению количества вещества реагирующего в объеме частицы катализатора с учетом распределения концентрации по радиусу в соответствии с уравнением (2. 30) к предельно возможному количеству при отсутствии внутри диффузионного торможения. Это количество будет равно произведению объема частицы на скорость реакции в единице объема при концентрации внутри частицы, равной концентрации в объеме: (12. 19) Используя значение фактора эффективности можно записать уравнение скорости реакции в объеме частицы катализатора в следующем виде: (12. 20) С учетом того, что в объеме реактора доля свободного объема равна , а доля объема реактора, занятого катализатором равно (1 - ), можно записать уравнение скорости каталитического процесса, отнесенного к единице объема реактора в следующем виде: (12. 21)
Введем понятие коэффициента эффективности использования внутренней поверхности катализатора, или фактора эффективности. Эта величина будет равна отношению количества вещества реагирующего в объеме частицы катализатора с учетом распределения концентрации по радиусу в соответствии с уравнением (2. 30) к предельно возможному количеству при отсутствии внутри диффузионного торможения. Это количество будет равно произведению объема частицы на скорость реакции в единице объема при концентрации внутри частицы, равной концентрации в объеме: (12. 19) Используя значение фактора эффективности можно записать уравнение скорости реакции в объеме частицы катализатора в следующем виде: (12. 20) С учетом того, что в объеме реактора доля свободного объема равна , а доля объема реактора, занятого катализатором равно (1 - ), можно записать уравнение скорости каталитического процесса, отнесенного к единице объема реактора в следующем виде: (12. 21)
 Проделанный анализ является обоснованием возможности применения для расчета каталитических процессов в реакторах так называемой квазигомогенной модели, которая по форме записи совпадает с обычной моделью химической кинетики, но константа скорости в которой является сложной функцией 1) пористости частицы, 2) размера частиц катализатора, 3) коэффициента диффузии внутри частиц катализатора, 4) удельной поверхности контакта фаз, 5) химической природы реагирующих компонентов и 6) состава катализатора. Основным параметром, определяющим влияние внутренней диффузии на общую скорость процесса, является модуль Тиле: Из приведенного уравнения следует, что параметр является линейной функцией размера частицы r 0. Поэтому, если наблюдаемая скорость процесса зависит от размера частиц, лимитирующей стадией процесса является внутренняя диффузия и для интенсификации процесса необходимо уменьшать размеры частиц катализатора. НО делать это можно не беспредельно, так как при уменьшении размера частиц увеличивается гидравлическое сопротивление слоя частиц и растет расход энергии, необходимой для прокачивания реакционной смеси через слой катализатора. Поэтому необходимо находить компромисс между увеличением скорости процесса и растущим сопротивлением слоя частиц.
Проделанный анализ является обоснованием возможности применения для расчета каталитических процессов в реакторах так называемой квазигомогенной модели, которая по форме записи совпадает с обычной моделью химической кинетики, но константа скорости в которой является сложной функцией 1) пористости частицы, 2) размера частиц катализатора, 3) коэффициента диффузии внутри частиц катализатора, 4) удельной поверхности контакта фаз, 5) химической природы реагирующих компонентов и 6) состава катализатора. Основным параметром, определяющим влияние внутренней диффузии на общую скорость процесса, является модуль Тиле: Из приведенного уравнения следует, что параметр является линейной функцией размера частицы r 0. Поэтому, если наблюдаемая скорость процесса зависит от размера частиц, лимитирующей стадией процесса является внутренняя диффузия и для интенсификации процесса необходимо уменьшать размеры частиц катализатора. НО делать это можно не беспредельно, так как при уменьшении размера частиц увеличивается гидравлическое сопротивление слоя частиц и растет расход энергии, необходимой для прокачивания реакционной смеси через слой катализатора. Поэтому необходимо находить компромисс между увеличением скорости процесса и растущим сопротивлением слоя частиц.
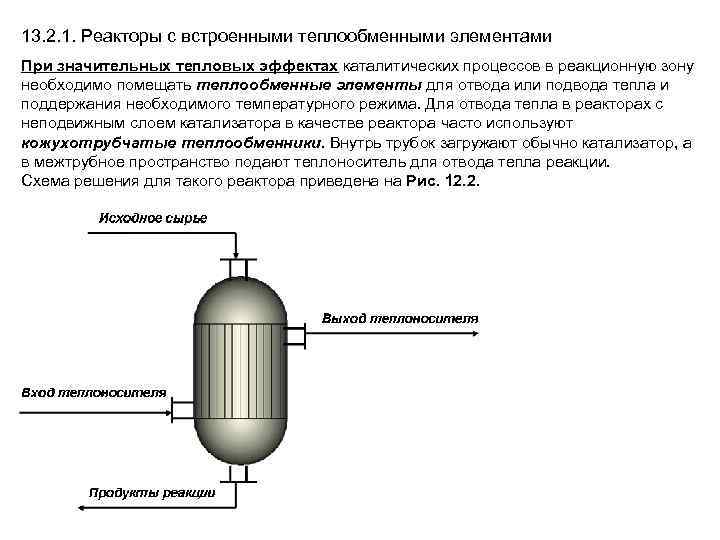 13. 2. 1. Реакторы с встроенными теплообменными элементами При значительных тепловых эффектах каталитических процессов в реакционную зону необходимо помещать теплообменные элементы для отвода или подвода тепла и поддержания необходимого температурного режима. Для отвода тепла в реакторах с неподвижным слоем катализатора в качестве реактора часто используют кожухотрубчатые теплообменники. Внутрь трубок загружают обычно катализатор, а в межтрубное пространство подают теплоноситель для отвода тепла реакции. Схема решения для такого реактора приведена на Рис. 12. 2.
13. 2. 1. Реакторы с встроенными теплообменными элементами При значительных тепловых эффектах каталитических процессов в реакционную зону необходимо помещать теплообменные элементы для отвода или подвода тепла и поддержания необходимого температурного режима. Для отвода тепла в реакторах с неподвижным слоем катализатора в качестве реактора часто используют кожухотрубчатые теплообменники. Внутрь трубок загружают обычно катализатор, а в межтрубное пространство подают теплоноситель для отвода тепла реакции. Схема решения для такого реактора приведена на Рис. 12. 2.
 Одна из главных проблем при создании и эксплуатации такого типа реакторов организация засыпки катализатора в трубки таким образом, чтобы обеспечить одинаковое сопротивление всех трубок. Только в этом случае будет обеспечено равномерное распределение реакционной смеси по всем трубкам и одинаковая конверсия по поперечному сечению аппарата. Для засыпки катализатора в трубки созданы специальные устройства, обеспечивающие замер сопротивления в трубках по мере их заполнения. Несмотря на сложности в создании и эксплуатации таких реакторов, они получили широкое распространение вследствие надежности поддержания заданного температурного режима и обеспечения за счет этого высокого качества продукции.
Одна из главных проблем при создании и эксплуатации такого типа реакторов организация засыпки катализатора в трубки таким образом, чтобы обеспечить одинаковое сопротивление всех трубок. Только в этом случае будет обеспечено равномерное распределение реакционной смеси по всем трубкам и одинаковая конверсия по поперечному сечению аппарата. Для засыпки катализатора в трубки созданы специальные устройства, обеспечивающие замер сопротивления в трубках по мере их заполнения. Несмотря на сложности в создании и эксплуатации таких реакторов, они получили широкое распространение вследствие надежности поддержания заданного температурного режима и обеспечения за счет этого высокого качества продукции.
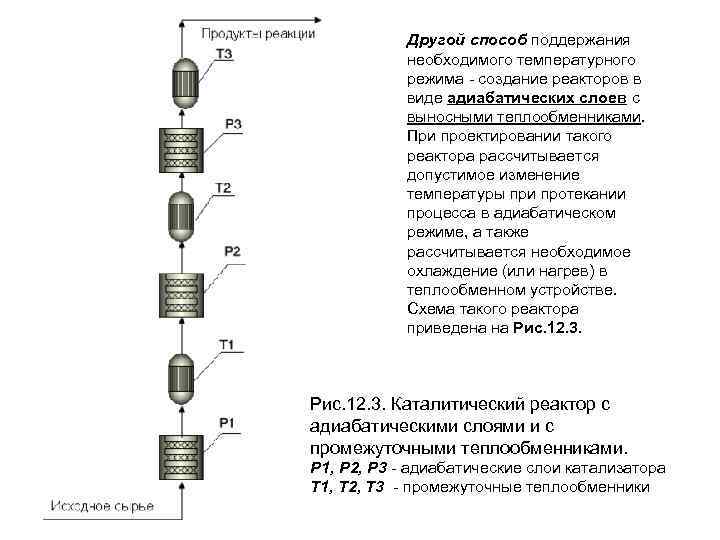 Другой способ поддержания необходимого температурного режима - создание реакторов в виде адиабатических слоев с выносными теплообменниками. При проектировании такого реактора рассчитывается допустимое изменение температуры при протекании процесса в адиабатическом режиме, а также рассчитывается необходимое охлаждение (или нагрев) в теплообменном устройстве. Схема такого реактора приведена на Рис. 12. 3. Каталитический реактор с адиабатическими слоями и с промежуточными теплообменниками. Р 1, Р 2, Р 3 - адиабатические слои катализатора Т 1, Т 2, Т 3 - промежуточные теплообменники
Другой способ поддержания необходимого температурного режима - создание реакторов в виде адиабатических слоев с выносными теплообменниками. При проектировании такого реактора рассчитывается допустимое изменение температуры при протекании процесса в адиабатическом режиме, а также рассчитывается необходимое охлаждение (или нагрев) в теплообменном устройстве. Схема такого реактора приведена на Рис. 12. 3. Каталитический реактор с адиабатическими слоями и с промежуточными теплообменниками. Р 1, Р 2, Р 3 - адиабатические слои катализатора Т 1, Т 2, Т 3 - промежуточные теплообменники
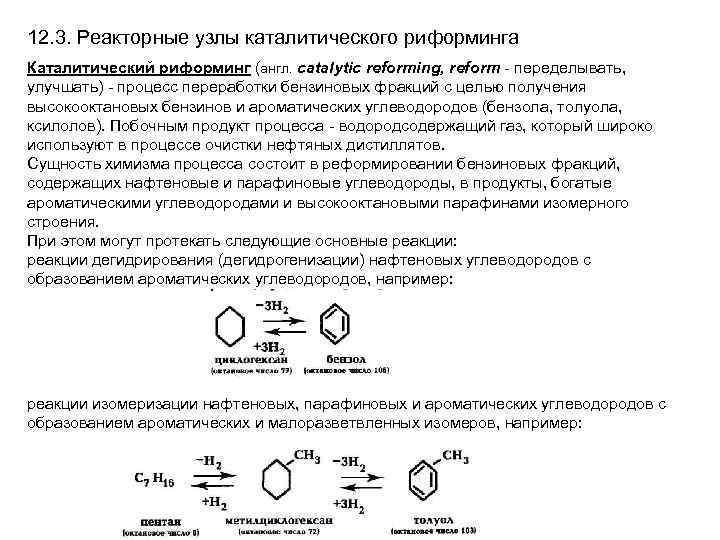 12. 3. Реакторные узлы каталитического риформинга Каталитический риформинг (англ. catalytic reforming, reform - переделывать, улучшать) - процесс переработки бензиновых фракций с целью получения высокооктановых бензинов и ароматических углеводородов (бензола, толуола, ксилолов). Побочным продукт процесса - водородсодержащий газ, который широко используют в процессе очистки нефтяных дистиллятов. Сущность химизма процесса состоит в реформировании бензиновых фракций, содержащих нафтеновые и парафиновые углеводороды, в продукты, богатые ароматическими углеводородами и высокооктановыми парафинами изомерного строения. При этом могут протекать следующие основные реакции: реакции дегидрирования (дегидрогенизации) нафтеновых углеводородов с образованием ароматических углеводородов, например: реакции изомеризации нафтеновых, парафиновых и ароматических углеводородов с образованием ароматических и малоразветвленных изомеров, например:
12. 3. Реакторные узлы каталитического риформинга Каталитический риформинг (англ. catalytic reforming, reform - переделывать, улучшать) - процесс переработки бензиновых фракций с целью получения высокооктановых бензинов и ароматических углеводородов (бензола, толуола, ксилолов). Побочным продукт процесса - водородсодержащий газ, который широко используют в процессе очистки нефтяных дистиллятов. Сущность химизма процесса состоит в реформировании бензиновых фракций, содержащих нафтеновые и парафиновые углеводороды, в продукты, богатые ароматическими углеводородами и высокооктановыми парафинами изомерного строения. При этом могут протекать следующие основные реакции: реакции дегидрирования (дегидрогенизации) нафтеновых углеводородов с образованием ароматических углеводородов, например: реакции изомеризации нафтеновых, парафиновых и ароматических углеводородов с образованием ароматических и малоразветвленных изомеров, например:
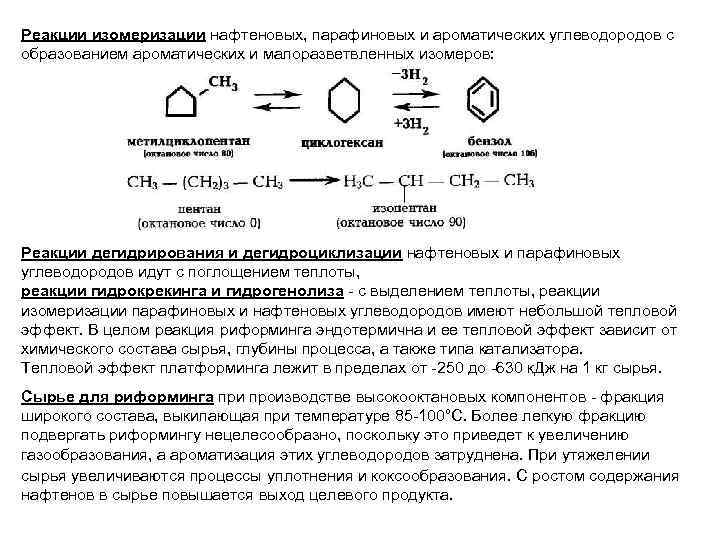 Реакции изомеризации нафтеновых, парафиновых и ароматических углеводородов с образованием ароматических и малоразветвленных изомеров: Реакции дегидрирования и дегидроциклизации нафтеновых и парафиновых углеводородов идут с поглощением теплоты, реакции гидрокрекинга и гидрогенолиза - с выделением теплоты, реакции изомеризации парафиновых и нафтеновых углеводородов имеют небольшой тепловой эффект. В целом реакция риформинга эндотермична и ее тепловой эффект зависит от химического состава сырья, глубины процесса, а также типа катализатора. Тепловой эффект платформинга лежит в пределах от -250 до -630 к. Дж на 1 кг сырья. Сырье для риформинга при производстве высокооктановых компонентов - фракция широкого состава, выкипающая при температуре 85 -100°С. Более легкую фракцию подвергать риформингу нецелесообразно, поскольку это приведет к увеличению газообразования, а ароматизация этих углеводородов затруднена. При утяжелении сырья увеличиваются процессы уплотнения и коксообразования. С ростом содержания нафтенов в сырье повышается выход целевого продукта.
Реакции изомеризации нафтеновых, парафиновых и ароматических углеводородов с образованием ароматических и малоразветвленных изомеров: Реакции дегидрирования и дегидроциклизации нафтеновых и парафиновых углеводородов идут с поглощением теплоты, реакции гидрокрекинга и гидрогенолиза - с выделением теплоты, реакции изомеризации парафиновых и нафтеновых углеводородов имеют небольшой тепловой эффект. В целом реакция риформинга эндотермична и ее тепловой эффект зависит от химического состава сырья, глубины процесса, а также типа катализатора. Тепловой эффект платформинга лежит в пределах от -250 до -630 к. Дж на 1 кг сырья. Сырье для риформинга при производстве высокооктановых компонентов - фракция широкого состава, выкипающая при температуре 85 -100°С. Более легкую фракцию подвергать риформингу нецелесообразно, поскольку это приведет к увеличению газообразования, а ароматизация этих углеводородов затруднена. При утяжелении сырья увеличиваются процессы уплотнения и коксообразования. С ростом содержания нафтенов в сырье повышается выход целевого продукта.
 При получении концентратов индивидуальных ароматических углеводородов риформингу подвергают узкие фракции. Например, для получения бензола и толуола используют фракцию 62 -105°С, а ксилолов - фракцию 105 -140°С. Использование в процессе риформинга весьма чувствительных к отравлению различными примесями платиновых катализаторов ужесточает требования к сырью по содержанию серы, азота, воды и металлов. Сырье процесса риформинга обычно подвергают гидроочистке. При гидроочистке наряду с сернистыми соединениями удаляются также смолы, непредельные углеводороды, азотистые и металлоорганические соединения. В процессе риформинга применяют три типа катализаторов: 1) монометаллические (серии АП), 2) биметаллические и 3) полиметаллические (серии КР). Катализатор включает три компонента: 1) активный носитель — оксид алюминия, 2) металл — тонко диспергированную по поверхности платину и 3) кислотный промотор – галогенид алюминия Al. Cl 3 или Al. F 3. Биметаллические и полиметаллические катализаторы содержат кроме платины рений, палладий, германий, иридий и др.
При получении концентратов индивидуальных ароматических углеводородов риформингу подвергают узкие фракции. Например, для получения бензола и толуола используют фракцию 62 -105°С, а ксилолов - фракцию 105 -140°С. Использование в процессе риформинга весьма чувствительных к отравлению различными примесями платиновых катализаторов ужесточает требования к сырью по содержанию серы, азота, воды и металлов. Сырье процесса риформинга обычно подвергают гидроочистке. При гидроочистке наряду с сернистыми соединениями удаляются также смолы, непредельные углеводороды, азотистые и металлоорганические соединения. В процессе риформинга применяют три типа катализаторов: 1) монометаллические (серии АП), 2) биметаллические и 3) полиметаллические (серии КР). Катализатор включает три компонента: 1) активный носитель — оксид алюминия, 2) металл — тонко диспергированную по поверхности платину и 3) кислотный промотор – галогенид алюминия Al. Cl 3 или Al. F 3. Биметаллические и полиметаллические катализаторы содержат кроме платины рений, палладий, германий, иридий и др.
 Селективность катализатора - способность ускорять целевые реакции - обеспечить наибольший выход жидких продуктов и водорода, т. е. с максимальной глубиной должны протекать реакции ароматизации и с минимальной - реакции гидрокрекинга и гидрогенолиза. Стабильность катализатора — способность сохранять во времени активность и селективность. Она определяет продолжительность межрегенерационного цикла и общий срок службы катализатора. Катализаторы риформинга относятся к бифункциональным, т. е. обеспечивают две основные функции: дегидрирующую (гидрирующую) и кислотную. Металлический компонент ускоряет реакции дегидрирования, способствует образованию ароматических углеводородов и частичному удалению промежуточных продуктов реакции, ведущих к коксообразованию. Металлы-промоторы полиметаллических катализаторов, помимо взаимодействия с основным активным компонентом (платиной), влияют на селективность процесса, взаимодействуя с носителем (оксидом алюминия). Кислотные свойства катализатора определяют его крекирующую и изомеризующую активность, а также глубину превращения сырья. Для усиления кислотной функции катализатор промотируют галогеном. Катализатор с течением времени покрывается коксом и сернистыми продуктами уплотнения, происходит его дезактивация. При пяти - шестимесячных пробегах количество кокса может достигать 10% (по массе) на катализатор.
Селективность катализатора - способность ускорять целевые реакции - обеспечить наибольший выход жидких продуктов и водорода, т. е. с максимальной глубиной должны протекать реакции ароматизации и с минимальной - реакции гидрокрекинга и гидрогенолиза. Стабильность катализатора — способность сохранять во времени активность и селективность. Она определяет продолжительность межрегенерационного цикла и общий срок службы катализатора. Катализаторы риформинга относятся к бифункциональным, т. е. обеспечивают две основные функции: дегидрирующую (гидрирующую) и кислотную. Металлический компонент ускоряет реакции дегидрирования, способствует образованию ароматических углеводородов и частичному удалению промежуточных продуктов реакции, ведущих к коксообразованию. Металлы-промоторы полиметаллических катализаторов, помимо взаимодействия с основным активным компонентом (платиной), влияют на селективность процесса, взаимодействуя с носителем (оксидом алюминия). Кислотные свойства катализатора определяют его крекирующую и изомеризующую активность, а также глубину превращения сырья. Для усиления кислотной функции катализатор промотируют галогеном. Катализатор с течением времени покрывается коксом и сернистыми продуктами уплотнения, происходит его дезактивация. При пяти - шестимесячных пробегах количество кокса может достигать 10% (по массе) на катализатор.
 Для восстановления активности и селективности катализаторов их периодически, а на установках с движущимся слоем непрерывно подвергают окислительной регенерации осушенными дымовыми газами при температуре 300 -500 °С и давлении 1, 0 -1, 5 МПа. Во избежание отравления катализатора также применяют инертный газ (азот) высокой чистоты, содержащий не выше 0, 5 % кислорода (по объему). Остаточное содержание кокса после регенерации — менее 0, 02 % (по массе) на катализатор. По окончании выжига кокса проводится восстановительная регенерация катализатора водородом. При обработке катализатора водородом происходит восстановление сернистых соединений до сероводорода, что позволяет снизить содержание серы в катализаторе до 0, 03 — 0, 05 % (по массе). Для поддержания кислотной функции катализатора в газосырьевой поток вводят галогеносодержащие соединения (например, дихлорэтан, водный раствор HCl). Срок службы катализаторов риформинга составляет для катализатора серий АП и КР в среднем 36 -45 и 40 -72 месяцев, соответственно. Температура процессов риформинга обычно находится в интервале 450 -530°С. Повышение температуры ускоряет все основные реакции, при этом возрастает роль реакций ароматизации и гидрокрекинга, увеличиваются выход ароматических углеводородов и октановые числа продуктов риформинга.
Для восстановления активности и селективности катализаторов их периодически, а на установках с движущимся слоем непрерывно подвергают окислительной регенерации осушенными дымовыми газами при температуре 300 -500 °С и давлении 1, 0 -1, 5 МПа. Во избежание отравления катализатора также применяют инертный газ (азот) высокой чистоты, содержащий не выше 0, 5 % кислорода (по объему). Остаточное содержание кокса после регенерации — менее 0, 02 % (по массе) на катализатор. По окончании выжига кокса проводится восстановительная регенерация катализатора водородом. При обработке катализатора водородом происходит восстановление сернистых соединений до сероводорода, что позволяет снизить содержание серы в катализаторе до 0, 03 — 0, 05 % (по массе). Для поддержания кислотной функции катализатора в газосырьевой поток вводят галогеносодержащие соединения (например, дихлорэтан, водный раствор HCl). Срок службы катализаторов риформинга составляет для катализатора серий АП и КР в среднем 36 -45 и 40 -72 месяцев, соответственно. Температура процессов риформинга обычно находится в интервале 450 -530°С. Повышение температуры ускоряет все основные реакции, при этом возрастает роль реакций ароматизации и гидрокрекинга, увеличиваются выход ароматических углеводородов и октановые числа продуктов риформинга.
 На выбор температуры процесса влияет углеводородный состав сырья. Чем выше содержание парафиновых углеводородов в сырье, тем более высокая температура требуется для получения заданного октанового числа. При нафтеновом сырье минимальные температуры в реакторе поддерживают в интервале 450 -460°С, при парафиновом – 480 -490°С. Максимальный нагрев ограничивается температурой 520 -530°С. Дальнейшее повышение температуры нежелательно, так как процесс сопровождается повышенным газообразованием и ускоренным закоксовыванием катализатора. Поскольку реакции риформинга в целом эндотермичны, а реакторы работают в адиабатическом режиме, процесс протекает ступенчато, последовательно в нескольких аппаратах, с промежуточным подогревом реакционной смеси. При этом падение температуры в реакторах при риформировании бензина составляет от 10 до 43 °С и при ароматизации — от 10 до 70°С. Объем катализатора увеличивают от первой к последующей ступени контакта. Это обеспечивает получение более качественных продуктов. Давление влияет на течение и результаты процесса риформинга. Повышение давления препятствует отравлению и закоксовыванию катализатора. Вместе с тем, с повышением давления уменьшается выход ароматических УВ, возрастают скорости реакций гидрокрекинга, а это ведет к увеличению выхода газообразных углеводородов, снижению выхода водорода и жидкой продукции. При снижении рабочего давления и, следовательно, парциального давления водорода возрастает селективность процесса, увеличивается выход ароматики и уменьшается выход газообразных углеводородов. Снижение парциального давления водорода ухудшает его гидрирующую способность, повышает возможность закоксовывания катализатора и отравления его сернистыми соединениями.
На выбор температуры процесса влияет углеводородный состав сырья. Чем выше содержание парафиновых углеводородов в сырье, тем более высокая температура требуется для получения заданного октанового числа. При нафтеновом сырье минимальные температуры в реакторе поддерживают в интервале 450 -460°С, при парафиновом – 480 -490°С. Максимальный нагрев ограничивается температурой 520 -530°С. Дальнейшее повышение температуры нежелательно, так как процесс сопровождается повышенным газообразованием и ускоренным закоксовыванием катализатора. Поскольку реакции риформинга в целом эндотермичны, а реакторы работают в адиабатическом режиме, процесс протекает ступенчато, последовательно в нескольких аппаратах, с промежуточным подогревом реакционной смеси. При этом падение температуры в реакторах при риформировании бензина составляет от 10 до 43 °С и при ароматизации — от 10 до 70°С. Объем катализатора увеличивают от первой к последующей ступени контакта. Это обеспечивает получение более качественных продуктов. Давление влияет на течение и результаты процесса риформинга. Повышение давления препятствует отравлению и закоксовыванию катализатора. Вместе с тем, с повышением давления уменьшается выход ароматических УВ, возрастают скорости реакций гидрокрекинга, а это ведет к увеличению выхода газообразных углеводородов, снижению выхода водорода и жидкой продукции. При снижении рабочего давления и, следовательно, парциального давления водорода возрастает селективность процесса, увеличивается выход ароматики и уменьшается выход газообразных углеводородов. Снижение парциального давления водорода ухудшает его гидрирующую способность, повышает возможность закоксовывания катализатора и отравления его сернистыми соединениями.
 При риформинге на алюмоплатиновых катализаторах для процессов, вырабатывающих высокооктановые компоненты бензина, давление в последнем реакторе составляет 4 МПа, при получении индивидуальных ароматических углеводородов - 2, 0 -3, 0 МПа. В случае использования полиметаллических катализаторов давление на установках с неподвижным слоем катализатора снижают до 1, 5 -2, 0 МПа, а с движущим слоем — до 0, 7 -1, 5 МПа. Наряду с давлением и температурой важными параметрами процесса являются скорость подачи сырья и кратность циркуляции водородсодержащего газа, которые для установок с неподвижным слоем катализатора соответственно находятся в пределах 1, 2 — 1, 5 ч-1 и 1100 -1800 м 3/м 3 сырья. Для установок с непрерывной регенерацией катализатора эти показатели составляют соответственно 1, 8— 1, 9 ч-1 и 800 -900 м 3/м 3 сырья. За рубежом существует ряд разновидностей процесса каталитического риформинга: гидроформинг, платформинг, катформинг, гудриформинг, ультраформинг, магниформинг, рениформинг и др. Эти процессы различаются назначением, типом катализаторов, аппаратурным и технологическим оформлением. Схема установки каталитического риформинга со стационарным слоем катализатора представлена на Рис. 12. 4.
При риформинге на алюмоплатиновых катализаторах для процессов, вырабатывающих высокооктановые компоненты бензина, давление в последнем реакторе составляет 4 МПа, при получении индивидуальных ароматических углеводородов - 2, 0 -3, 0 МПа. В случае использования полиметаллических катализаторов давление на установках с неподвижным слоем катализатора снижают до 1, 5 -2, 0 МПа, а с движущим слоем — до 0, 7 -1, 5 МПа. Наряду с давлением и температурой важными параметрами процесса являются скорость подачи сырья и кратность циркуляции водородсодержащего газа, которые для установок с неподвижным слоем катализатора соответственно находятся в пределах 1, 2 — 1, 5 ч-1 и 1100 -1800 м 3/м 3 сырья. Для установок с непрерывной регенерацией катализатора эти показатели составляют соответственно 1, 8— 1, 9 ч-1 и 800 -900 м 3/м 3 сырья. За рубежом существует ряд разновидностей процесса каталитического риформинга: гидроформинг, платформинг, катформинг, гудриформинг, ультраформинг, магниформинг, рениформинг и др. Эти процессы различаются назначением, типом катализаторов, аппаратурным и технологическим оформлением. Схема установки каталитического риформинга со стационарным слоем катализатора представлена на Рис. 12. 4.
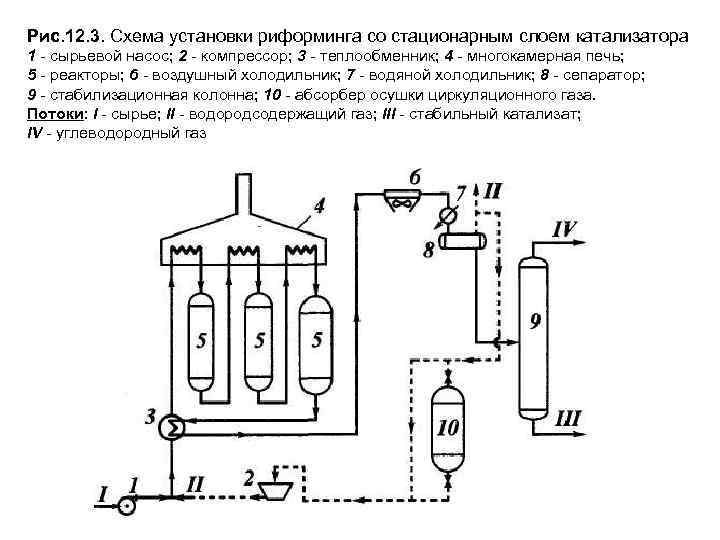 Рис. 12. 3. Схема установки риформинга со стационарным слоем катализатора 1 - сырьевой насос; 2 - компрессор; 3 - теплообменник; 4 - многокамерная печь; 5 - реакторы; 6 - воздушный холодильник; 7 - водяной холодильник; 8 - сепаратор; 9 - стабилизационная колонна; 10 - абсорбер осушки циркуляционного газа. Потоки: I - сырье; II - водородсодержащий газ; III - стабильный катализат; IV - углеводородный газ
Рис. 12. 3. Схема установки риформинга со стационарным слоем катализатора 1 - сырьевой насос; 2 - компрессор; 3 - теплообменник; 4 - многокамерная печь; 5 - реакторы; 6 - воздушный холодильник; 7 - водяной холодильник; 8 - сепаратор; 9 - стабилизационная колонна; 10 - абсорбер осушки циркуляционного газа. Потоки: I - сырье; II - водородсодержащий газ; III - стабильный катализат; IV - углеводородный газ
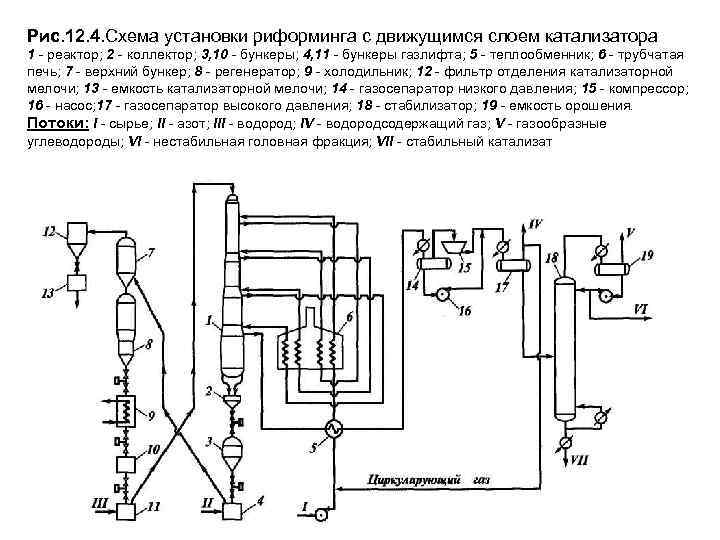 Рис. 12. 4. Схема установки риформинга с движущимся слоем катализатора 1 - реактор; 2 - коллектор; 3, 10 - бункеры; 4, 11 - бункеры газлифта; 5 - теплообменник; 6 - трубчатая печь; 7 - верхний бункер; 8 - регенератор; 9 - холодильник; 12 - фильтр отделения катализаторной мелочи; 13 - емкость катализаторной мелочи; 14 - газосепаратор низкого давления; 15 - компрессор; 16 - насос; 17 - газосепаратор высокого давления; 18 - стабилизатор; 19 - емкость орошения. Потоки: I - сырье; II - азот; III - водород; IV - водородсодержащий газ; V - газообразные углеводороды; VI - нестабильная головная фракция; VII - стабильный катализат
Рис. 12. 4. Схема установки риформинга с движущимся слоем катализатора 1 - реактор; 2 - коллектор; 3, 10 - бункеры; 4, 11 - бункеры газлифта; 5 - теплообменник; 6 - трубчатая печь; 7 - верхний бункер; 8 - регенератор; 9 - холодильник; 12 - фильтр отделения катализаторной мелочи; 13 - емкость катализаторной мелочи; 14 - газосепаратор низкого давления; 15 - компрессор; 16 - насос; 17 - газосепаратор высокого давления; 18 - стабилизатор; 19 - емкость орошения. Потоки: I - сырье; II - азот; III - водород; IV - водородсодержащий газ; V - газообразные углеводороды; VI - нестабильная головная фракция; VII - стабильный катализат
 На Рис. 12. 4. представлена схема установки каталитического риформинга с движущемся слоем катализатора. Гидроочищенное сырье после смешения с водородсодержащим газом и нагрева до температуры реакции в теплообменнике 5 и первой секции четырехсекционной трубчатой печи 6 поступает в первую (верхнюю) ступень четырехступенчатого реактора 1. Затем газопродуктовая смесь последовательно проходит все ступени реактора с промежуточным подогревом в трубчатой печи. Катализатор в реакторе движется плотным слоем сверху вниз. С низа реактора катализатор через систему шлюзования попадает в нижний бункер 4 газлифта. Транспорт катализатора в верхний бункер 7 блока регенерации осуществляется азотом. Из верхнего бункера катализатор поступает в регенератор 8, далее посредством шлюзования проходит холодильник 9 и попадает в бункер газлифта 11. Из бункера 11 катализатор транспортируется водородом на верх реактора. Вышедшая из реактора газопродуктовая смесь проходит теплообменники и холодильники и поступает на разделение. Вначале разделение газовой и жидкой фаз происходит в сепараторе низкого давления 14. Из этого сепаратора газ компрессором 15, а жидкость насосом 16 подают на смешение, а затем после охлаждения поток поступает в сепаратор высокого давления 17. Из сепаратора высокого давления водородсодержащий газ направляют на циркуляцию, а избыток - на гидроочистку. Жидкость направляют в стабилизатор. Применение такой схемы обусловлено низким давлением в реакторе.
На Рис. 12. 4. представлена схема установки каталитического риформинга с движущемся слоем катализатора. Гидроочищенное сырье после смешения с водородсодержащим газом и нагрева до температуры реакции в теплообменнике 5 и первой секции четырехсекционной трубчатой печи 6 поступает в первую (верхнюю) ступень четырехступенчатого реактора 1. Затем газопродуктовая смесь последовательно проходит все ступени реактора с промежуточным подогревом в трубчатой печи. Катализатор в реакторе движется плотным слоем сверху вниз. С низа реактора катализатор через систему шлюзования попадает в нижний бункер 4 газлифта. Транспорт катализатора в верхний бункер 7 блока регенерации осуществляется азотом. Из верхнего бункера катализатор поступает в регенератор 8, далее посредством шлюзования проходит холодильник 9 и попадает в бункер газлифта 11. Из бункера 11 катализатор транспортируется водородом на верх реактора. Вышедшая из реактора газопродуктовая смесь проходит теплообменники и холодильники и поступает на разделение. Вначале разделение газовой и жидкой фаз происходит в сепараторе низкого давления 14. Из этого сепаратора газ компрессором 15, а жидкость насосом 16 подают на смешение, а затем после охлаждения поток поступает в сепаратор высокого давления 17. Из сепаратора высокого давления водородсодержащий газ направляют на циркуляцию, а избыток - на гидроочистку. Жидкость направляют в стабилизатор. Применение такой схемы обусловлено низким давлением в реакторе.
 12. 4. 1. Кинетическая модель процесса риформинга В процессе риформинга происходит большое число одновременно протекающих реакций. Полная кинетическая модель такого процесса должна содержать большое число дифференциальных уравнений, описывающих превращение каждого компонента реакционной смеси. Создание такой системы уравнений довольно сложно и её использование связано со значительными вычислительными трудностями. Кроме того, для идентификации такой модели потребовалось бы аналитическое определение состава смеси по всем компонентам, что также связано с большими затратами труда и времени. Поэтому, при разработке кинетической модели исходят из так называемого метода групповых превращений. При этом происходят в основном следующие полезные химические реакции: 1) Циклопарафины превращаются в ароматические УВ (реакция дегидрирования). 2) Парафины превращаются в циклопарафины (реакция циклизации). 3) Парафины превращаются в изопарафины (реакция изомеризации) Протекают также некоторые побочные реакции: 5) Часть парафинов и циклопарафинов подвергается крекингу, превращаясь при этом в углеводородные газы. 6) Часть циклопарафинов и ароматических углеводородов теряет боковые цепи, которые при этом также превращаются в углеводородные газы.
12. 4. 1. Кинетическая модель процесса риформинга В процессе риформинга происходит большое число одновременно протекающих реакций. Полная кинетическая модель такого процесса должна содержать большое число дифференциальных уравнений, описывающих превращение каждого компонента реакционной смеси. Создание такой системы уравнений довольно сложно и её использование связано со значительными вычислительными трудностями. Кроме того, для идентификации такой модели потребовалось бы аналитическое определение состава смеси по всем компонентам, что также связано с большими затратами труда и времени. Поэтому, при разработке кинетической модели исходят из так называемого метода групповых превращений. При этом происходят в основном следующие полезные химические реакции: 1) Циклопарафины превращаются в ароматические УВ (реакция дегидрирования). 2) Парафины превращаются в циклопарафины (реакция циклизации). 3) Парафины превращаются в изопарафины (реакция изомеризации) Протекают также некоторые побочные реакции: 5) Часть парафинов и циклопарафинов подвергается крекингу, превращаясь при этом в углеводородные газы. 6) Часть циклопарафинов и ароматических углеводородов теряет боковые цепи, которые при этом также превращаются в углеводородные газы.


