ПНТ_Лекция-10-1_pres.ppt
- Количество слайдов: 40
 Процессы и агрегаты нефтегазовых технологий Лекция 12: Термокаталитические процессы вторичной переработки нефти. Каталитические процессы – введение в теорию и аппаратурное оформление Введение 12. 1. Каталитические процессы – введение в теорию 12. 1. 1. Основные стадии и область протекания каталитических процессов 12. 1. 2. Учет внешней диффузии в гетерогенно-каталитических процессах 12. 1. 3. Методы определения лимитирующей стадии гетерогенного процесса 12. 13. 1. По характеру движения жидкости 12. 1. 3. 2. По температурной зависимости overall reaction rate 12. 2. Общие сведения о промышленных катализаторах 12. 2. 1. Химический состав и свойства промышленных катализаторов 12. 2. 2. Схемы получения промышленных катализаторов 12. 3. Основные конструкции каталитических реакторных узлов 12. 3. 1. Реакторы с неподвижным слоем катализатора а) с осевым вводом б) с радиальным вводом 12. 3. 2. Реакторы с псевдоожиженным слоем катализатора
Процессы и агрегаты нефтегазовых технологий Лекция 12: Термокаталитические процессы вторичной переработки нефти. Каталитические процессы – введение в теорию и аппаратурное оформление Введение 12. 1. Каталитические процессы – введение в теорию 12. 1. 1. Основные стадии и область протекания каталитических процессов 12. 1. 2. Учет внешней диффузии в гетерогенно-каталитических процессах 12. 1. 3. Методы определения лимитирующей стадии гетерогенного процесса 12. 13. 1. По характеру движения жидкости 12. 1. 3. 2. По температурной зависимости overall reaction rate 12. 2. Общие сведения о промышленных катализаторах 12. 2. 1. Химический состав и свойства промышленных катализаторов 12. 2. 2. Схемы получения промышленных катализаторов 12. 3. Основные конструкции каталитических реакторных узлов 12. 3. 1. Реакторы с неподвижным слоем катализатора а) с осевым вводом б) с радиальным вводом 12. 3. 2. Реакторы с псевдоожиженным слоем катализатора
 12. 1. Каталитические процессы 12. 1. 1. Основные стадии и область протекания каталитических процессов Каталитические процессы - протекают с участием катализаторов. Катализаторы образуют с одним из реагентов промежуточное соединение, которое затем реагирует с другим реагентом с образованием конечного продукта и выделением катализатора в неизменном виде. Различают гомогенные и гетерогенные катализаторы. При гомогенном катализе катализатор и реагенты находятся в одной фазе. В промышленности, как правило, гомогенный катализ является основным или кислотным. При этом промежуточное соединение образуется либо с ионом ОН- при основном катализе, либо с ионом Н+ при кислотном катализе. При гетерогенном катализе катализатор и регенты находятся в разных фазах. Катализатор, как правило, находится на поверхности твердой фазы, а реагенты находятся в газовой или жидкой фазе. На поверхности твердого катализатора находятся так называемые активные центры. Реагент сорбируется на поверхности катализатора, образуя с активным центром промежуточное соединение, которое либо реагирует с другим реагентом, образуя продукт реакции и освобождая активный центр для следующих актов взаимодействия, либо просто распадается с выделением продукта реакции. Типичный гетерогенный катализатор представляет собой пористый твердый материал с сильно развитой внутренней поверхностью пор и большой удельной поверхностью, где «островками» расположены активные каталитические центры (“active sites”).
12. 1. Каталитические процессы 12. 1. 1. Основные стадии и область протекания каталитических процессов Каталитические процессы - протекают с участием катализаторов. Катализаторы образуют с одним из реагентов промежуточное соединение, которое затем реагирует с другим реагентом с образованием конечного продукта и выделением катализатора в неизменном виде. Различают гомогенные и гетерогенные катализаторы. При гомогенном катализе катализатор и реагенты находятся в одной фазе. В промышленности, как правило, гомогенный катализ является основным или кислотным. При этом промежуточное соединение образуется либо с ионом ОН- при основном катализе, либо с ионом Н+ при кислотном катализе. При гетерогенном катализе катализатор и регенты находятся в разных фазах. Катализатор, как правило, находится на поверхности твердой фазы, а реагенты находятся в газовой или жидкой фазе. На поверхности твердого катализатора находятся так называемые активные центры. Реагент сорбируется на поверхности катализатора, образуя с активным центром промежуточное соединение, которое либо реагирует с другим реагентом, образуя продукт реакции и освобождая активный центр для следующих актов взаимодействия, либо просто распадается с выделением продукта реакции. Типичный гетерогенный катализатор представляет собой пористый твердый материал с сильно развитой внутренней поверхностью пор и большой удельной поверхностью, где «островками» расположены активные каталитические центры (“active sites”).
 При гетерогенном катализе можно выделить следующие основные стадии процесса: 1) транспорт реагентов из объема сплошной фазы к поверхности раздела фаз, называемой также интерфейсом ( «внешний» и «внутренний» ); 2) адсорбция (хемосорбция) реагента на поверхности твердой фазы, на ее активных центрах, с образованием промежуточных соединений; 3) химическое превращение промежуточного соединения в продукты реакции. 4) десорбция продукта реакции с поверхности катализатора; 5) диффузия продукта от поверхности раздела фаз в объем сплошной фазы. В зависимости от соотношения скоростей отдельных стадий гетерогенного каталитического процесса общая скорость процесса лимитируется, или определяется скоростью наиболее медленной стадии. Принято выделять транспорт реагентов к внешней поверхности частиц катализатора. Этот процесс называется внешней диффузией. Далее происходит транспорт реагентов внутрь пористых частиц катализатора. Этот процесс называется внутренней диффузией. Если наиболее медленной стадией является транспорт реагента к внешней поверхности частиц катализатора, то процесс происходит во внешне-диффузионной области. Если наиболее медленной стадией является транспорт реагента внутри пористой частицы катализатора, то считают, что процесс происходит во внутри-диффузионной области. Если наиболее медленной стадией является сама химическая реакция, то считают, что процесс происходит в кинетической области, так как общая скорость процесса лимитируется скоростью химической реакции на поверхности катализатора.
При гетерогенном катализе можно выделить следующие основные стадии процесса: 1) транспорт реагентов из объема сплошной фазы к поверхности раздела фаз, называемой также интерфейсом ( «внешний» и «внутренний» ); 2) адсорбция (хемосорбция) реагента на поверхности твердой фазы, на ее активных центрах, с образованием промежуточных соединений; 3) химическое превращение промежуточного соединения в продукты реакции. 4) десорбция продукта реакции с поверхности катализатора; 5) диффузия продукта от поверхности раздела фаз в объем сплошной фазы. В зависимости от соотношения скоростей отдельных стадий гетерогенного каталитического процесса общая скорость процесса лимитируется, или определяется скоростью наиболее медленной стадии. Принято выделять транспорт реагентов к внешней поверхности частиц катализатора. Этот процесс называется внешней диффузией. Далее происходит транспорт реагентов внутрь пористых частиц катализатора. Этот процесс называется внутренней диффузией. Если наиболее медленной стадией является транспорт реагента к внешней поверхности частиц катализатора, то процесс происходит во внешне-диффузионной области. Если наиболее медленной стадией является транспорт реагента внутри пористой частицы катализатора, то считают, что процесс происходит во внутри-диффузионной области. Если наиболее медленной стадией является сама химическая реакция, то считают, что процесс происходит в кинетической области, так как общая скорость процесса лимитируется скоростью химической реакции на поверхности катализатора.
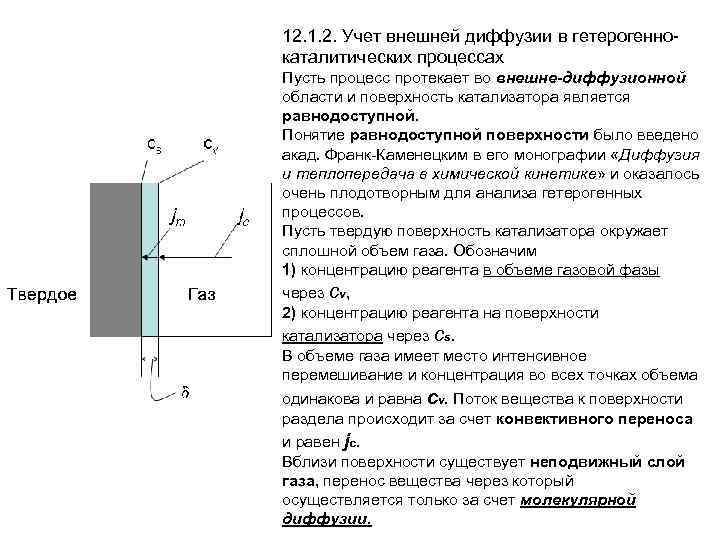 12. 1. 2. Учет внешней диффузии в гетерогеннокаталитических процессах Пусть процесс протекает во внешне-диффузионной области и поверхность катализатора является равнодоступной. Понятие равнодоступной поверхности было введено акад. Франк-Каменецким в его монографии «Диффузия и теплопередача в химической кинетике» и оказалось очень плодотворным для анализа гетерогенных процессов. Пусть твердую поверхность катализатора окружает сплошной объем газа. Обозначим 1) концентрацию реагента в объеме газовой фазы через сv, 2) концентрацию реагента на поверхности катализатора через cs. В объеме газа имеет место интенсивное перемешивание и концентрация во всех точках объема одинакова и равна сv. Поток вещества к поверхности раздела происходит за счет конвективного переноса и равен jc. Вблизи поверхности существует неподвижный слой газа, перенос вещества через который осуществляется только за счет молекулярной диффузии.
12. 1. 2. Учет внешней диффузии в гетерогеннокаталитических процессах Пусть процесс протекает во внешне-диффузионной области и поверхность катализатора является равнодоступной. Понятие равнодоступной поверхности было введено акад. Франк-Каменецким в его монографии «Диффузия и теплопередача в химической кинетике» и оказалось очень плодотворным для анализа гетерогенных процессов. Пусть твердую поверхность катализатора окружает сплошной объем газа. Обозначим 1) концентрацию реагента в объеме газовой фазы через сv, 2) концентрацию реагента на поверхности катализатора через cs. В объеме газа имеет место интенсивное перемешивание и концентрация во всех точках объема одинакова и равна сv. Поток вещества к поверхности раздела происходит за счет конвективного переноса и равен jc. Вблизи поверхности существует неподвижный слой газа, перенос вещества через который осуществляется только за счет молекулярной диффузии.
 Диффузионный поток через неподвижный диффузионный слой толщиной описывается 1 -м законом Фика: На поверхности катализатора протекает гетерогенная реакция. Допустим, что гетерогенная реакция имеет первый порядок по реагенту. Тогда скорость гетерогенной реакции будет равна: (12. 1) Скорость диффузионного потока в соответствии с 1 -м законом Фика будет равна: (12. 2) Учитывая, что толщина диффузионного слоя достаточно мала, можно заменить производную в уравнении (12. 2) ее конечно разностным эквивалентом. Тогда уравнение (12. 2) можно записать в следующем виде: (12. 2 а) Разность концентраций на границах диффузионного слоя равна величине (а) А разность пространственной координаты по толщине диффузионного слоя равна толщине диффузионного слоя: (б)
Диффузионный поток через неподвижный диффузионный слой толщиной описывается 1 -м законом Фика: На поверхности катализатора протекает гетерогенная реакция. Допустим, что гетерогенная реакция имеет первый порядок по реагенту. Тогда скорость гетерогенной реакции будет равна: (12. 1) Скорость диффузионного потока в соответствии с 1 -м законом Фика будет равна: (12. 2) Учитывая, что толщина диффузионного слоя достаточно мала, можно заменить производную в уравнении (12. 2) ее конечно разностным эквивалентом. Тогда уравнение (12. 2) можно записать в следующем виде: (12. 2 а) Разность концентраций на границах диффузионного слоя равна величине (а) А разность пространственной координаты по толщине диффузионного слоя равна толщине диффузионного слоя: (б)
 Подставляя выражения (а) и (б) в уравнение (12. 2 а), получим следующее уравнение для величины диффузионного потока через пограничный слой: (12. 2 б) Обозначим величину отношения коэффициента диффузии к толщине пограничного слоя через . Эта величина называется коэффициентом массопередачи: (12. 3) Окончательно получим выражение для диффузионного потока через пограничный слой: (12. 4) В установившемся состоянии количество вещества, доставляемого к поверхности раздела фаз за счет массопередачи равно количеству вещества, реагирующего на единице поверхности в химической реакции (12. 5) Разрешим уравнение (2. 5) относительно концентрации на поверхности и подставим полученное выражение в уравнение для скорости реакции на поверхности: (12. 6) (12. 7)
Подставляя выражения (а) и (б) в уравнение (12. 2 а), получим следующее уравнение для величины диффузионного потока через пограничный слой: (12. 2 б) Обозначим величину отношения коэффициента диффузии к толщине пограничного слоя через . Эта величина называется коэффициентом массопередачи: (12. 3) Окончательно получим выражение для диффузионного потока через пограничный слой: (12. 4) В установившемся состоянии количество вещества, доставляемого к поверхности раздела фаз за счет массопередачи равно количеству вещества, реагирующего на единице поверхности в химической реакции (12. 5) Разрешим уравнение (2. 5) относительно концентрации на поверхности и подставим полученное выражение в уравнение для скорости реакции на поверхности: (12. 6) (12. 7)
 Разделим числитель и знаменатель выражения (12. 7) на величину произведения. В итоге получим выражение: (12. 8) Обозначим знаменатель выражения (12. 8) через 1/kef (12. 9) Это уравнение выражает закон аддитивности сопротивлений, в соответствии с которым общее сопротивление гетерогенного процесса является суммой диффузионного и кинетического сопротивлений. В итоге получаем уравнение скорости гетерогенного процесса в следующем виде: (12. 10) Из выражения (12. 9) вытекают три возможных режима гетерогенных процессов, протекающих на равнодоступной поверхности: 1) При величине коэффициента массопередачи и В этом случае общая скорость процесса определятся скоростью химической реакции на поверхности и говорят, что процесс протекает в кинетической области, или при кинетическом контроле.
Разделим числитель и знаменатель выражения (12. 7) на величину произведения. В итоге получим выражение: (12. 8) Обозначим знаменатель выражения (12. 8) через 1/kef (12. 9) Это уравнение выражает закон аддитивности сопротивлений, в соответствии с которым общее сопротивление гетерогенного процесса является суммой диффузионного и кинетического сопротивлений. В итоге получаем уравнение скорости гетерогенного процесса в следующем виде: (12. 10) Из выражения (12. 9) вытекают три возможных режима гетерогенных процессов, протекающих на равнодоступной поверхности: 1) При величине коэффициента массопередачи и В этом случае общая скорость процесса определятся скоростью химической реакции на поверхности и говорят, что процесс протекает в кинетической области, или при кинетическом контроле.
 2) При величине коэффициента массопередачи и В этом случае общая скорость процесса определяется скоростью массопередачи, и говорят, что процесс протекает в диффузионной области, или при диффузионном контроле. 3) При соизмеримых величинах коэффициентах массопередачи и константы скорости химической реакции процесс протекает в смешанной, диффузионнокинетической области, или при смешанном контроле. 1. 1. 3 Методы определения лимитирующей стадии гетерогенного процесса 1) По зависимости общей скорости процесса от скорости обтекания частиц твердого вещества потоком жидкости (сжимаемой – газа, или капельной – несжимаемой). Если процесс протекает в диффузионной области, то его скорость, как и скорость массопередачи будут зависеть от скорости движения жидкости. Если режим движения жидкости при обтекании является турбулентным, то наблюдаемая скорость процесса будет пропорциональна скорости движения жидкости в степени 0. 8. Если режим движения ламинарный, то скорость процесса будет зависеть от скорости потока в степени 0. 5.
2) При величине коэффициента массопередачи и В этом случае общая скорость процесса определяется скоростью массопередачи, и говорят, что процесс протекает в диффузионной области, или при диффузионном контроле. 3) При соизмеримых величинах коэффициентах массопередачи и константы скорости химической реакции процесс протекает в смешанной, диффузионнокинетической области, или при смешанном контроле. 1. 1. 3 Методы определения лимитирующей стадии гетерогенного процесса 1) По зависимости общей скорости процесса от скорости обтекания частиц твердого вещества потоком жидкости (сжимаемой – газа, или капельной – несжимаемой). Если процесс протекает в диффузионной области, то его скорость, как и скорость массопередачи будут зависеть от скорости движения жидкости. Если режим движения жидкости при обтекании является турбулентным, то наблюдаемая скорость процесса будет пропорциональна скорости движения жидкости в степени 0. 8. Если режим движения ламинарный, то скорость процесса будет зависеть от скорости потока в степени 0. 5.
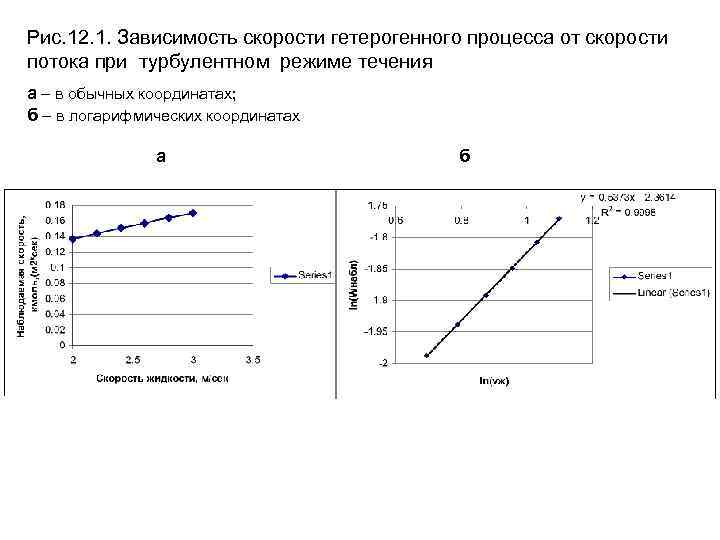 Рис. 12. 1. Зависимость скорости гетерогенного процесса от скорости потока при турбулентном режиме течения а – в обычных координатах; б – в логарифмических координатах а б
Рис. 12. 1. Зависимость скорости гетерогенного процесса от скорости потока при турбулентном режиме течения а – в обычных координатах; б – в логарифмических координатах а б
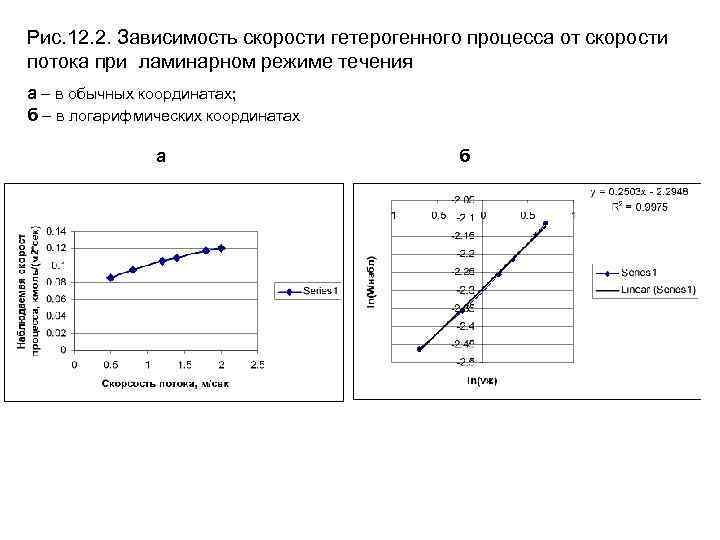 Рис. 12. 2. Зависимость скорости гетерогенного процесса от скорости потока при ламинарном режиме течения а – в обычных координатах; б – в логарифмических координатах а б
Рис. 12. 2. Зависимость скорости гетерогенного процесса от скорости потока при ламинарном режиме течения а – в обычных координатах; б – в логарифмических координатах а б
 2) По температурной зависимости наблюдаемой константы скорости Если так называемая эффективная энергия активации гетерогенного процесса составляет величину более 40 к. Дж/моль, то процесс лимитируется скоростью химической реакции и протекает в кинетической области. Если эффективная энергия активации равна 10 -20 к. Дж/ моль, то процесс проходит в диффузионной области. Если эффективная энергия активации лежит в пределах от 20 до 40 к. Дж/моль, то процесс происходит в смешанной, диффузионно-кинетической области. Если исследовать температурную зависимость наблюдаемой константы скорости гетерогенного процесса в широких температурных пределах, то можно наблюдать переход из кинетической области в диффузионную, вследствие того, что при дальнейшем росте скорости реакции транспорт реагента к поверхности реакции становится меньше скорости его расхода и процесс переходит в диффузионную область. На Рис. 12. 3. представлена температурная зависимость наблюдаемой константы скорости в пределах от 300 до 1500 К. Из данных следует, что при температуре порядка 900 К, происходит переход из кинетической области в диффузионную. На разных участках температурной зависимости можно определить энергию активации. Для кинетической области – Рис. 12. 3 а этой области как видно из рисунка она составляет величину, равную произведению величины углового коэффициента на значение универсальной газовой постоянной.
2) По температурной зависимости наблюдаемой константы скорости Если так называемая эффективная энергия активации гетерогенного процесса составляет величину более 40 к. Дж/моль, то процесс лимитируется скоростью химической реакции и протекает в кинетической области. Если эффективная энергия активации равна 10 -20 к. Дж/ моль, то процесс проходит в диффузионной области. Если эффективная энергия активации лежит в пределах от 20 до 40 к. Дж/моль, то процесс происходит в смешанной, диффузионно-кинетической области. Если исследовать температурную зависимость наблюдаемой константы скорости гетерогенного процесса в широких температурных пределах, то можно наблюдать переход из кинетической области в диффузионную, вследствие того, что при дальнейшем росте скорости реакции транспорт реагента к поверхности реакции становится меньше скорости его расхода и процесс переходит в диффузионную область. На Рис. 12. 3. представлена температурная зависимость наблюдаемой константы скорости в пределах от 300 до 1500 К. Из данных следует, что при температуре порядка 900 К, происходит переход из кинетической области в диффузионную. На разных участках температурной зависимости можно определить энергию активации. Для кинетической области – Рис. 12. 3 а этой области как видно из рисунка она составляет величину, равную произведению величины углового коэффициента на значение универсальной газовой постоянной.
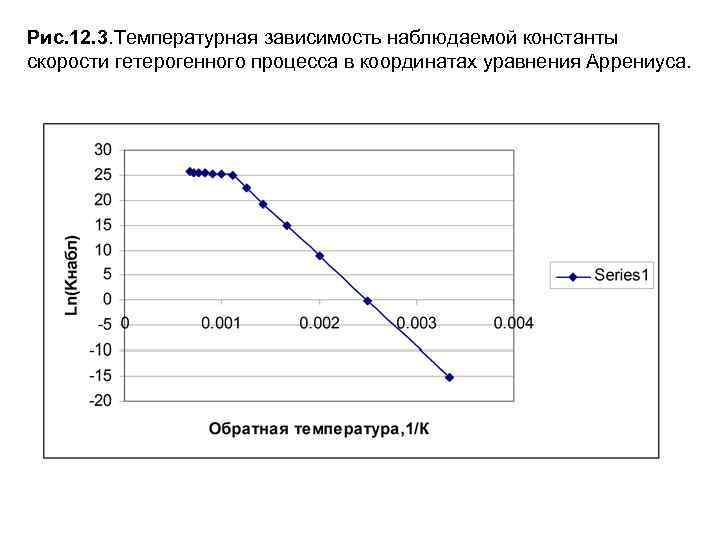 Рис. 12. 3. Температурная зависимость наблюдаемой константы скорости гетерогенного процесса в координатах уравнения Аррениуса.
Рис. 12. 3. Температурная зависимость наблюдаемой константы скорости гетерогенного процесса в координатах уравнения Аррениуса.
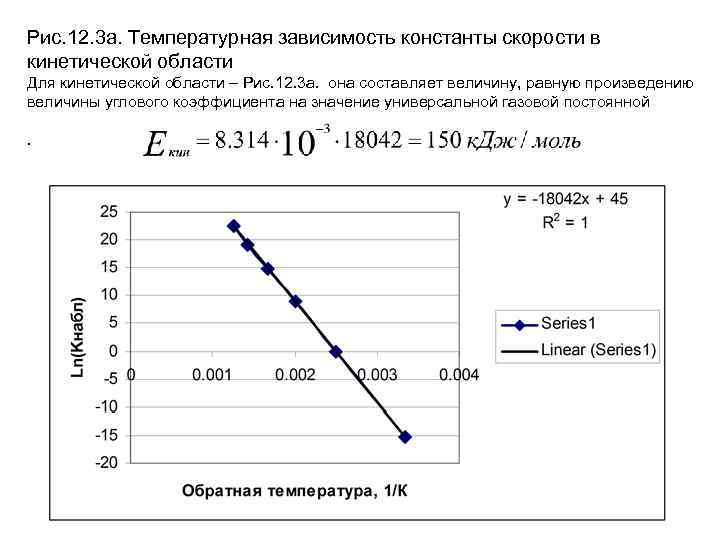 Рис. 12. 3 а. Температурная зависимость константы скорости в кинетической области Для кинетической области – Рис. 12. 3 а. она составляет величину, равную произведению величины углового коэффициента на значение универсальной газовой постоянной.
Рис. 12. 3 а. Температурная зависимость константы скорости в кинетической области Для кинетической области – Рис. 12. 3 а. она составляет величину, равную произведению величины углового коэффициента на значение универсальной газовой постоянной.
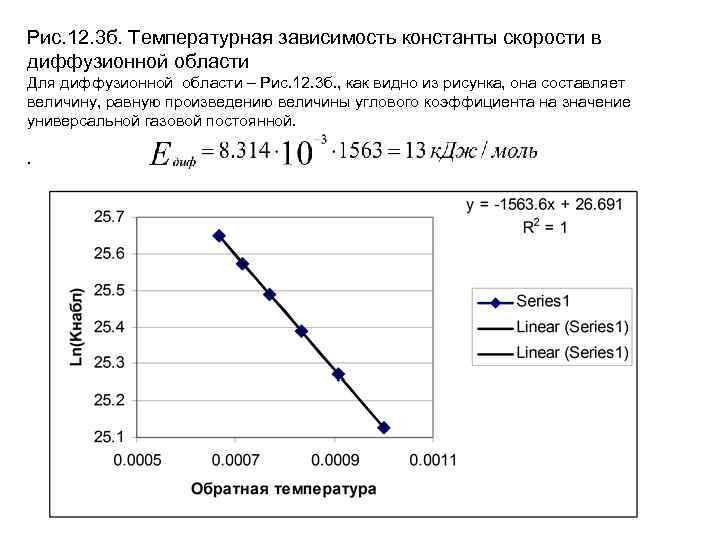 Рис. 12. 3 б. Температурная зависимость константы скорости в диффузионной области Для диффузионной области – Рис. 12. 3 б. , как видно из рисунка, она составляет величину, равную произведению величины углового коэффициента на значение универсальной газовой постоянной. .
Рис. 12. 3 б. Температурная зависимость константы скорости в диффузионной области Для диффузионной области – Рис. 12. 3 б. , как видно из рисунка, она составляет величину, равную произведению величины углового коэффициента на значение универсальной газовой постоянной. .
 Катализаторы - сложные вещества, аморфные или кристаллические, имеющие пористую структуру. Важными параметрами катализаторов служат 1) форма и размер частиц, 2) плотность, удельная поверхность пор, их форма и размер, определяющие доступность для реагентов. Катализаторы подвергают промотированию - вводят промотор (активатор) в состав катализатора или подмешивают его к катализаторной массе. Промотор - это добавка в небольших количествах вещества, которое само по себе может быть каталитически неактивным в отношении данной реакции, но сильно повышает активность и селективность катализатора или улучшает какие-либо его свойства. Промотирование катализаторов каталитического крекинга позволяет осуществлять при регенерации, во-первых, окисление оксида углерода в диоксид, во-вторых, улавливание оксидов серы из дымовых газов регенерации и последующее их восстановление в сероводород в зоне крекинга и вывод сероводорода на этапе разделения продуктов реакции. Технология и техника производства катализаторов включают почти все процессы и аппараты химической технологии. Катализаторы могут быть получены: 1) методом осаждения с последующей сушкой и прокалкой из растворов исходных контактных масс; 2) методом пропитки и нанесения активных компонентов на твердые пористые носители; 3) механическим смешением компонентов и последующим гранулированием - при мокром способе смешивают суспензию с раствором исходных веществ с последующими отжимом, экструзией или прессованием, при сухом способе измельчают исходные вещества с последующими увлажнением, формовкой экструзией или прессованием, термообработкой; 4) плавлением, спеканием исходных компонентов.
Катализаторы - сложные вещества, аморфные или кристаллические, имеющие пористую структуру. Важными параметрами катализаторов служат 1) форма и размер частиц, 2) плотность, удельная поверхность пор, их форма и размер, определяющие доступность для реагентов. Катализаторы подвергают промотированию - вводят промотор (активатор) в состав катализатора или подмешивают его к катализаторной массе. Промотор - это добавка в небольших количествах вещества, которое само по себе может быть каталитически неактивным в отношении данной реакции, но сильно повышает активность и селективность катализатора или улучшает какие-либо его свойства. Промотирование катализаторов каталитического крекинга позволяет осуществлять при регенерации, во-первых, окисление оксида углерода в диоксид, во-вторых, улавливание оксидов серы из дымовых газов регенерации и последующее их восстановление в сероводород в зоне крекинга и вывод сероводорода на этапе разделения продуктов реакции. Технология и техника производства катализаторов включают почти все процессы и аппараты химической технологии. Катализаторы могут быть получены: 1) методом осаждения с последующей сушкой и прокалкой из растворов исходных контактных масс; 2) методом пропитки и нанесения активных компонентов на твердые пористые носители; 3) механическим смешением компонентов и последующим гранулированием - при мокром способе смешивают суспензию с раствором исходных веществ с последующими отжимом, экструзией или прессованием, при сухом способе измельчают исходные вещества с последующими увлажнением, формовкой экструзией или прессованием, термообработкой; 4) плавлением, спеканием исходных компонентов.
 Катализаторы должны обладать рядом важнейших свойств: высокие каталитическую активность и селективность (избирательность), термостойкость, достаточные механическую прочность и износостойкость, устойчивость к отравлению возможными каталитическими ядами, приемлемые срок службы и стоимость, возможность регенерироваться. 1) Каталитическая активность - характеризует изменение скорости данной реакции при введении в реакционную систему катализатора, она определяется выходом целевых продуктов на единицу количества сырья. Ее выражают количеством полученного продукта (или прореагировавшего вещества) в единицу времени на единицу объема катализатора. 2) Селективность (избирательность) - способность катализатора избирательно ускорять целевую реакцию и давать максимальный выход целевого продукта; оценивается отношением скорости целевой реакции к общей скорости превращения необходимых веществ. 3) Термостойкость катализаторов - их способность сохранять активность при повышении температуры и способность к регенерации. При каталитическом, крекинге, риформинге, гидроочистке и других процессах катализатор восстанавливают путем выжига кокса с его поверхности. В регенераторе катализатор нагревается до температуры, превышающей температуру режима реакции в реакторе. При несоблюдении режима регенерации катализатор может терять активность и оплавляться. 4) Износостойкость и прочность катализаторов - обеспечивается прочностью и малой плотностью зерен, сфероидальностью, рельефом их поверхности. 5) Устойчивость к отравлению – способность противостоять каталитическим ядам. Каталитические яды частично или полностью подавляют активность катализаторов. Механизм действия каталитических ядов сводится к хемосорбции их молекул на активных центрах катализатора или химическому взаимодействию другого типа. Действие их, как правило, весьма специфично. Яды, отравляющие одни катализаторы, инертны по отношению к другим.
Катализаторы должны обладать рядом важнейших свойств: высокие каталитическую активность и селективность (избирательность), термостойкость, достаточные механическую прочность и износостойкость, устойчивость к отравлению возможными каталитическими ядами, приемлемые срок службы и стоимость, возможность регенерироваться. 1) Каталитическая активность - характеризует изменение скорости данной реакции при введении в реакционную систему катализатора, она определяется выходом целевых продуктов на единицу количества сырья. Ее выражают количеством полученного продукта (или прореагировавшего вещества) в единицу времени на единицу объема катализатора. 2) Селективность (избирательность) - способность катализатора избирательно ускорять целевую реакцию и давать максимальный выход целевого продукта; оценивается отношением скорости целевой реакции к общей скорости превращения необходимых веществ. 3) Термостойкость катализаторов - их способность сохранять активность при повышении температуры и способность к регенерации. При каталитическом, крекинге, риформинге, гидроочистке и других процессах катализатор восстанавливают путем выжига кокса с его поверхности. В регенераторе катализатор нагревается до температуры, превышающей температуру режима реакции в реакторе. При несоблюдении режима регенерации катализатор может терять активность и оплавляться. 4) Износостойкость и прочность катализаторов - обеспечивается прочностью и малой плотностью зерен, сфероидальностью, рельефом их поверхности. 5) Устойчивость к отравлению – способность противостоять каталитическим ядам. Каталитические яды частично или полностью подавляют активность катализаторов. Механизм действия каталитических ядов сводится к хемосорбции их молекул на активных центрах катализатора или химическому взаимодействию другого типа. Действие их, как правило, весьма специфично. Яды, отравляющие одни катализаторы, инертны по отношению к другим.
 Синтетические цеолитсодержащие катализаторы каталитического крекинга производят на отечественных катализаторных фабриках, а также за рубежом (фирмы «Mobil Oil Corp. » , «Akzo Chemie» , «Engelhard Corp. » и др. ). Катализаторы выпускают в двух вариантах: 1) шариковый (диаметром 3 -4 мм) для процессов с движущимся слоем и 2) микросферический (средний диаметр частиц около 60 мкм) для установок с псевдоожиженным слоем катализатора. Химический состав алюмосиликатного катализатора выражают формулой {Аl 2 О 3 • 4 Si. O 2 • Н 2 О + n. Н 2 О}. Катализатор может быть аморфным или кристаллическим. Основной компонент - активная окись кремния. Ее содержание составляет 75 -80%. Удельная поверхность катализатора от 150 до 500 м 2/г. Средний радиус пор 5 -10 нм. Цеолитсодержащий катализатор представляет собой аморфную алюмосиликатную матрицу с равномерно распределенными по объему кристаллами цеолита (массовая доля 3 -20%). Цеолиты придают катализатору повышенные активность, селективность и стабильность. Цеолит представляет собой алюмосиликат с трехмерной кристаллической структурой. В катализаторах используют цеолиты типа X и У с мольным соотношением Si. O 2 : Аl 2 О 3, составляющим 2, 3 -3, 0 и 3, 1 -6, 0 и радиусом пор 8 -13 и 8 -9 А соответственно. Объем внутренних пор превышает 50% объема частиц. Цеолиты содержат катионы щелочных металлов и редкоземельных элементов (церия и др. ). Это значительно повышает их термическую стабильность.
Синтетические цеолитсодержащие катализаторы каталитического крекинга производят на отечественных катализаторных фабриках, а также за рубежом (фирмы «Mobil Oil Corp. » , «Akzo Chemie» , «Engelhard Corp. » и др. ). Катализаторы выпускают в двух вариантах: 1) шариковый (диаметром 3 -4 мм) для процессов с движущимся слоем и 2) микросферический (средний диаметр частиц около 60 мкм) для установок с псевдоожиженным слоем катализатора. Химический состав алюмосиликатного катализатора выражают формулой {Аl 2 О 3 • 4 Si. O 2 • Н 2 О + n. Н 2 О}. Катализатор может быть аморфным или кристаллическим. Основной компонент - активная окись кремния. Ее содержание составляет 75 -80%. Удельная поверхность катализатора от 150 до 500 м 2/г. Средний радиус пор 5 -10 нм. Цеолитсодержащий катализатор представляет собой аморфную алюмосиликатную матрицу с равномерно распределенными по объему кристаллами цеолита (массовая доля 3 -20%). Цеолиты придают катализатору повышенные активность, селективность и стабильность. Цеолит представляет собой алюмосиликат с трехмерной кристаллической структурой. В катализаторах используют цеолиты типа X и У с мольным соотношением Si. O 2 : Аl 2 О 3, составляющим 2, 3 -3, 0 и 3, 1 -6, 0 и радиусом пор 8 -13 и 8 -9 А соответственно. Объем внутренних пор превышает 50% объема частиц. Цеолиты содержат катионы щелочных металлов и редкоземельных элементов (церия и др. ). Это значительно повышает их термическую стабильность.
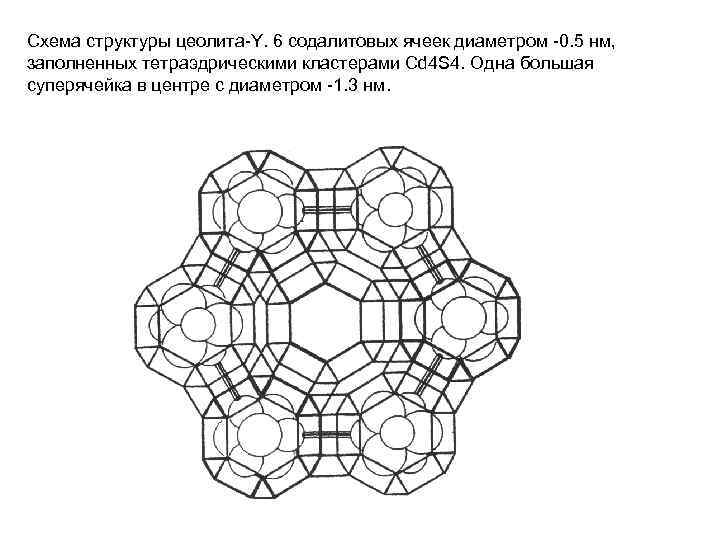 Схема структуры цеолита-Y. 6 содалитовых ячеек диаметром -0. 5 нм, заполненных тетраэдрическими кластерами Cd 4 S 4. Одна большая суперячейка в центре с диаметром -1. 3 нм.
Схема структуры цеолита-Y. 6 содалитовых ячеек диаметром -0. 5 нм, заполненных тетраэдрическими кластерами Cd 4 S 4. Одна большая суперячейка в центре с диаметром -1. 3 нм.
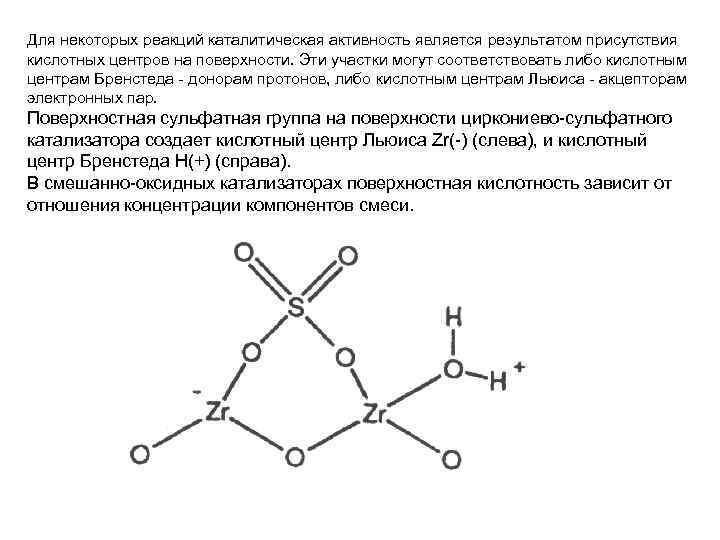 Для некоторых реакций каталитическая активность является результатом присутствия кислотных центров на поверхности. Эти участки могут соответствовать либо кислотным центрам Бренстеда - донорам протонов, либо кислотным центрам Льюиса - акцепторам электронных пар. Поверхностная сульфатная группа на поверхности циркониево-сульфатного катализатора создает кислотный центр Льюиса Zr(-) (слева), и кислотный центр Бренстеда Н(+) (справа). В смешанно-оксидных катализаторах поверхностная кислотность зависит от отношения концентрации компонентов смеси.
Для некоторых реакций каталитическая активность является результатом присутствия кислотных центров на поверхности. Эти участки могут соответствовать либо кислотным центрам Бренстеда - донорам протонов, либо кислотным центрам Льюиса - акцепторам электронных пар. Поверхностная сульфатная группа на поверхности циркониево-сульфатного катализатора создает кислотный центр Льюиса Zr(-) (слева), и кислотный центр Бренстеда Н(+) (справа). В смешанно-оксидных катализаторах поверхностная кислотность зависит от отношения концентрации компонентов смеси.
 Технологическая схема производства микросферического алюмосиликатного катализатора каталитического крекинга представлена на Рис. 12. 4. Катализаторная фабрика имеет три основных отделения: 1) сырьевое, 2) формовочно-промывочное и 3) сушильно-прокалочное. Исходным сырьем служит «силикат-глыба» , гидроксид алюминия Аl(ОН)3, вода и серная кислота. Сырьевое отделение включает два блока. В первом блоке готовят «жидкое стекло» (раствор Na 2 O • n. Si. O 2), во втором — раствор сульфата алюминия Al 2(SO 4)3. Формовочно-промывочное отделение включает узел формовки микросферического алюмосиликатного гидрогеля и узел мокрой обработки гидрогеля. В процессе формования должны соблюдаться дозировка компонентов и температура (10 -12°С).
Технологическая схема производства микросферического алюмосиликатного катализатора каталитического крекинга представлена на Рис. 12. 4. Катализаторная фабрика имеет три основных отделения: 1) сырьевое, 2) формовочно-промывочное и 3) сушильно-прокалочное. Исходным сырьем служит «силикат-глыба» , гидроксид алюминия Аl(ОН)3, вода и серная кислота. Сырьевое отделение включает два блока. В первом блоке готовят «жидкое стекло» (раствор Na 2 O • n. Si. O 2), во втором — раствор сульфата алюминия Al 2(SO 4)3. Формовочно-промывочное отделение включает узел формовки микросферического алюмосиликатного гидрогеля и узел мокрой обработки гидрогеля. В процессе формования должны соблюдаться дозировка компонентов и температура (10 -12°С).
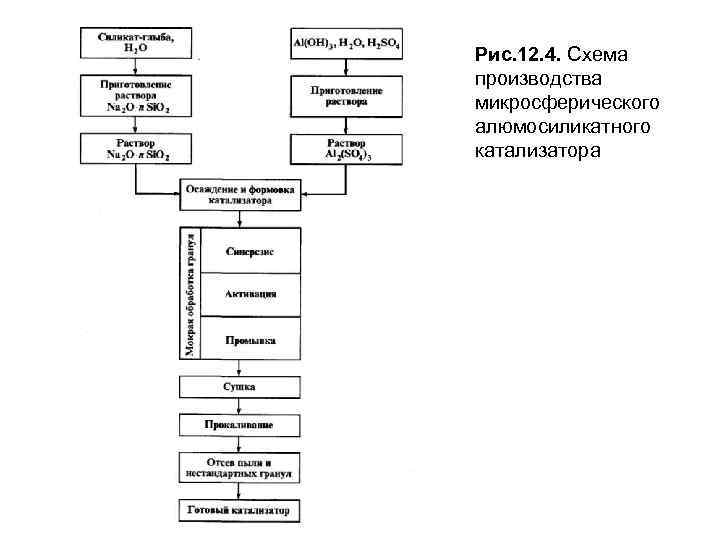 Рис. 12. 4. Схема производства микросферического алюмосиликатного катализатора
Рис. 12. 4. Схема производства микросферического алюмосиликатного катализатора
 Формирование микросфер производят с помощью смесителя-распылителя, распыляя смесь гелеобразующих растворов воздухом (Рис. 12. 5). Образующиеся капельки геля ударяются о поверхность масла, движутся по его поверхности от центра к периферии, теряют скорость и начинают опускаться. Гранулы, пройдя слой масла, поступают в поток формовочной воды и уносятся в транспортирующий желоб и промывочный чан. В образованных глобулах геля происходит синерезис - процесс самопроизвольного выделения интермицеллярной жидкости (воды), сжатие скелета и уменьшение объема. Активация состоит в обработке катализатора слабым раствором сульфата алюминия. В результате происходит катионообмен: неактивные катионы Na+ замещаются активными катионами Аl 3+. Промытый катализатор поступает в сушильно-прокалочное отделение, где в сушильной колонне его сушат воздухом при температуре в верху колонны 315°С, в низу - 485°С. Далее катализатор прокаливают дымовыми газами в цилиндрической прокалочной колонне с расширенной верхней частью в кипящем слое при температуре 600 -650°С. После прокалки катализатор постепенно охлаждают. Представленная схема производства катализатора соответствует гелевой технологии. Более совершенной является так называемая золевая технология, отличие которой состоит в приготовлении и подаче в узел смешения суспензии каолина. При производстве цеолитсодержащего катализатора в узел смешения растворов вводят суспензию цеолита.
Формирование микросфер производят с помощью смесителя-распылителя, распыляя смесь гелеобразующих растворов воздухом (Рис. 12. 5). Образующиеся капельки геля ударяются о поверхность масла, движутся по его поверхности от центра к периферии, теряют скорость и начинают опускаться. Гранулы, пройдя слой масла, поступают в поток формовочной воды и уносятся в транспортирующий желоб и промывочный чан. В образованных глобулах геля происходит синерезис - процесс самопроизвольного выделения интермицеллярной жидкости (воды), сжатие скелета и уменьшение объема. Активация состоит в обработке катализатора слабым раствором сульфата алюминия. В результате происходит катионообмен: неактивные катионы Na+ замещаются активными катионами Аl 3+. Промытый катализатор поступает в сушильно-прокалочное отделение, где в сушильной колонне его сушат воздухом при температуре в верху колонны 315°С, в низу - 485°С. Далее катализатор прокаливают дымовыми газами в цилиндрической прокалочной колонне с расширенной верхней частью в кипящем слое при температуре 600 -650°С. После прокалки катализатор постепенно охлаждают. Представленная схема производства катализатора соответствует гелевой технологии. Более совершенной является так называемая золевая технология, отличие которой состоит в приготовлении и подаче в узел смешения суспензии каолина. При производстве цеолитсодержащего катализатора в узел смешения растворов вводят суспензию цеолита.
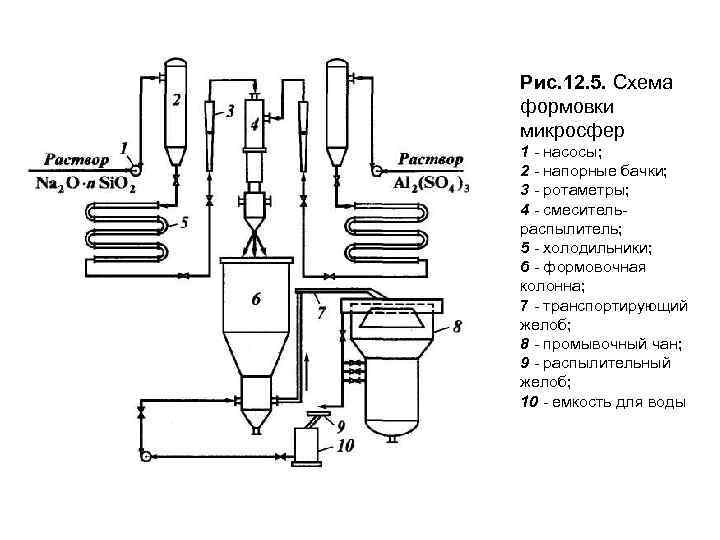 Рис. 12. 5. Схема формовки микросфер 1 - насосы; 2 - напорные бачки; 3 - ротаметры; 4 - смесительраспылитель; 5 - холодильники; 6 - формовочная колонна; 7 - транспортирующий желоб; 8 - промывочный чан; 9 - распылительный желоб; 10 - емкость для воды
Рис. 12. 5. Схема формовки микросфер 1 - насосы; 2 - напорные бачки; 3 - ротаметры; 4 - смесительраспылитель; 5 - холодильники; 6 - формовочная колонна; 7 - транспортирующий желоб; 8 - промывочный чан; 9 - распылительный желоб; 10 - емкость для воды
 Силикагель получается при подкислении растворов силикатов щелочных металлов с последующей промывкой и высушиванием образовавшегося геля. Na 2 Si. O 3 + 2 HCl = 2 Na. Cl + H 2 Si. O 3 = Si. O 2 + H 2 O Силикагель имеет огромную площадь поверхности (до 800 м 2/г), состоящую из групп — Si. OH, расположенных на расстоянии 0, 5 нм друг от друга. Эти группы являются активными центрами, причём активность данной партии силикагеля зависит от числа и активности таких центров. В активном адсорбенте, то есть таком, из которого удалена адсорбированная на его поверхности вода, многие центры будут активны. Такая активация происходит при нагревании геля до 150 -200°C. При нагревании до более высокой температуры в интервале 200 -400°С активность теряется в результате образования связей Si-O, происходящего с отщеплением воды. Эта стадия, однако, обратима. При нагревании выше 400°С размер поверхности силикагеля необратимо уменьшается. Активные центры взаимодействуют с полярными растворёнными веществами главным образом за счёт образования водородных связей.
Силикагель получается при подкислении растворов силикатов щелочных металлов с последующей промывкой и высушиванием образовавшегося геля. Na 2 Si. O 3 + 2 HCl = 2 Na. Cl + H 2 Si. O 3 = Si. O 2 + H 2 O Силикагель имеет огромную площадь поверхности (до 800 м 2/г), состоящую из групп — Si. OH, расположенных на расстоянии 0, 5 нм друг от друга. Эти группы являются активными центрами, причём активность данной партии силикагеля зависит от числа и активности таких центров. В активном адсорбенте, то есть таком, из которого удалена адсорбированная на его поверхности вода, многие центры будут активны. Такая активация происходит при нагревании геля до 150 -200°C. При нагревании до более высокой температуры в интервале 200 -400°С активность теряется в результате образования связей Si-O, происходящего с отщеплением воды. Эта стадия, однако, обратима. При нагревании выше 400°С размер поверхности силикагеля необратимо уменьшается. Активные центры взаимодействуют с полярными растворёнными веществами главным образом за счёт образования водородных связей.
 Рис. 12. 6. Фотография гранул силикагеля до термической активации
Рис. 12. 6. Фотография гранул силикагеля до термической активации
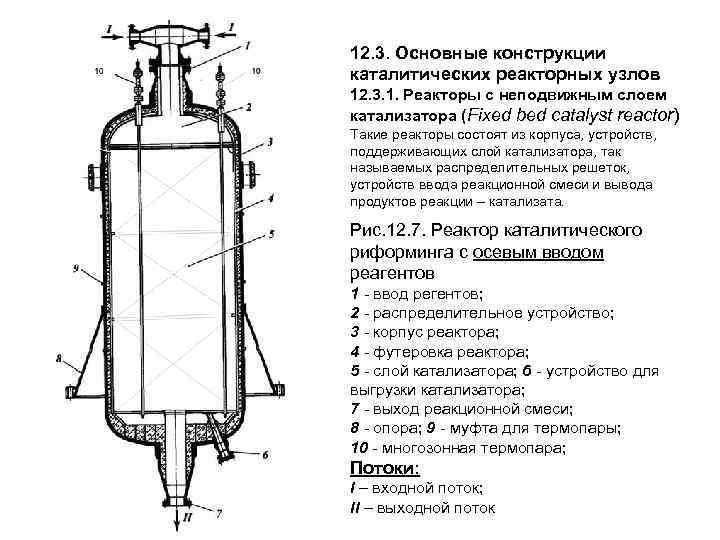 12. 3. Основные конструкции каталитических реакторных узлов 12. 3. 1. Реакторы с неподвижным слоем катализатора (Fixed bed catalyst reactor) Такие реакторы состоят из корпуса, устройств, поддерживающих слой катализатора, так называемых распределительных решеток, устройств ввода реакционной смеси и вывода продуктов реакции – катализата. Рис. 12. 7. Реактор каталитического риформинга с осевым вводом реагентов 1 - ввод регентов; 2 - распределительное устройство; 3 - корпус реактора; 4 - футеровка реактора; 5 - слой катализатора; 6 - устройство для выгрузки катализатора; 7 - выход реакционной смеси; 8 - опора; 9 - муфта для термопары; 10 - многозонная термопара; Потоки: I – входной поток; II – выходной поток
12. 3. Основные конструкции каталитических реакторных узлов 12. 3. 1. Реакторы с неподвижным слоем катализатора (Fixed bed catalyst reactor) Такие реакторы состоят из корпуса, устройств, поддерживающих слой катализатора, так называемых распределительных решеток, устройств ввода реакционной смеси и вывода продуктов реакции – катализата. Рис. 12. 7. Реактор каталитического риформинга с осевым вводом реагентов 1 - ввод регентов; 2 - распределительное устройство; 3 - корпус реактора; 4 - футеровка реактора; 5 - слой катализатора; 6 - устройство для выгрузки катализатора; 7 - выход реакционной смеси; 8 - опора; 9 - муфта для термопары; 10 - многозонная термопара; Потоки: I – входной поток; II – выходной поток
 Такие реакторы с неподвижным слоем катализатора и осевым вводом реагентов получили широкое распространение в промышленности, однако они имеют некоторые принципиальные недостатки, которые особенно резко проявляются при создании реакторных узлов большой производительности. 1) Они отличаются высоким гидравлическим сопротивлением, что требует больших затрат энергии на перекачку реакционной смеси. 2) Вследствие высоких скоростей смеси в таких реакторах заметную роль играет измельчение катализатора и повышенный пылеунос. Это приводит к ухудшению работы циркуляционного контура и сокращению срока службы катализатора.
Такие реакторы с неподвижным слоем катализатора и осевым вводом реагентов получили широкое распространение в промышленности, однако они имеют некоторые принципиальные недостатки, которые особенно резко проявляются при создании реакторных узлов большой производительности. 1) Они отличаются высоким гидравлическим сопротивлением, что требует больших затрат энергии на перекачку реакционной смеси. 2) Вследствие высоких скоростей смеси в таких реакторах заметную роль играет измельчение катализатора и повышенный пылеунос. Это приводит к ухудшению работы циркуляционного контура и сокращению срока службы катализатора.
 На Рис. 12. 8. изображено устройство реактора каталитического риформинга с неподвижным слоем катализатора с радиальным вводом реагентов. В реакторе такого типа площадь поверхности, перпендикулярная направлению потока реагентов, гораздо больше, чем при осевом потоке при том же объем слоя катализатора. За счет этого линейная скорость потока в слое гораздо ниже, что приводит к уменьшению гидравлического сопротивления. Время контакта не изменяется при изменении направления потока, что обеспечивает сохранение степени превращения. При этом существенно сокращаются затраты энергии на перемещение потока реакционной смеси через реактор. Основная проблема конструктивного оформления реакторов с радиальным потоком реагентов - создание такого распределительного устройства, которое бы обеспечивало равные радиальные скорости потока в разных точках по оси реактора. Для этого сопротивление в осевом направлении должно быть много меньше радиального сопротивления слоя.
На Рис. 12. 8. изображено устройство реактора каталитического риформинга с неподвижным слоем катализатора с радиальным вводом реагентов. В реакторе такого типа площадь поверхности, перпендикулярная направлению потока реагентов, гораздо больше, чем при осевом потоке при том же объем слоя катализатора. За счет этого линейная скорость потока в слое гораздо ниже, что приводит к уменьшению гидравлического сопротивления. Время контакта не изменяется при изменении направления потока, что обеспечивает сохранение степени превращения. При этом существенно сокращаются затраты энергии на перемещение потока реакционной смеси через реактор. Основная проблема конструктивного оформления реакторов с радиальным потоком реагентов - создание такого распределительного устройства, которое бы обеспечивало равные радиальные скорости потока в разных точках по оси реактора. Для этого сопротивление в осевом направлении должно быть много меньше радиального сопротивления слоя.
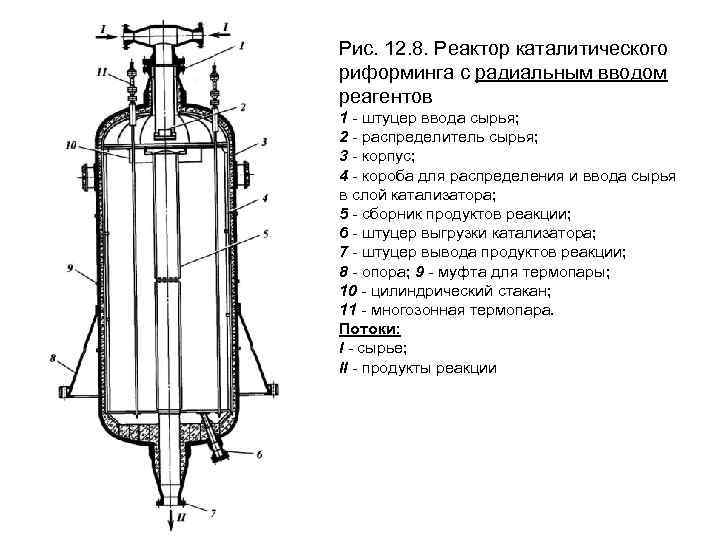 Рис. 12. 8. Реактор каталитического риформинга с радиальным вводом реагентов 1 - штуцер ввода сырья; 2 - распределитель сырья; 3 - корпус; 4 - короба для распределения и ввода сырья в слой катализатора; 5 - сборник продуктов реакции; 6 - штуцер выгрузки катализатора; 7 - штуцер вывода продуктов реакции; 8 - опора; 9 - муфта для термопары; 10 - цилиндрический стакан; 11 - многозонная термопара. Потоки: I - сырье; II - продукты реакции
Рис. 12. 8. Реактор каталитического риформинга с радиальным вводом реагентов 1 - штуцер ввода сырья; 2 - распределитель сырья; 3 - корпус; 4 - короба для распределения и ввода сырья в слой катализатора; 5 - сборник продуктов реакции; 6 - штуцер выгрузки катализатора; 7 - штуцер вывода продуктов реакции; 8 - опора; 9 - муфта для термопары; 10 - цилиндрический стакан; 11 - многозонная термопара. Потоки: I - сырье; II - продукты реакции
 В качестве распределительного устройства в последнее время применяют так называемые скэллопы из сетки Джонсона. Эта сетка состоит из элементов, имеющих в поперечном сечении форму трапеции. Это обеспечивает небольшое сопротивление при малом зазоре между отдельными элементами. Такая конструкция обеспечивает отсутствие истирания катализатора, обеспечивает устранение пылеобразования. Предпочтительным является направление движения потока от наружной поверхности к центру слоя. Поэтому распределительные элементы из сетки Джонсона – скэллопы располагают по наружной поверхности каталитического слоя, а коллектор для сбора продуктов реакции в виде трубы располагают в центре каталитического слоя. Линейная скорость потока реакционной смеси увеличивается по ходу потока, что обеспечивает равномерное прижимание частиц и отсутствие их ударов при колебаниях скорости потока. Коллектор сбора продуктов также собирают из элементов сетки Джонсона, что обеспечивает равномерное сопротивление в радиальном направлении и по оси реактора. На рис. 3. 3 изображена схема движения потоков в реакторе с радиальным вводом реагентов, конструкция которого показана на рис. 3. 2.
В качестве распределительного устройства в последнее время применяют так называемые скэллопы из сетки Джонсона. Эта сетка состоит из элементов, имеющих в поперечном сечении форму трапеции. Это обеспечивает небольшое сопротивление при малом зазоре между отдельными элементами. Такая конструкция обеспечивает отсутствие истирания катализатора, обеспечивает устранение пылеобразования. Предпочтительным является направление движения потока от наружной поверхности к центру слоя. Поэтому распределительные элементы из сетки Джонсона – скэллопы располагают по наружной поверхности каталитического слоя, а коллектор для сбора продуктов реакции в виде трубы располагают в центре каталитического слоя. Линейная скорость потока реакционной смеси увеличивается по ходу потока, что обеспечивает равномерное прижимание частиц и отсутствие их ударов при колебаниях скорости потока. Коллектор сбора продуктов также собирают из элементов сетки Джонсона, что обеспечивает равномерное сопротивление в радиальном направлении и по оси реактора. На рис. 3. 3 изображена схема движения потоков в реакторе с радиальным вводом реагентов, конструкция которого показана на рис. 3. 2.
 12. 3. 2. Реакторы с псевдоожиженнм слоем катализатора Наряду с реакторами с неподвижным слоем катализатора в промышленности получили широкое распространение реакторы с псевдоожиженным слоем катализатора. Псевдоожиженный (кипящий) слой (англ. fluidized bed) - слой мелкозернистых твердых частиц, находящихся в результате воздействия движущейся сквозь него газообразной или жидкой среды в псевдоожиженном (взвешенном, подвижном) состоянии, при котором силы тяжести, архимедовы силы и силы, обусловленные гидродинамическим сопротивлением и действующие на совокупность частиц слоя со стороны среды, уравновешены. При этом твердые частицы, перемещаясь в потоке в различных направлениях, находятся в движении в пределах слоя, а расстояние между ними и объем слоя меняются в зависимости от скорости среды, проходящей через него. Псевдоожиженный слой обладает следующим рядом свойств, аналогичных свойствам жидкости: подвижность, текучесть, вязкость, осаждение и всплывание твердых тел, барботаж газовых пузырей. В нефтепереработке псевдоожиженный слой применяют в реакционных аппаратах установок каталитического крекинга, риформинга, коксования, гидрокрекинга и др. При фильтрации среды через неподвижный слой твердых частиц с ростом скорости W увеличивается гидравлическое сопротивление слоя р. (Рис. 3. 4).
12. 3. 2. Реакторы с псевдоожиженнм слоем катализатора Наряду с реакторами с неподвижным слоем катализатора в промышленности получили широкое распространение реакторы с псевдоожиженным слоем катализатора. Псевдоожиженный (кипящий) слой (англ. fluidized bed) - слой мелкозернистых твердых частиц, находящихся в результате воздействия движущейся сквозь него газообразной или жидкой среды в псевдоожиженном (взвешенном, подвижном) состоянии, при котором силы тяжести, архимедовы силы и силы, обусловленные гидродинамическим сопротивлением и действующие на совокупность частиц слоя со стороны среды, уравновешены. При этом твердые частицы, перемещаясь в потоке в различных направлениях, находятся в движении в пределах слоя, а расстояние между ними и объем слоя меняются в зависимости от скорости среды, проходящей через него. Псевдоожиженный слой обладает следующим рядом свойств, аналогичных свойствам жидкости: подвижность, текучесть, вязкость, осаждение и всплывание твердых тел, барботаж газовых пузырей. В нефтепереработке псевдоожиженный слой применяют в реакционных аппаратах установок каталитического крекинга, риформинга, коксования, гидрокрекинга и др. При фильтрации среды через неподвижный слой твердых частиц с ростом скорости W увеличивается гидравлическое сопротивление слоя р. (Рис. 3. 4).
 При определенном значении скорости фильтрации сцепление между частицами нарушается и слой частиц переходит в псевдоожиженное состояние. Скорость среды, при которой слой твердых частиц переходит в псевдоожиженное состояние, называют критической или скоростью начала псевдоожижения WK. В дальнейшем с увеличением скорости среды W слой расширяется, порозность его увеличивается и в результате гидравлическое сопротивление слоя потоку остается постоянным. Скачкообразное уменьшение гидравлического сопротивления в момент наступления псевдоожиженного состояния слоя на величину р0 связано с преодолением сил сцепления частиц. При дальнейшем увеличении скорости среды наступает режим пневмотранспорта, когда частицы начинают уноситься из слоя. Верхним пределом существования псевдоожиженного слоя является скорость витания одиночной частицы WB. Отношение скорости среды в пределах интервала скоростей существования псевдоожиженного слоя WK — WB к скорости начала псевдоожижения называют числом псевдоожижения K = W/WK.
При определенном значении скорости фильтрации сцепление между частицами нарушается и слой частиц переходит в псевдоожиженное состояние. Скорость среды, при которой слой твердых частиц переходит в псевдоожиженное состояние, называют критической или скоростью начала псевдоожижения WK. В дальнейшем с увеличением скорости среды W слой расширяется, порозность его увеличивается и в результате гидравлическое сопротивление слоя потоку остается постоянным. Скачкообразное уменьшение гидравлического сопротивления в момент наступления псевдоожиженного состояния слоя на величину р0 связано с преодолением сил сцепления частиц. При дальнейшем увеличении скорости среды наступает режим пневмотранспорта, когда частицы начинают уноситься из слоя. Верхним пределом существования псевдоожиженного слоя является скорость витания одиночной частицы WB. Отношение скорости среды в пределах интервала скоростей существования псевдоожиженного слоя WK — WB к скорости начала псевдоожижения называют числом псевдоожижения K = W/WK.
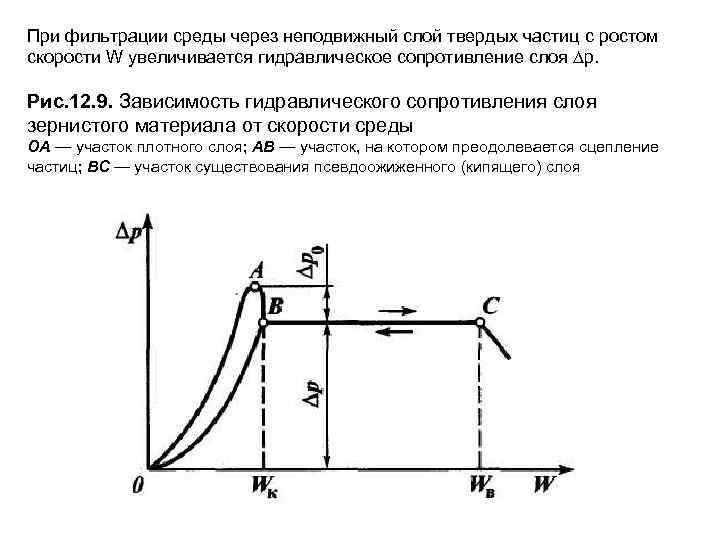 При фильтрации среды через неподвижный слой твердых частиц с ростом скорости W увеличивается гидравлическое сопротивление слоя р. Рис. 12. 9. Зависимость гидравлического сопротивления слоя зернистого материала от скорости среды ОА — участок плотного слоя; АВ — участок, на котором преодолевается сцепление частиц; ВС — участок существования псевдоожиженного (кипящего) слоя
При фильтрации среды через неподвижный слой твердых частиц с ростом скорости W увеличивается гидравлическое сопротивление слоя р. Рис. 12. 9. Зависимость гидравлического сопротивления слоя зернистого материала от скорости среды ОА — участок плотного слоя; АВ — участок, на котором преодолевается сцепление частиц; ВС — участок существования псевдоожиженного (кипящего) слоя
 Достоинства псевдоожиженного слоя: 1) большая поверхность взаимодействия контактирующих фаз; 2) интенсивное перемешивание твердой фазы, приводящее к практическому выравниванию температур и концентраций в рабочем объеме, что исключает локальный перегрев (или переохлаждение) в тепловых и реакционных процессах; 3) высокие значения коэффициентов эффективной теплопроводности и теплоотдачи от псевдоожиженного слоя к поверхности; 4) подвижность (текучесть) слоя, что позволяет создавать аппараты для непрерывных процессов. Недостатки псевдоожиженного слоя: 1) уменьшение движущей силы процесса в связи с интенсивным перемешиванием (однако это обычно компенсируют применением противоточно-ступенчатой схемы аппарата), 2) износ твердых частиц, 3) эрозия аппаратуры. В зависимости от режима псевдоожижения и структуры слоя различают следующие варианты псевдоожиженного слоя: 1) однородный, 2) неоднородный, 3) с барботажем газовых пузырей, 4) с каналообразованием и 5) фонтанирующий.
Достоинства псевдоожиженного слоя: 1) большая поверхность взаимодействия контактирующих фаз; 2) интенсивное перемешивание твердой фазы, приводящее к практическому выравниванию температур и концентраций в рабочем объеме, что исключает локальный перегрев (или переохлаждение) в тепловых и реакционных процессах; 3) высокие значения коэффициентов эффективной теплопроводности и теплоотдачи от псевдоожиженного слоя к поверхности; 4) подвижность (текучесть) слоя, что позволяет создавать аппараты для непрерывных процессов. Недостатки псевдоожиженного слоя: 1) уменьшение движущей силы процесса в связи с интенсивным перемешиванием (однако это обычно компенсируют применением противоточно-ступенчатой схемы аппарата), 2) износ твердых частиц, 3) эрозия аппаратуры. В зависимости от режима псевдоожижения и структуры слоя различают следующие варианты псевдоожиженного слоя: 1) однородный, 2) неоднородный, 3) с барботажем газовых пузырей, 4) с каналообразованием и 5) фонтанирующий.
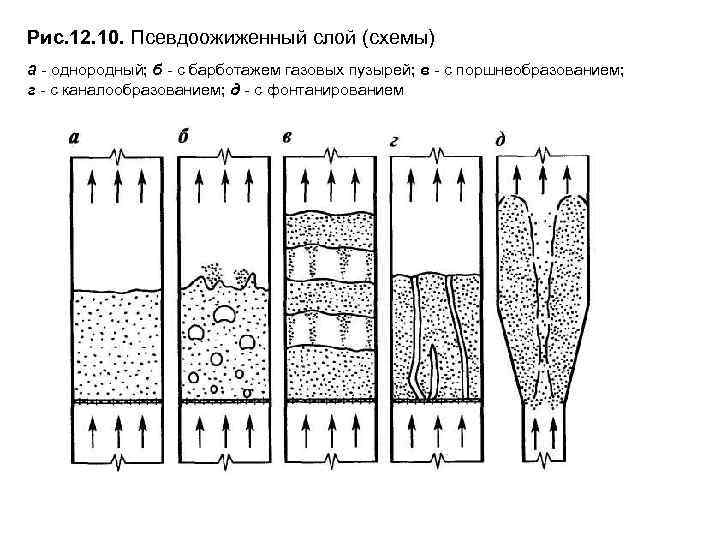 Рис. 12. 10. Псевдоожиженный слой (схемы) а - однородный; б - с барботажем газовых пузырей; в - с поршнеобразованием; г - с каналообразованием; д - с фонтанированием
Рис. 12. 10. Псевдоожиженный слой (схемы) а - однородный; б - с барботажем газовых пузырей; в - с поршнеобразованием; г - с каналообразованием; д - с фонтанированием
 На характер псевдоожижения и структуру слоя оказывают влияние как технологические параметры (физические свойства ожижающей среды, геометрические характеристики и плотность твердых частиц, скорость ожижающего агента, пульсации потока), так и конструктивные (высота и диаметр слоя, форма аппарата, конструкция газораспределительных устройств, секционирующие слой насадки и т. п. ). При использовании в качестве ожижающей среды жидкости наблюдается более однородная структура слоя, а газа — неоднородный псевдоожиженный слой, состоящий из непрерывной фазы и пузырей, при этом одна часть ожижающей среды проходит через пузыри, другая — фильтруется через непрерывную фазу слоя. В зависимости от особенностей реализации процесса может образовываться фонтанирующий слой (в конических аппаратах); сменно-циклический псевдоожиженный слой (подача среды в циклическом режиме или зонально со сменой во времени зон подачи по площади решетки); заторможенный — слой, высота которого ограничена верхней решеткой; секционированный — псевдоожижение в насадке. Псевдоожиженный слой получают в гравитационном поле и поле центробежных или магнитных сил (для ферромагнитных частиц), а также вибрационным способом (виброкипящий слой), сочетанием перечисленных воздействий на сыпучий материал. При использовании одновременно двух ожижающих сред (жидкой и газообразной) псевдоожиженный слой называют трехфазным.
На характер псевдоожижения и структуру слоя оказывают влияние как технологические параметры (физические свойства ожижающей среды, геометрические характеристики и плотность твердых частиц, скорость ожижающего агента, пульсации потока), так и конструктивные (высота и диаметр слоя, форма аппарата, конструкция газораспределительных устройств, секционирующие слой насадки и т. п. ). При использовании в качестве ожижающей среды жидкости наблюдается более однородная структура слоя, а газа — неоднородный псевдоожиженный слой, состоящий из непрерывной фазы и пузырей, при этом одна часть ожижающей среды проходит через пузыри, другая — фильтруется через непрерывную фазу слоя. В зависимости от особенностей реализации процесса может образовываться фонтанирующий слой (в конических аппаратах); сменно-циклический псевдоожиженный слой (подача среды в циклическом режиме или зонально со сменой во времени зон подачи по площади решетки); заторможенный — слой, высота которого ограничена верхней решеткой; секционированный — псевдоожижение в насадке. Псевдоожиженный слой получают в гравитационном поле и поле центробежных или магнитных сил (для ферромагнитных частиц), а также вибрационным способом (виброкипящий слой), сочетанием перечисленных воздействий на сыпучий материал. При использовании одновременно двух ожижающих сред (жидкой и газообразной) псевдоожиженный слой называют трехфазным.
 Главные преимущества реакторов с псевдооожиженным слоем: • низкое гидравлическое сопротивление • высокая интенсивность процессов тепло- и массообмена между твердой фазой и ожижающей газовой средой. В таких реакторах легко обеспечить равномерную температуру в слое катализатора и обеспечить протекание процесса в кинетической или внутридиффузионной области, так как вследствие высокой интенсивности процессов переноса тепла и массы в слое внешняя диффузия в таких реакторах не является лимитирующей стадией.
Главные преимущества реакторов с псевдооожиженным слоем: • низкое гидравлическое сопротивление • высокая интенсивность процессов тепло- и массообмена между твердой фазой и ожижающей газовой средой. В таких реакторах легко обеспечить равномерную температуру в слое катализатора и обеспечить протекание процесса в кинетической или внутридиффузионной области, так как вследствие высокой интенсивности процессов переноса тепла и массы в слое внешняя диффузия в таких реакторах не является лимитирующей стадией.
 12. 4. Учет внутренней диффузии в гетерогенных каталитических процессах Катализаторы для каталитических процессов изготавливают в виде частиц различной формы, чаще всего в виде таблеток цилиндрической или сферической формы. Эти таблетки имеют развитую пористую структуру, что позволяет создавать катализаторы, имеющие внутреннюю поверхность пор, достигающих нескольких сотен м 2 на грамм. При такой структуре гранул большая часть химических превращений протекает внутри частицы катализатора. Рассмотрим вывод уравнения математической модели каталитического процесса, протекающего внутри пористой частицы катализатора. Для анализа процессов и вывода уравнений математической модели чаще всего используют так называемую квазигомогенную модель частицы катализатора. В соответствии с этой моделью частицу рассматривают как некую изотропную среду, обладающую проницаемостью для реагентов и продуктов реакции и обладающую каталитическими свойствами к превращению исходного реагента в продукты реакции. При этих допущениях можно считать, что транспорт вещества внутри пористой частицы катализатора подчинятся закону диффузии Фика, а скорость гетерогенной реакции на внутренней поверхности катализатора может быть отнесена к единице объема катализатора при введении так называемой удельной поверхности, т. е. поверхности, отнесенной к единице объема катализатора.
12. 4. Учет внутренней диффузии в гетерогенных каталитических процессах Катализаторы для каталитических процессов изготавливают в виде частиц различной формы, чаще всего в виде таблеток цилиндрической или сферической формы. Эти таблетки имеют развитую пористую структуру, что позволяет создавать катализаторы, имеющие внутреннюю поверхность пор, достигающих нескольких сотен м 2 на грамм. При такой структуре гранул большая часть химических превращений протекает внутри частицы катализатора. Рассмотрим вывод уравнения математической модели каталитического процесса, протекающего внутри пористой частицы катализатора. Для анализа процессов и вывода уравнений математической модели чаще всего используют так называемую квазигомогенную модель частицы катализатора. В соответствии с этой моделью частицу рассматривают как некую изотропную среду, обладающую проницаемостью для реагентов и продуктов реакции и обладающую каталитическими свойствами к превращению исходного реагента в продукты реакции. При этих допущениях можно считать, что транспорт вещества внутри пористой частицы катализатора подчинятся закону диффузии Фика, а скорость гетерогенной реакции на внутренней поверхности катализатора может быть отнесена к единице объема катализатора при введении так называемой удельной поверхности, т. е. поверхности, отнесенной к единице объема катализатора.
 В этом случае, частица катализатора может характеризоваться эффективным коэффициентом диффузии, Deff и константой скоростью, отнесенной к единице объема катализатора kv. С учетом введенных понятий, можно записать: (12. 13) Где - коэффициент молекулярной диффузии, м 2/сек - пористость катализатора, отношение свободного объема пор Vпор к объему катализатора Vкат, м 3/ м 3. - коэффициент извилистости пор, отношение средней длины транспортной Поры к радиусу частицы катализатора , м/м. - константа скорости гетерогенного процесса отнесенная к единице объема пористой частицы катализатора, 1/сек (для реакции первого порядка) khet - константа скорости гетерогенного процесса, м/сек (для реакции первого порядка); Sуд- удельная поверхность катализатора, отнесенная к единице объема твердой фазы, м 2/м 3.
В этом случае, частица катализатора может характеризоваться эффективным коэффициентом диффузии, Deff и константой скоростью, отнесенной к единице объема катализатора kv. С учетом введенных понятий, можно записать: (12. 13) Где - коэффициент молекулярной диффузии, м 2/сек - пористость катализатора, отношение свободного объема пор Vпор к объему катализатора Vкат, м 3/ м 3. - коэффициент извилистости пор, отношение средней длины транспортной Поры к радиусу частицы катализатора , м/м. - константа скорости гетерогенного процесса отнесенная к единице объема пористой частицы катализатора, 1/сек (для реакции первого порядка) khet - константа скорости гетерогенного процесса, м/сек (для реакции первого порядка); Sуд- удельная поверхность катализатора, отнесенная к единице объема твердой фазы, м 2/м 3.
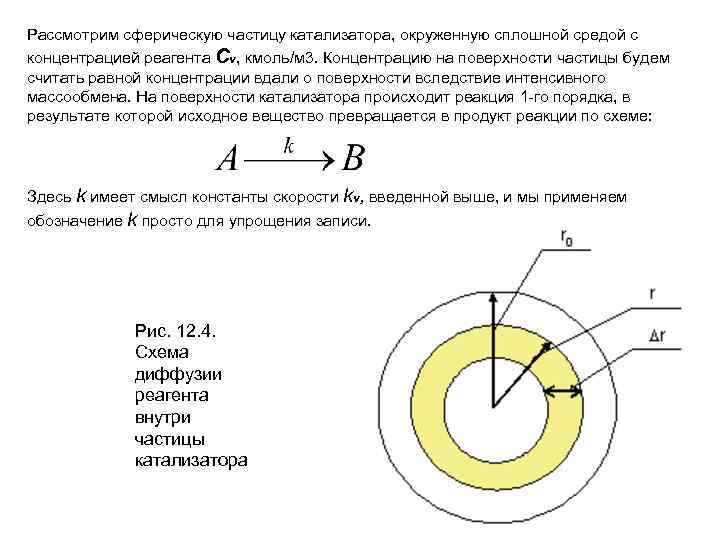 Рассмотрим сферическую частицу катализатора, окруженную сплошной средой с концентрацией реагента Сv, кмоль/м 3. Концентрацию на поверхности частицы будем считать равной концентрации вдали о поверхности вследствие интенсивного массообмена. На поверхности катализатора происходит реакция 1 -го порядка, в результате которой исходное вещество превращается в продукт реакции по схеме: Здесь k имеет смысл константы скорости kv, введенной выше, и мы применяем обозначение k просто для упрощения записи. Рис. 12. 4. Схема диффузии реагента внутри частицы катализатора
Рассмотрим сферическую частицу катализатора, окруженную сплошной средой с концентрацией реагента Сv, кмоль/м 3. Концентрацию на поверхности частицы будем считать равной концентрации вдали о поверхности вследствие интенсивного массообмена. На поверхности катализатора происходит реакция 1 -го порядка, в результате которой исходное вещество превращается в продукт реакции по схеме: Здесь k имеет смысл константы скорости kv, введенной выше, и мы применяем обозначение k просто для упрощения записи. Рис. 12. 4. Схема диффузии реагента внутри частицы катализатора


