Lek_3_stomat_kompl_i_elektrod_prots.ppt
- Количество слайдов: 34

Процеси комплексоутворення та осадження в біологічних рідинах. Електродні процеси. Лекція 3 стомат

Комплексні сполуки • Комплексні сполуки – складні речовини, що містять комплексоутворювач, який координує навколо себе групи-ліганди і утворює координаційну сферу.

Теорія Вернера (1893 р. ): Сучасна теорія: 1) Комплексоутворювачами є 1) Центральний атом – елементи, які мають комплексоутворювач має незайняті електронні оболонки (найчастіше dкрім головних валентностей елементи) на які вони – побічні і утворює з можуть приймати ліганди. лігандами додаткові зв’язки. 2) Ліганди – частинки з надлишком електронної 2) Ліганди – це частинки, що густини (аніони чи полярні об’єднюються із молекули), це донори в комплексоутворювачем в утвореному з координаційну сферу. комплексоутворювачем донорно-акцепторному зв’язку. 3) Число зв’язків – координаційне число. Найчастіше 2, 4, 6.
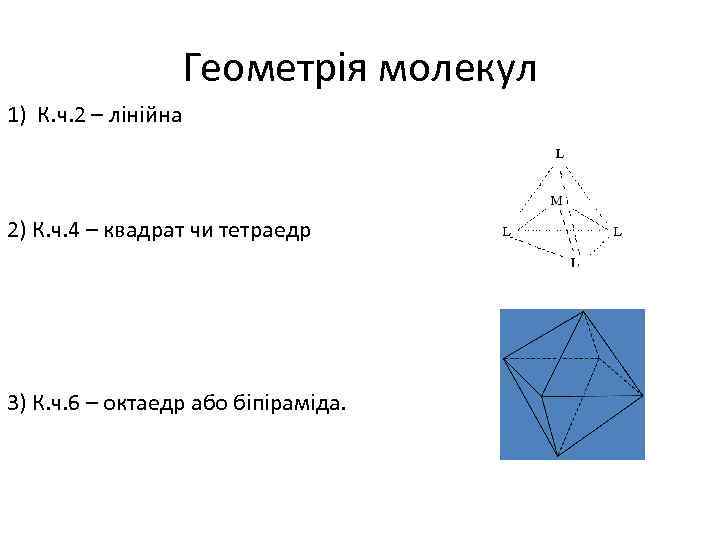
Геометрія молекул 1) К. ч. 2 – лінійна 2) К. ч. 4 – квадрат чи тетраедр 3) К. ч. 6 – октаедр або біпіраміда.

Класифікації комплексних сполук: 1) неорганічні комплекси 2) органічні (хелати). Неорганічні комплекси класифікують за типом лігандів: 1) Ацидокомплекси. Ліганди аніони кислот: Cl - хлоро; F - флуоро; SO 2 -4 - сульфато ; CN- - ціано ; SCN тіоціано; OH- -гідроксо. 2) Нейтральні комплекси: Аквакомплекси – Н 2 О Аміачні комплекси – NН 3
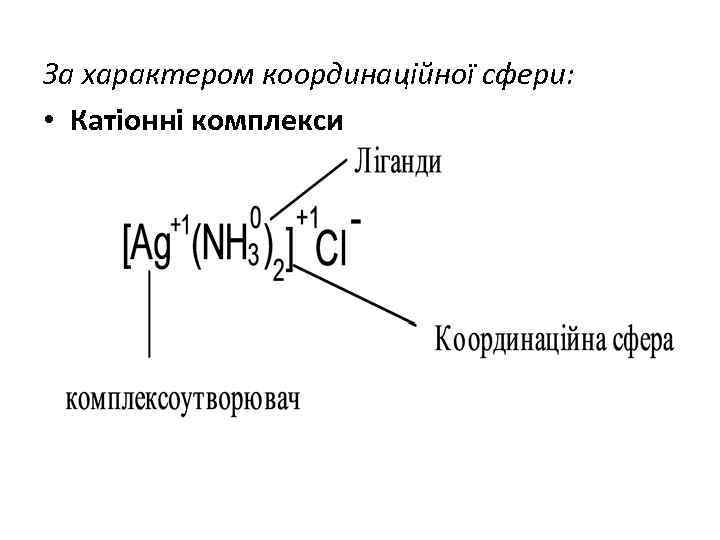
За характером координаційної сфери: • Катіонні комплекси
![• Аніонні комплекси 4 Fe. Cl 3 + 3 K 4[Fe(CN)6] → Fe • Аніонні комплекси 4 Fe. Cl 3 + 3 K 4[Fe(CN)6] → Fe](https://present5.com/presentation/26554412_237433428/image-7.jpg)
• Аніонні комплекси 4 Fe. Cl 3 + 3 K 4[Fe(CN)6] → Fe 4[Fe(CN)6]3↓ + 12 KCl Синій осад
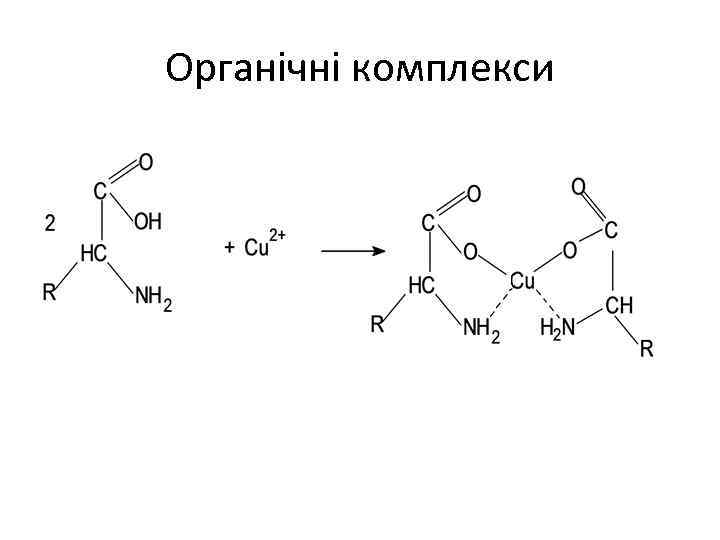
Органічні комплекси
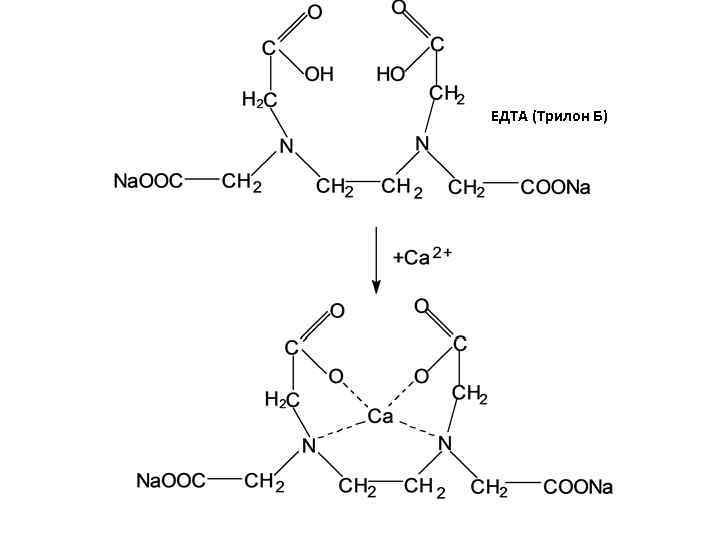
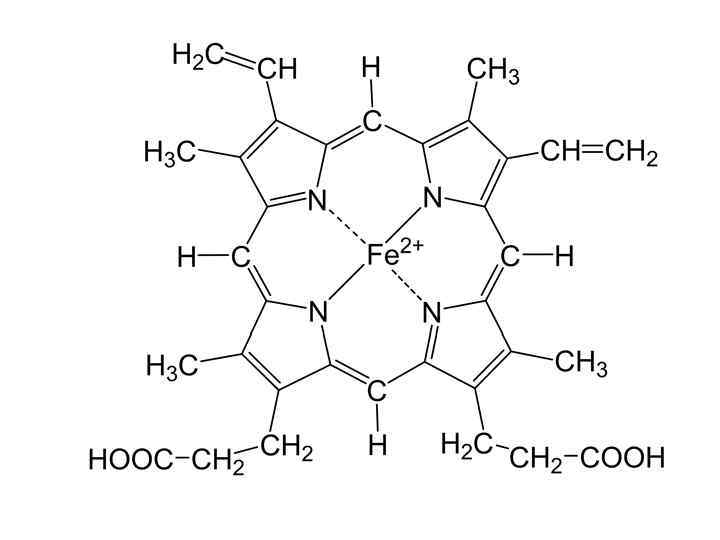
ЕДТА (Трилон Б)

• Умови осадження осадів. • Ag. Cl ↔ Ag+ + Cl • Тверда фаза насичений розчин • У насиченому розчині [Ag+] · [Cl-]=Kр=ДР(Ag. Cl) • У загальному вигляді: • Am. Bn ↔m. An+ + n. B-m • ДРAm. Bn = [An+]m · [B-m]n

• Розчинність визначають за формулою: • Осад утворюється якщо: ЙД > ДР • Якщо ЙД < ДР – йде розчинення. • [Ag+] · [Cl-] < ДР(Ag. Cl) • [Ag+] · [Cl-] = ДР(Ag. Cl)

• Розчинність понижується при додаванні електролітів з однойменними йонами. • Щоб розчинити осад необхідно зв’язати один із йонів в менш розчинну сполуку чи газ. • Основний компонент кісткової тканини – гідроксоапатит • 5 Са 2+ + 3 НРО 4 -2 + Н 2 О ↔ Са 5(ОН)·(РО 4)3 +4 Н+ • ДР = 1, 6 · 10 -58 • У плазмі крові [Ca 2+] = 2, 5 · 10 -3 моль/дм 3 • [HPO 42 -] = 2, 9 · 10 -4 моль/дм 3 • ЙДСа. НРО 4 = 2, 7 · 10 -7 – утворюються мікрокристали Са. НРО 4

• У слабколужному середовищі: • 5 Са. НРО 4 + 6 ОН- → Са 5(ОН)(РО 4)3 + 2 РО 43 - +5 Н 2 О • Підвищення кислотності приводить до розчинення гідроксоапатиту (при карієсі) • За наявності F- утворюється фтороапатит • Са 2 F(PO 4)3 – стійкий до дії кислот. • Надлишок йонів – утворення каміння в нирках, печінці, на стінках кровоносних судин.

Електрохімічні процеси І. Процеси в тканинах і біологічних рідинах під дією зовнішнього струму. Використовується – для діагностики захворювань та лікування при порушенні нормальних значень електропровідності. ІІ. Процеси утворення електродного потенціалу без зовнішнього поля. Використовується: 1) для практичного визначення р. Н, концентрації йонів та окисно-відновних потенціалів за допомогою спеціальних приладів. 2) знання природи біо потенціалів допомагає розшифровувати електрокардіаграми та енцефалограми. Ставити правильний діагноз.
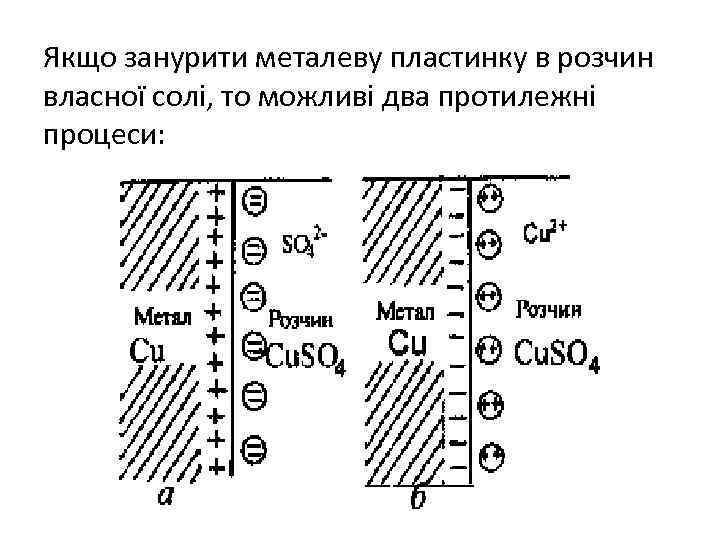
Якщо занурити металеву пластинку в розчин власної солі, то можливі два протилежні процеси:

а) перехід йонів металу із пластинки в розчин під дією диполів води: Ме Меn+ + nē б) осадження йонів Меn+ на пластинці: Меn+ + nē Ме чим більша буде різниця υ1 -υ2 тим негативнішим буде заряд електроду.

Рівноважний стан різниці потенціалів на межі метал-розчин називають електродним потенциалом визначається рівнянням Нернста Е 0 – нормальний (стандартний потенціал виміряний при 298 К р = 1 атм. , а с = 1 моль/л), В; а– концентрація (активність) йонів в моль/л; R – газова стала (8, 314 Дж/моль*К); T – абсолютна температура, К; n – число електронів, що втрачаються металом при утворенні катіонів F – стала Фарадея

Якщо ввести сталі числові значення R і F то при стандартній температурі 298 о. С рівняння Нернста прийме вигляд Коли с=1 моль/л, то Е = Ео – стандартний потенціал Виміряти електродний потенціал можна лише помістивши його в замкнуте коло із іншим електродом (електродом порівняння) за допомогою гальванометра.
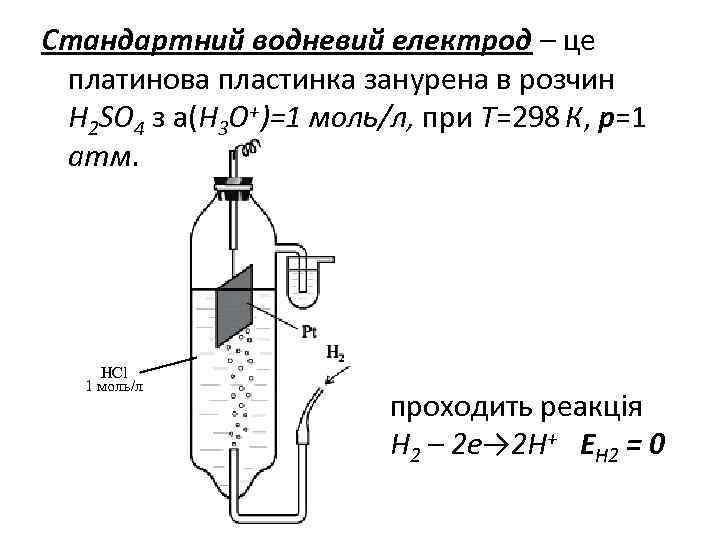
Стандартний водневий електрод – це платинова пластинка занурена в розчин H 2 SO 4 з а(Н 3 О+)=1 моль/л, при T=298 К, р=1 атм. HCl 1 моль/л проходить реакція Н 2 – 2 е→ 2 Н+ ЕН 2 = 0

Електроди І роду. Це металеві пластинки занурені в розчин власних солей, оборотні відносно катіона або аніона і двохфазні. Ме/Меn+ Гальваноз- виникнення електричного струму при наявності кількох металів Електроди ІІ роду складаються із металу покритого його важкорозчинною сполукою (сіллю, оксидом, гідроксидом) і зануреного в розчин добре розчинної сполуки з тим же аніоном. Ме/Ме. An, Ann. Ці електроди оборотні як відносно катіона так і відносно аніона,

Найбільш широке застосування мають хлорсрібний і каломельний електроди. Хлорсрібний складається із срібної дротини покритою шаром Аg. CI і зануреної в розчин КСІ. Аg/Аg. CI, КСІ електрод має власний потенціал +0, 202 В використовується як електрод порівняння для проведення серійних вимірювань потенціалу. Для дуже точних визначень користуються каломельним електродом

Практичне значення потенціометрії у можливості визначати активність потенціалвизначаючих йонів розчинах йонселективними мембранними электродами Мембрана може змінювати потенціал через різницю концентрацій у внутрішній і зовнішній її частині скляні електроди мають виготовленну із спеціального скла скляну кульку В середині електрода НСІ допоміжний электрод – хлорсрібний. На межі контакту виникає потенціал за рахунок різниці концентрацій. H+|скляна мембрана|HCl|Ag. Cl, Ag
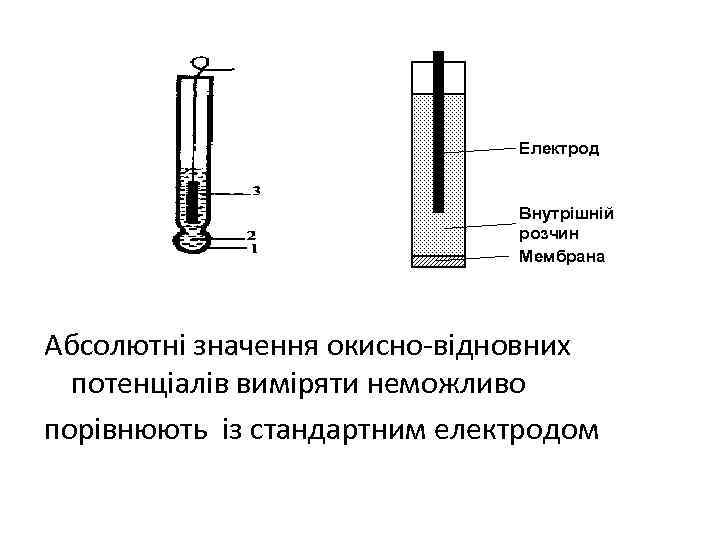
Електрод Внутрішній розчин Мембрана Абсолютні значення окисно-відновних потенціалів виміряти неможливо порівнюють із стандартним електродом

Окисно-відновні процеси Супроводжуються зміною ступеня окислення Відновниками – речовини, які в процесі реакції віддають електрони. Окисники – приймають електрони. відіграють важливу роль в процесах обміну в організмі людини, забезпечують енергією.

В організмі людини розрізняють 3 типи окисно-відновних реакцій: 1) з участю атомів Оксигену, утворенням нових зв’язків з атомами карбону: 2) ферментативне дегідрування:

3) переносення електронів відновника до окисника без участі кисню і водню атом Fe у гемі цитохромів може приєднювати та віддавати один електрон: цит(Fe+3) + e цит(Fe+2) проходить ступінчато через ряд проміжних окисно-відновних стадій, кожна з яких характеризується своїм окисно-відновним потенціалом. Вимірювання біопотенціалів покладено в основу таких методів як електрокардіографія, електроенцефалографія і ін.

На величину електродного потенціалу впливають багато факторів: -температура; -концентрація; -активність металу; -активність йонів металу; -середовище розчину.

Кількісна залежність між величиною потенціалу, співвідношенням окисленої і відновленої форми і температурою дається рівнянням Нернста-Петерса: [окисл. ] – концентрація (активність) окисленої форми в моль/л; [відновл. ] – концентрація (активність) відновленої форми в моль/л; якщо [окисл. ] = [відновл. ], то = 0 і Е = Е 0

Значення приведені в довідниках. Служать кількісною мірою окислювальної і відновної здатності різних окисновідновних систем. . Знаючи значення потенціалу системи можна розрахувати зміну енергії Гіббса за формулою: ∆G=-n. FE де ∆G – вільна енергія Гіббса E – електрорушійна сила елемента ∆G<0 – пряма реакція ∆G>0 – зворотня реакція

Біологічне окислення є джерелом енергії в організмі, багатоступінчате відбувається шляхом перенесення електронів або протонів. Стандартизація окислювально-відновних біохімічних потенціалів в біохімії відрізняється від електрохімічних. Їх проводять при активності а = 1 моль/л , T = 298 К , та р. Н = 7. Стандартні окисно-відновні потенціали позначають Е 0І= Е 0 – 0, 059∙р. Н = Е 0 – 0, 42 В. для системи Н 2/2 Н 3 О+ + 2 е Е = -0, 42 В Від’ємне значення редокс-потенціалу свідчить про здатність даної пари бути відновником.

чим позитивніший редокс-потенціал, тим сильніше проявляється здатність окисника. Ео НАДН/НАД+= – 0, 32 В, може віддавати електрони, Ео 0, 5 О 2/Н 2 О=+0, 81 В. , приймає електрони. Величина окисно-відновного біохімічного потенціалу дає змогу передбачити напрямок потоку електронів та розрахувати зміну енергії при переносі електронів від однієї редокс-пари до другої.

Дифузійний потенціал -додатковий потенціал на межі розчин- причина його виникнення полягає у різній швидкості руху катіона і аніона. Мембранний потенциал – виникає на напівпроникній перегородці, яка вибірково пропускає катіони і затримує аніони, що приводить до нагромадження по обидві сторони мембрани зарядів протилежного знаку виникають у клітинах рослинних і тваринних організмів - приводить до утворення різних біопотенціалів та біострумів. Відмінність у йонному складі всередині і зовні клітини приводить до появи і ще одного потенціалу - потенціалу спокою.

З рівняння Нернста Е = – 75 м. В Якщо нервову тканину збуджувати електрично, хімічно чи механічно, клітинна мембранна стає більш прониклою для йонів Na+, що приводить до зміни мембранного потенціалу Е = 50 м. В. Раптове підвищення чи зниження мембранного потенціалу називають потенціалом дії. Потенціали дії створюють біопотенціали та біоструми, тому два електроди, прикладені до різних ділянок тіла, реєструють різницю потенціалів. Це покладено в основу електрокардіографічних і інших методів діагностики.
Lek_3_stomat_kompl_i_elektrod_prots.ppt