e253c387879d3e3e93a131c0dfb39a87.ppt
- Количество слайдов: 84

Problemegenerale analizei medicamentelor FR X - capitolul “Monografii- Metode generale de analiză”: n Prelevareaprobelor pentru analiz. ă n Controlul organoleptic n Determin ri fizice şi fizico-chimice ă n Determin ri cantitative ă n Determin ri farmacognostice ă n Determin ri farmacotehnice ă n Determin ri biologiceşi biochimice ă n Controlul preparatelorradiofarmaceutice n Analiza medicamentului defineste in sens larg examinarea partilor constituiente ale unui intreg reprezentat de medicament, presupunand specific determinarea calitativa si/sau cantitativa compozitiei a si/sau structuriisubstantelor sau amestecurilorutilizand strategii metode si instrumente , caracteristice. 1
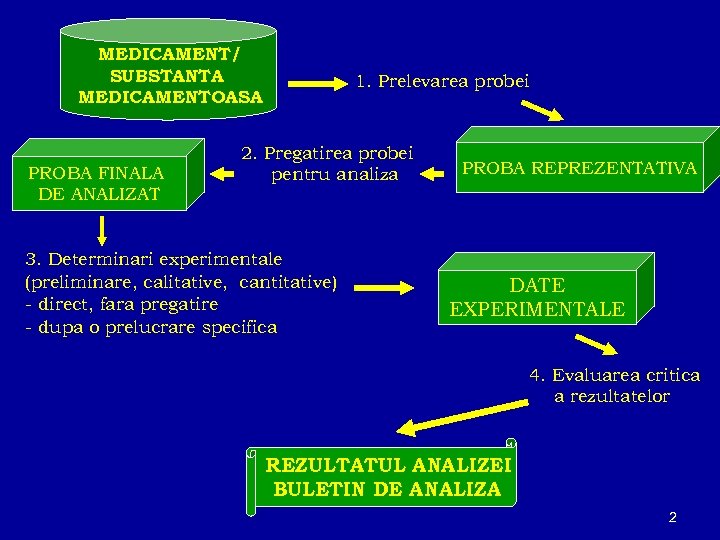
MEDICAMENT/ SUBSTANTA MEDICAMENTOASA PROBA FINALA DE ANALIZAT 1. Prelevarea probei 2. Pregatirea probei pentru analiza 3. Determinari experimentale (preliminare, calitative, cantitative) - direct, fara pregatire - dupa o prelucrare specifica PROBA REPREZENTATIVA DATE EXPERIMENTALE 4. Evaluarea critica a rezultatelor REZULTATUL ANALIZEI BULETIN DE ANALIZA 2

PRELEVAREA PROBELOR PENTRU ANALIZ A « Probele prelevate pentru determinarilecalitativ şi cantitative e trebuie să reprezinte sub toate aspectele caracteristicile , , produsului din lotulsau seria respectiva (FR-X) » FR-X: • lot - o cantitatede materie primă, presupusă a fi unitară, din care se obţin una sau mai multe serii de produse serie - totalitatea unităţilor de produs obţinute în condi ţii identice într-un singur ciclu de operaţii , • • • recipient- conţine unităţile de produs care constituieo serie, ex. flacoane fiole, folii tuburi, cutii pungi etc. , , , ambalaj- conţinerecipientele grupate adecvat 3
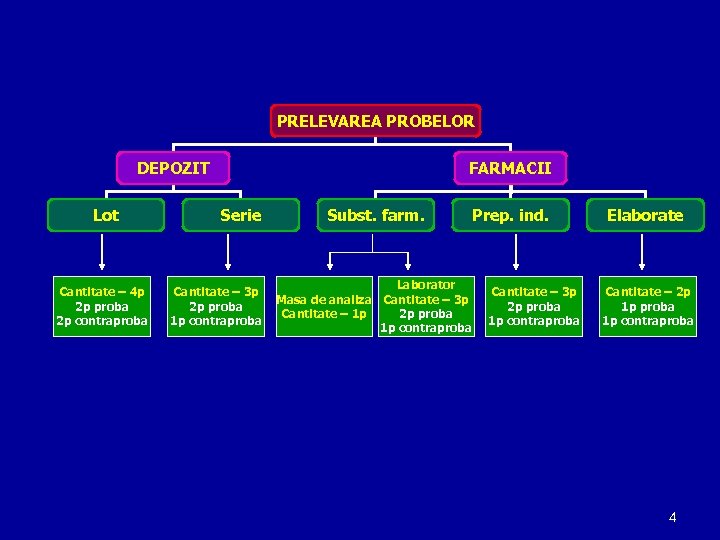
PRELEVAREA PROBELOR DEPOZIT Lot Cantitate – 4 p 2 p proba 2 p contraproba FARMACII Serie Cantitate – 3 p 2 p proba 1 p contraproba Subst. farm. Laborator Masa de analiza Cantitate – 3 p Cantitate – 1 p 2 p proba 1 p contraproba Prep. ind. Cantitate – 3 p 2 p proba 1 p contraproba Elaborate Cantitate – 2 p 1 p proba 1 p contraproba 4
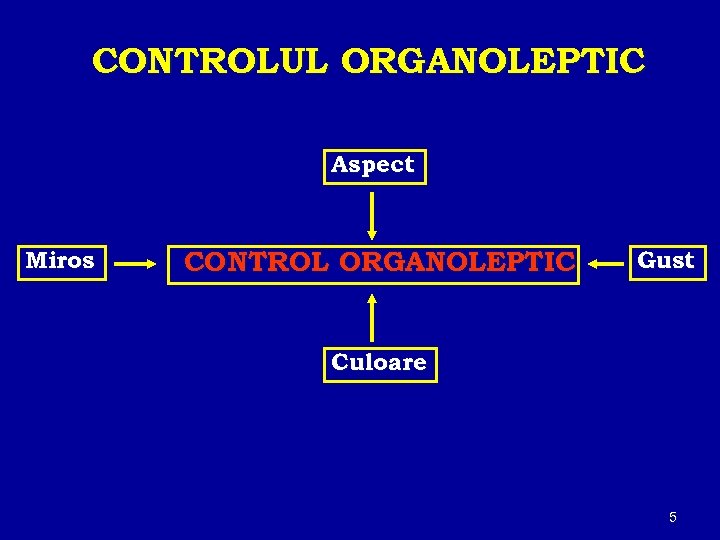
CONTROLUL ORGANOLEPTIC Aspect Miros CONTROL ORGANOLEPTIC Gust Culoare 5

DETERMINARI FIZICE, FIZICO-CHIMICE ŞI CHIMICE DETERMINAREASOLUBILITĂŢII n n prevederile de la alineatul "Solubilitate" au un caracter orientativ privind solubilitatea substanţelor în diferiţi solvenţi prevederile înscrise în cadrul altor alineate, cum ar fi "solubilitatea în alcool", au un caracter obligatoriu, fiind considerate teste de puritate n Solubilitatea poate fi exprimată prin specificarea volumului de solvent (în mililitri) necesar pentru a dizolva 1 g substanţă solidă sau 1 ml substanţă lichidă, la temperatura de 20 20 C. n Verificarea solubilităţii substanţelor farmaceutice nu este necesar să se efectueze în toţi solvenţii prevăzuţi în monografie, ci este necesar să se controlezesolubilitatea în cel puţin doi solvenţi diferiţi. n Dacă se constată prezenţa unor impurităţi insolubile, se verifică solubilitatea şi în ceilalţi solvenţi prevăzuţi. 6

n Diferitele solubilităţi pot fi exprimate şi cu ajutorul unor expresii - în acest caz prevederile de solubilitate se referă la temperatura de 20 5 o. C. Expresii folosite foarte uşor solubil puţin solubil foarte puţin solubil greu solubil foarte greu solubil practic insolubil Volumul de solvent(ml) necesar pentru a dizolva 1 g substanţă solidă sau 1 ml substanţă lichid ă cel mult 1 ml de la 1 ml pân la 10 ml ă de la 10 ml pân la 30 ml ă de la 30 ml pân la 100 ml ă de la 100 ml pân la 500 ml ă de la 500 ml pân la 1000 ml ă de la 1000 ml pân la 10. 000 ml ă mai mult de 10. 000 ml 7

DETERMINAREA INDICILOR n Indice de aciditate = numărul de miligrame de hidroxid de potasiu necesar pentru neutralizarea acizilor graşi liberi conţinuţi în 1 g probă de analizat (uleiuri volatile, uleiuri grase, balsamuri, ceruri etc. ). n Se calculează conformulei: în care: - IA = indice de aciditate - V = volumul de KOH 0. 1 mol/l în apă folosit la titrare (ml) - m = masa probei luate în lucru (grame) - 5. 61 = numărul de miligrame de KOH corespunzător la 1 ml KOH 0. 1 mol/l. 8

n Indice de saponificare = numărul de miligrame de hidroxid de potasiu necesar pentru neutralizarea acizilor liberi şi a acizilor rezultaţi din saponificarea a 1 g probă de analizat. n Se calculează conformulei: în care: - IS = indice de saponificare - V 1 = volumul de HCl 0. 5 mol/l folosit la titrarea martorului (ml) - V 2 = volumul de HCl 0. 5 mol/l folosit la titrarea probei (ml) - m = masa probei luate în lucru (grame) - 28. 05 = numărul de miligrame de KOH corespunzător la 1 ml KOH 0. 5 mol/l în alcool. 9

n Indice de ester = numărul de miligrame de hidroxid de potasiu necesar pentru neutralizarea acizilor graşi rezultaţi din saponificarea a 1 g probă de analizat. n Se calculează conformulei: în care: - IE = indice de ester - IS = indice de saponificare - IA = indice de aciditate. 10

n Indice de hidroxil = numărul de miligrame de hidroxid de potasiu echivalent cu acidul acetic consumat prin acetilarea a 1 g probă de analizat. n Se calculează conformulei: în care: - IH = indice de hidroxil - V 1 = volumul de KOH 0. 5 mol/l în alcool folosit la titrarea martorului (ml) - V 2 = volumul de KOH 0. 5 mol/l în alcool folosit la titrarea probei (ml) - m = masa probei luate în lucru (grame) - IA = indice de aciditate -28. 05 = numărul de miligrame de KOH corespunzător la 1 ml KOH 0. 5 mol/l în alcool. 11

n Indice de iod = numărul de grame de iod fixat de 100 g probă de analizat. n Se calculează conformulei: în care: - II = indice de iod - V 1 = volumul de Na 2 S 2 O 3 0. 1 mol/l folosit la titrarea martorului (ml) - V 2 = volumul de Na 2 S 2 O 3 0. 1 mol/l folosit la titrarea probei (ml) - m = masa probei luate în lucru (grame) - 0. 01269 = numărul de grame de iod corespunzător la 1 ml Na 2 S 2 O 3 0. 1 mol/l. 12

n Indice de peroxid = numărul de mililitri de tiosulfat de sodiu 0. 01 mol/l oxidat de iodul eliberat din acidul iodhidric prin acţiunea peroxizilor din 1 g probă de analizat. n Se calculează conformulei: în care: - IP = indice de peroxid - V 1 = volumul de Na 2 S 2 O 3 0. 01 mol/l folosit la titrarea martorului (ml) - V 2 = volumul de Na 2 S 2 O 3 0. 01 mol/l folosit la titrarea probei (ml) - m = masa probei luate în lucru (grame). 13
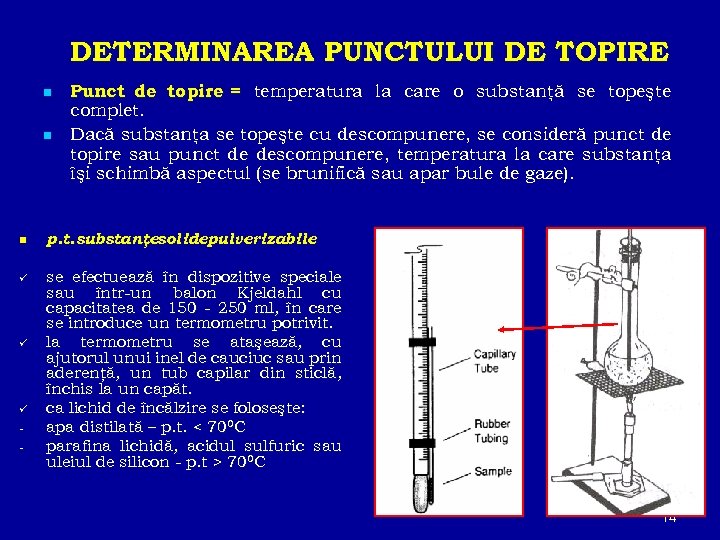
DETERMINAREA PUNCTULUI DE TOPIRE n n Punct de topire = temperatura la care o substanţă se topeşte complet. Dacă substanţa se topeşte cu descompunere, se consideră punct de topire sau punct de descompunere, temperatura la care substanţa îşi schimbă aspectul (se brunifică sau apar bule de gaze). n p. t. substanţesolidepulverizabile ü se efectuează în dispozitive speciale sau într-un balon Kjeldahl cu capacitatea de 150 - 250 ml, în care se introduce un termometru potrivit. la termometru se ataşează, cu ajutorul unui inel de cauciuc sau prin aderenţă, un tub capilar din sticlă, închis la un capăt. ca lichid de încălzire se foloseşte: apa distilată – p. t. < 700 C parafina lichidă, acidul sulfuric sau uleiul de silicon - p. t > 700 C ü ü - 14
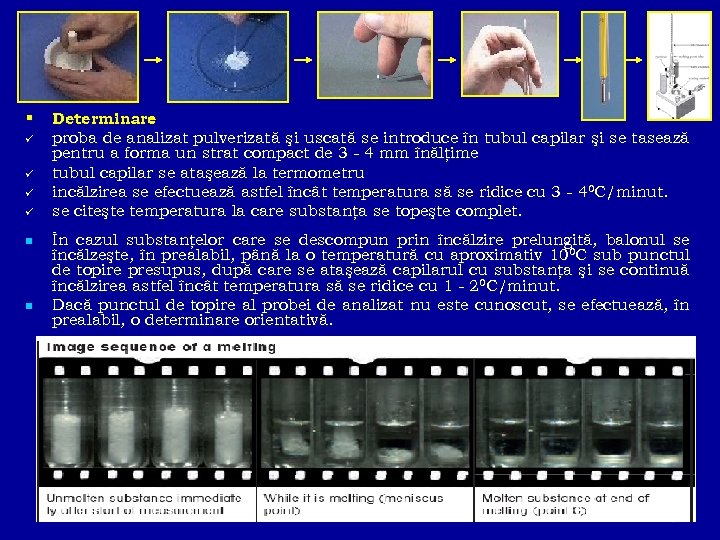
Determinare : ü ü n n proba de analizat pulverizată şi uscată se introduce în tubul capilar şi se tasează pentru a forma un strat compact de 3 - 4 mm înălţime tubul capilar se ataşează la termometru incălzirea se efectuează astfel încât temperatura să se ridice cu 3 - 40 C/minut. se citeşte temperatura la care substanţa se topeşte complet. În cazul substanţelor care se descompun prin încălzire prelungită, balonul se încălzeşte, în prealabil, până la o temperatură cu aproximativ 100 C sub punctul de topire presupus, după care se ataşează capilarul cu substanţa şi se continuă încălzirea astfel încât temperatura să se ridice cu 1 - 20 C/minut. Dacă punctul de topire al probei de analizat nu este cunoscut, se efectuează, în prealabil, o determinare orientativă. 15
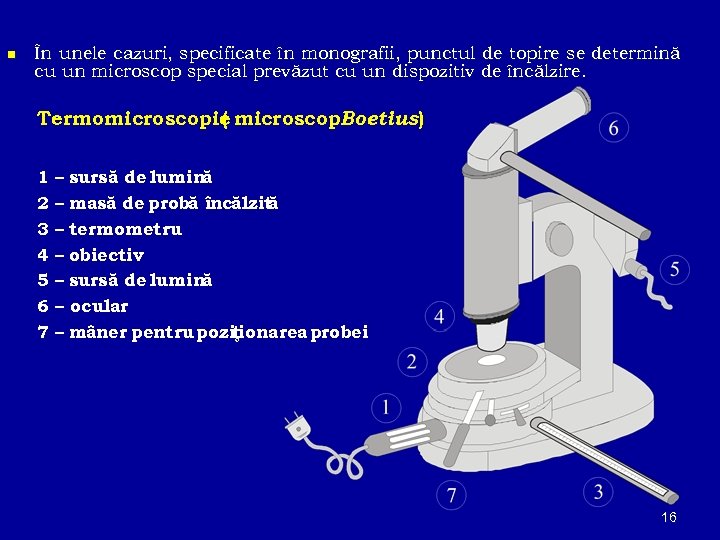
n În unele cazuri, specificate în monografii, punctul de topire se determină cu un microscop special prevăzut cu un dispozitiv de încălzire. Termomicroscopie microscop. Boetius) ( 1 2 3 4 5 6 7 – sursă de lumină – masă de probă încălzit ă – termometru – obiectiv – sursă de lumină – ocular – mâner pentru pozi ţionarea probei 16

DETERMINAREA CONCENTRAŢIEI ÎN ALCOOL n n n ü ü ü n se bazează pe distilarea alcoolului se determina densitatea sau indicele de refracţie a distilatului hidroalcoolic. Determinare : se foloseşte un aparat de distilare cu alonjă care trebuie să pătrundă în apă se distilă nu mai mult de 30 minute se determină densitatea relativă cu ajutorul picnometrului şi se citeste concentraţia în alcool a distilatului (% m/V) din tabele alcoolmetrice. se calculează dupa formula: în care: - c = concentraţia în alcool a distilatului corespunzătoare densităţii relative (% m/V) - m = masa probei luate în lucru (g). 17
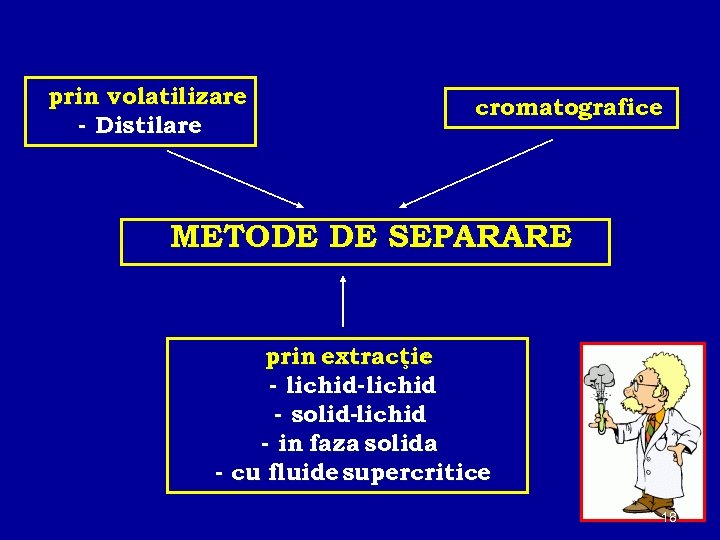
prin volatilizare - Distilare cromatografice METODE DE SEPARARE prin extracţie : - lichid-lichid - solid-lichid - in faza solida - cu fluide supercritice 18

METODE DE SEPARARE PRIN VOLATILIZARE DISTILAREA Distilarea este una din cele mai vechi metode de separare si purificare a lichidelor. Separarea se bazează pe diferenţele dintre presiunile de vapori ale lichidelor care compun un amestec. Pe scurt, distilarea presupune încălzirea lichidelor, separând vaporii si recondensându-i pentru a obţine un nou lichid care va fi concentrat în compuşi mai volatili. PARAMETRII DE LUCRU ŞI EFICIENŢĂ: ü echilibrulde distributievapori-lichid ü volatilitatea relativa ü talerul teoretic 19
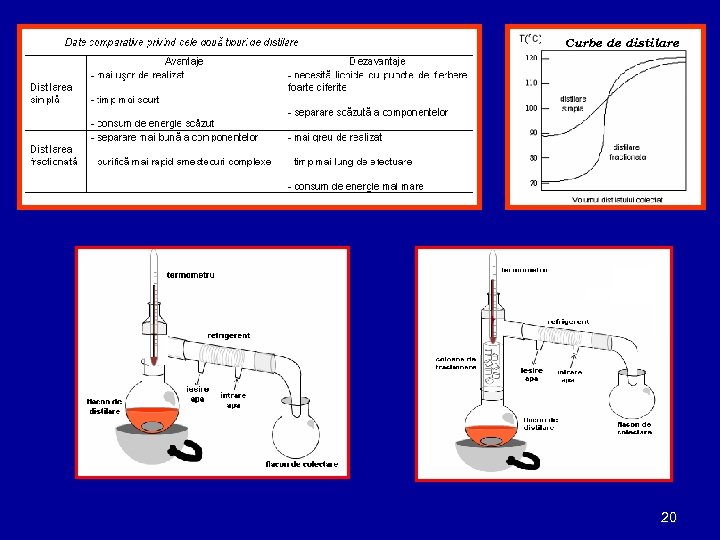
Curbe de distilare 20

METODE DE SEPARARE PRIN EXTRACTIE EXTRACŢIA LICHID – LICHID q Extracţie= transferul unei substanţe dizolvate dintr-un solvent în alt solvent nemiscibil cu primul. q Distribuţia substanţei respective între cele două faze depinde de solubilitatea acesteia în cei doi solvenţi. Componenţii supuşi distribuţiei interfazice manifestă preferinţe pentru unul sau altul dintre solvenţi, participând selectiv la procesul de transfer. q q Dacă la echilibru concentraţiile componenţilor sunt sensibil diferite între cei doi solvenţi, procesul poate fi utilizat în scopul separării lor. 21
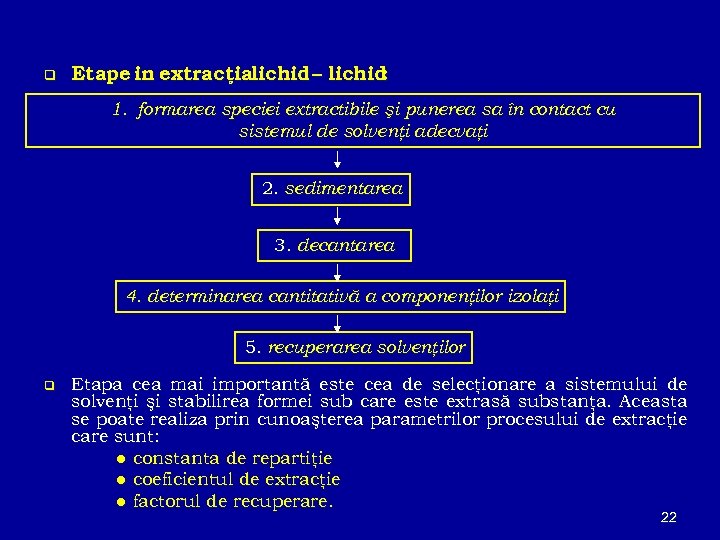
q Etape in extracţialichid – lichid : 1. formarea speciei extractibile şi punerea sa în contact cu sistemul de solvenţi adecvaţi 2. sedimentarea 3. decantarea 4. determinarea cantitativă a componenţilor izolaţi 5. recuperarea solvenţilor q Etapa cea mai importantă este cea de selecţionare a sistemului de solvenţi şi stabilirea formei sub care este extrasă substanţa. Aceasta se poate realiza prin cunoaşterea parametrilor procesului de extracţie care sunt: ● constanta de repartiţie ● coeficientul de extracţie ● factorul de recuperare. 22

PROCEDEE DE EXTRACŢIE LICHID-LICHID q După sensul de curgere al lichidului şi după principiul de funcţionare al instalaţiei: 1. Extracţiasimplă 2. Extracţiacontinuă 3. Distribuţiaîn contracurent. 23

EXTRACŢIA SOLID-LICHID Principii generale q se aplică atunci cand este o fază solidă sau semi-solidă (material vegetal, pulberi de forme farmaceutice solide etc. ) q implică operaţiile de extracţie de tip percolare, filtrare şi spălare. q o o q Are 2 etape realizate în acelaşi aparat sau în aparate separate: , contactul solventului cu materialul solid supus extracţiei constituientului solubil (solut) în solvent separarea sau spălarea soluţiei de reziduul solid şi transferul Procesul complet include recuperarea solutului separat şi a solventului, prin evaporare sau distilare. APARATURA q q o o depinde de prima etapă termeni ce indicǎ tipul de aparat utilizat: “solidbed” sau “fixedbed” - se referă la orice operaţie în care prin materialul solid fix trece solventul utilizat pentru extracţie “dispersedcontact” se referă la operaţiile în care particulele solide, suspendate în fluid sunt în mişcare relativă unele faţă de altele şi faţă de solvent, în timpul contactului solid-solvent. 24

EXTRACTIA IN FAZA SOLIDA (SOLID-PHASE-EXTRACTION, SPE) este un proces de separare prin care compuşi dizolvaţi sau suspendaţi într-un amestec lichid sunt separaţi de alti compusi din amestec în funcţie de proprietăţile lor fizice şi chimice q poate fi folosită pentru a izola analiţii de interes dintr-o mare varietate de matrici, inclusiv urină, sânge, apă, băuturi, sol, şi ţesuturi de origine animală q utilizează afinitatea substanţelor dizolvate sau suspendate într-un lichid (faza mobilă), pentru un solid prin care proba este trecută (faza staţionară) pentru a separa dintr-un amestec componentele dorite şi nedorite q rezultatul ü analiţii de interes doriţi sau impurităţile nedorite din proba sunt reţinute pe faza staţionară ü partea care trece prin faza staţionară este colectată sau casată (daca conţine analiţii doriţi sau impurităţile nedorite) ü in cazul în care porţiunea reţinută în faza staţionară include analiţii doriţi, aceştia pot fi apoi separaţi din faza staţionară prin colectare printr-un proces suplimentar, în care faza staţionară se spală cu un eluent corespunzător. q 25

CROMATOGRAFIA DE LICHIDE DE INALTĂ PERFORMANŢĂ HIGH PERFORMANCE/PRESSURE LIQUID CHROMATOGRAPHY (HPLC) q ü ü Cromatografia de lichide de înaltă performanţă/înaltă presiune (High Performance/Pressure Liquid Chromatography - HPLC) sau de înaltă viteză (High Speed Liquid Chromatography – HSLC) este o tehnică: modernă şi rapidă care elimină unele dezavantaje ale cromatografiei planare utilizată pentru separarea şi determinarea soluţilor organici şi anorganici din orice probe, în special substanţe şi produse farmaceutice, biologice, alimentare, industriale, de mediu etc. Clasificare În funcţie de mecanismele care stau la baza separării componentelor, cromatografia de lichide se clasificǎ astfel: q cromatografie prin adsorbţie q cromatografie prin repartiţie q cromatografie cu faze inverse q cromatografie prin schimb ionic q cromatografie prin excluziune moleculară. 26
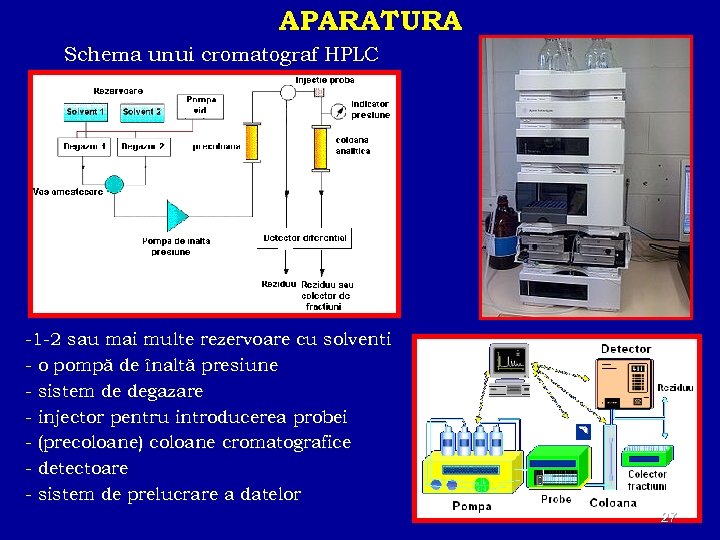
APARATURA Schema unui cromatograf HPLC -1 -2 sau mai multe rezervoare cu solventi - o pompă de înaltă presiune - sistem de degazare - injector pentru introducerea probei - (precoloane) coloane cromatografice - detectoare - sistem de prelucrare a datelor 27

APLICAŢIILE HPLC ANALIZA CALITATIVA v Separarea si identificarea substanţelormedicamentoase Identificarea unui componentprezentintr-un amestecse poate face dupa cromatografiere prin: ü Metodecromatografice : - Dupa marimilede retentie - Metoda adaosului standard - Metoda retentieirelative ü Metodespectrale Alcaloizi din ergot elimoclavina lisergol 28
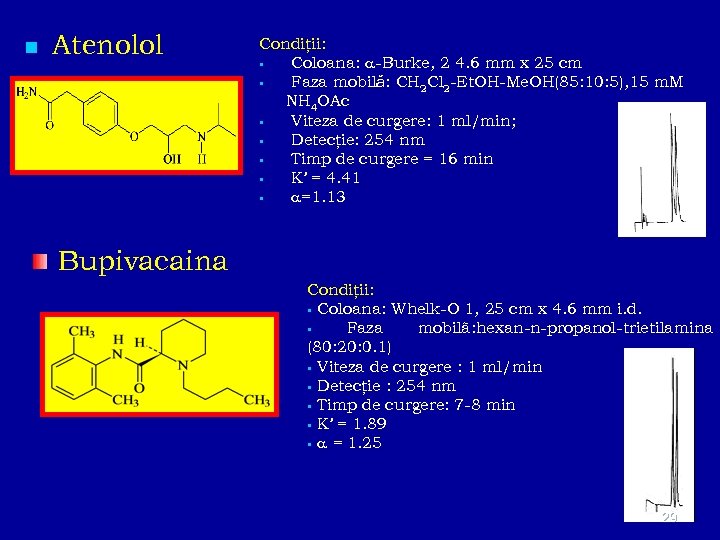
n Atenolol Condiţii: Coloana: -Burke, 2 4. 6 mm x 25 cm Faza mobilǎ: CH 2 Cl 2 -Et. OH-Me. OH(85: 10: 5), 15 m. M NH 4 OAc Viteza de curgere: 1 ml/min; Detecţie: 254 nm Timp de curgere = 16 min K’ = 4. 41 =1. 13 Bupivacaina Condiţii: Coloana: Whelk-O 1, 25 cm x 4. 6 mm i. d. Faza mobilã: hexan-n-propanol-trietilamina (80: 20: 0. 1) Viteza de curgere : 1 ml/min Detecţie : 254 nm Timp de curgere: 7 -8 min K’ = 1. 89 = 1. 25 29
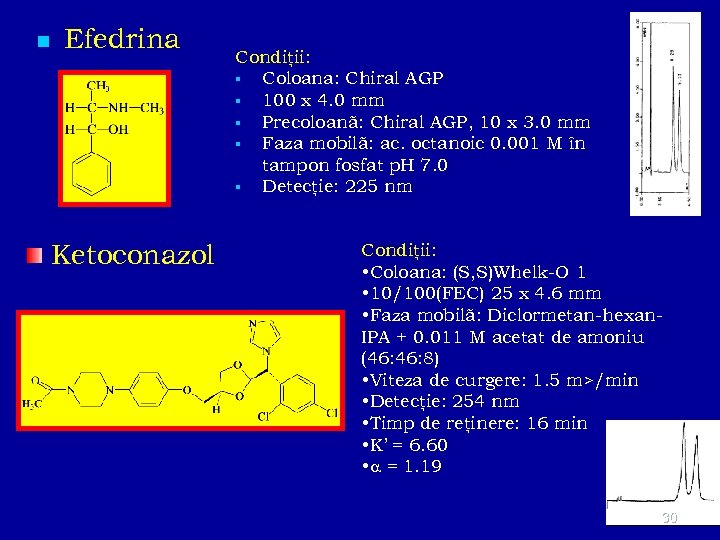
n Efedrina Ketoconazol Condiţii: Coloana: Chiral AGP 100 x 4. 0 mm Precoloanã: Chiral AGP, 10 x 3. 0 mm Faza mobilã: ac. octanoic 0. 001 M în tampon fosfat p. H 7. 0 Detecţie: 225 nm Condiţii: • Coloana: (S, S)Whelk-O 1 • 10/100(FEC) 25 x 4. 6 mm • Faza mobilã: Diclormetan-hexan. IPA + 0. 011 M acetat de amoniu (46: 8) • Viteza de curgere: 1. 5 m>/min • Detecţie: 254 nm • Timp de reţinere: 16 min • K’ = 6. 60 • = 1. 19 30

v n n ü ü Analiza produşilor modificaţi chimic (prin derivatizare) este adesea necesară pentru a atinge o cromatografie satisfăcătoare. se aplică pentru componentele de toate polarităţile şi greutăţile moleculare şi este un avantaj al HPLC faţă de gaz-cromatografie. Este utilizată pentru a creşte sensibilitatea detecţiei cand detectările utilizate nu sunt satisfăcătoare pentru componentele nederivate. Absorbţia în UV şi fluorescenţa pot fi obţinute cu ajutorul unor reactivi. UV: N-succinimid-p-nitrofenilacetat (SNPA), fenilhidrazină şi 3, 5 dinitrobenzen (DNBC). derivaţii fluorescenţi pot fi formaţi cu agenţi de tipul: cloruri de dansil (DNS-Cl), 4 -bromometil-7 -metoxicumarina (BMC) şi cu unele amine fluorescente. 31

v Detectarea imunologică Tehnica implică colectarea de solvent în fracţiuni mici (1 ml) şi prelevări de medicament în fracţiuni. q Necesitã mult timp, dar au reversibilitate şi selectivitate mai mare decat detectările convenţionale. q q În multe cazuri, lichidele biologice pot fi injectate direct în coloană. HPLC cu detectare imunologică este utilizată pentru analiza metaboliţilor care sunt dificil de izolat din lichidele biologice prin extracţie (glucuronidele). Astfel de compuşi polari nu pot fi observaţi în concentraţii mici prin detectări convenţionale, ele fiind mascate de componentele endogene. q Poate fi utilizată pentru determinarea: canabinoidelor, opioidelor, lisergidelor, glicozidelor cardiotonice din lichidele biologice. q 32

ANALIZA CANTITATIVA n Se bazeaza pe corelatia care exista intre aria (inaltimea) picului si concentratia componentului respectiv. n Metodele de determinare constau in masurarea: Aria picului: - metode manuale - metode electronice Concentratiaprobei: - metoda normariilor - calibrare cu standard extern - metoda standardului intern - metoda adausului standard v v 33

v Determinareacantitativãa substanţelorfarmaceutice Determinarea cantitativã a vitaminei B-12 din ser Condiţii: • HPLC/ICP-MS • ICP = Inductively coupled plasma emission spectrometer • HPLC/ICP-MS cu sistem de lucru LC-10 A, ELAN 6100, Waitress’s LC • Coloana: COSMOSIL, 5 C 18 -AR • Faza mobilã: apã-ac. acetic-isopropanol (90: 1: 9) • Viteza de curgere: 10 ml/min n Determinarea amitriptilinei şi perfenazinei Condiţii: • HPLC/Agilent 1000 • Coloana: cianopropil • Faza mobilã: acetonitril-metanol-fosfat monopotasic • Viteza de curgere 2. 0 m. L/min • Detecţie: UV 215 nm n 34

n Determinarea omapatrilatului din plasmã (inhibitor de endopeptidazã) Condiţii • HPLC: Waters 510 HPLC pump, Waters automated gradient • Coloana analiticã BDS Hypercil C 8 (3 m, 50 mm× 2 mm ID) precedatã de Hypercil C 8. • Faza mobilã: 62. 5 % apã şi 37. 5 % acetonitril, cu acetat de amoniu 1 mmol/L la p. H 5. 5. • Viteza de curgere: 0. 2 m. L/min, • Volumul injectat 25 L. v • • • Alte determin cantitative ǎri Determinarea activit antioxidante a capsaicinei; ăţii Determinarea cantitativ ă a aminoacizilor din lichidul cefalorahidian; Determinarea cantitativa cumarinei din extracte alcoolice. ǎ 35

GAZ – CROMATOGRAFIA GAS-CHROMATOGRAPHY (GC) Definitie Atunci când se foloseşte un gaz ca fază mobilă într-un sistem cromatografic, tehnica este denumită gaz-cromatografie (GC, cromatografie de gaze, cromatografie in faza gazoasa). Această tehnică se efectuează întotdeauna într-o coloană cromatografică deoarece faza mobilă trebuie să curgă în mod continuu. v v Clasificare cromatografia gaz-lichid (GLC): - faza staţionară este un lichid - fenomenul de separare loc prin repartiţie cromatografică cromatografia gaz-solid (GSC) - faza staţionară este o suprafaţă solidă - fenomenul de separare loc prin adsorbţie. 36
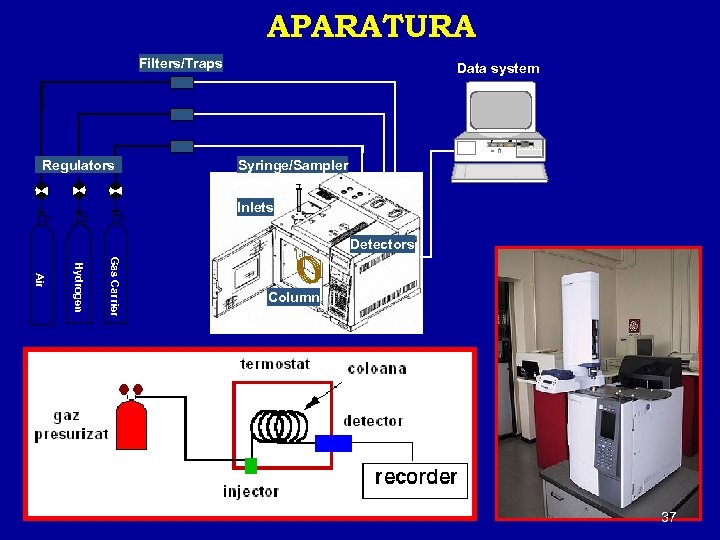
APARATURA Filters/Traps Data system H RESET Regulators Syringe/Sampler Inlets Detectors Gas Carrier Hydrogen Air Column 37

APLICAŢIILE GAZ-CROMATOGRAFIEI 1. Identificarea compuşilor medicamentoşi si cercetarea impuritatil se folosesc mărimile de reţinere VR şi t. R ü identitatea timpului de reţinere al unui component cu acela al aceluiaşi component pur oferă un indiciu că cei doi componenţi sunt identici ü timpii de reţinere sunt proporţionali cu punctele de fierbere ale componenţilor care ies din coloană în ordinea acestora ü folosind diferite faze staţionare selective componenţii se pot separa chiar dacă au aceleaşi puncte de fierbere ü timpul de retenţie depinde de diferiţi factori (lungimea coloanei, diametru, temperatura). Din această cauză, în scopuri calitative se utilizează aşanumiţii timpi de retenţie relativi, trr, definiţi prin relaţia: ü unde: t. A = timpul de retenţie al componentei A; tet = timpul de retenţie al etalonului. 38

Se practică adăugarea în amestecul de analizat a unei componente pure. Dacă are loc creşterea pe cromatogramă a maximului ce corespunde componentului adăugat, aceasta se consideră drept dovadă a identităţii componentei - etalon. ü Operaţia se efectuează pentru aceeaşi probă de analizat pe mai multe coloane cu diferiţi adsorbanţi. ü 2. Studii de stabilitate pentru materii prime si produse finite cu posibilitatea identificarii produsilor de degradare. 3. Studii farmacocinetice studii de biodisponibilitate (determinarea – concentratiei plasmatice). 39

4. Determinarea cantitativă a compuşilor medicamentoşi Principala problemă a analizei cantitative în gaz-cromatografie este măsurarea ariei picurilor. ü Aria picurilor este proporţională cu cantitatea de substanţă ce se găseşte în zona eluată. ü Aria maximului picului poate fi calculată prin mai multe metode: - măsurarea înălţimii maximului simetric, considerându-l de forma unui triunghi, când aria este proporţională cu înălţimea: metodă destul de precisă, dar exactitatea ei depinde de măsura în care forma maximului rămâne neschimbată dacă cantitatea de substanţă variază. ü - planimetrarea ariei de sub pic - aparatele moderne evalueaza ariile cu ajutorul dispozitivelor de integrare şi a computerelor. Prin metodele enumerate se măsoară aria sau cantitatea de substanţă proporţională cu aria de sub pic. Aceste cantităţi trebuie transformate în valori sau procente ale componenţilor analizaţi. n - Gaz-cromatografele moderne efectuează automat determinările cantitative prin ataşarea la aparat a unui calculator adecvat. 40

Definitie : CROMATOGRAFIA PRIN SCHIMB IONIC ION EXCHANGE CHROMATOGRAPHY (IEC) Este o tehnica cromatografica in care faza staţionară este constituita din compuşi în a căror structură se află grupări acide sau bazice ionizabile capabile să reţină cationi sau anioni, in anumite conditii experimentale. q q Aceşti compuşi poartă numele de răşini schimbătoare de ioni. Ionii schimbatorului pot fi inlocuiti de alţi ioni fie din faza mobilă, fie din probă, de unde denumirea de cromatografie prin schimb ionic. q Clasificare: cromatografie de schimb cationic: ü schimbătorul reţine ionii încărcaţi pozitiv, înlocuind ionul H+ al acestuia ü Ex: (-SO H, -PO H ) 3 3 2 v vcromatografie ü ü de schimb anionic: schimbătorul reţine ionii încărcaţi negativ, inlocuind ionul X- al acestuia Ex: (-RN+H 3 X-) 41
1 2 3 4 42

APARATURA 43

APLICAŢIILE CROMATOGRAFIEI IONICE Cromatografia ionica se dezvoltă în zilele noastre cu aplicaţii în: • analiza medicamentelor • chimia anorganică • chimia organică 44
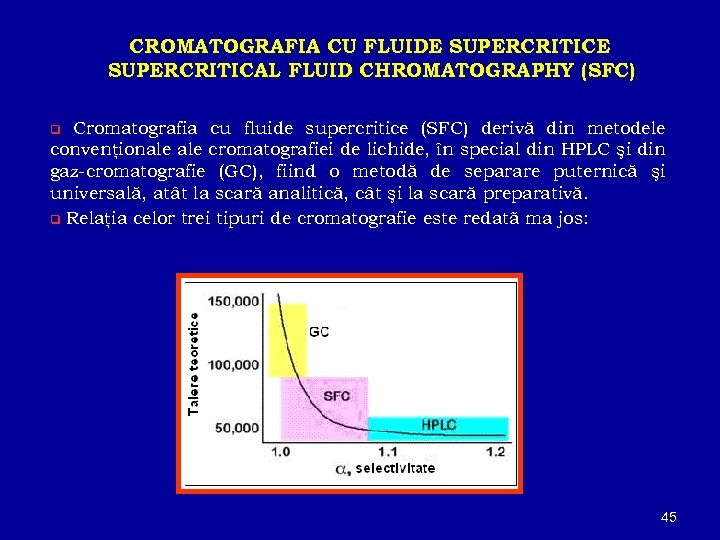
CROMATOGRAFIA CU FLUIDE SUPERCRITICAL FLUID CHROMATOGRAPHY (SFC) Cromatografia cu fluide supercritice (SFC) derivă din metodele convenţionale cromatografiei de lichide, în special din HPLC şi din gaz-cromatografie (GC), fiind o metodă de separare puternică şi universală, atât la scară analitică, cât şi la scară preparativă. q Relaţia celor trei tipuri de cromatografie este redatã ma jos: q 45
46

Caracterisiticile fluidelorsupercritice 3 Densitate(Kg/m ) Vâscozitate(c. P) Difuziune (mm 2/s) 1 0. 01 1 -10 1000 0. 5 -1. 0 0. 001 100 -800 0. 05 -0. 1 0. 01 -0. 1 Gaz Lichid Fluid supercritic Lichid Densitatemare Gaz X Fluid supercritic X Difuzibilitate mare X X Vâscozitatescăzută X X Compresibilitate mare X X 47
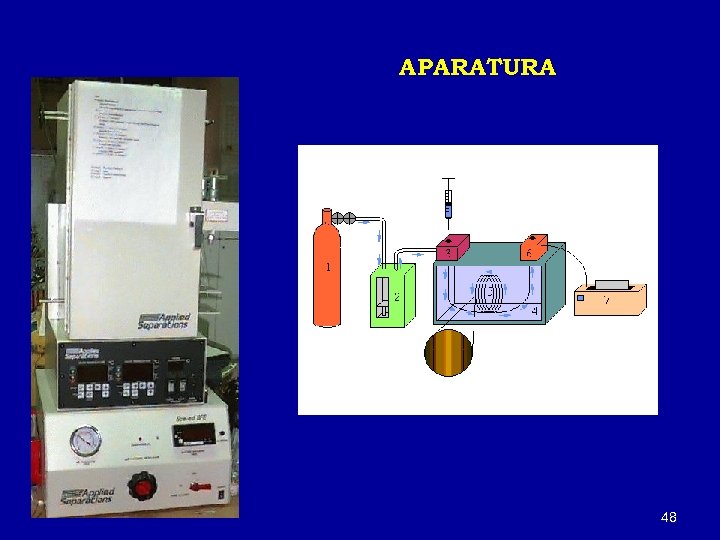
APARATURA 48

APLICAŢIILE CROMATOGRAFIEI CU FLUIDE SUPERCRITICE 1. Determinarea unor sulfonamide Condiţii: o Aparatura: Sistem Gilson SF 3 p. SFC o Coloana: 250 x 4, 6 mm cu fazã staţionarã cianopropil (mãrimea particulelor 5 mm) o Temperatura: 50 o C o Sistem injecţie: Model 7125, 10 ml o Faza mobilã: CO 2 modificat cu metanol (10% primele 5 minute, creştere liniarã la 15% timp de 10 minute) o Viteza de curgere: 2 ml, 21 minute o Presiunea: 180 bari o Detecţie: UV 230 nm TIC 49
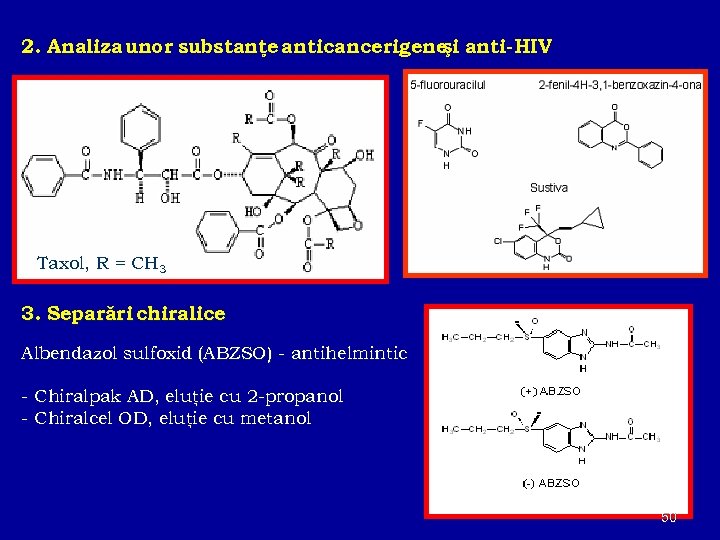
2. Analiza unor substanţe anticancerigene anti-HIV şi Taxol, R = CH 3 3. Separări chiralice Albendazol sulfoxid (ABZSO) - antihelmintic - Chiralpak AD, eluţie cu 2 -propanol - Chiralcel OD, eluţie cu metanol 50

5. Alte aplicatii o o Separări de vitamine liposolubile Separări de acizi graşi Separarea benzodiazepinelor din ser Purificǎri de substanţe farmaceutice Cromatografia cu fluide supercritice a fost conceputa mai ales pentru separarea: o substantelor termolabile o compusilor nevolatili o unor macromolecule 51

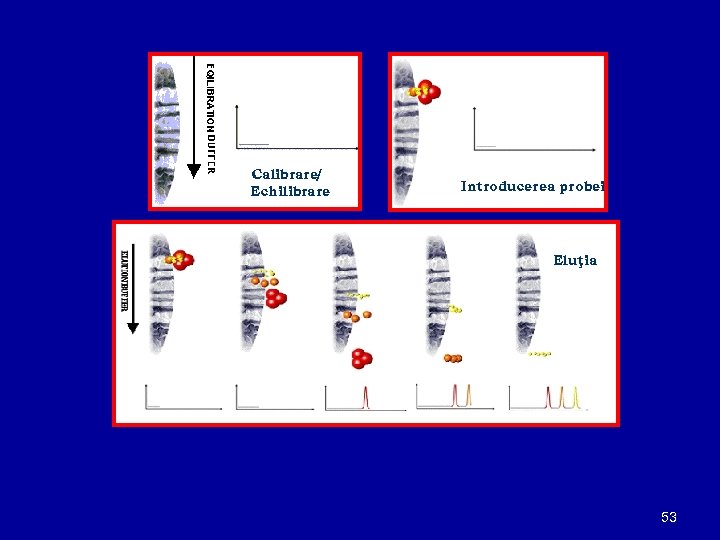
CROMATOGRAFIA DE EXCLUDERE Definiţie Cromatografia de excludere sterică este o metodă prin : care moleculele se separă pe baza mărimii lor sau în termeni tehnici, pe baza volumului hidrodinamic. În mod curent, se aplică moleculelor mari sau complecşilor macromoleculari, cum ar fi proteinele şi polimerii industriali. Clasificare : n cromatografie de filtrare prin gel (Gel Filtration. Chromatography , GFC) - faza mobilă este o soluţie apoasă. n cromatografie de permeaţie prin gel (Gel Permeation Chromatography GPC) - faza mobilă este de natură organică. , n cromatografia de excludere de mărime 52
Calibrare/ Echilibrare Introducerea probei Eluţia 53
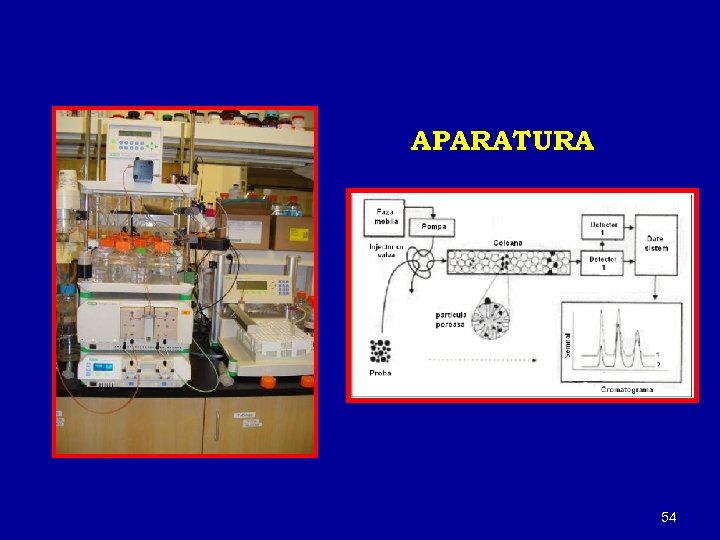
APARATURA 54

APLICAŢIILE CROMATOGRAFIEI DE EXCLUDERE 1. SEPARAREA MOLECULELOR n ü ü Separarea moleculelor cu mărime diferită gelurile care exclud substanţele cu mase moleculare mai mari de 5. 000 u. a. m. realizează o veritabilă desalefiere, deoarece ionii minerali care difuzează liber pot fi eliminaţi în acest mod separarea iodului nefixat în cursul purificării unui trasor, după marcarea unei proteine cu 131 I. Analiza unui amestecde macromolecule purificarea fracţiunilor plasmatice pentru prepararea de medicamente sau reactivi de diagnostic analiza stabilităţii materialelor plastice (ambalaje) Separarea celulelor limfocitele izolate de monocite Fracţionareamoleculelormici analiza peptidelor analiza coloranţilor 55

2. DETERMINAREA MASEI MOLECULARE n etalonarea directă a coloanei cromatografice cu etaloane de masă molară cunoscută n etalonarea indirectă, plecând de la determinarea volumului hidrodinamic ü determinarea masei molare a imunoglobulinelor Ig. G din forme farmceutice, presupunând că 90 % sunt sub formă de monomeri şi 10 % sub formă de dimeri. 3. DETERMINAREA DISTRIBUŢIEI MASELOR MOLECULARE ü se bazeaza pe relatia liniara dintre volumul de elutie si logaritmul masei moleculare. 4. DETERMINAREA PURITĂŢII UNOR SUBSTANŢE FARMACEUTICE Ex: determinarea unor proteine cu mase moleculare mari (ca impuritati) in insulina. 56
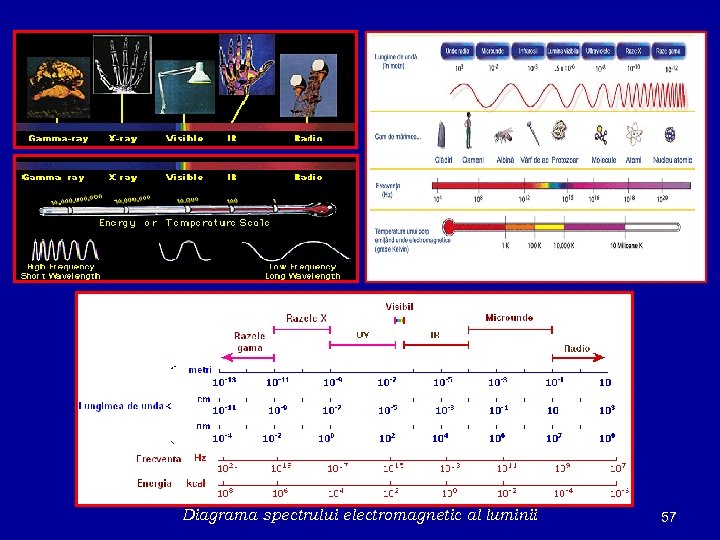
Diagrama spectrului electromagnetic al luminii 57

SPECTROMETRIA UV - VIS q Regiunea spectrală: UV - îndepărtat: 100 - 200 nm UV - apropiat: 200 - 400 nm VIS: 400 - 800 nm. Absorbtia luminii in UV-VIS se datoreaza prezentei cromoforilor. Cromofori (grupe cromofore) sunt grupe de atomi, care prezente într-o substanţă pot da naştere la spectre electronice (de absorbţie). q ü Grupă auxocromă ü este o grupă de atomi saturată care, ataşată unui cromofor , modifică lungimea de undă ( max) la care loc absorbţia şi intensitatea maximă de absorbţie. q 58
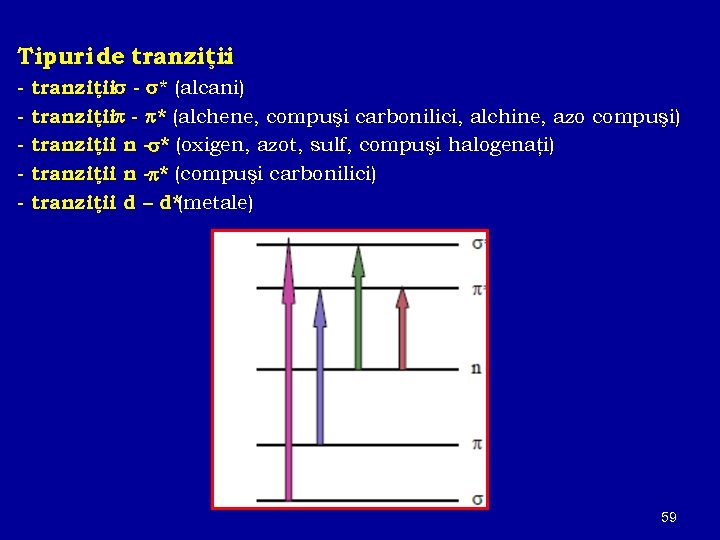
Tipuri de tranziţii : - tranziţii - * (alcani) tranziţii - * (alchene, compuşi carbonilici, alchine, azo compuşi) tranziţii n - * (oxigen, azot, sulf, compuşi halogenaţi) tranziţii n - * (compuşi carbonilici) tranziţii d – d* (metale) 59
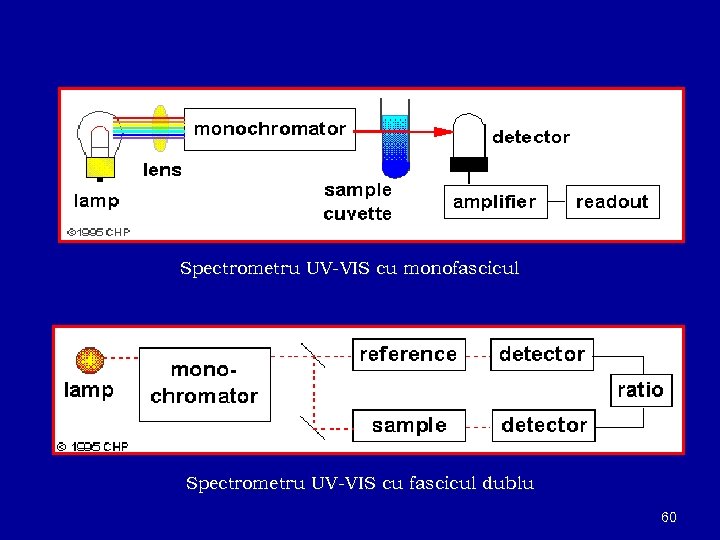
Spectrometru UV-VIS cu monofascicul Spectrometru UV-VIS cu fascicul dublu 60
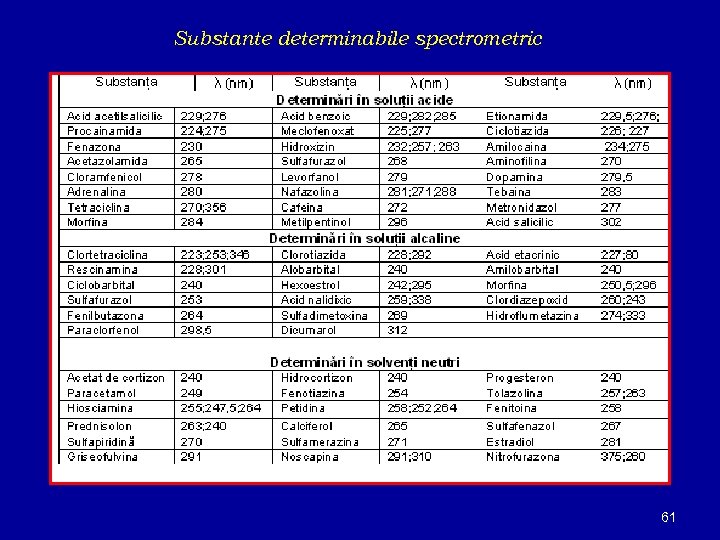
Substante determinabile spectrometric 61

SPECTROSCOPIA ÎN INFRAROŞU INFRARED SPECTROSCOPY (IR) Grupeaza metode de identificare si dozare nedestructive bazate pe absorbtia sau reflexia de catre probe a radiatiilor electromagnetice cuprinse intre 0, 75 - 1000 µm: q q Regiunea fundamentala 2, 5 - 25 µm = regiunea IR analitic 62

63
64
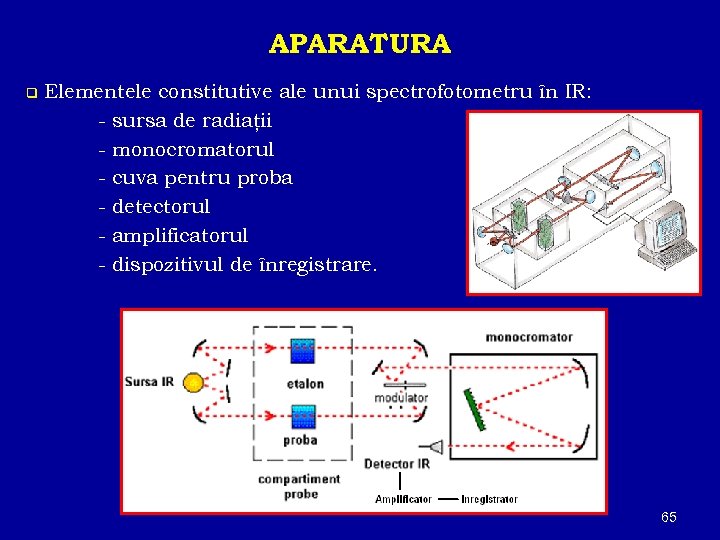
APARATURA q Elementele constitutive ale unui spectrofotometru în IR: - sursa de radiaţii - monocromatorul - cuva pentru proba - detectorul - amplificatorul - dispozitivul de înregistrare. 65

APLICAŢIILE SPECTROSCOPIEI ÎN IR ü nu există compuşi care să prezinte spectre IR identice. domeniul frecvenţelor < 1500 cm-1 (regiunea amprentelor digitale) sunt mult utilizate pentru stabilirea identităţii substanţelor analizate. ü 1. IDENTIFICAREA SUBSTANŢELOR MEDICAMENTOASE se compară spectrul substanţei de analizat cu spectrul obţinut în aceleaşi condiţii cu substanţe etalon ü se compară spectrul substanţei de analizat cu spectrul etalon (din cataloage sau monografii) la care s-au precizat valorile benzilor de absorbţie caracteristice şi care trebuie să fie prezente şi în spectrul substanţei de analizat. ü Spectrul etalon = se obţine utilizând drept substanţe aşa - numitele substanţe de referinţă pentru IR (s. r. i. r. ) înscrise în capitolul Standarde al farmacopeelor. 66

Exemple: acetazolamidă, acid iopanoic, acid nalidixic ü p-aminobenzoat de etil, ampicilina sodică, trihidrat de ampicilină, benzilpenicilina potasică, palmitat de cloramfenicol, clordiazepoxid, acetat de clortestosteronă, cloxacilina sodică ü clorhidrat de cocaină, acetat de cortizon, acetat de dezoxicortizon, dexametazona, dextran 40 şi 70, diazepam, ergocalciferol ü lactobionat de eritromicină, furosemid, hidroclorotiazidă, hidrocortizonă, hidroxiprogesteronă ü 67

2. DECELAREA MEDICAMENTOASE IMPURITĂŢILOR SUBSTANŢELOR Impurităţile substanţelor medicamentoase provenite din procesul de obţinere, cât şi cele rezultate prin degradarea substanţei păstrate în condiţii necorespunzătoare produc modificări vizibile atunci când se efectuează o analiză atentă a spectrului înregistrat. q Se observă: ü modificăriale benzilor de absorbţie care trebuie să caracterizeze substanţa pură ü apariţia altor benzi caracteristice unor legături sau funcţiinoi. q 68

3. DETERMINAREA MEDICAMENTOASE CANTITATIVĂ A SUBSTANŢELOR determinarea cantitativă a substanţelor medicamentoase ca atare ü determinarea cantitativă a substanţelor medicamentoase din produsele farmaceutice. ü q ü ü Probleme: realizarea unor condiţii standardizate respectarea legii Lambert-Beer. Exemplu: Alilestrenolul - se foloseste solvent CCl 4. - maximele de absorbţie caracteristice = 1310 cm-1, 1650 cm-1. - legea Lambert-Beer se verifică folosind soluţii de concentraţii = 0, 5 -2 g% (m/v). - se poate determina în aceste condiţii şi din diverse produse farmaceutice. ü 69
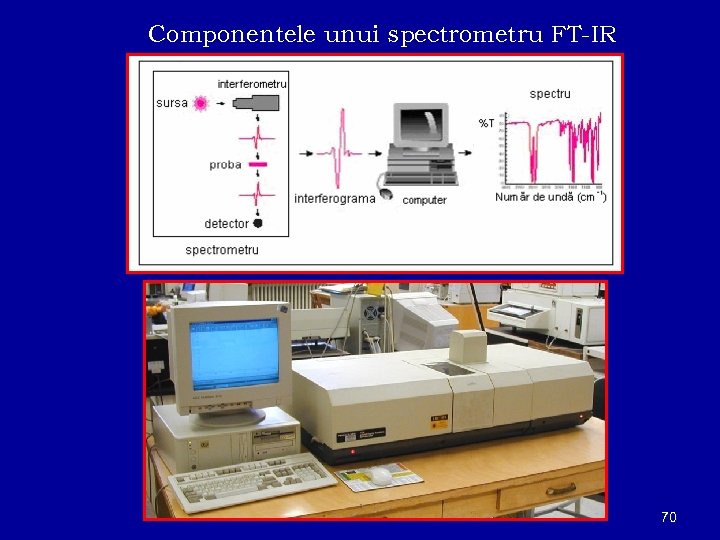
Componentele unui spectrometru FT-IR 70

Avantajele. FT-IR Viteză : ü deoarece toate frecvenţele sunt măsurate determinărilor FT-IR sunt de ordinul secundelor q simultan, majoritatea Sensibilitate : ü sensibilitatea metodei este mult îmbunătăţită deoarece detectorii utilizaţi sunt mai sensibili, zgomotul de fond este mult scăzut, iar scanarea rapidă permite coadiţia mai multor scanări, reducând zgomotul măsurat întâmplător la nivelul dorit (semnal mediu) q Simplitateaaparaturii : ü oglinda mobilă a interferometrului este singura parte a aparatului care se mişcă continuu, astfel încât este foarte puţin posibilă o defectare mecanică q Calibrarea internă : ü aceste aparate utilizează ca standard de calibrare internă a lungimii de undă, lasere cu He, Ne. Aparatura are auto-calibrare şi nu necesită o calibrare de către utilizator. q 71

APLICAŢIILE FT-IR metodă utilizată pentru identificarea oricărei probe. q sensibilitatea va face posibilă identificarea unei cantităţi foarte mici de impurităţi, ceea ce demonstrează că analiza FT-IR este o metodă valoroasă în controlul de calitate sau în aplicaţiile asigurării calităţii. q sensibilitatea şi precizia detectorilor FT-IR, la care se adaugă gama largă de software de algoritm au crescut utilizarea practică a metodei în analiza cantitativă. Evaluare şi identificare : q de compuşi organici, anorganici q în formularea medicamentelor q în determinarea omogenităţii materialelor q în medicina legală. q 72
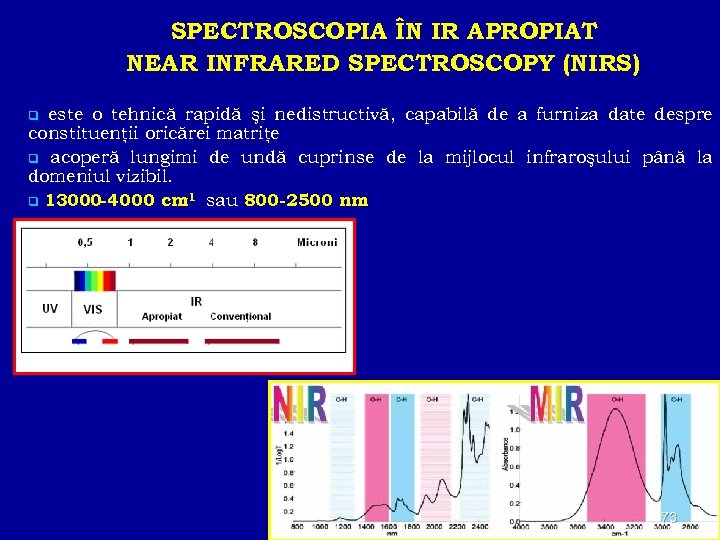
SPECTROSCOPIA ÎN IR APROPIAT NEAR INFRARED SPECTROSCOPY (NIRS) este o tehnică rapidă şi nedistructivă, capabilă de a furniza date despre constituenţii oricărei matriţe q acoperă lungimi de undă cuprinse de la mijlocul infraroşului până la domeniul vizibil. -1 q 13000 -4000 cm sau 800 -2500 nm q 73
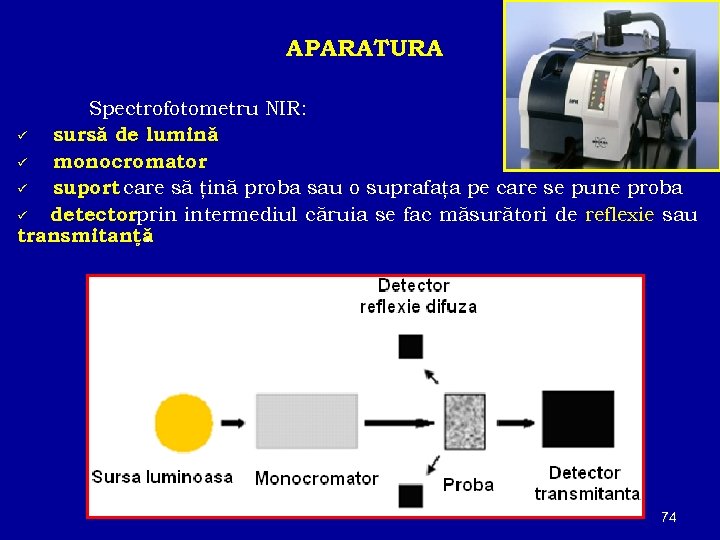
APARATURA Spectrofotometru NIR: ü sursă de lumină ü monocromator ü suport care să ţină proba sau o suprafaţa pe care se pune proba ü detectorprin intermediul căruia se fac măsurători de reflexie sau transmitanţă. 74
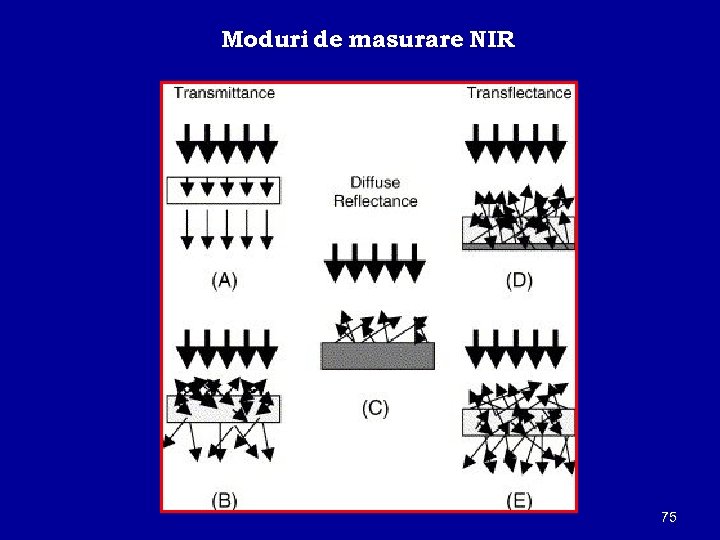
Moduri de masurare NIR 75
AVANTAJE NIR q nu este necesara prepararea probei → reducere timp de analiza q metoda nedistructiva q cantitati mici de reactivi q metoda excelenta pentru analiza probelor solide q metoda neinvaziva 76

SPECTROSCOPIA DE MASA - MASS SPECTROSCOPY (MS) Definitie : Spectroscopia de masă este o metodă instrumentală de analiză care se bazează pe fragmentarea moleculelor substanţelor organice sub acţiunea unor radiaţii cu energii mari de până la 100 e. V, iar din analiza - numărului - sarcinii - masei fragmentelor rezultate - se obţin informaţii asupra • structurii • identităţii substanţelor cercetate. Datorită acumulării de energie are loc fragmentarea moleculelor cu ruperea unor legături interatomice, proces prin care rezultă : - mai ales ioni pozitivi (rar negativi) - radicali - ioni radicali - molecule neutre. Aceste fragmente constituie piese importante de reconstituire a structurii moleculare. 77
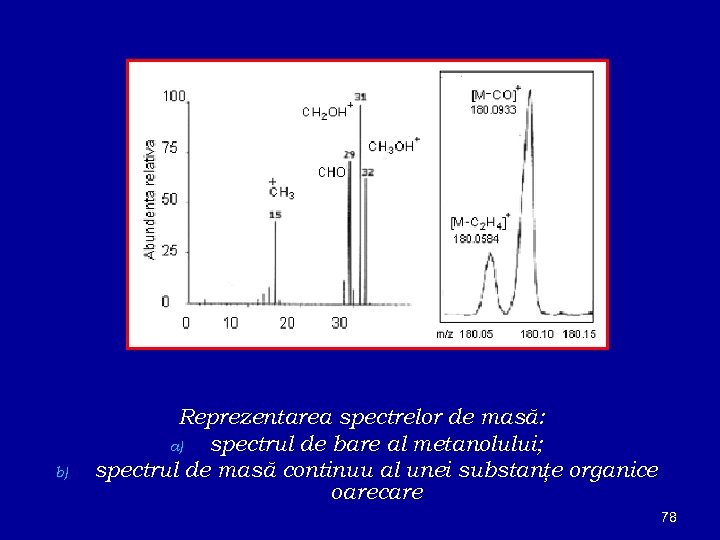
b) Reprezentarea spectrelor de masă: a) spectrul de bare al metanolului; spectrul de masă continuu al unei substanţe organice oarecare 78
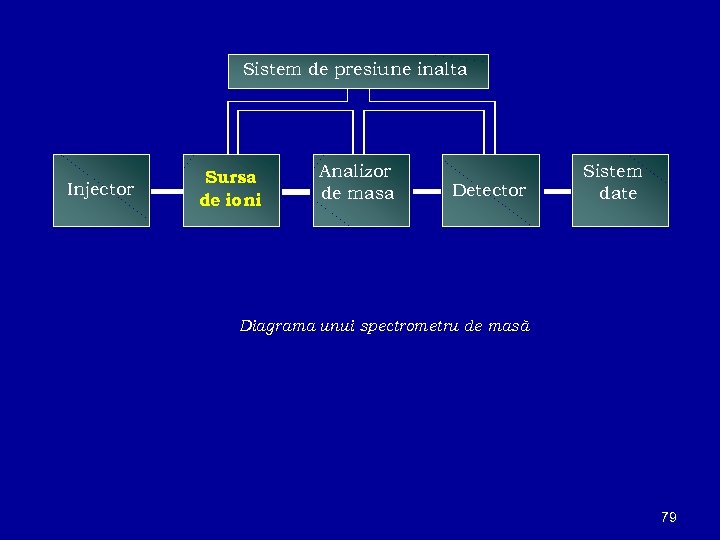
Sistem de presiune inalta Injector Sursa de ioni Analizor de masa Detector Sistem date Diagrama unui spectrometru de masă 79

Surse de ionizare 1. 2. 3. 4. 5. 6. Ionizarea prin impact electronic (Electron ionisation - EI) Ionizarea chimicã (Chemical ionisation – CI) Bombardarea cu atomi rapizi (Fast Atom/Ion Bombardment – FAB) Ionizarea prin desorbţie laser asistată de o matrice (Matrix assisted laser desorption ionization MALDI) Ionizarea la Presiune Atmosferică (Atmospheric Pressure Chemical Ionization - APCI) Ionizarea prin electrospray (Electrospray Ionization - ESI) 80

APLICAŢIILE SPECTROSCOPIEI DE MASĂ Interpretareaspectrelor + + + 81

Identificarea unui compus cu ajutorul spectrotecii MS Există spectroteci care corespund unor colecţii (biblioteci) de spectre de masă ale substanţelor cunoscute, în care sunt incluse (codate) principalele picuri ale acestora. Utilizarea acestor spectroteci, în care se caută picurile care interesează, implică următoarele etape: reducerea datelor prin care spectrul substanţei care ne interesează este redus la , cel mult 16 picuri, acordând preferinţă picurilor mai grele, mai semnificative decât picurilor uşoare; fiecare spectru este redus în bibliotecă la 8 picuri - precercetarea care constă în selecţionarea spectrelor reduse din spectrotecă, la , acelea care au picuri cu aceleaşi poziţii ca şi picurile din spectrul redus al substanţei cercetate, chiar dacă intensitatea lor este diferită - cercetarea principală care constă în reluarea selecţiei precedente printr-un , algoritm mai subtil care include printre criteriile de alegere: • intensitatea • masa • raritatea picului, afectând un indice de identitate de la 0 la 1000 fiecărui spectru, prin aceasta realizându-se o clasare prin similaritatea descrescătoare. Există numeroşi algoritmi de cercetare, iar prin modificarea criteriilor de alegere se poate reduce cercetarea prin verificarea şi alegerea între diverse clasamente. Cea mai importantă spectrotecă de masă este aceea a NIST (National Institut of Standards and Technology), care includea peste 250000 de spectre la nivelul anului 1996, iar în prezent numărul spectrelor este desigur mai mare. - 82

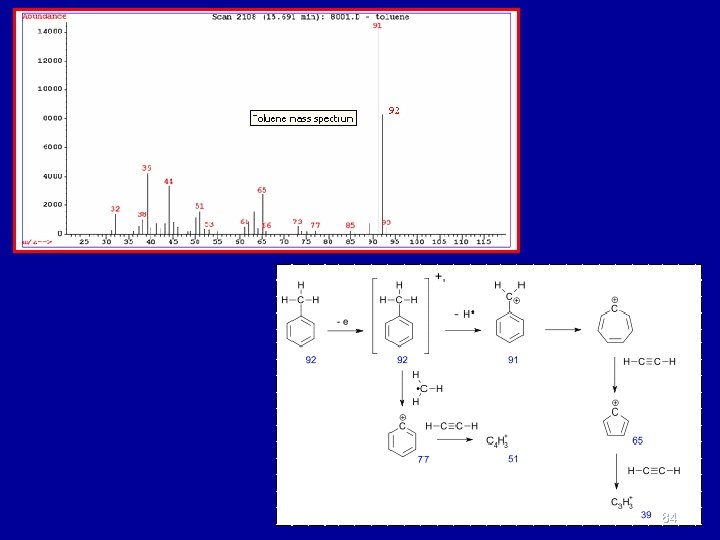
Stabilirea formulei moleculare Spectrele de masă pot fi utilizate cu şanse mari de certitudine pentru stabilirea formulei moleculare a unei substanţe, deoarece poziţia fiecărui pic care provine din fragmentarea unui ion precedent (exceptând cazul unor reamenajări) oferă informaţii care se pot utiliza pentru stabilirea ionului în cauză. Exemplu: - prezenţa unui pic cu (M-1)+ - ionul s-a format prin pierderea unui atom de hidrogen - prezenţa unui pic cu masa (M-15)+ - ionul provine din ionul M+ prin pierderea foarte probabilă a unei grupe de metil (CH 3 cu masa M=15) - daca ionul M+ conduce la un ion cu masa (M-18)+ - ionul a pierdut o moleculă de apă. Trebuie să se ţină seama că, de regulă, procesul de fragmentare sau cel de reamenajare a ionilor care se formează din ionul molecular trebuie să conducă la radicali sau ioni mai stabili decât ionul din care provin. 83
84
e253c387879d3e3e93a131c0dfb39a87.ppt