проблема производства и исследования ЛС.pptx
- Количество слайдов: 13

Проблема создания и воспроизводства лекарственных средств

Лекарственное средство – однокомпонентный или комплексный обладающий профилактической и лечебной эффективностью. состав, Лекарственное вещество – индивидуальное химическое соединение, используемое в качестве лекарственного средства. Лекарственная форма – физическое состояние лекарственного средства, удобное для применения. Лекарственный препарат – дозированное лекарственное средство в адекватной для индивидуального применения лекарственной форме и оптимальным оформлением с приложением аннотации о его свойствах и использовании. В настоящее время каждое лекарственное вещество проходит 3 стадии изучения: фармацевтическую, фармакокинетическую, фармакодинамическую.

1. Фармацевтическая стадия - установление наличия полезного действия лекарственного вещества, после чего оно подвергается доклиническому изучению других показателей. а) определение острой токсичности, т. е. смертельная доза для 50 % опытных животных; б) определение субхронической токсичности – длительное введение вещества в терапевтических дозах (определение тератогенности, эмбриотоксичности, мутагенности, канцерогенность, аллергенность); в) допуск к клиническим испытаниям. 2. Фармакокинетическая - изучает судьбу лекарственного вещества в организме: а) пути его введения б)всасывание в)распределение в биожидкостях г) проникновение через защитные барьеры д) доступ к органу-мишени е) пути и скорость биотрансформации ж) пути выведения из организма (с мочой, калом, потом и дыханием).

3. Фармакодинамическая - изучение проблем распознавания лекарственного вещества (или его метаболитов) мишенями и их последующего взаимодействия. Мишенями могут служить органы, ткани, клетки, клеточные мембраны, ферменты, нуклеиновые кислоты, регуляторные молекулы (гормоны, витамины, нейромедиаторы и т. д. ), а также биорецепторы. Взаимодействие между лекарственным веществом и рецептором или акцептором, приводящее к активации (стимулированию) или дезактивации (ингибированию) биомишени и сопровождающееся ответом организма в целом, в основном обеспечивается за счет слабых связей – водородных, электростатических, гидрофобных.
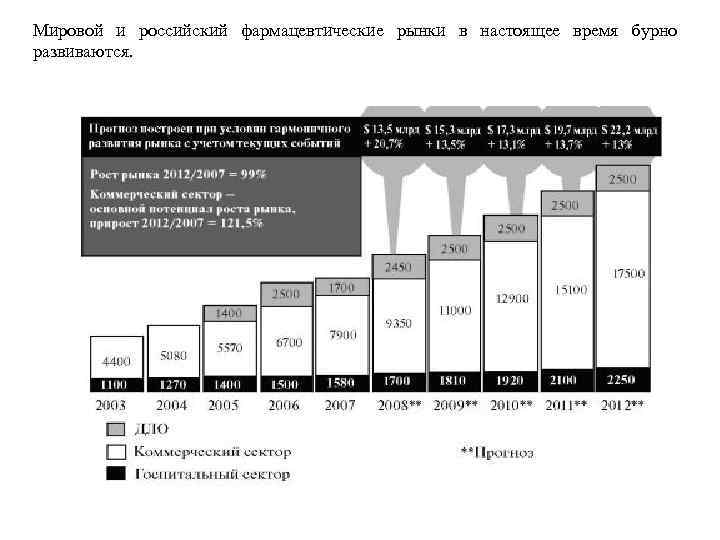
Мировой и российский фармацевтические рынки в настоящее время бурно развиваются.

1. Дженериковые ЛС доминируют на рынке. Доля инновационных ЛС все еще остается небольшой: так, в 2008 г. она составит в среднем около 13%. Дженерик (генерик, женерик, генерический препарат; англ. Generic) — это непатентованный лекарственный препарат, являющийся воспроизведением оригинального препарата, на действующее вещество которого истёк срок патентной защиты. Может отличаться от оригинального препарата по составу вспомогательных веществ. Необходимое требование для продажи дженериков — доказанная фармацевтическая, биологическая и терапевтическая эквивалентность исходному препарату. Инновационные лекарственные средства и лекарственные технологии – это новые ЛС, новые лекарственные формы или средства доставки лекарств, защищенные патентом. Инновационный препарат – это новое лекарственное средство, у которого под защитой патента находится не бренд (торговая марка), а действующее вещество, воздействующее на определённую биологическую мишень. Патентная защита инновационного лекарственного средства действует в зависимости от патентного законодательства конкретной страны (например, 12 лет в США, до 25 лет в России). С окончанием срока действия патента законодательные ограничения на продажу лекарственного средства теряют силу. С этого момента практически любая фирма, имеющая возможность освоить технологию производства лекарственного средства, получает возможность выхода на рынок.
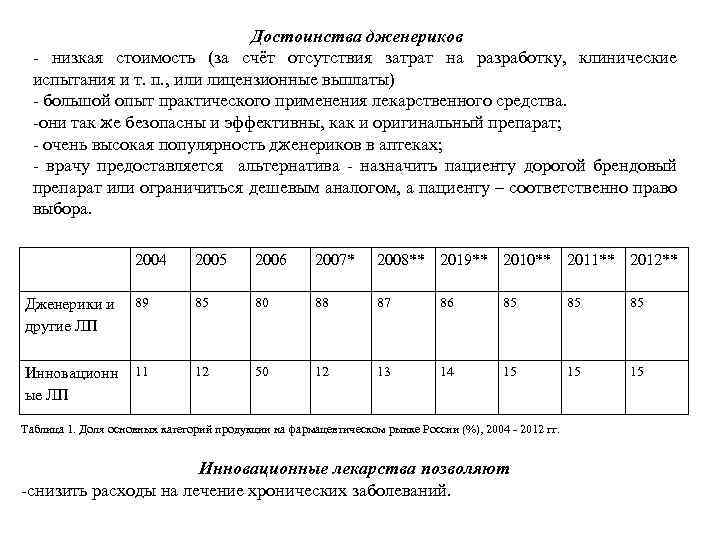
Достоинства дженериков - низкая стоимость (за счёт отсутствия затрат на разработку, клинические испытания и т. п. , или лицензионные выплаты) - большой опыт практического применения лекарственного средства. -они так же безопасны и эффективны, как и оригинальный препарат; - очень высокая популярность дженериков в аптеках; - врачу предоставляется альтернатива - назначить пациенту дорогой брендовый препарат или ограничиться дешевым аналогом, а пациенту – соответственно право выбора. 2004 2005 2006 2007* 2008** 2019** 2010** 2011** 2012** Дженерики и другие ЛП 89 85 80 88 87 86 85 85 85 Инновационн ые ЛП 11 12 50 12 13 14 15 15 15 Таблица 1. Доля основных категорий продукции на фармацевтическом рынке России (%), 2004 - 2012 гг. Инновационные лекарства позволяют -снизить расходы на лечение хронических заболеваний.

2. Объём импортных ЛС – более 70%, и только 5% готовых ЛП производится на основе отечественных субстанций На фармацевтическом рынке России полностью отсутствуют отечественные антибиотики нового поколения, противотуберкулезные, ЛС для лечения онкологических заболеваний и обезболивающие препараты, инсулин и многие другие лекарства. Такое положение вещей не только негативно сказывается на здоровье средне- и малообеспеченных слоев населения, но и, безусловно, ставит под угрозу само существование фармацевтической отрасли в России. Из сказанного следует, что интересы здравоохранения, в том числе клинической медицины, требуют стимулирования исследований по созданию инновационных ЛС. Для решения создавшейся ситуации необходимо: -проводить исследования, направленные на создание лекарств на основе отобранных в эксперименте веществ. В конце 1970 -х гг. П. В. Лопатиным была сформулирована концепция лекарства как материализованной программы доставки лекарственного вещества к биологической мишени и предложена закрытая графическая модель процесса его разработки.
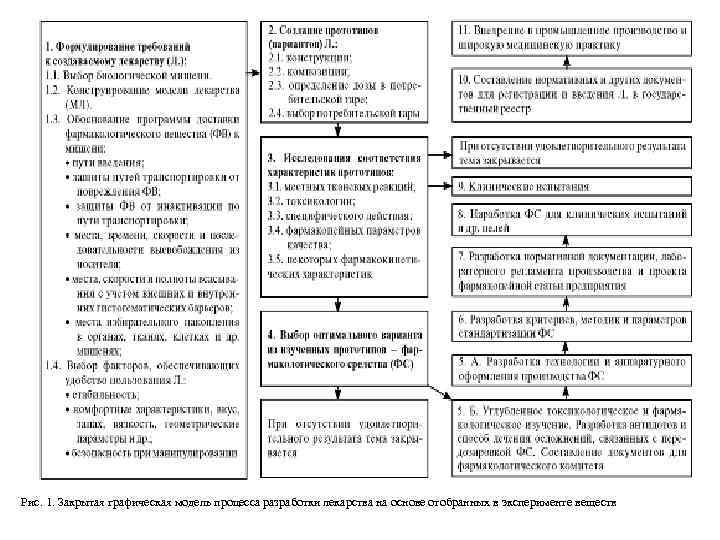
Рис. 1. Закрытая графическая модель процесса разработки лекарства на основе отобранных в эксперименте веществ

Модель включает несколько блоков последовательного решения необходимых задач. 1. Первый блок (этап) предусматривает формулировку требований к создаваемому лекарству. На первом этапе выбирается биологическая мишень, к которой должны быть доставлены соответствующие лекарственные вещества. Это может быть выполнено на основе теоретических и экспериментальных изысканий. 2. Второй блок предусматривает создание прототипов лекарства, т. е. вариантов композиций и конструкций его, из которых в дальнейшем будет отобран лучший. На этом этапе помимо поиска оптимальной конструкции и композиции потенциального лекарства определяется доза действующего вещества в потребительской таре и сама потребительская тара. 3. Затем проводятся исследования соответствия характеристик прототипов лекарства ранее сформулированным требованиям (блоки 3 и 4). 4. На 5 -м и 6 -м этапах научно-исследовательской работы ведутся параллельные исследования, направленные на углубленное терапевтическое, токсикологическое и фармакологическое изучение фармакологического средства; разрабатываются антидоты и способы лечения осложнений, связанных с передозировкой фармакологического средства; составляются документы, необходимые для разрешения клинических испытаний.

Одновременно другая группа исследователей (технологов) разрабатывает технологию и аппаратурное оформление производства фармакологического средства, необходимые для лабораторной наработки его с целью углубленных лабораторных испытаний, разработки критериев, методов, методик и параметров стандартизации и контроля качества. 5. После этого на 7 -м этапе разрабатывается нормативная документация, обеспечивающая наработку ЛС для клинических испытаний и, в случае их успешного завершения, последующего продвижения, в том числе лабораторный регламент производства, предварительные нормативно-технические требования (проекты ВФС или Фармакопейные статьи предприятия). 6. Важнейшим этапом (блок 8) является наработка фармакологического средства для клинических испытаний. Следует подчеркнуть, что наибольшего успеха достигают организации, имеющие собственную наработочную базу. В России такие базы имеют ряд ведущих научно-исследовательских центров и производственных фармацевтических организаций, в частности: ОАО «Нижфарм» , ОАО «Хим. Фарм. Комбинат» , ЗАО «Акрихин» , ЗАО «Верофарм» и др. Это позволяет в сжатые сроки разрабатывать нормативные документы, необходимые и для промышленного выпуска продукции (блок 10), в том числе опытно-промышленные и другие регламенты, ФСП, ВФ и ФС, а также при регистрации ЛС и введения их в государственный реестр лекарств.

В условиях острой конкурентной борьбы вся деятельность в области разработки инновационных ЛС должна охраняться. Непременным условиям эффективной охраны интеллектуальной собственности является высокая морально-нравственная зрелость персонала. Биоэтические позиции специалистов, занятых в цепи исследований и разработок по созданию лекарств и продвижению их на рынок, а также производству и доведению их до потребителя, т. е. в сфере обращения лекарств, являются решающим элементом в решении проблемы эффективной медицинской помощи, основанной на принципах доказательной терапии, доказательной фармакотерапии, фармацевтической бдительности и фармакоэкономики.

проблема производства и исследования ЛС.pptx