3липиды мембран 2 часть.ppt
- Количество слайдов: 53

ПРИНЦИПЫ ОРГАНИЗАЦИИ ЛИПИДНОГО БИСЛОЯ

ПОДВИЖНОСТЬ ЛИПИДОВ В МЕМБРАНЕ

ØИЗМЕНЕНИЕ ОРИЕНТАЦИИ ПОЛЯРНЫХ ГОЛОВ ØЛАТЕРАЛЬНОЕ ДВИЖЕНИЕ ØКОЛЕБАНИЯ АЦИЛЬНЫХ ЦЕПЕЙ ØОБРАЗОВАНИЕ КИНКОВ И ПЕРЕМЕЩЕНИЕ ИХ ВДОЛЬ АЦИЛЬНЫХ ЦЕПЕЙ ØРОТАЦИОННАЯ ПОДВИЖНОСТЬ ØФЛИП-ФЛОП ØВЫХОД ИЗ БИСЛОЯ
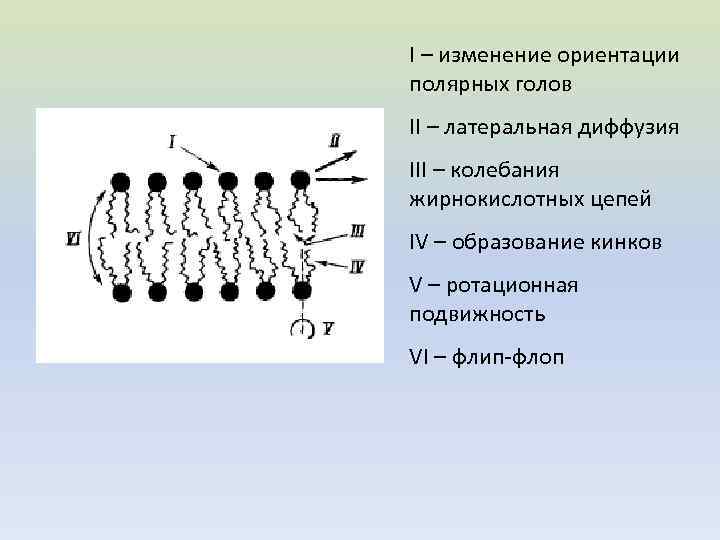
I – изменение ориентации полярных голов II – латеральная диффузия III – колебания жирнокислотных цепей IV – образование кинков V – ротационная подвижность VI – флип-флоп
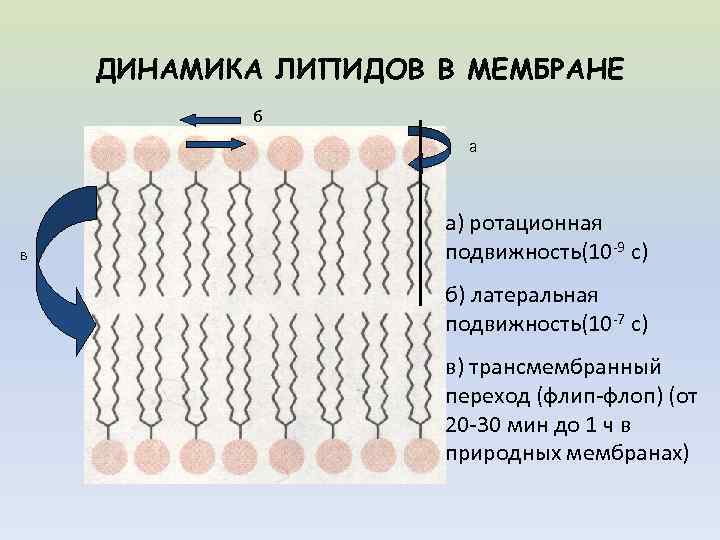
ДИНАМИКА ЛИПИДОВ В МЕМБРАНЕ б а в а) ротационная подвижность(10 -9 с) б) латеральная подвижность(10 -7 с) в) трансмембранный переход (флип-флоп) (от 20 -30 мин до 1 ч в природных мембранах)

УПАКОВКА ЛИПИДОВ В МЕМБРАНЕ, ПОДВИЖНОСТЬ ЖИРНОКИСЛОТНЫХ ХВОСТОВ, ОБРАЗОВАНИЕ КИНКОВ
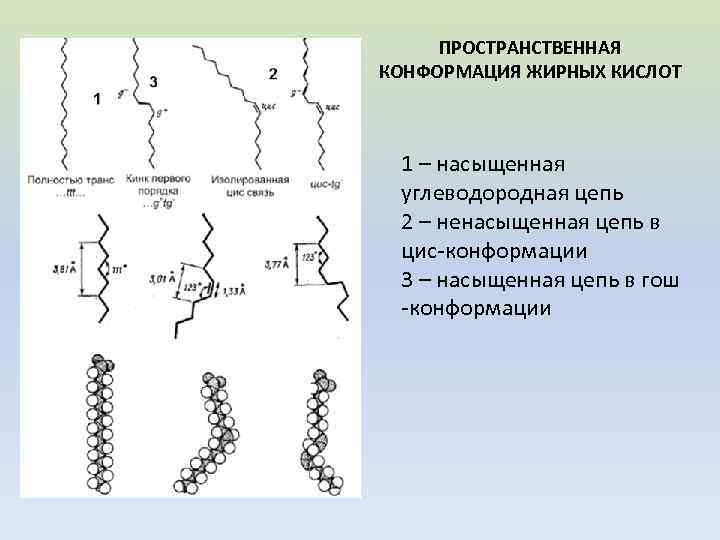
ПРОСТРАНСТВЕННАЯ КОНФОРМАЦИЯ ЖИРНЫХ КИСЛОТ 1 – насыщенная углеводородная цепь 2 – ненасыщенная цепь в цис-конформации 3 – насыщенная цепь в гош -конформации
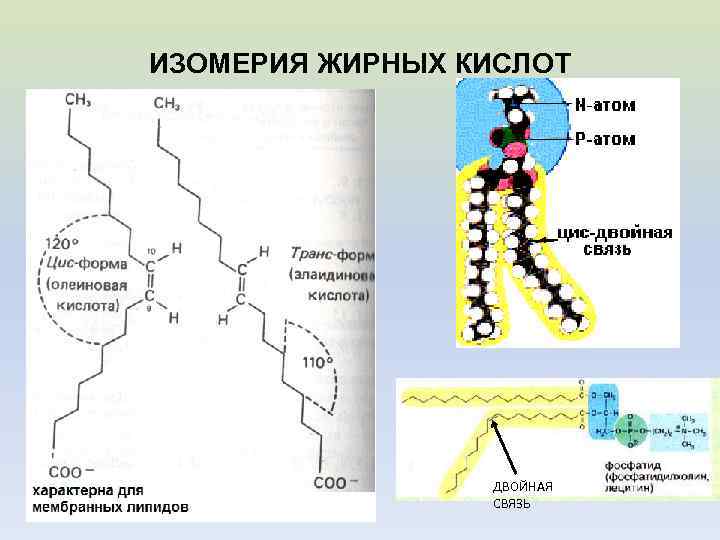
ИЗОМЕРИЯ ЖИРНЫХ КИСЛОТ ДВОЙНАЯ СВЯЗЬ

ОБРАЗОВАНИЕ ДЕФЕКТОВ В МЕМБРАННОМ БИСЛОЕ

ГЕОМЕТРИЯ БИСЛОЯ 2 РАЗМЕРЫ МОЛЕКУЛЫ ЛИПИДА: ХВОСТ НМ, ГОЛОВКА РАССЧИТАННАЯ ТОЛЩИНА БИСЛОЯ 0, 5 – 0, 7 НМ, 5, 0 – 5, 4 НМ В ДЕЙСТВИТЕЛЬНОСТИ: ТОЛЩИНА БИСЛОЯ ЛИПИДОВ В МЕМБРАНЕ – 4 НМ 3, 5 СЛЕДОВАТЕЛЬНО, ЖИРНЫЕ КИСЛОТЫ РАСПОЛОЖЕНЫ В БИСЛОЕ РЫХЛО
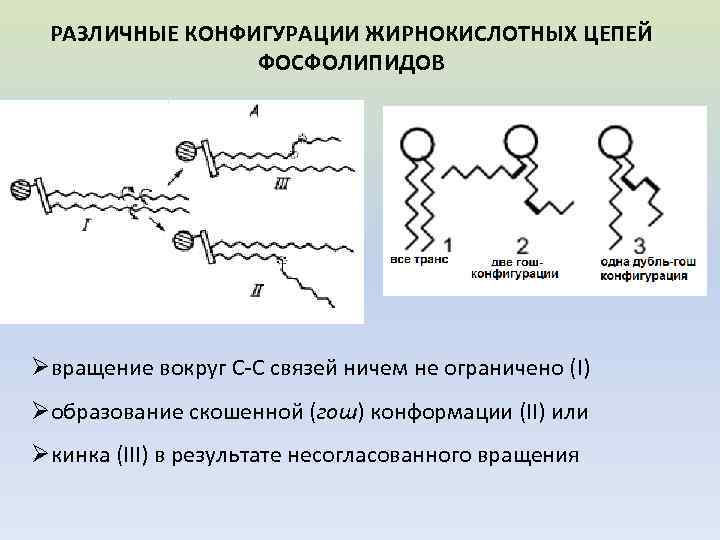
РАЗЛИЧНЫЕ КОНФИГУРАЦИИ ЖИРНОКИСЛОТНЫХ ЦЕПЕЙ ФОСФОЛИПИДОВ Øвращение вокруг С-С связей ничем не ограничено (I) Øобразование скошенной (гош) конформации (II) или Øкинка (III) в результате несогласованного вращения
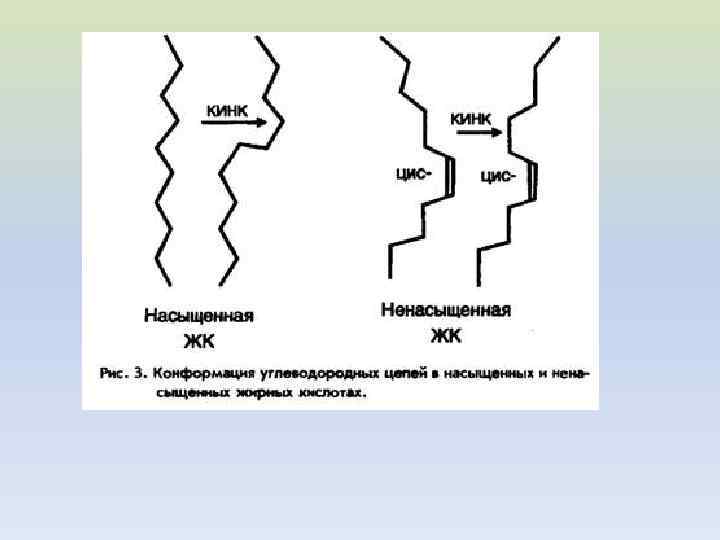
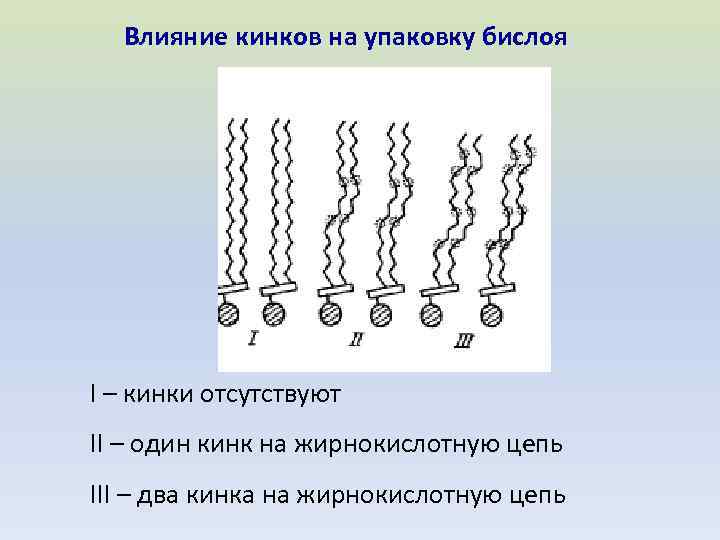
Влияние кинков на упаковку бислоя I – кинки отсутствуют II – один кинк на жирнокислотную цепь III – два кинка на жирнокислотную цепь
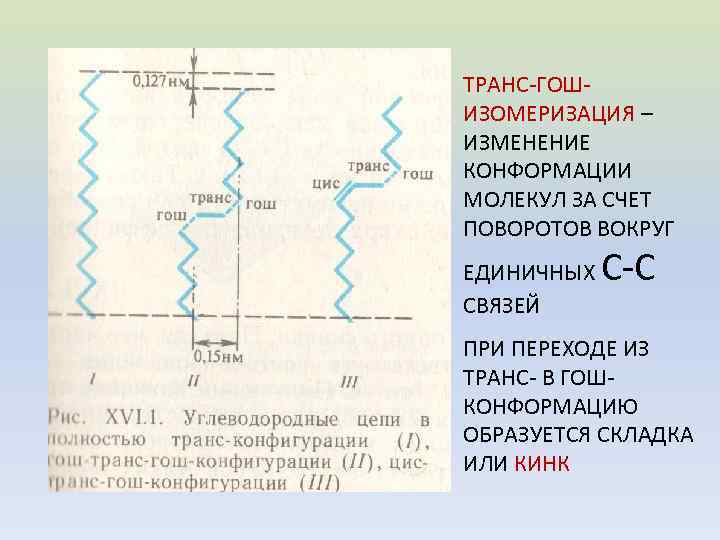
ТРАНС-ГОШИЗОМЕРИЗАЦИЯ – ИЗМЕНЕНИЕ КОНФОРМАЦИИ МОЛЕКУЛ ЗА СЧЕТ ПОВОРОТОВ ВОКРУГ ЕДИНИЧНЫХ СВЯЗЕЙ С-С ПРИ ПЕРЕХОДЕ ИЗ ТРАНС- В ГОШКОНФОРМАЦИЮ ОБРАЗУЕТСЯ СКЛАДКА ИЛИ КИНК
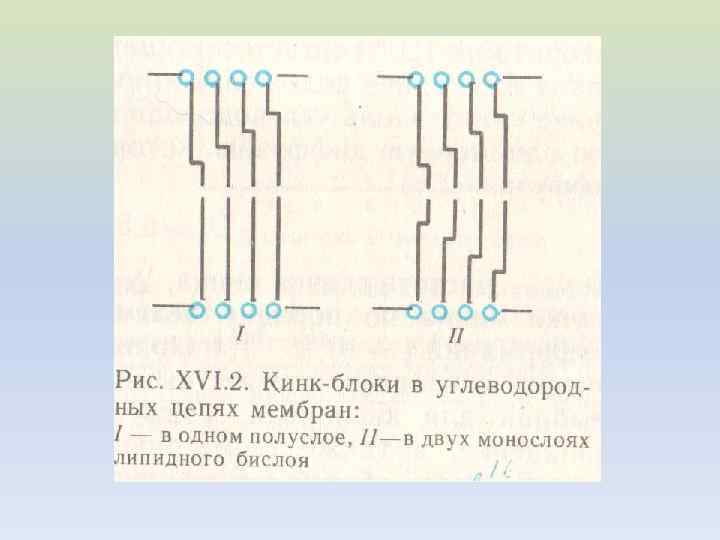

Образованию кинков способствует переход трансконфигурации в гош-конфигурацию, причем образование их может происходить вдоль всей углеводородной цепи, включая не только ненасыщенные, но и насыщенные участки. Поэтому последовательное формирование вдоль цепи кинков можно представить себе как их движение.
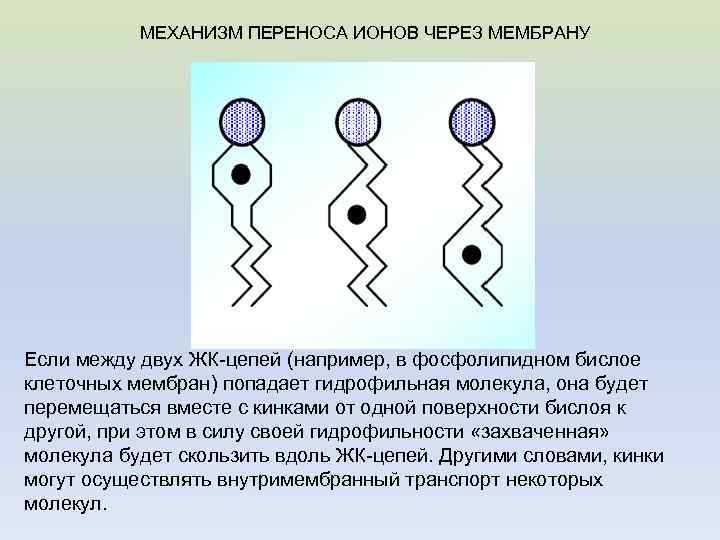
МЕХАНИЗМ ПЕРЕНОСА ИОНОВ ЧЕРЕЗ МЕМБРАНУ Если между двух ЖК-цепей (например, в фосфолипидном бислое клеточных мембран) попадает гидрофильная молекула, она будет перемещаться вместе с кинками от одной поверхности бислоя к другой, при этом в силу своей гидрофильности «захваченная» молекула будет скользить вдоль ЖК-цепей. Другими словами, кинки могут осуществлять внутримембранный транспорт некоторых молекул.
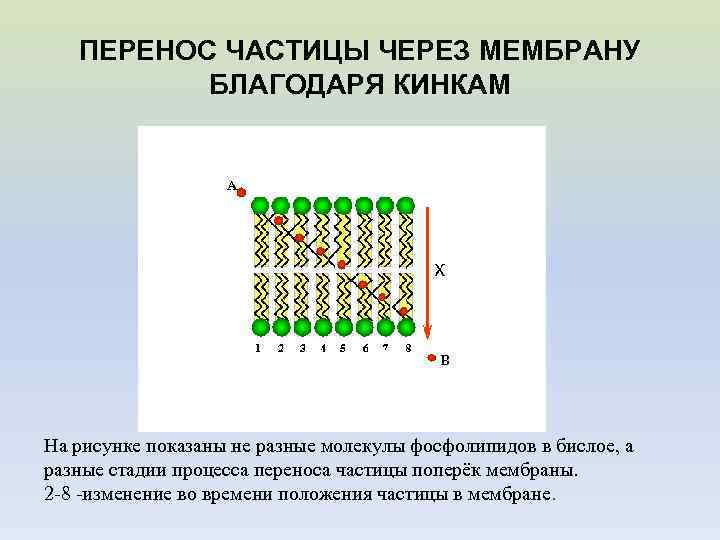
ПЕРЕНОС ЧАСТИЦЫ ЧЕРЕЗ МЕМБРАНУ БЛАГОДАРЯ КИНКАМ На рисунке показаны не разные молекулы фосфолипидов в бислое, а разные стадии процесса переноса частицы поперёк мембраны. 2 -8 -изменение во времени положения частицы в мембране.

ФАЗОВЫЕ ПЕРЕХОДЫ В ЛИПИДНОМ БИСЛОЕ
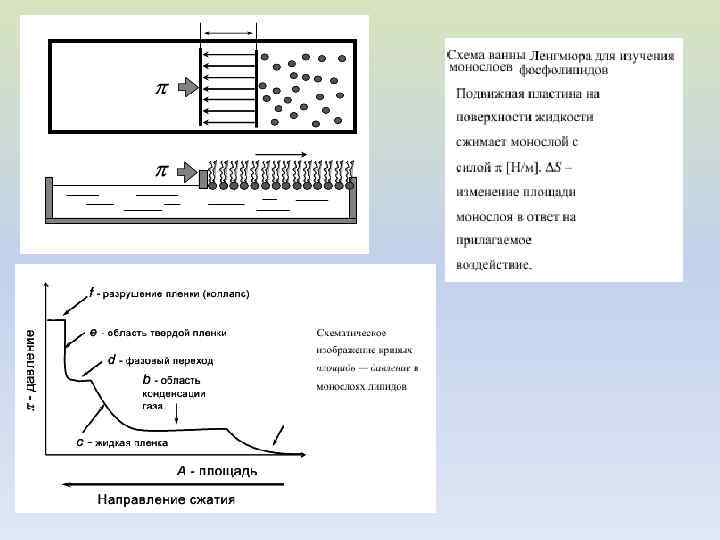
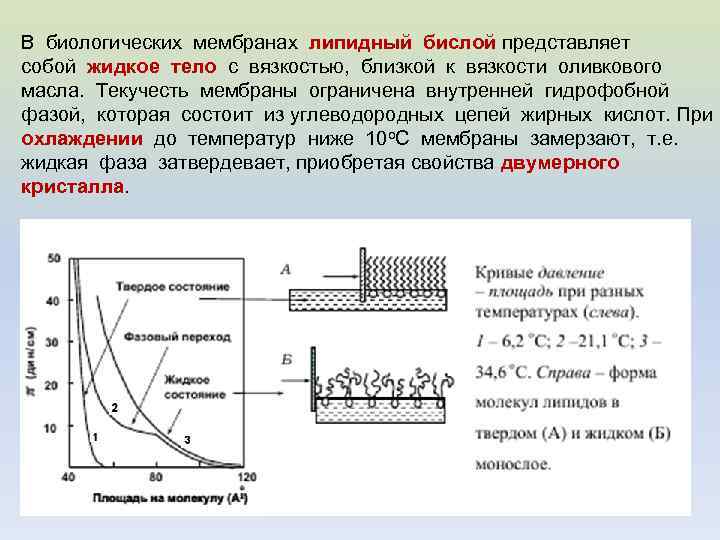
В биологических мембранах липидный бислой представляет собой жидкое тело с вязкостью, близкой к вязкости оливкового масла. Текучесть мембраны ограничена внутренней гидрофобной фазой, которая состоит из углеводородных цепей жирных кислот. При охлаждении до температур ниже 10 о. С мембраны замерзают, т. е. жидкая фаза затвердевает, приобретая свойства двумерного кристалла.
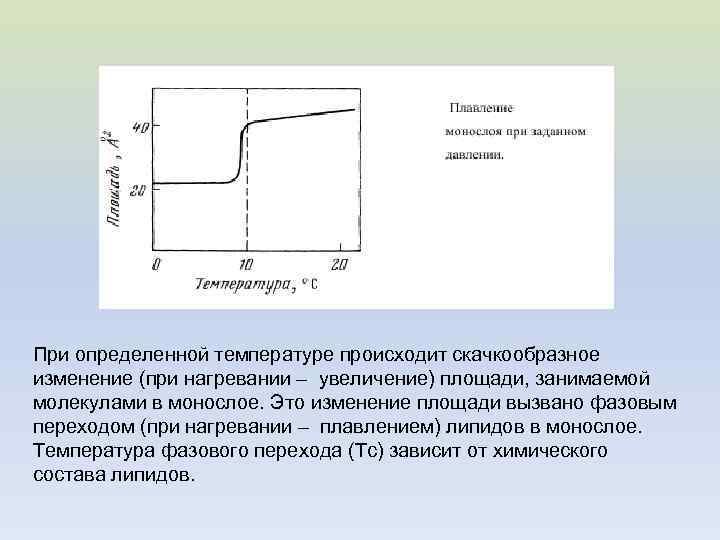
При определенной температуре происходит скачкообразное изменение (при нагревании – увеличение) площади, занимаемой молекулами в монослое. Это изменение площади вызвано фазовым переходом (при нагревании – плавлением) липидов в монослое. Температура фазового перехода (Tc) зависит от химического состава липидов.
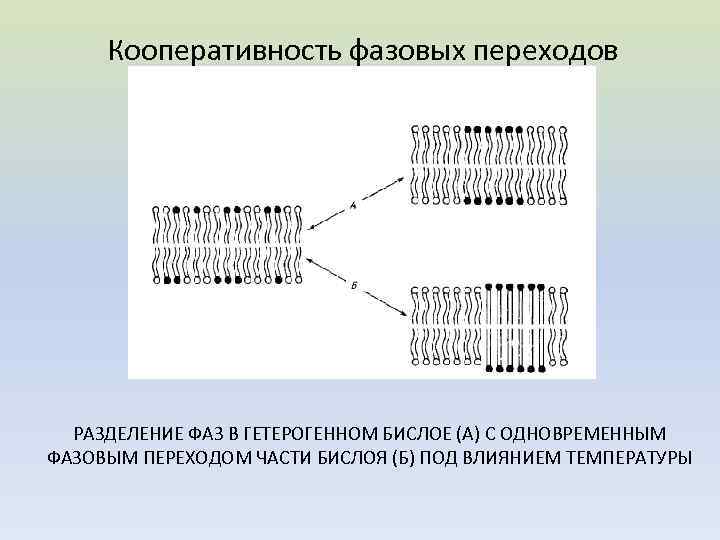
Кооперативность фазовых переходов РАЗДЕЛЕНИЕ ФАЗ В ГЕТЕРОГЕННОМ БИСЛОЕ (А) С ОДНОВРЕМЕННЫМ ФАЗОВЫМ ПЕРЕХОДОМ ЧАСТИ БИСЛОЯ (Б) ПОД ВЛИЯНИЕМ ТЕМПЕРАТУРЫ

Переходит из одного состояния в другое одновременно несколько молекул, объединенных в группу - кооперативную единицу. В пределах кооперативной единицы все молекулы находятся в одинаковом состоянии, образуя либо кристаллическую (твёрдую) фазу либо жидкую фазу. Каждая группа может изменять своё фазовое состояние по закону "всё или ничего" и притом совершенно независимо от других групп.


МЕТОД ДИФФЕРЕНЦИАЛЬНОЙ СКАНИРУЮЩЕЙ МИКРОКАЛОРИМЕТРИИ Метод, основанный на измерении разницы тепловых потоков, идущих от испытуемого образца и образца сравнения.
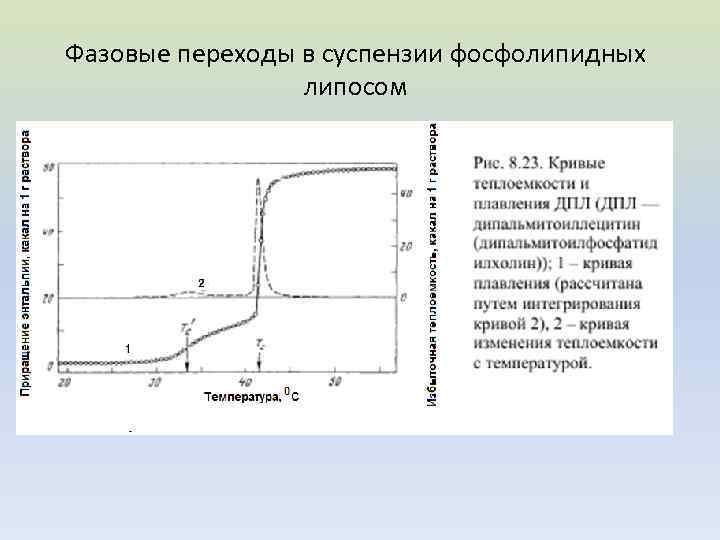
Фазовые переходы в суспензии фосфолипидных липосом
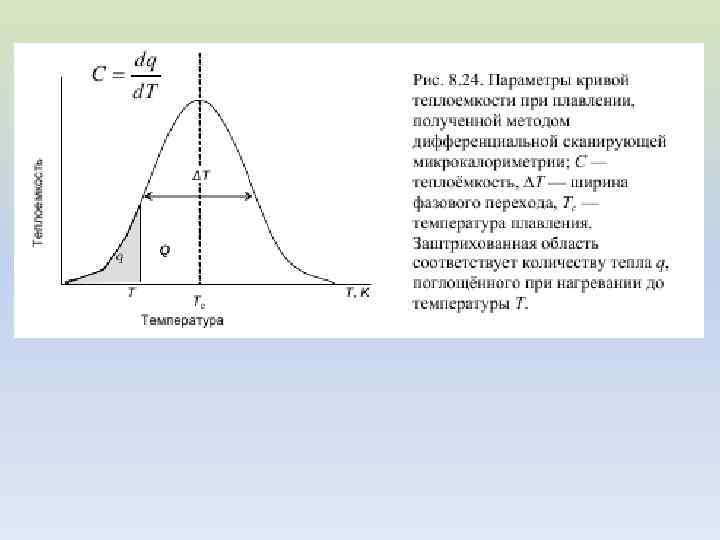

Анализ кривых ДСК Пусть удельная теплота плавления липида равна Qm, количество липидов в образце - m кмоль. Общее количество энергии, поглощённой образцом во всем интервале температур плавления T 1–T 2 равно площади под кривой C = f(T)

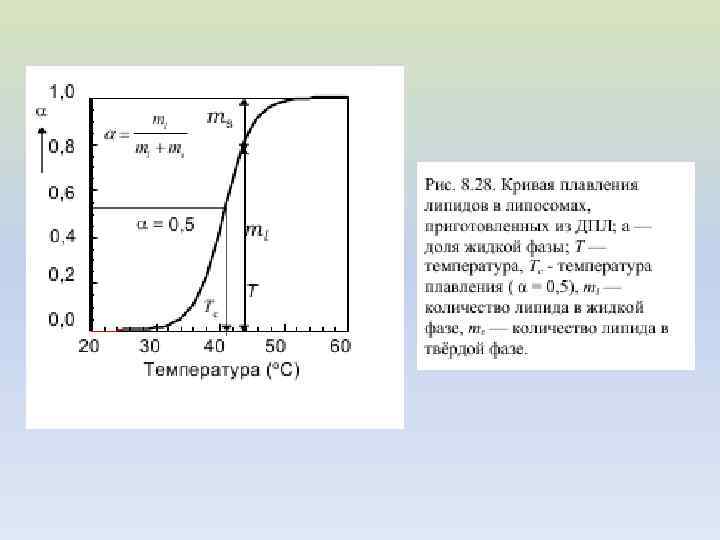
В интервале температур от T 1 до текущей температуры T расплавится количество молей липида ml, и при этом поглотится количество тепла, равное При температуре T мольная доля липидов, находящихся в жидкой фазе равна Измеряя отношение площадей под кривой C=f(T) при разных температурах можно построить кривую плавления α = f(T)
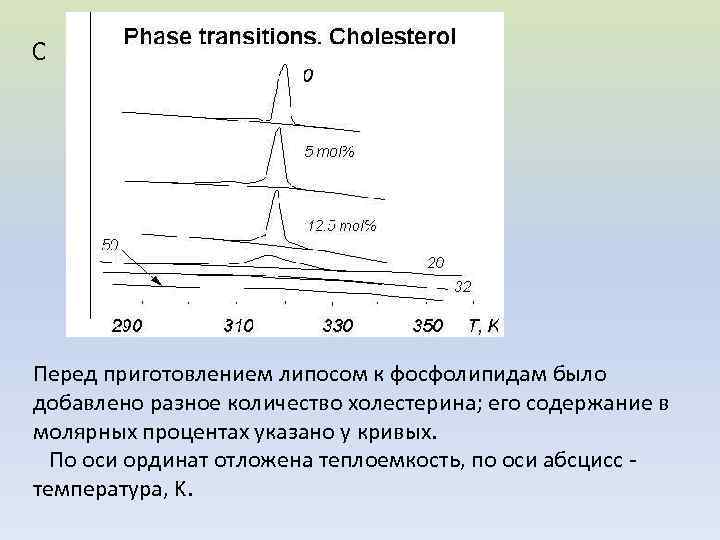
С Перед приготовлением липосом к фосфолипидам было добавлено разное количество холестерина; его содержание в молярных процентах указано у кривых. По оси ординат отложена теплоемкость, по оси абсцисс - температура, K.
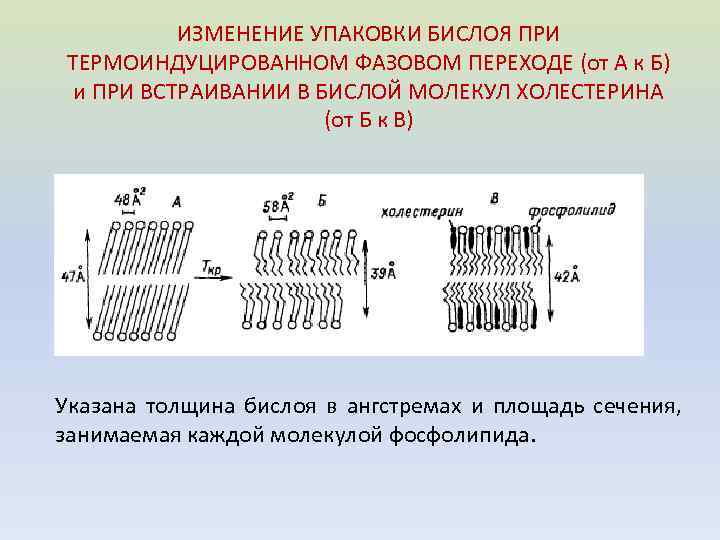
ИЗМЕНЕНИЕ УПАКОВКИ БИСЛОЯ ПРИ ТЕРМОИНДУЦИРОВАННОМ ФАЗОВОМ ПЕРЕХОДЕ (от А к Б) и ПРИ ВСТРАИВАНИИ В БИСЛОЙ МОЛЕКУЛ ХОЛЕСТЕРИНА (от Б к В) Указана толщина бислоя в ангстремах и площадь сечения, занимаемая каждой молекулой фосфолипида.
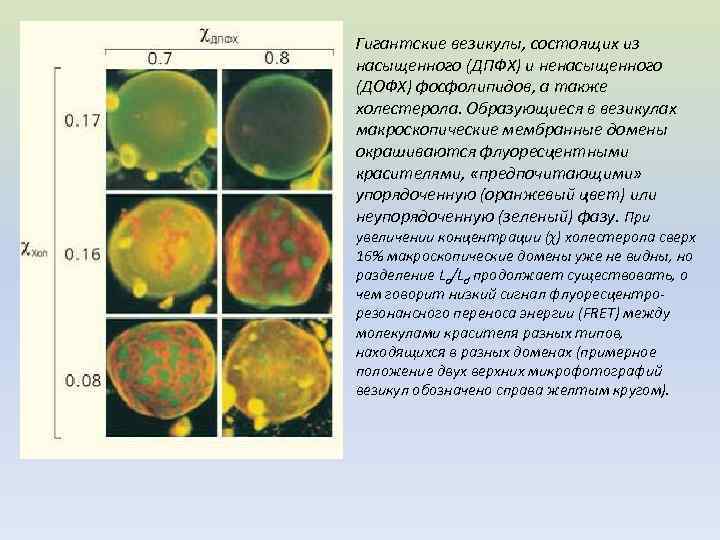
Гигантские везикулы, состоящих из насыщенного (ДПФХ) и ненасыщенного (ДОФХ) фосфолипидов, а также холестерола. Образующиеся в везикулах макроскопические мембранные домены окрашиваются флуоресцентными красителями, «предпочитающими» упорядоченную (оранжевый цвет) или неупорядоченную (зеленый) фазу. При увеличении концентрации (χ) холестерола сверх 16% макроскопические домены уже не видны, но разделение Lo/Ld продолжает существовать, о чем говорит низкий сигнал флуоресцентрорезонансного переноса энергии (FRET) между молекулами красителя разных типов, находящихся в разных доменах (примерное положение двух верхних микрофотографий везикул обозначено справа желтым кругом).
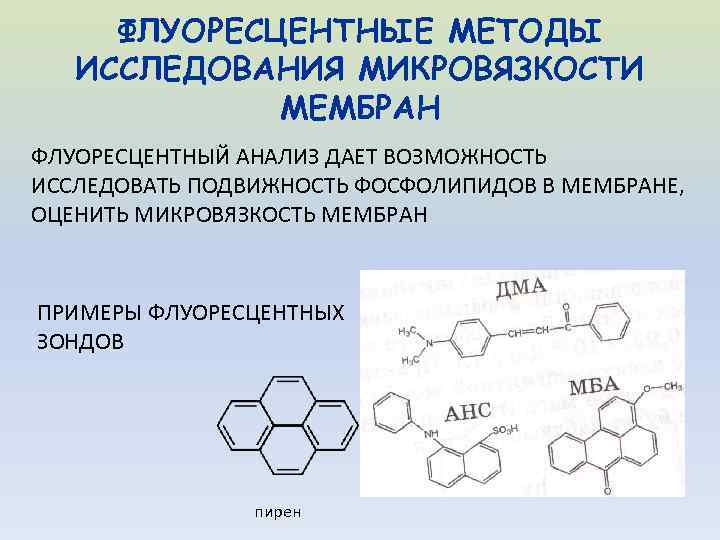
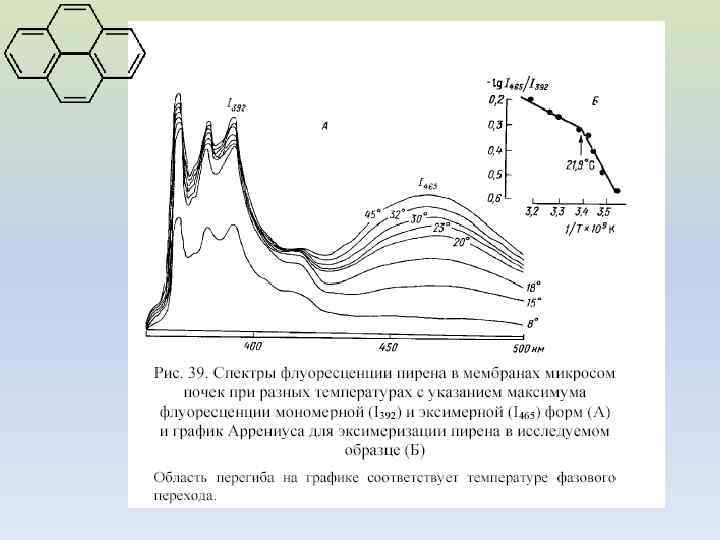
ФЛУОРЕСЦЕНТНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ МИКРОВЯЗКОСТИ МЕМБРАН ФЛУОРЕСЦЕНТНЫЙ АНАЛИЗ ДАЕТ ВОЗМОЖНОСТЬ ИССЛЕДОВАТЬ ПОДВИЖНОСТЬ ФОСФОЛИПИДОВ В МЕМБРАНЕ, ОЦЕНИТЬ МИКРОВЯЗКОСТЬ МЕМБРАН ПРИМЕРЫ ФЛУОРЕСЦЕНТНЫХ ЗОНДОВ пирен
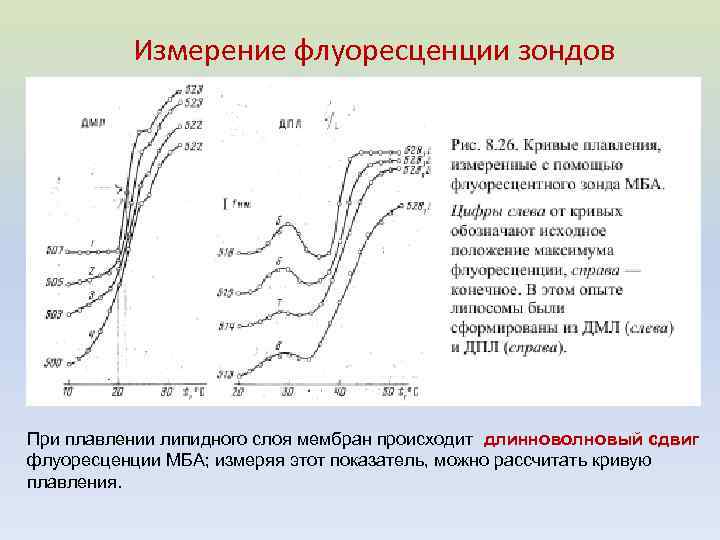
Измерение флуоресценции зондов При плавлении липидного слоя мембран происходит длинноволновый сдвиг флуоресценции МБА; измеряя этот показатель, можно рассчитать кривую плавления.
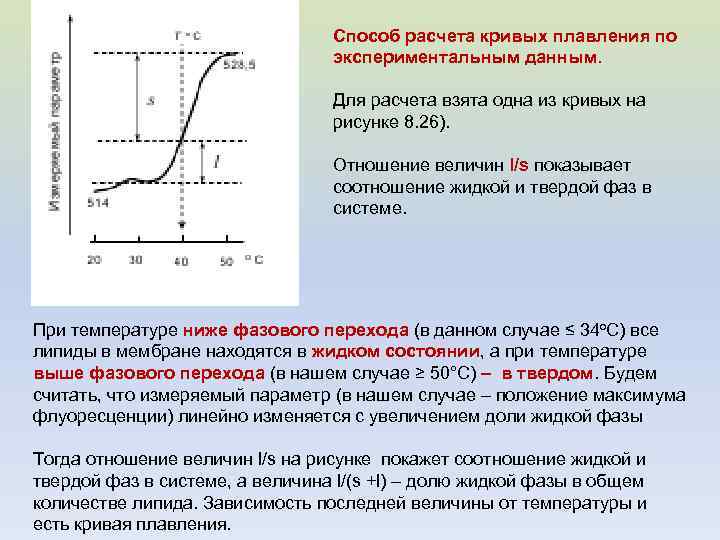
Способ расчета кривых плавления по экспериментальным данным. Для расчета взята одна из кривых на рисунке 8. 26). Отношение величин l/s показывает соотношение жидкой и твердой фаз в системе. При температуре ниже фазового перехода (в данном случае ≤ 34 о. С) все липиды в мембране находятся в жидком состоянии, а при температуре выше фазового перехода (в нашем случае ≥ 50°C) – в твердом. Будем считать, что измеряемый параметр (в нашем случае – положение максимума флуоресценции) линейно изменяется с увеличением доли жидкой фазы Тогда отношение величин l/s на рисунке покажет соотношение жидкой и твердой фаз в системе, а величина l/(s +l) – долю жидкой фазы в общем количестве липида. Зависимость последней величины от температуры и есть кривая плавления.
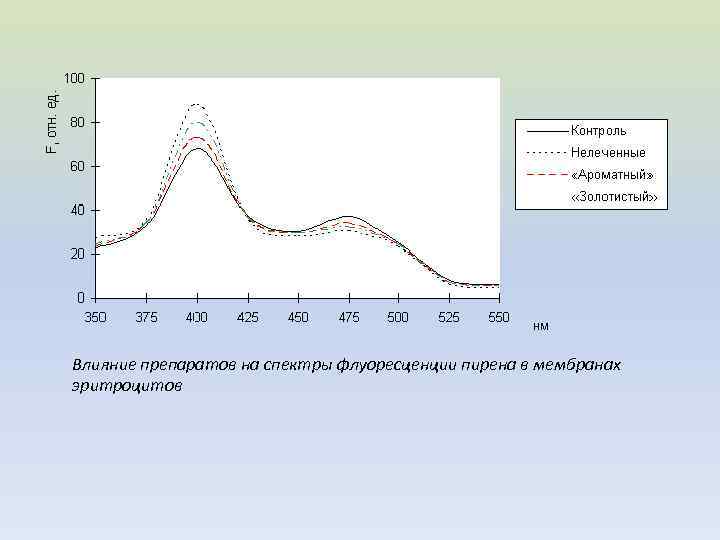
Влияние препаратов на спектры флуоресценции пирена в мембранах эритроцитов

СПИНОВЫЕ ЗОНДЫ Спиновыми зондами называют стабильные радикалы (в которых неспаренный электрон принадлежит практически во всех случаях группе иминоксила >N·=O), которые встраиваются в биомолекулы или в липидный слой мембран без образования ковалентных связей и в этом отношении отличаются от спиновых меток.
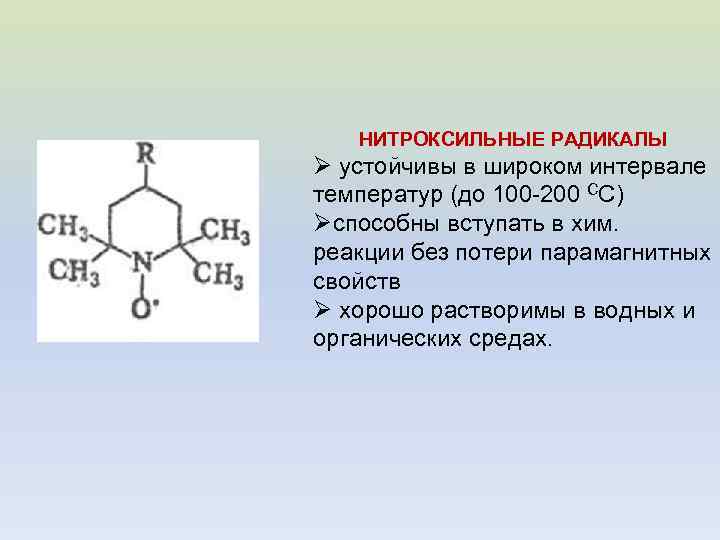
НИТРОКСИЛЬНЫЕ РАДИКАЛЫ Ø устойчивы в широком интервале температур (до 100 -200 СС) Øспособны вступать в хим. реакции без потери парамагнитных свойств Ø хорошо растворимы в водных и органических средах.
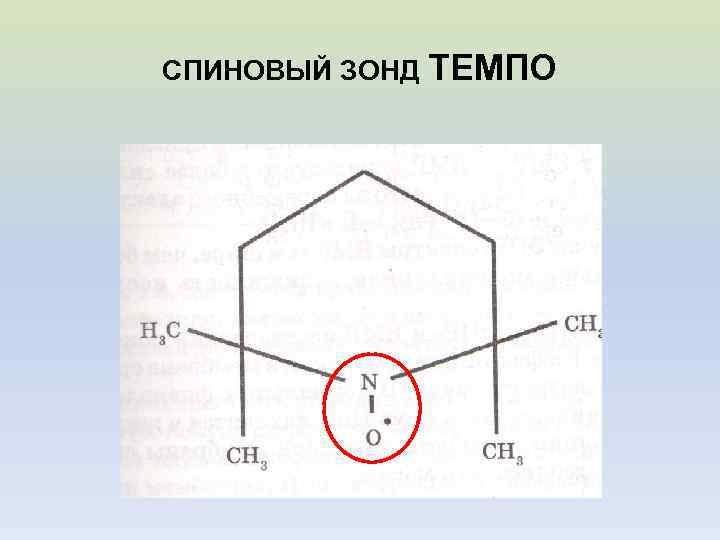
СПИНОВЫЙ ЗОНД ТЕМПО
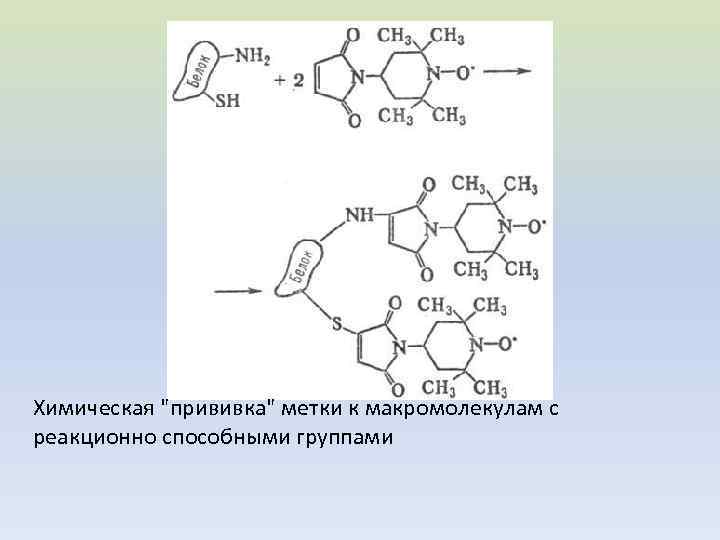
Химическая "прививка" метки к макромолекулам с реакционно способными группами

Реакции макромолекул с бирадикалами и спиновыми ловушками. Спиновая ловушка - соединение, образующее стабильные радикалы при взаимодействии с активными радикалами.

Применение спиновых зондов основано на зависимости спектров ЭПР этих соединений от условий микроокружения в мембране: вязкости, полярности среды и других. Поскольку при фазовом переходе происходит изменение этих свойств (например, микровязкость возрастает при плавлении твердого бислоя), зонды могут применяться также и для изучения кривых плавления.

Характеристики свойств микроокружения: Øинтегральная характеристика вращательной подвижности зонда – время корреляции (обозначаемое обычно как τ); Øхарактеристика асимметрии вращательного движения – параметр упорядоченности (S). Величина τ близка к среднему времени поворота молекулы зонда вокруг любой из осей на угол один радиан.
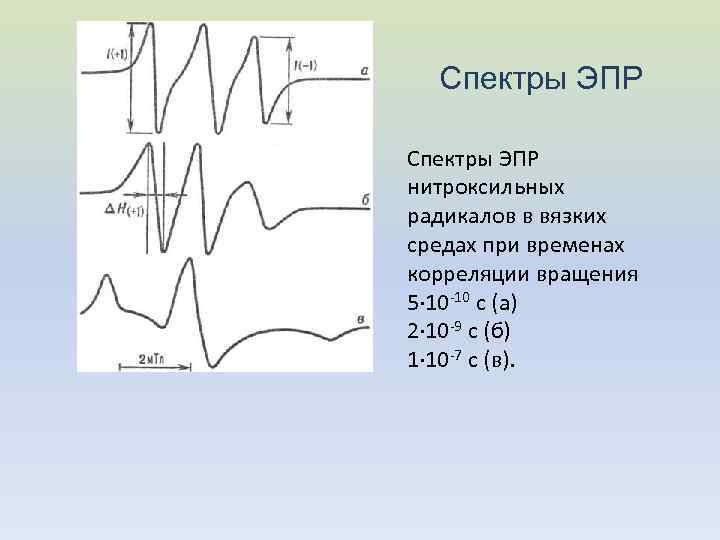
Спектры ЭПР нитроксильных радикалов в вязких средах при временах корреляции вращения 5· 10 -10 с (a) 2· 10 -9 с (б) 1· 10 -7 с (в).
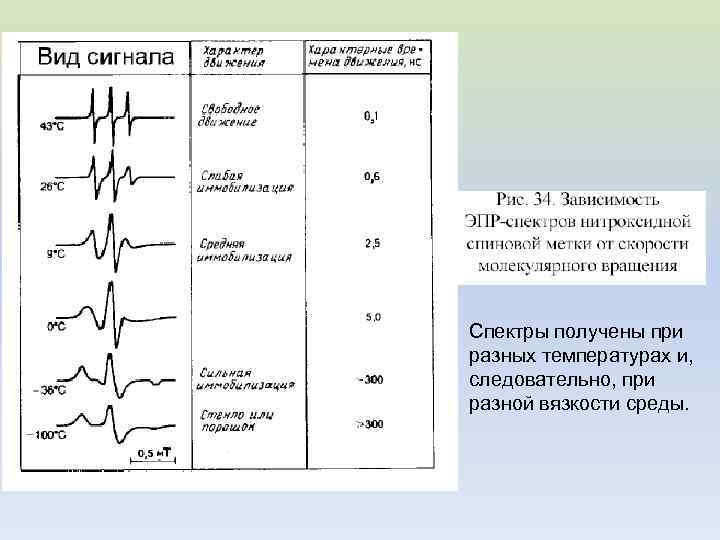
Спектры получены при разных температурах и, следовательно, при разной вязкости среды.
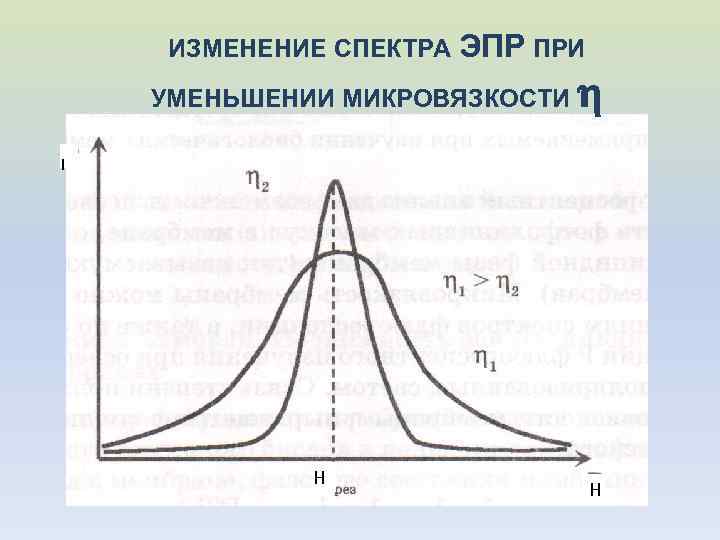
ИЗМЕНЕНИЕ СПЕКТРА ЭПР ПРИ УМЕНЬШЕНИИ МИКРОВЯЗКОСТИ I Н Н
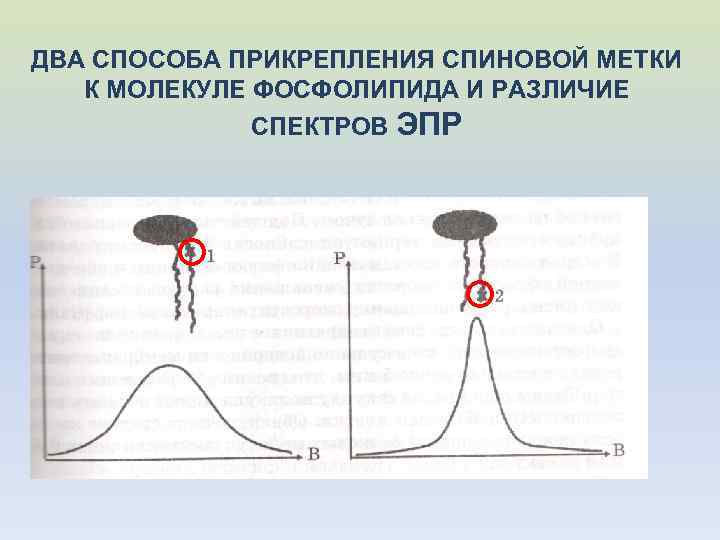
ДВА СПОСОБА ПРИКРЕПЛЕНИЯ СПИНОВОЙ МЕТКИ К МОЛЕКУЛЕ ФОСФОЛИПИДА И РАЗЛИЧИЕ СПЕКТРОВ ЭПР
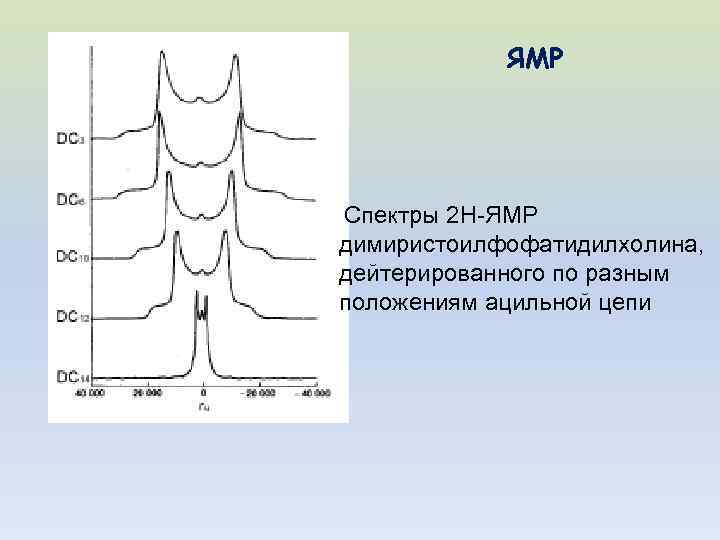
ЯМР Спектры 2 Н-ЯМР димиристоилфофатидилхолина, дейтерированного по разным положениям ацильной цепи

Величины подвижности Т 1 для различных атомов углерода в молекуле фосфатидилхолина в составе мембраны при температуре выше критической (рассчитаны по данным ЯМРспектроскопии)
3липиды мембран 2 часть.ppt