лаб д-ка бакт.ppt
- Количество слайдов: 41

ПРИНЦИПЫ МИКРОБИОЛОГИЧЕСКОЙ ДИАГНОСТИКИ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ

Лабораторная диагностика инфекционных заболеваний основана на обнаружении в организме больного: • микроорганизма, вызвавшего болезнь, • микробных компонентов (антигенов, генетического материала), • продуктов жизнедеятельности (токсинов и др. ), • изменений в показателях гомеостаза под действием этого микроба (например, формулы крови, биохимического состава крови и др. ).

Задачи микробиологических исследований: • идентифицировать микроорганизмы в исследуемом материале, • определить их видовую принадлежность, морфологические, биохимические, токсигенные и антигенные свойства, • установить чувствительность выделенных микроорганизмов к антимикробным препаратам.

Основная цель МД: • Установить факт наличия (отсутствия) возбудителя в организме больного или объекте окружающей среды

Показатели присутствия возбудителя: • Обнаружение микроба, вызвавшего болезнь • микробных компонентов (антигенов и генетической информации) • продуктов их жизнедеятельности (токсинов) • специфических защитных факторов макроорганизма (антител)
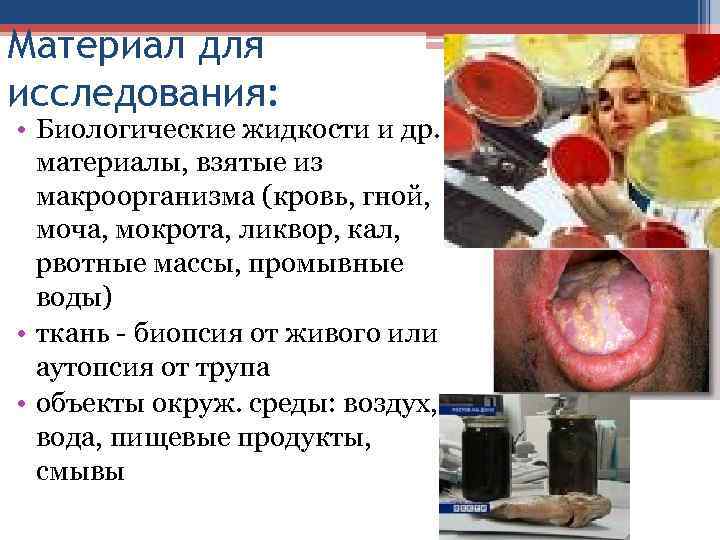
Материал для исследования: • Биологические жидкости и др. материалы, взятые из макроорганизма (кровь, гной, моча, мокрота, ликвор, кал, рвотные массы, промывные воды) • ткань - биопсия от живого или аутопсия от трупа • объекты окруж. среды: воздух, вода, пищевые продукты, смывы

Правила забора материала • Вид материала определяется клинической картиной болезни, т. е. он должен соответствовать предполагаемой локализации возбудителя на данном этапе патогенеза • Количество материала должно быть достаточным для проведения исследований и их повторения • по возможности материал берут в начальном периоде болезни (типичная локализация) • забор материала проводят до антимикробной химиотерапии или после выделения препарата • Материал берут непосредственно из очага инфекции в момент наибольшего содержания в нем возбудителя • Забор проводят в асептических условиях для предупреждения контаминации

Любой клинический материал потенциально опасен • • Правила биологической безопасности: максимально короткие сроки передачи материала для исследований специальные транспортные среды обязательные сопроводительные документы предупреждение попадания в материал антимикробных факторов - дезинфектантов, антибиотиков, антисептиков

В процессе транспортировки • Оберегать от действия света, тепла, холода, механических повреждений в специальных изотермических контейнерах с их последующим обезззараживанием

Методы микробиологической диагностики • Бактериоскопический (микроскопический) • Бактериологический (культуральный) • Биологический • Серологический • Аллергический • Молекулярно-генетический (геноиндикаторный)

Бактериоскопический метод

Используется для предварительного диагноза: • На основании морфологических особенностей: формы, наличия капсул, спор, жгутиков, особенностей строения клеточной стенки, особенностей химического состава, локализации в тканях и т. п. Используют: • разные виды микроскопии • различные виды микроскопических препаратов: «раздавленная капля» и «висячая капля» • мазок, окрашенный простыми и сложными методами
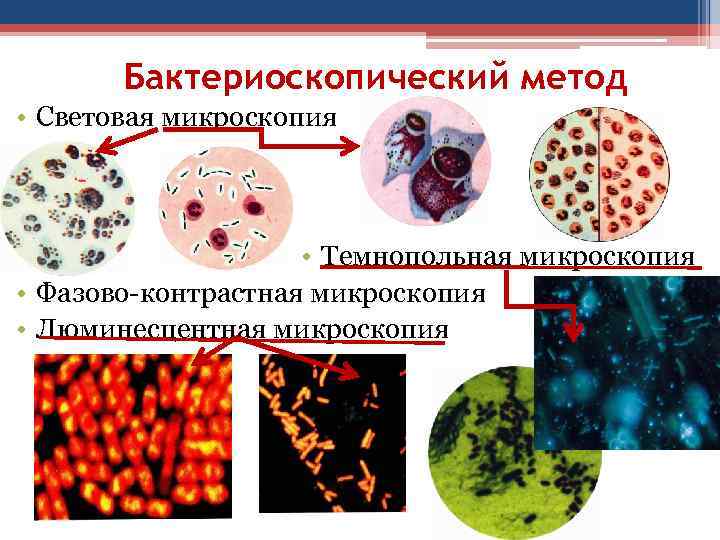
Бактериоскопический метод • Световая микроскопия • Темнопольная микроскопия • Фазово-контрастная микроскопия • Люминесцентная микроскопия
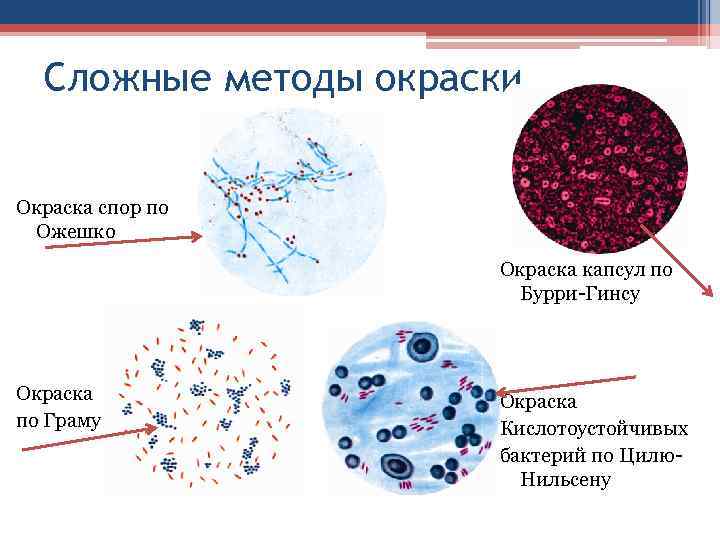
Сложные методы окраски Окраска спор по Ожешко Окраска капсул по Бурри-Гинсу Окраска по Граму Окраска Кислотоустойчивых бактерий по Цилю. Нильсену
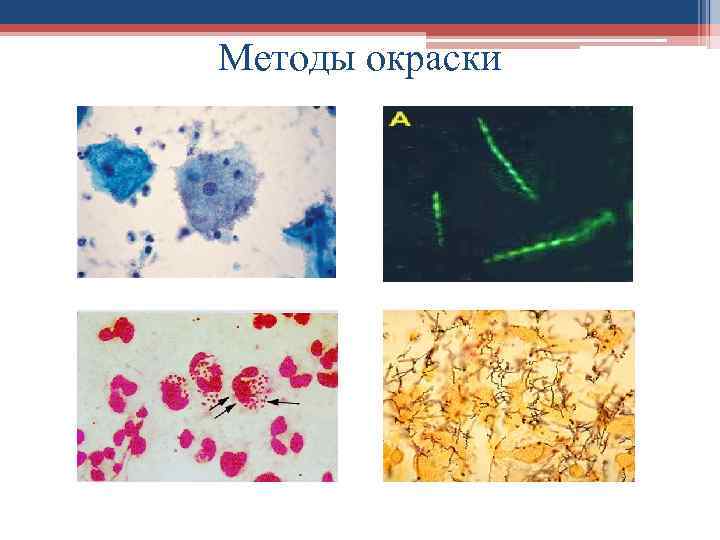
Методы окраски
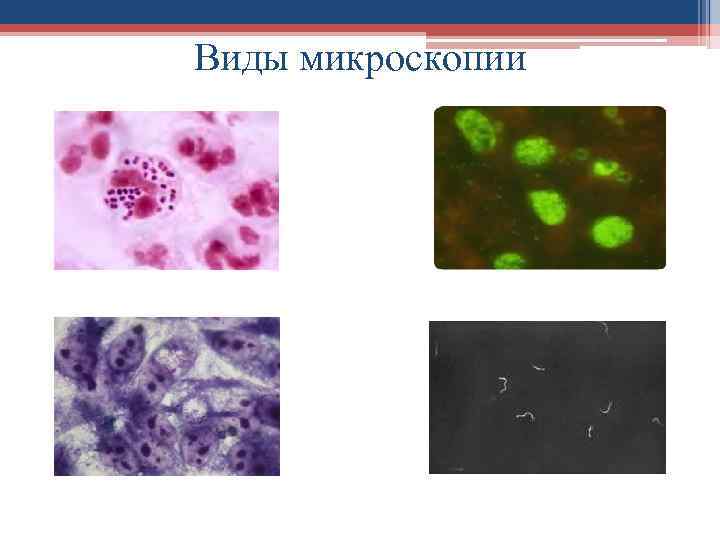
Виды микроскопии

Бактериологический метод

Бактериологический метод «Золотой стандарт прикладной микробиологии» Заключается в выделении чистой культуры возбудителя из клинического материала и его идентификации. Используют стерильные питательные среды (по консистенции -жидкие, плотные, по назначению – универсальные, специальные, элективные, дифференциально-диагностические)

Этапы выделения и идентификации чистых культур бактерий 1 -й день. • Микроскопия исследуемого материала. • Посев исследуемого материала на питательные среды (плотную, жидкую).

2 -й день. • Изучение культуральных свойств. • Пересев колоний на плотные питательные среды для накопления чистой культуры.

3 -й день Идентификация выделенной культуры: • Проверка чистоты выделенной культуры. • Изучение биохимических свойств: сахаролитических, протеолитических. • Изучение фагочувствительности, колициночувствительности, чувствительности к антибиотикам и др. свойств
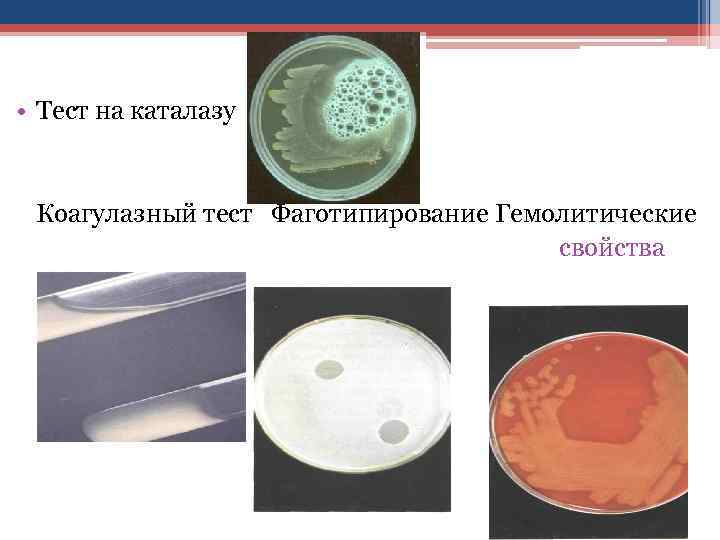
• Тест на каталазу Коагулазный тест Фаготипирование Гемолитические свойства

Биологический метод Заражение исследуемым материалом восприимчивых лабораторных животных в целях лабораторной диагностики с последующей идентификацией по клиническим симптомам и результатам патолого-анатомического вскрытия: • для выделения чистой культуры возбудителя при невозможности использовать искусственные питательные среды (микобактерии лепры – армадиллы, возбудители туляремии – белые мыши) • для ускорения выделения чистой культуры возбудителя по морфологическим признакам (пневмококк образует капсулы в тканях при заражении белых мышей) • Для проведения реакции биологической нейтрализации токсина антитоксической сывороткой при диагностике клостридиозов для определения типа и вида микробного

Выбор экспериментальных животных определяется целью работы. Наиболее часто используют для заражения: • кроликов, • морских свинок, • белых мышей • белых крыс.

Методы заражения Инфекционный материал вводят: • внутрь, • в дыхательные пути, • внутрибрюшинно, • внутривенно, • внутримышечно, • внутрикожно, • подкожно, • в переднюю камеру глаза, • через трепанационное отверстие черепа, • субокципитально (в большую цистерну головного мозга).

СЕРОЛОГИЧЕСКИЙ МЕТОД • Определение специфических антител (иммуноглобулинов) в сыворотке крови больного, • обнаружение микробного антигена в исследуемом материале. • Используют реакции иммунитета.

Основные серологические реакции (классические): • • • Агглютинации Преципитации Лизиса Нейтрализации Их различные модификации

Серологические методы современные • Позволяют поставить микробиологический диагноз в течение короткого промежутка времени (от неск. минут до неск. часов) с момента доставки исследуемого материала в лабораторию. • выявление антигенов возбудителя радиоиммунным (РИА), иммуноферментным (ИФА), иммунофлюоресцентным (РИФ) методами, • выявление антител к взбудителю - РИА, ИФА.
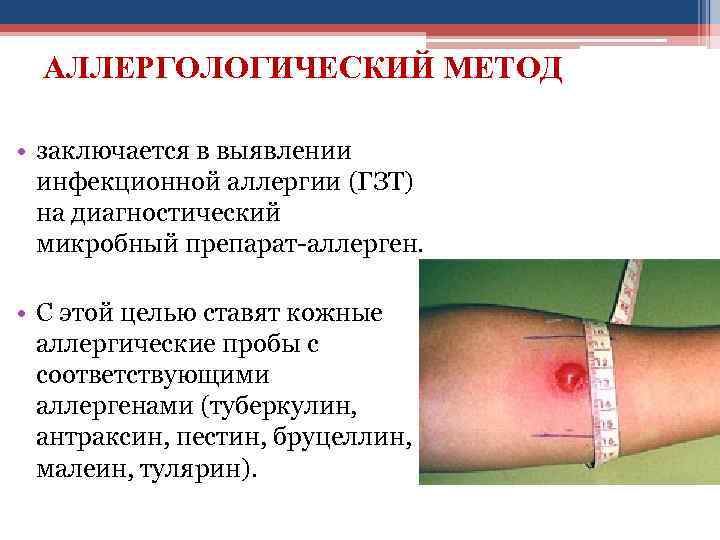
АЛЛЕРГОЛОГИЧЕСКИЙ МЕТОД • заключается в выявлении инфекционной аллергии (ГЗТ) на диагностический микробный препарат-аллерген. • С этой целью ставят кожные аллергические пробы с соответствующими аллергенами (туберкулин, антраксин, пестин, бруцеллин, малеин, тулярин).

Аллергические пробы • 1 группа (in vivo): кожные пробы, осуществляемые непосредственно на больном и выявляющие аллергию немедленного (через 20 мин) и замедленного (через 24 -48 час) типов. • 2 группа (in vitro): аллергические пробы, основанные на изучении процессов сенсибилизации не в организме больного, а в пробирке.

Молекулярно-генетический метод ПОЛИМЕРАЗНАЯ ЦЕПНАЯ РЕАКЦИЯ (ПЦР) Метод основан на выявлении в исследуемом материале ДНК возбудителя Идея ПЦР основана на том, что ген можно размножить в пробирке, увеличивая количество его копий в миллионы раз. Механизм ПЦР заключается в синтезе in vitro коротких нуклеотидных последовательностей для последующего анализа.

Для проведения ПЦР • нужны пара олигонуклеотидов (праймеров), комплементарных исследуемому фрагменту, и фермент ДНК-полимераза. • Праймеры способны распознавать гомологичные последовательности в денатурированной ДНК, связываться с ними и служить затравкой для ферментативного синтеза копий участка изучаемого гена. • Каждый цикл синтеза удваивает число копий фрагментамишени, т. е. количество продукта (амплификата) в процессе ПЦР нарастает в геометрической прогрессии. • 25 -35 циклов реакции дают достаточно амплификата для дальнейшего изучения даже из единичного фрагмента ДНК.

Метод ПЦР (метод полимеразной цепной реакции, PCR, polymerase chain reaction) • является прямым и самым современным методом анализа ДНК. • позволяет специфично увеличивать (копировать амплифицировать) количество исследуемого образца ДНК в десятки и сотни раз. • В течение нескольких часов с помощью ПЦР из одного фрагмента молекулы ДНК можно получить 50 млрд. идентичных молекул. • Такое количество копий фрагмента ДНК становится видимым в ультрафиолете после проведения электрофореза в агарозном геле.

Метод ПЦР теоретически позволяет обнаружить даже 1 копию ДНК в образце, не имея, таким образом, предела чувствительности. Еще одно преимущество ПЦР заключается в том, что для нее характерна не только абсолютная чувствительность, но и абсолютная специфичность. ПЦР не дает ложноположительных результатов, при условии, что метод выполняется правильно.

Метод ПЦР открыл американский химик Кэрри Б. Мюллисом в 1983 году, за что он был удостоен Нобелевской премии. В настоящее время метод получает все большую популярность для диагностики пациентов и имеет ряд преимуществ:

Преимущества метода: • Метод ПЦР направлен на поиск самого возбудителя, а не антител к нему • Метод ПЦР обладает высокой специфичностью – в исследуемом материале выявляется уникальный, характерный только для данного возбудителя фрагмент ДНК • Метод ПЦР обладает наиболее высокой чувствительностью среды известных методов диагностики • Метод ПЦР автоматизирован и позволяет получить результаты анализа в течение одного рабочего дня • Метод ПЦР универсален – одна порция биологического материала позволяет провести исследования на наличие возбудителей целого ряда заболеваний

Оборудование для ПЦР в классическом формате амплификаторы (термоциклеры), оборудование для гельэлектрофореза, системы документации гелей, Электрофорез Термоциклеры Гель-документация

Модификации ПЦР • ЦР в режиме реального времени (real-time PCR) – мониторинг амплификации в процессе исследования • дополнительная амплификация с внутренними праймерами (nested-PCR) – высокая чувствительность при нетипичной локализации возбудителя • ПЦР c обратной транскрипцией (reverse transcriptase PCR, RT-PCR) • множественная ПЦР (multiplex PCR) – одновременное выявление нескольких патогенов.

ПЦР в реальном времени (Real. Time PCR) • Ее принципиальной особенностью является мониторинг и количественный анализ накопления продуктов ПЦР и автоматическая регистрация и интерпретация полученных результатов. ПЦР в реальном времени не требует стадии электрофореза, что позволяет снизить требования, предъявляемые к ПЦР лаборатории.

Оборудование для ПЦР-анализа в режиме реального времени

Место ПЦР в современной лабораторной диагностике инфекций ПЦР-метод является не заменой традиционных морфологических, биохимических или иммунологических методик, но их существенным и необходимым дополнением.
лаб д-ка бакт.ppt