ПРИНЦИП ПАУЛИ.pptx
- Количество слайдов: 68
 «Принцип Паули. Правило Хунда. Правило Клечковского» Капасова Роза Каблгапаровна г. Усть-Каменогорск, 2011
«Принцип Паули. Правило Хунда. Правило Клечковского» Капасова Роза Каблгапаровна г. Усть-Каменогорск, 2011
 Раскрыть физический смысл принципа Паули, правил Хунда и Клечковского для правильного составления электронных формул многоэлектронных атомов химических элементов.
Раскрыть физический смысл принципа Паули, правил Хунда и Клечковского для правильного составления электронных формул многоэлектронных атомов химических элементов.
 электронная формула, графическая конфигурация электронной формулы, спаренные и неспаренные электроны, принцип Паули, правило Хунда, правило Клечковского, формула распределения, формула заполнения, симметрия атома составлять электронные формулы многоэлектронных атомов химических элементов, и интерпретировать полученные результаты с позиций принципа Паули, правила Хунда, правила Клечковского понятийным аппаратом квантовомеханической теории строения многоэлектронных атомов химических элементов
электронная формула, графическая конфигурация электронной формулы, спаренные и неспаренные электроны, принцип Паули, правило Хунда, правило Клечковского, формула распределения, формула заполнения, симметрия атома составлять электронные формулы многоэлектронных атомов химических элементов, и интерпретировать полученные результаты с позиций принципа Паули, правила Хунда, правила Клечковского понятийным аппаратом квантовомеханической теории строения многоэлектронных атомов химических элементов
 онимание физического смысла принципа Паули, правил Хунда и Клечковского для правильного составления электронных формул многоэлектронных атомов химических элементов. онимание основ квантовомеханической теории строения многоэлектронного атома. мение составлять электронные формулы многоэлектронных атомов химических элементов различных семейств, и интерпретировать полученные результаты с позиций квантовой механики Понимание принципиальных отличий в составлении электронных формул многоэлектронных атомов химических элементов различных семейств. Понимание современного состояния и развития теоретической химии.
онимание физического смысла принципа Паули, правил Хунда и Клечковского для правильного составления электронных формул многоэлектронных атомов химических элементов. онимание основ квантовомеханической теории строения многоэлектронного атома. мение составлять электронные формулы многоэлектронных атомов химических элементов различных семейств, и интерпретировать полученные результаты с позиций квантовой механики Понимание принципиальных отличий в составлении электронных формул многоэлектронных атомов химических элементов различных семейств. Понимание современного состояния и развития теоретической химии.
 • • • электронная формула графическая конфигурация электронной формулы спаренные и неспаренные электроны принцип Паули правило Хунда правило Клечковского формула распределения формула заполнения симметрия атома
• • • электронная формула графическая конфигурация электронной формулы спаренные и неспаренные электроны принцип Паули правило Хунда правило Клечковского формула распределения формула заполнения симметрия атома
 Принцип Паули. Правило Хунда. Правило Клечковского План изложения: 1. Принцип минимальной энергии, принцип Паули. Правило Хунда и следствие из него. Правило Клечковского. 2. Формула распределения, формула заполнения. 3. Формулы заполнения (электронные и графические) – элементов І – ІІІ периодов 4. Формулы заполнения (электронные и графические) элементов больших периодов 5. Семейства химических элементов 6. Симметрия атома химического элемента
Принцип Паули. Правило Хунда. Правило Клечковского План изложения: 1. Принцип минимальной энергии, принцип Паули. Правило Хунда и следствие из него. Правило Клечковского. 2. Формула распределения, формула заполнения. 3. Формулы заполнения (электронные и графические) – элементов І – ІІІ периодов 4. Формулы заполнения (электронные и графические) элементов больших периодов 5. Семейства химических элементов 6. Симметрия атома химического элемента
 Многоэлектронные атомы В многоэлектронных атомах электрон движется не только в поле ядра, но и в поле, создаваемом другими электронами. В результате, энергии электронов определяются значениями двух квантовых чисел: n и l. Поэтому энергия уровней (на основании изучения спектров атомов и квантовомеханических расчетов) возрастает с увеличением n и l в ряду 1 s< 2 p< 3 s< 3 p< 4 s~ 3 d< 4 p< 5 s< 4 d< 5 p< 6 s< 4 f< 5 d< 6 p< 7 s< 5 f ~ 6 d< 7 p (принцип минимальной энергии) Состояние электронов в многоэлектронных атомах отвечает квантово-механическому закону или принципу Паули.
Многоэлектронные атомы В многоэлектронных атомах электрон движется не только в поле ядра, но и в поле, создаваемом другими электронами. В результате, энергии электронов определяются значениями двух квантовых чисел: n и l. Поэтому энергия уровней (на основании изучения спектров атомов и квантовомеханических расчетов) возрастает с увеличением n и l в ряду 1 s< 2 p< 3 s< 3 p< 4 s~ 3 d< 4 p< 5 s< 4 d< 5 p< 6 s< 4 f< 5 d< 6 p< 7 s< 5 f ~ 6 d< 7 p (принцип минимальной энергии) Состояние электронов в многоэлектронных атомах отвечает квантово-механическому закону или принципу Паули.
 Принцип Паули Установлено (фундаментальный факт естествознания), что частицы с полуцелым спином (электроны, нейтроны и протоны) описываются антисимметричными волновыми функциями и подчиняются статистике Ферми. Дирака; эти частицы называются фермионами. Частицы с нулевым или целочисленным спином (фотоны, π-мезоны) описываются симметричными волновыми функциями и подчиняются статистике Бозе-Эйнштейна; эти частицы называются бозонами.
Принцип Паули Установлено (фундаментальный факт естествознания), что частицы с полуцелым спином (электроны, нейтроны и протоны) описываются антисимметричными волновыми функциями и подчиняются статистике Ферми. Дирака; эти частицы называются фермионами. Частицы с нулевым или целочисленным спином (фотоны, π-мезоны) описываются симметричными волновыми функциями и подчиняются статистике Бозе-Эйнштейна; эти частицы называются бозонами.
 Принцип Паули Электроны описываются антисимметричными полными волновыми функциями. Это важнейшее положение называют принципом реализации симметрии или принципом Паули. Для системы из N электронов волновая функция атома принимает вид определителя: χα (1)χα (2) …χα (N) где 1 и 2 – координаты электронов; α, ß, χß (1) χß (2)…χß (N) символы квантовых состояний, определя - ………………. емых набором квантовых чисел. Если α и ß χτ (1) …χτ (N) одинаковы, определитель матрицы равен 0, и, следовательно, описываемая им система не существует.
Принцип Паули Электроны описываются антисимметричными полными волновыми функциями. Это важнейшее положение называют принципом реализации симметрии или принципом Паули. Для системы из N электронов волновая функция атома принимает вид определителя: χα (1)χα (2) …χα (N) где 1 и 2 – координаты электронов; α, ß, χß (1) χß (2)…χß (N) символы квантовых состояний, определя - ………………. емых набором квантовых чисел. Если α и ß χτ (1) …χτ (N) одинаковы, определитель матрицы равен 0, и, следовательно, описываемая им система не существует.
 Принцип Паули Из фундаментального факта естествознания , что системы электронов описываются антисимметричными волновыми функциями следует запрет Паули: в многоэлектронной системе (в атоме, молекуле, кристалле) не может быть двух электронов в одинаковом квантовом состоянии, т. е. двух электронов, у которых все четыре квантовых числа совпадают. Принцип Паули ограничивает число электронов в атоме, обладающих определенным значением n.
Принцип Паули Из фундаментального факта естествознания , что системы электронов описываются антисимметричными волновыми функциями следует запрет Паули: в многоэлектронной системе (в атоме, молекуле, кристалле) не может быть двух электронов в одинаковом квантовом состоянии, т. е. двух электронов, у которых все четыре квантовых числа совпадают. Принцип Паули ограничивает число электронов в атоме, обладающих определенным значением n.
 Принцип Паули ПАУЛИ (Pauli), Вольфганг 25 апреля 1890 г. – 15 декабря 1958 г. Нобелевская премия по физике, 1945 г. Из запрета Паули следует, что на одной АО может находиться не более двух электронов с условием, что их спины антипараллельны (ms =+1/2 ms= -1/2): на одной АО электроны характеризуются одинаковыми значениями квантовых чисел n, l, mi и вследствие запрета Паули должны различаться квантовым числом ms.
Принцип Паули ПАУЛИ (Pauli), Вольфганг 25 апреля 1890 г. – 15 декабря 1958 г. Нобелевская премия по физике, 1945 г. Из запрета Паули следует, что на одной АО может находиться не более двух электронов с условием, что их спины антипараллельны (ms =+1/2 ms= -1/2): на одной АО электроны характеризуются одинаковыми значениями квантовых чисел n, l, mi и вследствие запрета Паули должны различаться квантовым числом ms.
 Принцип Паули ПАУЛИ (Pauli), Вольфганг Он подвергал собственные работы такому беспощадному критическому анализу, что его публикации фактически свободны от ошибок. Коллеги называли его «совестью физики» . Кроме Нобелевской премии, Паули был награжден медалью Франклина Франклиновского института (1952) и медалью Макса Планка Германского физического общества (1958).
Принцип Паули ПАУЛИ (Pauli), Вольфганг Он подвергал собственные работы такому беспощадному критическому анализу, что его публикации фактически свободны от ошибок. Коллеги называли его «совестью физики» . Кроме Нобелевской премии, Паули был награжден медалью Франклина Франклиновского института (1952) и медалью Макса Планка Германского физического общества (1958).
 Принцип Паули Принцип запрета Паули играет фундаментальную роль для понимания строения и поведения атомов, атомных ядер, свойств металлов и других физических явлений. Он объясняет химическое взаимодействие элементов и их прежде непонятное расположение в периодической системе. Сам Паули использовал принцип запрета для того, чтобы понять магнитные свойства простых металлов и некоторых газов.
Принцип Паули Принцип запрета Паули играет фундаментальную роль для понимания строения и поведения атомов, атомных ядер, свойств металлов и других физических явлений. Он объясняет химическое взаимодействие элементов и их прежде непонятное расположение в периодической системе. Сам Паули использовал принцип запрета для того, чтобы понять магнитные свойства простых металлов и некоторых газов.
 Принцип Паули • Следствием принципа является наличие электронных оболочек в структуре атома, из чего, в свою очередь, следует разнообразие химических элементов и их соединений. В итоге, все электроны не могут быть в одном квантовом состоянии с наименьшей энергией (для невозбуждённого атома), а заполняют последовательно квантовые состояния с наименьшей суммарной энергией. Подчеркнем, что принцип Паули – следствие антисимметричности волновой функции, и поэтому он справедлив только для фермионов.
Принцип Паули • Следствием принципа является наличие электронных оболочек в структуре атома, из чего, в свою очередь, следует разнообразие химических элементов и их соединений. В итоге, все электроны не могут быть в одном квантовом состоянии с наименьшей энергией (для невозбуждённого атома), а заполняют последовательно квантовые состояния с наименьшей суммарной энергией. Подчеркнем, что принцип Паули – следствие антисимметричности волновой функции, и поэтому он справедлив только для фермионов.
 Электронные конфигурации атомов Фундаментальные условия (принцип наименьшей энергии и принцип Паули) составляют основу принципа построения электронных конфигураций атомов и молекул. Для этого надо определить, сколько всего электронов в разных квантовых состояниях может одновременно находиться в одном слое, в подуровне, на атомной орбитали. Т. е. необходимо определить емкость энергетического уровня.
Электронные конфигурации атомов Фундаментальные условия (принцип наименьшей энергии и принцип Паули) составляют основу принципа построения электронных конфигураций атомов и молекул. Для этого надо определить, сколько всего электронов в разных квантовых состояниях может одновременно находиться в одном слое, в подуровне, на атомной орбитали. Т. е. необходимо определить емкость энергетического уровня.
 Электронные конфигурации атомов Электронной конфигурацией называется распределение электронов атома по различным квантовым состояниям. Согласно принципу наименьшей энергии электрон, присоединяемый к атому, занимает в нем свободный уровень с наименьшей энергией. Если бы не запрет Паули, то все электроны в любом атоме занимали бы уровень 1 s. Но вследствие запрета Паули число электронов, занимающих данный уровень, строго ограничено. Составим таблицу…
Электронные конфигурации атомов Электронной конфигурацией называется распределение электронов атома по различным квантовым состояниям. Согласно принципу наименьшей энергии электрон, присоединяемый к атому, занимает в нем свободный уровень с наименьшей энергией. Если бы не запрет Паули, то все электроны в любом атоме занимали бы уровень 1 s. Но вследствие запрета Паули число электронов, занимающих данный уровень, строго ограничено. Составим таблицу…
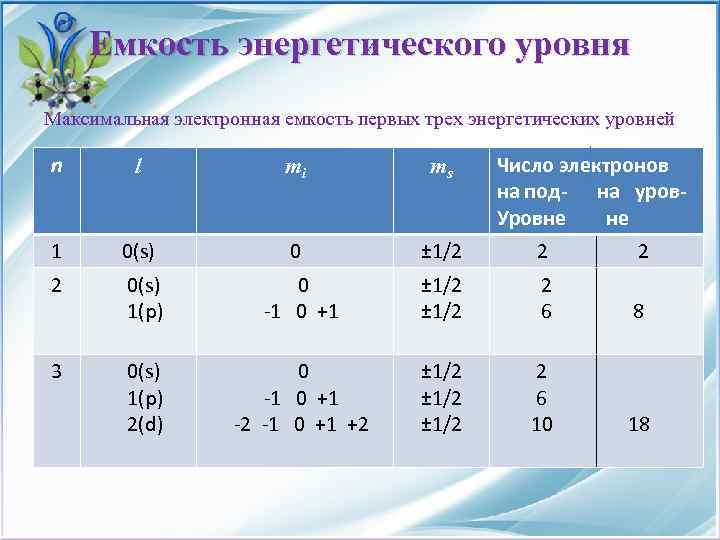 Емкость энергетического уровня Максимальная электронная емкость первых трех энергетических уровней n l mi ms 1 0(s) 0 ± 1/2 2 2 ± 1/2 2 6 8 ± 1/2 6 10 18 2 3 0(s) 1(p) 0 -1 0 +1 0(s) 0 1(p) -1 0 +1 2(d) -2 -1 0 +1 +2 Число электронов на под- на уров. Уровне не
Емкость энергетического уровня Максимальная электронная емкость первых трех энергетических уровней n l mi ms 1 0(s) 0 ± 1/2 2 2 ± 1/2 2 6 8 ± 1/2 6 10 18 2 3 0(s) 1(p) 0 -1 0 +1 0(s) 0 1(p) -1 0 +1 2(d) -2 -1 0 +1 +2 Число электронов на под- на уров. Уровне не
 Емкость энергетического уровня Из таблицы видно, что число орбиталей на данном энергетическом уровне в зависимости от значения n образует арифметическую прогрессию, где первый член a 1= 1, а последний an =2 l+1. Разность прогрессии равна 2, а число членов – n. Сумма Sn прогрессии будет равна: Sn=(a 1+an)·n / 2= (1+2 l+1)·n/2= (l+1)·n, а с учетом l = n-1, Sn=(n-1+1)·n=n 2.
Емкость энергетического уровня Из таблицы видно, что число орбиталей на данном энергетическом уровне в зависимости от значения n образует арифметическую прогрессию, где первый член a 1= 1, а последний an =2 l+1. Разность прогрессии равна 2, а число членов – n. Сумма Sn прогрессии будет равна: Sn=(a 1+an)·n / 2= (1+2 l+1)·n/2= (l+1)·n, а с учетом l = n-1, Sn=(n-1+1)·n=n 2.
 Емкость энергетического уровня Итак, общее число орбиталей на энергетическом уровне со значением главного квантового числа n равно n 2. А так как на одной орбитали может находиться лишь два электрона, получаем, что максимальная электронная емкость энергетического уровня составляет 2 n 2.
Емкость энергетического уровня Итак, общее число орбиталей на энергетическом уровне со значением главного квантового числа n равно n 2. А так как на одной орбитали может находиться лишь два электрона, получаем, что максимальная электронная емкость энергетического уровня составляет 2 n 2.
 Электронные конфигурации атомов 1. На АО, т. е в состоянии с данными квантовыми числами n, l, mi может находиться не более двух электронов: один с ms=+1/2, другой с ms= -1/2. Схематически АО можно изобразить в виде квадрата, а электроны - стрелками ms =+1/2 ms= -1/2 2. Подуровень (подслой, подоболочка) - это совокупность электронов с данными двумя квантовыми числами n, l. Подуровень nl ns np nd nf Число орбиталей 1 3 5 7 Предельное число е 2 6 10 14 Электроны в данном nl подуровне называют эквивалентными, они могут различаться только квантовыми числами mi и ms
Электронные конфигурации атомов 1. На АО, т. е в состоянии с данными квантовыми числами n, l, mi может находиться не более двух электронов: один с ms=+1/2, другой с ms= -1/2. Схематически АО можно изобразить в виде квадрата, а электроны - стрелками ms =+1/2 ms= -1/2 2. Подуровень (подслой, подоболочка) - это совокупность электронов с данными двумя квантовыми числами n, l. Подуровень nl ns np nd nf Число орбиталей 1 3 5 7 Предельное число е 2 6 10 14 Электроны в данном nl подуровне называют эквивалентными, они могут различаться только квантовыми числами mi и ms
 Электронные конфигурации атомов 3. Каждый квантовый слой или квантовый уровень распадается на n подуровней. Максимальное число е- в уровне равно 2 n 2. Подуровни состоят из орбиталей. На каждой орбитали могут находиться максимум два е- с противоположными спинами. Наиболее устойчивым (основным) состоянием атома будет то, когда е- на разных орбиталях имеют параллельные спины, когда они наиболее удалены друг от друга.
Электронные конфигурации атомов 3. Каждый квантовый слой или квантовый уровень распадается на n подуровней. Максимальное число е- в уровне равно 2 n 2. Подуровни состоят из орбиталей. На каждой орбитали могут находиться максимум два е- с противоположными спинами. Наиболее устойчивым (основным) состоянием атома будет то, когда е- на разных орбиталях имеют параллельные спины, когда они наиболее удалены друг от друга.
 Правило Хунда В 1927 г. Хунд сформулировал эмпирические правила, регулирующие порядок заполнения атомных орбиталей электронами (правила Хунда). Ввёл (1931) представления о пи- и сигма-электронах и о пи - и сигма-связях в молекулах. Исследовал закономерности взаимодействия угловых моментов в двухатомных молекулах (случаи Хунда). В 1928 -1932 гг. принимал участие (наряду с Р. С. Малликеном и Дж. Э. Леннард-Джонсом) в разработке основного метода квантовой химии – метода молекулярных орбиталей.
Правило Хунда В 1927 г. Хунд сформулировал эмпирические правила, регулирующие порядок заполнения атомных орбиталей электронами (правила Хунда). Ввёл (1931) представления о пи- и сигма-электронах и о пи - и сигма-связях в молекулах. Исследовал закономерности взаимодействия угловых моментов в двухатомных молекулах (случаи Хунда). В 1928 -1932 гг. принимал участие (наряду с Р. С. Малликеном и Дж. Э. Леннард-Джонсом) в разработке основного метода квантовой химии – метода молекулярных орбиталей.
 Правило Хунда ХУНД (Hund), Фридрих 4 февраля 1896 г. – 31 марта 1986 г. Правило Хунда: при заполнении подуровней и уровней эквивалентными электронами наиболее устойчивым будет состояние с максимальным числом неспаренных е- на вырожденных орбиталях (состояние с максимальным суммарным спином).
Правило Хунда ХУНД (Hund), Фридрих 4 февраля 1896 г. – 31 марта 1986 г. Правило Хунда: при заполнении подуровней и уровней эквивалентными электронами наиболее устойчивым будет состояние с максимальным числом неспаренных е- на вырожденных орбиталях (состояние с максимальным суммарным спином).
 Правило Хунда. Электронно-графическая схема атома азота
Правило Хунда. Электронно-графическая схема атома азота
 Правило Хунда Для запоминания правила Хунда существует мнемоническое «правило трамвайного вагона» : Ты приглядись, решив присесть, К местам трамвайного вагона: Когда ряды пустые есть, Подсаживаться нет резона.
Правило Хунда Для запоминания правила Хунда существует мнемоническое «правило трамвайного вагона» : Ты приглядись, решив присесть, К местам трамвайного вагона: Когда ряды пустые есть, Подсаживаться нет резона.
 Электронные конфигурации атомов Существует определенная форма записи состояния электрона в атоме. Электронная формула (ЭФ) – условная запись строения атома посредством электронных уровней и подуровней. Своего рода шифр: уровень → nlх ← число электронов на подуровне ↑подуровень Например, для основного состояния атома водорода ЭФ имеет вид: уровень → 1 s 1 ← число электронов на подуровне ↑подуровень Это означает, что на первом энергетическом уровне на s подуровне находится 1 электрон. 7 s 1 3 d 4 Существует и другая форма записи распределения электронов по подуровням – с помощью квантовых ячеек.
Электронные конфигурации атомов Существует определенная форма записи состояния электрона в атоме. Электронная формула (ЭФ) – условная запись строения атома посредством электронных уровней и подуровней. Своего рода шифр: уровень → nlх ← число электронов на подуровне ↑подуровень Например, для основного состояния атома водорода ЭФ имеет вид: уровень → 1 s 1 ← число электронов на подуровне ↑подуровень Это означает, что на первом энергетическом уровне на s подуровне находится 1 электрон. 7 s 1 3 d 4 Существует и другая форма записи распределения электронов по подуровням – с помощью квантовых ячеек.
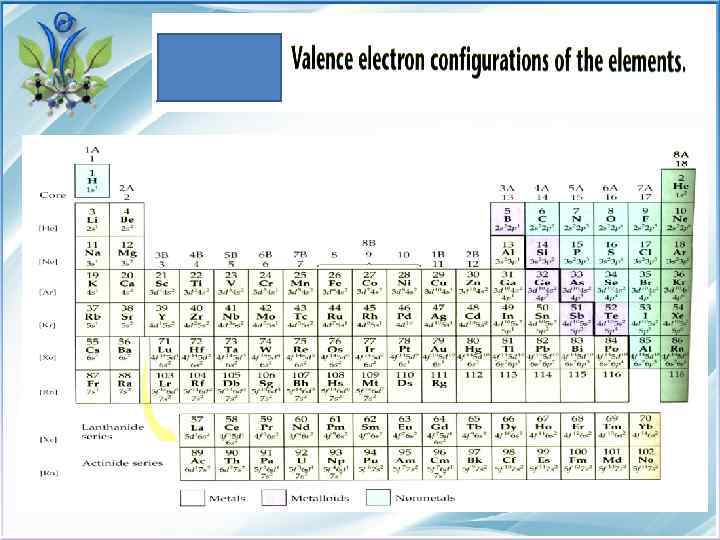
 Электронные конфигурации атомов Из т. видно s-подуровень – 1 квантовая ячейка (2 эл), р- подуровень -3 кв яч d подуровень 5 кв яч f подуровень 7 кв. яч. Максимальная емкость подуровней s-2 е, р-6 е, … Система обозначения в каком порядке и сколько электронов можно поместить на каждый уровень. Н-р: ЭФ атома хлора 17 Cl +17 1 s 22 p 63 s 23 p 5 ЭФ несет определенную информацию. 1. Можно указать валентные электроны. ВЭ – е внешнего уровня и предвнешнего d- подуровня, если он застроен не полностью. Для большинства элементов число ВЭ совпадает с номером группы. Н-р: Технеций в 7 группе, имеет 7 ВЭ d 5 s 2
Электронные конфигурации атомов Из т. видно s-подуровень – 1 квантовая ячейка (2 эл), р- подуровень -3 кв яч d подуровень 5 кв яч f подуровень 7 кв. яч. Максимальная емкость подуровней s-2 е, р-6 е, … Система обозначения в каком порядке и сколько электронов можно поместить на каждый уровень. Н-р: ЭФ атома хлора 17 Cl +17 1 s 22 p 63 s 23 p 5 ЭФ несет определенную информацию. 1. Можно указать валентные электроны. ВЭ – е внешнего уровня и предвнешнего d- подуровня, если он застроен не полностью. Для большинства элементов число ВЭ совпадает с номером группы. Н-р: Технеций в 7 группе, имеет 7 ВЭ d 5 s 2
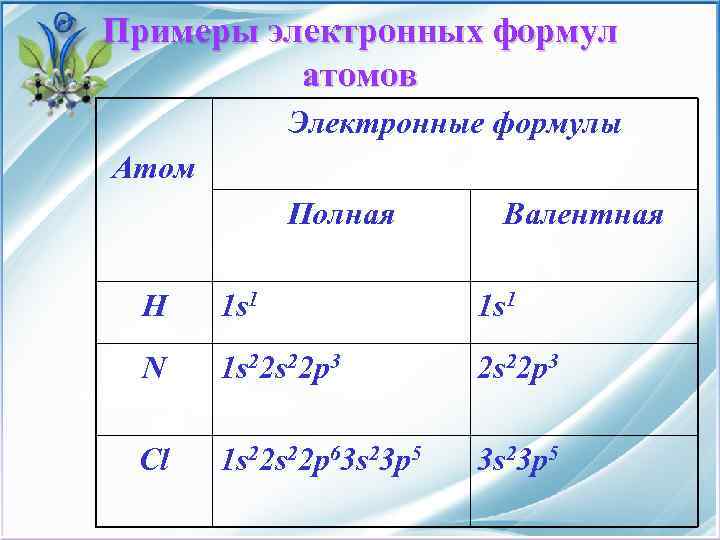 Примеры электронных формул атомов Электронные формулы Атом Полная Валентная H 1 s 1 N 1 s 22 p 3 2 s 22 p 3 Cl 1 s 22 p 63 s 23 p 5
Примеры электронных формул атомов Электронные формулы Атом Полная Валентная H 1 s 1 N 1 s 22 p 3 2 s 22 p 3 Cl 1 s 22 p 63 s 23 p 5
 Электронные конфигурации атомов Второй вывод из ЭФ – спинвалентность элемента. Спинвалентность – это число одиночных неспаренных валентных электронов атомов данного элемента. Определяется по правилу Хунда: на подуровне д. б. максимальное число неспаренных электронов. Атомы могут находиться в двух состояниях: нормальном и возбужденном. С 1 s 22 p 2 6 С* 1 s 22 s 12 p 3 6 Спинвалентность увеличивается, т. к. атому энергетически выгодно быть многовалентным Ti 4 s 23 d 2 Ti* 4 s 13 d 3 Cпинвалентность равная 4 для титана более характерна.
Электронные конфигурации атомов Второй вывод из ЭФ – спинвалентность элемента. Спинвалентность – это число одиночных неспаренных валентных электронов атомов данного элемента. Определяется по правилу Хунда: на подуровне д. б. максимальное число неспаренных электронов. Атомы могут находиться в двух состояниях: нормальном и возбужденном. С 1 s 22 p 2 6 С* 1 s 22 s 12 p 3 6 Спинвалентность увеличивается, т. к. атому энергетически выгодно быть многовалентным Ti 4 s 23 d 2 Ti* 4 s 13 d 3 Cпинвалентность равная 4 для титана более характерна.
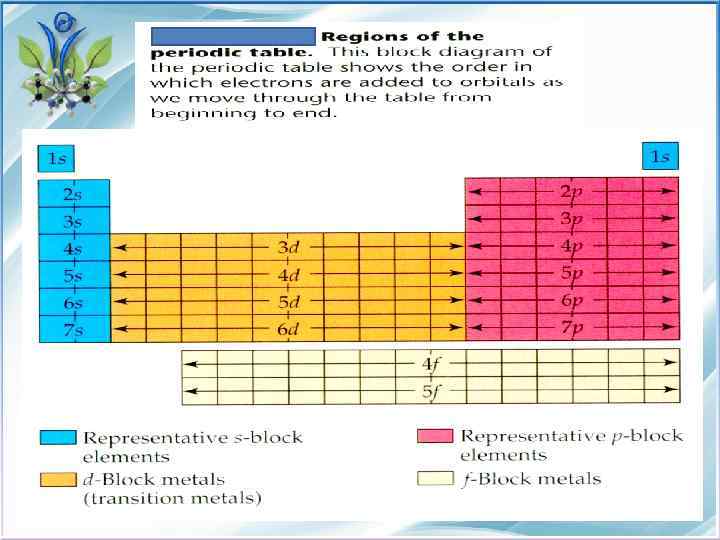
 Электронные конфигурации атомов По конфигурации валентных слоев все элементы делятся на 4 семейства. Тип семества Застраиваемые подуровни Тип эл. конфигурации s внешний ns ns 1 -2 p внешний np ns 2 np 1 -6 d предвнешний (n-1)d 1 -10 ns 1 -2 f третий снаружи(n-2)f 1 -14 (n-1)d 1 -10 ns 2
Электронные конфигурации атомов По конфигурации валентных слоев все элементы делятся на 4 семейства. Тип семества Застраиваемые подуровни Тип эл. конфигурации s внешний ns ns 1 -2 p внешний np ns 2 np 1 -6 d предвнешний (n-1)d 1 -10 ns 1 -2 f третий снаружи(n-2)f 1 -14 (n-1)d 1 -10 ns 2
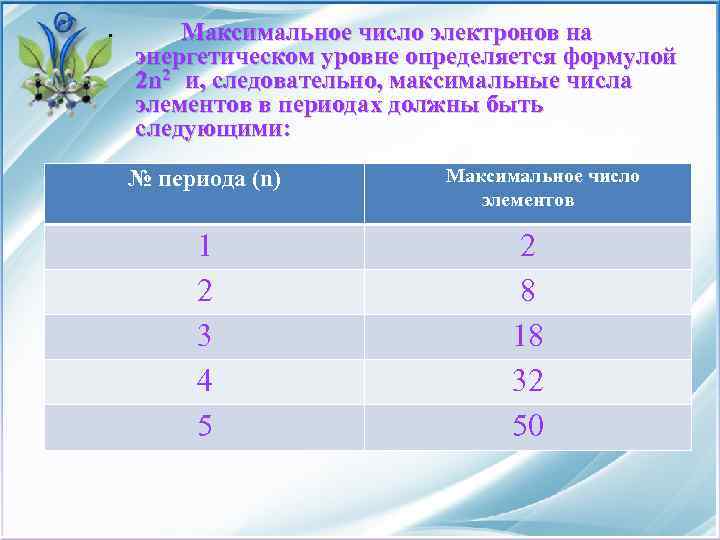 Максимальное число электронов на энергетическом уровне определяется формулой 2 n 2 и, следовательно, максимальные числа элементов в периодах должны быть следующими: Максимальное число № периода (n) элементов • 1 2 3 4 5 2 8 18 32 50
Максимальное число электронов на энергетическом уровне определяется формулой 2 n 2 и, следовательно, максимальные числа элементов в периодах должны быть следующими: Максимальное число № периода (n) элементов • 1 2 3 4 5 2 8 18 32 50
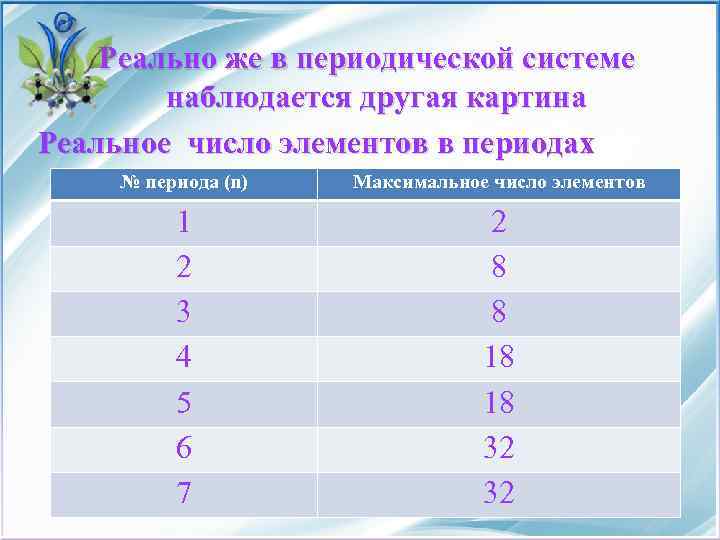 Реально же в периодической системе наблюдается другая картина Реальное число элементов в периодах № периода (n) Максимальное число элементов 1 2 3 4 5 6 7 2 8 8 18 18 32 32
Реально же в периодической системе наблюдается другая картина Реальное число элементов в периодах № периода (n) Максимальное число элементов 1 2 3 4 5 6 7 2 8 8 18 18 32 32
 Принцип наименьшей энергии • Как видно из таблицы, периоды располагаются парами. Исключение составляет только первый период, содержащий всего два элемента, у которых заполняется первый энергетический уровень, состоящий из одного подуровня, и нет внутренних электронов, которые могли бы повлиять на строение внешнего уровня. В остальных же случаях наблюдается следующая картина: строение третьего периода подобно строению второго (и оба содержат по 8 элементов), строение пятого периода подобно строению четвертого ( в обоих по 18 элементов), строение седьмого подобно строению шестого (по 32 элемента).
Принцип наименьшей энергии • Как видно из таблицы, периоды располагаются парами. Исключение составляет только первый период, содержащий всего два элемента, у которых заполняется первый энергетический уровень, состоящий из одного подуровня, и нет внутренних электронов, которые могли бы повлиять на строение внешнего уровня. В остальных же случаях наблюдается следующая картина: строение третьего периода подобно строению второго (и оба содержат по 8 элементов), строение пятого периода подобно строению четвертого ( в обоих по 18 элементов), строение седьмого подобно строению шестого (по 32 элемента).
 Правило Клечковского Значительно лучшее совпадение с действительностью дает распределение электронов по (n+l) - группам, предложенное В. М. Клечковским Клечковский Всеволод Маврикеевич 28. 11. 1900 – 2. 05. 1972 Лауреат Сталинской премии 1952 г Основное направление исследований – применение метода «меченых» атомов в агрохимии. Создал ряд приборов для этой цели
Правило Клечковского Значительно лучшее совпадение с действительностью дает распределение электронов по (n+l) - группам, предложенное В. М. Клечковским Клечковский Всеволод Маврикеевич 28. 11. 1900 – 2. 05. 1972 Лауреат Сталинской премии 1952 г Основное направление исследований – применение метода «меченых» атомов в агрохимии. Создал ряд приборов для этой цели
 Правило Клечковского Правило Клечковского: 1. Заполнение подуровней электронами происходит в последовательности увеличения суммы соответствующих им значений главного и орбитального квантовых чисел (n+l). 2. В случае одинаковых значений этой суммы для нескольких подуровней, заполняется сначала тот подуровень, для которого n имеет наименьшее значение. Рассмотрим конкретное применение этого правила:
Правило Клечковского Правило Клечковского: 1. Заполнение подуровней электронами происходит в последовательности увеличения суммы соответствующих им значений главного и орбитального квантовых чисел (n+l). 2. В случае одинаковых значений этой суммы для нескольких подуровней, заполняется сначала тот подуровень, для которого n имеет наименьшее значение. Рассмотрим конкретное применение этого правила:
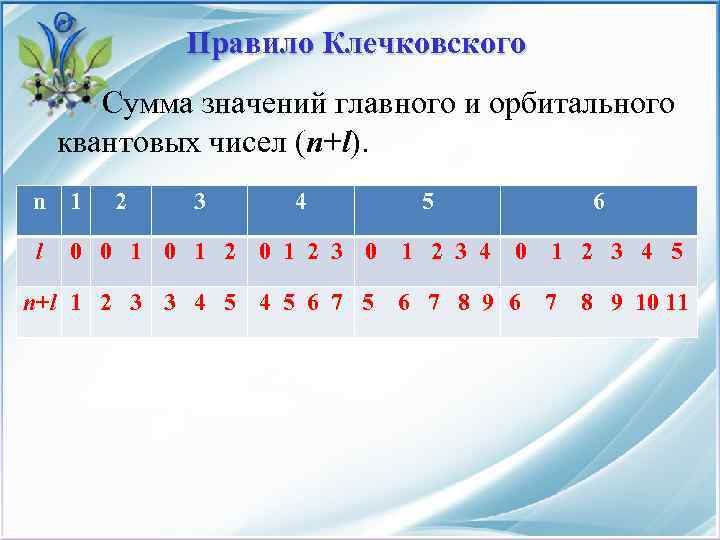 Правило Клечковского Сумма значений главного и орбитального квантовых чисел (n+l). n 1 l 2 3 4 5 0 0 1 2 3 4 6 0 1 2 3 4 5 n+l 1 2 3 3 4 5 6 7 8 9 10 11
Правило Клечковского Сумма значений главного и орбитального квантовых чисел (n+l). n 1 l 2 3 4 5 0 0 1 2 3 4 6 0 1 2 3 4 5 n+l 1 2 3 3 4 5 6 7 8 9 10 11
 Правило Клечковского Для первых двух значений сумм n+l , равных соответственно 1 и 2, нет альтернативных вариантов, и заполнение подуровней происходит в следующей последовательности: 1 s и затем 2 s. Начиная со значения суммы, равной 3, возникает два варианта: заполнять 2 р или 3 s подуровень. В соответствии с правилом Клечковского, выбираем тот подуровень, для которого n имеет меньшее значение, т. е. 2 р- подуровень. Затем заполняется 3 s подуровень.
Правило Клечковского Для первых двух значений сумм n+l , равных соответственно 1 и 2, нет альтернативных вариантов, и заполнение подуровней происходит в следующей последовательности: 1 s и затем 2 s. Начиная со значения суммы, равной 3, возникает два варианта: заполнять 2 р или 3 s подуровень. В соответствии с правилом Клечковского, выбираем тот подуровень, для которого n имеет меньшее значение, т. е. 2 р- подуровень. Затем заполняется 3 s подуровень.
 Правило Клечковского Далее значение n+l =4. Таких значений опять два: для 3 р и для 4 s – подуровней. Сначала 3 р-, а затем 4 s-подуровень. 3 dподуровень остается свободным, т. к. сумма n+l для него больше, чем для 4 s.
Правило Клечковского Далее значение n+l =4. Таких значений опять два: для 3 р и для 4 s – подуровней. Сначала 3 р-, а затем 4 s-подуровень. 3 dподуровень остается свободным, т. к. сумма n+l для него больше, чем для 4 s.
 Правило Клечковского Применяя правило Клечковского, получим следующую последовательность заполнения энергетических подуровней: 1 s< 2 p< 3 s< 3 p< 4 s~ 3 d< 4 p< 5 s< 4 d< 5 p< 6 s< 4 f< 5 d< 6 p Такое заполнение происходит до определенного момента. Если рассмотреть изменение энергии подуровней с увеличением заряда ядра атома, то можно увидеть, что энергия всех подуровней снижается. Но скорость понижения энергии у разных подуровней неодинакова.
Правило Клечковского Применяя правило Клечковского, получим следующую последовательность заполнения энергетических подуровней: 1 s< 2 p< 3 s< 3 p< 4 s~ 3 d< 4 p< 5 s< 4 d< 5 p< 6 s< 4 f< 5 d< 6 p Такое заполнение происходит до определенного момента. Если рассмотреть изменение энергии подуровней с увеличением заряда ядра атома, то можно увидеть, что энергия всех подуровней снижается. Но скорость понижения энергии у разных подуровней неодинакова.
 Правило Клечковского Поэтому, если до кальция 3 dподуровень был по энергии выше 4 s, то начиная со скандия и последующих элементов, его энергия снижается, что видно по иону железа Fe 2+ (1 s 22 p 63 s 23 p 63 d 6). Из электронного строения иона видно, что два валентных электрона железа ушли с менее энергетически выгодного 4 sподуровня. Аналогичная инверсия энергий наблюдается у 5 s и 4 f, а также у 6 s и 5 f – подуровней.
Правило Клечковского Поэтому, если до кальция 3 dподуровень был по энергии выше 4 s, то начиная со скандия и последующих элементов, его энергия снижается, что видно по иону железа Fe 2+ (1 s 22 p 63 s 23 p 63 d 6). Из электронного строения иона видно, что два валентных электрона железа ушли с менее энергетически выгодного 4 sподуровня. Аналогичная инверсия энергий наблюдается у 5 s и 4 f, а также у 6 s и 5 f – подуровней.
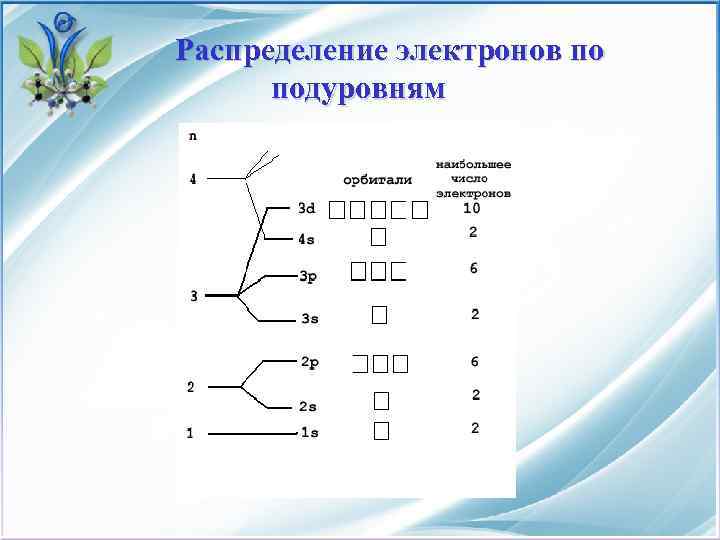 Распределение электронов по подуровням
Распределение электронов по подуровням
 Распределение электронов по подуровням Такое проникновение s – электрона служит настолько существенным фактором для энергетически выгодного упрочнения связи наружного 4 s-электрона с ядром, что s - электронная вакансия в ряде случаев побеждает в конкуренции за связь с ядром d- вакансию, ожидающую своего очередного заселения и превентивно (внеочередным образом) заселяется (4 s-вакансии заселяются до 3 d). Щукарев С. А. назвал s – электроны превенторами, а р – электроны, пунктуалами.
Распределение электронов по подуровням Такое проникновение s – электрона служит настолько существенным фактором для энергетически выгодного упрочнения связи наружного 4 s-электрона с ядром, что s - электронная вакансия в ряде случаев побеждает в конкуренции за связь с ядром d- вакансию, ожидающую своего очередного заселения и превентивно (внеочередным образом) заселяется (4 s-вакансии заселяются до 3 d). Щукарев С. А. назвал s – электроны превенторами, а р – электроны, пунктуалами.
 Распределение электронов по подуровням Сергей Александрович Щукарев (27 июля 1893, Санкт-Петербург — 31 марта 1984 Основное место в трудах занимает развитие и разработка фундаментальных научных проблем, связанных с периодическим законом Д. И. Менделеева, синтеза двух важнейших линий развития химии — периодического закона и химической термодинамики.
Распределение электронов по подуровням Сергей Александрович Щукарев (27 июля 1893, Санкт-Петербург — 31 марта 1984 Основное место в трудах занимает развитие и разработка фундаментальных научных проблем, связанных с периодическим законом Д. И. Менделеева, синтеза двух важнейших линий развития химии — периодического закона и химической термодинамики.
 Правило Клечковского В дальнейшем было установлено, что ПОЛНОСТЬЮ И НАПОЛОВИНУ ЗАПОЛНЕННЫЕ ПОДУРОВНИ ОБЛАДАЮТ ПОВЫШЕННОЙ УСТОЙЧИВОСТЬЮ. Для d - подуровня устойчивыми электронными конфигурациями являются d 10 и d 5, а для f - подуровня – соответственно f 14 и f 7. Этим объясняются аномалии в строении внешних энергетических уровней некоторых элементов.
Правило Клечковского В дальнейшем было установлено, что ПОЛНОСТЬЮ И НАПОЛОВИНУ ЗАПОЛНЕННЫЕ ПОДУРОВНИ ОБЛАДАЮТ ПОВЫШЕННОЙ УСТОЙЧИВОСТЬЮ. Для d - подуровня устойчивыми электронными конфигурациями являются d 10 и d 5, а для f - подуровня – соответственно f 14 и f 7. Этим объясняются аномалии в строении внешних энергетических уровней некоторых элементов.
 Правило Клечковского Например, у хрома валентные уровни теоретически должны иметь конфигурацию 3 d 4 4 s 2, а реально - 3 d 54 s 1; у меди должно быть 3 d 9 4 s 2, а на самом деле, 3 d 104 s 1. Аналогичные переходы электронов с s - подуровня на d наблюдаются у молибдена, золота, а также у f – элементов. Есть аномалии в строении внешних энергетических уровней, в основном, у актиноидов.
Правило Клечковского Например, у хрома валентные уровни теоретически должны иметь конфигурацию 3 d 4 4 s 2, а реально - 3 d 54 s 1; у меди должно быть 3 d 9 4 s 2, а на самом деле, 3 d 104 s 1. Аналогичные переходы электронов с s - подуровня на d наблюдаются у молибдена, золота, а также у f – элементов. Есть аномалии в строении внешних энергетических уровней, в основном, у актиноидов.
 Выводы: 1. Заполнение энергетических подуровней атомов электронами в невозбужденном состоянии подчиняется трем правилам: - принципу Паули; - правилу Хунда; - принципу наименьшей энергии (правилу Клечковского).
Выводы: 1. Заполнение энергетических подуровней атомов электронами в невозбужденном состоянии подчиняется трем правилам: - принципу Паули; - правилу Хунда; - принципу наименьшей энергии (правилу Клечковского).
 Решение задач • Задача 1. Могут ли электроны иона Rb+ находиться на следующих орбиталях: а) 4 р; б) 3 f; в)5 s; г) 5 р? Решение. Электронная конфигурация атома рубидия: 1 s 22 p 63 s 23 p 6 4 s 23 d 102 p 64 p 6 5 s 1. Ион Rb+ образуется при удалении одного валентного электрона из атома рубидия и имеет электронную конфигурацию 1 s 22 p 63 s 23 p 6 4 s 23 d 102 p 64 p 6 5 s 0.
Решение задач • Задача 1. Могут ли электроны иона Rb+ находиться на следующих орбиталях: а) 4 р; б) 3 f; в)5 s; г) 5 р? Решение. Электронная конфигурация атома рубидия: 1 s 22 p 63 s 23 p 6 4 s 23 d 102 p 64 p 6 5 s 1. Ион Rb+ образуется при удалении одного валентного электрона из атома рубидия и имеет электронную конфигурацию 1 s 22 p 63 s 23 p 6 4 s 23 d 102 p 64 p 6 5 s 0.
 Значит, ни на 5 р, ни на 5 s – орбиталях невозбужденного иона Rb+ электронов нет. Однако, электроны могут переходить на эти орбитали при возбуждении атома. Изобразим предпоследний уровень (n=4) 4 s 24 p 64 d 04 f 0. На нем находится 8 электронов, как и у любого s – элемента главной подгруппы І или ІІ группы Периодической таблицы, у которого заполняется s – подуровень. Почему 4 d и 4 f – пустые?
Значит, ни на 5 р, ни на 5 s – орбиталях невозбужденного иона Rb+ электронов нет. Однако, электроны могут переходить на эти орбитали при возбуждении атома. Изобразим предпоследний уровень (n=4) 4 s 24 p 64 d 04 f 0. На нем находится 8 электронов, как и у любого s – элемента главной подгруппы І или ІІ группы Периодической таблицы, у которого заполняется s – подуровень. Почему 4 d и 4 f – пустые?
 Дело в том, что энергия 4 d – подуровня выше, чем 5 s, a 4 f – даже выше, чем 6 s, а сначала заполняются подуровни с меньшей энергией (правило Клечковского). Итак, электроны Rb+ могут находиться на 4 р – орбиталях. Осталось выяснить, могут ли они находиться на 3 f – орбиталях. При n = 3 орбитальное квантовое число l принимает значения 0, 1, 2, которые соответствуют s, p, d – подуровням. А 3 f – подуровня попросту не существует.
Дело в том, что энергия 4 d – подуровня выше, чем 5 s, a 4 f – даже выше, чем 6 s, а сначала заполняются подуровни с меньшей энергией (правило Клечковского). Итак, электроны Rb+ могут находиться на 4 р – орбиталях. Осталось выяснить, могут ли они находиться на 3 f – орбиталях. При n = 3 орбитальное квантовое число l принимает значения 0, 1, 2, которые соответствуют s, p, d – подуровням. А 3 f – подуровня попросту не существует.
 Решение задач Задача 2. Сколько элементов было бы в V периоде, если бы спиновое квантовое число имело единственное значение – 1. Решение: В реальности спиновое квантовое число принимает два значения ± 1/2. Если же оно имело бы единственное значение, то электронная оболочка могла бы вместить вдвое меньшее число электронов (принцип Паули), следовательно, элементов в периоде было бы в 2 раза меньше.
Решение задач Задача 2. Сколько элементов было бы в V периоде, если бы спиновое квантовое число имело единственное значение – 1. Решение: В реальности спиновое квантовое число принимает два значения ± 1/2. Если же оно имело бы единственное значение, то электронная оболочка могла бы вместить вдвое меньшее число электронов (принцип Паули), следовательно, элементов в периоде было бы в 2 раза меньше.
 Решение задач Задача 3. Какие квантовые числа и как должны, по вашему мнению, измениться, при переходе от нашего мира к 1) одномерному; 2) пятимерному?
Решение задач Задача 3. Какие квантовые числа и как должны, по вашему мнению, измениться, при переходе от нашего мира к 1) одномерному; 2) пятимерному?
 Orbital Diagrams and Electron configuration Task: draw the orbital diagram for the electron configuration of oxygen, atomic number 8. How many unpaired electrons does an oxygen atom possess? Analyze and plan. Because oxygen has an atomic number of 8, each oxygen atom has 8 electrons. Figure below shows it.
Orbital Diagrams and Electron configuration Task: draw the orbital diagram for the electron configuration of oxygen, atomic number 8. How many unpaired electrons does an oxygen atom possess? Analyze and plan. Because oxygen has an atomic number of 8, each oxygen atom has 8 electrons. Figure below shows it.
 Orbital Diagrams and Electron configuration The electrons( represented as arrows) are placed in the orbital's (represented as boxes) beginning with lowest-energy orbital, the 1 s. Each orbital can hold a maximum of two electrons( the Pauli exclusion principle). Because the 2 p orbital's are degenerate, we place one electron in each of these orbital's( spin-up) before pairing any electrons( Hund”s rule).
Orbital Diagrams and Electron configuration The electrons( represented as arrows) are placed in the orbital's (represented as boxes) beginning with lowest-energy orbital, the 1 s. Each orbital can hold a maximum of two electrons( the Pauli exclusion principle). Because the 2 p orbital's are degenerate, we place one electron in each of these orbital's( spin-up) before pairing any electrons( Hund”s rule).
 Orbital Diagrams and Electron configuration Solve: Two electrons each go into the 1 s and 2 s orbital's with their spin paired. This leaves 4 electrons for the three generate 2 p orbitals. Following Hund”s rule we put one electron into each 2 p orbital until all three orbital's have one electron each. The fourth electron is then paired up with one of the three electrons already in 2 p orbital, so that is the representation-
Orbital Diagrams and Electron configuration Solve: Two electrons each go into the 1 s and 2 s orbital's with their spin paired. This leaves 4 electrons for the three generate 2 p orbitals. Following Hund”s rule we put one electron into each 2 p orbital until all three orbital's have one electron each. The fourth electron is then paired up with one of the three electrons already in 2 p orbital, so that is the representation-
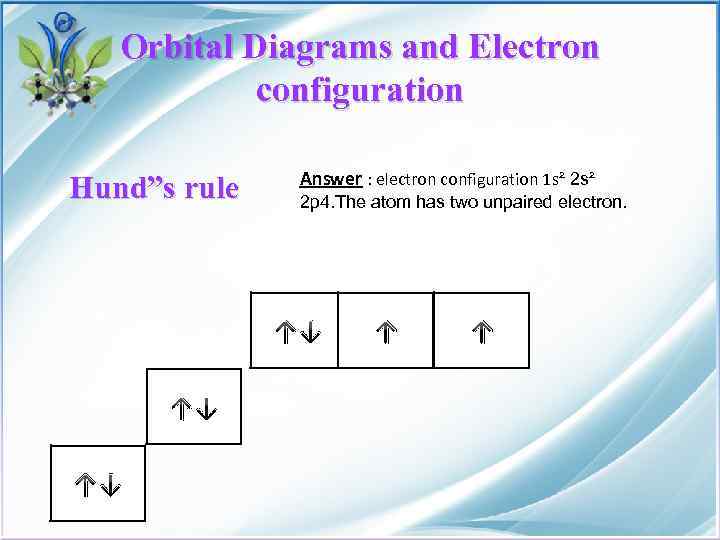 Orbital Diagrams and Electron configuration Hund”s rule Answer : electron configuration 1 s² 2 p 4. The atom has two unpaired electron. ↑↓ ↑↓ ↑↓ ↑ ↑
Orbital Diagrams and Electron configuration Hund”s rule Answer : electron configuration 1 s² 2 p 4. The atom has two unpaired electron. ↑↓ ↑↓ ↑↓ ↑ ↑
 Subshells of the Hydrogen Atom Task: Predict the number of subshells in the fourth shell, that is, for n=4. Give the label for each of these subshells. How many orbitals are in each of these subshells.
Subshells of the Hydrogen Atom Task: Predict the number of subshells in the fourth shell, that is, for n=4. Give the label for each of these subshells. How many orbitals are in each of these subshells.
 Subshells of the Hydrogen Atom Task: Predict the number of subshells in the fourth shell, that is, for n=4. Give the label for each of these subshells. How many orbitals are in each of these subshells.
Subshells of the Hydrogen Atom Task: Predict the number of subshells in the fourth shell, that is, for n=4. Give the label for each of these subshells. How many orbitals are in each of these subshells.
 Solution There are 4 subshells in the fourth shell, corresponding to the four possible values of L(0, 1, 2, 3). These subshells are labeled 4 s, 4 p, 4 d, 4 f. The number given in the designation of subshells is the principal quantum number –n: the letter designates the value of the angular momentum quantum number-l, for l=0, s; for l=1; p; l=2; d; l=3; f. These is one 4 s orbital(when l=0), these is only one possible value of m(i). There are three 4 p orbital(when l=1, there are three possible values of m(i)1, 0, (-1). There are five 4 d orbitals (when l=2, there are five allowed values of m(i)2, 1, 0 -1, -2, ) There ear seven 4 f orbitals(when l=3, there are seven permitted values of m(i)3, 2, 1, 0, -1, -2, -3) Practice exercise What is the designation for the subshells with n=5 and 1. How many orbitals are in this subshells? Indicate the values of m(i) for each of these orbitals.
Solution There are 4 subshells in the fourth shell, corresponding to the four possible values of L(0, 1, 2, 3). These subshells are labeled 4 s, 4 p, 4 d, 4 f. The number given in the designation of subshells is the principal quantum number –n: the letter designates the value of the angular momentum quantum number-l, for l=0, s; for l=1; p; l=2; d; l=3; f. These is one 4 s orbital(when l=0), these is only one possible value of m(i). There are three 4 p orbital(when l=1, there are three possible values of m(i)1, 0, (-1). There are five 4 d orbitals (when l=2, there are five allowed values of m(i)2, 1, 0 -1, -2, ) There ear seven 4 f orbitals(when l=3, there are seven permitted values of m(i)3, 2, 1, 0, -1, -2, -3) Practice exercise What is the designation for the subshells with n=5 and 1. How many orbitals are in this subshells? Indicate the values of m(i) for each of these orbitals.
 Задачи на самостоятельное решение • Задача 1. Напишите электронные конфигурации следующих элементов: N, Si, Fе, Кr, Те, W. Задача 2. Могут ли электроны иона Аl 3+ находиться на следующих орбиталях: а) 2 р; б) 1 р; в) 3 d? Задача 3. Какой инертный газ и ионы каких элементов имеют одинаковую электронную конфигурацию с частицей, возникающей в результате удаления из атома кальция всех валентных электронов? Задача 4. Напишите электронную конфигурацию атома неона в первом возбужденном состоянии.
Задачи на самостоятельное решение • Задача 1. Напишите электронные конфигурации следующих элементов: N, Si, Fе, Кr, Те, W. Задача 2. Могут ли электроны иона Аl 3+ находиться на следующих орбиталях: а) 2 р; б) 1 р; в) 3 d? Задача 3. Какой инертный газ и ионы каких элементов имеют одинаковую электронную конфигурацию с частицей, возникающей в результате удаления из атома кальция всех валентных электронов? Задача 4. Напишите электронную конфигурацию атома неона в первом возбужденном состоянии.
 Нахождение электрона в атоме • Орбиталь - область пространства вокруг ядра атома, где наиболее вероятно нахождение электрона. • На одной орбитали может находиться не более двух электронов.
Нахождение электрона в атоме • Орбиталь - область пространства вокруг ядра атома, где наиболее вероятно нахождение электрона. • На одной орбитали может находиться не более двух электронов.
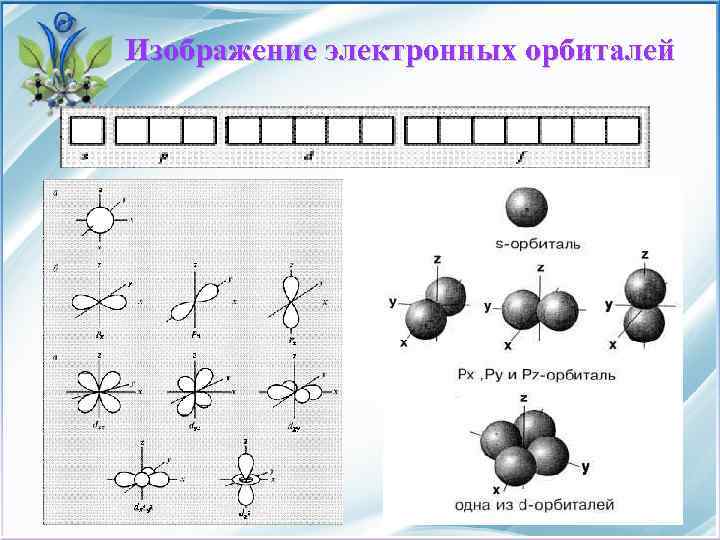 Изображение электронных орбиталей
Изображение электронных орбиталей
 Энергетический уровень (электронный слой) • Энергетический уровень (1, 2, 3…)-характеризует энергию связи электрона с ядром. • На одном уровне располагаются электроны, имеющие орбитали разной формы, но с близким по величине запасом энергии. • Внутри энергетического уровня в зависимости от формы орбиталей различают подуровни (s, p, d, f).
Энергетический уровень (электронный слой) • Энергетический уровень (1, 2, 3…)-характеризует энергию связи электрона с ядром. • На одном уровне располагаются электроны, имеющие орбитали разной формы, но с близким по величине запасом энергии. • Внутри энергетического уровня в зависимости от формы орбиталей различают подуровни (s, p, d, f).
 Контролирующие материалы • Выполните задания из каждого раздела • Проверьте правильность выполнения заданий • Поставьте себе оценку за работу
Контролирующие материалы • Выполните задания из каждого раздела • Проверьте правильность выполнения заданий • Поставьте себе оценку за работу
 Задание 1 Вставьте пропущенные слова: 1. Атом со. Атом - это наименьшая … частица химического элемента. 2. стоит из … и … оболочки. 3. … состоит из протонов и нейтронов. 4. В 1911 г. английский ученый … доказал, что в центре атома имеется … заряженное ядро. 5. В состав атомного ядра входят … и … 6. Число электронов, движущихся вокруг ядра атома, равно … … элемента. 7. Порядковый номер химического элемента совпадает с … … его атома. 8. Электроны, которые обладают наименьшим запасом энергии, находятся на первом … уровне. 9. Число энергетических уровней у элементов определяется по номеру … 10. На одной орбитали может располагаться только …электрона.
Задание 1 Вставьте пропущенные слова: 1. Атом со. Атом - это наименьшая … частица химического элемента. 2. стоит из … и … оболочки. 3. … состоит из протонов и нейтронов. 4. В 1911 г. английский ученый … доказал, что в центре атома имеется … заряженное ядро. 5. В состав атомного ядра входят … и … 6. Число электронов, движущихся вокруг ядра атома, равно … … элемента. 7. Порядковый номер химического элемента совпадает с … … его атома. 8. Электроны, которые обладают наименьшим запасом энергии, находятся на первом … уровне. 9. Число энергетических уровней у элементов определяется по номеру … 10. На одной орбитали может располагаться только …электрона.
 Критерий выставления оценок • „ 5”-все задания выполнены без ошибок или с 1 незначительной ошибкой • „ 4”- задания выполнены с 2 -3 незначительными ошибками • „ 3”- задания вызывают затруднения, выполнены с 4 -5 ошибками • „ 2”- задания не выполнены
Критерий выставления оценок • „ 5”-все задания выполнены без ошибок или с 1 незначительной ошибкой • „ 4”- задания выполнены с 2 -3 незначительными ошибками • „ 3”- задания вызывают затруднения, выполнены с 4 -5 ошибками • „ 2”- задания не выполнены
 Все материалы могут быть найдены на сайте:
Все материалы могут быть найдены на сайте:


