26_Khromatograficheskie_metody.ppt
- Количество слайдов: 54

Применение хроматографии в количественном анализе - Ионообменная хроматография - Газовая хроматография - Высокоэффективная жидкостная хроматография

Ионообменная хроматография В основе лежит обмен ионами между ионообменником и раствором Ионообменник состоит из матрицы, в которой распределены ионогенные группы, включающие прочно связанные с матрицей ионы (ковалентная связь), и менее прочно связанные противоионы (ионная связь) Противоионы могут легко отщепляться от ионита и заменяться одноименным ионом

Катионный обмен Катионит в Н-форме R — SO 3–H+ Катионит в солевой форме + M+ R — SO 3–M+ + H+ матрица ионогенная группа Различают катиониты (катионообменники) и аниониты (анионообменники)

Анионный обмен R—N(CH 3)3+OH– + A– R—N(CH 3)3+ A– + OH– Иониты могут неорганическими, природными или синтетическими Например, матрица синтетического катионита КУ-2 состоит из сополимера стирола и дивинилбензола, сульфогруппа (ионногенная группа) обеспечивает сильнокислотные свойства R — SO 3–H+

Ионообменные смолы имеют соответствующую маркировку: КУ – катионит универсальный, активная группа –SO 3 H КБ – катионит буферный, активная группа –COOH АВ – анионит высокосновный, активная группа –СH 2 N(CH 3)3 Cl АН – анионит низкоосновный, активная группа –NH 3 OH

Обменная ёмкость ионитов (удельная ёмкость) – характеризует способность ионитов к ионному обмену и определяется числом ммоль обмениваемых ионов, приходящихся на 1 г сухого ионита или на 1 мл набухшего ионита (для наиболее распространённых ионитов 2 -10 ммоль/г) Обменная ёмкость ионитов зависит от природы и числа ионогенных групп в ионите, их способности к ионизации, температуры
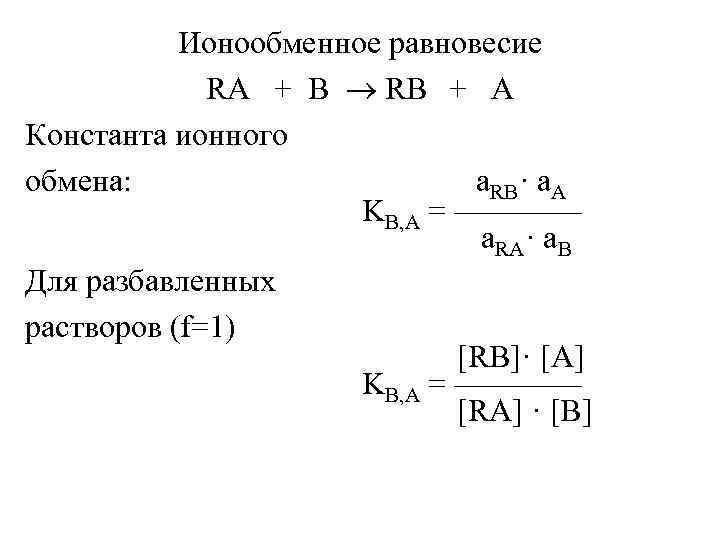
Ионообменное равновесие RA + B RB + A Константа ионного обмена: a. RB· a. A KB, A = ———— a. RA· a. B Для разбавленных растворов (f=1) [RB]· [A] KB, A = ———— [RA] · [B]
![Преобразуя выражение, получим: [RB] [B] —— = KB, A · —— [RA] [A] Отношение Преобразуя выражение, получим: [RB] [B] —— = KB, A · —— [RA] [A] Отношение](https://present5.com/presentation/13978880_167603851/image-8.jpg)
Преобразуя выражение, получим: [RB] [B] —— = KB, A · —— [RA] [A] Отношение равновесных концентраций ионов в фазе сорбента прямо пропорционально отношению равновесных концентраций тех же ионов в растворе
![Графически выражение будет иметь вид: [RB]/[RA] KB, A= tg [B]/[A] Графически выражение будет иметь вид: [RB]/[RA] KB, A= tg [B]/[A]](https://present5.com/presentation/13978880_167603851/image-9.jpg)
Графически выражение будет иметь вид: [RB]/[RA] KB, A= tg [B]/[A]

= 45 o KB, A= 1 – сродство ионов к иониту одинаково, обмена не происходит < 45 o KB, A< 1 – сорбируемость вытесняемого иона выше (равновесие смещено влево) > 45 o KB, A= 1 – сорбируемость иона-вытеснителя больше (равновесие смещено вправо)

Сродство ионов к сорбенту зависит от ряда факторов (заряда иона, поляризуемость и др) Установлены ряды сорбируемости ионов на ионообменниках Иониты характеризуются коэффициетном селективности и коэффициентом распределения

коэффициент селективности (фактор разделения) – характеризует способность ионита к разделению смеси двух ионов, находящихся в растворе Пусть RB + A + C RA + B + C RC + B + A [RB]· [A] KB, A = ———— [RA] · [B] [RC]· [A] KC, A = ———— [RA] · [C]
![Найдем соотношение: KB, A / KC, A KB, A [RB] · [C] —— = Найдем соотношение: KB, A / KC, A KB, A [RB] · [C] —— =](https://present5.com/presentation/13978880_167603851/image-13.jpg)
Найдем соотношение: KB, A / KC, A KB, A [RB] · [C] —— = ———— = В/С KC, A [RC] · [B] В/С – фактор разделения ионов В и С В/С = 1 – разделение ионов не осуществляется

Коэффициент распределения D – характеризует количественно способность ионита к обмену и сорбции ионов D = g 1/g 2 g 1 = n 1/V g 2 = n 2/V n 1 – количество ионов, сорбированное ионитом массой m из раствора объемом V, содержащего при равновесии количество n 2 тех же ионов

Методы ионообменной хроматографии 1. Статический Ионит вводится непосредственно в анализируемый раствор, после поглощения ионитом анализируемого компонента, ионит удаляют из раствора, затем при помощи подходящего растворителя извлекают анализируемый компонент и проводят соответствующий анализ

2. Динамический (элюентная ионообменная хр. ) Ионный обмен проводят в хроматографических колонках Стеклянная трубка с краном в нижней части Стеклянная вата Ионит (промытый водой и выдержанный в растворе HCl несколько часов для набухания) Зеркало (слой жидкости 1 -1, 5 см) В слое иониты не должны находиться пузырьки воздуха

Разделение ионов при их элюировании подвижной фазой осуществляется вследствие неодинакового сродства ионов к сорбенту, различий констант ионного обмена, коэффициентов распределения и связанной с этим разности скоростей перемещения зон, содержащих соответствующие ионы Глубина и скорость ионообменного разделения ионов зависят от природы самих ионов, сорбента, подвижной фазы, температуры, размеров колонки, физического состояния ионита (размер зерен, степень набухания), скорости перемещения подвижной фазы

Элюентная (проявительная) хроматография При элюировании вещества перемещаются вдоль колонки с разными скоростями в соответствии с их сорбируемостью Первым выходит наименее сорбирумый компонент Между зонами компонентов имеются зоны чистого растворителя.

Регенерация ионитов После завершения ионного обмена и разделения ионов, иониты можно регенерировать, т. е. снова перевести в исходное состояние R—SO 3–H+ + M+ R—SO 3–M+ + H+ Промывая солевую форму катионита раствором кислоты регенерируется его H-форма Регенерация позволяет многократно использовать ионообменники для проведения ионного обмена

Применение ионообменной хроматографии 1. Разделения смесей электролитов 2. Очистки растворов электролитов от примесей 3. Концентрирования разбавленных растворов электролитов 4. Количественного определения электролитов

Газовая хроматография Основана на различии в равновесном распределении летучих компонентов смеси между двумя фазами: Газоадсорбционная хроматография (ГАХ) ПФ – газ-носитель НФ – твердый носитель – силикагель, уголь, оксид алюминия (адсорбенты с высокой удельной поверхностью) Распределение веществ между НФ и ПФ определяется процессом адсорбции

Газожидкостная хроматография (ГЖХ) ПФ – газ-носитель НФ – жидкость, нанесенная на поверхность твердого тела (полигликоли, гидроксиламины, насыщенные углеводороды и др) НФ д. б. хорошим растворителем для компонентов смеси, нелетучей, химически инертной, д. обладать небольшой вязкостью и при нанесении на тв. тело образовывать плёнку Для равномерного нанесения жидкую фазу смешивают с легколетучим растворителем и добавляют твердый носитель
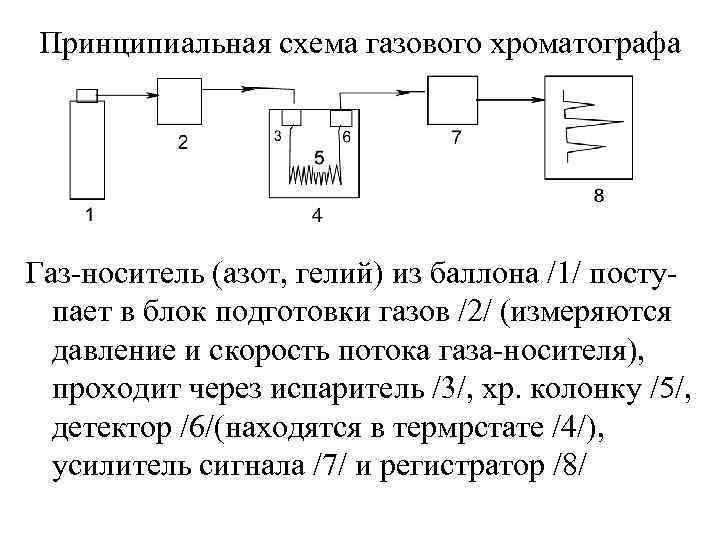
Принципиальная схема газового хроматографа Газ-носитель (азот, гелий) из баллона /1/ поступает в блок подготовки газов /2/ (измеряются давление и скорость потока газа-носителя), проходит через испаритель /3/, хр. колонку /5/, детектор /6/(находятся в термрстате /4/), усилитель сигнала /7/ и регистратор /8/

В испаритель с температурой, достаточной для испарения смеси, с помощью микрошприца вводится проба анализируемого вещества, которая испаряется и потоком газа уносится в хроматографическую колонку После разделения в колонке компонентов на зоны, они проходят детектор, в котором генерируется электрический сигнал Сигнал усиливается усилителем и регистрируется самописцем на бумаге в виде хроматограммы
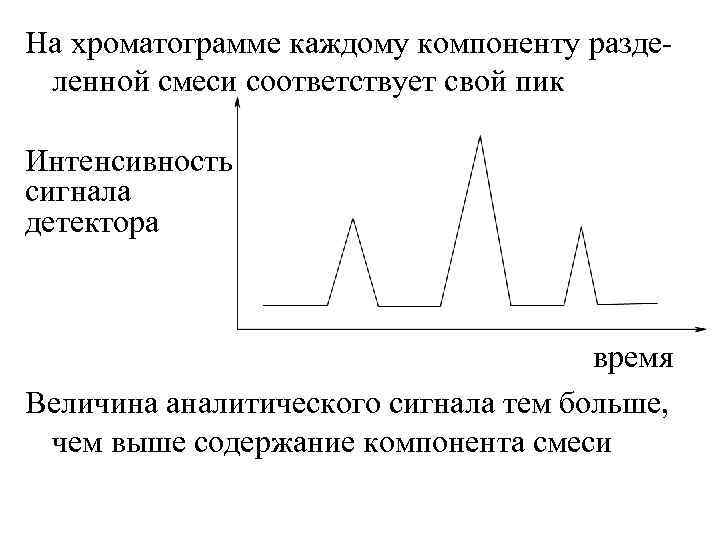
На хроматограмме каждому компоненту разделенной смеси соответствует свой пик Интенсивность сигнала детектора время Величина аналитического сигнала тем больше, чем выше содержание компонента смеси

Параметры разделения Разделение веществ в хроматографической колонке обусловлено взаимодействием двух факторов: 1. Эффективностью колонки 2. Селективностью неподвижной жидкой фазы Эффективность колонки характеризуется степенью расширения стартовой зоны вещества по мере прохождения его через колонку и определяется шириной пика хроматограммы

Чем меньше ширина пика ( l ) хроматограммы, тем эффективнее колонка
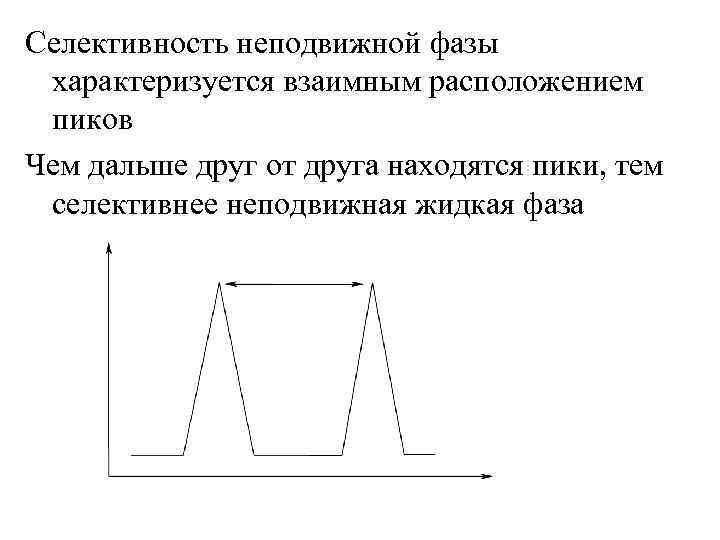
Селективность неподвижной фазы характеризуется взаимным расположением пиков Чем дальше друг от друга находятся пики, тем селективнее неподвижная жидкая фаза
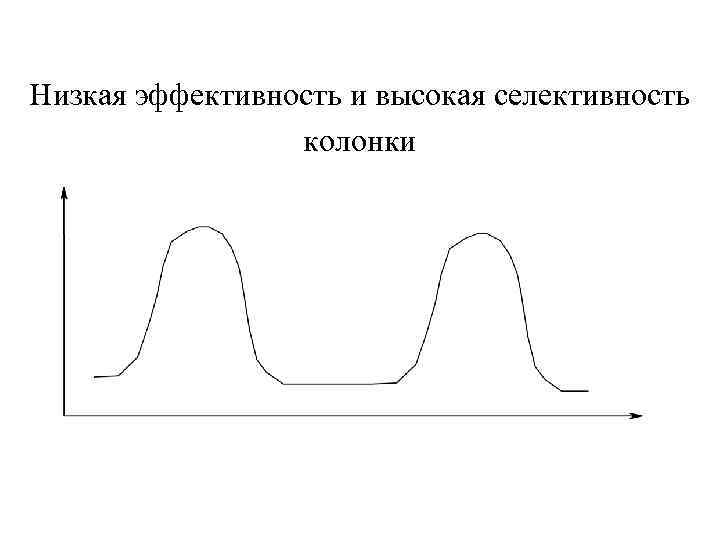
Низкая эффективность и высокая селективность колонки
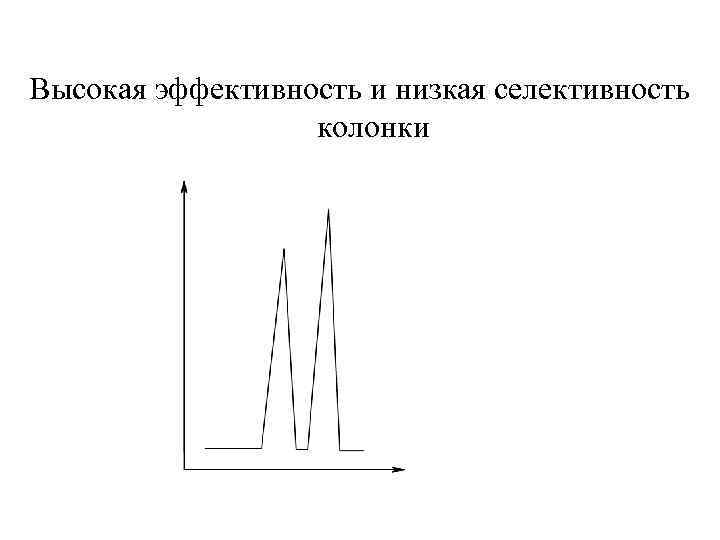
Высокая эффективность и низкая селективность колонки
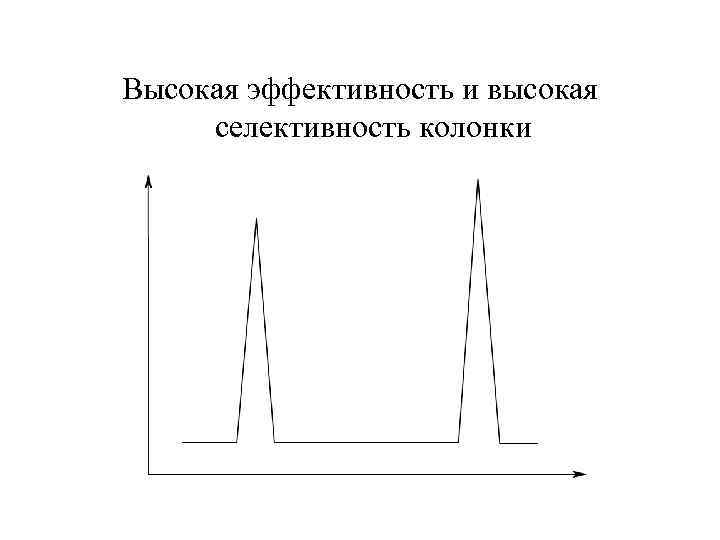
Высокая эффективность и высокая селективность колонки

Теория теоретических тарелок Теория основана на некоторых допущениях: 1. Колонка состоит из определенного числа теоретических тарелок 2. Равновесие на каждой тарелке считается достигнутым до того, как подвижная фаза переместиться на следующую тарелку (т. е. равновесие устанавливается мгновенно)

3. На любой тарелке в любой момент времени число молекул сорбируемых компонентов пробы меньше числа сорбируемых молекул элюента 4. Все протекающие в колонке процессы рассматриваются как взаимно независимые

Теоретическая тарелка – это зона, высота которой соответствует достижению равновесия между двумя фазами Чем больше теоретических тарелок в колонке, тем большее число раз устанавливается равновесие, тем эффективнее колонка Эффективность колонки – это характеристика качества колонки, определяемая числом теоретических тарелок и высотой теоретической тарелки

Количественной мерой эффективности хроматографической колонки служат высота H, эквивалентная теоретической тарелке (ВЭТТ), и число теоретических тарелок n n = 5, 545 (t /a 1/2)2 t – время удерживания компонента смеси a 1/2 – полуширина пика Чем больше число теоретических тарелок, тем эффективнее работа хроматографической колонки

Определив число теоретических тарелок и зная длину колонки L, можно вычислить ВЭТТ H=L/n Чем меньше ВЭТТ, тем менее размыта полоса компонента при его выходе из колонки Чем больше n и меньше H, тем полнее отделение полосы данного компонента от полос остальных компонентов при их разделении

Теория теоретических тарелок дает возможность сравнить эффективность различных колонок, оценить качество сорбента и заполнения колонки Хроматография позволяет не только разделять компоненты смеси, но и определять её качественный и количественный состав

Качественный анализ Качественной характеристикой вещества является время удерживания данного компонента Время удерживания компонента – это время, прошедшее с момента ввода пробы до момента выхода максимума пика Время удерживания зависит от природы хроматографируемого вещества и газаносителя, скорости прохождения ПФ через колонку, природы и массы НФ, температуры, длины колонки
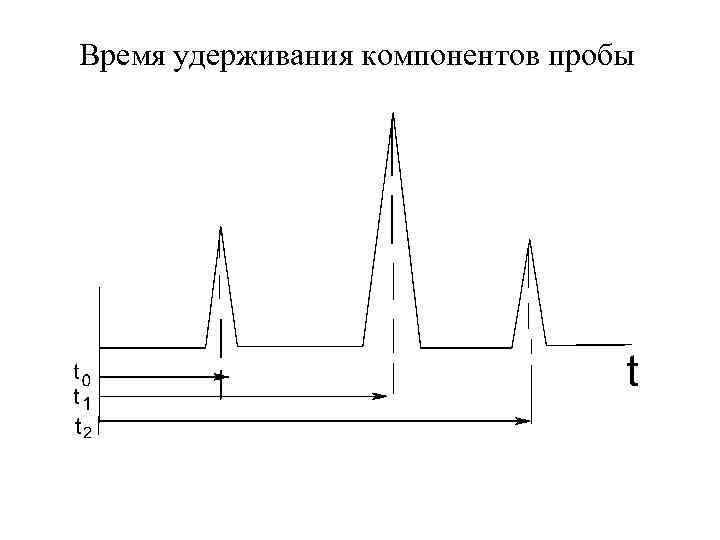
Время удерживания компонентов пробы

Более эффективно данное вещество характеризуется, если учитывать исправленное время удерживания tиспр = tудер – t 1 Это разность между временем удерживания данного компонента и временем удерживания газа-носителя

Для идентификации компонента сравнивают время удерживания неизвестного компонента и время удерживания эталона Если величины совпадают, то с большой долей вероятности можно говорить об идентичности компонентов

Количественный анализ Основан на допущении, что площадь пика на хроматограмме, соответствующая данному компоненту, прямо пропорциональна его количеству Чем больше площадь пика, тем больше количество данного компонента

Способы измерения площади пика: 1. Проводят касательные к тылу и фронту пика и соединяют их линией, параллельной нулевой линии Площадь полученного треугольниика составляет 96% от истинной и пропорциональна количеству вещества в пробе

2. Для расчета площади симметричных пиков находят произведение высоты пика на его полуширину (84% площади пика) Точность измерения площади пика зависит от отношения высоты пика к его ширине (оптимальное отношение лежит в пределах от 2 до 10)

Методы расчета хроматограмм 1. Метод абсолютной калибровки Готовится серия эталонных растворов с известной массой определяемого компонента Каждый эталон-й раствор хроматографируется и определяется площадь пика Строится график Sx — m компонента Хроматографируется раствор с неизвестной концентрацией, определяется площадь пика и по графику находится масса анализируемого компонента

2. Метод внутренней нормализации На одной и той же хроматограмме измеряют площади всех пиков и находят их сумму Так как mi/Si = const Можно записать : mа/Sа = mb/Sb = mc/Sc Находят массовую долю каждого комп-та в %: Sа · 100 Sа=————% Sa + Sb + S c Sb · 100 Sc · 100 Sb=————% Sc=————% Sa + Sb + S c

И для неизвестного компонента будет верно соотношение: Si · 100 Si = ————% S 1 + S 2 + S 3 Сумма площадей всех пиков должна соответствовать 100% содержанию всех компонентов смеси (должны элюироваться все компоненты смеси)

3. Метод внутреннего стандарта Готовят эталонную смесь (включает массу определяемого компонента и точно известную массу стандарта) Смесь хроматографируют и сравнивают площади пиков определяемого вещества и стандарта Т. к. площадь пика пропорциональна массе вещества: Si = m i Sст = mст

Тогда: Si mi — = —— Sст mст Отсюда находят mi Это соотношение верно, если детектор одинаково чувствителен к компонентам смеси

Если чувствительность детектора разная по отношению к разным компонентам анализируемой смеси, то расчеты проводят с учетом поправочного коэффициента Составляют искуственную смесь из определяемого в-ва и стандарта, хроматографируют и определяют коэффициент поправки Si = k m i mi Sст k = ——— Si mст Sст = k mст

В качестве стандарта используют вещества, родственные определяемому Чем меньше различаются площади Si и Sст , тем меньше ошибка определения, поэтому анализ обычно проводят в таких условиях, когда площади Si и Sст соизмеримы Пики стандарта и определяемого вещества не должны перекрываться

Высокоэффективная жидкостная хроматография Метод ГЖХ неприменим для малолетучих веществ, термически нестойких и веществ с большой молярной массой Эти недостатки отсутствуют в ВЭЖХ ВЖХ или жидкостная хроматография высокого давления, основана на тех же принципаах, что и ГЖХ ПФ и НФ – жидкости

Разделение компонентов основано на различии их коэффициентов распределения между НФ и ПФ Измерения проводят при комнатной температуре ПФ подается в колонку под давлением ВЭЖХ применяется для идентификации, разделения и определения разных веществ: лекарст. препаратов, оптически активных соединений, белков, аминокислот, полисахаридов, красителей и др

26_Khromatograficheskie_metody.ppt