Ассоциация.ppt
- Количество слайдов: 30

Применение теории Дебая. Хюккеля. Ионная ассоциация. Полиэлектролиты Лекция 4

Модификации 2 -го приближения ДХ

Модель квазикристаллической решетки



Применение теории Дебая—Хюккеля к слабым электролитам

Учет степени диссоциации слабого электролита
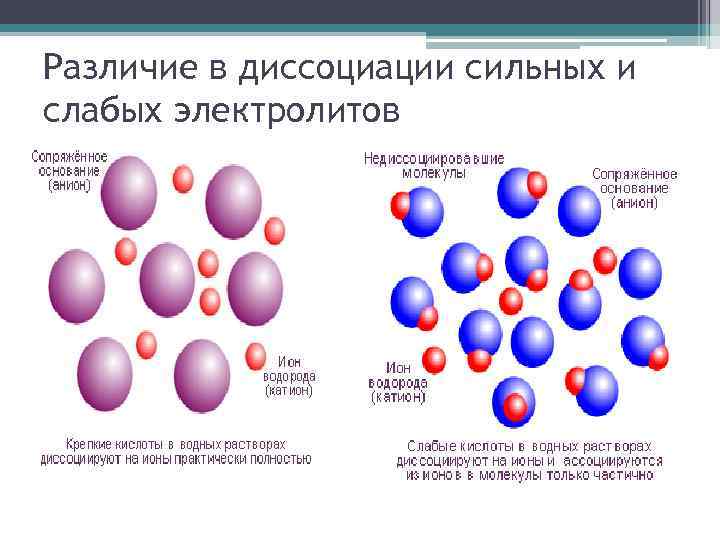
Различие в диссоциации сильных и слабых электролитов

Необходимость подстановки активностей ионов • Подстановка активностей вместо концентрации необходима также при записи выражений для ионного произведения воды, p. H, произведения растворимости Ls, констант ассоциации комплексных соединений и констант диссоциации амфолитов. • Практические растворы всегда содержат смеси нескольких электролитов, т. е. всегда более двух видов ионов. • Проблема расчета (предсказания) коэффициентов активности в таких системах еще не получила оптимального решения.

Ионная ассоциация • Учет возможности приближения противоположно заряженных ионов на расстояния, когда энергия электростатического притяжения больше энергии теплового движения. • В этом случае образуется новая частица – ионная пара, которая состоят из двух противоположно заряженных ионов, удерживаемых электростатическими силами, дисперсионными, ион-дипольными или некоторыми др. взаимодействиями. • При возбуждении в газовой фазе или под действием полярных растворителей в ионные пары могут превращаться в молекулы ковалентных соединений, например, третичные алкилгалогениды. • ионные пары могут возникать как интермедиаты в гетеролитических реакциях. • В неполярных растворителях И. п. могут ассоциироваться в димеры, тримеры и агрегаты более высокого порядка, вплоть до мицелл.

Виды ионных пар • Различают контактные (тесные) ионные пары, в которых ионы X+ и Y- находятся в непосредственном контакте (обозначаются Х+Y-), и • Сольватно - разделенные (рыхлые), в которых между ионами находится одна или (реже) несколько молекул сольватирующего агента, например, растворителя (обозначаются Х+ || Y- или X+SY-). • Нередко тесные и рыхлые ионные пары (напр. , ионные пары карбанионов или анион-радикалов) имеют различные электронные, колебательные или спектры ЯМР, что позволяет определять по отдельности их концентрации и исследовать равновесие между ними. • В общем случае ион-реагент в свободном состоянии, в виде контактной или сольватно разделенной пары имеет различную реакционную способность.

Контактные и сольватно разделенная ионные пары

Константа ионной ассоциации

Ионные тройники
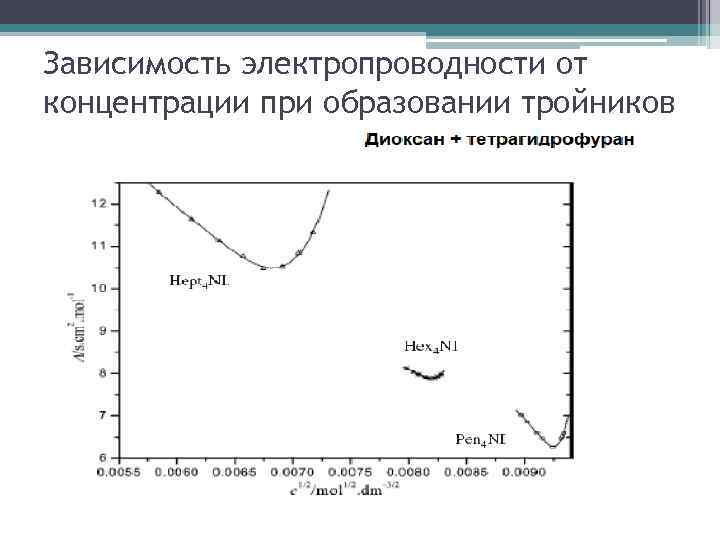
Зависимость электропроводности от концентрации при образовании тройников

Ионные квадруполи

Определение полиэлектролитов • Полимеры, в макромолекулах которых содержатся ионогенные группы. • В растворе макромолекула полиэлектролита называется полиионом, • Полиион окружен эквивалентным количеством противоионов (малых ионов с зарядами противоположного знака). • Размеры полииона на несколько порядков больше, чем противоионов.
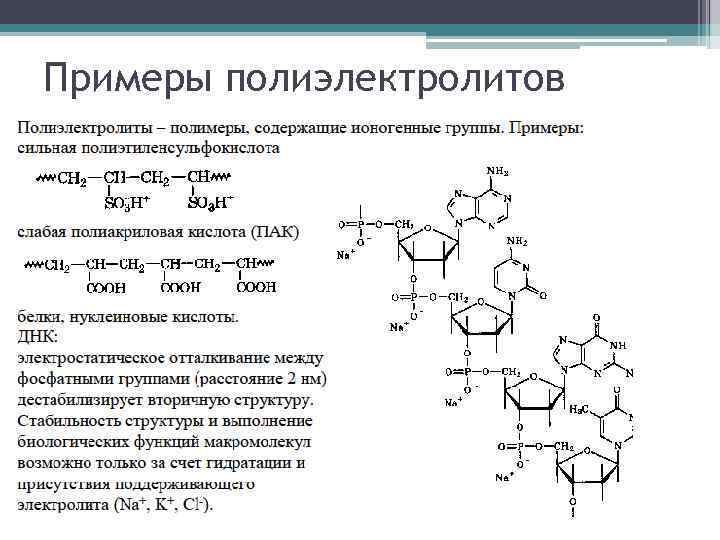
Примеры полиэлектролитов

Сильные полиэлектролиты • Различают поликислоты, полиоснования и полиамфолиты. • Ионогенные группы сильных полиэлектролитов в водных растворах полностью ионизованы независимо от значения р. Н. • Сильные поликислоты содержат сульфо-, сульфатные или фосфатные группы, • Например • поливинилсульфокислота [—CH 2 CH(SO 3 H)—]n, • сильные полиоснования в основном содержат четвертичные аммониевые группы

Слабые полиэлектролиты • Заряд слабых поликислот и полиоснований определяется величинами констант диссоциации К ионогенных групп и существенно зависит от р. Н раствора. • Типичные слабые поликислоты содержат карбоксильную группу, например: полиакриловая кислота [—СН 2 СН(СООН)— ]и, • слабые полиоснования - первичные, вторичные, третичные аминогруппы, способные протонироваться в водных средах, • Например: поливиниламин [CH 2 CH(NH 2)]n, • поливинилпиридины.

Полиамфолиты • содержат как кислотные, так и основные группы. • Суммарный заряд полиамфолитов при изменении р. Н раствора может менять знак; . • Полиамфолитами являются белки и нуклеиновые кислоты. • Полиэлектролиты могут быть как линейными, так и пространственно сшитыми

Изоэлектрическая точка • значение р. Н, при котором суммарный заряд полиамфолита равен нулю, называется изоэлектрической точкой р. I • Это характеристика состояния раствора амфотерного электролита (амфолита), при котором суммарный электрический заряд амфолита равен нулю. • Амфолит – это соединение, способное присоединять или отщеплять протоны, превращаясь либо в положительно, либо в отрицательно заряженные ионы

Особенности изоэлектрической точки • В ИЭТ амфолит не перемещается в электрическом поле. • Соответствует р. Н раствора, при котором одинаковы концентрации положительно и отрицательно заряженных форм (напр. , для аминокислот) или числа ионизированных кислотных и основных групп (напр. , для макромолекул белкови др. полиамфолитов). • Значение р. Н в ИЭТ (обозначают р. I, или р. НI) • Определяется величинами констант диссоциации кислотной и основной функций: • p. I = 0, 5(р. К 1+р. K 2).
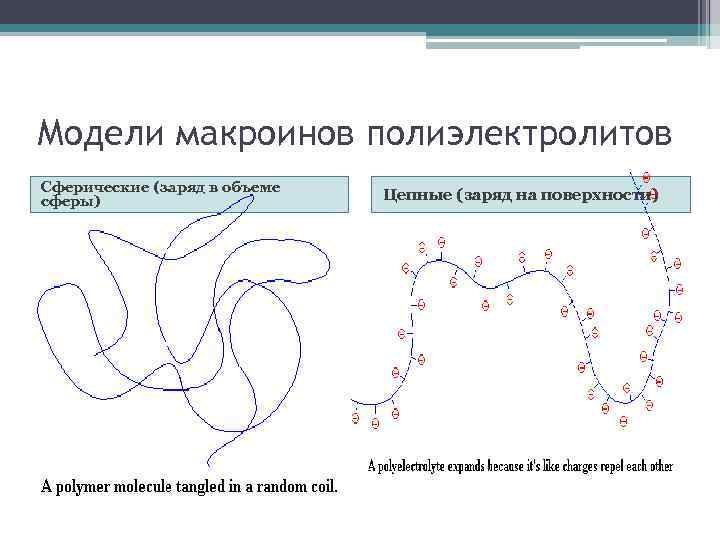
Модели макроинов полиэлектролитов Сферические (заряд в объеме сферы) Цепные (заряд на поверхности)

Модель случайно свернутой цепи
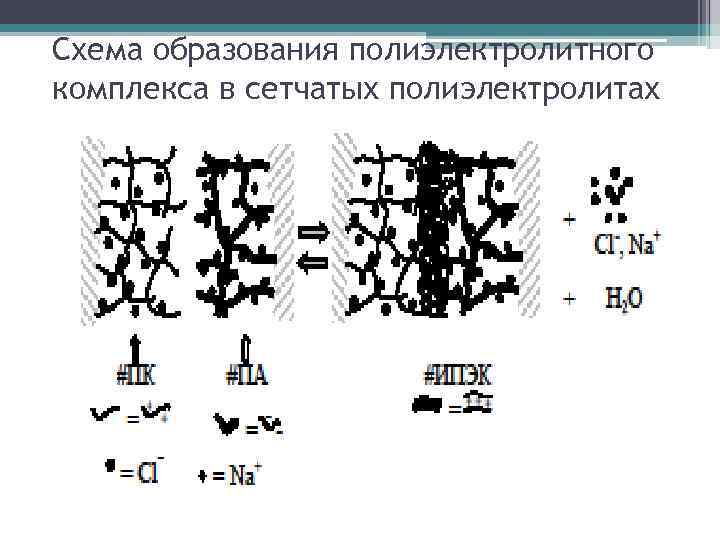
Схема образования полиэлектролитного комплекса в сетчатых полиэлектролитах

Полная обменную емкость ионитов ПОЕ Рассчитывают ПОЕ ионита по формуле Компоненты формулы • где N 0 – исходная концентрация Na. OH, мгэкв/мл; • Nx – равновесная • концентрация Na. OH, мгэкв/мл; • V – объем раствора, мл; g – навеска полимера, г.
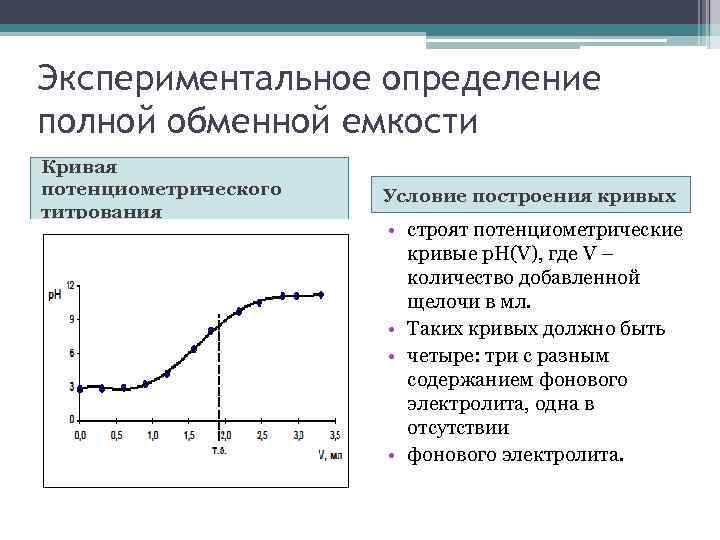
Экспериментальное определение полной обменной емкости Кривая потенциометрического титрования Условие построения кривых • строят потенциометрические кривые р. Н(V), где V – количество добавленной щелочи в мл. • Таких кривых должно быть • четыре: три с разным содержанием фонового электролита, одна в отсутствии • фонового электролита.
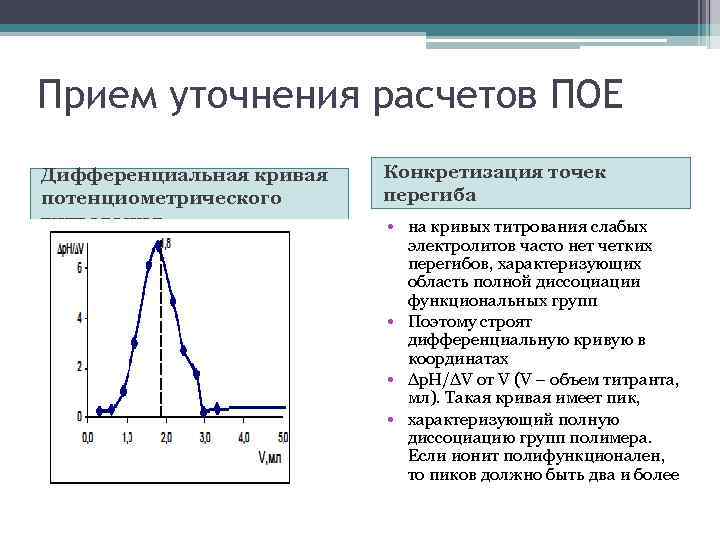
Прием уточнения расчетов ПОЕ Дифференциальная кривая потенциометрического титрования Конкретизация точек перегиба • на кривых титрования слабых электролитов часто нет четких перегибов, характеризующих область полной диссоциации функциональных групп • Поэтому строят дифференциальную кривую в координатах • Δр. Н/ΔV от V (V – объем титранта, мл). Такая кривая имеет пик, • характеризующий полную диссоциацию групп полимера. Если ионит полифункционален, то пиков должно быть два и более

Контрольные вопросы • Что такое ионофоры и ионогены? • Из каких энергий складывается энергия кристаллической решетки? • Основные положения теории ДХ • Средний коэффициент активности - формула
Ассоциация.ppt