Применение ПЦР в оценке рисков развития наследственных


















Иванова А.А. ПЦР и наследственные болезни.ppt
- Количество слайдов: 23
 Применение ПЦР в оценке рисков развития наследственных заболевания Иванова А. А.
Применение ПЦР в оценке рисков развития наследственных заболевания Иванова А. А.
 Полимеразная цепная реакция (ПЦР) - была изобретена в 1983 году американским биохимиком Кери Муллисом. Его целью было создание метода, который бы позволил амплифицировать ДНК в ходе многократных последовательных удвоений исходной молекулы ДНК с помощью фермента ДНК-полимеразы. Первая публикация по методу ПЦР появилась в ноябре 1985 года в журнале Science. Через 8 лет после этого за изобретение метода ПЦР Кэри Муллис получил Нобелевскую премию. ПЦР лежит в основе ДНК-диагностики любых наследственных заболеваний. С помощью ПЦР можно непосредственно исследовать места локализации предполагаемых мутаций или полиморфных сайтов, а также изучать наличие любых других специфических особенностей ДНК.
Полимеразная цепная реакция (ПЦР) - была изобретена в 1983 году американским биохимиком Кери Муллисом. Его целью было создание метода, который бы позволил амплифицировать ДНК в ходе многократных последовательных удвоений исходной молекулы ДНК с помощью фермента ДНК-полимеразы. Первая публикация по методу ПЦР появилась в ноябре 1985 года в журнале Science. Через 8 лет после этого за изобретение метода ПЦР Кэри Муллис получил Нобелевскую премию. ПЦР лежит в основе ДНК-диагностики любых наследственных заболеваний. С помощью ПЦР можно непосредственно исследовать места локализации предполагаемых мутаций или полиморфных сайтов, а также изучать наличие любых других специфических особенностей ДНК.
 Помимо амплификации ДНК, ПЦР позволяет производить множество других манипуляций с нуклеиновыми кислотами (введение мутаций, сращивание фрагментов ДНК) и широко используется в биологической и медицинской практике, например, для диагностики заболеваний (наследственных, инфекционных), для установления отцовства, для клонирования генов, выделения новых генов. Материалом для проведения исследований методом ПЦР служат, как правило, биологические жидкости и выделения организма: кровь, моча, слюна, мокрота. Прежде чем сдать анализ ПЦР, необходимо проконсультироваться со специалистом и тщательно подготовиться к процедуре. Анализ крови для исследования методом ПЦР берется обычно натощак.
Помимо амплификации ДНК, ПЦР позволяет производить множество других манипуляций с нуклеиновыми кислотами (введение мутаций, сращивание фрагментов ДНК) и широко используется в биологической и медицинской практике, например, для диагностики заболеваний (наследственных, инфекционных), для установления отцовства, для клонирования генов, выделения новых генов. Материалом для проведения исследований методом ПЦР служат, как правило, биологические жидкости и выделения организма: кровь, моча, слюна, мокрота. Прежде чем сдать анализ ПЦР, необходимо проконсультироваться со специалистом и тщательно подготовиться к процедуре. Анализ крови для исследования методом ПЦР берется обычно натощак.
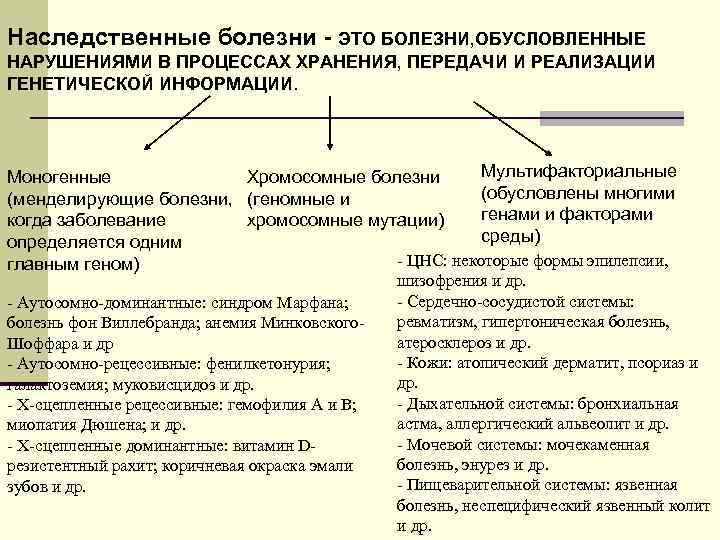
 Наследственные болезни - ЭТО БОЛЕЗНИ, ОБУСЛОВЛЕННЫЕ НАРУШЕНИЯМИ В ПРОЦЕССАХ ХРАНЕНИЯ, ПЕРЕДАЧИ И РЕАЛИЗАЦИИ ГЕНЕТИЧЕСКОЙ ИНФОРМАЦИИ. Моногенные Хромосомные болезни Мультифакториальные (менделирующие болезни, (геномные и (обусловлены многими когда заболевание хромосомные мутации) генами и факторами определяется одним среды) главным геном) - ЦНС: некоторые формы эпилепсии, шизофрения и др. - Аутосомно-доминантные: синдром Марфана; - Сердечно-сосудистой системы: болезнь фон Виллебранда; анемия Минковского- ревматизм, гипертоническая болезнь, Шоффара и др атеросклероз и др. - Аутосомно-рецессивные: фенилкетонурия; - Кожи: атопический дерматит, псориаз и галактоземия; муковисцидоз и др. др. - Х-сцепленные рецессивные: гемофилия А и B; - Дыхательной системы: бронхиальная миопатия Дюшена; и др. астма, аллергический альвеолит и др. - Х-сцепленные доминантные: витамин D- - Мочевой системы: мочекаменная резистентный рахит; коричневая окраска эмали болезнь, энурез и др. зубов и др. - Пищеварительной системы: язвенная болезнь, неспецифический язвенный колит и др.
Наследственные болезни - ЭТО БОЛЕЗНИ, ОБУСЛОВЛЕННЫЕ НАРУШЕНИЯМИ В ПРОЦЕССАХ ХРАНЕНИЯ, ПЕРЕДАЧИ И РЕАЛИЗАЦИИ ГЕНЕТИЧЕСКОЙ ИНФОРМАЦИИ. Моногенные Хромосомные болезни Мультифакториальные (менделирующие болезни, (геномные и (обусловлены многими когда заболевание хромосомные мутации) генами и факторами определяется одним среды) главным геном) - ЦНС: некоторые формы эпилепсии, шизофрения и др. - Аутосомно-доминантные: синдром Марфана; - Сердечно-сосудистой системы: болезнь фон Виллебранда; анемия Минковского- ревматизм, гипертоническая болезнь, Шоффара и др атеросклероз и др. - Аутосомно-рецессивные: фенилкетонурия; - Кожи: атопический дерматит, псориаз и галактоземия; муковисцидоз и др. др. - Х-сцепленные рецессивные: гемофилия А и B; - Дыхательной системы: бронхиальная миопатия Дюшена; и др. астма, аллергический альвеолит и др. - Х-сцепленные доминантные: витамин D- - Мочевой системы: мочекаменная резистентный рахит; коричневая окраска эмали болезнь, энурез и др. зубов и др. - Пищеварительной системы: язвенная болезнь, неспецифический язвенный колит и др.
 Моногенные болезни n Разнообразие моногенных заболеваний достаточно велико и их количество по некоторым данным достигает 5000. n С клинической точки зрения это очень разные, достаточно тяжелые болезни. n Причиной каждого из этих заболеваний является повреждение или мутация одного гена. n Следствием мутации может быть нарушение структуры или синтеза кодируемого геном белка, часто сопровождающиеся изменением его количественного содержания вплоть до полного отсутствия. n Мутации могут передаваться из поколения в поколение, но порой могут возникать в половых клетках родителей спонтанно. n Большинство мутаций, ассоциированных с моногенными заболеваниями, жестко детерминируют развитие болезни, и факторы окружающей среды не оказывают или оказывают небольшое влияние на развитие заболевания. n Среди моногенных болезней значительный процент составляют ферментопатии, различные формы умственной отсталости, дефекты органов слуха, зрения, скелетные дисплазии, врожденные пороки развития, болезни нервной, эндокринной, соединительно-тканной, иммунной и других систем.
Моногенные болезни n Разнообразие моногенных заболеваний достаточно велико и их количество по некоторым данным достигает 5000. n С клинической точки зрения это очень разные, достаточно тяжелые болезни. n Причиной каждого из этих заболеваний является повреждение или мутация одного гена. n Следствием мутации может быть нарушение структуры или синтеза кодируемого геном белка, часто сопровождающиеся изменением его количественного содержания вплоть до полного отсутствия. n Мутации могут передаваться из поколения в поколение, но порой могут возникать в половых клетках родителей спонтанно. n Большинство мутаций, ассоциированных с моногенными заболеваниями, жестко детерминируют развитие болезни, и факторы окружающей среды не оказывают или оказывают небольшое влияние на развитие заболевания. n Среди моногенных болезней значительный процент составляют ферментопатии, различные формы умственной отсталости, дефекты органов слуха, зрения, скелетные дисплазии, врожденные пороки развития, болезни нервной, эндокринной, соединительно-тканной, иммунной и других систем.
 Мультифакториальные болезни n обусловлены комбинированным действием неблагоприятных внешних и генетических факторов риска, формирующих наследственную предрасположенность к заболеванию. n К мультифакториальным заболеваниям относятся подавляющее большинство хронических болезней человека, сердечно- сосудистые, эндокринные, иммунные, нервно-психические, онкологические и др. заболевания.
Мультифакториальные болезни n обусловлены комбинированным действием неблагоприятных внешних и генетических факторов риска, формирующих наследственную предрасположенность к заболеванию. n К мультифакториальным заболеваниям относятся подавляющее большинство хронических болезней человека, сердечно- сосудистые, эндокринные, иммунные, нервно-психические, онкологические и др. заболевания.
 Способы выявления наследственных заболеваний n Цитогенетические позволяют исследовать под микроскопом с использованием различных специфических окрасок тонкую организацию хромосом человека и ее нарушения, которые приводят к появлению хромосомных болезней. n Биохимические Некоторые из наследственных болезней характеризуются выраженными биохимическими изменениями, которые связаны с нарушениями определенного метаболического пути. Эта группа заболеваний объединена в особый класс, называемый наследственные нарушения обмена веществ (НБО). Диагностика НБО включает качественный и количественный анализ различных метаболитов в образцах биологических жидкостей, определение активности ферментов в культуре клеток или лейкоцитах периферической крови. Многие из этих исследований довольно сложные и проводятся с помощью таких высокотехнологичных методов как высокоэффективная жидкостная хроматография, хроматомасс-спектрометрия, тандемная масс-спектрометрия и т. д. n Синдромологические Большинство наследственных заболеваний характеризуется поражением многих органов и систем и разнообразной клинической симптоматикой. Задача врача-генетика заключается в том, чтобы, используя имеющиеся у него специальные знания о проявлении наследственных болезней, и, детально обследовав больного и членов его семьи, постараться поставить диагноз наследственного синдрома. Во многих случаях врач пользуется для этого специальной литературой и компьютерными программами, которые содержат описания и фотографии больных с различными наследственными синдромами. n Молекулярно-генетические методы это самые современные методы исследования генетического материала клеток человека, который представлен дезоксирибунуклеиновой (ДНК) и рибунонуклеиновой (РНК) кислотами.
Способы выявления наследственных заболеваний n Цитогенетические позволяют исследовать под микроскопом с использованием различных специфических окрасок тонкую организацию хромосом человека и ее нарушения, которые приводят к появлению хромосомных болезней. n Биохимические Некоторые из наследственных болезней характеризуются выраженными биохимическими изменениями, которые связаны с нарушениями определенного метаболического пути. Эта группа заболеваний объединена в особый класс, называемый наследственные нарушения обмена веществ (НБО). Диагностика НБО включает качественный и количественный анализ различных метаболитов в образцах биологических жидкостей, определение активности ферментов в культуре клеток или лейкоцитах периферической крови. Многие из этих исследований довольно сложные и проводятся с помощью таких высокотехнологичных методов как высокоэффективная жидкостная хроматография, хроматомасс-спектрометрия, тандемная масс-спектрометрия и т. д. n Синдромологические Большинство наследственных заболеваний характеризуется поражением многих органов и систем и разнообразной клинической симптоматикой. Задача врача-генетика заключается в том, чтобы, используя имеющиеся у него специальные знания о проявлении наследственных болезней, и, детально обследовав больного и членов его семьи, постараться поставить диагноз наследственного синдрома. Во многих случаях врач пользуется для этого специальной литературой и компьютерными программами, которые содержат описания и фотографии больных с различными наследственными синдромами. n Молекулярно-генетические методы это самые современные методы исследования генетического материала клеток человека, который представлен дезоксирибунуклеиновой (ДНК) и рибунонуклеиновой (РНК) кислотами.
 Молекулярно-генетичкский метод n основан на анализе нуклеиновых кислот, в первую очередь, молекул ДНК. Основной целью этих методов является диагностика мутаций, исследование их ассоциации с наследственными заболеваниями, а также выявление гетерозиготных и гомозиготных носителей мутации. n Внедрению молекулярно-генетической методологии в клиническую практику способствовала разработка метода полимеразной цепной реакции (ПЦР) или специфической амплификации ДНК.
Молекулярно-генетичкский метод n основан на анализе нуклеиновых кислот, в первую очередь, молекул ДНК. Основной целью этих методов является диагностика мутаций, исследование их ассоциации с наследственными заболеваниями, а также выявление гетерозиготных и гомозиготных носителей мутации. n Внедрению молекулярно-генетической методологии в клиническую практику способствовала разработка метода полимеразной цепной реакции (ПЦР) или специфической амплификации ДНК.
 ДНК - диагностика Изучает непосредственную причину заболевания Наиболее адекватная и точная диагностика Возможна даже в тех случаях, когда неизвестен ген, ответственный за заболевание
ДНК - диагностика Изучает непосредственную причину заболевания Наиболее адекватная и точная диагностика Возможна даже в тех случаях, когда неизвестен ген, ответственный за заболевание
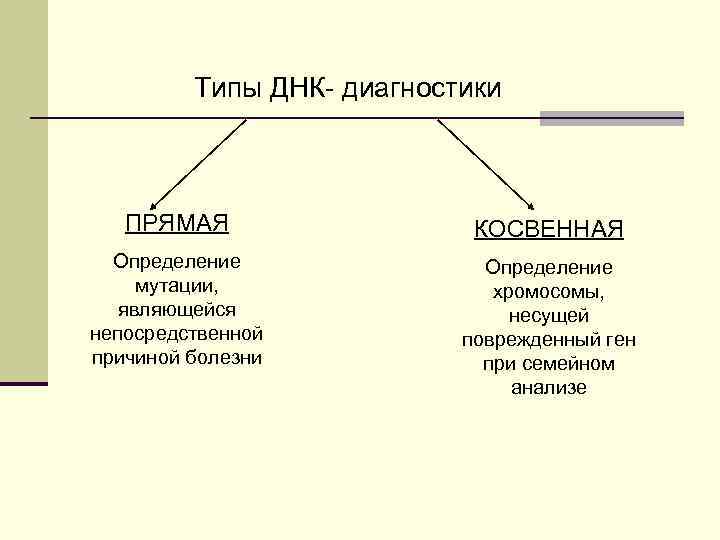
 Типы ДНК- диагностики ПРЯМАЯ КОСВЕННАЯ Определение мутации, хромосомы, являющейся несущей непосредственной поврежденный ген причиной болезни при семейном анализе
Типы ДНК- диагностики ПРЯМАЯ КОСВЕННАЯ Определение мутации, хромосомы, являющейся несущей непосредственной поврежденный ген причиной болезни при семейном анализе
 Прямая ДНК-диагностика Основу прямой диагностики составляет идентификация мутаций в самом гене. Преимущества метода: -100%-ная точность -возможна при сомнительном диагнозе -возможна при полилокусном заболевании -возможна безпробандная диагностика Недостатки метода: - Необходимо знание структуры гена - Информативна не для всей семьи
Прямая ДНК-диагностика Основу прямой диагностики составляет идентификация мутаций в самом гене. Преимущества метода: -100%-ная точность -возможна при сомнительном диагнозе -возможна при полилокусном заболевании -возможна безпробандная диагностика Недостатки метода: - Необходимо знание структуры гена - Информативна не для всей семьи
 Косвенная ДНК-диагностика Основана на анализе внутри- и внегенных полиморфных сайтов. В качестве последних обычно выступают короткие ДНК- последовательности одних и тех же гомологичных участков хромосом, различающихся по первичной структуре. Эти диагностические полиморфные сайты могут располагаться либо внутри самого гена, либо в непосредственной близости от него. Преимущества метода: + не требуется знание гена и спектра мутаций в нем + информативна практически для всей семьи + абсолютная уверенность в клиническом диагнозе Недостатки метода: - Точность 95 -99% - Обязательно наличие одного локуса заболевания - Обязательно проведение семейного анализа
Косвенная ДНК-диагностика Основана на анализе внутри- и внегенных полиморфных сайтов. В качестве последних обычно выступают короткие ДНК- последовательности одних и тех же гомологичных участков хромосом, различающихся по первичной структуре. Эти диагностические полиморфные сайты могут располагаться либо внутри самого гена, либо в непосредственной близости от него. Преимущества метода: + не требуется знание гена и спектра мутаций в нем + информативна практически для всей семьи + абсолютная уверенность в клиническом диагнозе Недостатки метода: - Точность 95 -99% - Обязательно наличие одного локуса заболевания - Обязательно проведение семейного анализа
 Методы прямой ДНК-диагностики: n Количественная флюоресцентная ПЦР. n Real-time ПЦР. n Анализ кривой плавления n MLPA – анализ (количественная лигазная реакция) n Ресеквенирование
Методы прямой ДНК-диагностики: n Количественная флюоресцентная ПЦР. n Real-time ПЦР. n Анализ кривой плавления n MLPA – анализ (количественная лигазная реакция) n Ресеквенирование
 Количественная флуоресцентная ПЦР (QF PCR) n Анализ дозы гена n Анализ экспрессии генов Метод флуоресцентной количественной полимеразной цепной реакции (quantitative Fluorescent PCR – QF-PCR) заключается в амплификации коротких тандемных повторов ДНК (STR), расположенных на исследуемой хромосоме или сцепленных с исследуемым геном. Использование в ПЦР специальной флуоресцентной метки позволяет идентифицировать количество аллелей STR-маркеров при разделении на капиллярном электрофорезе и точно определять дозу каждого фрагмента ДНК гена или хромосомы, для этого в реакционную смесь добавляют специфический флюоресцентный зонд и далее через 30 -40 циклов определяют уровень флюоресценции. Интерпретация результатов проводится с учетом количества пиков на электрофореграмме и их относительной высоты.
Количественная флуоресцентная ПЦР (QF PCR) n Анализ дозы гена n Анализ экспрессии генов Метод флуоресцентной количественной полимеразной цепной реакции (quantitative Fluorescent PCR – QF-PCR) заключается в амплификации коротких тандемных повторов ДНК (STR), расположенных на исследуемой хромосоме или сцепленных с исследуемым геном. Использование в ПЦР специальной флуоресцентной метки позволяет идентифицировать количество аллелей STR-маркеров при разделении на капиллярном электрофорезе и точно определять дозу каждого фрагмента ДНК гена или хромосомы, для этого в реакционную смесь добавляют специфический флюоресцентный зонд и далее через 30 -40 циклов определяют уровень флюоресценции. Интерпретация результатов проводится с учетом количества пиков на электрофореграмме и их относительной высоты.
 Real-time ПЦР n Анализ дозы гена (делеции/дупликации) n Определение точковых замен n Анализ экспрессии генов - онкологические исследования - трисомии - анализ плодного материала по кровотоку матери - генотерапия
Real-time ПЦР n Анализ дозы гена (делеции/дупликации) n Определение точковых замен n Анализ экспрессии генов - онкологические исследования - трисомии - анализ плодного материала по кровотоку матери - генотерапия
 Real-time ПЦР n это группа методик, дающих возможность качественного анализа продуктов ПЦР в режиме реального времени по ходу проведения реакции. Основными этапами данного метода являются: n Определение выхода продукта реакции после каждого цикла амплификации. n Построение по этим данным кинетической кривой PCR. n Определение относительной концентрации субстрата на основании анализа этой кривой. n Для детекции PCR-продукта используются флуоресцентные красители, обеспечивающие флуоресценцию, прямо пропорциональную количеству ПЦР- продукта - репортерную флуоресценцию. Механизмы ее генерации различаются в зависимости от конкретного типа real -time PCR.
Real-time ПЦР n это группа методик, дающих возможность качественного анализа продуктов ПЦР в режиме реального времени по ходу проведения реакции. Основными этапами данного метода являются: n Определение выхода продукта реакции после каждого цикла амплификации. n Построение по этим данным кинетической кривой PCR. n Определение относительной концентрации субстрата на основании анализа этой кривой. n Для детекции PCR-продукта используются флуоресцентные красители, обеспечивающие флуоресценцию, прямо пропорциональную количеству ПЦР- продукта - репортерную флуоресценцию. Механизмы ее генерации различаются в зависимости от конкретного типа real -time PCR.
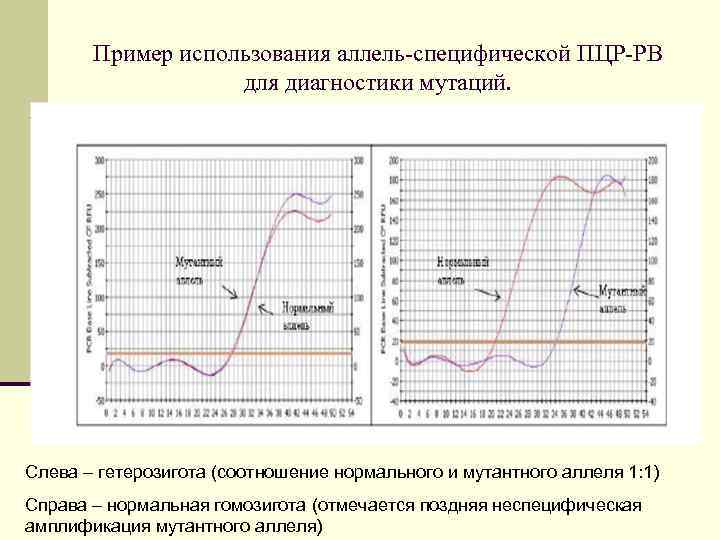
 Пример использования аллель-специфической ПЦР-РВ для диагностики мутаций. Слева – гетерозигота (соотношение нормального и мутантного аллеля 1: 1) Справа – нормальная гомозигота (отмечается поздняя неспецифическая амплификация мутантного аллеля)
Пример использования аллель-специфической ПЦР-РВ для диагностики мутаций. Слева – гетерозигота (соотношение нормального и мутантного аллеля 1: 1) Справа – нормальная гомозигота (отмечается поздняя неспецифическая амплификация мутантного аллеля)
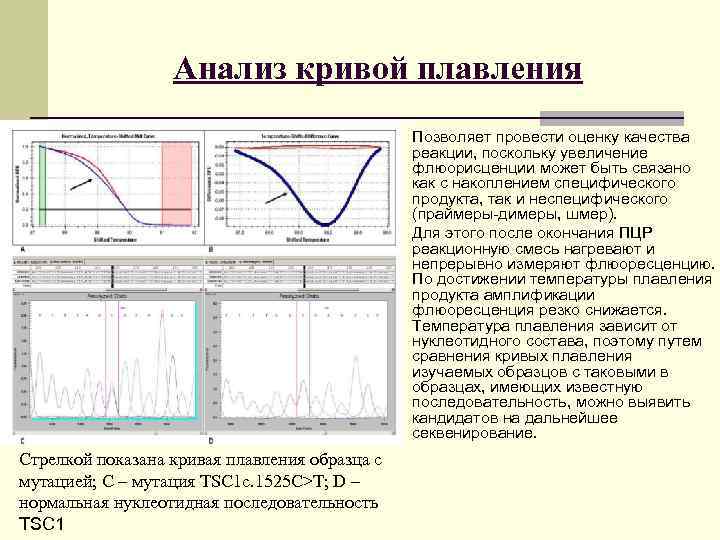
 Анализ кривой плавления - Позволяет провести оценку качества реакции, поскольку увеличение флюорисценции может быть связано как с накоплением специфического продукта, так и неспецифического (праймеры-димеры, шмер). - Для этого после окончания ПЦР реакционную смесь нагревают и непрерывно измеряют флюоресценцию. По достижении температуры плавления продукта амплификации флюоресценция резко снижается. Температура плавления зависит от нуклеотидного состава, поэтому путем сравнения кривых плавления изучаемых образцов с таковыми в образцах, имеющих известную последовательность, можно выявить кандидатов на дальнейшее секвенирование. Стрелкой показана кривая плавления образца с мутацией; С – мутация TSC 1 c. 1525 C>T; D – нормальная нуклеотидная последовательность TSC 1
Анализ кривой плавления - Позволяет провести оценку качества реакции, поскольку увеличение флюорисценции может быть связано как с накоплением специфического продукта, так и неспецифического (праймеры-димеры, шмер). - Для этого после окончания ПЦР реакционную смесь нагревают и непрерывно измеряют флюоресценцию. По достижении температуры плавления продукта амплификации флюоресценция резко снижается. Температура плавления зависит от нуклеотидного состава, поэтому путем сравнения кривых плавления изучаемых образцов с таковыми в образцах, имеющих известную последовательность, можно выявить кандидатов на дальнейшее секвенирование. Стрелкой показана кривая плавления образца с мутацией; С – мутация TSC 1 c. 1525 C>T; D – нормальная нуклеотидная последовательность TSC 1
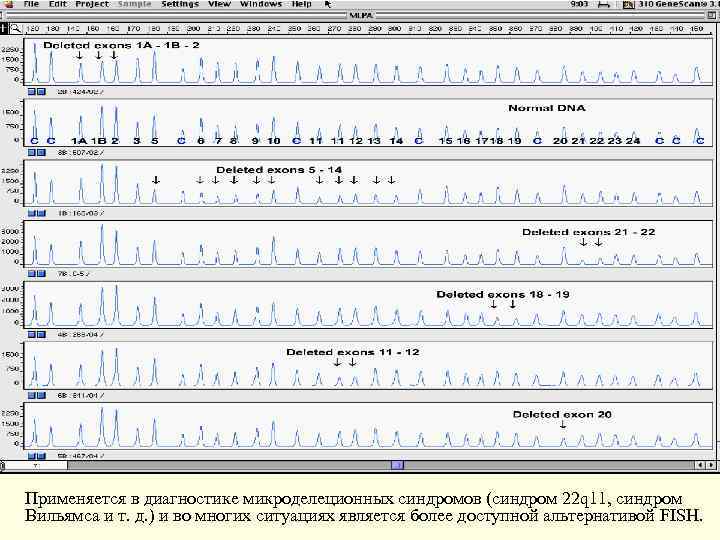
 MLPA – анализ (мультиплексная амплификация лигазно-связаных проб) n Определение числа копий фрагмента (дозы гена) - Носительство Х-сцепленных делеций для женщин - Аутосомные делеции/дупликации - Микроделеционные синдромы - Анеуплоидии - Определение числа копий гена/псевдогена n Анализ однонуклеотидных замен (SNP) На первом этапе анализа производится денатурация ДНК и ее гибридизация со специфичными пробами (зондами). Зонды расположены очень близко друг от друга, к одному из их концов присоединена последовательность для прикрепления универсального праймера. На следующем этапе происходит специфичное лигирование проб с помощью фермента лигазы. Далее производится мультиплексная ПЦР- амплификация с использованием универсальных праймеров; при этом многократно увеличивается только количество лигированных фрагментов. Продукты амплификации, имеющие разные размеры, сепарирубтся посредством капиллярного электрофореза. Наличие пика и его высота на электрофореграмме отражает состояние данного генетического локуса (норма, делеция или дупликация).
MLPA – анализ (мультиплексная амплификация лигазно-связаных проб) n Определение числа копий фрагмента (дозы гена) - Носительство Х-сцепленных делеций для женщин - Аутосомные делеции/дупликации - Микроделеционные синдромы - Анеуплоидии - Определение числа копий гена/псевдогена n Анализ однонуклеотидных замен (SNP) На первом этапе анализа производится денатурация ДНК и ее гибридизация со специфичными пробами (зондами). Зонды расположены очень близко друг от друга, к одному из их концов присоединена последовательность для прикрепления универсального праймера. На следующем этапе происходит специфичное лигирование проб с помощью фермента лигазы. Далее производится мультиплексная ПЦР- амплификация с использованием универсальных праймеров; при этом многократно увеличивается только количество лигированных фрагментов. Продукты амплификации, имеющие разные размеры, сепарирубтся посредством капиллярного электрофореза. Наличие пика и его высота на электрофореграмме отражает состояние данного генетического локуса (норма, делеция или дупликация).
 Применяется в диагностике микроделеционных синдромов (синдром 22 q 11, синдром Вильямса и т. д. ) и во многих ситуациях является более доступной альтернативой FISH.
Применяется в диагностике микроделеционных синдромов (синдром 22 q 11, синдром Вильямса и т. д. ) и во многих ситуациях является более доступной альтернативой FISH.
 Ресеквенирование - Повторное секвенирование генома с целью выявления разнообразных структурных вариаций (однонуклеотидных полиморфизмов, или «снипов» , а также инсерций, делеций, повторов, инверсий, транслокаций). В отличие от секвенирования неизвестных последовательностей de novo, при котором прочтения соотносятся друг с другом и собираются в контиги, для ре- секвенирования достаточно просто «картировать» прочтения на референсную последовательность, уже имеющуюся под рукой. Снипы выглядят как однонуклеотидные замены в коротких прочтениях, при этом количество прочтений с заменой говорит о состоянии аллеля — гомозиготном (все прочтения с заменой) или гетерозиготном (половина прочтений с заменой).
Ресеквенирование - Повторное секвенирование генома с целью выявления разнообразных структурных вариаций (однонуклеотидных полиморфизмов, или «снипов» , а также инсерций, делеций, повторов, инверсий, транслокаций). В отличие от секвенирования неизвестных последовательностей de novo, при котором прочтения соотносятся друг с другом и собираются в контиги, для ре- секвенирования достаточно просто «картировать» прочтения на референсную последовательность, уже имеющуюся под рукой. Снипы выглядят как однонуклеотидные замены в коротких прочтениях, при этом количество прочтений с заменой говорит о состоянии аллеля — гомозиготном (все прочтения с заменой) или гетерозиготном (половина прочтений с заменой).
 Заключение n Заключение, полученное с помощью ДНК-диагностики, дает оценку вероятности возникновения заболеваний, ассоциированных с теми или иными мутациями/полиморфизмами и профилактические и лечебно-диагностические рекомендации для пациента и лечащего врача. n Проведенные исследования показали, что у 5, 3% людей в возрасте до 25 лет разовьются болезни, обусловленные наследственными факторами, а в течение жизни у 60% людей разовьются болезни, связанные с наследственной предрасположенностью. n Ограничение современных возможностей лечения наследственных заболеваний и непредсказуемый характер передачи генов от поколения к поколению заставляют сосредоточить внимание на профилактике, как на наиболее надежном и эффективном способе предотвращения этих болезней. n Знание степени вероятности возникновения полигенных болезней позволяет снизить величину риска развития заболевания в результате лечения до развития необратимых поражений, поскольку наличие тех или иных полиморфизмов не приводит с неизбежностью к болезни.
Заключение n Заключение, полученное с помощью ДНК-диагностики, дает оценку вероятности возникновения заболеваний, ассоциированных с теми или иными мутациями/полиморфизмами и профилактические и лечебно-диагностические рекомендации для пациента и лечащего врача. n Проведенные исследования показали, что у 5, 3% людей в возрасте до 25 лет разовьются болезни, обусловленные наследственными факторами, а в течение жизни у 60% людей разовьются болезни, связанные с наследственной предрасположенностью. n Ограничение современных возможностей лечения наследственных заболеваний и непредсказуемый характер передачи генов от поколения к поколению заставляют сосредоточить внимание на профилактике, как на наиболее надежном и эффективном способе предотвращения этих болезней. n Знание степени вероятности возникновения полигенных болезней позволяет снизить величину риска развития заболевания в результате лечения до развития необратимых поражений, поскольку наличие тех или иных полиморфизмов не приводит с неизбежностью к болезни.
 Благодарю за внимание!
Благодарю за внимание!

