04_Lyuminestsentsia_2-2011.ppt
- Количество слайдов: 32
 Применение люминесценции Ю. А. Владимиров и А. Н. Осипов 2011
Применение люминесценции Ю. А. Владимиров и А. Н. Осипов 2011

 Книги по применению флуоресцентных методов
Книги по применению флуоресцентных методов
 Применение фотолюминесценции 1. 2. 3. 4. 5. 6. Анализ – флуоресценция природных соединений. Анализ – образование флуоресцирующих веществ. Гематоэнцефалический и гистогематический барьеры. Иммунный анализ – флуоресцентные метки. Доступность для кислорода – фосфоресценция. Вращательная подвижность – поляризация флуоресценции 7. Поступательная диффузия – эксимеризация пирена. 8. Расстояние между группами – перенос энергии. 9. Изучение биопотенциалов – распределение заряженных зондов. 10. Флуоресцентная микроскопия
Применение фотолюминесценции 1. 2. 3. 4. 5. 6. Анализ – флуоресценция природных соединений. Анализ – образование флуоресцирующих веществ. Гематоэнцефалический и гистогематический барьеры. Иммунный анализ – флуоресцентные метки. Доступность для кислорода – фосфоресценция. Вращательная подвижность – поляризация флуоресценции 7. Поступательная диффузия – эксимеризация пирена. 8. Расстояние между группами – перенос энергии. 9. Изучение биопотенциалов – распределение заряженных зондов. 10. Флуоресцентная микроскопия
 Механизм флуоресценции Горизонтальные линии обозначают уровни энергии электронов в молекуле красителя. Флуоресцентный краситель переходит в возбужденное состояние при поглощении кванта света. Он теряет небольшое количество энергии за счет тепловых колебаний, а остальную энергию высвечивает в виде кванта. (более подробно см. на www. dekker. com. )
Механизм флуоресценции Горизонтальные линии обозначают уровни энергии электронов в молекуле красителя. Флуоресцентный краситель переходит в возбужденное состояние при поглощении кванта света. Он теряет небольшое количество энергии за счет тепловых колебаний, а остальную энергию высвечивает в виде кванта. (более подробно см. на www. dekker. com. )
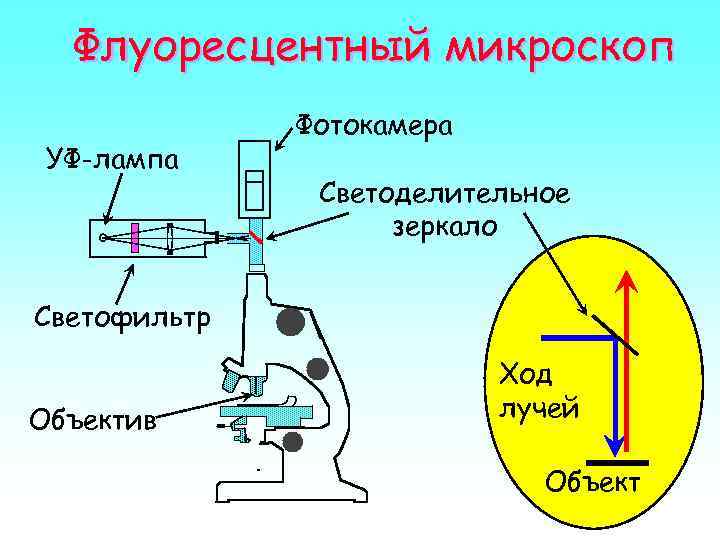 Флуоресцентный микроскоп УФ-лампа Фотокамера Светоделительное зеркало Светофильтр Объектив Ход лучей Объект
Флуоресцентный микроскоп УФ-лампа Фотокамера Светоделительное зеркало Светофильтр Объектив Ход лучей Объект
 Схема флуоресцентного микроскопа Свет от источника света отражается от полупроницаемого зеркала и проходит к изучаемому образцу. Излучаемая образцом флуоресценция имеющая большую длину волны проходит через зеркало к окуляру. (более подробно см. на www. dekker. com. )
Схема флуоресцентного микроскопа Свет от источника света отражается от полупроницаемого зеркала и проходит к изучаемому образцу. Излучаемая образцом флуоресценция имеющая большую длину волны проходит через зеркало к окуляру. (более подробно см. на www. dekker. com. )
 Схема конфокального микроскопа Луч света от источника сканирует образец с помощью колеблющихся зеркал. Кват флуоресценции исходящий от образца проходит через очень тонкое отверстие и попадает на детектор с помощью которого формируется изображение. (более подробно см. на www. dekker. com. ) Конфокальный микроскоп Encyclopedia of Biomaterials and Biomedical Engineering DOI: 10. 1081/EEBBE-120024153 Copyright # 2005 by Taylor & Francis. All rights reserved.
Схема конфокального микроскопа Луч света от источника сканирует образец с помощью колеблющихся зеркал. Кват флуоресценции исходящий от образца проходит через очень тонкое отверстие и попадает на детектор с помощью которого формируется изображение. (более подробно см. на www. dekker. com. ) Конфокальный микроскоп Encyclopedia of Biomaterials and Biomedical Engineering DOI: 10. 1081/EEBBE-120024153 Copyright # 2005 by Taylor & Francis. All rights reserved.
 Изображения клеток Spirogyra, полученные с и без оптического разделения
Изображения клеток Spirogyra, полученные с и без оптического разделения
 Анализ – флуоресценция природных соединений Ю. А. Владимиров, Е. Н. Любитов, В. И. Оленев, П. В. Сергеев, and В. А. Чистяков. Установка для флуориметрического определения серотонина и других биогенных аминов. Журнал прикладной спектроскопии 8: 700 -703, 1968.
Анализ – флуоресценция природных соединений Ю. А. Владимиров, Е. Н. Любитов, В. И. Оленев, П. В. Сергеев, and В. А. Чистяков. Установка для флуориметрического определения серотонина и других биогенных аминов. Журнал прикладной спектроскопии 8: 700 -703, 1968.
 Анализ – образование или разрушение флуоресцирующих веществ Паринариевая кислота флуоресцирует. При действии свободных радикалов на липиды мембран она разрушается и флуоресценция фосфолипида, содержащего паринариевую кислоту, исчезает. R. K. Dubey, Y. Y. Tyurina, V. A. Tyurin, D. G. Gillespie, R. A. Branch, E. K. Jackson, and V. E. Kagan. Estrogen and tamoxifen metabolites protect smooth muscle cell membrane phospholipids against peroxidation and inhibit cell growth. Circ Res 84 (2): 229 -39, 1999.
Анализ – образование или разрушение флуоресцирующих веществ Паринариевая кислота флуоресцирует. При действии свободных радикалов на липиды мембран она разрушается и флуоресценция фосфолипида, содержащего паринариевую кислоту, исчезает. R. K. Dubey, Y. Y. Tyurina, V. A. Tyurin, D. G. Gillespie, R. A. Branch, E. K. Jackson, and V. E. Kagan. Estrogen and tamoxifen metabolites protect smooth muscle cell membrane phospholipids against peroxidation and inhibit cell growth. Circ Res 84 (2): 229 -39, 1999.
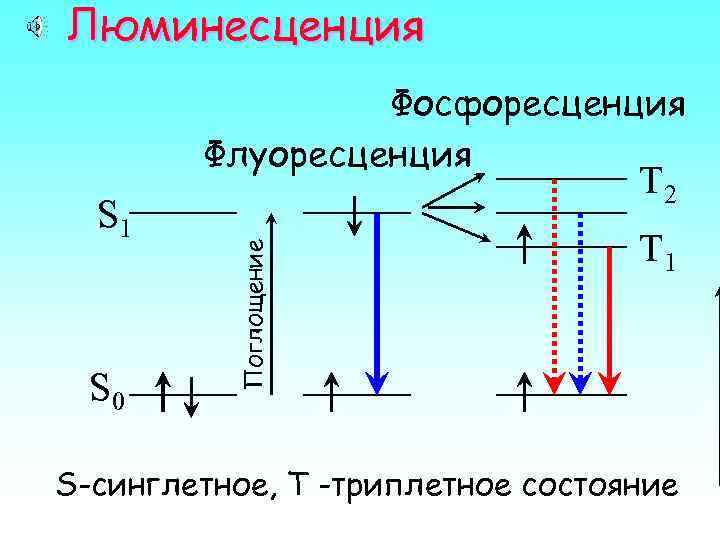 Люминесценция Фосфоресценция Флуоресценция S 0 Поглощение S 1 T 2 T 1 S-синглетное, T -триплетное состояние
Люминесценция Фосфоресценция Флуоресценция S 0 Поглощение S 1 T 2 T 1 S-синглетное, T -триплетное состояние
 Спектры триптофана 1 -Возбуждение флуоресценции 2 - Флуоресценция 3 - Фосфоресценция
Спектры триптофана 1 -Возбуждение флуоресценции 2 - Флуоресценция 3 - Фосфоресценция
 Доступность для кислорода – фосфоресценция
Доступность для кислорода – фосфоресценция
 Вращательная подвижность – поляризация флуоресценции Коэффициент поляризации Схема установки для измерения
Вращательная подвижность – поляризация флуоресценции Коэффициент поляризации Схема установки для измерения
 Триптофан в вязкой среде (глицерин)
Триптофан в вязкой среде (глицерин)
 Поступательная диффузия. Эксимеризация пирена P* P + фотон (370 -390 нм) P + P* (PP)* P + фотон (470 нм) F Флуоресценция мономера Флуоресценция эксимера Высокая текучесть Высокая микровязкость 350 400 450 500 nm
Поступательная диффузия. Эксимеризация пирена P* P + фотон (370 -390 нм) P + P* (PP)* P + фотон (470 нм) F Флуоресценция мономера Флуоресценция эксимера Высокая текучесть Высокая микровязкость 350 400 450 500 nm
 Расстояние между группами – перенос энергии 1. D + hn. Da D* Возбуждение донора 2. D* D + hn. Df Флуоресценция донора 3. D* + A D + A* Перенос энергии 4. A* A + hn. Af Флуоресценция акцептора 3 1 2 4
Расстояние между группами – перенос энергии 1. D + hn. Da D* Возбуждение донора 2. D* D + hn. Df Флуоресценция донора 3. D* + A D + A* Перенос энергии 4. A* A + hn. Af Флуоресценция акцептора 3 1 2 4
 Диффузионный перенос энергии. Определение подвижности пептидной цепи. N N k. D+ hn 1 * k. D– T T* T* * 4 N T N* 3 5 Поглощение Т 1 -Т 2 2 длина волны
Диффузионный перенос энергии. Определение подвижности пептидной цепи. N N k. D+ hn 1 * k. D– T T* T* * 4 N T N* 3 5 Поглощение Т 1 -Т 2 2 длина волны
 Индуктивно-резонансный (не диффузионный) перенос энергии Спектры возбуждения и флуоресценции донора Спектры возбуждения и флуоресценции акцептора Спектр возбуждения акцептора при 50% переноса энергии. Длина волны Спектр возбуждения акцептора при 100% переноса энергии.
Индуктивно-резонансный (не диффузионный) перенос энергии Спектры возбуждения и флуоресценции донора Спектры возбуждения и флуоресценции акцептора Спектр возбуждения акцептора при 50% переноса энергии. Длина волны Спектр возбуждения акцептора при 100% переноса энергии.
 Расстояние между группами – перенос энергии R 0 А R 0
Расстояние между группами – перенос энергии R 0 А R 0
 Миграция энергии на пирен P* P + фотон (370 -390 нм) P + P* (PP)* P + фотон (470 нм) Флуоресценция мономера Флуоресценция эксимера Возбуждение при 334 nm При 286 nm 350 400 450 500 nm
Миграция энергии на пирен P* P + фотон (370 -390 нм) P + P* (PP)* P + фотон (470 нм) Флуоресценция мономера Флуоресценция эксимера Возбуждение при 334 nm При 286 nm 350 400 450 500 nm
 Флуоресцентные зонды Ю. А. Владимиров
Флуоресцентные зонды Ю. А. Владимиров
 Флуоресцентные зонды Чувствителен к электрическому полю O– O S Чувствительны к полярности окружения O O CH 3 H C HN 3 O N H C 3 O АНС МБА ДМХ
Флуоресцентные зонды Чувствителен к электрическому полю O– O S Чувствительны к полярности окружения O O CH 3 H C HN 3 O N H C 3 O АНС МБА ДМХ
 АНС флуоресцирует только в неполярной среде АНС¯ Липосома из нейтральных липидов АНС — в липиде. Флуоресценция яркая. Липосома, заряженная отрицательно АНС — в воде. Флуоресценция слабая.
АНС флуоресцирует только в неполярной среде АНС¯ Липосома из нейтральных липидов АНС — в липиде. Флуоресценция яркая. Липосома, заряженная отрицательно АНС — в воде. Флуоресценция слабая.
 Флуоресценция АНС 20 F (отн. ед. ) 100 40 200 400 Деев и сотр. 1967 „. 60 80 100 80 60 40 0 600 800 1000 Содержание жирных кислот в липосомах (m. M)
Флуоресценция АНС 20 F (отн. ед. ) 100 40 200 400 Деев и сотр. 1967 „. 60 80 100 80 60 40 0 600 800 1000 Содержание жирных кислот в липосомах (m. M)
 Влияние полярности окружения на спектры поглощения и флуоресценции
Влияние полярности окружения на спектры поглощения и флуоресценции
 F Спектры поглощения и флуоресценции МБА 0, 5 0 300 400 nm
F Спектры поглощения и флуоресценции МБА 0, 5 0 300 400 nm
 Полярность окружения Растворители 1 2 3 4 5 МБА 430 ls 420 ДМХ 410 поглощение МБА ДМХ 550 ls 6 540 530 Добрецов и сотр. 1977 Растворители 1 - хлороформ 2 - ацетон 3 - диметилформамид 4 - бутанол 5 - метанол 6 - вода z - параметр 520 флуоресценция 60 70 z 80 90 полярности Колтовера
Полярность окружения Растворители 1 2 3 4 5 МБА 430 ls 420 ДМХ 410 поглощение МБА ДМХ 550 ls 6 540 530 Добрецов и сотр. 1977 Растворители 1 - хлороформ 2 - ацетон 3 - диметилформамид 4 - бутанол 5 - метанол 6 - вода z - параметр 520 флуоресценция 60 70 z 80 90 полярности Колтовера
 Фазовые переходы с МБА lm ДМЛ lm ДПЛ +вал 518 нм 507 нм 514 нм 503 нм 10 То С 20 30 То С 40 50 Валиномицин/фосфолипид 1: 700
Фазовые переходы с МБА lm ДМЛ lm ДПЛ +вал 518 нм 507 нм 514 нм 503 нм 10 То С 20 30 То С 40 50 Валиномицин/фосфолипид 1: 700
 Пирен как флуоресцентный зонд Деев и сотр. 1967 г. F (отн. ед. ) 30 25 20 15 10 5 Пирен Интактный ЛНП 360 Окисленный ЛНП 380 400 420 Длина волны, нм
Пирен как флуоресцентный зонд Деев и сотр. 1967 г. F (отн. ед. ) 30 25 20 15 10 5 Пирен Интактный ЛНП 360 Окисленный ЛНП 380 400 420 Длина волны, нм
 Спектры флуоресценции пирена F Вода Этанол 8 Липосомы Гептан + 0, 5% этанол 4 0 F 4 0 350 400 450 500 нм
Спектры флуоресценции пирена F Вода Этанол 8 Липосомы Гептан + 0, 5% этанол 4 0 F 4 0 350 400 450 500 нм


