ПРИМЕНЕНИЕ ИММУННЫХ МЕТОДОВ.ppt
- Количество слайдов: 43
 ПРИМЕНЕНИЕ ИММУНОХИМИЧЕСКИЕХ МЕТОДОВ МЕТОДО В АНАЛИЗЕ НАРКОТИЧЕСКИХ СРЕДСТВ И ПСИХОТРОПНЫХ ВЕЩЕСТВ. ГБОУ ВПО СПХФА МЗ РФ, заведующая кафедрой фармацевтической химии, доцент, к. х. н. Стрелова О. Ю.
ПРИМЕНЕНИЕ ИММУНОХИМИЧЕСКИЕХ МЕТОДОВ МЕТОДО В АНАЛИЗЕ НАРКОТИЧЕСКИХ СРЕДСТВ И ПСИХОТРОПНЫХ ВЕЩЕСТВ. ГБОУ ВПО СПХФА МЗ РФ, заведующая кафедрой фармацевтической химии, доцент, к. х. н. Стрелова О. Ю.
 Иммунохимический анализ — лабораторный иммунологический метод качественного или количественного определения различных соединений, макромолекул, вирусов и пр. , в основе которого лежит специфическая реакция антигенантитело. + =
Иммунохимический анализ — лабораторный иммунологический метод качественного или количественного определения различных соединений, макромолекул, вирусов и пр. , в основе которого лежит специфическая реакция антигенантитело. + =
 АНТИГЕН – вещество, взаимодействующее специфическими рецепторами Т- и В-лимфоцитов. со Вне организма АНТИГЕНАМИ называют вещества, способные вызвать на себя иммунный ответ. Иммуногенностью обладают корпускулярные формы (микроорганизмы, эритроциты), макромолекулярные вещества (белки, полисахариды, гликопротеины, липополисахариды, липопротеины) и гаптены низкомолекулярные вещества, не способные вызывать образование антител, но после коньюгирования с высокомолекулярными носителями, приобретающие иммуногенные свойства.
АНТИГЕН – вещество, взаимодействующее специфическими рецепторами Т- и В-лимфоцитов. со Вне организма АНТИГЕНАМИ называют вещества, способные вызвать на себя иммунный ответ. Иммуногенностью обладают корпускулярные формы (микроорганизмы, эритроциты), макромолекулярные вещества (белки, полисахариды, гликопротеины, липополисахариды, липопротеины) и гаптены низкомолекулярные вещества, не способные вызывать образование антител, но после коньюгирования с высокомолекулярными носителями, приобретающие иммуногенные свойства.
 АНТИТЕЛА – специальные белки, продуцируемые плазматическими клетками (В-лимфоцитами), имеющие характерную общую структуру и общие физико-химические свойства, что отражает их второе групповое название ИММУНОГЛОБУЛИНЫ. ◦ ПОЛИКЛОНАЛЬНЫЕ – неспецифические иммуноглобулины сыворотки (преимущественно Ig. M, Ig. G, Ig. A) ◦ МОНОКЛОНАЛЬНЫЕ – индивидуальные антитела определенной специфичности (иммуноглобулины класса Ig. G или Ig. M; подкласса Ig. G 1 или Ig. G 2 и др. )
АНТИТЕЛА – специальные белки, продуцируемые плазматическими клетками (В-лимфоцитами), имеющие характерную общую структуру и общие физико-химические свойства, что отражает их второе групповое название ИММУНОГЛОБУЛИНЫ. ◦ ПОЛИКЛОНАЛЬНЫЕ – неспецифические иммуноглобулины сыворотки (преимущественно Ig. M, Ig. G, Ig. A) ◦ МОНОКЛОНАЛЬНЫЕ – индивидуальные антитела определенной специфичности (иммуноглобулины класса Ig. G или Ig. M; подкласса Ig. G 1 или Ig. G 2 и др. )
 Структурный фрагмент антител В основе молекулы – тетрамер, симметричный комплекс из двух легких и двух тяжелых полипептидных цепей; Fab- область, пептидная последовательность, область распознавания антигена.
Структурный фрагмент антител В основе молекулы – тетрамер, симметричный комплекс из двух легких и двух тяжелых полипептидных цепей; Fab- область, пептидная последовательность, область распознавания антигена.
 Характеристики используемых антител 1. Поли или моноклональные антитела 2. Различного типа (Jg G или Jg М) и подтипа (Jg G 1 или Jg G 2 a) 3. Моно- или поливалентные 4. Моно- или биспецифические 5. Нативные или полученные химическим или генноинженерным путем 6. Антиаллотипические или антиидиотипические антитела 7. Меченные или связанные с твердым носителем
Характеристики используемых антител 1. Поли или моноклональные антитела 2. Различного типа (Jg G или Jg М) и подтипа (Jg G 1 или Jg G 2 a) 3. Моно- или поливалентные 4. Моно- или биспецифические 5. Нативные или полученные химическим или генноинженерным путем 6. Антиаллотипические или антиидиотипические антитела 7. Меченные или связанные с твердым носителем
 1 2 1 2
1 2 1 2
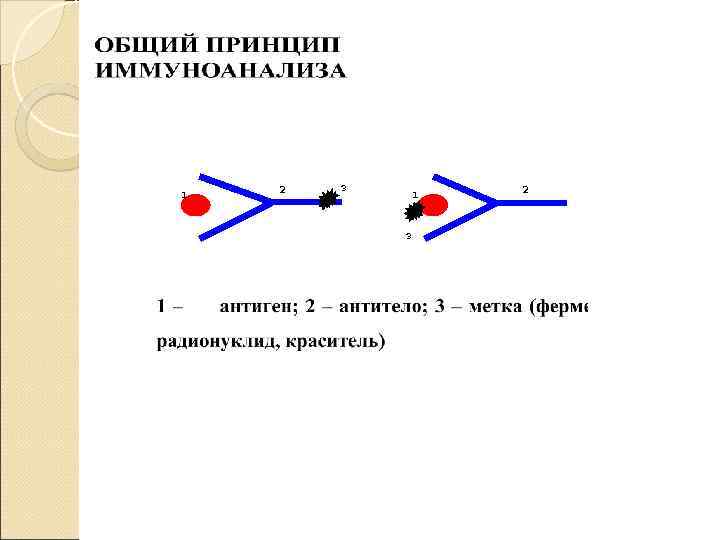
 ТИП ПРИМЕНЯЕМОЙ МЕТКИ ЧАСТИЦЫ (ЭРИТРОЦИТЫ, ЛАТЕКС) ЗОЛИ МЕТАЛЛОВ (КОЛЛОИДНОЕ ЗОЛОТО) РАДИОНУКЛИДЫ (ЙОД-125) ФЕРМЕНТЫ, СУБСТРАТЫ, КО-ФАКТОРЫ (ПЕРОКСИДАЗА ХРЕНА, -ГАЛАКТОЗИДАЗА) ПОТЕНЦИАЛЬНЫЕ ЛЮМИНОФОРЫ (ЭФИРЫ АКРИДИНА, ФЛУОРЕСЦЕИН) ЭЛЕКТРОХИМИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА (ДИМЕТИЛАМИНОМЕТИЛФЕРРОЦЕН)
ТИП ПРИМЕНЯЕМОЙ МЕТКИ ЧАСТИЦЫ (ЭРИТРОЦИТЫ, ЛАТЕКС) ЗОЛИ МЕТАЛЛОВ (КОЛЛОИДНОЕ ЗОЛОТО) РАДИОНУКЛИДЫ (ЙОД-125) ФЕРМЕНТЫ, СУБСТРАТЫ, КО-ФАКТОРЫ (ПЕРОКСИДАЗА ХРЕНА, -ГАЛАКТОЗИДАЗА) ПОТЕНЦИАЛЬНЫЕ ЛЮМИНОФОРЫ (ЭФИРЫ АКРИДИНА, ФЛУОРЕСЦЕИН) ЭЛЕКТРОХИМИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА (ДИМЕТИЛАМИНОМЕТИЛФЕРРОЦЕН)
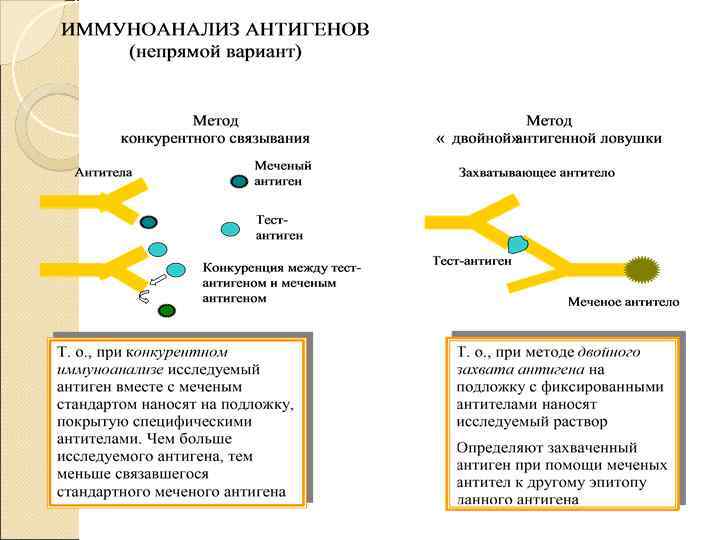
 Основа метода 1. Конкурентное связывание: в системе одновременно присутствует анализируемое соединение и его меченное аналог, конкурирующие за ограниченное количество центров специфического связывания, (выполняется в условиях ограниченного количества реагента) 2. Неконкурентное связывание: в системе присутствует только анализируемое соединение и специфическое ему антитело (анализ выполняется в условиях избытка реагента), «сэндвич» -метод (двойной антигенной ловушки); 3. Неравновесный режим: используется одна антигенная детерминанта и строго контролируемый избыток реагента.
Основа метода 1. Конкурентное связывание: в системе одновременно присутствует анализируемое соединение и его меченное аналог, конкурирующие за ограниченное количество центров специфического связывания, (выполняется в условиях ограниченного количества реагента) 2. Неконкурентное связывание: в системе присутствует только анализируемое соединение и специфическое ему антитело (анализ выполняется в условиях избытка реагента), «сэндвич» -метод (двойной антигенной ловушки); 3. Неравновесный режим: используется одна антигенная детерминанта и строго контролируемый избыток реагента.
 Результат исследования
Результат исследования
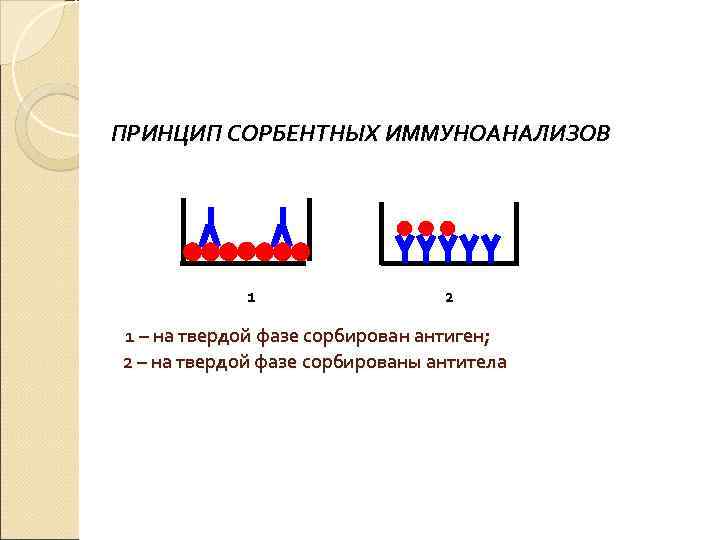 ПРИНЦИП СОРБЕНТНЫХ ИММУНОАНАЛИЗОВ 1 2 1 – на твердой фазе сорбирован антиген; 2 – на твердой фазе сорбированы антитела
ПРИНЦИП СОРБЕНТНЫХ ИММУНОАНАЛИЗОВ 1 2 1 – на твердой фазе сорбирован антиген; 2 – на твердой фазе сорбированы антитела
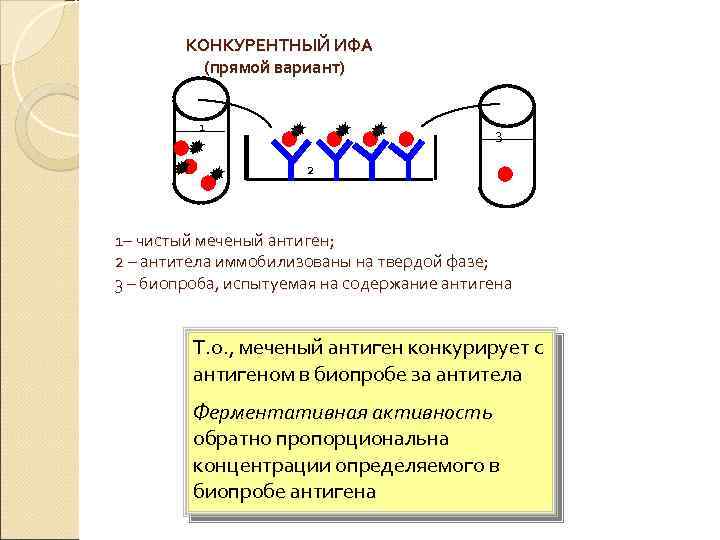 КОНКУРЕНТНЫЙ ИФА (прямой вариант) 1 3 2 1– чистый меченый антиген; 2 – антитела иммобилизованы на твердой фазе; 3 – биопроба, испытуемая на содержание антигена Т. о. , меченый антиген конкурирует с антигеном в биопробе за антитела Ферментативная активность обратно пропорциональна концентрации определяемого в биопробе антигена
КОНКУРЕНТНЫЙ ИФА (прямой вариант) 1 3 2 1– чистый меченый антиген; 2 – антитела иммобилизованы на твердой фазе; 3 – биопроба, испытуемая на содержание антигена Т. о. , меченый антиген конкурирует с антигеном в биопробе за антитела Ферментативная активность обратно пропорциональна концентрации определяемого в биопробе антигена
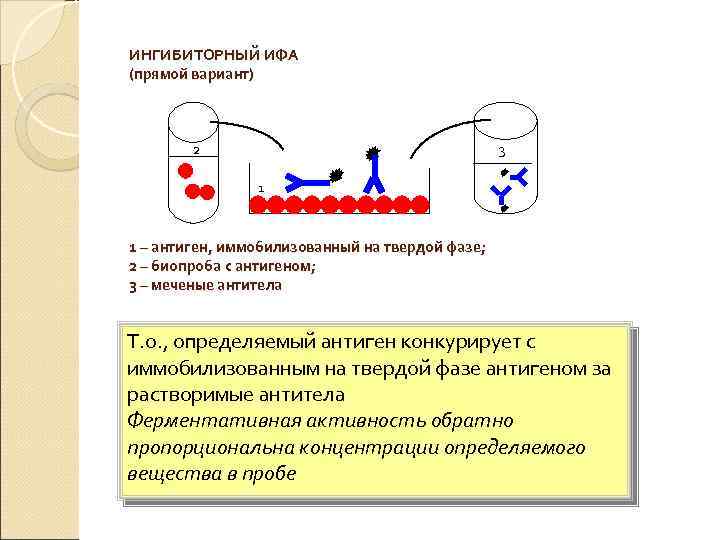 ИНГИБИТОРНЫЙ ИФА (прямой вариант) 3 2 1 1 – антиген, иммобилизованный на твердой фазе; 2 – биопроба с антигеном; 3 – меченые антитела Т. о. , определяемый антиген конкурирует с иммобилизованным на твердой фазе антигеном за растворимые антитела Ферментативная активность обратно пропорциональна концентрации определяемого вещества в пробе
ИНГИБИТОРНЫЙ ИФА (прямой вариант) 3 2 1 1 – антиген, иммобилизованный на твердой фазе; 2 – биопроба с антигеном; 3 – меченые антитела Т. о. , определяемый антиген конкурирует с иммобилизованным на твердой фазе антигеном за растворимые антитела Ферментативная активность обратно пропорциональна концентрации определяемого вещества в пробе
 Инструментальные иммунохимические методы Иммуноферментный метод анализа (ИФА) гомогенный вариант гетерогенный (сорбционный) вариант Поляризационный флуороиммуноанализ (ПФИА)
Инструментальные иммунохимические методы Иммуноферментный метод анализа (ИФА) гомогенный вариант гетерогенный (сорбционный) вариант Поляризационный флуороиммуноанализ (ПФИА)
 Иммуноферментный метод анализа
Иммуноферментный метод анализа



 ПФИА технология Поляризационный флуоресцентный иммуноанализ технология ПФИА используется на анализаторах TDx и Ax. Sym
ПФИА технология Поляризационный флуоресцентный иммуноанализ технология ПФИА используется на анализаторах TDx и Ax. Sym
 АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ МЕТОДА ИФА ДОСТОИНСТВА ◦ СЕРИЙНОСТЬ И ЭКСПРЕССНОСТЬ (ГОМОГЕННЫЙ ВАРИАНТ) ◦ СТАБИЛЬНОСТЬ РЕАГЕНТОВ В ТЕЧЕНИЕ ГОДА ◦ ВЫСОКАЯ ЧУВСТВИТЕЛЬНОСТЬ ГЕТЕРОГЕННЫЙ ВАРИАНТ ДО 10 НГ/МЛ ГОМОГЕННЫЙ ВАРИАНТ ДО 300 -500 НГ/МЛ НЕДОСТАТКИ ◦ ВОЗМОЖНОСТЬ ЛОЖНОПОЛОЖИТЕЛЬНЫХ РЕЗУЛЬТАТОВ ◦ ГРУППОВОЙ АНАЛИЗ ◦ ВЛИЯНИЕ ТЕМПЕРАТУРЫ, КАК ПРИ ХРАНЕНИИ РЕАГЕНТОВ, ТАК И НА ПРОТЕКАНИЕ ПРОЦЕССОВ ПРИ АНАЛИЗЕ ◦ ВЛИЯНИЕ р. Н СРЕДЫ ◦ НЕПРЕРЫВНОСТЬ СТАДИЙ ◦ ТРУДНОСТЬ АВТОМАТИЗАЦИИ В ГЕТЕРОГЕННОМ ВАРИАНТЕ ◦ ДЛИТЕЛЬНОСТЬ АНАЛИЗА В ГЕТЕРОГЕННОМ ВАРИАНТЕ ◦ ИЗМЕНЕНИЕ ФЕРМЕНТАТИВНОЙ АКТИВНОСТИ ПРИ ВОЗМОЖНОМ ЗАГРЯЗНЕНИИ ◦ ВЫСОКИЙ ПРОЦЕНТ СУБЪЕКТИВНЫХ ОШИБОК
АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ МЕТОДА ИФА ДОСТОИНСТВА ◦ СЕРИЙНОСТЬ И ЭКСПРЕССНОСТЬ (ГОМОГЕННЫЙ ВАРИАНТ) ◦ СТАБИЛЬНОСТЬ РЕАГЕНТОВ В ТЕЧЕНИЕ ГОДА ◦ ВЫСОКАЯ ЧУВСТВИТЕЛЬНОСТЬ ГЕТЕРОГЕННЫЙ ВАРИАНТ ДО 10 НГ/МЛ ГОМОГЕННЫЙ ВАРИАНТ ДО 300 -500 НГ/МЛ НЕДОСТАТКИ ◦ ВОЗМОЖНОСТЬ ЛОЖНОПОЛОЖИТЕЛЬНЫХ РЕЗУЛЬТАТОВ ◦ ГРУППОВОЙ АНАЛИЗ ◦ ВЛИЯНИЕ ТЕМПЕРАТУРЫ, КАК ПРИ ХРАНЕНИИ РЕАГЕНТОВ, ТАК И НА ПРОТЕКАНИЕ ПРОЦЕССОВ ПРИ АНАЛИЗЕ ◦ ВЛИЯНИЕ р. Н СРЕДЫ ◦ НЕПРЕРЫВНОСТЬ СТАДИЙ ◦ ТРУДНОСТЬ АВТОМАТИЗАЦИИ В ГЕТЕРОГЕННОМ ВАРИАНТЕ ◦ ДЛИТЕЛЬНОСТЬ АНАЛИЗА В ГЕТЕРОГЕННОМ ВАРИАНТЕ ◦ ИЗМЕНЕНИЕ ФЕРМЕНТАТИВНОЙ АКТИВНОСТИ ПРИ ВОЗМОЖНОМ ЗАГРЯЗНЕНИИ ◦ ВЫСОКИЙ ПРОЦЕНТ СУБЪЕКТИВНЫХ ОШИБОК
 Иммунохроматографические методы (ИХА) – основе лежит принцип непрямого конкурентного взаимодействия между сорбированным на тест-полоске антигеном и антигеном в биологической жидкости за центры связывания с меченным антителом (коллоидное золото).
Иммунохроматографические методы (ИХА) – основе лежит принцип непрямого конкурентного взаимодействия между сорбированным на тест-полоске антигеном и антигеном в биологической жидкости за центры связывания с меченным антителом (коллоидное золото).
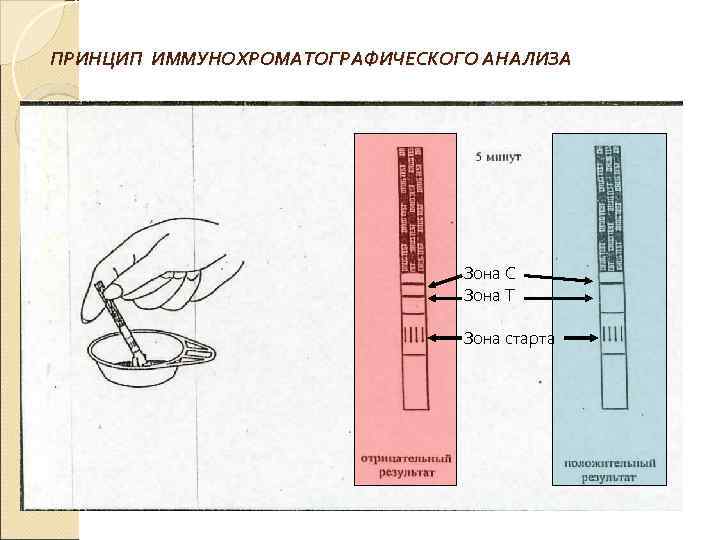 ПРИНЦИП ИММУНОХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА Зона С Зона Т Зона старта
ПРИНЦИП ИММУНОХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА Зона С Зона Т Зона старта
 АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ МЕТОДА ИХА ДОСТОИНСТВА ◦ ОТСУТСТВИЕ ПРОБОПОДГОТОВКИ И КОНЦЕНТРИРОВАНИЯ ◦ ВЫСОКАЯ ЧУВСТВИТЕЛЬНОСТЬ (на осн. гр. 300 -500 НГ/МЛ) ◦ ОПРЕДЕЛЯЮТСЯ ОСНОВНЫЕ ГРУППЫ НАРКОТИЧЕСКИХ СРЕДСТВ (КРОМЕ ЛСД) И ПСИХОТРОПНЫХ ВЕЩЕСТВ. ◦ ПРОСТ И БЫСТР В ИСПОЛЬЗОВАНИИ ◦ НЕ ТРЕБУЕТ ТОЧНОГО ДОЗИРОВАНИЯ ПРОБ И РЕАГЕНТОВ И ИСПОЛЬЗУЮТСЯ ИХ МАЛЫЕ КОЛИЧЕСТВА ◦ РЕАГЕНТЫ СТАБИЛЬНЫ В ТЕЧЕНИЕ 1, 5 ЛЕТ ◦ ПРОСТОТА В ИНТЕРПРЕТАЦИИ РЕЗУЛЬТАТА НЕДОСТАТКИ ◦ НИЗКАЯ СПЕЦИФИЧНОСТЬ ВЕДЕТ К УВЕЛИЧЕНИЮ ЛОЖНОПОЛОЖИТЕЛЬНЫХ РЕЗУЛЬТАТОВ ◦ ГРУППОВОЙ АНАЛИЗ ◦ ВЫСОКАЯ ВЕРОЯТНОСТЬ ФАЛЬСИФИКАЦИИ РЕЗУЛЬТАТОВ
АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ МЕТОДА ИХА ДОСТОИНСТВА ◦ ОТСУТСТВИЕ ПРОБОПОДГОТОВКИ И КОНЦЕНТРИРОВАНИЯ ◦ ВЫСОКАЯ ЧУВСТВИТЕЛЬНОСТЬ (на осн. гр. 300 -500 НГ/МЛ) ◦ ОПРЕДЕЛЯЮТСЯ ОСНОВНЫЕ ГРУППЫ НАРКОТИЧЕСКИХ СРЕДСТВ (КРОМЕ ЛСД) И ПСИХОТРОПНЫХ ВЕЩЕСТВ. ◦ ПРОСТ И БЫСТР В ИСПОЛЬЗОВАНИИ ◦ НЕ ТРЕБУЕТ ТОЧНОГО ДОЗИРОВАНИЯ ПРОБ И РЕАГЕНТОВ И ИСПОЛЬЗУЮТСЯ ИХ МАЛЫЕ КОЛИЧЕСТВА ◦ РЕАГЕНТЫ СТАБИЛЬНЫ В ТЕЧЕНИЕ 1, 5 ЛЕТ ◦ ПРОСТОТА В ИНТЕРПРЕТАЦИИ РЕЗУЛЬТАТА НЕДОСТАТКИ ◦ НИЗКАЯ СПЕЦИФИЧНОСТЬ ВЕДЕТ К УВЕЛИЧЕНИЮ ЛОЖНОПОЛОЖИТЕЛЬНЫХ РЕЗУЛЬТАТОВ ◦ ГРУППОВОЙ АНАЛИЗ ◦ ВЫСОКАЯ ВЕРОЯТНОСТЬ ФАЛЬСИФИКАЦИИ РЕЗУЛЬТАТОВ
 Применение массспектрометрических методов анализа
Применение массспектрометрических методов анализа
 Определение Масс-спектрометрия - физико-химический метод анализа, заключающийся в переводе молекул образца в ионизованную форму с последующим разделением и регистрацией образующихся при этом положительных или отрицательных ионов. Масс-спектр – зависимость интенсивности сигнала детектора от отношения массы иона к его заряду. Единица размерности – Дальтон (Да).
Определение Масс-спектрометрия - физико-химический метод анализа, заключающийся в переводе молекул образца в ионизованную форму с последующим разделением и регистрацией образующихся при этом положительных или отрицательных ионов. Масс-спектр – зависимость интенсивности сигнала детектора от отношения массы иона к его заряду. Единица размерности – Дальтон (Да).
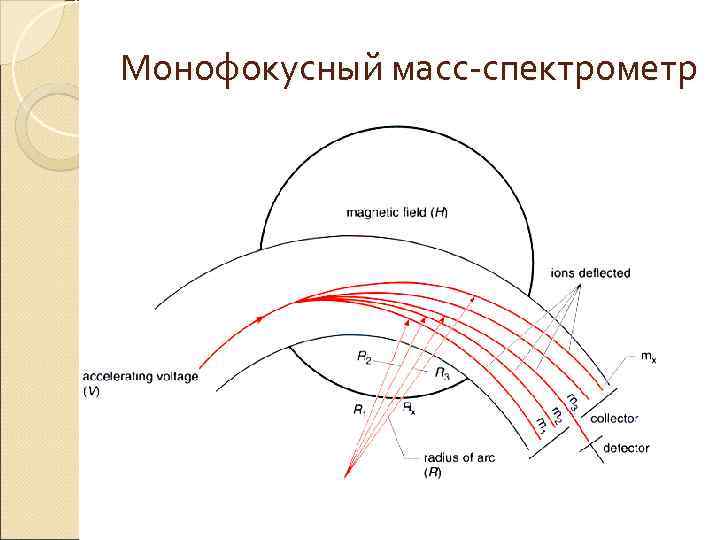 Монофокусный масс-спектрометр
Монофокусный масс-спектрометр
 Возможности метода Позволяет получить информацию о: молекулярной массе (пик молекулярного иона), элементному и изотопному составу (пик молекулярного иона, базовые, осколочные пики), структуре исследуемого органического вещества по фрагментам и характеристичным группам (базовые и осколочные пики, ),
Возможности метода Позволяет получить информацию о: молекулярной массе (пик молекулярного иона), элементному и изотопному составу (пик молекулярного иона, базовые, осколочные пики), структуре исследуемого органического вещества по фрагментам и характеристичным группам (базовые и осколочные пики, ),
 продолжение Качественный и количественный анализ. Чувствительность рутинного анализа – фемтограммы (10 -15 г) или септомоли(10 -21 моль). Металлургия, химия, биология, полупроводниковая техника, геология, экология и …. Точность определения массы – измеряется в ppm; погрешность - Mass Error = (5 ppm)(201. 1001)/106 = 0. 0010 amu ( от 201. 0991 до 201. 1011 – только один возможный брутто-состав).
продолжение Качественный и количественный анализ. Чувствительность рутинного анализа – фемтограммы (10 -15 г) или септомоли(10 -21 моль). Металлургия, химия, биология, полупроводниковая техника, геология, экология и …. Точность определения массы – измеряется в ppm; погрешность - Mass Error = (5 ppm)(201. 1001)/106 = 0. 0010 amu ( от 201. 0991 до 201. 1011 – только один возможный брутто-состав).
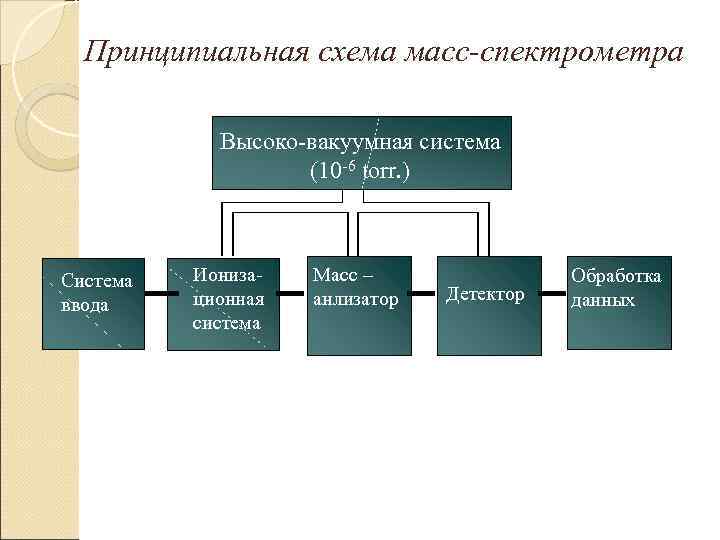 Принципиальная схема масс-спектрометра Высоко-вакуумная система (10 -6 torr. ) Система ввода Ионизационная система Масс – анлизатор Детектор Обработка данных
Принципиальная схема масс-спектрометра Высоко-вакуумная система (10 -6 torr. ) Система ввода Ионизационная система Масс – анлизатор Детектор Обработка данных
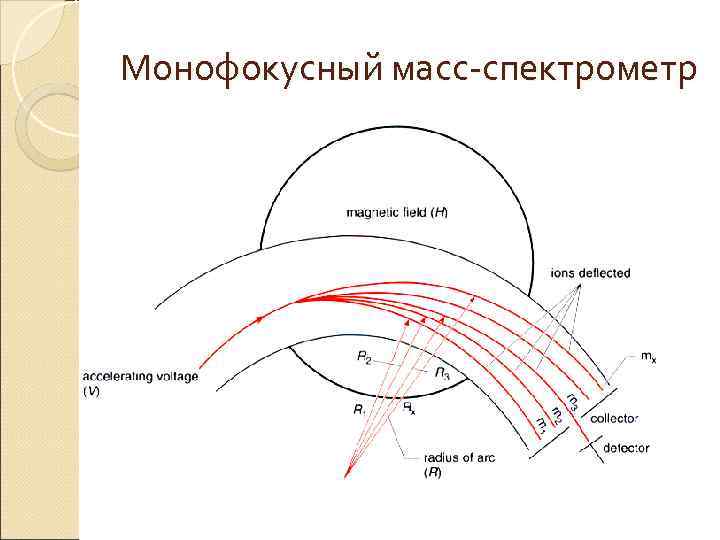 Монофокусный масс-спектрометр
Монофокусный масс-спектрометр
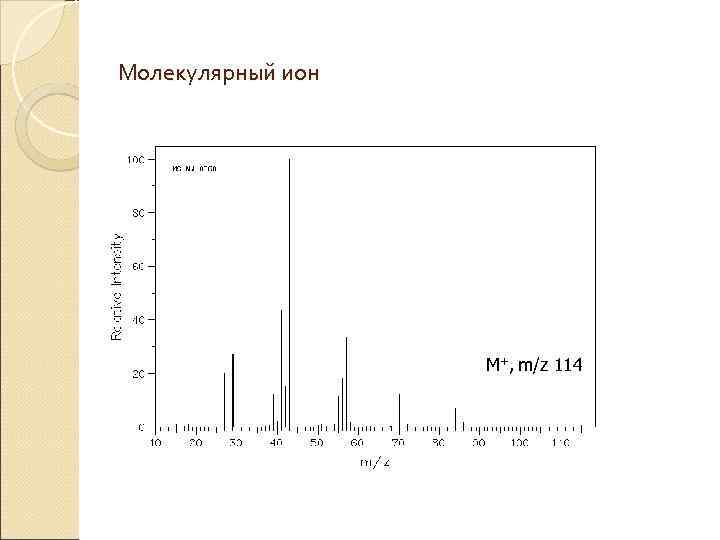 Молекулярный ион M+, m/z 114
Молекулярный ион M+, m/z 114
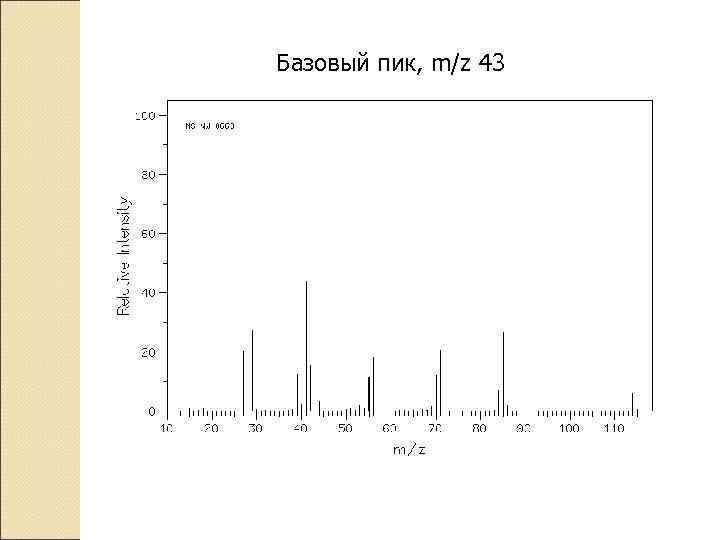 Базовый пик, m/z 43
Базовый пик, m/z 43
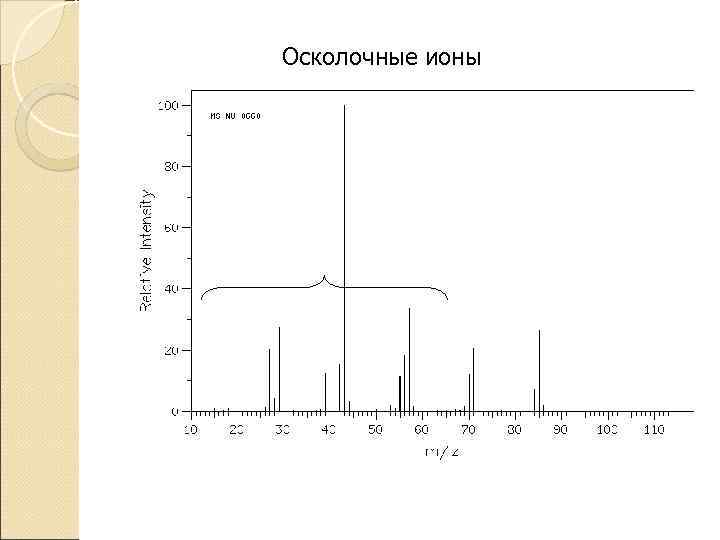 Осколочные ионы
Осколочные ионы
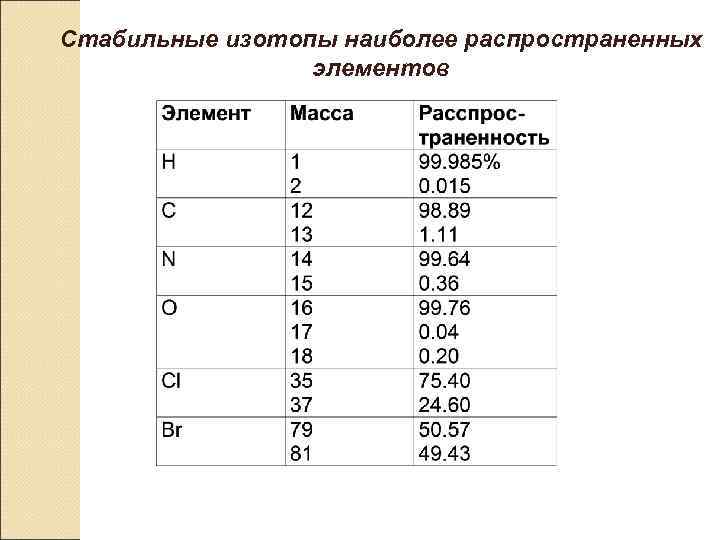 Стабильные изотопы наиболее распространенных элементов
Стабильные изотопы наиболее распространенных элементов
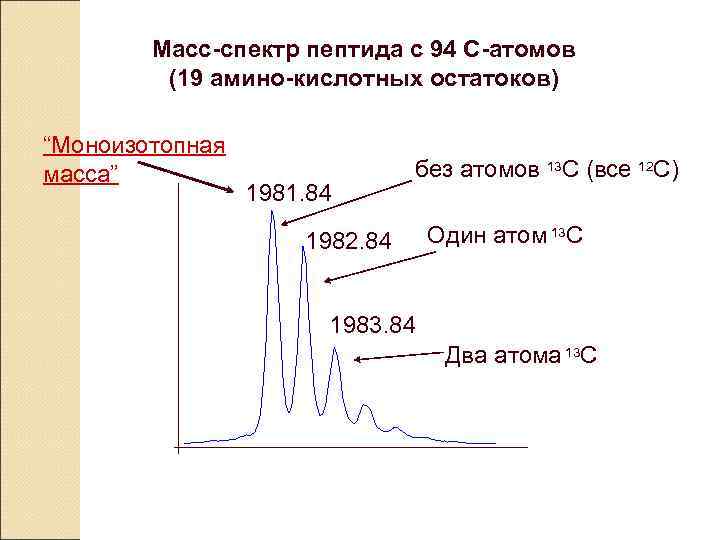 Масс-спектр пептида с 94 C-атомов (19 амино-кислотных остатоков) “Моноизотопная масса” 1981. 84 без атомов 13 C (все 12 C) 1982. 84 Один атом 13 C 1983. 84 Два атома 13 C
Масс-спектр пептида с 94 C-атомов (19 амино-кислотных остатоков) “Моноизотопная масса” 1981. 84 без атомов 13 C (все 12 C) 1982. 84 Один атом 13 C 1983. 84 Два атома 13 C
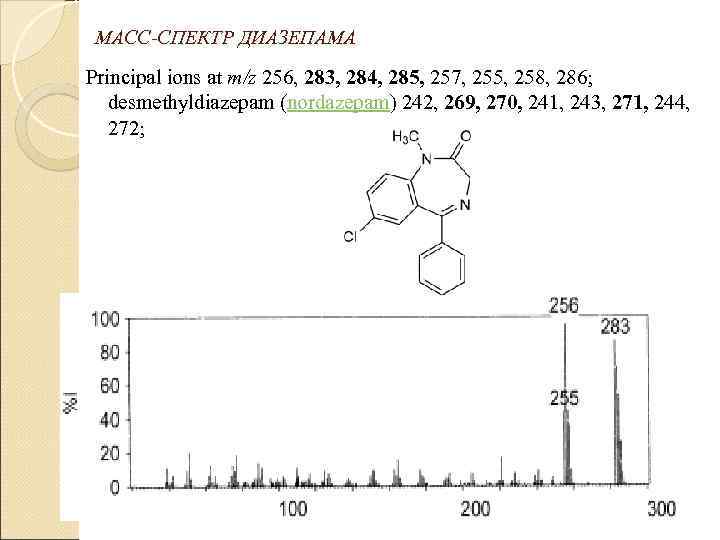 МАСС-СПЕКТР ДИАЗЕПАМА Principal ions at m/z 256, 283, 284, 285, 257, 255, 258, 286; desmethyldiazepam (nordazepam) 242, 269, 270, 241, 243, 271, 244, 272;
МАСС-СПЕКТР ДИАЗЕПАМА Principal ions at m/z 256, 283, 284, 285, 257, 255, 258, 286; desmethyldiazepam (nordazepam) 242, 269, 270, 241, 243, 271, 244, 272;
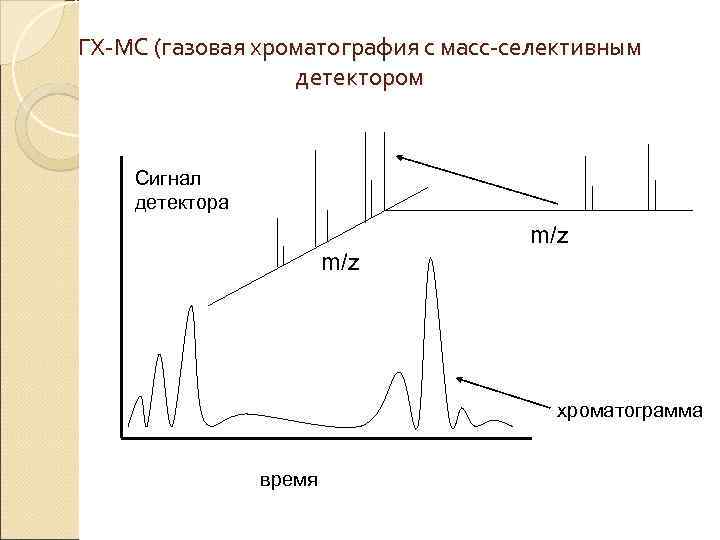 ГХ-МС (газовая хроматография с масс-селективным детектором Сигнал детектора m/z хроматограмма время
ГХ-МС (газовая хроматография с масс-селективным детектором Сигнал детектора m/z хроматограмма время
 Масс-спектрометрия высокого разрешения Измерение точной массы иона (4 -6 знаков после запятой) однозначно определяет его элементный и изотопный состав. Обычно используется в системах ионизации: электроспрей, МАЛДИ; системах разделения ионов: времяпролетный, ионная ловушка. В процессе эксперимента необходимо использовать стандарт массы.
Масс-спектрометрия высокого разрешения Измерение точной массы иона (4 -6 знаков после запятой) однозначно определяет его элементный и изотопный состав. Обычно используется в системах ионизации: электроспрей, МАЛДИ; системах разделения ионов: времяпролетный, ионная ловушка. В процессе эксперимента необходимо использовать стандарт массы.
 LC-ion trap GC-TOF LC-ion trap – FT-ICR
LC-ion trap GC-TOF LC-ion trap – FT-ICR
 Нобелевская премия по химии 2002 “. . . for their developments of soft desorption ionisation methods for mass spectrometric analysis of biological macromolecules”. 1/4 to John B. Fenn (USA) 1/4 to Koichi Tanaka (Japan) Virginia Commonwealth University Shimadzu. Corp. Kyoto Electrospray Laser Ionization
Нобелевская премия по химии 2002 “. . . for their developments of soft desorption ionisation methods for mass spectrometric analysis of biological macromolecules”. 1/4 to John B. Fenn (USA) 1/4 to Koichi Tanaka (Japan) Virginia Commonwealth University Shimadzu. Corp. Kyoto Electrospray Laser Ionization
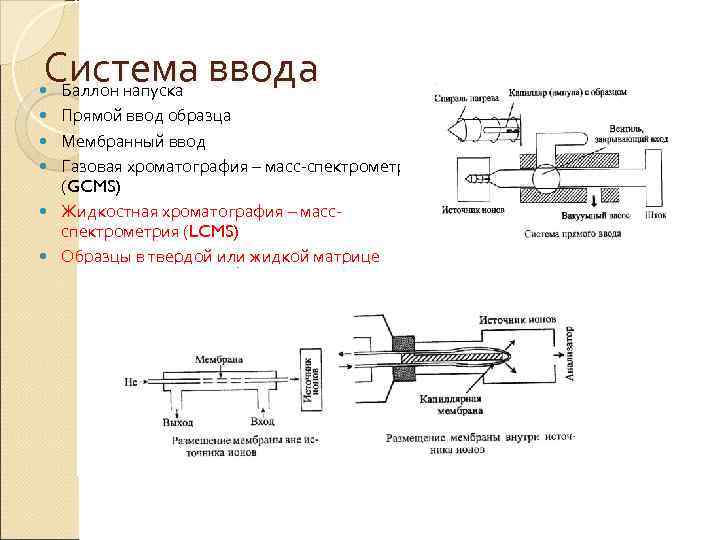 Система ввода Баллон напуска Прямой ввод образца Мембранный ввод Газовая хроматография – масс-спектрометрия (GCMS) Жидкостная хроматография – массспектрометрия (LCMS) Образцы в твердой или жидкой матрице
Система ввода Баллон напуска Прямой ввод образца Мембранный ввод Газовая хроматография – масс-спектрометрия (GCMS) Жидкостная хроматография – массспектрометрия (LCMS) Образцы в твердой или жидкой матрице


