Варианты биосенсоров.ppt
- Количество слайдов: 56

Приклади біоселективних елементів ферментних біосенсорів для прямого та інгібіторного визначення аналітів в харчовій промисловості та с/г Лабораторія біомолекулярної електроніки Солдаткін О. П. 1
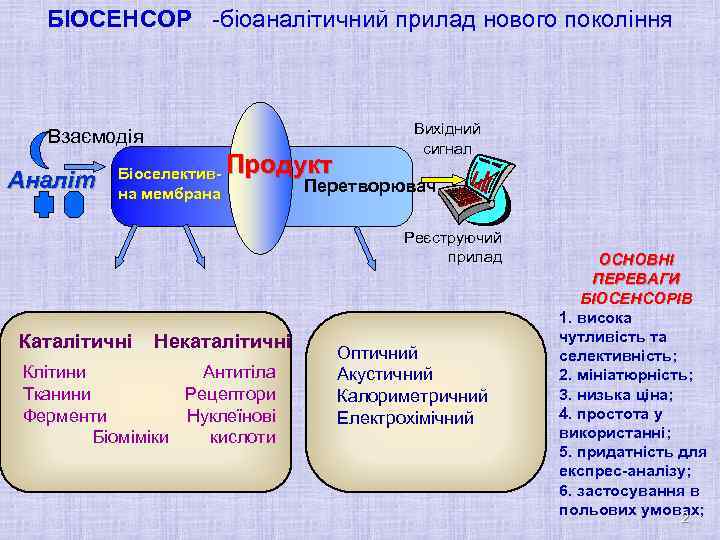
БІОСЕНСОР -біоаналітичний прилад нового покоління Взаємодія Аналіт Біоселективна мембрана Продукт Вихідний сигнал Перетворювач Реєструючий прилад Каталітичні Некаталітичні Клітини Антитіла Тканини Рецептори Ферменти Нуклеїнові Біоміміки кислоти Оптичний Акустичний Калориметричний Електрохімічний ОСНОВНІ ПЕРЕВАГИ БІОСЕНСОРІВ 1. висока чутливість та селективність; 2. мініатюрність; 3. низька ціна; 4. простота у використанні; 5. придатність для експрес-аналізу; 6. застосування в польових умовах; 2 2

Біоселективний розпізнавальний елемент – це один із ключових елементів любого біосенсора, він визначає його здатність відповідати селективно на наявність певного аналіту чи групи аналітів в аналізованому зразку запобігаючи інтерференції інших речовин. Біоселективний елемент повинен бути в тісному контакті з перетворювачем, що досягається іммобілізацією. 3

Приклади біоселективних елементів: Каталітичного типу 1) 2) 3) 4) 5) 6) На основі ферментів: а) для прямого визначення субстратів; б) для інгібіторного визначення токсичних речовин; в) для визначення реактиваторів ферментів. На основі клітин мікроорганізмів; На основі клітинних органел (хлоропластів, наприклад); На основі матричних полімерів- біоміміків. 4
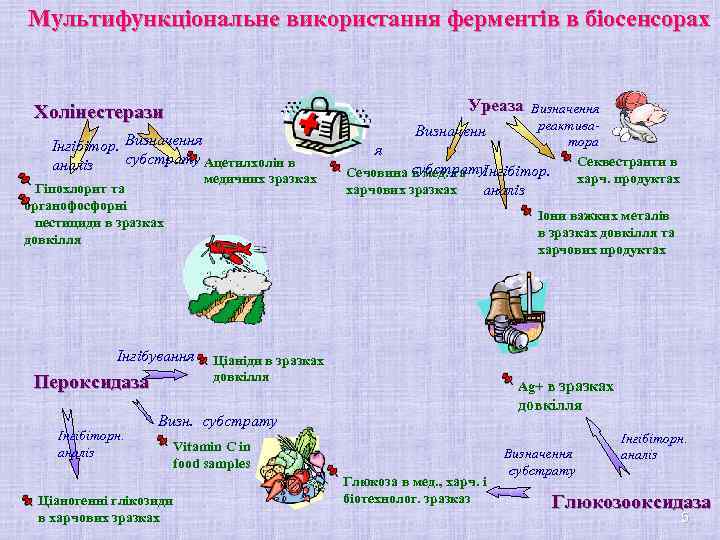
Мультифункціональне використання ферментів в біосенсорах Уреаза Холінестерази Інгібітор. Визначення субстрату Ацетилхолін в аналіз медичних зразках Гіпохлорит та органофосфорні пестициди в зразках довкілля Іони важких металів в зразках довкілля та харчових продуктах Інгібування Пероксидаза Інгібіторн. аналіз Визначення реактива. Визначенн тора я Секвестранти в Сечовина субстрату в мед. та Інгібітор. харч. продуктах харчових зразках аналіз Ціаніди в зразках довкілля Ag+ в зразках довкілля Визн. субстрату Vitamin C in food samples Ціаногенні глікозиди в харчових зразках Глюкоза в мед. , харч. і біотехнолог. зразказ Визначення субстрату Інгібіторн. аналіз Глюкозооксидаза 5
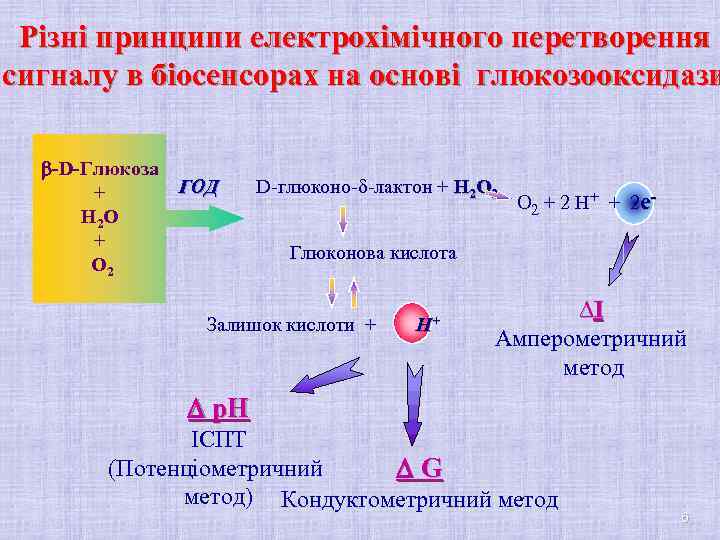
Різні принципи електрохімічного перетворення сигналу в біосенсорах на основі глюкозооксидази b-D-Глюкоза + H 2 O + O 2 ГОД D-глюконо-d-лактон + H 2 O 2 + 2 H + + 2 e - Глюконова кислота Залишок кислоти + H+ DI Амперометричний метод D p. H ІСПТ (Потенціометричний DG метод) Кондуктометричний метод 6

Розробка амперометричних ферментних біосенсорів для контролю якості напоїв у виноробстві (соки, виноградне сусло, тощо) Ферменти – гліцеролоксидаза, лактатоксидаза, алкогольоксидаза глюкозооксидаза, Перетворювачі - амперометричні електроди Аналіти – гліцерол, глюкоза, лактат, етанол 7
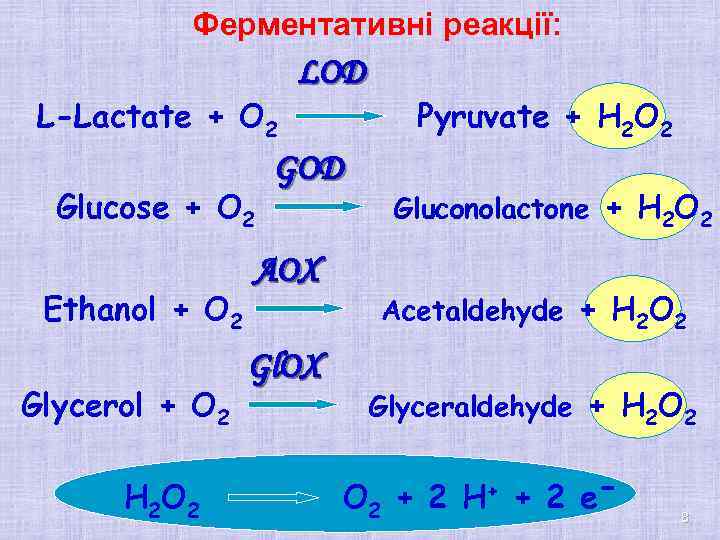
Ферментативні реакції: L-Lactate + О 2 Glucose + О 2 Ethanol + О 2 Glycerol + О 2 Н 2 О 2 LОД GОД AOX Gl. OX Pyruvate + Н 2 О 2 Gluconolactone + Н 2 О 2 Acetaldehyde + Н 2 О 2 Glyceraldehyde + Н 2 О 2 + 2 Н+ + 2 eˉ 8
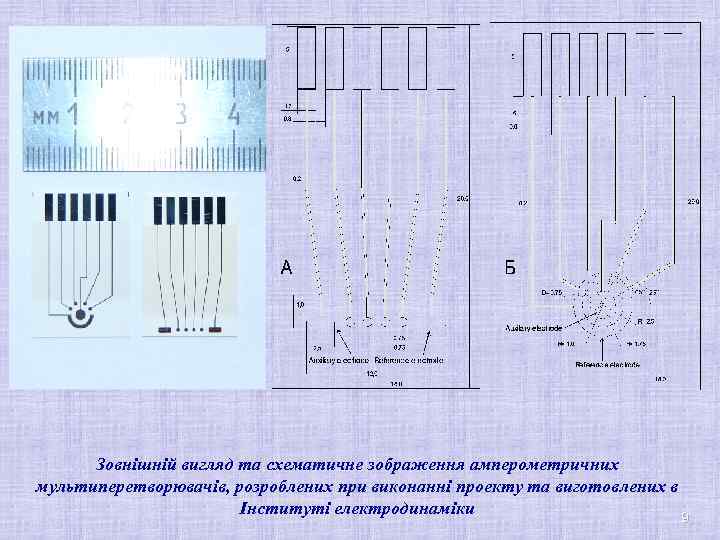
Зовнішній вигляд та схематичне зображення амперометричних мультиперетворювачів, розроблених при виконанні проекту та виготовлених в Інституті електродинаміки 9 9
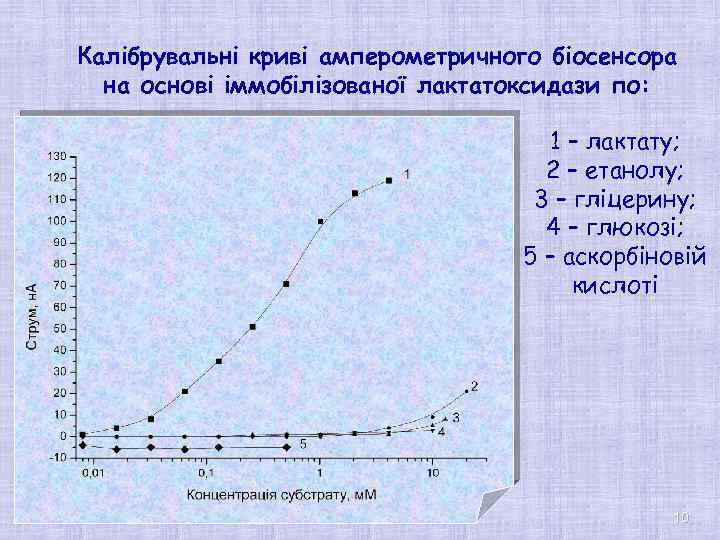
Калібрувальні криві амперометричного біосенсора на основі іммобілізованої лактатоксидази по: 1 – лактату; 2 – етанолу; 3 – гліцерину; 4 – глюкозі; 5 – аскорбіновій кислоті 10
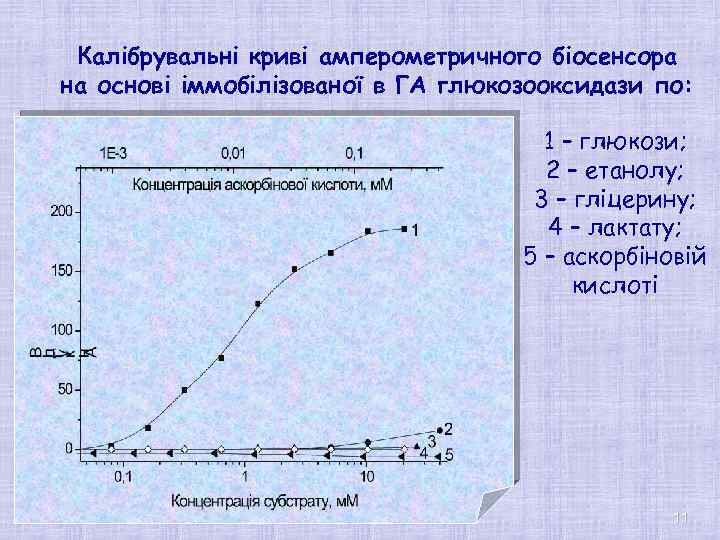
Калібрувальні криві амперометричного біосенсора на основі іммобілізованої в ГА глюкозооксидази по: 1 – глюкози; 2 – етанолу; 3 – гліцерину; 4 – лактату; 5 – аскорбіновій кислоті 11
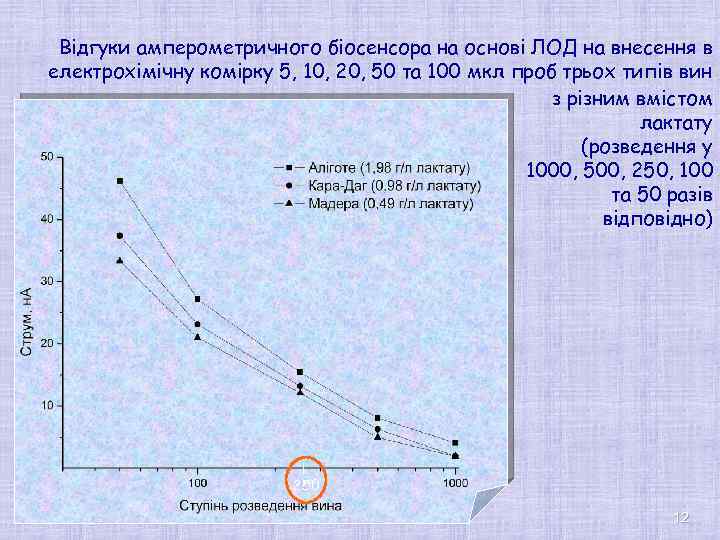
Відгуки амперометричного біосенсора на основі ЛОД на внесення в електрохімічну комірку 5, 10, 20, 50 та 100 мкл проб трьох типів вин з різним вмістом лактату (розведення у 1000, 500, 250, 100 та 50 разів відповідно) 250 12
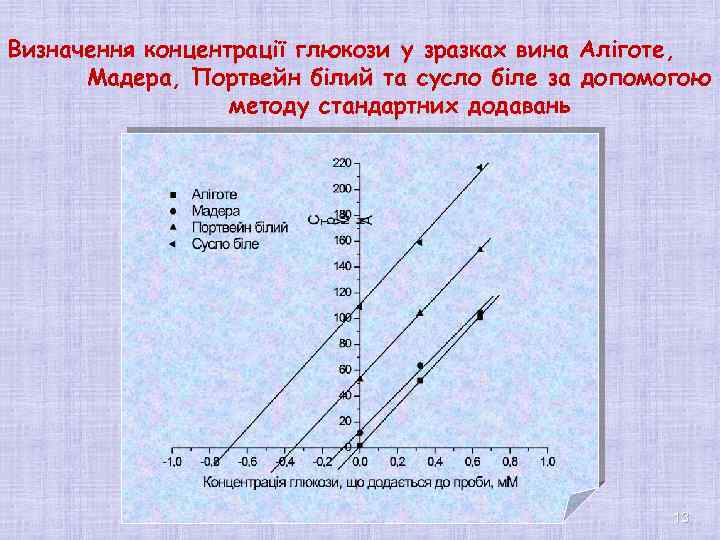
Визначення концентрації глюкози у зразках вина Аліготе, Мадера, Портвейн білий та сусло біле за допомогою методу стандартних додавань 13
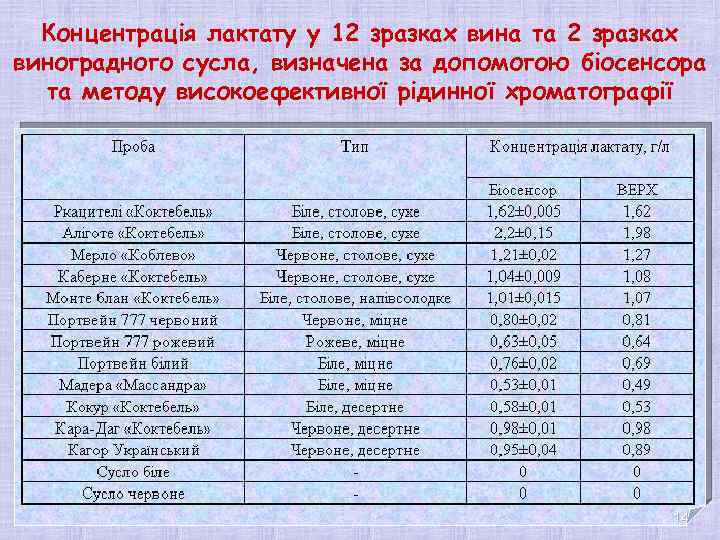
Концентрація лактату у 12 зразках вина та 2 зразках виноградного сусла, визначена за допомогою біосенсора та методу високоефективної рідинної хроматографії 14
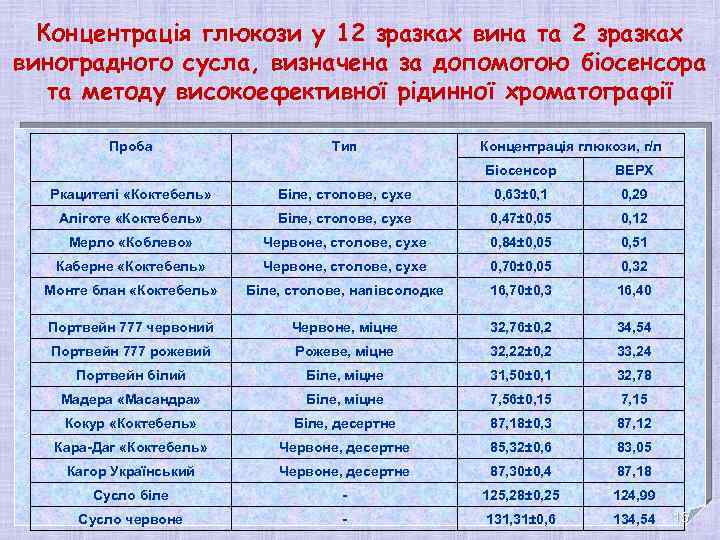
Концентрація глюкози у 12 зразках вина та 2 зразках виноградного сусла, визначена за допомогою біосенсора та методу високоефективної рідинної хроматографії Проба Тип Концентрація глюкози, г/л Біосенсор ВЕРХ Ркацителі «Коктебель» Біле, столове, сухе 0, 63± 0, 1 0, 29 Аліготе «Коктебель» Біле, столове, сухе 0, 47± 0, 05 0, 12 Мерло «Коблево» Червоне, столове, сухе 0, 84± 0, 05 0, 51 Каберне «Коктебель» Червоне, столове, сухе 0, 70± 0, 05 0, 32 Монте блан «Коктебель» Біле, столове, напівсолодке 16, 70± 0, 3 16, 40 Портвейн 777 червоний Червоне, міцне 32, 76± 0, 2 34, 54 Портвейн 777 рожевий Рожеве, міцне 32, 22± 0, 2 33, 24 Портвейн білий Біле, міцне 31, 50± 0, 1 32, 78 Мадера «Масандра» Біле, міцне 7, 56± 0, 15 7, 15 Кокур «Коктебель» Біле, десертне 87, 18± 0, 3 87, 12 Кара-Даг «Коктебель» Червоне, десертне 85, 32± 0, 6 83, 05 Кагор Український Червоне, десертне 87, 30± 0, 4 87, 18 Сусло біле - 125, 28± 0, 25 124, 99 Сусло червоне - 131, 31± 0, 6 134, 54 15
Комп’ютеризована установка, розроблена в Україні, для роботи з масивом амперометричних перетворювачів 16

Розробка кондуктометричних ферментних біосенсорів для визначення сахарів 17

Зовнішній вигляд кондуктометричних планарних гребінчатих перетворювачів 18

Принцип роботи ферментного біосенсора для визначення лактози β-галактозидаза (Е. С. 3. 2. 1. 23) лактоза + Н 2 О галактоза + α-D-глюкоза мутаротаза (Е. С. 5. 1. 3. 3) α-D-глюкоза β-D-глюкоза глюкозооксидаза (Е. С. 1. 1. 3. 4) β-D-глюкоза + О 2 D-глюконолактон + Н 2 О 2 D-глюконова кислота + Н 2 О залишок кислоти + Н+ 19
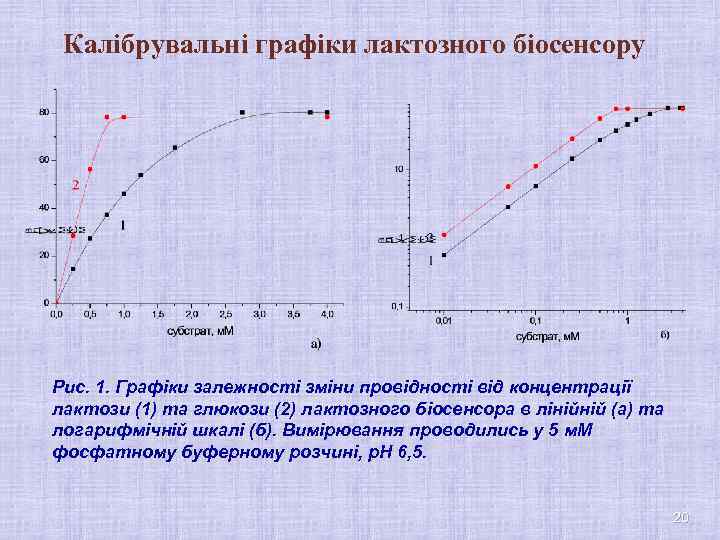
Калібрувальні графіки лактозного біосенсору Рис. 1. Графіки залежності зміни провідності від концентрації лактози (1) та глюкози (2) лактозного біосенсора в лінійній (а) та логарифмічній шкалі (б). Вимірювання проводились у 5 м. М фосфатному буферному розчині, р. Н 6, 5. 20
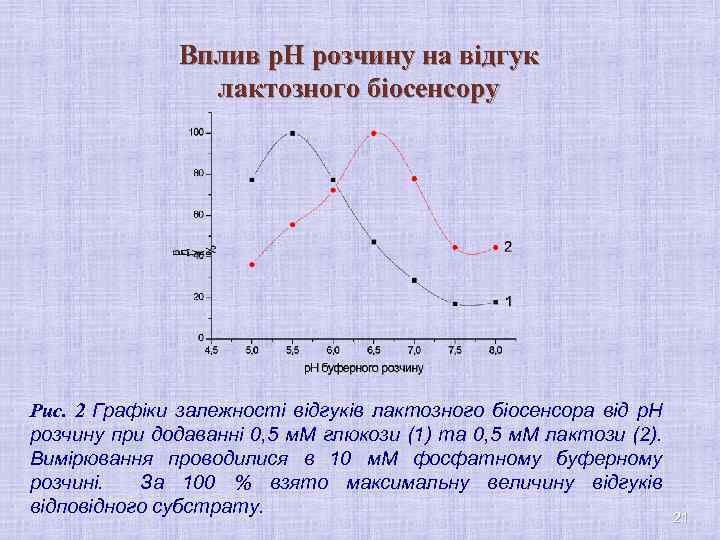
Вплив р. Н розчину на відгук лактозного біосенсору Рис. 2 Графіки залежності відгуків лактозного біосенсора від р. Н розчину при додаванні 0, 5 м. М глюкози (1) та 0, 5 м. М лактози (2). Вимірювання проводилися в 10 м. М фосфатному буферному розчині. За 100 % взято максимальну величину відгуків відповідного субстрату. 21
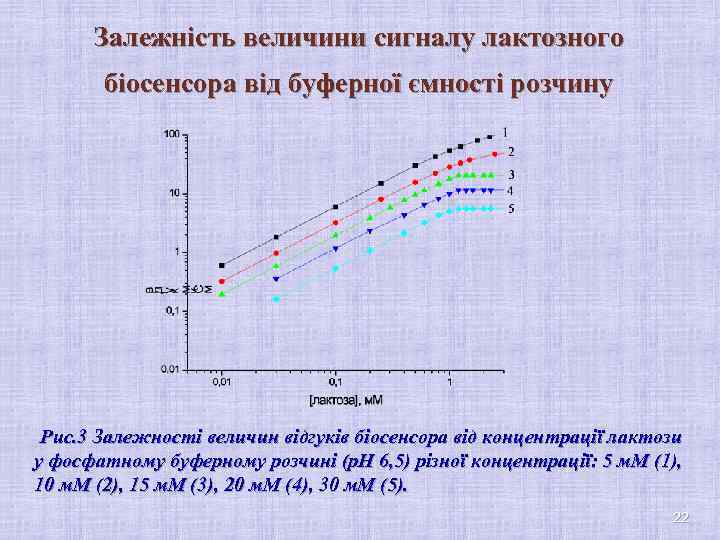
Залежність величини сигналу лактозного біосенсора від буферної ємності розчину Рис. 3 Залежності величин відгуків біосенсора від концентрації лактози у фосфатному буферному розчині (р. Н 6, 5) різної концентрації: 5 м. М (1), 10 м. М (2), 15 м. М (3), 20 м. М (4), 30 м. М (5). 22
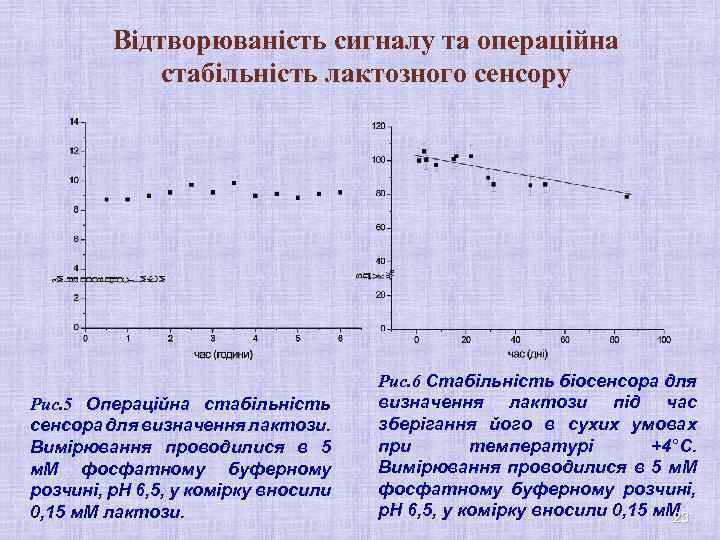
Відтворюваність сигналу та операційна стабільність лактозного сенсору Рис. 5 Операційна стабільність сенсора для визначення лактози. Вимірювання проводилися в 5 м. М фосфатному буферному розчині, р. Н 6, 5, у комірку вносили 0, 15 м. М лактози. Рис. 6 Стабільність біосенсора для визначення лактози під час зберігання його в сухих умовах при температурі +4°С. Вимірювання проводилися в 5 м. М фосфатному буферному розчині, р. Н 6, 5, у комірку вносили 0, 15 м. М 23
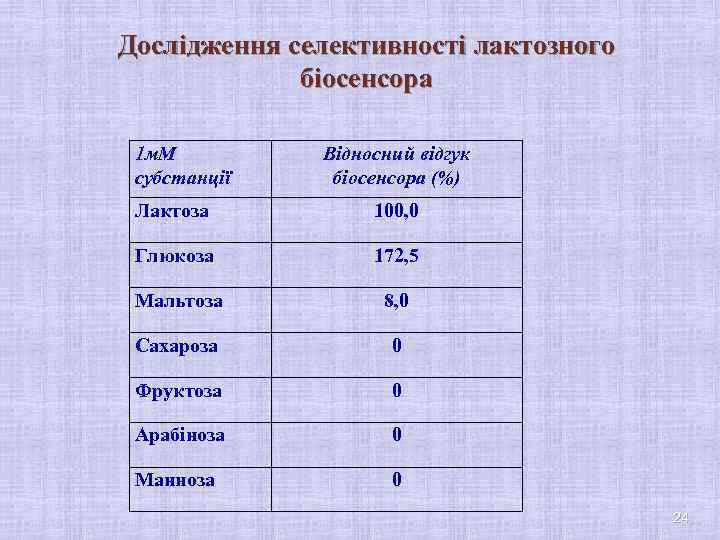
Дослідження селективності лактозного біосенсора 1 м. М субстанції Відносний відгук біосенсора (%) Лактоза 100, 0 Глюкоза 172, 5 Мальтоза 8, 0 Сахароза 0 Фруктоза 0 Арабіноза 0 Манноза 0 24

Принцип роботи ферментного біосенсора для визначення сахарози інвертаза (Е. С. 3. 2. 1. 26) Сахароза + Н 2 О β-D-фруктоза + α-D-глюкоза, мутаротаза (Е. С. 5. 1. 3. 3) α-D-глюкоза β-D-глюкоза, глюкозооксидаза (Е. С. 1. 1. 3. 4) β-D-глюкоза + О 2 D-глюконолактон + Н 2 О 2, D-глюконова кислота + Н 2 О залишок кислоти + Н* Інвертаза, мутаротаза і глюкозооксидаза поступово розщеплюють сахарозу до перекису водню та D-глюконолактону. Глюконолактон в свою чергу спонтанно гідролізується до глюконової кислоти, яка дисоціює на залишок кислоти і протон, при цьому змінюється провідність розчину, яку і можна реєструвати за допомогою кондуктометричного перетворювача. 25
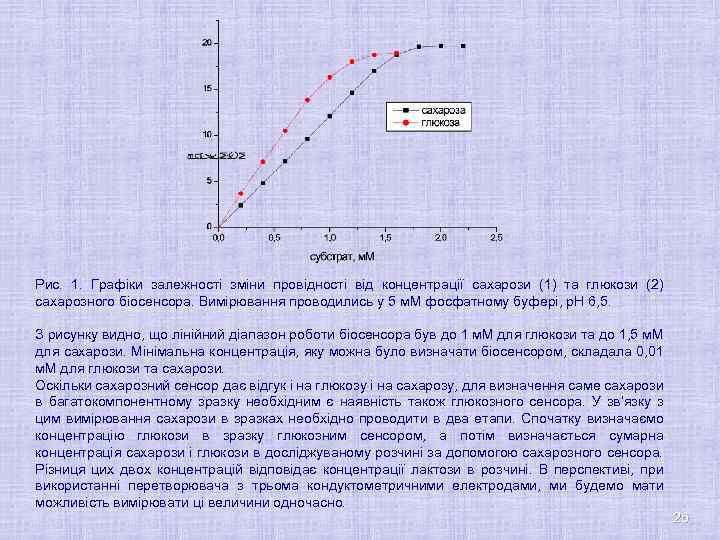
Рис. 1. Графіки залежності зміни провідності від концентрації сахарози (1) та глюкози (2) сахарозного біосенсора. Вимірювання проводились у 5 м. М фосфатному буфері, р. Н 6, 5. З рисунку видно, що лінійний діапазон роботи біосенсора був до 1 м. М для глюкози та до 1, 5 м. М для сахарози. Мінімальна концентрація, яку можна було визначати біосенсором, складала 0, 01 м. М для глюкози та сахарози. Оскільки сахарозний сенсор дає відгук і на глюкозу і на сахарозу, для визначення саме сахарози в багатокомпонентному зразку необхідним є наявність також глюкозного сенсора. У зв’язку з цим вимірювання сахарози в зразках необхідно проводити в два етапи. Спочатку визначаємо концентрацію глюкози в зразку глюкозним сенсором, а потім визначається сумарна концентрація сахарози і глюкози в досліджуваному розчині за допомогою сахарозного сенсора. Різниця цих двох концентрацій відповідає концентрації лактози в розчині. В перспективі, при використанні перетворювача з трьома кондуктометричними електродами, ми будемо мати можливість вимірювати ці величини одночасно. 26
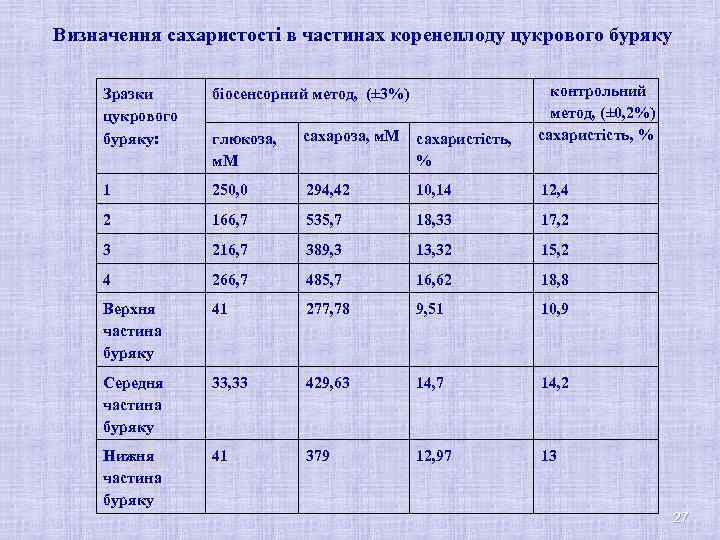
Визначення сахаристості в частинах коренеплоду цукрового буряку контрольний метод, (± 0, 2%) сахаристість, % Зразки цукрового буряку: біосенсорний метод, (± 3%) глюкоза, м. М сахаристість, % 1 250, 0 294, 42 10, 14 12, 4 2 166, 7 535, 7 18, 33 17, 2 3 216, 7 389, 3 13, 32 15, 2 4 266, 7 485, 7 16, 62 18, 8 Верхня частина буряку 41 277, 78 9, 51 10, 9 Середня частина буряку 33, 33 429, 63 14, 7 14, 2 Нижня частина буряку 41 379 12, 97 13 27

Принцип роботи ферментного біосенсора для визначення мальтози (α-глюкозидаза) (Е. С. 3. 2. 1. 20) мальтоза + Н 2 О α-D-глюкоза + α-D-глюкоза (мутаротаза) (Е. С. 5. 1. 3. 3) α-D-глюкоза β-D-глюкоза (глюкозооксидоза) (Е. С. 1. 1. 3. 4) β-D-глюкоза + О 2 D-глюконолактон + Н 2 О 2 D-глюконова кислота + Н 2 О залишок кислоти + Н+ 28
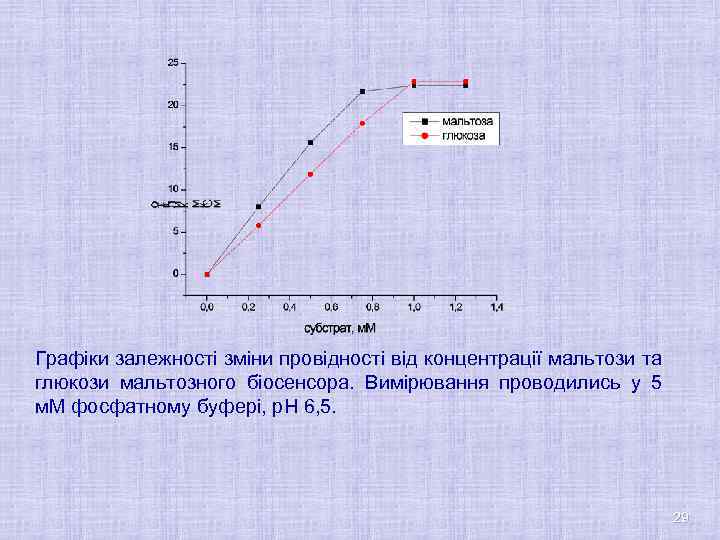
Графіки залежності зміни провідності від концентрації мальтози та глюкози мальтозного біосенсора. Вимірювання проводились у 5 м. М фосфатному буфері, р. Н 6, 5. 29

Біферментний амперометричний біосенсор для визначення АТФ і глюкози GOD D-glucose + O 2 ―—→ D-gluconic acid + H 2 O 2 (1) +600 m. V H 2 O 2 ―—→ 2 H+ + O 2 + 2 e(2) HK D-glucose + ATP ―→ D-glucose-6 -phosphate + ADP (3) 30
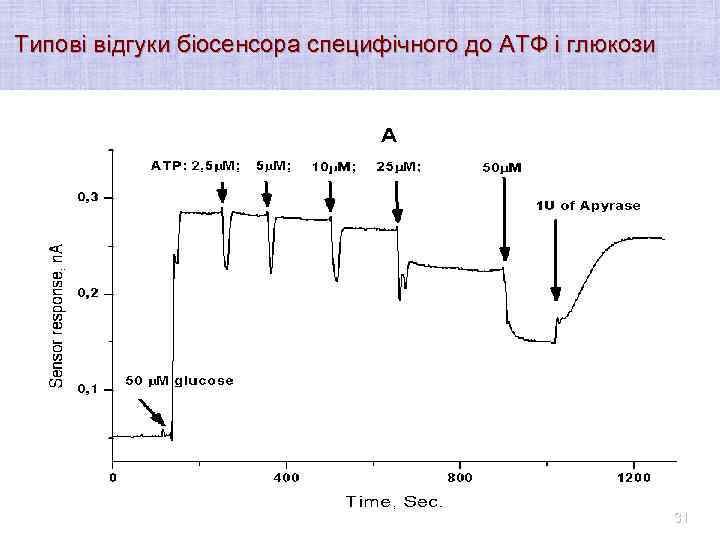
Типові відгуки біосенсора специфічного до АТФ і глюкози 31
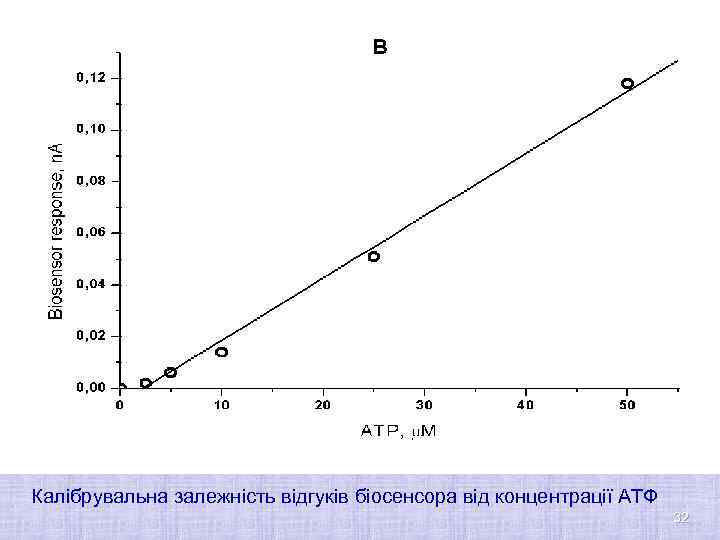
Калібрувальна залежність відгуків біосенсора від концентрації АТФ 32

Потенціометричні ферментні біосенсори на основі інгібіторного аналізу 33

Ферментативні реакції, що лежать в основі роботи біосенсорів Холінестерази можна використовувати при створенні біосенсорів для визначення концентрацій як субстратів (ацетил холін і бутирил холін), так и антихолінестеразних компонентів (пестициди, гербіциди та глікоалкалоїди). 34
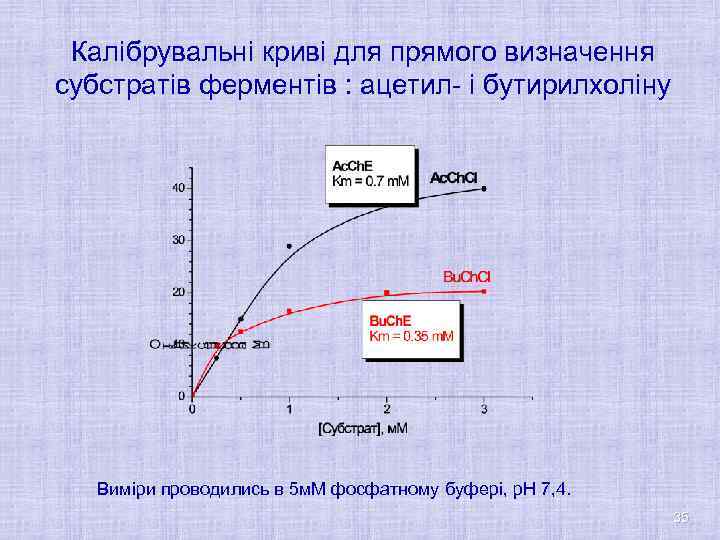
Калібрувальні криві для прямого визначення субстратів ферментів : ацетил- і бутирилхоліну Виміри проводились в 5 м. М фосфатному буфері, р. Н 7, 4. 35
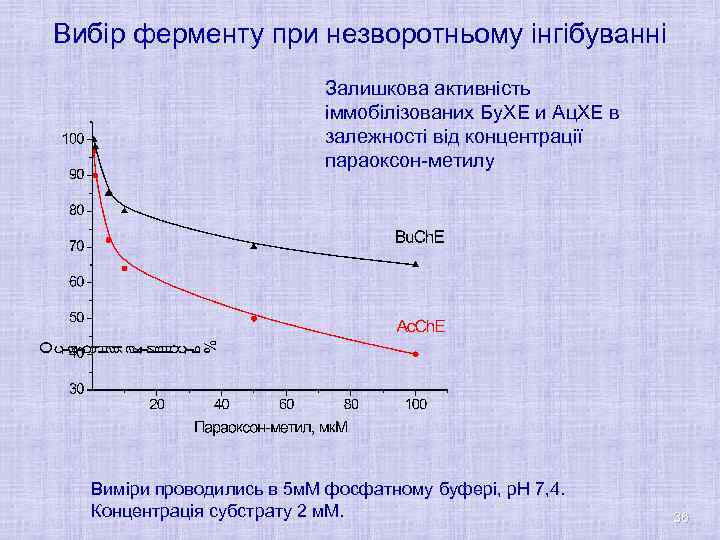
Вибір ферменту при незворотньому інгібуванні Залишкова активність іммобілізованих Бу. ХЕ и Ац. ХЕ в залежності від концентрації параоксон-метилу Виміри проводились в 5 м. М фосфатному буфері, р. Н 7, 4. Концентрація субстрату 2 м. М. 36
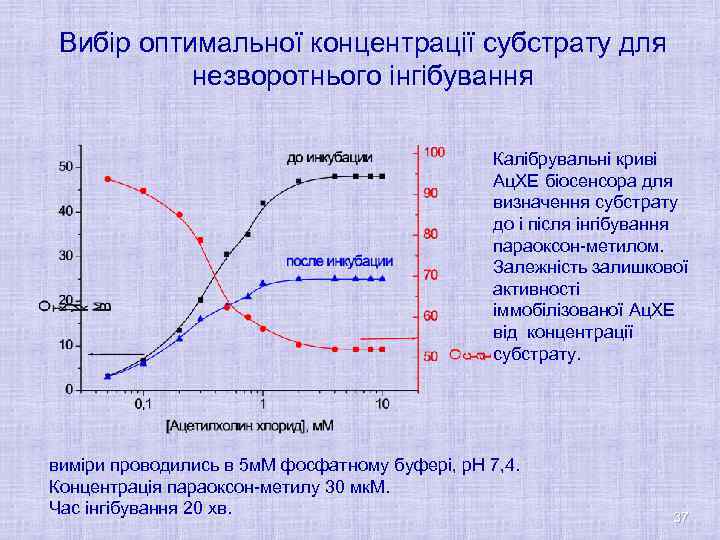
Вибір оптимальної концентрації субстрату для незворотнього інгібування Калібрувальні криві Ац. ХЕ біосенсора для визначення субстрату до і після інгібування параоксон-метилом. Залежність залишкової активності іммобілізованої Ац. ХЕ від концентрації субстрату. виміри проводились в 5 м. М фосфатному буфері, р. Н 7, 4. Концентрація параоксон-метилу 30 мк. М. Час інгібування 20 хв. 37
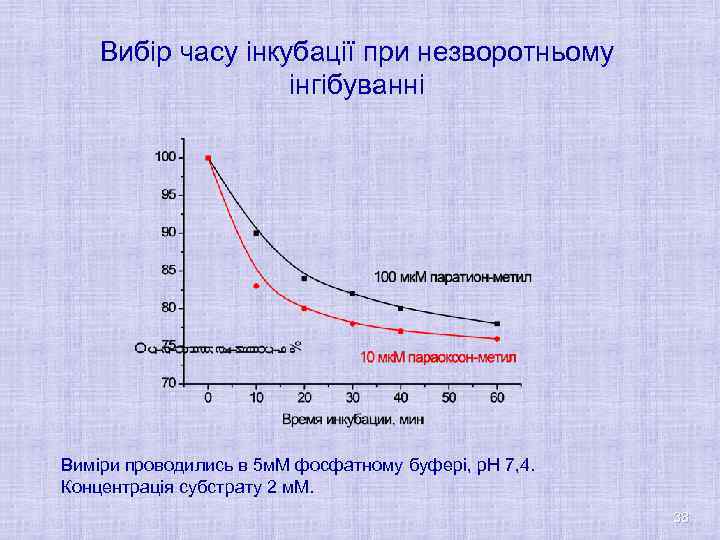
Вибір часу інкубації при незворотньому інгібуванні Виміри проводились в 5 м. М фосфатному буфері, р. Н 7, 4. Концентрація субстрату 2 м. М. 38

Калібрувальні криві для визначення пестицидів Виміри проводились в 5 м. М фосфатному буфері, р. Н 7, 4. Концентрація субстрату 2 м. М. Час інкубації 20 хв. 39
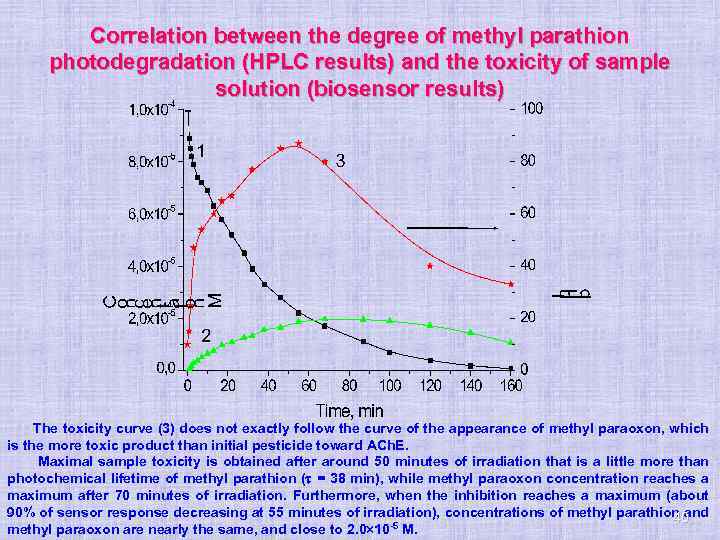
Correlation between the degree of methyl parathion photodegradation (HPLC results) and the toxicity of sample solution (biosensor results) The toxicity curve (3) does not exactly follow the curve of the appearance of methyl paraoxon, which is the more toxic product than initial pesticide toward ACh. E. Maximal sample toxicity is obtained after around 50 minutes of irradiation that is a little more than photochemical lifetime of methyl parathion ( = 38 min), while methyl paraoxon concentration reaches a maximum after 70 minutes of irradiation. Furthermore, when the inhibition reaches a maximum (about 90% of sensor response decreasing at 55 minutes of irradiation), concentrations of methyl parathion and 40 methyl paraoxon are nearly the same, and close to 2. 0 10 -5 M.
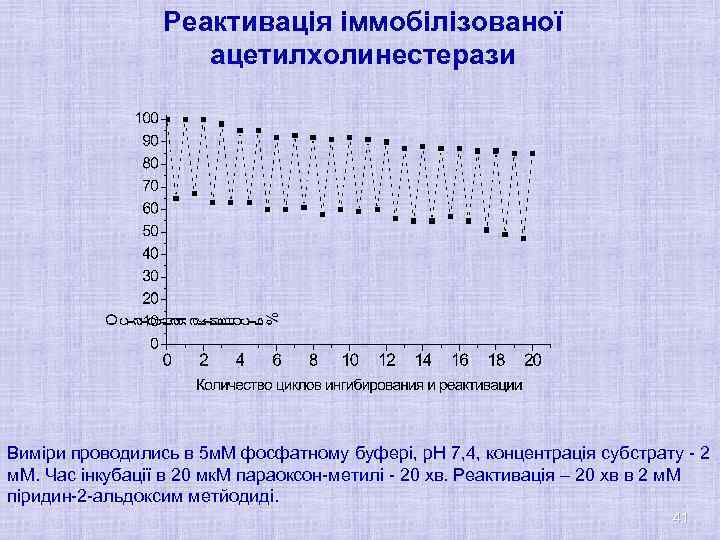
Реактивація іммобілізованої ацетилхолинестерази Виміри проводились в 5 м. М фосфатному буфері, р. Н 7, 4, концентрація субстрату - 2 м. М. Час інкубації в 20 мк. М параоксон-метилі - 20 хв. Реактивація – 20 хв в 2 м. М піридин-2 -альдоксим метйодиді. 41

Зворотнє інгібування холінестераз Глікоалкалоїди в картоплі ( -чаконін, -соланін) Нормальний вміст в картоплі – до 200 мг/кг ваги, може варіювати від 20 до 1500 мг/кг Поражена хворобою картопля – 5 000 мг/кг Позеленівша картопля – більше ніж 2 000 мг/кг Глікоалкалоїди в помідорах (томатин) Зелені помідори – до 500 мг/кг ваги При дозріванні – зменшується до 5 мг/кг Летальна доза 3 -6 мг/кг ваги людини Токсини не гублять свої властивості в процесі приготування 42 їжі. T° деструкції соланіну біля 243 °C
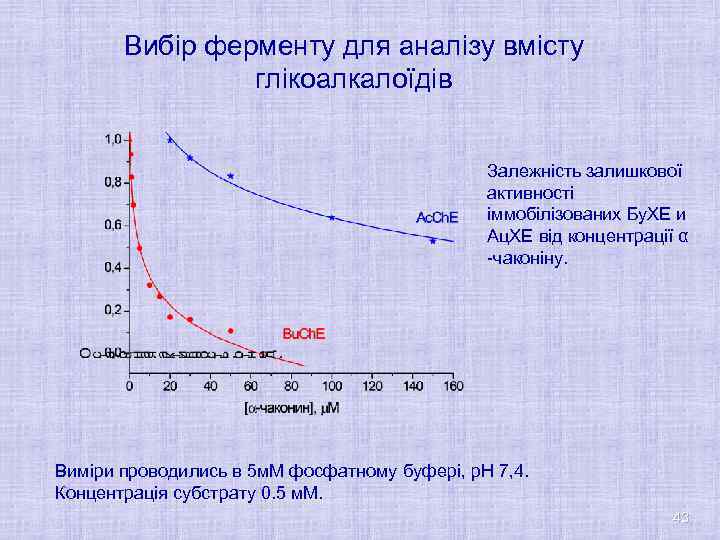
Вибір ферменту для аналізу вмісту глікоалкалоїдів Залежність залишкової активності іммобілізованих Бу. ХЕ и Ац. ХЕ від концентрації α -чаконіну. Виміри проводились в 5 м. М фосфатному буфері, р. Н 7, 4. Концентрація субстрату 0. 5 м. М. 43
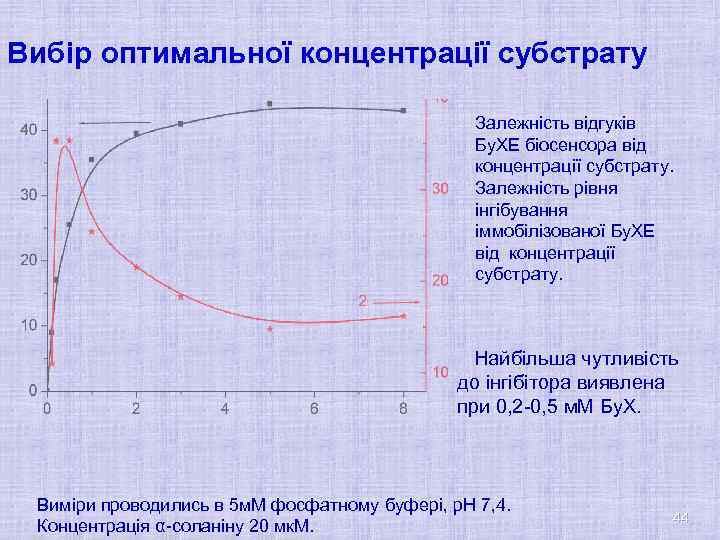
Вибір оптимальної концентрації субстрату Залежність відгуків Бу. ХЕ біосенсора від концентрації субстрату. Залежність рівня інгібування іммобілізованої Бу. ХЕ від концентрації субстрату. Найбільша чутливість до інгібітора виявлена при 0, 2 -0, 5 м. М Бу. Х. Виміри проводились в 5 м. М фосфатному буфері, р. Н 7, 4. Концентрація α-соланіну 20 мк. М. 44
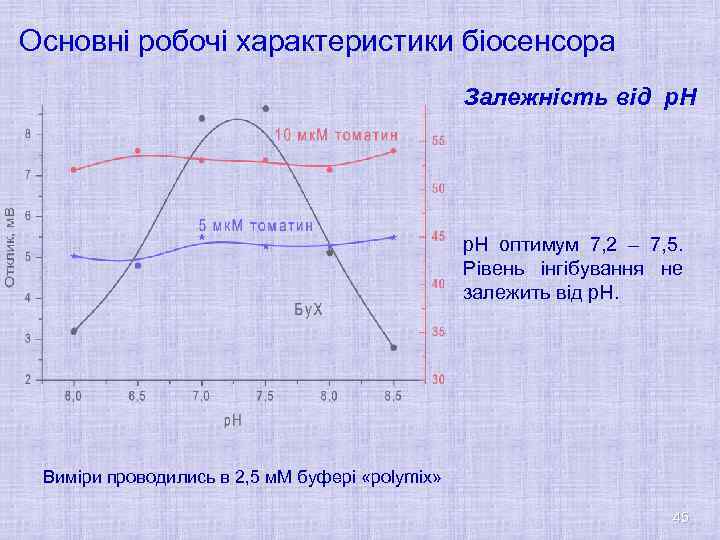
Основні робочі характеристики біосенсора Залежність від р. Н оптимум 7, 2 – 7, 5. Рівень інгібування не залежить від р. Н. Виміри проводились в 2, 5 м. М буфері «polymix» 45
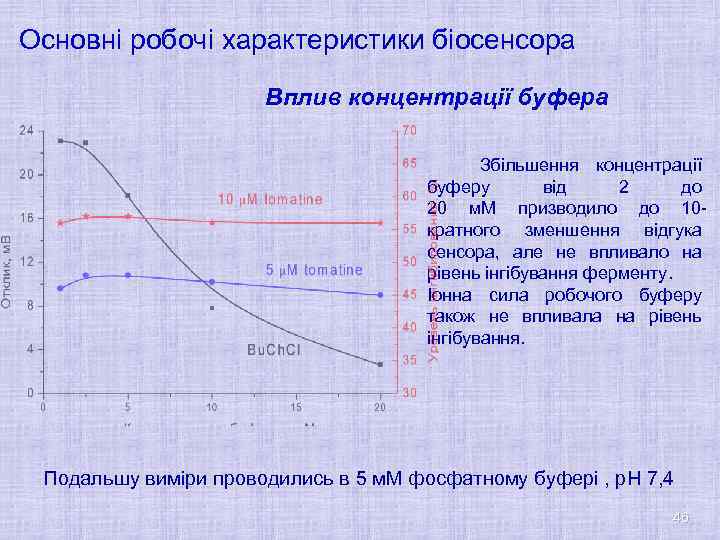
Основні робочі характеристики біосенсора Вплив концентрації буфера Збільшення концентрації буферу від 2 до 20 м. М призводило до 10 кратного зменшення відгука сенсора, але не впливало на рівень інгібування ферменту. Іонна сила робочого буферу також не впливала на рівень інгібування. Подальшу виміри проводились в 5 м. М фосфатному буфері , р. Н 7, 4 46

Типові кінетичні криві відгуків бутирилхолінестеразного біосенсора Typical Тresponse curves of Bu. Ch. E biosensor Більш точна процедура Більш швидка процедура Виміри проводились в 5 м. М фосфатному буфері, р. Н 7, 4. Концентрація субстрату 1 м. М. Концентрація інгібітора - 20 мк. М α-соланін. 47
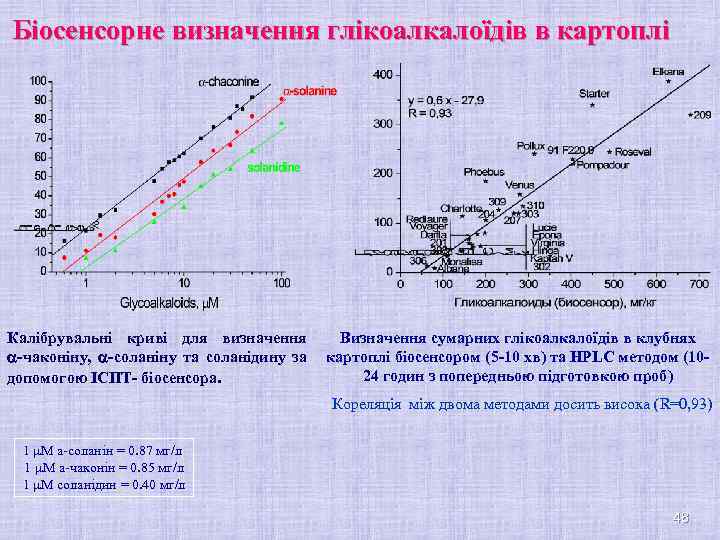
Біосенсорне визначення глікоалкалоїдів в картоплі Калібрувальні криві для визначення -чаконіну, -соланіну та соланідину за допомогою IСПТ- біосенсора. Визначення сумарних глікоалкалоїдів в клубнях картоплі біосенсором (5 -10 хв) та HPLC методом (1024 годин з попередньою підготовкою проб) Кореляція між двома методами досить висока (R=0, 93) 1 m. M a-соланін = 0. 87 мг/л 1 m. M a-чаконін = 0. 85 мг/л 1 m. M соланідин = 0. 40 мг/л 48

Поцедура аналізу біосенсором дуже проста і швидка ØПомити картоплю; ØВичавити краплю соку (порядку 20 мкл); ØПровести виміри біосенсором. Час одного анализу з попередньою підготовкою зразку – 15 - 20 хв. Поцедура аналізу традиційним методом займає біля суток ØЄкстракція глікоалкалоїдів; ØПереведення в необхідну розчинну форму; ØВидалення інтерферуючих компонентів; ØАналіз. 49
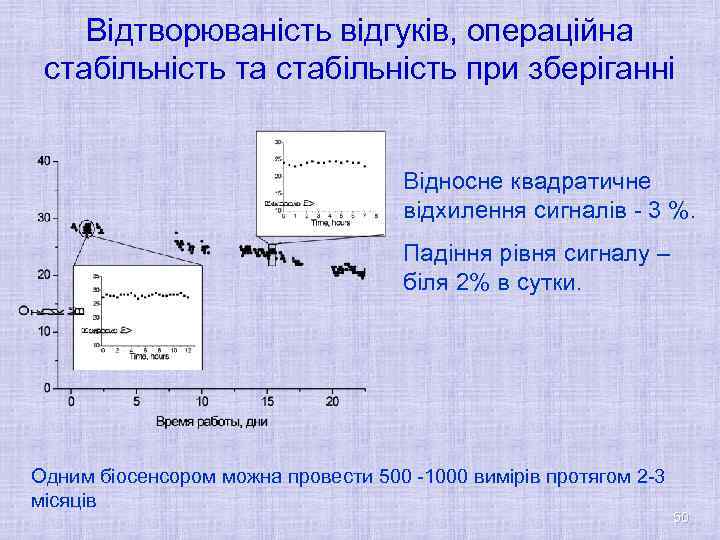
Відтворюваність відгуків, операційна стабільність та стабільність при зберіганні Відносне квадратичне відхилення сигналів - 3 %. Падіння рівня сигналу – біля 2% в сутки. Одним біосенсором можна провести 500 -1000 вимірів протягом 2 -3 місяців 50
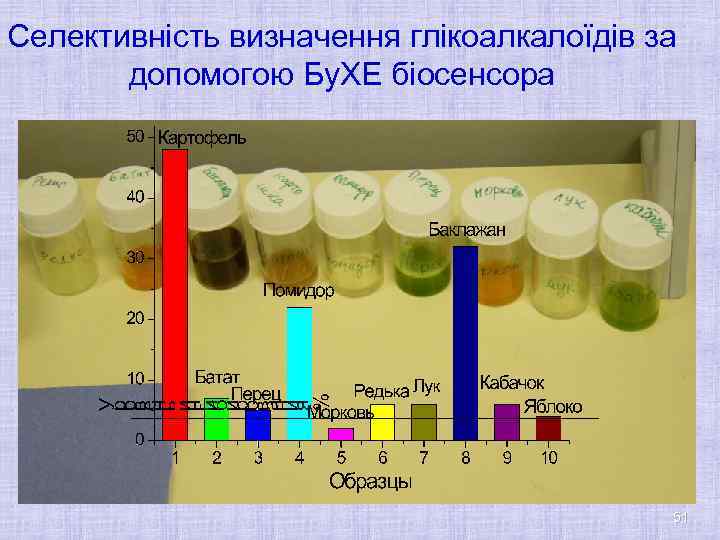
Селективність визначення глікоалкалоїдів за допомогою Бу. ХЕ біосенсора 51

Градієнт вмісту глікоалкалоїдів в картоплині Шари товщиною 3 мм були приготовлені нарізкою картоплі в напрямку від шкірки до шкірки (зразки з 1 по 8) Сорт Producent Rubempré 52
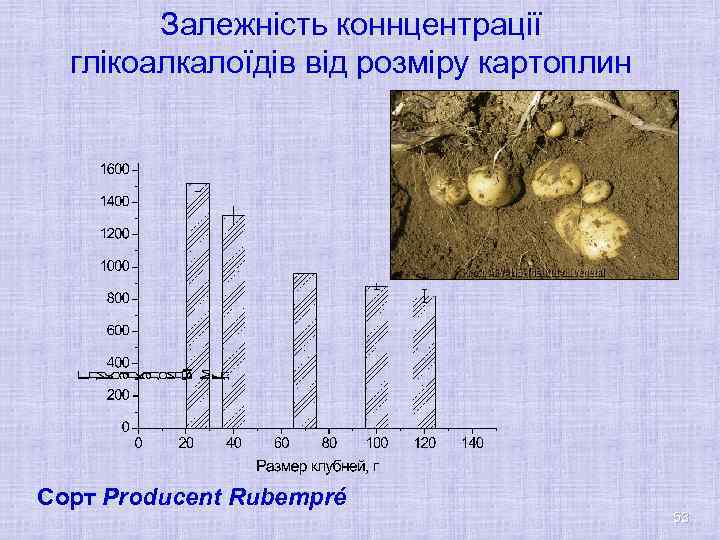
Залежність коннцентрації глікоалкалоїдів від розміру картоплин Сорт Producent Rubempré 53
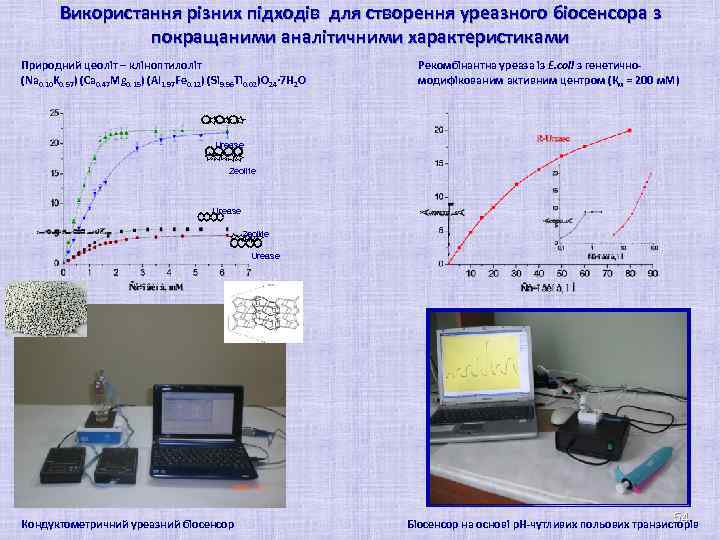
Використання різних підходів для створення уреазного біосенсора з покращаними аналітичними характеристиками Природний цеоліт – кліноптилоліт (Na 0. 10 K 0. 57) (Ca 0. 47 Mg 0. 15) (Al 1. 97 Fe 0. 12) (Si 9. 96 Ti 0. 02)O 24· 7 H 2 O Рекомбінантна уреаза із E. coli з генетичномодифікованим активним центром (Км = 200 м. М) Urease Zeolite Urease A Кондуктометричний уреазний біосенсор C B 54 Біосенсор на основі р. Н-чутливих польових транзисторів

Запитання до лекційного матеріалу 1) Приклади біоселективних елементів каталітичного типу; 2) Варіанти використання ферментів в біосенсорах. 3) Різні принципи електрохімічного перетворення сигналу в біосенсорах на прикладі глюкозооксидози. 4) Приклади амперметричних ферментних біосенсорів та реакцій на основі яких працює біосенсор. 5) Приклади потенціометричних ферментних біосенсорів та реакцій на основі яких працює біосенсор. 6) Приклади кондуктометричних ферментних біосенсорів та реакцій на основі яких працює біосенсор 55

ДЯКУЮ! 56
Варианты биосенсоров.ppt